料酒是以黄酒、蒸馏酒或食用酒精为主体,添加食用盐(可加入植物香辛料),配制加工而成的液体调味料[1],富含氨基酸、酯类、醛类与有机酸类等物质,可在烹饪中对食物起增香、去腥、提鲜等效果[2]。目前市售料酒主要有3种生产工艺:①以黄酒为基酒,添加食盐和香辛料制成,属于原酿料酒,营养丰富,风味突出;②以黄酒与食用酒精混合制成基酒,属于配制料酒,营养物质较少;③以食用酒精为主体,加入食盐、香辛料等辅料调配而成,营养物质含量少,品质较低[3]。此外,为提高辅料中营养物质的提取率,将辅料与谷物共发酵生产料酒,常见于菇类料酒的生产[4-5]。
近年来,料酒成为我国销量增长最快的调味品,具有庞大的市场规模。根据《2024—2029年中国料酒行业发展分析与投资咨询报告》,料酒的需求量占调味品市场约三分之一,其需求量稳步增长,市场潜力巨大[6]。随着大众生活水平的提高,消费者对料酒品质的要求也越来越高。目前国内对料酒的研究主要集中在风味物质与有害物质的形成与调控机制、发酵剂与工艺创新以及质量安全等方面,本文总结了料酒的滋味物质(氨基酸态氮、核苷酸、非挥发性有机酸)及挥发性风味物质(醇类、醛类、酯类、其他类)来源及其呈味特征;阐述了料酒中高级醇、生物胺、氨基甲酸乙酯等主要有害物质的危害及其形成机制,并针对性地提出了降低料酒中主要有害物质的方法,以期提高料酒品质,促进料酒行业健康发展。
1 料酒的风味物质
料酒的主要风味物质主要来自基酒[7-8],一部分来自香辛料。基酒中的氨基酸态氮、核苷酸及非挥发性有机酸等物质含量直接决定料酒的滋味;醇类、醛类、酯类及挥发性酸类等挥发性风味物质的种类与含量决定了料酒的风味。
1.1 料酒中的滋味物质
1.1.1 氨基酸态氮
氨基酸态氮是指以氨基酸形式存在的氮源,是料酒中主要的营养物质与滋味来源[9],由发酵醪液中蛋白质水解产生,料酒中常见的氨基酸有18种,不同氨基酸对料酒风味的贡献不同。其中谷氨酸和天冬氨酸是料酒中最主要的呈鲜氨基酸,二者侧链上存在-COOH或-SO3H等基团,本身呈酸味,但这两个氨基酸的钠盐在溶液中解离后呈现鲜味;丙氨酸和甘氨酸既呈甜味也呈鲜味;苏氨酸和蛋氨酸呈甜味、赖氨酸呈苦味;丝氨酸虽不呈味,但可作为调味增鲜剂使用,使食物色泽更鲜亮[10-12]。由于料酒中氨基酸含量与氨基酸态氮含量成正比,因此常以氨基酸态氮含量反映料酒中氨基酸含量。SB/T 10416—2007《调味料酒》规定,特级调味料酒中氨基酸态氮含量应≥0.40 g/L[1]。
为使料酒品质达到特级标准,需增加基酒中氨基酸态氮的含量。提升基酒中氨基酸态氮含量的方法主要有发酵工艺优化及优良发酵剂筛选。研究表明,将后发酵时间延长约10 d,基酒中氨基酸态氮含量提升35%~104.8%[13];将前发酵温度从26 ℃提高至30 ℃,基酒中氨基酸态氮含量提升100%[9];将麦曲添加量从4%增加至8%时,氨基酸态氮含量提升46.5%[14];在基酒发酵过程中添加0.3%~3.0%黄曲霉(Aspergillus flavus)培养制成的熟麦曲,酒体中氨基酸态氮含量提升至少70%[15]。陈孝[16]从酒曲中筛选出一株高产蛋白酶黄曲霉菌株CX1,复配酿酒酵母(Saccharomyces cerevisiae)制成酒曲进行黄酒酿造,黄酒中氨基酸态氮含量达1.62 g/L;在基酒发酵过程中,外源添加碱性蛋白酶,所得料酒氨基酸态氮含量不低于0.5 mg/L[17]。
上述方法中,延长发酵时间可有效提升酒样氨基酸态氮含量,但此类方法会延长生产周期,增加生产成本;与传统麦曲相比,添加由黄曲霉培养制成的熟麦曲能显著提升基酒中氨基酸态氮含量;与外源添加蛋白酶相比,高产蛋白酶黄曲霉菌株CX1的强化发酵可显著提升酒样中氨基酸态氮含量,但需评估曲霉的安全性;此外,有研究表明氨基酸态氮含量也不能太高,过高会导致酒体浑浊,产生高级醇、苦味和涩味氨基酸与不良气味,影响料酒品质[18];将基酒氨基酸态氮含量控制在0.50~0.60 g/L时终止发酵,可避免苦涩味氨基酸与有害物质的产生,最大限度保留料酒的鲜味[19]。
1.1.2 核苷酸
核苷酸是料酒鲜味的重要来源,由基酒酿造过程中核酸降解产生,一般以钠盐形式存在[20]。在核苷酸的同分异构体中,只有5'-核苷酸有呈鲜作用,其中5'-肌苷酸(inosine 5'-monophosphate,IMP)和5'-鸟苷酸(5'-guamosine monophosphate,GMP)是料酒中最主要的呈鲜核苷酸[21]。同时呈味核苷酸对甜味、肉味、醇厚感有增效作用,对酸味、苦味、腥味、焦味等不良风味有消除或抑制作用[22]。
为增强料酒鲜味,李茜云等[23]在料酒中添加了不同食用菌,制备得到8种富含核苷酸的食用菌料酒,经测定发现料酒中核苷酸的含量越高,料酒的等效鲜味浓度(equivalent umami concentration,EUC)值越高,进一步证实核苷酸含量与料酒鲜味的关系;为进一步提升料酒的鲜味,优化料酒中谷氨酸钠与IMP或与GMP的比例,可将鲜味强度分别提升8倍和30倍[24-25]。与单一提高料酒中核苷酸含量的方法相比,调整核苷酸与氨基酸盐的比例,二者的协同效应能显著提升料酒鲜味强度。
1.1.3 非挥发性有机酸
料酒中非挥发性有机酸主要来自基酒,包括乳酸、柠檬酸、琥珀酸、苹果酸等,其中乳酸和柠檬酸的含量占料酒总非挥发性有机酸含量的80%以上[26]。其中,乳酸呈爽口酸味与涩味,主要产生于黄酒酿造的苹果酸-乳酸发酵(malolactic fermentation,MLF)阶段[27],赋予料酒回味感;柠檬酸呈温和爽快酸味,主要产生于主发酵过程,另有少量来源于原料、酒母及酒曲,它们与带有爽快酸味的苹果酸、刺激性酸味的酒石酸、带有酸味与鲜味的琥珀酸等,共同组成料酒的整体滋味[28]。适宜浓度的酸能有效增强酒体浓厚感并降低甜度,酸度过高则会破坏酒体的整体风味平衡,易导致酒体酸败[29]。因此,SB/T 10416—2007《调味料酒》规定料酒中的总酸含量(以乙酸计)要求≤1.5%[1]。
1.2 料酒中的挥发性风味物质
1.2.1 醇类
料酒中的醇类物质主要在基酒的酿造过程产生,兼具呈味与呈香作用,同时也是合成酯类香气物质的前体。乙醇是含量最多的醇类,具有酒精香味,稀释后带甜味,并产生温和的灼烧感[30]。异丁醇、异戊醇和2-苯乙醇是料酒中最主要的高级醇,其中,2-苯乙醇含量最高,主要由酿酒酵母通过Ehrlich途径和莽草酸途径合成[30]。
适量高级醇可赋予酒体香气,并使口感更加丰满、协调。异丁醇呈苹果香、苦味和可可香,异戊醇带有涩味和刺激味,2-苯乙醇则具有玫瑰花香味,三者对料酒风味有重要贡献[31]。此外,在料酒生产过程中,生姜等香辛料经热处理产生的芳樟醇、α-松油醇等不饱和醇,也对香气和风味贡献较大。其余醇类物质的风味阈值较高,对整体风味贡献较小[32]。
1.2.2 醛类
料酒中的醛类物质主要由基酒发酵过程中微生物的脂肪酸代谢、氨基酸转氨基作用或Strecker降解产生[33],对整体香气起衬托和协调的作用。乙醛、苯乙醛、糠醛和苯甲醛是料酒的主要醛类物质。其中,苯乙醛呈浓烈花果香,糠醛带有焦香,苯甲醛呈杏仁及焦糖香气[32]。
乙醛在基酒总醛中占比较高,过量的乙醛会产生辛辣味且具有毒性,须将其含量控制在30 mg/L以下[34-35]。研究表明,通过黄酒陈酿可促进乙醛与乙醇反应生成无毒、具有清雅果香和酒香的乙缩醛,在降低乙醛含量的同时提升酒体的柔和度与醇厚感[36]。
1.2.3 酯类
料酒中的酯类物质主要由基酒发酵过程中微生物代谢和基酒陈化过程中醇类和酸类的酯化反应产生[37-38],风味阈值较低,为料酒提供花香味、果香味等,是料酒香味最主要的来源,对酒体香气和品质起决定性作用。乙酯是料酒中最丰富、含量最多的酯类,对酒的风味贡献占比最大,其中乳酸乙酯、乙酸乙酯、己酸乙酯和苯乙酸乙酯等关键香气化合物对酒体香气和品质起重要作用。此外,酯类物质之间存在协同作用,可进一步增强料酒香味,如乳酸乙酯与乙酸乙酯比例为9∶1时,可显著增强料酒的酯香和果香[37]。
1.3 其他类挥发性风味物质
料酒中酚类物质主要来自基酒和香辛料[32],为料酒提供特殊香气的同时赋予其保健功能。市面大部分料酒均检测到儿茶素、表儿茶素、绿原酸、芦丁、咖啡酸、原儿茶酸、丁香酸、阿魏酸、β-香豆酸、丁香酚等酚类物质,料酒生产常用的丁香、肉桂、月桂叶等香辛料中均含有香气强烈的丁香酚[39]。此外,有研究表明黄酒中的多酚可以降低小鼠的血脂含量,抑制基质金属蛋白酶2(matrix metalloproteinases-2,MMP-2)和MMP-9的表达以及增加内源性组织金属蛋白酶抑制因子(tissue inhibitor of metalloproteinases-1,TIMP-1)和TIMP-2的表达,从而显著降低小鼠动脉粥状硬化区域,减缓心血管疾病症状[40-41]。
料酒中的醚类物质主要来自八角、茴香、大蒜等香辛料[42]。其中含苯环的醚类大多具有香气强烈、风味阈值低、特征性强等特点。八角、茴香等香辛料中的茴香醚为料酒带来辛甜香气;大蒜中的二烯丙基三硫醚具有强烈刺激气味及大蒜特有的辛辣味,为料酒带来特殊香气[43]。萜类物质通常来自八角、桂皮、花椒、生姜等香辛料,含量少但种类丰富,以异戊二烯为结构单位倍数的烃类及其含氧衍生物形式存在[44]。多款料酒中检测到β-石竹烯、水芹烯等萜类物质,前者赋予料酒辛香、木香、柑橘香及樟脑香,后者赋予料酒薄荷及黑胡椒香气[32]。吡嗪类物质产生于高温下氨基酸与还原糖的美拉德反应,可为料酒提供强烈的坚果特征香气,主要有2,3,5,6-四甲基吡嗪、2,3-二甲基吡嗪等[44]。此外,料酒中挥发性有机酸也是料酒整体风味的组成部分,其中乙酸具有食醋类酸味与刺激性气味,适量的酸味可使酒体风味更加协调[32]。
2 料酒中主要有害物质
2.1 高级醇
高级醇是一类含有3个及以上碳原子的一元醇,常见的高级醇有正丙醇、异戊醇、异丁醇和2-苯乙醇,主要由酿酒酵母通过Ehrlich途径和Harris通路合成[45]。适量的高级醇可使料酒风味更丰富、协调,但含量过高会产生异杂味、危害消费者健康,因此需要控制高级醇含量,在保证料酒风味的同时不对人体造成危害。目前国内对料酒中高级醇含量尚无明确的限量标准,但黄酒中高级醇含量的适宜范围为80~540 mg/L[46]。
2.2 生物胺
生物胺(biogenic amines,BAs)是一类由氨基酸脱羧或由醛和酮的氨基化与转氨基作用形成的有害物,广泛存在于生物以及富含氨基酸和蛋白质的发酵食品中[47-48]。料酒作为富含氨基酸的发酵调味品,BAs含量较高。少量摄入BAs会迅速被人体代谢,但过量摄入BAs会引起头痛、心悸、腹泻、呕吐和水肿等症状,甚至危及生命。组胺和酪胺会对人体产生毒性,腐胺、尸胺、精胺、亚精胺等则会抑制组胺和酪胺代谢酶的活性,从而加剧组胺和酪胺的毒性[49]。此外,酒精会抑制人体胺类氧化酶的活性,使人体更易中毒[47]。目前国内未出台料酒中BAs含量的限量标准,但T/BWDP 0001—2022《北京市酒庄葡萄酒中BAs限量及检测方法》规定葡萄酒中组胺含量限量为8 mg/L、酪胺和腐胺的限量为10 mg/L、尸胺和苯乙胺的限量为3 mgL,为优质基酒生产提供了参考。
2.3 氨基甲酸乙酯
氨基甲酸乙酯(ethyl carbamate,EC)是在基酒酿造过程中产生的一种有害物质,属2A类致癌物,可干扰中枢神经系统,长期或过量接触可能损害肝脏解毒功能。黄酒中酿酒酵母产生氨基甲酸乙酯的途径主要有3种[50](见图1)。
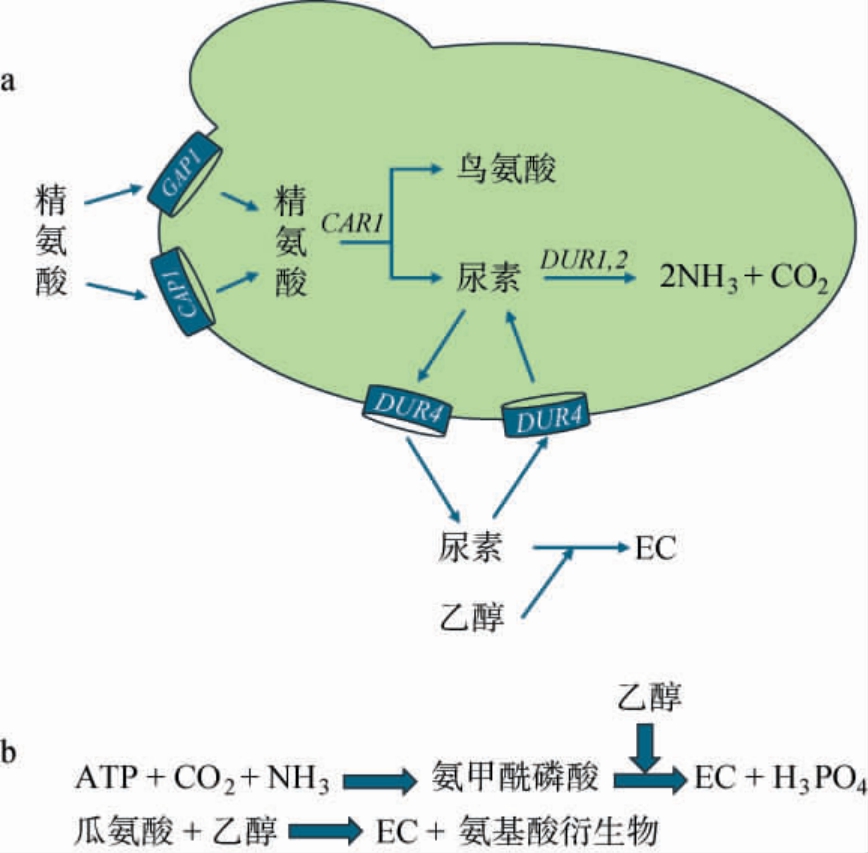
图1 黄酒中酿酒酵母产氨基甲酸乙酯的途径
Fig.1 Pathways of ethyl carbamates production by Saccharomyces cerevisiae in cooking wine
a:黄酒中EC主要生成途径(CAN1编码精氨酸转运蛋白,GAP1编码氨基酸转运蛋白,CAR1编码精氨酸酶,DUR1,2编码尿素酰氨分解酶,DUR3编码尿素转运蛋白,DUR4编码尿素渗透酶);b:黄酒中次要EC产生途径。
由图1可知,90%的EC由尿素与乙醇反应产生[51]。我国现阶段对酒类产品中EC含量并未制定强制标准,但早在2002年联合国粮农组织开始重点监控酒类产品中的EC,并规定其含量不能超过20 μg/L,减少EC前体尿素的积累可有效控制料酒中EC的含量。
3 有害物质含量的控制
3.1 高级醇
可通过发酵工艺优化降低基酒中高级醇含量。研究表明,与传统双边发酵工艺相比,先糖化后发酵工艺可使基酒中的高级醇含量(329.26 mg/L)降低21%[52];延长陈酿时间,黄酒中高级醇含量为338 mg/L,降低35.2%[53];在成品黄酒中添加树脂,可有效吸附高级醇,高级醇含量为327.6 mg/L,减少37%[53];在基酒发酵过程中添加200 mg/L的NH4Cl可使高级醇的含量降低64%[54];减压蒸馏工艺可将酒体中高级醇降低至153.58 mg/L,减少67.9%[55];通过超声催陈处理(300 W、60 kHz、30 ℃、40 min)可使基酒高级醇含量降低22.3%,极大缩短陈酿时间[53]。
采用酿酒酵母与非酿酒酵母菌株如毕赤酵母(Pichia)、异常威克汉姆酵母(Wickerhamomycesanomalus)、植物乳植杆菌(Lactiplantibacillus plantarum)等协同发酵可降低高级醇的生成[56],酿酒酵母协同毕赤酵母发酵可使基酒总高级醇含量下降65.1%[57];酿酒酵母协同异常威克汉姆酵母发酵可使基酒中高级醇下降4.47%~26.91%[58];酿酒酵母协同植物乳植杆菌发酵可使基酒中高级醇下降8.72%~33.36%[59]。采用基因工程技术构建工程菌,如构建丙酮酸脱羧酶编码基因THI3和支链氨基酸转氨酶编码基因BAT2缺失的酿酒酵母,可使基酒中高级醇含量下降15.28%;在酿酒酵母中过表达乙醛脱氢酶基因ALD6,产出的基酒总高级醇含量较出发菌株下降72.04%[58]。
综上所述,在基因工程技术的应用中,过表达ALD6基因能显著降低基酒中高级醇含量,但该方法会导致乙酸含量上升,且因法规、潜在食品安全风险与市场接受度低等问题,未能在食品工业中使用;在成品酒中添加树脂可有效吸附高级醇,但会因非特性吸附其他风味物质,影响料酒风味;与树脂吸附相似,减压蒸馏也会在降醇的同时破坏料酒风味。超声波催陈、添加可同化氮源、菌株协同发酵皆能达到降醇效果,且操作简单、成本低,未来降低料酒高级醇含量可朝此类方向进行。
3.2 生物胺
基酒中BAs的积累受温度、酒精度、pH值、氨基酸浓度等因素的影响[60-61];研究表明,将黄酒分别于4 ℃与20 ℃条件下贮藏30 d,4 ℃贮藏的黄酒BAs含量显著低于20 ℃贮藏的黄酒[62];将黄酒在-2~0 ℃贮藏4 d,黄酒中BAs含量降低26%[60];黄酒中酒精度也会影响BAs含量,与12%vol的酒精度相比,15%vol酒精度可有效抑制酒中产胺杂菌生长,进而减少BAs的生成[61];在浸米阶段应用真空浸泡技术可显著降低原料中游离氨基酸浓度,有效降低黄酒中BAs含量[63];在MLF阶段,维持较低pH(pH3.2)可有效抑制杂菌生长,减少BAs生成[64]。除酿造工艺优化外,在酿酒过程中酒精发酵结束后,外源添加溶菌酶杀灭醪液中原有乳酸菌,静置一段时间后接入优良乳酸菌进行MLF,与不添加溶菌酶进行MLF的酒样相比,最终酒产品中的BAs含量显著降低[65];在基酒酿造前期的浸米阶段,抑制产胺杂菌的生长可有效减少基酒BAs生成,LIU S P等[66]在黄酒酿造的浸米过程中接种非产胺乳酸菌JN01,通过菌种竞争抑制产胺杂菌的生长,基酒中BAs含量降低了87.7%,极大提升了基酒品质;牛天娇[67]在150种乳酸菌中筛选得到耐高酸、高乙醇的优质乳酸菌,其总胺降解率>30%;采用基因工程技术,敲除酿酒酵母的特定基因(如PEP4),构建工程菌株,可在不影响发酵性能的情况下,BAs含量降低50%以上[68];LIU S P等[69]使用基因工程技术,在大肠杆菌中异源表达糖多孢菌的胺氧化酶基因,并将产出的胺氧化酶经体外纯化后用于黄酒中BAs的降解,降解率达31.72%。
上述降低料酒BAs的方法中,采用基因工程技术构建酿酒酵母工程菌效果显著,但因法规、潜在食品安全风险、市场接受度低等问题未能在食品工业中使用,而将体外表达纯化的胺氧化酶应用于BAs的降解可避免上述问题。酒精发酵后加入溶菌酶等方法虽能降低BAs含量,但会延长生产周期、增加生产成本。调整发酵工艺参数虽能降低料酒中BAs含量,但效果有限,而在基酒酿造前期的浸米阶段,抑制产胺杂菌的生长,可显著抑制BAs生成且不影响基酒的风味,为降低料酒中BAs含量、提高料酒品质提供新方向。
3.3 氨基甲酸乙酯
经紫外诱变筛选精氨酸缺陷型的酿酒酵母,可使基酒中尿素含量降低67%[70];酸性脲酶的外源添加,可降解酒体中85%的尿素[71];在发酵中选用酿酒酵母非偏好氮源,可促使酿酒酵母以尿素为氮源,消耗基酒中约30%的尿素[72];外源添加辣蓼提取物,可上调尿素酰胺水解酶基因DUR1,2和DUR3的表达以减少尿素的积累,可使黄酒中EC下降72%[73];应用基因工程技术,敲除酿酒酵母中编码精氨酸酶的基因CAR1,可使酒体中尿素与EC含量分别降低77.89%和73.78%[74];酵母菌中过表达尿素酰胺水解酶基因DUR1,2,黄酒中EC含量降低55%[75];对酿酒酵母中GATA调控因子Gln3p和Gat1p的核定位调控序列进行修饰,可使酿酒酵母的尿素利用率达63.2%[76];在酿酒酵母中表达外源苹果酸转运酶基因和苹果乳酸酶基因,并敲除CAR1基因,可构建同时降低EC和BAs含量的工程菌株[77]。除了降解EC前体尿素的策略外,也可直接降解基酒中的EC。利用功能微生物(如根瘤土壤杆菌(Agrobacterium tumefaciens))发酵液制成EC降解剂,黄酒中的EC降解率达95%[78]。
使用功能微生物直接降解EC与使用脲酶降解尿素效果突出,但此方法存在明显不足。脲酶需要镍离子存在才可发挥活性,而镍离子对人体有害,不可用于料酒生产[73];功能微生物存在降解机理不明晰,无法分离,难以实现产业化。此外,外源添加辣蓼提取物与基因工程技术皆能显著降低EC含量,但前者影响料酒整体风味,后者则因法规、潜在安全风险与市场接受度等问题未能在食品工业中应用。同时,有研究发现部分尿素合成相关基因是酿酒酵母生长所必须的基因,未来研究使用基因工程技术降低料酒EC含量时,需系统识别并规避该类菌株生长关键基因,以平衡代谢工程改造与菌株生理功能之间的关系。
3 结论
料酒作为一种烹饪常用的传统调味品,广受消费者喜爱,但料酒中高级醇、BAs和EC等有害物质超标,严重影响产品安全与品质,而氨基酸态氮含量不足则影响其风味。为了提高料酒风味物质,降低料酒酿造中有害物质,一般采用制备工艺优化及基因工程技术等方式,但存在成本高、工艺复杂、风味不稳定等局限性。尤其是基因工程技术,虽在实验室条件下效果显著,但因法规限制、潜在安全风险及市场接受度低等问题,尚未广泛应用于工业生产。未来研究应解析风味物质与有害物质之间的代谢机制;明确高级醇对风味的贡献阈值,避免过度调控导致风味损失,平衡料酒的安全性与风味;加快制定料酒中有害物质的限量国家标准,为行业质量控制提供依据,促进料酒产业健康可持续发展。
[1] 中华人民共和国商务部.SB/T 10416—2007调味料酒[S].北京:中国标准出版社,2007.
[2] 焦新萍,曾金红,王灵芝,等.料酒品质评价检测技术的研究进展[J].食品安全导刊,2020(27):176-177.
[3] 董颖娜.基于模式识别的料酒品质研究及其指纹图谱建立[D].杭州:浙江农林大学,2018.
[4] 徽海神黄酒集团有限公司.一种杏鲍菇料酒的生产方法:CN108949420A[P].2018-12-07.
[5] 茅台学院.一种高粱香辛料酒及其制备工艺:CN117305039A[P].2023-12-29.
[6] 中国行业研究网.2024-2029年中国料酒行业发展分析与投资咨询报告[EB/OL].(2024-05-10).https://www.chinairn.com/report/20240510/0952233.html.
[7] 李红蕾,冯涛,荣志伟.黄酒酿制过程中风味物质变化规律的研究[J].食品工业,2011,32(12):69-72.
[8] 袁华伟,尹礼国,徐洲,等.SPME/GC-MS联用分析六种香辛料挥发性成分[J].中国调味品,2018,43(9):151-159.
[9] 潘慧青.黄酒中氨基酸态氮的来源及酿造工艺的影响[D].无锡:江南大学,2015.
[10] 王真,陈超,纪晓萌,等.酱油鲜味物质及其检测方法研究进展[J].中国酿造,2024,43(8):7-12.
[11] 毛健.黄酒酿造关键技术与工程应用[M].北京:化学工业出版社,2020:277-278.
[12] 张华芳,曹栩菡.酱油中丝氨酸含量分析方法研究[J].化学工程与装备,2018(9):290-293.
[13] 赵梅,冷云伟,李鹏.黄酒发酵过程分析及关键点的控制[J].江苏调味副食品,2009,26(5):30-34.
[14] 张兴亚,高梦莎,蒋予箭.糖化发酵剂对黄酒中高级醇含量的影响[J].中国酿造,2012,31(1):130-133.
[15] 刘双平,刘彩霞,王小壮,等.熟麦曲促进黄酒发酵的机理研究[J].中国食品学报,2023,23(4):57-65.
[16] 陈孝.高产氨基态氮菌株的筛选及在黄酒中的应用[D].武汉:湖北工业大学,2020.
[17] 合肥工业大学.一种利用黄酒酒糟生产高氨基酸态氮含量的料酒的方法:CN107455723B[P].2020-09-22.
[18] 潘慧青,曹钰,石慧媛,等.黄酒酿造后酵工艺对氨基酸态氮生成的影响[J].食品与生物技术学报,2016,35(2):144-150.
[19] 陈回军,高轶岚.绍兴黄酒酿造过程中氨基酸态氮量变化及控制研究[J].食品安全导刊,2020(18):116-118.
[20] ZHAO J,FLEET G H.Degradation of RNA during the autolysis of Saccharomyces cerevisiae produces predominantly ribonucleotides[J].J Ind Microbiol Biotechnol,2005,32(9):415-423.
[21] 顾俊浩,俞铮,张佳汇,等.鲜味物质及鲜味调味料的研发进展[J].食品工业科技,2023,44(15):418-426.
[22] 阎微,沈燕霆,李英雨,等.呈味核苷酸的新应用介绍[J].中国调味品,2012,37(3):6-8.
[23] 李茜云,马鹏程,郭明,等.新型食用菌料酒的制备以及功能性成分的研究[J].酿酒科技,2018(12):106-116.
[24] 崔桂友.呈味核苷酸及其在食品调味中的应用[J].中国调味品,2001(10):25-29.
[25] 沈浥.调味品中呈味核苷酸的研究进展和我国标准化现状[J].中国调味品,2017,42(1):177-180.
[26] 王培璇,毛健,李晓钟,等.不同地域黄酒中酸类物质差异性研究[J].食品工业科技,2014,35(10):190-194.
[27] 朱斌,骆佳琪,关斌,等.传统黄酒的风味成分及品质控制研究进展[J].中国酿造,2024,43(9):9-13.
[28] 严文怡,杨艳,谢雅婷,等.传统黄酒风味物质研究进展[J].食品安全质量检测学报,2023,14(14):115-124.
[29] 郭金英,杨慧.黄酒中主要有机酸的分析[J].酿酒科技,2014(10):94-96.
[30] 黄晓媛,钱敏,阮凤喜,等.黄酒中醇类物质的研究进展[J].食品工业,2022,43(1):237-240.
[31] 马博文.黄酒酿酒酵母对醇类物质的代谢调控研究进展[J].酿酒科技,2023(10):82-88.
[32] 康波,段鑫锐,张小龙,等.不同地区调味料酒的挥发性风味物质研究[J].中国调味品,2022,47(9):135-143.
[33] 于俊婷.黄酒中挥发性羰基化合物的检测方法优化及其在黄酒鉴别中的应用[D].无锡:江南大学,2023.
[34] 刘华.绍兴黄酒酵母及发酵过程中乙醛的初步研究[D].无锡:江南大学,2016.
[35] 国家卫生和计划生育委员会,国家食品药品监督管理总局.GB 31640—2016食用酒精[S].北京:中国标准出版社,2016.
[36] YANG Y J,AI L Z,MU Z Y,et al.Flavor compounds with high odor activity values(OAV>1)dominate the aroma of aged Chinese rice wine(Huangjiu)by molecular association[J].Food Chem,2022,383:132370.
[37] 于海燕,谢静茹,解铜,等.酯类化合物香气感知相互作用及其对黄酒感官属性的影响(英文)[J].食品科学,2021,42(14):218-225.
[38] 季津.气相色谱法分析发酵黄酒中酯类物质的研究[J].酿酒,2011,38(3):59-63.
[39] 陈磊,黄雪松.高效液相色谱法同时检测黄酒中的5-羟甲基糠醛和9种多酚[J].分析化学,2010,38(1):133-137.
[40] ZHAI X Y,CHI J F,TANG W L,et al.Yellow wine polyphenolic compounds inhibit matrix metalloproteinase-2,-9 expression and improve atherosclerotic plaque in LDL-receptor-knockout mice[J].J Pharm Sci,2014,125(2):132-141.
[41] LIN H,ZHANG J,NI T J,et al.Yellow wine polyphenolic compounds prevents doxorubicin-induced cardiotoxicity through activation of the Nrf2 signalling pathway[J].J Cell Mol Med,2019,23(9):6034-6047.
[42] 王伟,张永进,林琳,等.两种不同杀菌方式对神仙豆的营养组成及其挥发性成分的影响[J].现代食品科技,2015,31(1):245-253.
[43] 王德振,李佳,张玲玲,等.大蒜、洋葱、生姜和辣椒四种香辛料风味成分研究进展[J].中国调味品,2019,44(1):179-185.
[44] 肖云,李暄,刘丹彤,等.料酒的发展历史与去腥调味机理研究进展[J].食品与发酵工业,2023,49(9):334-339.
[45] 王兴龙,袁敏,袁留政,等.黄酒中安全风险性物质及控制的研究进展[J].食品与发酵科技,2015,51(1):96-100.
[46] 李健俊,屈春云,刘功良,等.饮料酒中高级醇的危害及其调控研究进展[J].食品与发酵工业,2023,49(14):321-329.
[47] 牛天娇,郭永杰,陈历水,等.黄酒生产过程中生物胺的形成及变化[J].中国酿造,2019,38(10):67-71.
[48] LANDETE J M,FERRER S,PARDO I.Biogenic amine production by lactic acid bacteria,acetic bacteria and yeast isolated from wine[J].Food Control,2006,18(12):1569-1574.
[49] 景智波,田建军,杨明阳,等.食品中与生物胺形成相关的微生物菌群及其控制技术研究进展[J].食品科学,2018,39(15):262-268.
[50] 杨佳,李新生,耿敬章,等.黄酒中氨基甲酸乙酯的研究进展[J].中国酿造,2020,39(3):7-11.
[51] 白卫东,沈棚,钱敏.黄酒中氨基甲酸乙酯形成机理及控制方法研究进展[J].中国酿造,2012,31(7):6-10.
[52] 龚耀平,周建弟,钱斌,等.不同酿造工艺对黄酒理化指标及高级醇含量影响的研究[J].中国酿造,2013,32(2):37-41.
[53] 闫春明.降低新酿黄酒中高级醇含量研究[D].合肥:合肥工业大学,2017.
[54] LIU S P,MA D L,LI Z H,et al.Assimilable nitrogen reduces the higher alcohols content of Huangjiu[J].Food Control,2021,121:107660.
[55] 浙江树人学院(浙江树人大学).一种降低黄酒中高级醇含量的方法:CN113122421B[P].2022-07-22.
[56] CIANI M,CAPECE A,COMITINI F,et al.Yeast interactions in inoculated wine fermentation[J].Front Microbiol,2016,7:555.
[57] JIANG J,LIU Y C,LI H H,et al.Modeling and regulation of higher alcohol production through the combined effects of the C/N ratio and microbial interaction[J].J Agr Food Chem,2019,67(38):10694-10701.
[58] 白永平,廖剑桥,刘克,等.异常威克汉姆酵母的筛选及其对黄酒风味影响的研究[J].食品与发酵科技,2024,60(6):53-61.
[59] 上海理工大学.一种降低黄酒中杂醇含量的植物乳杆菌及其应用:CN117264800A[P].2023-03-28.
[60] 俞剑燊,张凤杰,王德良,等.酿酒工艺对黄酒中生物胺的影响[J].中国酿造,2015,34(4):123-127.
[61] LORENZO C,BORDIGA M,PÉREZ-ÁLVAREZ E P,et al.The impacts of temperature,alcoholic degree and amino acids content on biogenic amines and their precursor amino acids content in red wine[J].Food Res Int,2017,99(P1):328-335.
[62] KIM J Y,KIM D,PARK P,et al.Effects of storage temperature and time on the biogenic amine content and microflora in Korean turbid rice wine,Makgeolli[J].Food Chem,2011,128(1):87-92.
[63] LI X,YAO J,LEI D,et al.The dynamic of biogenic amines and higher alcohols of Chinese rice wine during fermentation[J].Food Sci Biotechnol,2025,34(6):1423-1432.
[64] CINQUANTA L,DE STEFANO G,FORMATO D,et al.Effect of pH on malolactic fermentation in southern Italian wines[J].Eur Food Res Technol,2018,244(7):1261-1268.
[65] ISABEL L,SANTAMARIA P,TENORIO C,et al.Evaluation of lysozyme to control vinification process and histamine production in Rioja wines[J].J Microbiol Biotechnol,2009,19(9):1005-1012.
[66] LIU S P,SUN H L,LIU C X,et al.Reducing biogenic amine in seriflux and Huangjiu by recycling of seriflux inoculated with Lactobacillus plantarum JN01[J].Food Res Int,2021,150(PA):110793.
[67] 牛天娇.黄酒酿造中微生物菌群结构及对生物胺降解作用研究[D].哈尔滨:哈尔滨工业大学,2020.
[68] 天津科技大学.一株能降低黄酒中生物胺的酿酒酵母及其构建方法与应用:CN104046572B[P].2017-04-05.
[69] LIU S P,YAO H L,SUN M F,et al.Heterologous expression and characterization of amine oxidases from Saccharopolyspora to reduce biogenic amines in Huangjiu[J].LWT-Food Sci Technol,2022,169:113963.
[70] 方逸群,倪斌.黄酒酵母的性能改良及降低其产物中氨基甲酸乙酯含量的研究[J].酿酒科技,2018(7):27-33.
[71] YANG L Q,WANG S H,TIAN Y P.Purification,properties,and application of a novel acid urease from Enterobacter sp.[J]. Appl Biochem Biotechnol,2010,160(2):303-313.
[72] ZHAO X R,ZOU H J,FU J W,et al.Nitrogen regulation involved in the accumulation of urea in Saccharomyces cerevisiae[J]. Yeast,2013,30(11):437-447.
[73] PENG Q,ZHENG H J,XUE J R,et al.Mechanism of Polygonum hydropiper reducing ethyl carbamate in Chinese rice wine(Huangjiu)brewing[J].Food Microbiol,2025,125:104628.
[74] GUO X W,LI Y Z,GUO J,et al.Reduced production of ethyl carbamate for wine fermentation by deleting CAR1 in Saccharomyces cerevisiae[J].J Ind Microbiol Biotechnol,2016,43(5):671-679.
[75] WU D H,LI X M,LU J,et al.Constitutive expression of the DUR1,2 gene in an industrial yeast strain to minimize ethyl carbamate production during Chinese rice wine fermentation[J].FEMS Microbiol Lett,2016,363(1):fnv214.
[76] ZHAO X R,ZOU H J,CHEN J,et al.The modification of Gat1p in nitrogen catabolite repression to enhance non-preferred nitrogen utilization in Saccharomyces cerevisiae[J].Sci Rep,2016,6:21603.
[77] VASYAGIN E A,URAKOV V N,SHALAMITSKIY M Y,et al.Development of a wine yeast strain capable of malolactic fermentation and reducing the ethyl carbamate content in wine[J].Foods,2024,14(1):54.
[78] 大连工业大学.高效降解氨基甲酸乙酯的菌株及其应用:CN113174342B[P].2023-07-07.