中高温大曲是浓香型白酒生产专用的发酵剂[1],其含有的大量微生物和次级代谢产物赋予了浓香型白酒独特的风味特征。近年来,研究人员主要通过强化添加特定内源性微生物[2]来提高白酒大曲的质量和稳定性[3-4]。如在大曲生产中强化添加酿酒酵母可有效提高酯类物质含量[5],添加高产吡嗪类物质的芽孢杆菌则能显著提高吡嗪类物质含量[6]。然而针对大曲中产香菌的研究工作主要还是集中在南方地区高温大曲上,目前对北方中高温大曲产香菌的挖掘与研究尚需进一步深化。
酯化酶可以催化醇类物质与酸类物质发生酯化反应,产生己酸乙酯等白酒主要风味物质[7]。芽孢杆菌作为大曲中产生酯化酶的主要微生物[8-9],对白酒酿造起到了重要的作用[10]。研究表明从浓香型白酒大曲中筛选到高产酯化酶菌株主要是芽孢杆菌属(Bacillus),其在大曲样品成熟期中占绝对优势地位[11]。从高温大曲中筛选出的一株地衣芽孢杆菌(Bacillus licheniformis)SPEO-28优化发酵培养条件后产酯酶活力达22.83 U/mL[12]。从酱香型白酒大曲和糟醅中分离出的枯草芽孢杆菌(Bacillus subtilis)GTBS-93和GTBS-171的乳酸乙酯和己酸乙酯合成量分别达到47.94 mg/L和13.89 mg/L,这表明不同芽孢杆菌在产特定酯化酶和合成相应酯类物质的能力上存在差异[13]。将枯草芽孢杆菌(Bacillus subtilis)和贝莱斯芽孢杆菌(Bacillus velezensis)应用于强化大曲,结果表明强化大曲吡嗪类、醇类和酯类物质明显增加,四甲基吡嗪和苯乙醇含量分别提高了91%和70%[14]。酯化力是衡量大曲生酯生香能力的理化指标[15],因此研究酯化酶活力较高的芽孢杆菌对于提升白酒的香气浓郁度、改善酒体品质和增加产品稳定性有着重要意义。
本研究以北方中高温大曲为研究对象,基于传统培养分离法从中筛选出高酯化力的芽孢杆菌,并对其进行形态学观察及分子生物学鉴定。通过响应面法优化其培养条件,并培养强化菌液制备高品质强化大曲,为北方浓香型白酒品质提升与工艺稳定性控制提供重要参考价值。
1 材料与方法
1.1 材料与试剂
1.1.1 材料
中高温大曲、小麦等:河北某浓香型白酒厂。
1.1.2 化学试剂
无水乙醇、氢氧化钠、盐酸、硫酸、葡萄糖、己酸等(均为分析纯):天津欧博凯化工有限公司;革兰氏染色液:北京奥博星生物技术有限责任公司;细菌脱氧核糖核酸(deoxyribonucleic acid,DNA)提取试剂盒:天根生化科技有限公司。
1.1.3 培养基
分离培养基(牛肉膏蛋白胨琼脂培养基)、富集培养基(肉汤培养基):北京陆桥技术股份有限公司。
筛选培养基:牛肉膏蛋白胨琼脂培养基,添加0.1‰CaCl2和1%Tween-80 10 mL。
发酵培养基:葡萄糖20 g、淀粉20 g、酵母膏3 g、磷酸二氢钾2 g、磷酸氢二钾2 g、氯化钠5 g、硫酸铵2 g、氯化钙0.1 g、七水合硫酸镁0.5 g、七水合硫酸亚铁0.05 g、蒸馏水1 000 mL,初始pH 6.8~7.2,121 ℃、0.1 MPa条件下灭菌20 min后冷却,备用。
麦粉培养基[16]:将粉碎小麦与水按1∶0.4(g/mL)混合润麦2 h,润麦结束后在蒸锅里进行蒸煮40 min后取出,充分打散后,小麦与水按1.0∶0.2(g/mL)进行混匀,使其达到湿而不黏的程度后将原料按每瓶50 mL分装于500 mL锥形瓶中,121 ℃、0.1 MPa条件下灭菌20 min后冷却,备用。
1.2 仪器与设备
DW-25W198医用低温保存箱、HLR-310F实验室冷藏箱:海尔生物医疗股份有限公司;THZ-92C气浴恒温振荡器:上海博迅实业有限公司;DHP9082电热恒温培养箱、DHG-9070A电热鼓风干燥箱:上海一恒科学仪器有限公司;ZQLY-180N振荡培养箱:上海知楚仪器有限公司;GI54DS高压灭菌器:致微(厦门)仪器有限公司;SW-CJ-2F型双人双面净化工作台:苏州净化设备有限公司;PR223ZH/E电子天平:奥豪斯仪器有限公司。
1.3 方法
1.3.1 高酯化力芽孢杆菌的分离
牛肉膏蛋白胨琼脂培养基作为分离培养基,将其按每瓶200 mL分装至500 mL锥形瓶中,培养基灭菌后冷却。往灭菌好的90 mL生理盐水中加入10 g粉碎好的中高温大曲,用封口膜密封瓶口,置于摇床上150 r/min振荡混匀15 min。在无菌环境下,将混匀的液体取上清液加入生理盐水,梯度稀释至10-6制成菌悬液,分别吸取1 mL各浓度的菌悬液浇筑于培养皿中,将冷却至50 ℃后的细菌分离培养基倒平板,冷却后于37 ℃条件下倒置培养72 h。根据形态学初步鉴定菌落形态,将分离得到的形态与芽孢杆菌相近的菌株于细菌分离培养基平板上进行菌株纯化,分离至纯种,将纯化后单菌落于装有25%甘油的离心管-20 ℃密封保藏。
1.3.2 菌株的初筛
将初筛得到的纯化菌株接种于富集培养基37℃、150r/min振荡培养24 h,将纯化后的菌液用平板划线法接种于分离培养基中得到单菌落,将获得的单菌落接种于筛选培养基上,并设置3个平行,37 ℃培养72 h,测定菌落直径(d)及透明圈直径(D)的大小,计算D/d值,对D/d值大的菌株进行复筛[17]。
1.3.3 高酯化力芽孢杆菌的复筛
将D/d值较大的菌株用富集培养基活化,调整菌液浓度为1×108 CFU/mL,将菌液以10%(V/V)接种量接入麦粉培养基中,37 ℃条件下培养7 d,40 ℃烘干后粉碎。参照轻工行业标准QB/T 4257—2011《酿酒大曲通用分析方法》测定酯化力,对其中发酵麦曲酯化力高的菌株进行鉴定。酯化力酶活定义:以每50 g曲样在35 ℃经过7 d催化己酸和乙醇合成己酸乙酯质量为1 U,单位为mg/(50 g·7 d)。
1.3.4 菌株耐受性试验[18]
菌株耐高温实验:将纯化后的菌株划线接种于牛肉膏蛋白胨琼脂培养基中,分别在45 ℃、50 ℃、55 ℃、60 ℃条件下培养72 h,肉眼观察培养基上菌株生长状况。
菌株耐酸性实验:分别调节牛肉膏蛋白胨琼脂培养基的pH值为4、5、6、7,取100 μL菌液接种于培养基中,37 ℃条件下培养72 h,肉眼观察培养基上菌株生长状况。
菌株耐乙醇实验:分别向牛肉膏蛋白胨琼脂培养基中加入无水乙醇使培养基乙醇含量为6%、9%、12%、15%、18%,取100 μL菌液接种于培养基中,37 ℃培养72 h,肉眼观察培养基上菌株生长状况。
1.3.5 高酯化力芽孢杆菌的鉴定
菌落形态学观察:在无菌条件下将筛选出的菌株挑取后接种于分离培养基中,在37℃恒温培养箱内倒置培养72h,观察菌落形态。显微形态观察:在洁净载玻片中央滴加一滴无菌生理盐水,用接种针挑取少量菌丝均匀涂抹于生理盐水中,烘干后用革兰氏染色法染色,盖上盖玻片,置于显微镜下观察菌株。根据菌株的菌落和菌体的形态特征对其进行初步鉴定。
分子生物学鉴定[19]:以细菌基因组DNA为模板,用细菌16S rDNA通用引物进行聚合酶链式反应(polymerase chain reaction,PCR)扩增,引物序列:8F:5'-AGAGTTTGATCCTGGCTCAG-3';1 492R:5'-GGTTACCTTGTTACGACTT-3'。PCR扩增体系(50μL):5×PCRBuffer10μL,10mmol/L脱氧核糖核苷三磷酸(deoxy-ribonucleoside triphosphate,dNTP)1 μL,10 μmol/L 8F和1 492R各1 μL,Phusion超保真DNA聚合酶1 U,DNA模板1 μL。PCR扩增条件:94 ℃预变性2 min;94 ℃变性30 s,56 ℃退火30 s,72 ℃延伸90 s,27个循环;72 ℃再延伸5 min。PCR扩增产物经1%琼脂糖凝胶电泳检测合格后送微基生物科技(上海)有限公司测序,测序结果通过国家生物技术信息中心(National Center for Biotechnology Information,NCBI)数据库进行BLAST分析比对,用MEGA11.0软件构建系统发育树[20]。
1.3.6 菌株发酵条件优化单因素试验
将目的菌接种于发酵培养基进行扩大培养,调整菌液浓度为1×108 CFU/mL,将其接种于麦粉培养基中进行对培养时间、接种量和培养温度3个因素进行优化[21]。
设置基础发酵条件为温度37 ℃、接种量3%、培养时间72 h。分别考察不同培养时间(48 h、60 h、72 h、84 h)、接种量(1%、2%、3%、4%)、培养温度(37 ℃、42 ℃、46 ℃、52 ℃)对菌种发酵麦曲酯化力的影响,样品经40 ℃烘干至含水量约13%,粉碎后进行酯化力测定。每个培养时间做3个平行,重复3组实验。
1.3.7 发酵条件优化响应面试验
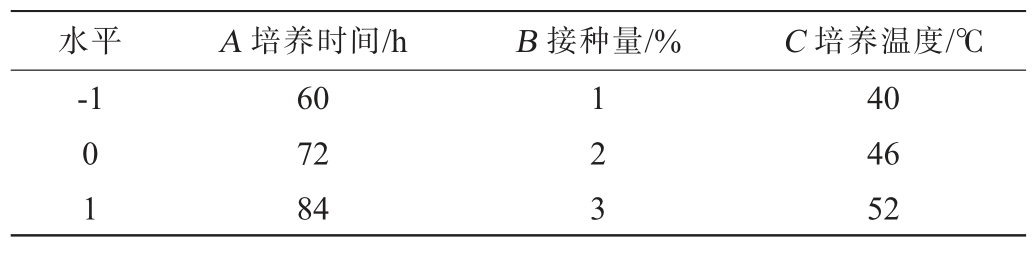
基于单因素试验结果,采用Box-Behnken设计法[22],选择培养时间、接种量和培养温度作为试验因素,以酯化力为响应值,使用Design-Expert 13.0软件设计3因素3水平响应面试验,试验因素与水平见表1。
表1 菌株发酵条件优化响应面试验因素与水平
Table 1 Factors and levels of response surface experiments for fermentation conditions optimization of the strain
1.3.8 添加目的菌株制备强化大曲
将浓度为1×108 CFU/mL的目的菌株菌液以2.8%的接种量加入麦粉培养基中,以初始pH6、培养温度46 ℃的培养条件培养75 h后得到目的菌株发酵麦曲,然后以原料总质量2%的比例将其添加至小麦中,以制备强化大曲。以正常未强化中高温大曲为对照组,大曲生产工艺参照QB/T 4258—2011《酿酒大曲术语》。
1.3.9 大曲感官评价及指标测定
大曲在干净卫生、干燥阴凉和正常通风的曲库中贮存3个月分别对其感官和理化指标进行测定,感官指标评价由6名省级白酒评委组成的小组对随机抽取的6块强化大曲和6块未强化大曲进行评价打分,感官评价标准参照大曲感官标准化评定表[23],水分、酸度、酯化力、糖化力、液化力和发酵力测定方法参照QB/T 4257—2011《酿酒大曲通用分析方法》,其中酯化力、糖化力、液化力和发酵力均以U表示。
1.3.10 数据处理
采用Origin 2022软件进行绘图;通过SPSS21软件进行差异显著性分析。
2 结果与分析
2.1 菌株的分离及筛选
2.1.1 菌株的初筛
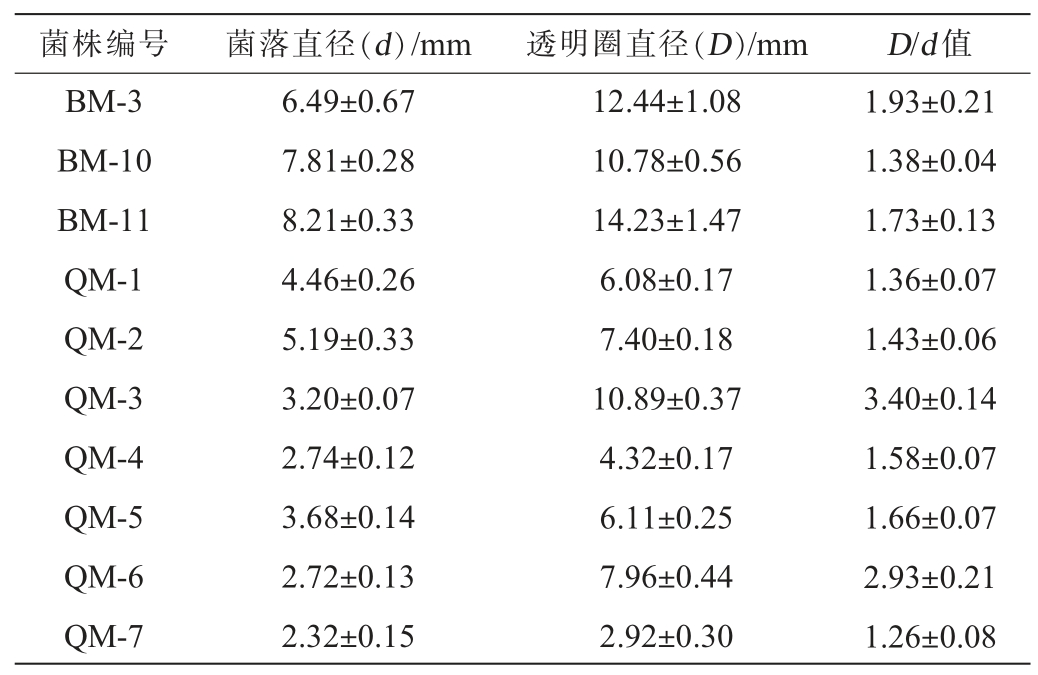
从中高温大曲样品中共筛选得到120株细菌,根据形态学鉴定结果发现有36株细菌的菌落形态与典型的芽孢杆菌极为相似,将纯化后的细菌接种在筛选培养基中,选择D/d值较大(>1.2)的结果见表2。由表2可知,共有10株菌D/d值>1.2,其均具有较强的Tween-80水解能力,其中D/d值较大的6株菌为BM-3、BM-11、QM-3、QM-4、QM-5、QM-6,将这6株菌进行菌株酯化力的测定。
表2 菌株透明圈直径测定结果
Table 2 Determination results of transparent zone diameter of the strain
2.1.2 菌株的复筛
以菌株的产酯能力为评价指标,初筛菌株BM-3、BM-11、QM-3、QM-4、QM-5、QM-6的复筛结果见图1。由图1可知,菌株酯化力与初筛测得的D/d值之间不存在严格的线性关系,可能是初筛和复筛时生长条件与培养基组成发生了改变[24],但可以明显看出菌株QM-3菌株发酵麦曲的酯化力最高为54.54U,与菌株BM-3、BM-11、QM-4、QM-5和QM-6之间存在显著差异(P<0.05)。除此之外,菌株QM-3发酵麦曲的酯化力明显高于从郎酒酒糟中筛选得到的枯草芽孢杆菌ZP-28(酯化力为28.362 U)[25],说明其具有较强的酯化能力。因此基于这些实验结果,选择菌株QM-3作为目标菌株进行耐受性试验以及菌种鉴定。
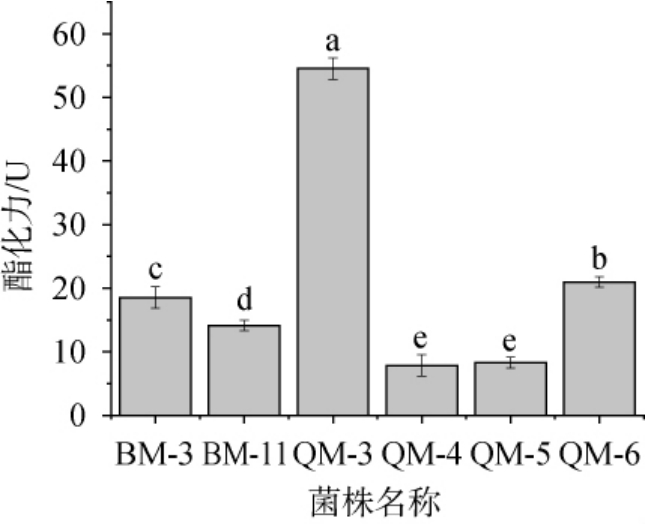
图1 初筛菌株的酯化力测定结果
Fig.1 Determination results of esterification power of preliminary screened strains
不同字母表示差异显著(P<0.05)。
2.2 菌株耐受性试验
2.2.1 耐高温试验
菌株QM-3的耐高温试验结果见表3。从表3可知,菌株QM-3具有较好的耐高温能力,当温度在45~50 ℃时,菌株QM-3的生长极为旺盛,表现出极强的生命力。在温度升高至55 ℃的情况下,该菌株依然能够保持良好的生长态势,未出现明显的生长抑制现象;即使在60 ℃时该菌株也依然可以维持生长活性并未停止生长,这表明该菌株具有较强的耐高温性。中高温大曲培曲过程中曲心温度最高可达60 ℃,此时绝大部分微生物因高温而死亡,从而影响香味物质合成和积累,因此耐高温特性对于白酒产香菌种而言至关重要[25]。
表3 菌株QM-3耐高温试验结果
Table 3 Test results of high-temperature resistance of strain QM-3
注:“+++”表明菌落生长旺盛;“++”表明菌落生长良好;“+”表明平板有菌生长;“-”表明无菌落生长,下同。
2.2.2 耐酸性试验
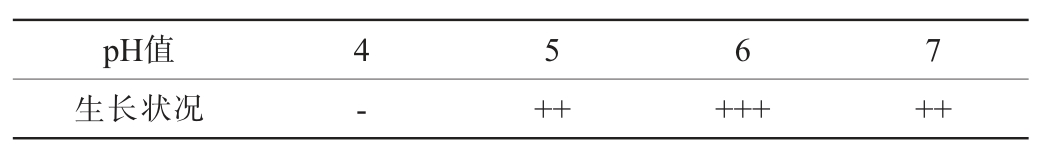
菌株QM-3的耐酸试验结果见表4。由表4可知,菌株QM-3的耐酸能力一般,当pH6时菌株生长最旺盛,代谢活动也最为活跃;当pH5时菌株表现出良好的生长态势,并未出现生长受到抑制的情况;当pH4时菌株无法进行正常的生长和繁殖,这符合芽孢杆菌最适生长pH范围。
表4 菌株QM-3耐酸性试验结果
Table 4 Test results of acid resistance of strain QM-3
2.2.3 耐乙醇试验
菌株QM-3的耐乙醇试验结果见表5。由表5可知,菌株QM-3乙醇耐受能力很强,在乙醇体积分数6%~9%时菌落生长旺盛,乙醇体积分数12%~15%时生长状况良好。在浓香型白酒的酿造过程中,随着发酵时间的延长,糟醅中的乙醇含量逐渐上升,其酒精度峰值可达到8%vol。因此,对于产香菌种而言,其对酒精的耐受性显得尤为关键,酒精耐受性不仅决定了菌种能否在较高酒精浓度环境中生存和繁殖,还直接关系到最终酒质的优劣,包括酒的风味、口感以及香气等各个方面。菌株QM-3所表现出的耐乙醇特性满足了这一生产需求。
表5 菌株QM-3耐乙醇试验结果
Table 5 Test results of ethanol resistance of strain QM-3
2.3 菌种鉴定
2.3.1 菌落形态学观察
对菌株QM-3菌落外观特性进行观察,结果见图2。由图2可知,菌落呈乳白色,圆形(直径约2~5 mm),不透明,表面褶皱,边缘不齐整,质地稠密,染色结果为革兰氏阳性菌,在显微镜下菌体呈杆状。
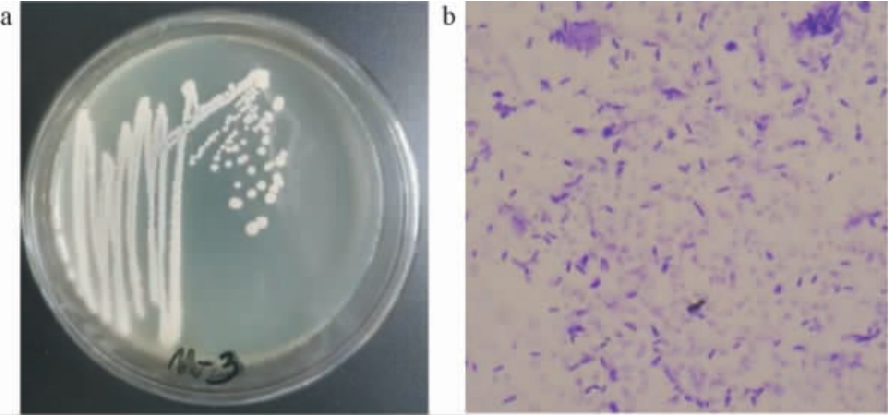
图2 菌株QM-3菌落形态(a)及细胞形态(b)
Fig.2 Colony morphology (a) and cell morphology (b) of strain QM-3
2.3.2 分子生物学鉴定
基于获得的16S rDNA序列使用MEGA 11.0软件中的邻接法构建菌株QM-3的系统发育树,结果见图3。由图3可知,QM-3与沙福芽孢杆菌(Bacillus safensis)位于同一系统发育枝上,相似度为88%,结合单菌落形态特征,确认该菌株为沙福芽孢杆菌(Bacillus safensis)。
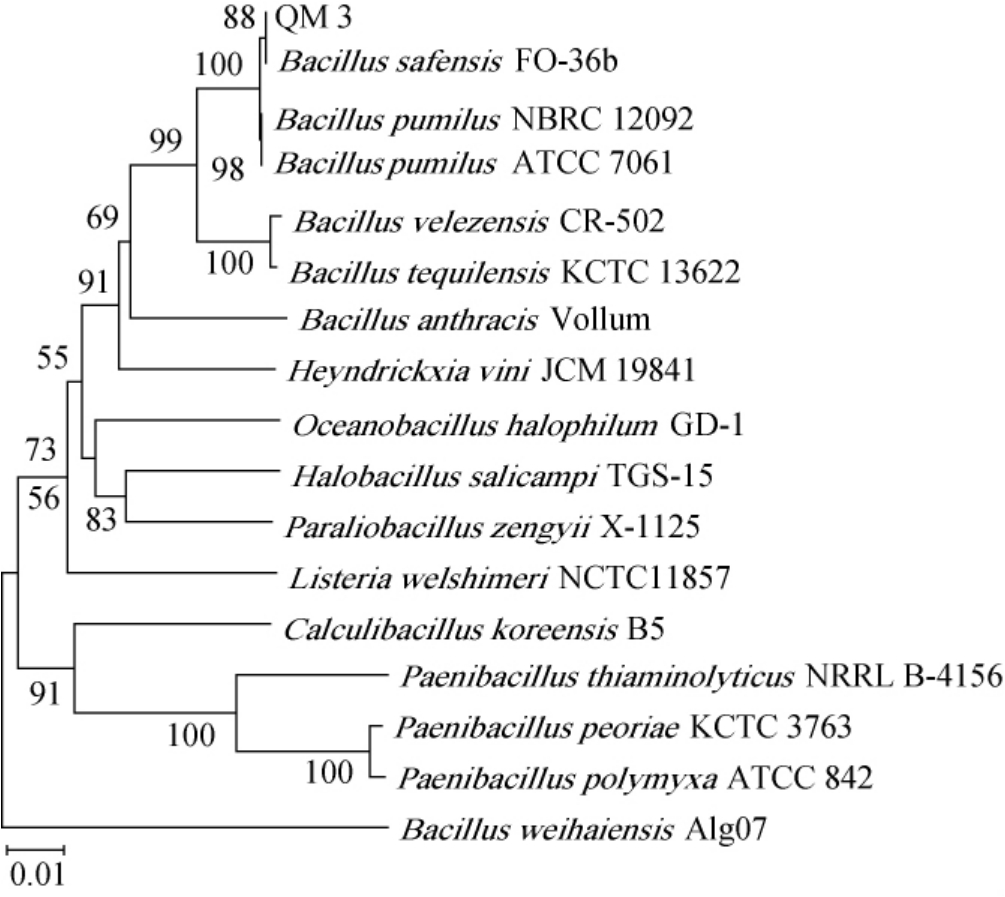
图3 基于16S rDNA序列菌株QM-3的系统发育树
Fig.3 Phylogenetic tree of strain QM-3 based on 16S rDNA sequence
2.4 发酵条件优化单因素试验
2.4.1 培养时间对菌株发酵麦曲酯化力的影响
培养时间对菌株发酵麦曲酯化力的影响结果见图4。由图4可知,随着培养时间的增加,菌株发酵麦曲的酯化力呈先上升后下降的趋势。当培养时间为48 h时,发酵麦曲酯化力较低,此时微生物的代谢活动和酶活性尚未达到最佳状态。随着培养时间的增加,酯化力不断上升,微生物代谢活动逐渐旺盛。当培养时间为72 h时达到峰值,此时微生物的代谢活动和酶活性达到了顶峰。继续延长培养时间,发酵麦曲的酯化力则呈现下降趋势。这是因为当稳定期持续一定时间后,菌种开始衰退,培养基中营养物质耗尽,发酵产物也抑制其自身的繁殖,细菌整体生长速率减慢直至停止[21]。因此最佳培养时间为72 h。
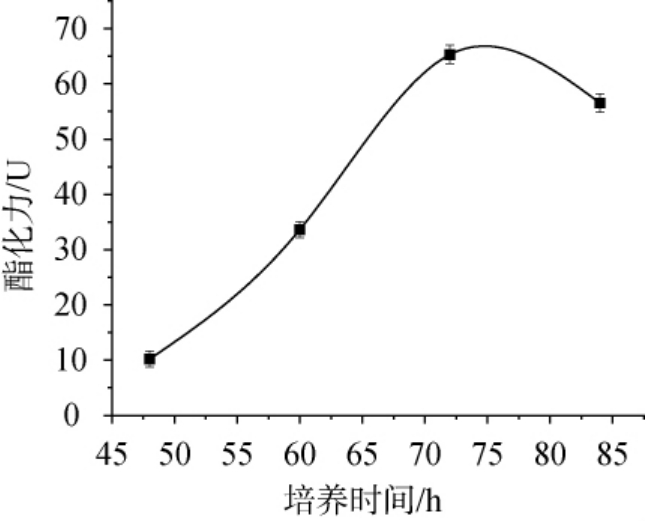
图4 培养时间对菌株发酵麦曲酯化力的影响
Fig.4 Effect of culture time on the esterification power of wheat Qu fermented by the strain
2.4.2 接种量对菌株发酵麦曲酯化力的影响
接种量对菌株发酵麦曲酯化力的影响结果见图5。由图5可知,随着接种量增加,发酵麦曲酯化力呈现先上升后趋于平稳的态势。当接种量为1%时,发酵麦曲的酯化力较低。接种量提升至2%时,发酵麦曲的酯化力达到峰值,与1%接种量相比有很大提升。随后继续增加接种量,发酵麦曲的酯化力趋于稳定甚至略有下降。这是因为接种量较少时,微生物从延滞期到稳定期的时间延长,不利于产酶;接种量增加时,在一样的发酵时间内会使菌体迅速繁殖提前进入稳定期和衰老期,导致营养物质被迅速且大量地消耗掉,不利于稳定产酶[21,26]。因此最佳菌株接种量为2%。
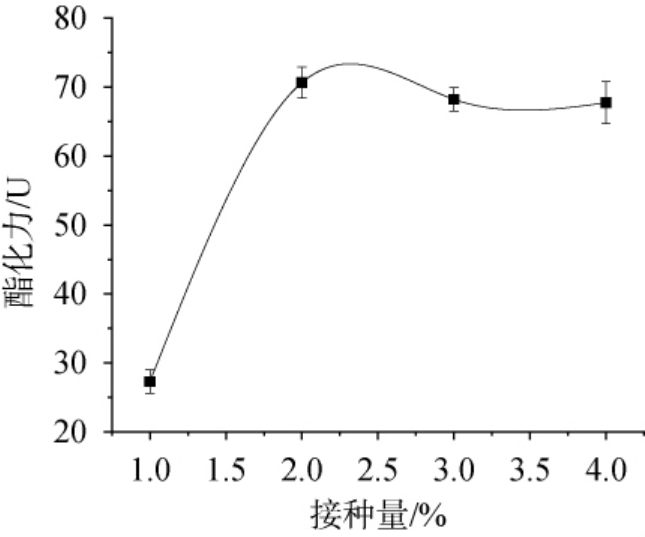
图5 接种量对菌株发酵麦曲酯化力的影响
Fig.5 Effect of inoculum on the esterification power of wheat Qu fermented by the strain
2.4.3 培养温度对菌株发酵麦曲酯化力的影响
培养温度对菌株发酵麦曲酯化力的影响结果见图6。由图6可知,当培养温度为37~52 ℃时,随着温度升高发酵麦曲的酯化力不断上升,并在46 ℃时达到峰值。随后再提高培养温度麦曲酯化力出现降低趋势。这是因为温度会影响菌株的生长,当温度较低时,菌株生长缓慢导致产酯酶量低;当温度过高时菌株生长受到抑制甚至失活,酯化酶的产出减少,并且会使酯化酶活力下降[27]。因此最佳培养温度为46 ℃。
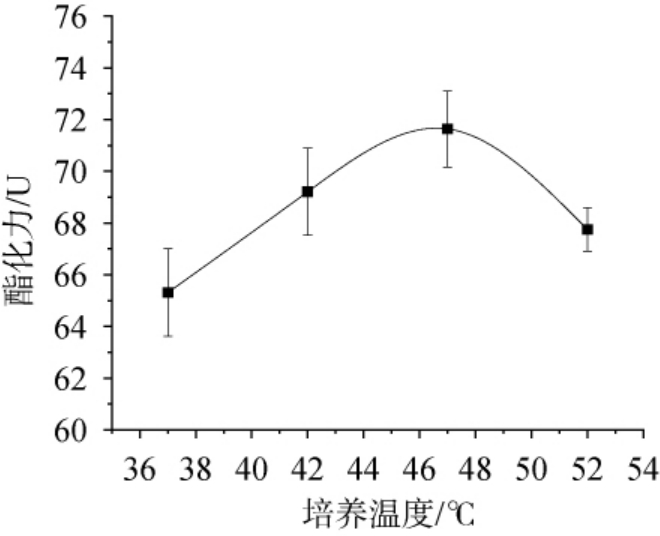
图6 培养温度对菌株发酵麦曲酯化力的影响
Fig.6 Effect of culture temperature on the esterification power of wheat Qu fermented by the strain
2.5 响应面试验
在单因素试验的基础上,以培养时间(A)、接种量(B)和培养温度(C)为自变量,以菌株发酵麦曲酯化力为评价指标进行响应面试验,使用Design-Expert 13.0软件设计3因素3水平的Box-Behnken响应面试验,试验设计与结果见表6,方差分析结果见表7。
表6 菌株发酵条件优化Box-Behnken试验设计及结果
Table 6 Design and results of Box-Behnken experiments for fermentation conditions optimization of the strain
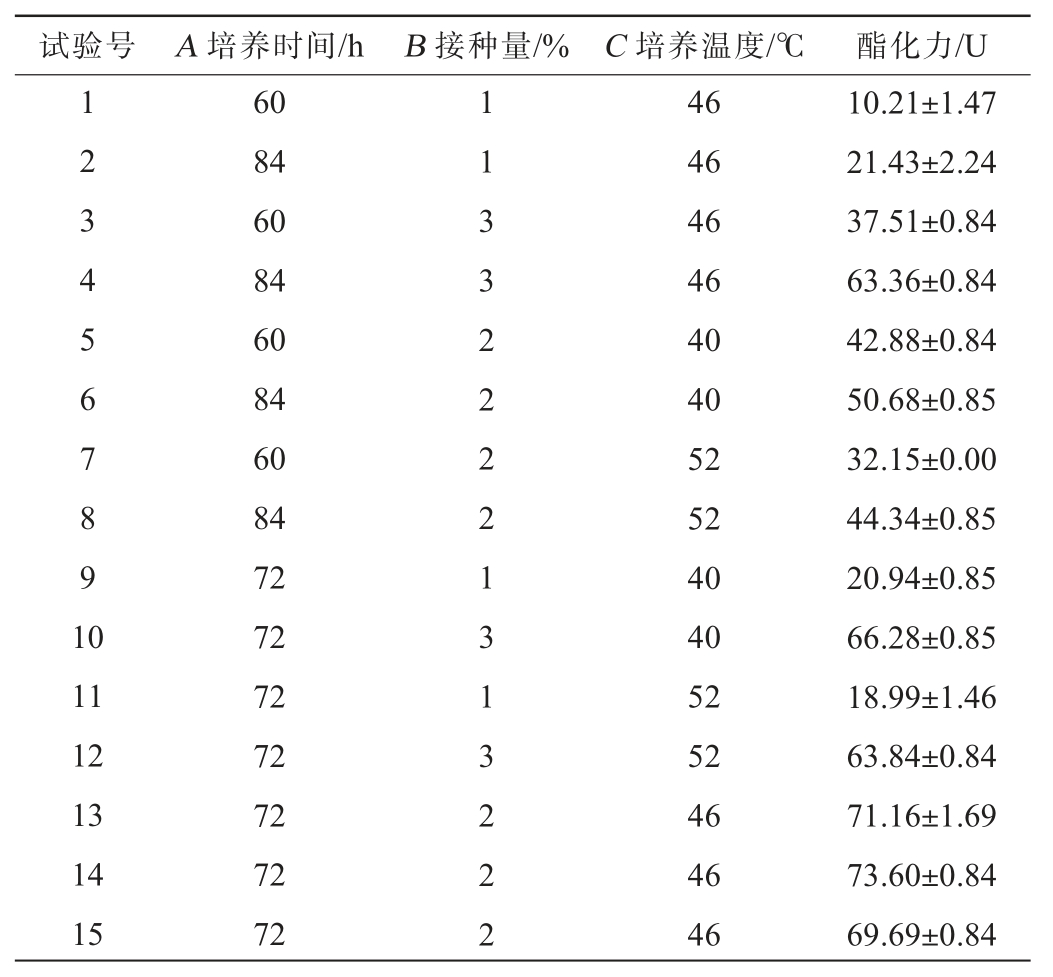
表7 回归模型方差分析
Table 7 Variance analysis of regression model
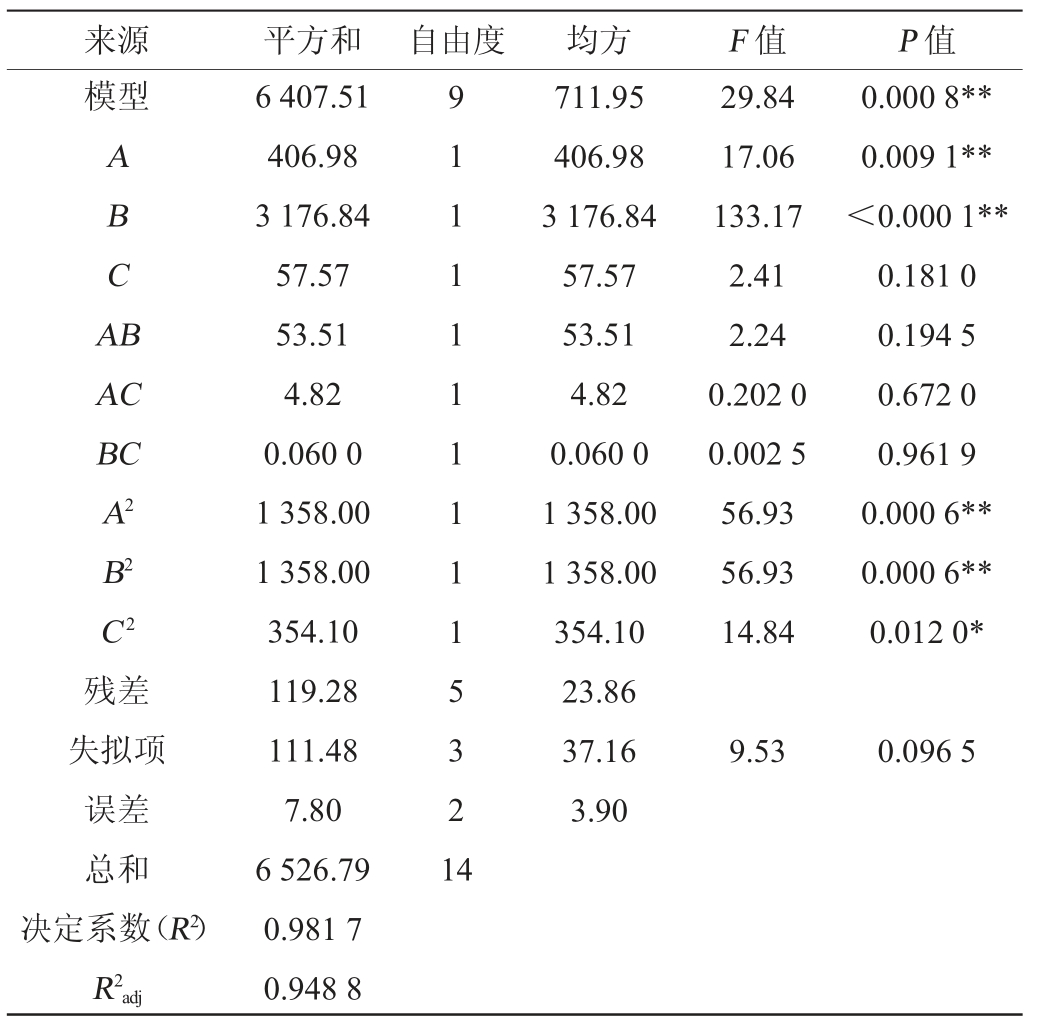
注:“**”表示对结果影响极显著(P<0.01),“*”表示对结果影响显著(P<0.05)。
使用Design-Expert13.0软件对结果进行多元二次回归拟合,得到酯化力的二元多项式回归方程为Y=71.48+7.13A+19.93B-2.68C+3.66AB+1.10AC-0.122 5BC-19.18A2-19.18B2-9.79C2。由表7可知,构建的模型存在极显著差异(P<0.01),说明具有统计学意义。失拟项无显著差异(P>0.05),说明模型高度拟合,决定系数R2为0.981 7,说明回归方程拟合程度较好,基于该回归方程所确定的最优条件科学可靠。由P值可知,一次项A、B,二次项A2、B2对结果影响极显著(P<0.01),C2对结果影响显著(P<0.05)。由F值可知,各因素对酯化力的影响顺序为接种量(B)>培养时间(A)>培养温度(C)。
根据二次响应面回归方程,用Design-Expert 13.0软件绘制各因素响应面交互作用图,结果见图7。等高线的疏密度和形状能反映因素间交互作用的显著性[28],曲面越陡、倾斜度越高,说明各因素间交互作用对响应值的影响越大[29]。
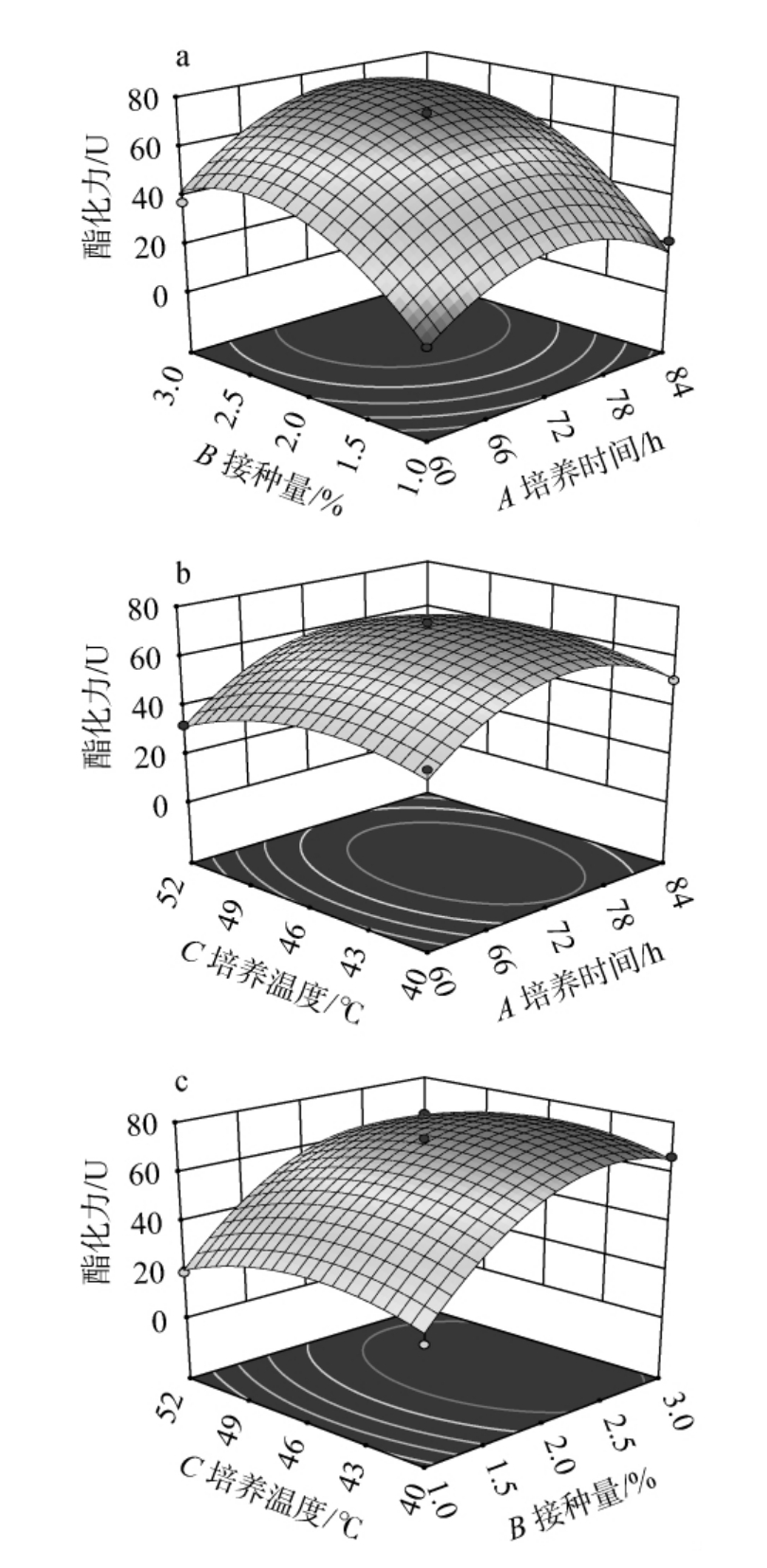
图7 培养时间、接种量和培养温度交互作用对酯化力影响的响应面和等高线
Fig.7 Response surface plots and contour lines of effect of interaction between culture time,inoculum and culture temperature on esterification power
由图7a可知,培养时间和接种量交互作用响应面等高线明显呈圆形,说明两者交互作用对酯化力影响不显著;由图7b可知,培养时间和培养温度交互作用响应面坡度较缓说明两者交互作用对酯化力影响不显著;由图7c可知,接种量和培养温度之间交互作用响应面坡度也比较平缓说明两者交互作用对酯化力影响不显著,与方差分析结果一致。
根据回归方程模型预测的最佳发酵条件为培养时间74.8h、接种量2.81%,培养温度45.7℃,此时酯化力为76.43U,为方便实际操作,将最优发酵条件修正为培养时间75 h、接种量2.8%,培养温度46 ℃,此条件下菌株的酯化力为76.52 U,与预测值相差不大,表示优化条件具有可行性。
2.6 强化大曲的制备
2.6.1 感官结果
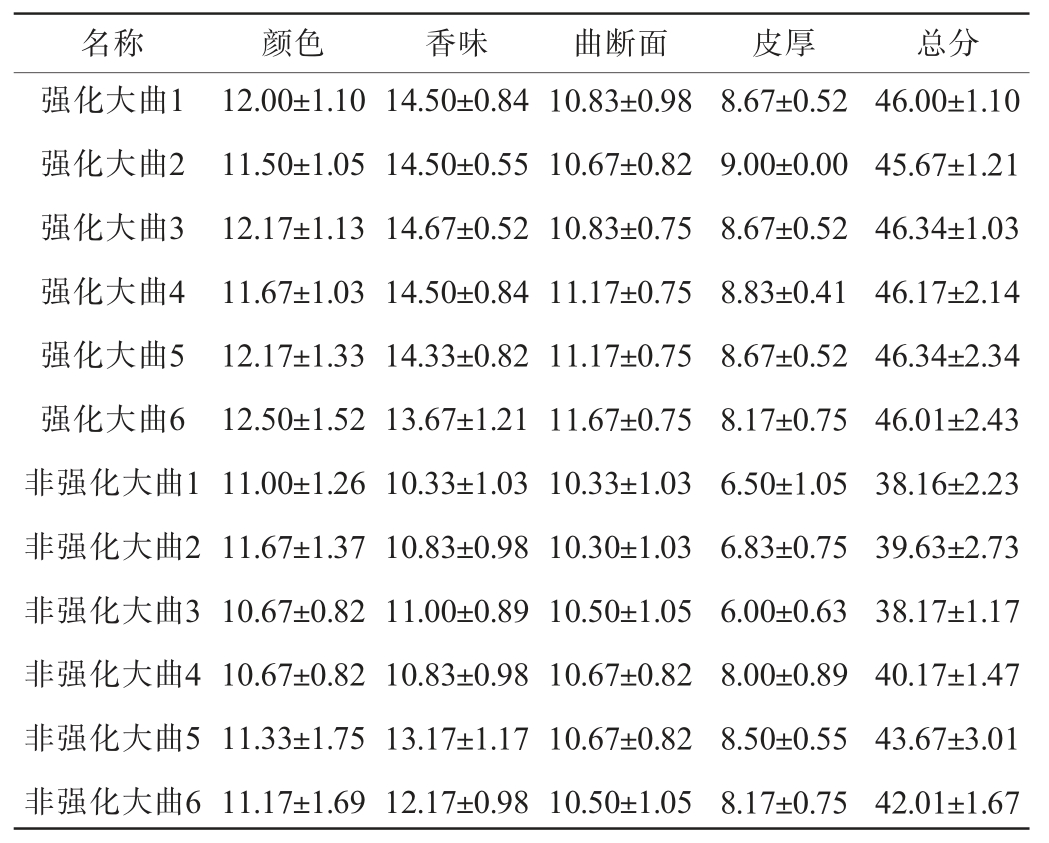
贮存3个月后强化大曲和未强化大曲外观见图8。在香气方面,强化曲的曲香味相较于未强化的普通中高温大曲更为浓郁,不仅散发出独特的曲香,还融合了粮食的醇厚香气和果香的清新甜美,使得整体香气层次更加丰富,复合香更为浓厚。由图8可知,在曲皮方面,强化大曲的曲皮明显比未经过强化的大曲曲皮要更薄,没有明显的裂缝和水圈现象,但是未强化大曲则有明显的裂缝及水圈现象,这些会影响微生物、酶活性降低大曲品质间接影响白酒的产量并可能破坏白酒原有风味。此外在大曲横断面方面,强化曲的菌丝生长状况较未强化大曲更为旺盛,菌丝密集且分布均匀,曲心部分呈现出浅褐色,色泽均匀,质地紧实,表明发酵过程充分且稳定。经过感官评价小组进行评估,大曲感官评价结果见表8。由表8可知,强化大曲的颜色、香味、曲断面和皮厚指标平均感官总得分达到46.088分,而未强化曲的平均感官总得分为40.302分。强化大曲的平均感官总得分高于未强化曲,且强化大曲平均感官总得分超过45分,达到优级曲标准。

图8 强化大曲(a)和未强化大曲(b)的外观对比结果
Fig.8 Appearance comparison results of the fortified Daqu (a) and the non-fortified Daqu (b)
表8 大曲感官评价结果
Table 8 Sensory evaluation results of Daqu
2.6.2 理化指标测定结果
贮存3个月后强化和未强化大曲理化指标对比见表9。
表9 强化和未强化的大曲理化指标对比
Table 9 Comparison of physicochemical indexes of fortified and non-fortified Daqu

注:同一列的不同字母代表显著性差异(P<0.05)。
由表9可知,强化大曲的水分和酯化力比未强化大曲高,但糖化力、液化力、发酵力和酸度稍低于未强化曲,这可能是因为添加芽孢杆菌影响了大曲内部的微生物种群结构及其数量分布,同时也改变了大曲中微生物的生态平衡,影响了某些关键酶的活性。有研究人员从郎酒酒糟中筛选并优化发酵条件得到酯化力达到33.6 U的枯草芽孢杆菌,其菌种酯化力低于本研究得到的菌株[30]。有研究人员将一株地衣芽孢杆菌(B.licheniformis)应用于浓香型大曲中得到的菌株强化大曲酯化力为386.70 U[31],低于本研究制备的强化大曲。因此添加QM-3制备强化曲酯化力提升较为显著,在生产过程中可以促进白酒风味物质的生成。
3 结论
本研究从北方某名优酒厂中高温大曲中筛选高酯化力芽孢杆菌,最终筛选出沙福芽孢杆菌(Bacillus safensis)QM-3。通过单因素试验及响应面试验设计优化得到菌株QM-3的最佳发酵条件为培养时间75 h、接种量2.8%、培养温度46 ℃,在此条件下酯化力为76.52 U,将其应用于强化大曲中能明显提高白酒中高温大曲的酯化力,显著提高大曲品质。本研究筛选得到的菌株具有更优良的酯化能力,其制备的强化大曲在白酒发酵过程中具有应用的潜力,在改善白酒产品的感官品质、风味层次以及提高产品的稳定性和一致性方面,具有一定的现实意义和应用价值。
[1] TU W Y,CAO X N,CHENG J,et al.Chinese Baijiu:the perfect works of microorganisms[J].Front Microbiol,2022,13:919044.
[2] OWUSU-KWARTENG J,TANO-DEBRAH K,AKABANDA F,et al.Technological properties and probiotic potential of Lactobacillus fermentum strains isolated from west African fermented millet dough[J]. BMC Microbiol,2015,15(1):261.
[3] JIN G Y,ZHU Y,XU Y.Mystery behind Chinese liquor fermentation[J].Trends Food Sci Tech,2017,63:18-28.
[4] LI H D,LIU S Y,LIU Y B,et al.Functional microorganisms in Baijiu Daqu:Research progress and fortification strategy for application[J].Front Microbiol,2023,14:1119675.
[5] LI W W,FAN G S,FU Z L,et al.Effects of fortification of Daqu with various yeasts on microbial community structure and flavor metabolism[J].Food Res Int,2019,129:108837.
[6] 梁慧珍,卢延想,刘正,等.高温大曲中高产吡嗪类物质芽孢杆菌的筛选与应用[J].中国酿造,2022,41(1):116-122.
[7] 宋川,刘双平,敖宗华,等.白酒酿造微生物酯化酶的研究进展[J].酿酒,2024,51(2):34-40.
[8] 蒋倩儿,梁会朋,李琳琳,等.芽孢杆菌在白酒酿造过程中的应用研究进展[J].食品工业科技,2025,46(8):391-401.
[9] XIA Y,LUO H B,WU Z Y,et al.Microbial diversity in Jiuqu and its fermentation features: Saccharification,alcohol fermentation and flavors generation[J].Appl Microbiol Biot,2022,107(1):25-41.
[10] 罗莉,李欣,常煦,等.芽孢杆菌在中国白酒酿造中的应用机理研究进展[J].酿酒科技,2019(1):99-104.
[11] 申孟林.浓香型白酒大曲发酵成熟过程中四种主要酶产生菌多样性分析[D].成都:西华大学,2019.
[12] 侯小歌,张杰,孙忠科,等.大曲产酯化酶芽孢菌的分离鉴定及其发酵条件优化研究[J].轻工学报,2018,33(4):13-20.
[13] 张颖.酱香型白酒高产四甲基吡嗪芽孢杆菌的筛选及应用[D].天津:天津科技大学,2023.
[14] HE G,DONG Y,HUANG J,et al.Alteration of microbial community for improving flavor character of Daqu by inoculation with Bacillus velezensis and Bacillus subtilis[J].LWT-Food Sci Tech,2019,111(4):1-8.
[15] 倪雪.凤香型大曲酯化力的测定方法探讨[J].酿酒,2015,42(3):70-72.
[16] 史洪丽,余梦婷,王世昕,等.高温大曲中高产四甲基吡嗪芽孢杆菌的筛选及其在酒醅堆积中的应用[J].中国酿造,2025,44(3):59-65.
[17] 贺奕森,唐涛,周玉岩,等.大曲中高产酯化酶霉菌的分离鉴定[J].中国食品工业,2023(2):105-107.
[18] 颜丽,刘秀河,李同乐.梁山大曲中高酯化力菌株的筛选及鉴定[J].中国酿造,2020,39(1):104-107.
[19] LIU Y B,LI M K,HONG X F,et al.Screening and identification of high yield tetramethylpyrazine strains in Nongxiangxing liquor Daqu and study on the mechanism of tetramethylpyrazine production[J].J Sci Food Agr,2023,103(14):6849-6860.
[20] TAMURA K,STECHER G,KUMAR S.MEGA11:Molecular evolutionary genetics analysis version 11[J]. Mol Biol Evol,2021,38(7): 3022-3027.
[21] 程爽,包朋鑫,徐玉晨,等.一株脂肪酶产生菌的筛选鉴定及其发酵条件优化[J].中国食品添加剂,2021,32(11):73-80.
[22] 李超伟,侯晓艳,张宿义,等.白酒大曲中氨基甲酸乙酯降解菌株的筛选及共发酵培养条件的优化[J].食品科学,2025,46(5):151-160.
[23] 董大伟,王晓慧,苏葛,等.中高温大曲存储后的感官质量研究[J].酿酒科技,2018(12):39-44.
[24] 鄢洪德,汪钊,李光伟.产酯酶微生物菌种的筛选研究[J].工业微生物,2007,37(6):44-48.
[25] 陈剑,蒋英丽,程伟,等.酱香型白酒酒糟中耐酸产酯香细菌的筛选[J].酿酒科技,2016(2):61-64.
[26] 胡斌.青砖茶渥堆中产脂肪酶菌株的筛选与应用[D].武汉:华中农业大学,2019.
[27] 朱俊颖,夏芊芊,甘晋铭,等.高产酯化酶红曲霉的筛选、鉴定及其产酶条件优化[J].中国酿造,2024,43(12):103-109.
[28] ÜNSAL MEHMET,I IK-GÜLSAÇ I IL,ÜRESIN ERSIN,et al.Optimisation of biomass catalytic depolymerisation conditions by using response surface methodology[J].Waste Manage Res,2019,3:322-331.
[29] 贺奕森.浓香型白酒大曲中霉菌的分离鉴定及应用[D].邯郸:河北工程大学,2023.
[30] 周榆林,陈剑,钟明叶,等.一株耐酸高酯化力细菌的鉴定及发酵条件研究[J].酿酒科技,2018(12):27-32.
[31] 陈晓茹,黄钧,周荣清,等.不同强化方式对浓香型白酒大曲特性的影响[J].食品与发酵工业,2021,47(15):50-55.