高血压是导致人类残疾和过早死亡的主要风险因素[1-2]。该病症通常伴有脑梗死、脑出血和肾脏损伤等,对公众健康构成严重威胁[3]。在高血压临床治疗中,传统药物虽有效控制血压,但长期服用可能引起一系列副作用[4]。如血管紧张素转换酶抑制剂可能引发头痛、心动迟缓和支气管痉挛等;钙通道阻滞剂则可能导致踝部水肿和面部潮红等不良反应[5]。相比之下,功能食品通过日常调节机体功能,如调节血压血糖血脂及增强免疫力等达到保健效果,具有安全性高、可长期食用等优势[6]。
山西老陈醋是我国四大名醋之首,除风味独特外,还具有降血压[7]、降血脂[8]及抗氧化[9]等多种健康功效,其功效成分主要包括有机酸、氨基酸[10]和多酚类化合物[11]。相关研究发现,老陈醋在生产过程中形成的类黑精具有抗氧化、抗菌及抗高血压等多种功效[12];此外,老陈醋所含有的川芎嗪不仅是发酵香气的重要来源,还具有强心、扩张血管和改善心脑血管的功能[13]。杜仲(Eucommia ulmoides)叶是杜仲科植物杜仲的干燥叶,富含黄酮类、酚酸类等化学成分,并含有维生素和氨基酸等营养元素,在发挥降压功效的同时兼具保护器官的作用,是1种温和无毒的天然降压药,具有良好应用前景[14-16]。罗布麻(Apocynum venetum)叶是1种传统中药材,以其金丝桃苷、槲皮素等优势化学成分来发挥降压、镇静、保护心脏及调节肠道菌群等多重功效,可作为1种天然的生物保健植物[17-21]。
随着经济社会的飞速发展,人们生活节奏和饮食习惯不断调整,健康意识不断增强,功能食品愈发受到人们青睐[22]。鉴于山西老陈醋在维持血压健康方面的潜力尚未被充分揭示,且中草药及其提取物用于降血压和改善多种心血管疾病的有效食物疗法有待深入挖掘[23]。因此,本研究以山西老陈醋为基础,科学复配杜仲叶与罗布麻叶水提液,制备1款具有降血压功效的复方醋口服液。选择自发性高血压大鼠(spontaneous hypertensionrat,SHR)为研究对象进行体内实验,测定各组大鼠体质量、血压、心率、脏器指数、血清生化指标,并结合代谢组学技术,筛选复方醋口服液缓解高血压疾病的潜在代谢通路及差异代谢物,验证其降血压的作用效果,旨在为研发具有维持血压健康水平功效的功能食品提供科学依据。
1 材料与方法
1.1 材料与试剂
山西老陈醋:山西紫林醋业股份有限公司;杜仲叶(执行标准:《中国药典》2020年):河北嘉恒冷背药业有限公司;罗布麻叶(执行标准:《中国药典》2020年):邵阳神农中药科技发展有限公司。
Wistar大鼠和无特定病原体(specific pathogen free,SPF)级SHR雄性大鼠(体质量为180~220 g,10周龄,动物实验许可证号(SCXK(京)2024-0001)),大鼠垫料和饲料:斯贝福(北京)生物技术有限公司。
木糖醇、三氯乙醛水合物(均为分析纯):上海麦克林化学试剂有限公司;硝苯地平片(10 mg/片):石药集团欧意药业有限公司;一氧化氮(nitric oxide,NO)试剂盒:南京建成生物工程研究所;内皮型一氧化氮合酶(endothelial nitricoxidesynthase,eNOs)试剂盒、血管紧张素Ⅱ(angiotensin II,AngⅡ)试剂盒、内皮素(endothelin,ET)试剂盒、去甲肾上腺素(norepinephrine,NE)试剂盒、前列腺素2(prostaglandin E2,PGE2)试剂盒、前列环素2(prostaglandin I2,PGI2)试剂盒、内皮源性超极化因子(endothelium derived hyperpolarizing factor,EDHF)试剂盒、醛固酮(aldosterone,ALD)试剂盒:上海酶联生物科技有限公司。
1.2 仪器与设备
SB25-12D超声波清洗机:宁波新芝生物科技股份有限公司;TG16-WS台式高速离心机:湖南湘仪实验室仪器开发有限公司;Heidolph旋转蒸发仪:德国HITACHI公司;SYNEK GY4多功能酶标仪:美国Bio Tek公司;Medlab大小鼠无创性血压测量系统:南京卡尔文生物科技有限公司。
1.3 方法
1.3.1 复方醋口服液的制备工艺流程及操作要点
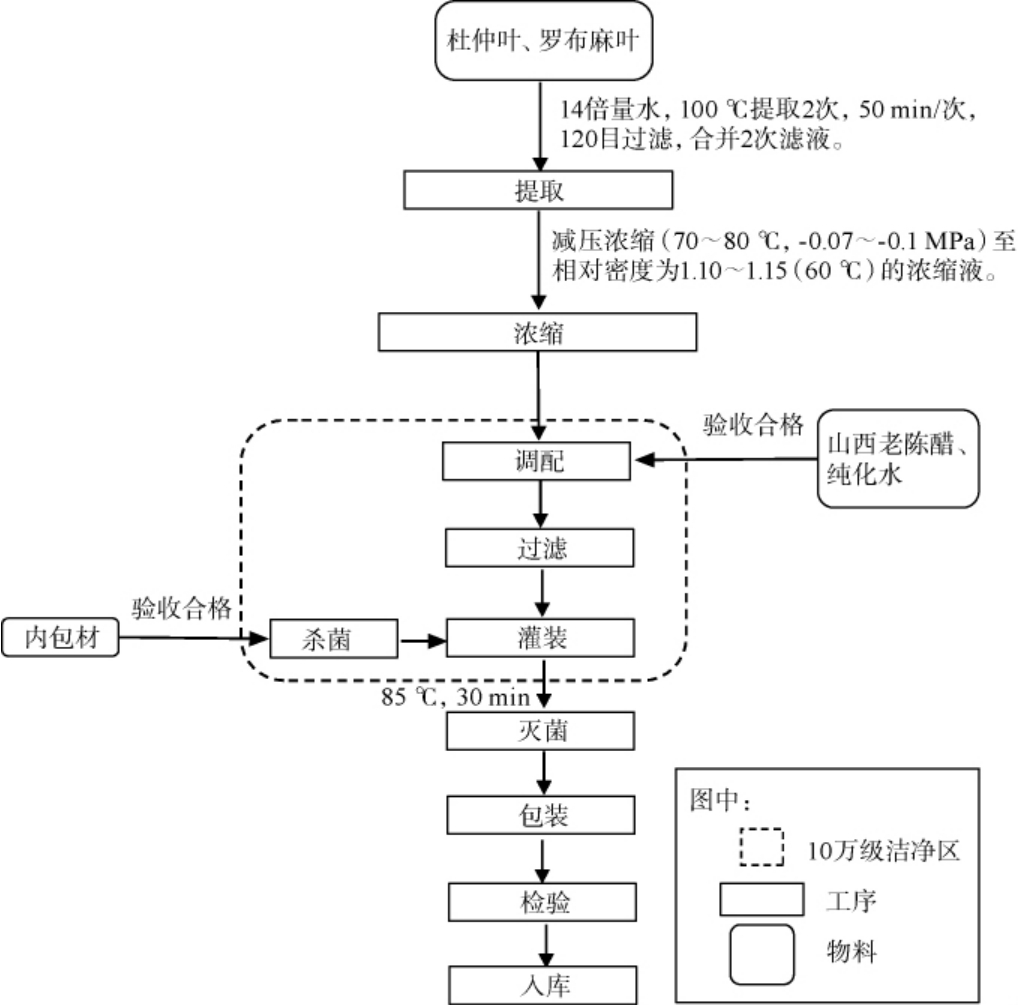
操作要点:
原料预处理:杜仲叶和罗布麻叶按质量比1∶1投料混合,采用水提法,按料液比为1∶14(kg/L)加水浸泡,100 ℃煎煮50 min,煎煮后过滤,煎煮2次,收集合并滤液,减压浓缩至滤液原体积的0.04倍,得浓缩液A。
调配过滤:取山西老陈醋(质量为杜仲叶原料质量的2倍)减压浓缩至原体积的50%后与浓缩液A复配混匀,添加木糖醇(质量为杜仲叶原料质量的50%)提高适口性并过滤。
灭菌:采用巴氏灭菌法,于65 ℃灭菌30 min,随后冷却至室温。
包装检验:将灭菌完成的口服液灌装于10 mL棕色玻璃瓶中,参照GB 4789.1—2016《食品安全国家标准 食品微生物学检验总则》检验合格后,即得复方醋口服液成品。
1.3.2 动物分组及给药
采用Wistar大鼠作为正常组(normalgroup,NC);将SHR大鼠随机分为模型组(model group,Model)、阳性对照组(positive control group,PC)、低剂量组(low-dose group,LD)、中剂量组(medium-dose group,MD)、高剂量组(high-dose group,HD),共计5组,每组10只。正常组及模型组均灌胃生理盐水;阳性对照组使用硝苯地平片,按体质量6 mg/kg的剂量灌胃;复方醋口服液低剂量组按体质量1.74 mL/kg的剂量灌胃,中剂量组按体质量3.48 mL/kg的剂量灌胃,高剂量组按体质量6.96 mL/kg的剂量灌胃,每日一次,各实验组均灌胃4周。
1.3.3 大鼠体质量、血压及心率的测定
每周对大鼠体质量进行测量;使用大小鼠无创血压测量系统,多次测量使大鼠适应测压环境,检测并记录大鼠清醒、安静状态下的收缩压、舒张压及心率。
1.3.4 大鼠血清及内脏组织收集
大鼠血清收集及保存:各组大鼠禁食12 h后,腹腔注射10%水合氯醛进行麻醉,随后心尖采血,血浆3 000 r/min离心15 min后取上层血清,-80 ℃保存。
大鼠内脏组织收集及脏器指数计算:经上述采血后,将处于麻醉状态的大鼠采用颈椎脱臼法处死,随后进行解剖,取心、肝、肾内脏称质量,计算其脏器指数,计算公式如下:
1.3.5 大鼠血清生化指标的测定
大鼠血清中血压相关因子(NO、eNOs、EDHF、PGE2、PGI2、ET、NE、AngII、ALD)含量:采用各因子试剂盒测定。
1.3.6 非靶向代谢组学检测
正常组(NC)、模型组(Model)、复方醋口服液中剂量组(MD)三组大鼠心尖采血后,血浆3 000 r/min离心15 min后取上层血清,-80 ℃保存血清样品。每组4个血清样本交由上海美吉生物医药科技有限公司对各组血清样本进行非靶向代谢组学检测分析。基于检测结果,在美吉生物云平台(https://cloud.majorbio.com)进行数据处理,采用主成分分析(principal component analysis,PCA)、正交偏最小二乘判别分析(orthogonal partial least squares discriminant analysis,OPLS-DA)、变量重要性投影(variable importance in projection,VIP)值对代谢物进行分析比较,揭示不同组别的代谢物成分差异。将P值<0.05且VIP值>1的代谢物定义为差异代谢物,绘制火山图。基于京都基因与基因组百科全书(Kyoto Encyclopedia of Genes and Genomes,KEGG)数据库(https://www.kegg.jp/kegg/pathway.html),对检测到的差异代谢物进行KEGG注释,通过富集分析和拓扑学分析以探究相关的代谢通路,并利用KEGG Mapper可视化工具对关键通路的代谢物作图。
1.3.7 数据处理
采用Origin 2018软件绘图,SPSS 27.0.1软件进行方差分析(analysis of variance,ANOVA)(P<0.05认为差异显著),结果以“平均值±标准差”表示。
2 结果与分析
2.1 复方醋口服液对大鼠血压的影响
分别对各组大鼠的收缩压(systolic blood pressure,SBP)和舒张压(diastolic blood pressure,DBP)进行动态检测分析,结果见图1。由图1可知,在灌胃期间,NC组Wistar大鼠的血压无明显波动且模型组(Model)SHR大鼠收缩压和舒张压在实验前后均显著高于NC组(P<0.05),说明该高血压模型建立成功。灌胃4周后,Model组SHR大鼠收缩压为(220.09±8.76)mmHg,舒张压为(160.97±8.01)mmHg,显著高于阳性对照组(PC)及复方醋口服液各剂量组(P<0.05),说明阳性药物及各剂量复方醋口服液均能有效降低SHR大鼠的血压。PC组与LD、MD和HD组相比,阳性药物治疗大鼠高血压的效果更佳。复方醋口服液各剂量干预后,大鼠收缩压均维持在(160.78±4.88)mmHg,舒张压均维持在(110.93±4.18)mmHg,表明复方醋口服液在1.74~6.96 mL/kg范围内对自发性高血压大鼠具有显著降血压作用(P<0.05)。
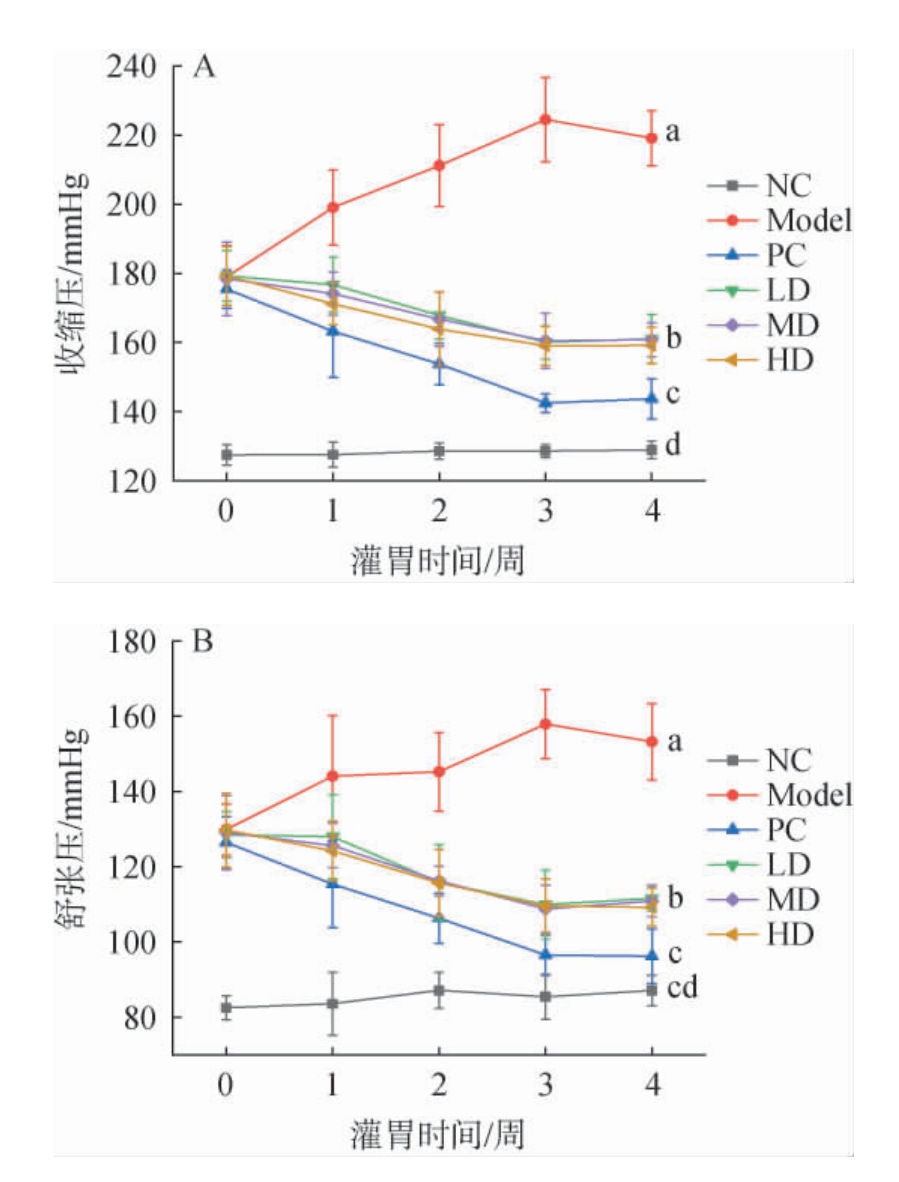
图1 复方醋口服液对大鼠收缩压(A)和舒张压(B)的影响
Fig.1 Effect of compound vinegar oral liquid on systolic (A) and diastolic (B) blood pressure of rats
不同小写字母表示各实验组间差异显著(P<0.05),下同。
2.2 复方醋口服液对大鼠心率及体质量的影响
复方醋口服液对SHR大鼠体质量的影响见图2A。由图2A可知,实验开始时,各组大鼠的体质量无显著性差异(P>0.05);模型组(Model)、阳性对照组(PC)和复方醋口服液各剂量组(LD、MD和HD)于第2周开始,体质量均显著低于正常组(NC)(P<0.05),说明高血压疾病对大鼠自身生长状况有着不良影响,会造成生长缓慢。经4周喂养后,Model组、PC、LD、MD和HD组大鼠的体质量分别为(310.35±6.40)g、(311.62±10.51)g、(314.22±10.46)g、(315.00±8.20)g和(314.75±11.48)g,均无显著差异(P>0.05),说明阳性药物及各剂量复方醋口服液对SHR大鼠生长状况无负面影响,同时可排除各组间大鼠因体质量差异所造成的实验误差。复方醋口服液对SHR大鼠心率的影响见图2B。由图2B可知,实验前后,Model组及PC、LD、MD和HD组SHR大鼠心率在460 bpm上下波动,均显著高于NC组(P<0.05),这一现象符合自发性高血压大鼠常伴随交感神经兴奋导致心率加快等症状[24],进一步验证了模型的可靠性。Model组大鼠心率与LD、MD和HD组间均无显著差异(P>0.05),说明复方醋口服液对SHR大鼠的心率不会造成负面影响。
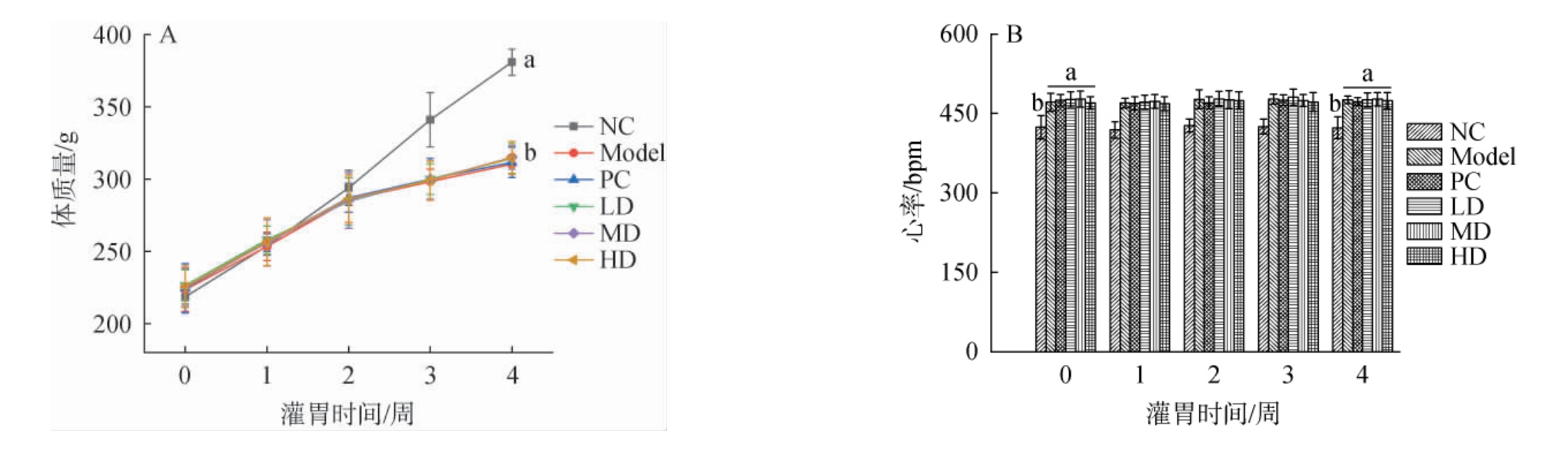
图2 复方醋口服液对大鼠体质量(A)和心率(B)的影响
Fig.2 Effect of compound vinegar oral liquid on body weight (A) and heart rate (B) of rats
2.3 复方醋口服液对大鼠脏器指数的影响
灌胃4周后各实验组大鼠脏器的质量及脏器指数结果见表1。由表1所示,与正常组(NC)大鼠相比,其余各组SHR大鼠的空腹体质量、心质量、肝质量、肾质量及心脏指数均显著降低(P<0.05),肝脏指数无显著差异(P>0.05),肾脏指数差异较小。这表明自发性高血压通常会导致大鼠体内内脏器官的损伤病变,造成心脏、肾脏等脏器质量降低。与Model组相比,PC与LD、MD、HD组大鼠各脏器指数间无显著差异(P>0.05),说明阳性药物及各剂量复方醋口服液均不会损伤自发性高血压大鼠的心、肝、肾脏等器官。
表1 复方醋口服液对大鼠脏器指数影响
Table 1 Effect of compound vinegar oral liquid on organ index of rats
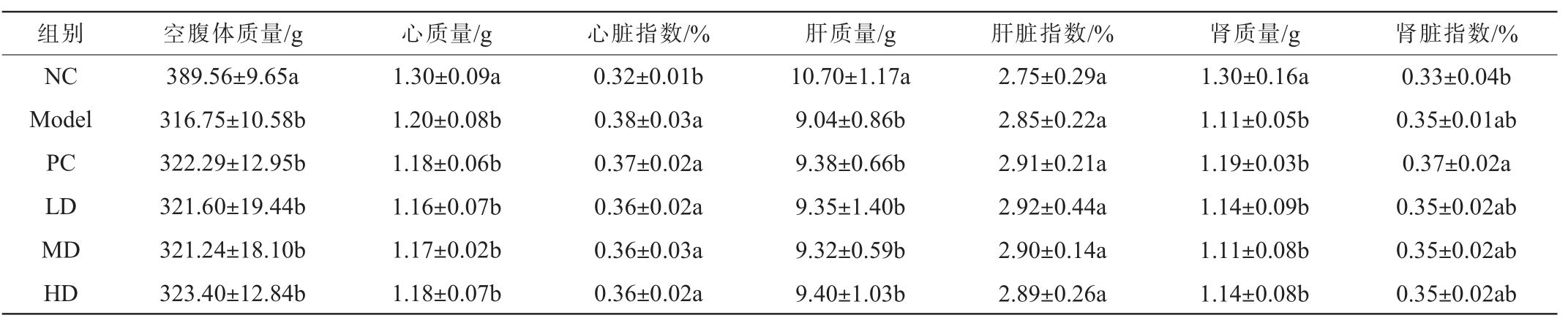
注:同一列不同小写字母表示各实验组间差异显著(P<0.05)。
2.4 复方醋口服液对大鼠血清血管舒张因子含量的影响
内皮型一氧化氮合酶(eNOS)是合成一氧化氮(NO)的关键酶,可维持血管正常形态、抑制血管平滑肌细胞增殖及保护血管内皮,在心脑血管疾病预防及治疗中发挥着重要作用[25]。由图3A、图3B可知,模型组(Model)大鼠血清中NO和eNOS含量分别为(3.23±0.59)μmol/L和(31.79±4.03)pg/mL,显著低于NC组(P<0.05)。经过4周灌胃干预后,阳性对照组(PC)和复方醋低剂量组(LD)的NO和eNOs水平有所改善;而复方醋口服液中、高剂量组(MD和HD)舒张因子的含量显著提高(P<0.05),NO含量分别为(3.93±0.38)μmol/L和(3.99±0.39)μmol/L,eNOs含量分别为(38.85±2.93)pg/mL和(38.83±2.27)pg/mL,进而发挥出更好的血管内皮保护作用。EDHF作为血管内皮细胞释放的舒血管物质,可通过激活平滑肌细胞钾通道引起超极化,抑制钙内流,从而舒张血管、降低血压[26]。PGE2和PGI2同样作为参与心血管稳态调节的重要舒血管物质,具有扩张血管、抑制血小板聚集等作用[27]。由图3C~图3E可知,与NC组相比,Model组大鼠血清EDHF、PGE2和PGI2含量分别为(207.58±11.43)ng/mL、(405.05±50.92)pg/mL和(130.86±19.36)pg/mL,显著低于NC组(P<0.05)。干预4周后,阳性药物和各剂量复方醋口服液均在一定程度上提升了EDHF、PGE2和PGI2水平,其中MD和HD组效果较显著(P<0.05),EDHF含量分别为(225.70±9.47)ng/mL和(225.70±9.75)ng/mL,PGE2含量分别为(455.64±38.74)pg/mL和(458.11±38.95)pg/mL,PGI2含量分别为(151.27±11.17)pg/mL和(155.74±23.41)pg/mL。实验结果表明,复方醋口服液各剂量组可通过上调血管舒张因子含量来发挥降血压的作用。
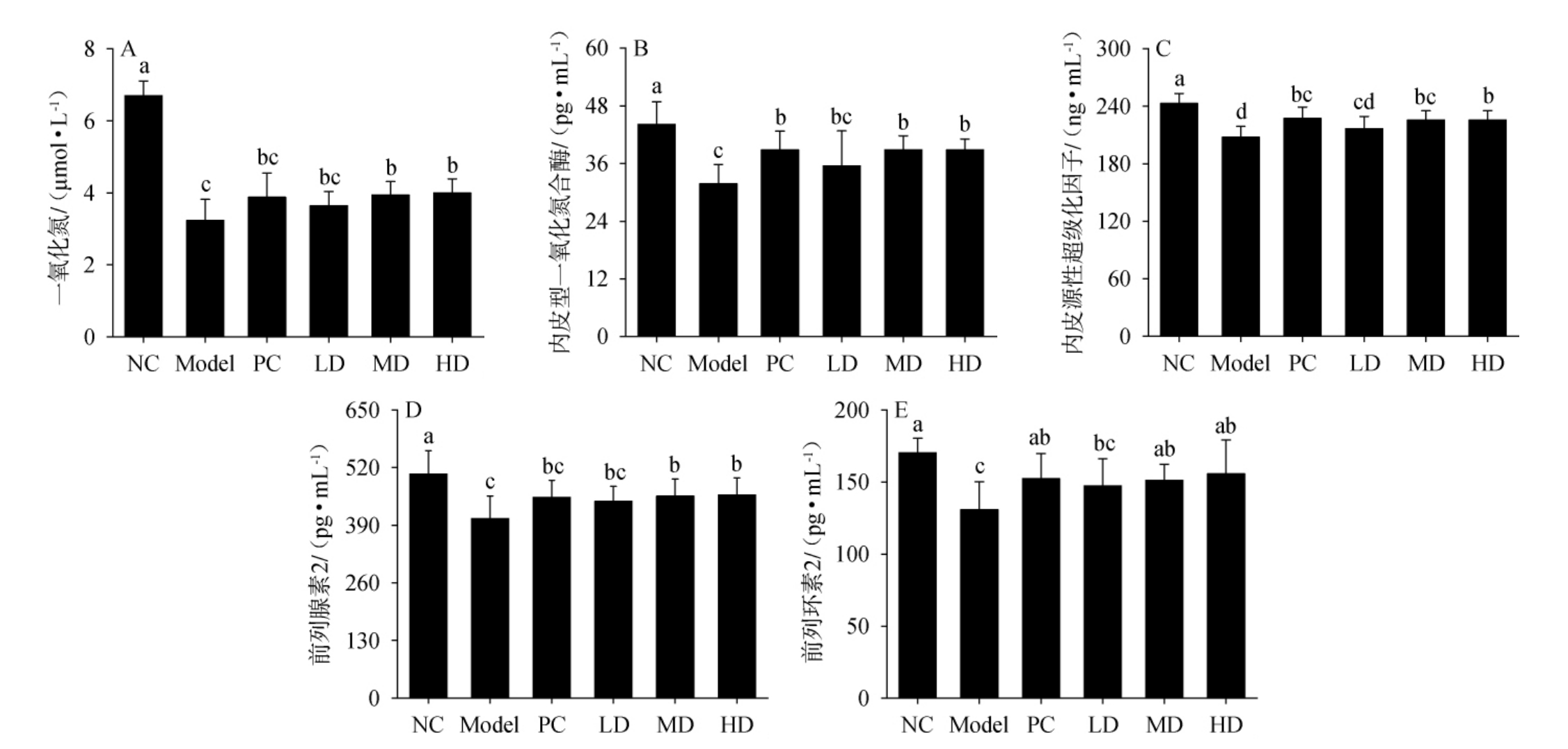
图3 复方醋口服液对大鼠一氧化氮(A)、内皮型一氧化氮合酶(B)、内皮源性超级化因子(C)、前列腺素2(D)和前列环素2(E)的影响
Fig.3 Effect of compound vinegar oral liquid on NO (A),endothelial nitric oxide synthase (B),endothelium derived hyperpolarizing factor (C),prostaglandin E2 (D) and prostaglandin I2 (E) of rats
2.5 复方醋口服液对大鼠血清血管收缩因子含量的影响
内皮素(ET)可通过与血管平滑肌ETA受体结合,介导细胞内钙离子持续升高,进而引发血管收缩和血压升高[28]。去甲肾上腺素(NE)、血管紧张素Ⅱ(AngⅡ)和醛固酮(ALD)共同参与血压调节,NE可促进血管收缩,AngⅡ除直接收缩血管外,还能刺激ALD分泌,增加血容量,导致血压升高[29]。由图4可知,模型组(Model)大鼠血清ET、NE、AngⅡ和ALD含量分别为(436.59±48.75)pg/mL、(5.82±0.45)ng/mL、(274.66±10.55)pg/mL和(696.11±55.92)pg/mL,显著高于正常组(P<0.05)。经过4周灌胃干预后,阳性对照组(PC)以及复方醋口服液低、中、高剂量组(LD、MD、HD)的血清ET、NE、AngⅡ和ALD含量较Model组均有所降低,且随着复方醋口服液剂量的增加,ET、NE、AngⅡ和ALD水平呈逐渐下降趋势,说明该复方醋口服液可能通过抑制ET、NE、AngⅡ和ALD的释放发挥降压作用。综合来看,MD和HD在降低ET、NE、AngⅡ和ALD水平的效果较显著(P<0.05),ET含量分别为(384.53±36.34)pg/mL和(382.46±27.36)pg/mL,NE含量分别为(5.18±0.59)ng/mL和(5.03±0.48)ng/mL,AngⅡ含量分别为(247.55±16.23)pg/mL和(244.81±12.81)pg/mL,ALD含量分别为(641.80±42.62)pg/mL和(636.23±38.82)pg/mL。实验结果表明,复方醋口服液各剂量可通过下调血管收缩因子含量来发挥降血压的作用。
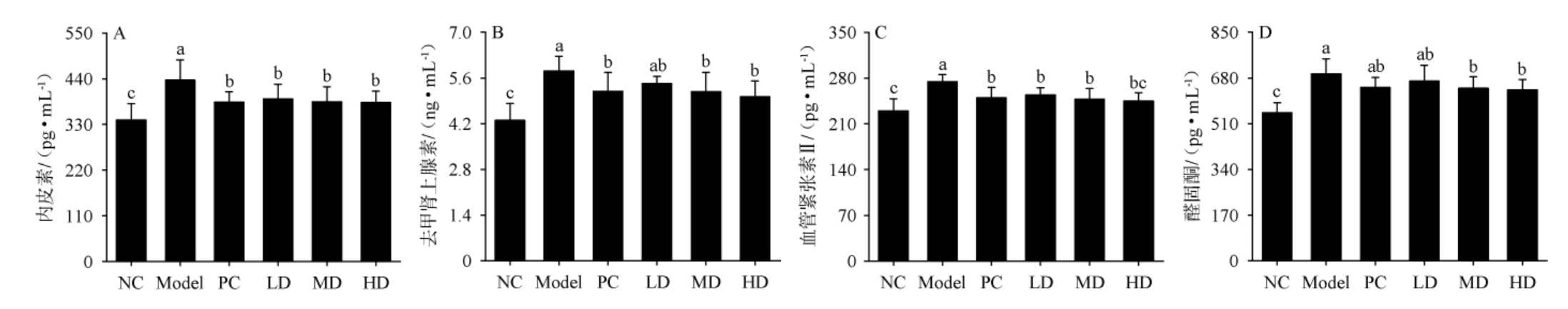
图4 复方醋口服液对大鼠内皮素(A)、去甲肾上腺素(B)、血管紧张素Ⅱ(C)和醛固酮(D)的影响
Fig.4 Effect of compound vinegar oral liquid on endothelin (A),norepinephrine (B),angiotensin II (C) and aldosterone (D) of rats
2.6 复方醋口服液对大鼠血清代谢组学检测分析
2.6.1 大鼠血清代谢物主成分分析及正交偏最小二乘判别分析
代谢组学主要分析代谢产物谱及代谢途径,阐明有关代谢物和生理生化指标的关系[30]。本研究采用非靶向代谢组学技术探究复方醋口服液对自发性高血压大鼠血清代谢物和代谢途径的影响。经前期对大鼠血压动态监测及血清相关生化指标测定,选取具有代表性的中剂量组(MD)与正常组(NC)、模型组(Model)对其血清代谢物进行PCA及OPLS-DA,结果见图5。由图5A的PCA结果显示,在阴离子模式下,共提取出两个主成分,累计方差贡献率为64.0%,能够解释原始数据的大部分信息。不同组的样本较分离且同一组的样本较聚集,说明复方醋口服液干扰了大鼠血清的代谢谱。利用OPLS-DA进一步区分两组间血清样本代谢谱的差异,由图5B、图5C可知,NC组与Model组明显分离(R2Y=0.999,Q2=0.906)。MD组与Model组也明显分离(R2Y=0.997,Q2=0.967),表明该OPLS-DA模型可靠,NC组、Model组和MD组大鼠血清的代谢物具有明显差异。
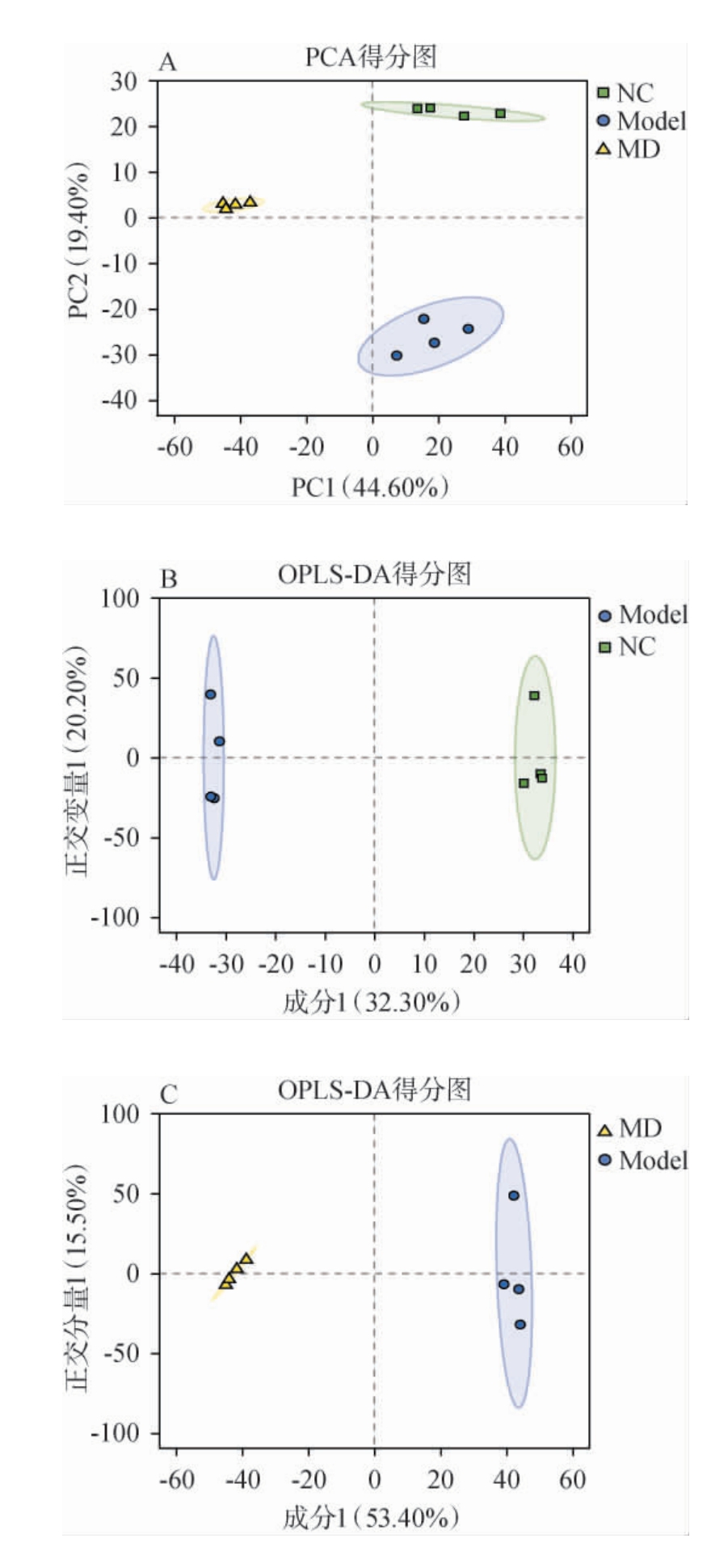
图5 大鼠血清代谢物主成分分析及正交偏最小二乘判别分析结果
Fig.5 Results of principal component analysis and orthogonal partial least squares discriminant analysis of serum metabolites in rats
2.6.2 大鼠血清差异代谢物的筛选
在大鼠血清中共检测出3 318个化合物,3组共有的代谢物有3 042种,其中主要包括脂类和类脂类分子、有机酸及其衍生物和有机杂环化合物等。基于OPLS-DA模型分析结果计算VIP值,以P<0.05且VIP>1为筛选标准,筛选出Model组与NC组、Model组与MD组之间的大鼠血清差异代谢物,并绘制火山图,结果见图6。由图6A可知,Model组与NC组共筛选出533个差异代谢物,其中281个上调,包括2-萘氧乙酸、11,12-环氧二十二碳三烯酸等;252个下调,包括γ-谷氨酰乙酰胺、头孢尼西等;从MD组和Model组中筛选出了798个差异代谢物,其中524个上调,包括5-羟基-N-甲基醌、异鼠李素3-葡糖酸甘等;274个下调,包括2-萘氧乙酸、牛蒡子酮等。
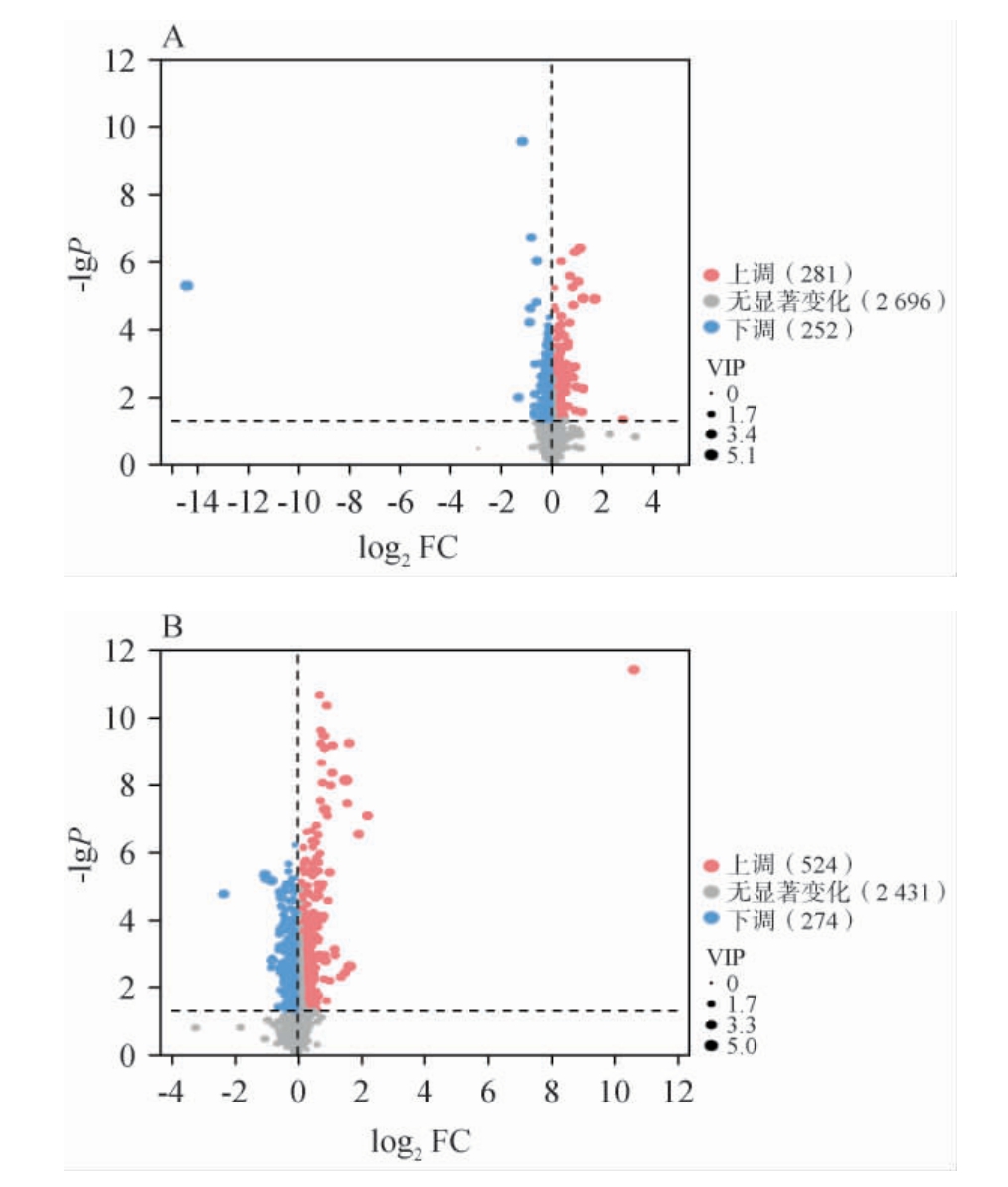
图6 大鼠血清中差异代谢物火山图
Fig.6 Volcano plot of differential metabolites in rat serum
A为NC组和Model组;B为MD组和Model组,下同。FC为差异表达量(fold change)。
将Model与NC组、Model与MD组间大鼠血清中VIP值top50的差异代谢物进行聚类分析,结果见图7。由图7A可知,与NC组相比,Model组大鼠血清代谢物苄基硫酸盐、胆固醇硫酸酯和3-羟基丁酸等相对丰度上调,N-花生四烯酰基缬氨酸、脯氨基羟基脯氨酸和N-棕榈酰苯丙氨酸等相对丰度下调;与Model组相比,MD组大鼠血清代谢物脯氨基羟基脯氨酸、N-棕榈酰苯丙氨酸和N-花生四烯酰基缬氨酸相对丰度上调,苄基硫酸盐、花生四烯酸和5-羟基内酯等相对丰度下调。
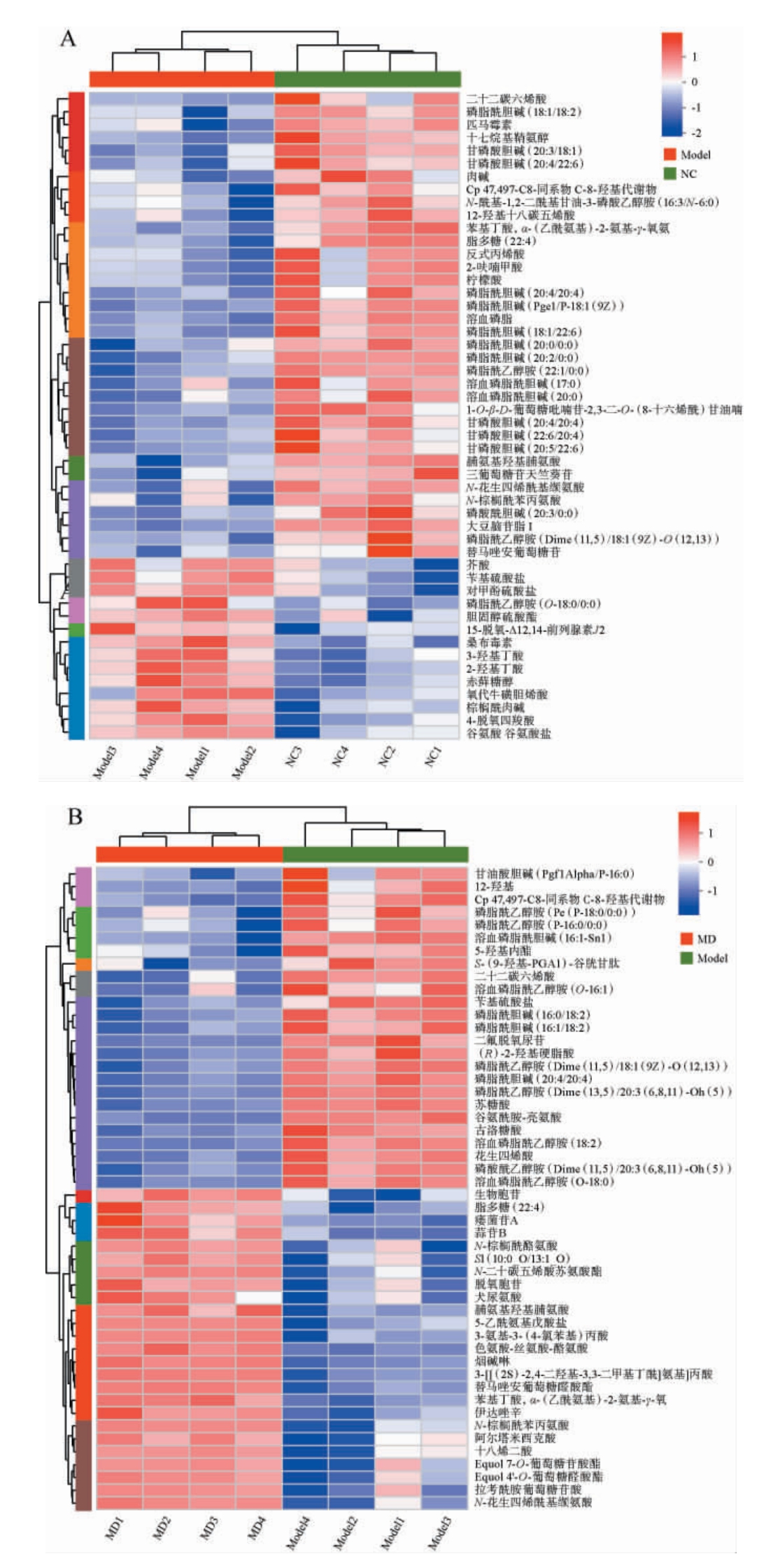
图7 大鼠血清中变量重要性投影值top50的差异代谢物聚类分析热图
Fig.7 Heat map of clustering analysis of the top50 differential metabolites based on variable importance projection values in rat serum
2.6.3 大鼠血清差异代谢物通路富集分析
氨基酸具有调节免疫力,降低炎症表达水平及减少氧化应激反应等作用,丙氨酸、天冬氨酸和谷氨酸代谢、精氨酸代谢和色氨酸代谢等氨基酸代谢途径的代谢产物可参与调节多种病理生理过程,且氨基酸大多富集在氨酰-转运核糖核酸(transfer ribonucleic acid,tRNA)通路上,在血压调节中发挥着重要的作用[31-34]。维生素B6代谢可辅助同型半胱氨酸在适宜条件下转化成胱硫醚,同时增强血管内皮功能,从而改善高血压[35]。甘油磷脂代谢产生的活性物质会影响膜功能,如果产生的物质损伤内皮细胞,则生成NO的量减少,血管舒张作用减弱,平滑肌收缩,进而促使血压升高[36]。使用KEGG通路富集进行拓扑学分析,确定各对比组差异代谢物的代谢途径,结果见图8。由图8A可知,Model组和NC组中,富集有重要影响的代谢通路包括丙氨酸、天冬氨酸和谷氨酸代谢,谷胱甘肽代谢,精氨酸生物合成,氨酰基tRNA生物合成和丙氨酸、酪氨酸和色氨酸生物合成等;由图8B可知,Model组和MD组中,富集有重要影响的代谢通路包括丙氨酸、天冬氨酸和谷氨酸代谢,花生四烯酸代谢,视黄醇代谢,精氨酸生物合成和缬氨酸、亮氨酸和异亮氨酸生物合成等。其中,丙氨酸、天冬氨酸和谷氨酸代谢,精氨酸生物合成,维生素B6代谢,色氨酸代谢和甘油磷脂代谢是两个对比组共同代谢途径,说明这五条代谢通路是复方醋口服液改善高血压疾病的潜在代谢通路。
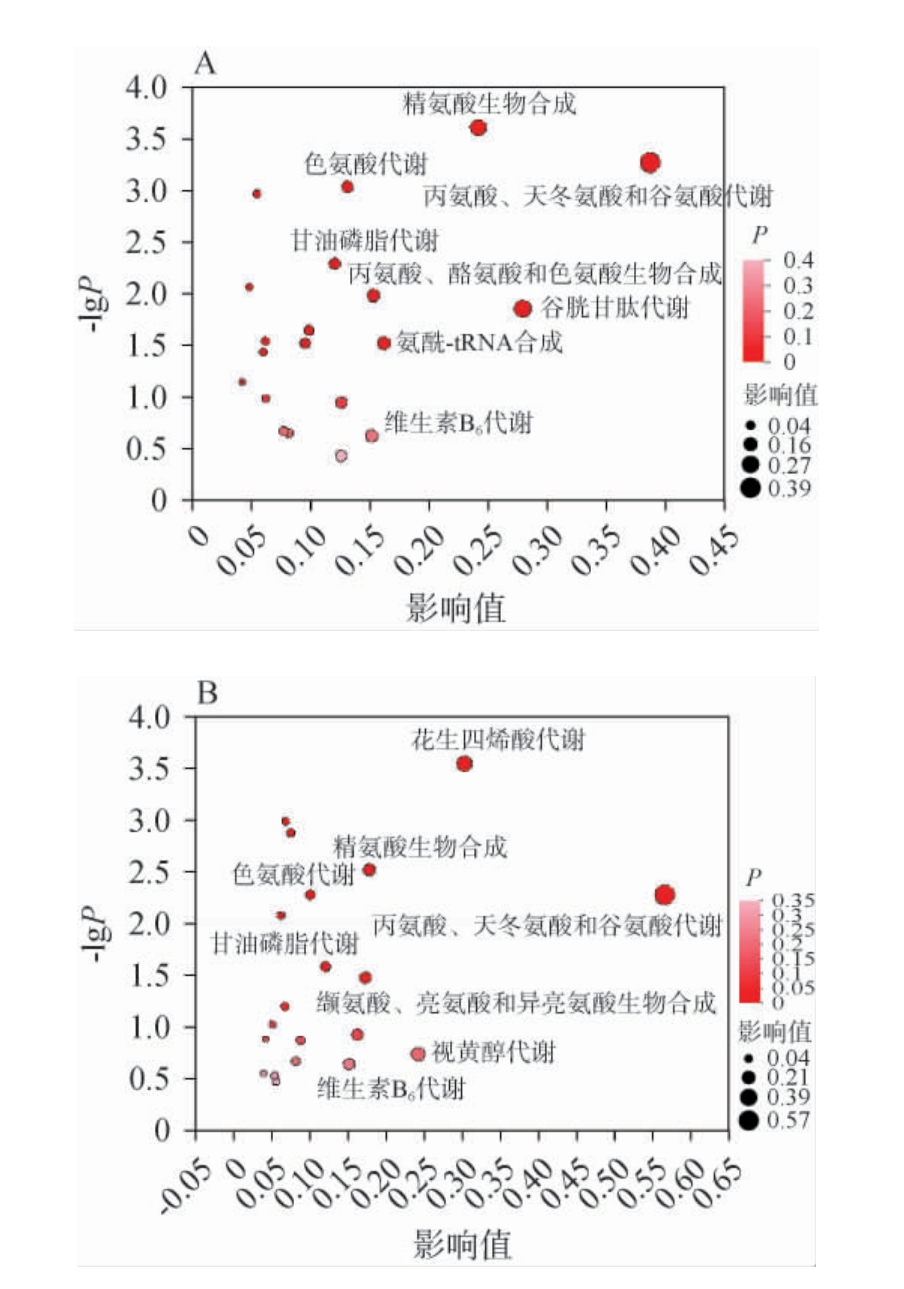
图8 大鼠血清中差异代谢物通路京都基因与基因组百科全书拓扑学分析图
Fig.8 Kyoto Encyclopedia of Genes and Genomes topology analysis diagram of differential metabolite pathways in rat serum
大鼠血清差异代谢物的主要代谢通路与涉及的代谢物见图9。由图9可知,在模型组(Model)与正常组(NC)中,上调代谢物为吲哚-3-乙醛、吲哚-3-乙酸和氨基苯甲酸,下调代谢物为N-乙酰基-L-天冬氨酸、L-天冬氨酸、精氨酸琥珀酸、4-吡哆酸、3-羟基氨基苯甲酸和柠檬酸;在复方醋口服液中剂量组(MD)与Model组中,上调代谢物为L-天冬氨酸、4-吡哆酸、N-乙酰基-L-天冬氨酸和N-乙酰鸟氨酸脱酰基酶,下调代谢物为氨基苯甲酸、谷氨酸和吲哚-3-乙酸。与Model组相比,和丙氨酸、天冬氨酸和谷氨酸代谢,精氨酸生物合成,色氨酸代谢和维生素B6代谢相关的N-乙酰基-L-天冬氨酸、L-天冬氨酸、4-吡哆酸和吲哚-3-乙酸等代谢物的表达量在MD组中出现显著回调。说明复方醋口服液可通过调节这4条潜在代谢通路中(如N-乙酰基-L-天冬氨酸、L-天冬氨酸、4-吡哆酸和吲哚-3-乙酸等)差异代谢物的含量来发挥对自发性高血压大鼠的降血压作用。
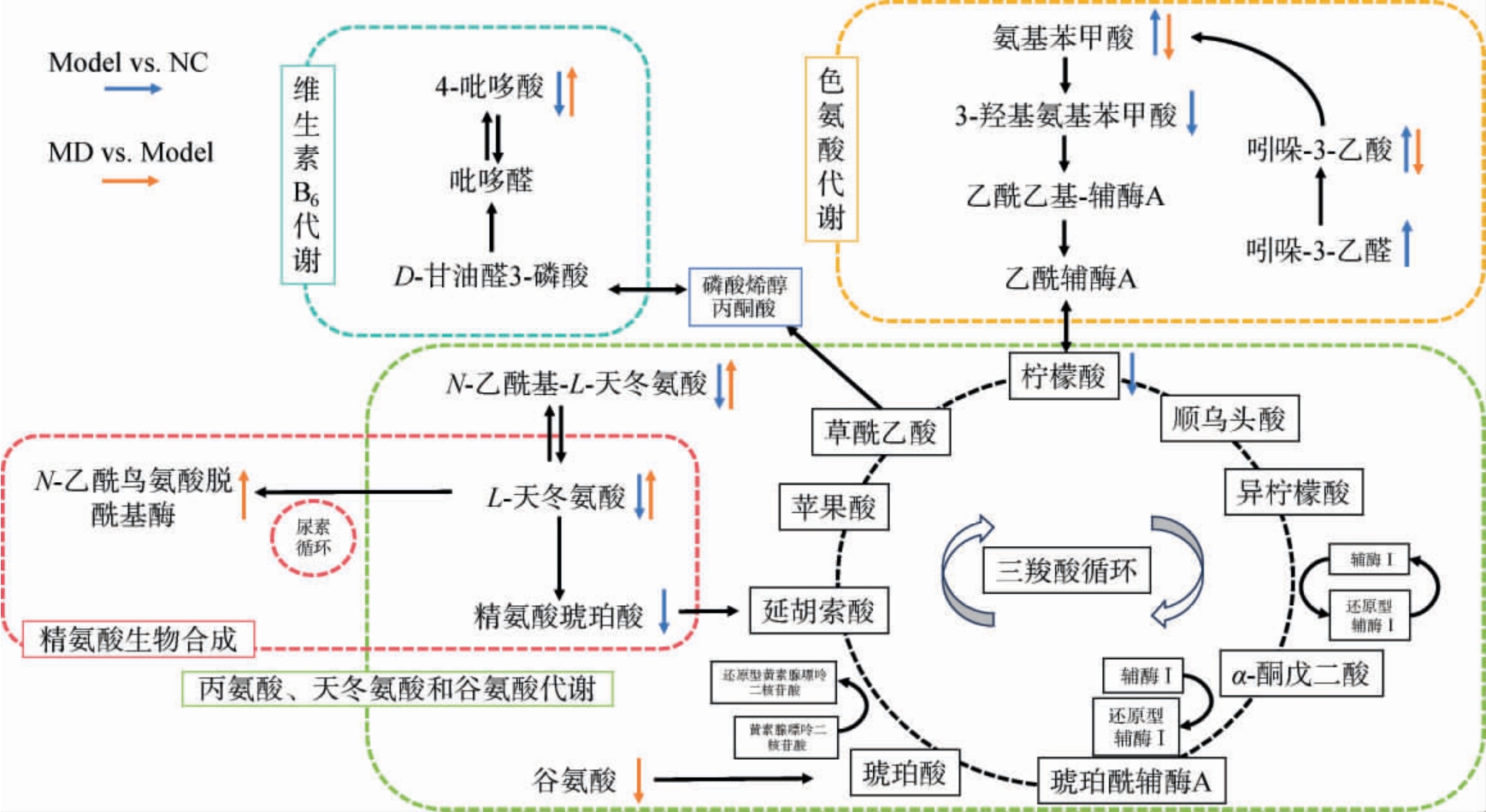
图9 大鼠血清中差异代谢物主要代谢通路及相关代谢物分析
Fig.9 Analysis of major metabolic pathways and related metabolites of differential metabolites in rat serum
3 结论
本研究科学复配山西老陈醋、杜仲叶与罗布麻叶水提液,制备一款具有降压功效的复方醋口服液。以自发性高血压大鼠为研究对象进行体内实验,测定各组大鼠体质量、血压、心率、脏器指数、血清生化指标,并结合代谢组学技术,筛选该口服液缓解高血压疾病的潜在代谢通路及差异代谢物。结果证实复方醋口服液在1.74~6.96 mL/kg范围内对自发性高血压大鼠具有稳定且显著的降压作用,同时对大鼠的心率、体质量均未产生不良影响。该口服液有效回调血清中血管舒张因子(NO、eNOs等)和血管收缩因子(ET、NE等)含量,从而平衡血管功能,且中、高剂量组效果尤为突出。基于非靶向代谢组学,揭示了该口服液可调节丙氨酸、天冬氨酸和谷氨酸代谢,精氨酸生物合成,色氨酸代谢和维生素B6代谢等核心代谢通路中N-乙酰基-L-天冬氨酸、L-天冬氨酸和4-吡哆酸等差异代谢物的含量改善高血压相关代谢紊乱。综上,复方醋口服液通过多靶点、多通路综合调控,有效降低血压,其作用与改善血管内皮功能及代谢紊乱密切相关。以上研究为该产品的研发与临床应用提供了理论支持。
[1] CAMPBELL N R C,NIEBYLSKI M L.Prevention and control of hypertension:Developing a global agenda[J].Curr Opin Cardiol,2014,29(4):324-330.
[2] PAUL L,MAHEE G O,XAVIER T,et al.Prevention of hypertension due to long working hours and other work hazards is needed to reduce the risk of cardiovascular disease[J].Scand J Work Env Hea,2024,51(1):48-52.
[3] 常丽辉.高血压的原因和可能的并发症[N].医药养生保健报,2024-04-30(012).
[4] NAWATA K.Risk factors for heart,cerebrovascular,and kidney diseases:evaluation of potential side effects of medications to control hypertension,hyperglycemia,and hypercholesterolemia[J].Front Cardiovas Med,2023,10:1103250.
[5] 谈莉莉.高血压患者常见药物不良反应及合理用药分析[J].智慧健康,2025,11(17):39-41,45.
[6] 陈少蕾,杨东红.基于中药药膳食疗的临床营养治疗方法[J].中外食品工业,2024(22):87-89.
[7] 陈树俊,胡坤.基于苦荞的功能醋粉对L-NNA诱导高血压大鼠降血压及抗氧化作用[J].中国酿造,2021,40(8):123-128.
[8] SONG J,QIU H R,DU P,et al.Polyphenols extracted from Shanxi-aged vinegar exert hypolipidemic effects on OA-induced HepG2 cells via the PPARα-LXRα-ABCA1 pathway[J].J Food Biochem,2022,46(2):e14029.
[9] XIA T,ZHANG J,YAO J H,et al.Shanxi aged vinegar protects against alcohol-induced liver injury via activating nrf2-mediated antioxidant and inhibiting tlr4-induced inflammatory response[J].Nutrients,2018,10(7):805.
[10] XIA T,YAO J H,ZHANG J,et al.Evaluation of nutritional compositions,bioactive compounds,and antioxidant activities of Shanxi aged vinegars during the aging process[J].J Food Sci,2018,83(10):2638-2644.
[11] XIE S K,SONG J,FAN B Q,et al.Elucidation and regulation of polyphenols in the smoking process of Shanxi aged vinegar[J].Foods,2021,10(7):1518.
[12] 吴子航,张祥龙,刘丹彤,等.中国传统食醋营养健康物质组成研究进展[J].中国酿造,2022,41(12):9-14.
[13] 向月华,唐蜜,刘鑫,等.解读山西老陈醋的化学秘语[J].化学教育(中英文),2024,45(1):2-8.
[14] 李婉玉,张家旭,谢兴文,等.杜仲叶化学成分、药理活性及现代应用研究进展[J].天然产物研究与开发,2024,36(5):900-917.
[15] BAO L,SUN Y L,WANG J M,et al.A review of"plant gold"Eucommia ulmoides Oliv.:A medicinal and food homologous plant with economic value and prospect[J].Heliyon,2024,10(2):e24851.
[16] GONG M,SU C F,FAN M Z,et al.Mechanism by which Eucommia ulmoides leaves regulate nonalcoholic fatty liver disease based on system pharmacology[J].J Ethnopharmacol,2021,282:114603.
[17] SHAO D,LIU X G,WU J Y,et al.Identification of the active compounds and functional mechanisms of Jinshui Huanxian formula in pulmonary fibrosisbyintegratingserumpharmacochemistry with net work pharmacology[J].Phytomedicine,2022,102:154177.
[18] GAO G,ABUBAKAR A S,CHEN J K,et al.Comparative genome and metabolome analyses uncover the evolution and flavonoid biosynthesis between Apocynum venetum and Apocynum hendersonii[J]. iScience,2023,26(5):106772.
[19] XIANG J,LAN R,TANG Y P,et al.Apocynum venetum leaf extract attenuates disruption of the blood-brain barrier and upregulation of matrix metalloproteinase-9/-2 in a rat model of cerebral ischemia-reperfusion injury[J].Neurochem Res,2012,37(8):1820-1828.
[20] ZHANG Y,LIU S,MA J L,et al.Apocynum venetum leaf extract alleviated doxorubicin-induced cardiotoxicity through the AKT/Bcl-2 signaling pathway[J].Phytomedicine,2022,94:153815.
[21] 陈小露,刘起棠,张洁帅,等.罗布麻叶的化学成分及药理作用研究进展[J].时珍国医国药,2022,33(11):2739-2742.
[22] HELKAR B P,SAHOO A,PATIL N.Review:Food industry by-productsused as a functional food ingredients[J].Int J Waste Res,2016,6(3):1-6.
[23] PARK J Y,KIM M J,CHOI Y A,et al.Anti-inflammatory effects of Clematis terniflora leaf on lipopolysaccharide-induced acute lung injury[J].Evidence Complem Altern Med,2024,2024(1):6653893.
[24] 林如.高血压与睡眠障碍的潜在共病机制和治疗展望[J].中国医药科学,2025,15(10):41-44,85.
[25] CHEN C H,CHEN F Y,GU L,et al.Discovery and validation of COX2 as a target of flavonoids in Apocyni Veneti Folium:Implications for the treatment of liver injury[J].J Ethnopharmacol,2024,326:117919.
[26] CONSTANTIN M,CRISTINA P,ANDREEA I V T,et al.Signaling paradigms of H2S-induced vasodilation: A comprehensive review[J].Antioxidants,2024,13(10):1158.
[27] CHENG H,HUANG H Y,GUO Z K,et al.Role of prostaglandin E2 in tissue repair and regeneration[J].Theranostics,2021,11(18):8836-8854.
[28] HOU J Y,LIU S H,ZHANG X D,et al.Structural basis of antagonist selectivity in endothelin receptors[J].Cell Discovery,2024,10(1):79.
[29] LOH H H,AZIZAN E A,SUKOR N.Connecting the dots: Renin-angiotensin-aldosterone system,vitamin D,and hypertension[J].J Hypertens,2025,43(7):1136-1145.
[30] JOSHI A D,RAHNAVARD A,KACHROO P,et al.An epidemiological introduction to human metabolomic investigations[J].Trends Endocrin Met,2023,34(9):505-525.
[31] 李文俊,姬燕梅,杨云红,等.彝族高血压患者代谢产物分析及相关机制研究[J].重庆医学,2023,52(19):2912-2918.
[32] 周雨昕,徐逸宁,张淑洁,等.色氨酸及其代谢产物在动脉粥样硬化中的作用及中医药干预研究进展[J].中医药导报,2025,31(5):152-158.
[33] LI D D,YANG C C,LIU P,et al.Effect of nitric oxide on the antifungal activity of oxidative stress and azoles against Candida albicans[J].Indian J Microbiol,2016,56(2):214-218.
[34] 王超臣,唐才智,冉庄,等.UHPLC-MS/MS非靶向代谢组学在移居高原人群高原性高血压血浆代谢研究中的应用[J].陆军军医大学学报,2024,46(19):2249-2258.
[35] 张雪姣,余帆,袁芹,等.叶酸和维生素B6与维生素B12联合干预对H型高血压患者血压变异性与动脉弹性的长期影响[J].中国心血管病研究,2020,18(9):797-801.
[36] TOMASZ R,ILPO V.Cholesterol,sphingolipids,and glycolipids:What do we know about their role in raft-like membranes?[J]. Chem Phys Lipids,2014,184:82-104.