生物胺(biogenic amine,BA)作为一类含有氨基的碱性有机化合物,主要通过微生物对游离氨基酸的脱羧过程形成,普遍存在于各类发酵食品中,过量摄入会引发头痛、心悸等毒性反应[1]。一定浓度的乙醇(酒精度<10%vol)会提高氨基酸脱羧酶的活性,抑制胺类氧化酶的活性,导致生物胺过度积累,同时乙醇和乙醛会增加生物胺的吸收而增强其毒性作用[2],因此,BAs的分析研究主要集中于黄酒、白酒、葡萄酒等酒类制品[3]。一些国家已经对葡萄酒中的组胺含量进行限制,其中德国的规定最严格(<2 mg/L)[4]。目前,我国对酒类制品中生物胺限量未有明确规定,但已有研究表明,生物胺在黄酒、葡萄酒、啤酒及白酒中的含量分别为78.30 mg/L、11.24 mg/L、4.79 mg/L、0.22~13.03 mg/L[5]。
食醋作为典型的开放式多菌种发酵食品,其生物胺风险不容忽视。魏泉增等[6]对香醋、陈醋和米醋3种食醋产品的总生物胺含量进行了检测,发现香醋总生物胺含量(150.87mg/L)显著高于陈醋(77.58mg/L)和米醋(13.48mg/L)。黄祖新[7]研究表明,红曲醋酿造过程中,红曲酒中生物胺的总含量最高,随着红曲醋发酵时间增长,各种生物胺趋势和含量都有明显的降低。邓朝霞[8]研究发现,醋液中生物胺含量随陈酿时间延长而呈下降趋势。微生物驱动的氨基酸脱羧反应是生物胺的核心来源。在传统固态发酵工艺中,酒精发酵阶段因醪液富集氨基酸前体,且微氧环境与适宜pH显著促进微生物合成氨基酸脱羧酶,因此,食醋的酒精发酵阶段被证实为生物胺积累的关键时期[9]。目前,鲜见关于食醋在酒精发酵阶段中生物胺含量的研究进展。
本研究以山西老陈醋酒精发酵过程中酒醪样品为研究对象,采用常规检测法测定酒醪中生物胺及常规理化指标,通过Illumina MiSeq测序技术解析微生物菌群结构,并探究生物胺与常规理化指标和优势菌属的相关性,旨在为山西老陈醋酿造工艺优化及安全生产提供理论依据,为提高山西老陈醋安全性奠定基础。
1 材料与方法
1.1 材料与试剂
1.1.1 材料
山西老陈醋在酒精发酵阶段(0 d、2 d、4 d、6 d、8 d)的醪液样品(编号分别为J0、J2、J4、J6、J8):山西某醋厂。
1.1.2 试剂
组胺盐酸盐、尸胺盐酸盐(均为色谱纯):西格玛奥德里奇(上海)贸易有限公司;酪胺盐酸盐、腐胺盐酸盐(均为色谱纯):上海源叶生物科技有限公司;精胺盐酸盐(均为色谱纯):上海吉至生化科技有限公司;亚精胺盐酸盐(色谱纯):德国Ehrenstorfer GmbH公司;色胺盐酸盐(色谱纯):上海阿拉丁生化科技股份有限公司;苯乙胺盐酸盐(均为色谱纯):国药集团化学试剂有限公司;QIAquick PCR Purification Kit:德国Qiagen公司;Tris-HCl(分析纯):北京索莱宝科技有限公司;乙二胺四乙酸钠(分析纯):天津市恒兴试剂有限公司;其他试剂均为国产分析纯。
1.2 仪器与设备
Agilent1200高效液相色谱仪:美国安捷伦科技有限公司;5425R离心机:艾本德(中国)有限公司;170-4406型水平电泳系统、Universial HoodⅡ型凝胶成像系统、T100型聚合酶链式反应(polymerase chain reaction,PCR)仪:美国Bio-Rad公司;NanoDrop2000微量紫外可见光分光光度计:美国Thermo Scientific公司;PB-21酸度计:赛多利斯科学仪器(北京)有限公司。
1.3 方法
1.3.1 酒醪常规理化指标及生物胺的测定
酒精度的测定:参见GB 5009.225—2023《食品安全国家标准酒和食用酒精中乙醇浓度的测定》[10]的比重计法;pH、总酸、还原糖、氨基酸态氮的测定:参照国标GB/T 19777—2013《地理标志产品 山西老陈醋》[11]中的方法;生物胺的测定:参照国标GB/T 5009.208—2016《食品安全国家标准食品中生物胺的测定》[12]的第一法液相色谱法。
1.3.2 DNA提取、PCR扩增、高通量测序
提取酒醪样品的DNA[13],以细菌特异性引物515F(5'-GTG-CCAGCMGCCGCGGTAA-3')和806R(5'-GGACTACHV-GGGTWTCTAA-3')对细菌16S rDNA V4区域基因序列进行聚合酶链式反应(PCR)扩增;以真菌特异性引物ITS1F(5'-CTTGGTCA-TTTAGAGGAAGTAA-3')和ITS1R(5'-GCTGCGTTCTT-CATCGATGC-3')对真菌ITS区基因序列进行PCR扩增[14-15]。PCR扩增体系(30 μL):上、下游引物各2 μL,模板基因组DNA 2 μL,2×Mix 15 μL,双蒸水(ddH2O)补足至30 μL。PCR扩增条件:94 ℃预变性10 min;94 ℃变性30 s,退火(细菌50 ℃,真菌52 ℃)30 s,72 ℃延伸105 s,共30个循环;72 ℃再延伸10 min,4 ℃保存。细菌及真菌PCR扩增产物经1%琼脂糖凝胶电泳检测合格后送至北京百迈客生物科技有限公司测序。
1.3.3 生物信息学分析
使用FLASH v1.2.7软件对测序数据进行拼接,使用Trimmomatic v0.33软件对拼接序列进行过滤,使用UCHIME v4.2软件去除嵌合体序列,获得有效序列。使用Usearch软件,将序列相似性达到97%以上的有效序列归为同一个操作分类单元(operational taxonomic units,OTU)[16]。选取每一个OTU的代表序列,在美国国立生物技术信息中心(National Center for Biotechnology Information,NCBI)的GenBank数据库中通过基本局部比对搜索工具(basic local alignment search tool,BLAST)进行物种注释,统计各样品中细菌和真菌在门和属水平的相对丰度[16]。
1.3.4 数据处理
采用SPSS27.0进行单因素方差分析(analysisofvariance,ANOVA);皮尔逊(Pearson)相关性系数法对生物胺与常规理化指标及微生物菌群的相关性进行评估;采用Origin 8.0软件绘图。
2 结果与分析
2.1 山西老陈醋酒精发酵过程中生物胺含量的变化
山西老陈醋酒精发酵阶段是生物胺形成的关键时期,其含量变化直接影响产品安全性与风味稳定性[9]。因此对山西老陈醋酒精发酵过程中酒醪生物胺含量进行监测,结果见图1。
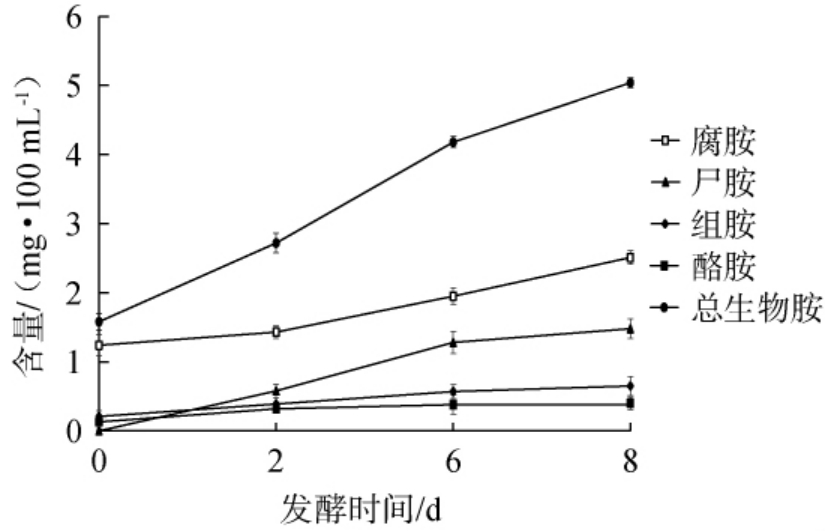
图1 山西老陈醋酒精发酵过程中生物胺含量的变化
Fig.1 Changes of biogenic amines content of Shanxi aged vinegar during alcohol fermentation
由图1可知,在酒精发酵阶段,生物胺总含量从起始(1.58mg/100 mL)逐渐上升,发酵至第8天达5.04mg/100mL。其中,腐胺和尸胺在酒精发酵过程中含量逐渐增加,且含量较高,分别由起始含量(1.24 mg/100 mL、未检出)上升至第8天的2.51 mg/100 mL、1.48 mg/100 mL。酒精发酵结束时,腐胺和尸胺的总含量占总生物胺含量的60%以上,这一结果与邓朝霞[8]的研究结论相一致。此外,酒醪样品中还检测到了组胺和酪胺,其含量在发酵过程中增加缓慢,分别由起始(0.21 mg/100 mL、0.13 mg/100 mL)上升至发酵第8天的0.65 mg/100 mL、0.40 mg/100 mL。这是由于酒精发酵过程中,原料中的氨基酸经霉菌(如根霉属)糖化酶和蛋白酶水解,在酵母菌协同作用下,乳酸菌通过合成氨基酸脱羧酶将氨基酸转化为生物胺[17]。综上,发酵过程中生物胺含量增加。
2.2 酒精发酵过程中常规理化指标的变化
山西老陈醋酒精发酵过程中理化指标的变化见图2。由图2A可知,发酵0~2 d时,酒精度快速增加,而还原糖含量快速下降;发酵2~8 d,酒精度缓慢上升,而还原糖缓慢下降;发酵结束(8 d)时,酒精度为9.05%vol,还原糖由发酵起始含量11.46 g/100 mL下降至0.96 g/100 mL。在有氧环境中,还原糖为酵母菌生长繁殖提供了有利条件,随着发酵持续进行,发酵液中还原糖含量减少,导致酒精生成量减少。
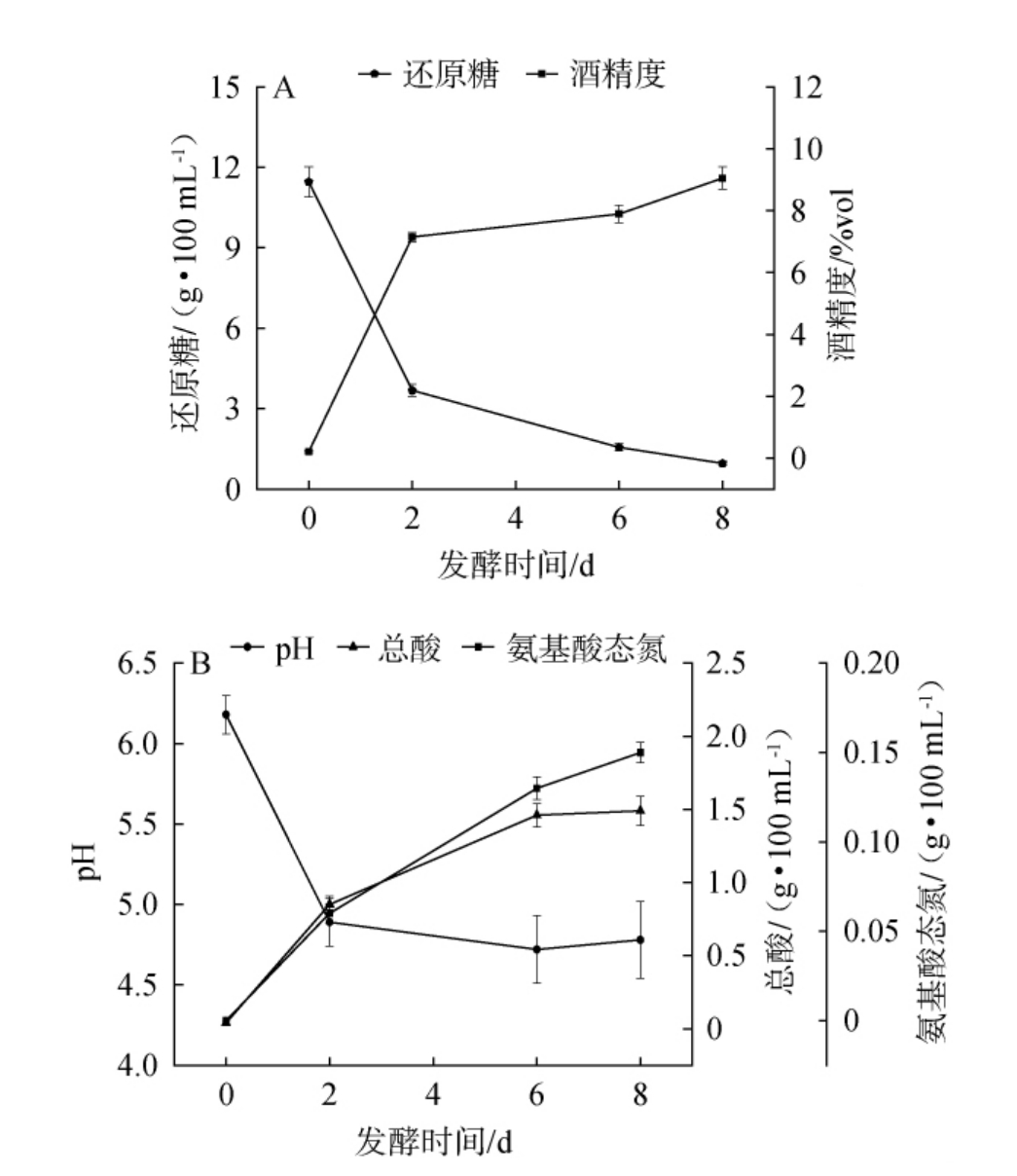
图2 山西老陈醋酒精发酵过程中常规理化指标的变化
Fig.2 Changes of physicochemical indexes of Shanxi aged vinegar during alcohol fermentation
由图2B可知,发酵0~8 d时,酒醪氨基酸态氮含量增加,由起始含量0上升至0.15 g/100 mL。发酵0~6 d时,总酸含量上升,而pH值下降;当发酵6~8 d时,总酸含量及pH值无明显变化;当发酵8 d时,其总酸含量及pH值分别为1.49 g/100 g和4.78,在酒精发酵初期(0~2 d),酵母菌、乳酸菌及芽孢杆菌等微生物的快速增殖导致酸性代谢产物(如有机酸)大量积累,促使酒醪总酸上升,pH值显著下降[19]。随着发酵进程的推进,酒醪中逐渐形成由多种代谢产物(如有机酸盐、氨基酸等)构成的缓冲体系,该体系能够中和酸碱波动。因此,在发酵中后期,酒醪总酸和pH值趋于稳定[20]。
2.3 山西老陈醋酒精发酵过程中微生物菌群结构分析
2.3.1 酒精发酵过程中细菌菌群结构分析
基于门和属水平山西老陈醋酒精发酵过程中细菌菌群结构见图3。
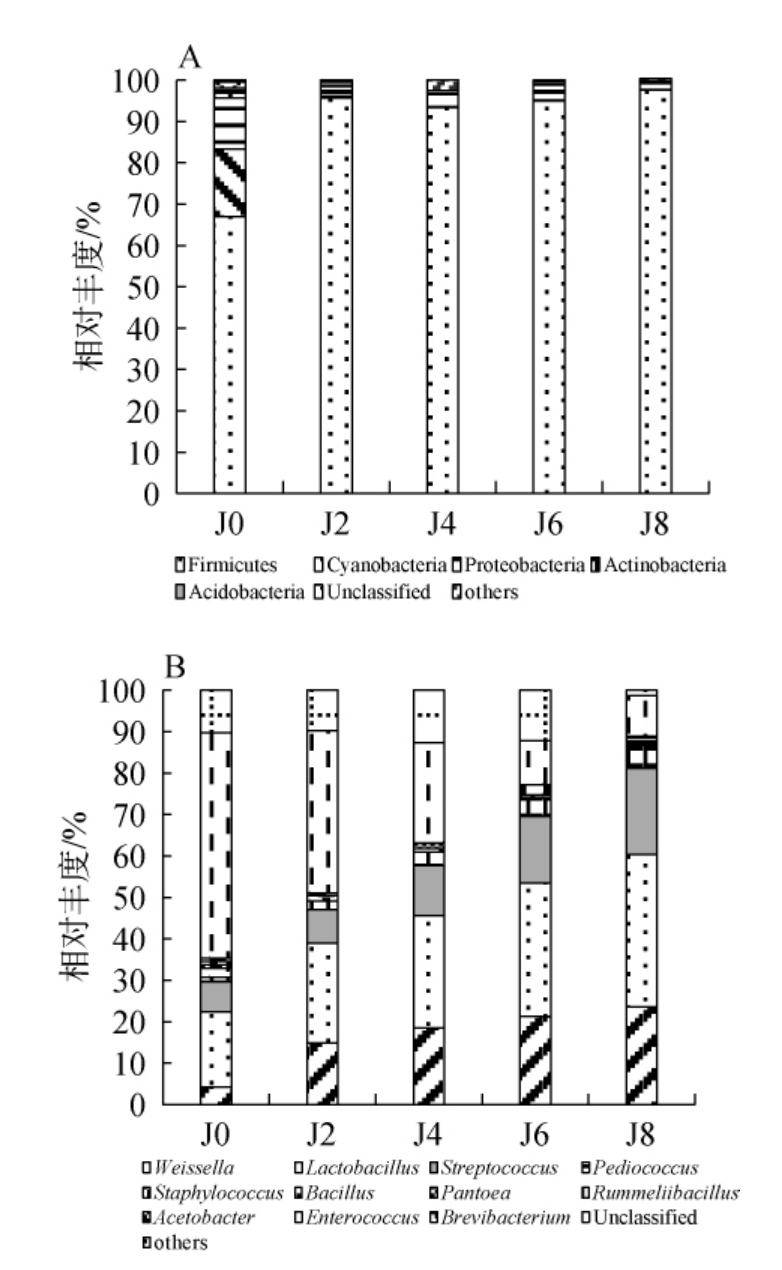
图3 基于门(A)和属(B)水平山西老陈醋酒精发酵过程中细菌群落结构
Fig.3 Bacterial community structure of Shanxi aged vinegar during alcohol fermentation at phylum (A) and genus (B) levels
将相对丰度<0.5%的物种归为Others。下同。
由图3A可知,山西老陈醋酒精发酵过程中酒醪样品中共检出6个细菌门(相对丰度>0.5%),其中厚壁菌门(Firmicutes)、变形菌门(Proteobacteria)、蓝细菌门(Cyanobacteria)是主要的优势细菌门(相对丰度>1%),平均相对丰度分别为88.76%、4.97%、4.31%。酒精发酵初期(0~2 d),厚壁菌门(Firmicutes)的相对丰度由66.96%上升至95.62%,之后相对丰度变化趋于平稳,发酵结束时相对丰度为97.58%。变形菌门(Proteobacteria)、蓝细菌门(Cyanobacteria)在发酵起始(0 d)的相对丰度最高,分别为12.36%、16.35%,随着发酵的进行相对丰度逐渐下降,酒精发酵结束时分别为1.45%、0.13%。WU Y F等[21]研究表明,山西老陈醋酒精发酵过程中厚壁菌门(Firmicutes)是主要的细菌门,其次是变形菌门(Proteobacteria),其相对丰度分别为52%、11%,与本研究结果相一致。
由图3B可知,山西老陈醋酒精发酵过程中酒醪样品检出12个细菌属(相对丰度>0.5%),其中乳酸杆菌属(Lacto bacillus)、魏斯氏菌属(Weissella)、链球菌属(Streptococcus)、片球菌属(Pediococcus)、芽孢杆菌属(Bacillus)、醋酸杆菌属(Acetobacter)是主要的优势菌属(相对丰度>1%),平均相对丰度分别为27.65%、16.48%、12.85%、3.34%、1.09%、1.08%。随着发酵时间在0~8 d范围内的增加,乳酸杆菌属(Lactobacillus)、魏斯氏菌属(Weissella)、链球菌属(Streptococcus)、片球菌属(Pediococcus)的相对丰度呈上升趋势,其中乳酸杆菌属(Lactobacillus)相对丰度由18.13%上升至36.69%,魏斯氏菌属(Weissella)的相对丰度由4.20%上升至23.61%,链球菌属(Streptococcus)相对丰度由7.27%上升至20.82%,片球菌属(Pediococcus)的相对丰度由1.14%上升至5.62%,这些微生物作为兼性厌氧或专性厌氧的乳酸菌群,具备高效代谢可利用碳水化合物(如糖类)的能力,通过同型或异型乳酸发酵途径产生大量乳酸及少量其他有机酸,导致发酵环境pH值迅速下降,抑制了多数不耐酸微生物的生长,从而为具有较强酸耐受性的乳酸菌群(特别是乳酸杆菌属)创造了竞争优势,使其在群落演替中相对丰度持续上升[22]。此外,芽孢杆菌属(Bacillus)、醋酸杆菌属(Acetobacter)相对丰度整体变化相对较小,其中芽孢杆菌属(Bacillus)相对丰度在0~8 d范围内呈下降趋势,由2.14%下降到0.48%;醋酸杆菌属(Acetobacter)相对丰度呈波动变化(0.41%~2.38%)。赵欣等[23]在山西老陈醋的酒精发酵过程检测到的细菌属分别为魏斯氏菌属、乳酸杆菌属、链球菌属、明串珠菌属、片球菌属、葡萄球菌属和乳球菌属,其中魏斯氏菌属、乳酸杆菌属和链球菌属是优势菌属,与本研究结果一致。
综上,山西老陈醋酒精发酵过程中细菌菌群结构呈现明显动态变化,可能与环境条件和营养成分的改变存在密切关系。
2.3.2 酒精发酵过程中真菌菌群结构分析
基于门和属水平山西老陈醋酒精发酵过程中真菌菌群结构见图4。
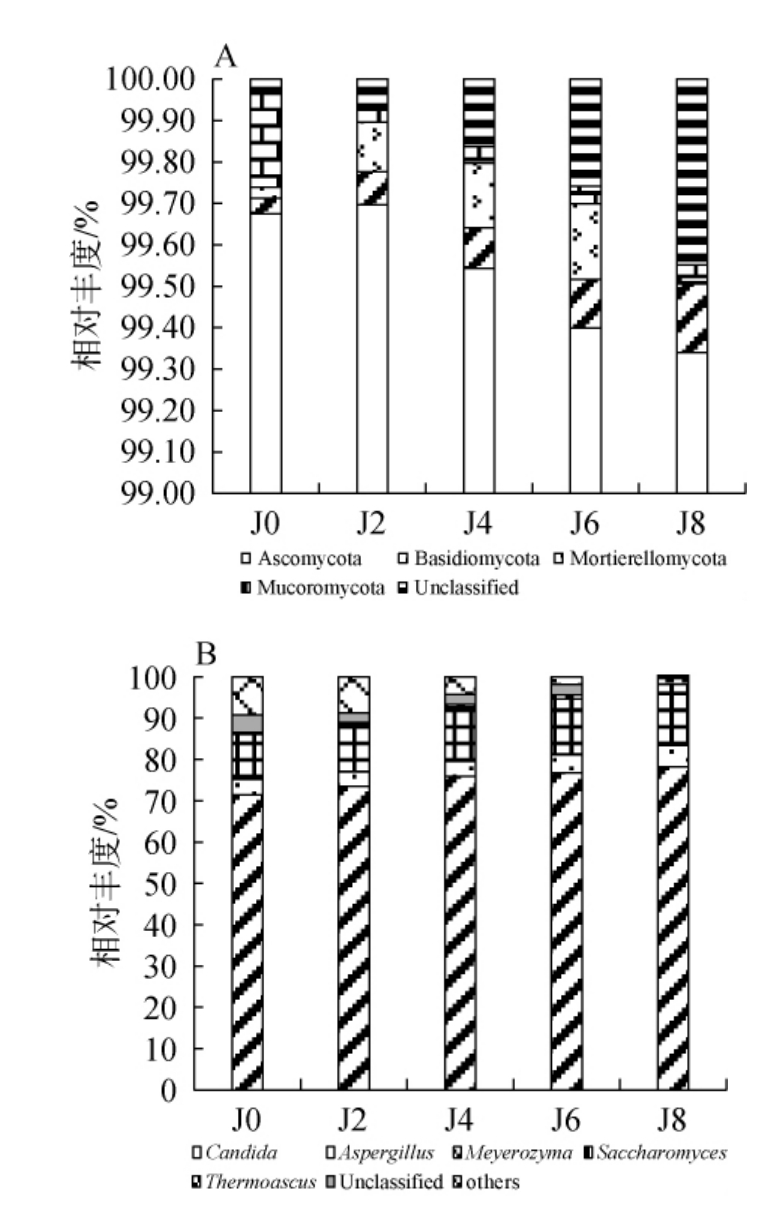
图4 基于门(A)和属(B)水平山西老陈醋酒精发酵过程中真菌群落结构
Fig.4 Fungal community structure of Shanxi aged vinegar during alcohol fermentation at phylum (A) and genus (B) levels
由图4A可知,山西老陈醋酒精发酵过程中酒醪样品中共鉴定出4个真菌门,分别为子囊菌门(Ascomycota)、担子菌门(Basidiomycota)、被孢霉门(Mortierellomycota)及毛霉门(Mucoromycota),其中,子囊菌门为优势菌门(相对丰度>1%),平均相对丰度为99.53%。子囊菌门(Ascomycota)在酒精发酵阶段中一直处于优势地位,其相对丰度为99.34%~99.70%。杨玲等[24]的研究表明,山西老陈醋酒精发酵第3天存在4个真菌门,其中子囊菌门(Ascomycota)以99.86%的平均相对丰度占据绝对优势。与本研究结果一致。
由图4B可知,山西老陈醋酒精发酵过程中共鉴定出5个真菌属(相对丰度>0.5%),其中假丝酵母菌属(Candida)、酿酒酵母属(Saccharomyces)和曲霉菌属(Aspergillus)是主要的优势真菌属,平均相对丰度分别为75.16%、12.59%、4.07%。李敏[25]研究发现,在山西老陈醋酒精发酵阶段,酿酒酵母属(Saccharomyces)、曲霉属(Aspergillus)和假丝酵母属(Candida)是主要优势菌群,与本研究结果类似。在酒精发酵过程中,酿酒酵母属(Saccharomyces)、曲霉菌属(Aspergillus)、假丝酵母菌属(Candida)的相对丰度呈上升趋势,其中酿酒酵母属(Saccharomyces)相对丰度由10.83%上升至14.39%,曲霉菌属(Aspergillus)的相对丰度由3.77%上升至5.18%,假丝酵母菌属(Candida)的相对丰度由71.37%上升至78.22%。此外,在酒精发酵过程中,尽管嗜热子囊菌属(Thermoascus)和迈耶氏酵母属(Meyerozyma)的相对丰度较低,但二者通过代谢协同作用,共同促进4-甲基愈创木酚(烟熏风味)和苯乙醇(玫瑰花香)等风味物质的生成[13]。
综上,山西老陈醋酒精发酵过程中真菌菌群结构呈现明显动态变化,可能与环境条件和营养成分的改变存在密切关系。
2.4 酒精发酵过程中生物胺与常规理化指标及微生物菌群相关性分析
2.4.1 生物胺与常规理化指标相关性分析
生物胺在酒精发酵过程中的形成不仅需要氨基酸前体物质,还需要在细胞体内外运输氨基酸和生物胺的转运蛋白[17],而理化环境的变化会影响氨基酸转化为生物胺的反应对酒精发酵过程中总酸、酒精度、还原糖和氨基酸态氮等常规理化指标与生物胺的相关性分析结果见表1。
表1 酒精发酵过程中生物胺与常规理化指标相关性
Table 1 Correlation between biogenic amines and conventional physicochemical indexes during alcohol fermentation
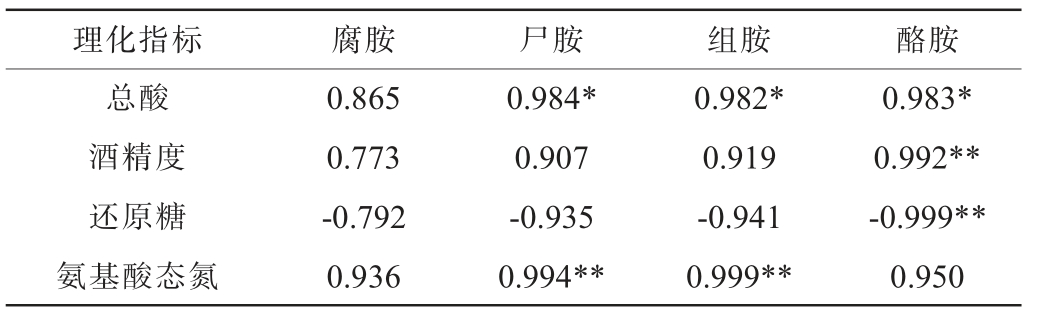
注:“*”表示相关性显著(P<0.05);“**”表示相关性极显著(P<0.01)。下同。
由表1可知,在山西老陈醋的酒精发酵过程中,酒醪的酒精度、总酸和氨基酸态氮与腐胺、尸胺、组胺和酪胺呈正相关。其中,总酸与尸胺、组胺和酪胺呈显著正相关(P<0.05),酒精度与酪胺呈极显著正相关(P<0.01),氨基酸态氮与尸胺和组胺呈极显著正相关(P<0.01)。这是由于生物胺主要产生于微生物的氨基酸脱羧代谢途径,该生化途径是微生物应对酸胁迫的重要适应性机制。脱羧反应的最终产物通过消耗质子(H+)并释放二氧化碳(CO2)提升pH值,同时,pH值能够通过抑制氨基酸脱羧酶的活性来调控生物胺的生成[16-17]。此外,氨基酸态氮作为生物胺合成的关键前体物质,其含量直接影响生物胺的生成[18-19]。还原糖与腐胺、尸胺、组胺和酪胺呈负相关,其中,还原糖与酪胺呈极显著负相关(P<0.01),其原因可能是糖会抑制微生物生长繁殖,使氨基酸转化为生物胺的反应减弱[17]。综上,酒精度、总酸和氨基酸态氮含量对生物胺积累起促进作用,而还原糖含量则对生物胺积累起抑制作用。
2.4.2 生物胺与微生物菌群相关性分析
采用Pearson相关系数法对细菌属和真菌属(相对丰度>0.5%)与生物胺(腐胺、尸胺、组胺、酪胺)进行相关性分析,结果见图5。
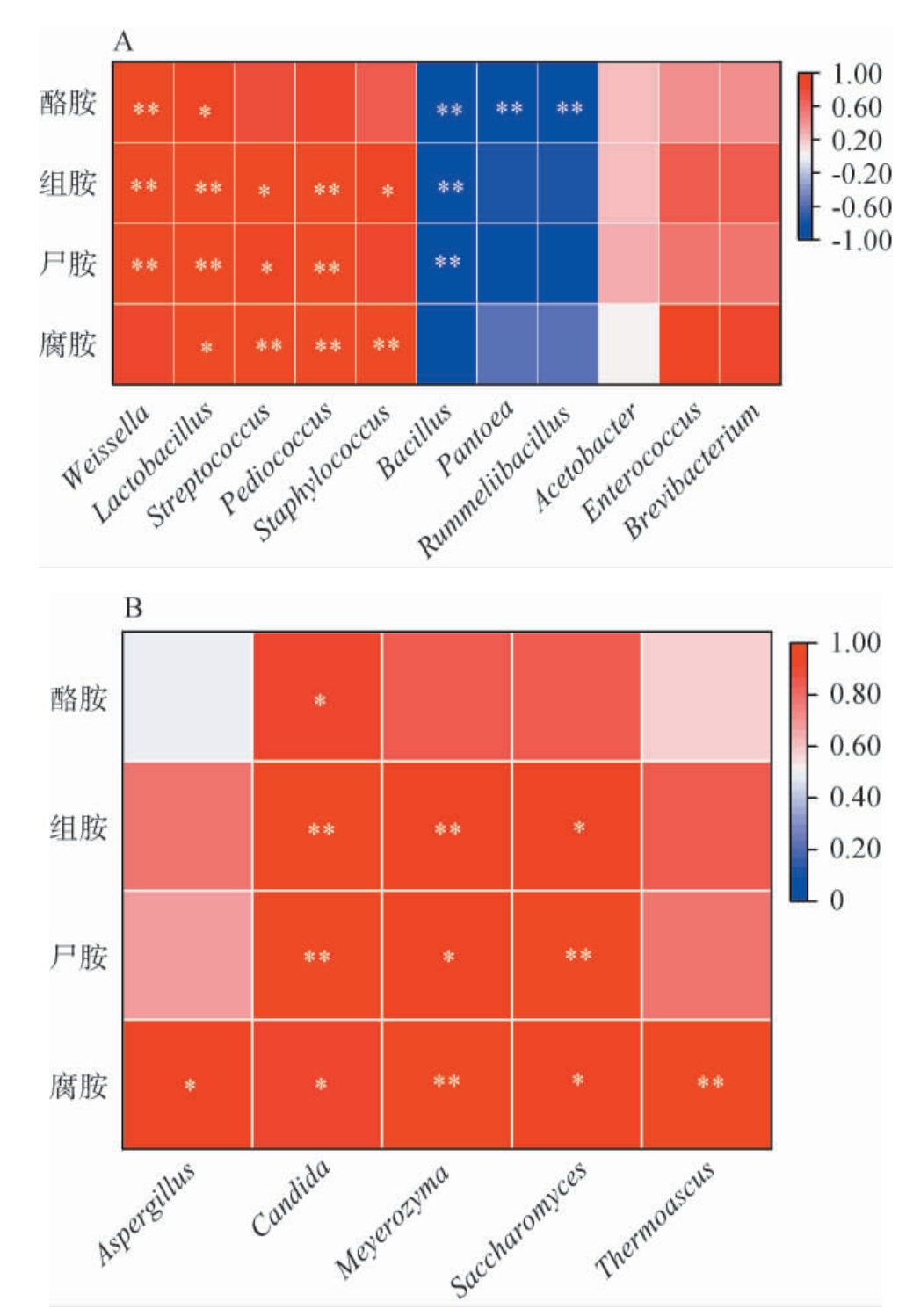
图5 酒精发酵过程中生物胺与细菌属(A)、真菌属(B)的相关性分析热图
Fig.5 Heatmap of correlation analysis among biogenic amines and bacterial genera (A) and fungal genera (B) during alcohol fermentation
由图5A可知,魏斯氏菌属(Weissella)、乳酸杆菌属(Lactobacillus)、链球菌属(Streptococcus)、片球菌属(Pediococcus)、葡萄球菌属(Staphylococcus)、肠球菌属(Enterococcus)和短杆菌属(Brevibacterium)与酒醪中酪胺、组胺、尸胺和腐胺的积累呈正相关。其中,腐胺与乳酸杆菌属呈显著正相关(P<0.05),与链球菌属、片球菌属及葡萄球菌属呈极显著正相关(P<0.01);尸胺与链球菌属呈显著相关(P<0.05),与魏斯氏菌属、乳酸杆菌属及片球菌属呈极显著正相关(P<0.01);组胺与链球菌属及葡萄球菌属呈显著正相关(P<0.05),与魏斯氏菌属、乳酸杆菌属、片球菌属呈极显著正相关(P<0.01);酪胺与乳酸杆菌属呈显著相关(P<0.05),与魏斯氏菌属呈极显著相关(P<0.01)。生物胺在发酵过程中主要通过氨基酸脱羧酶的作用形成,该酶催化底物中游离氨基酸的脱羧反应。现有研究证实,乳酸菌属是该类脱羧酶的主要分泌菌群,其代谢活动直接导致发酵体系中生物胺的累积[18]。研究表明,腐胺、尸胺和亚精胺的含量与乳酸菌属中的短乳杆菌(L.brevis)、发酵乳杆菌(L.fermentum)、希氏乳杆菌(L.hilgardii)和植物乳杆菌(L.plantarum)呈正相关[26]。陈历水等[27]研究表明,黄酒生产过程中酪胺的积累与乳杆菌属、魏斯氏属和片球菌属的丰度呈正相关。牛天娇[18]研究表明,与组胺形成具有相关性菌属为明串珠菌属(Leuconostoc)、糖多孢菌属(Saccharopolyspora)、片球菌属。
此外,芽孢杆菌属(Bacillus)、泛菌属(Pantoea)和乳鼠芽孢杆菌属(Rummeliibacillus)与酒醪中酪胺、组胺、尸胺和腐胺呈负相关。其中,尸胺、组胺和酪胺与芽孢杆菌属呈极显著负相关(P<0.01),酪胺与泛菌属、乳鼠芽孢杆菌属呈极显著负相关(P<0.01)。罗璇等[28]研究表明,发酵豆制备过程中芽孢杆菌属与腐胺、尸胺、组胺和酪胺等7种生物胺含量呈负相关。
由图5B可知,曲霉属(Aspergillus)、假丝酵母菌属(Candida)、迈耶氏酵母属(Meyerozyma)、酿酒酵母属(Saccharomyces)和嗜热子囊菌属(Thermoascus)与酒醪中酪胺、组胺、尸胺和腐胺呈正相关。酵母菌作为酒精发酵阶段的优势菌群,其中,假丝酵母菌属与腐胺和酪胺呈显著正相关(P<0.05),与尸胺、组胺呈极显著正相关(P<0.01);迈耶氏酵母属与尸胺呈显著正相关(P<0.05),与组胺、腐胺呈极显著正相关(P<0.01);酿酒酵母属与组胺、腐胺呈显著正相关(P<0.05),与尸胺成呈极显著正相关(P<0.01),汤苏文[26]研究发现,红曲酒酿造过程中假丝酵母菌属与腐胺和尸胺呈正相关关系。上述结果说明,酵母菌能促进生物胺生成。此外,嗜热子囊菌属与腐胺呈极显著正相关(P<0.01),曲霉属与腐胺的积累呈显著正相关(P<0.05),嗜热子囊菌属与曲霉属可以促进生物胺的生成。
综上,不同微生物菌属对山西老陈醋酒精发酵过程中生物胺的积累与降解作用存在显著差异。细菌中的魏斯氏菌属、乳酸杆菌属等可促进生物胺的积累,而芽孢杆菌属等会降解生物胺。真菌属中的曲霉属、假丝酵母菌属等可促进生物胺的积累,其中假丝酵母菌属等可明显促进生物胺形成。
3 结论
通过对山西老陈醋酒精发酵过程中酒醪的生物胺、常规理化指标和微生物菌群结构变化进行分析,结果表明,随着发酵进行,生物胺含量逐渐上升,其中以腐胺和尸胺为主,酒精度、总酸及氨基酸态氮含量逐渐上升,pH值和还原糖含量逐渐下降。酒醪样品中优势菌属为乳酸杆菌属(Lactobacillus)、魏斯氏菌属(Weissella)、链球菌属(Strepto coccus)、片球菌属(Pediococcus)、假丝酵母菌属(Candida)、酿酒酵母属(Saccharomyces)和曲霉菌属(Aspergillus)(相对丰度>1%)。相关性分析表明,总酸、酒精度、氨基酸态氮与腐胺、尸胺、组胺、酪胺积累呈正相关,还原糖则与之呈负相关;乳酸杆菌属、魏斯氏菌属、链球菌属等与生物胺积累呈正相关,而芽孢杆菌属(Bacillus)、泛菌属(Pantoea)和乳鼠芽孢杆菌属(Rummeliibacillus)则与之呈负相关。本研究可为山西老陈醋酒精发酵过程中生物胺的形成机制提供依据,为后续通过调控菌群结构和理化环境优化山西老陈醋品质提供理论支持。未来可进一步探讨关键产胺菌株的代谢途径及调控机制,通过定向调控微生物菌群结构控制山西老陈醋中的生物胺含量。
[1] 李书婷,尹礼国,吴正云,等.中国黄酒和白酒中生物胺的研究进展[J].食品与发酵工业,2024,50(10):327-334.
[2] 潘思弋,徐佳敏,张惠玲,等.一株降解生物胺乳酸菌用于葡萄酒苹果酸乳酸发酵的特性研究[J].食品与发酵工业,2023,49(24):140-147.
[3] SUN H L,LIU S P,MAO J Q,et al.New insights into the impacts of Huangjiu compontents on intoxication[J].Food Chem,2020,317:126420.
[4] 李芳芳,王艳丽,陈倩倩,等.硅烷化衍生-气相色谱-串联质谱法测定白酒中6种生物胺[J/OL].分析试验室,1-12[2025-11-24].https://link.cnki.net/urlid/11.2017.TF.20250718.0907.004.
[5] 范文来,徐岩,温永柱.白酒发酵与蒸馏过程中5种生物胺变化[J].食品工业科技,2015,36(9):144-146.
[6] 魏泉增,汤雅,李伟民.液相色谱-串联质谱测定食醋中生物胺含量[J].中国酿造,2019,38(4):170-173.
[7] 黄祖新.高效液相色谱法测定福建红曲醋的生物胺[J].福建分析测试,2015(4):43-47.
[8] 邓朝霞.永春老醋发酵过程中有机酸和生物胺变化分析及其细菌菌群结构分析[D].福州:福建师范大学,2014.
[9] 郑宇,张强,刘静,等.我国传统食醋生产过程中潜在危害因子的综述[J].天津科技大学学报,2019,34(4):1-8.
[10] 中华人民共和国国家卫生健康委员会,国家市场监督管理总局.GB 5009.225—2023食品安全国家标准酒和食用酒精中乙醇浓度的测定[S].北京:中国标准出版社,2023.
[11] 中华人民共和国国家质量监督检验检疫总局,中国国家标准化管理委员会.GB/T 19777—2013地理标志产品山西老陈醋[S].北京:中国标准出版社,2013.
[12] 中华人民共和国国家卫生和计划生育委员会,国家食品药品监督管理总局.GB/T 5009.208—2016食品安全国家标准 食品中生物胺的测定[S].北京:中国标准出版社,2016.
[13] 聂志强,韩玥,郑宇,等.宏基因组学技术分析传统食醋发酵过程微生物多样性[J].食品科学,2013,34(15):198-203.
[14] 孙晓琪,朱丹,张慧如,等.不同地区山西老陈醋酿造过程中细菌菌群多样性分析[J].中国酿造,2023,42(6):116-121.
[15] 朱丹,孙晓琪,张慧如,等.山西老陈醋发酵过程中真菌菌群结构及多样性[J].中国酿造,2023,42(6):103-108.
[16] 杨玲,刘春,彭佳伟,等.山西老陈醋和怀仁醋酒精发酵阶段细菌菌群多样性分析[J].中国酿造,2023,42(2):63-69.
[17] 许禄.黄酒酿造过程中生物胺变化规律的研究[D].上海:上海海洋大学,2016.
[18] 牛天娇.黄酒酿造中微生物菌群结构及对生物胺降解作用研究[D].哈尔滨:哈尔滨工业大学,2020.
[19] 任宇婷,乔美灵,孙子羽,等.清香型白酒发酵过程中高级醇形成规律[J].食品与发酵工业,2023,49(4):38-44.
[20] 陈旭峰,朱丹,郭宏萍,等.山西老陈醋酿造过程中理化指标动态变化及新淋醋品质分析[J].中国酿造,2021,40(12):52-57.
[21] WU Y F,XIA M L,ZHANG X F,et al.Unraveling the metabolic network of organic acids in solid-state fermentation of Chinese cereal vinegar[J].Food Sci Nutr,2021,9(8):4375-4384.
[22] 文悦,贾俊杰,敖宗华,等.浓香型白酒糟醅发酵过程微生物群落演替研究进展[J].中国酿造,2025,44(4):20-26.
[23] 赵欣,张钰婧,陈旭峰,等.不同生产模式和季节下山西老陈醋酒精和醋酸发酵微生物菌落总数最高峰时期真菌群落的对比分析[J].食品工业科技,2025,46(12):197-205.
[24] 杨玲,彭佳伟,郭旭凯,等.基于高通量测序山西老陈醋和怀仁醋酒精发酵初期酒醅真菌菌群研究[J].中国酿造,2024,43(4):109-114.
[25] 李敏.夏冬两季食醋微生物群落演替特征及其特征微生物研究[D].太原:太原理工大学,2019.
[26] 汤苏文.红曲酒传统酿造过程生物胺生成规律及调控技术研究[D].福州:福州大学,2021.
[27] 陈历水,沈雪梅,刘蕾,等.黄酒生产过程中细菌群落结构与生物胺含量变化分析[J].食品研究与开发,2018,39(11):76-83.
[28] 罗璇,程成,张琦,等.发酵豆制品理化性质与微生物群落对生物胺形成的影响[J].食品科学,2023,44(14):72-78.