近年来,为满足国内消费群体对高端手工雪茄的需求[1],烟草行业陆续开展了国产雪茄烟技术开发与应用等科技项目助推国产雪茄烟发展。但受产区间气候条件、烟叶微生物发酵工艺[2]参差不齐的影响,国产雪茄烟叶的质量风格、使用定位与国外原料仍有较大差距。
手工雪茄是由茄衣、茄套和茄芯3部分烟叶卷制而成的烟支,不同产区烟叶的搭配赋予了整支雪茄的香气风格与内在品质。国内优质雪茄烟叶产区分布广泛且各具特色。海南产区属热带海洋性季风气候,光温充足,降雨量充沛,土壤矿物质含量丰富,所产雪茄烟叶色泽均匀,香气浓郁,醇厚丰满[3]。四川什邡属亚热带季风性气候,日照时数和无霜期长,烟叶以木香、干草香为主,辅以蜜甜香,燃烧性好,灰色白[4]。湖南省地处亚热带季风气候区,光照、雨水条件较为适宜,雪茄烟叶风格较显著,香气质好,烟气飘逸、细腻且柔和,甜润感较突出,燃烧性好[5]。发酵工艺可改善烟叶的外观和内在质量,使烟叶达到加工工艺要求[6],是雪茄烟生产的核心工序。细菌和真菌在雪茄烟叶发酵过程中扮演着重要角色,不仅可分解烟叶中糖类、蛋白质等大分子物质,还可提供致香物质前体物,改善烟叶感官品质[7]。但前人研究发现,雪茄外包皮烟叶发酵时主要种属为棒状杆菌属(Corynebacterium)、葡萄球菌属(Staphylococcus)、不动杆菌属(Acinetobacter)、假单胞菌属(Pseudomonas),且烟叶细菌群落数量、结构会随发酵进程呈动态变化[8-9]。同时,叶长文等[10]研究发现,来源于不同产地国的雪茄样品中细菌和真菌群落多样性和结构存在显著差异,而其中来自同一产地国的GXB和MT样品菌群分布比较相似。
烟叶菌群组成受产区条件[11]、工艺水平[12]等因素的影响较大。截至目前,国内主要研究烟叶发酵工艺参数,国内不同产区雪茄烟叶发酵前后细菌群落变化的研究鲜见报道[13]。因此,解析不同产区雪茄烟叶发酵前后微生物群落演替变化规律对改善烟叶质量具有重要意义。鉴于此,本研究选取海南、湖南和四川3个雪茄产区的烟叶,利用高通量测序技术解析发酵前后烟叶微生物多样性及群落结构特征变化规律,为定向开发利用烟叶优势功能微生物提供理论参考。
1 材料与方法
1.1 材料与试剂
烟叶:取自2021年海南、湖南和四川雪茄产区中部烟叶,分别记为HA、HU、SC。发酵介质:蒸馏水。
1.2 仪器与设备
FA1204C电子分析天平:上海天美天平仪器有限公司;HWS-250恒温恒湿箱:上海苏盈试验仪器有限公司;HY-5型回旋式振荡器:常州荣华仪器制造有限公司;Eppendorf Centrifuge5424R高速台式冷冻离心机:德国Eppendorf公司;Illumina MiSeq测序仪:上海派森诺生物科技有限公司;E.Z.N.A. soil试剂盒:美国OMEGA公司;Forma-86C ULT Freezer超低温冰箱:美国赛默飞世尔科技(中国)有限公司。
soil试剂盒:美国OMEGA公司;Forma-86C ULT Freezer超低温冰箱:美国赛默飞世尔科技(中国)有限公司。
1.3 方法
1.3.1 烟叶发酵与取样
试验统一于河南农业大学烟草栽培生理生化基地实验室内进行。发酵前先将烟叶均匀平铺于实验台面,称取一定量的蒸馏水于喷雾装置中,将雾化水均匀喷于烟叶正面,烟叶背面亦按此操作进行处理。将回潮后烟叶置于密闭自封袋中回潮,待回潮均匀充分后,取3片采用烘箱法测量其水分。待回潮至含水率26%~28%时停止回潮,将回潮后的烟叶置于自封袋内作为发酵前样品,于恒温恒湿箱中在温度45 ℃、相对湿度80%条件下发酵20 d,作为发酵后样品。
分别于发酵前(0 d)和发酵完成后(20 d)取烟叶样品,海南、湖南和四川地区发酵前样品分别记为HA-1、HU-1、SC-1,发酵后烟叶样品分别记为HA-2、HU-2、SC-2,每次取样100 g,每个样品重复3次,样品采集后迅速置于液氮中冷冻,之后于-80 ℃超低温冰箱中保藏。
1.3.2 微生物脱氧核糖核酸提取
使用无菌剪刀各取发酵前后的烟叶100 g完全浸没于有磷酸盐缓冲液(phosphate buffer solution,PBS)的锥形瓶中,37 ℃、200 r/min振荡摇匀1 h。振荡结束后,于8 000 r/min离心5 min,收集沉淀。采用E.Z.N.A. soil试剂盒提取样品基因组脱氧核糖核酸(deoxyribonucleic acid,DNA),每个样品进行4次重复。
soil试剂盒提取样品基因组脱氧核糖核酸(deoxyribonucleic acid,DNA),每个样品进行4次重复。
1.3.3 聚合酶链式反应扩增及高通量测序
对细菌16S rDNA的V5~V7区和真菌的ITS1可变区进行聚合酶链式反应(polymerase chain reaction,PCR)扩增,细菌采用799F(5'-AACMGGATTAGATACCCKG-3')和1193R(5'-ACGTCATCCCCACCTTCC515F-3')扩增引物;真菌采用ITS1F(5'-CTTGGTCATTTAGAGGAAGTAA-3')和ITS2(5'-GCTGCGTTCTTCATCGATGC-3')扩增引物。
PCR扩增体系(10 μL)1 μL的DNA(质量浓度50 ng/μL)、2×Rapid Taq Master Mix(含Taq DNA聚合酶、脱氧核糖核苷三磷酸(deoxy-ribonucleoside triphosphates,dNTPs)、MgCl2以及反应缓冲液)5 μL、上游引物1 μL、下游引物1 μL,剩余体系用双蒸水(ddH2O)定量。PCR扩增程序:98 ℃预变性5 min,98 ℃变性30 s,52 ℃退火30 s,72 ℃延伸1 min,共25个循环,最终72 ℃延伸5 min。
扩增完成后使用Axygen凝胶回收试剂盒进行扩增片段回收,回收的DNA片段使用Tru Seq Nano DNA LT Library Prep Kit试剂盒进行文库构建,并使用Illumina MiSeq测序仪进行基因测序。PCR扩增参数、文库构建以及基因测序流程均参照文献[14]进行。
1.3.4 数据处理
使用USEARCH软件在相似性97%的水平上对有效数据进行聚类,得到操作分类单元(operational taxonomic unit,OTU),基于OTUs聚类结果,通过Alpha多样性指数、在门和属水平上细菌群落相对丰度分析对样品中物种进行注释与评估。采用OriginPro 2023软件绘制Venn图,Excel 2013软件进行数据处理及表格制作;利用Gephi软件(version 0.9.2)进行主要菌群关系可视化。
2 结果与分析
2.1 不同产区雪茄烟叶发酵前后细菌和真菌群落多样性分析
2.1.1 Alpha多样性分析
不同产区雪茄烟叶发酵前后细菌及真菌Alpha多样性分析结果分别见表1和表2。由表1、表2可知,烟叶的高通量测序覆盖率均高于0.999 0,表明实验数据能够全面地反映出烟叶表面微生物物种相对丰度及多样性状况。对不同产区发酵前的烟叶进行比较,细菌OTU数从高到低依次呈现为四川、海南、湖南,真菌OTU数则刚好相反,从高到低表现为湖南、海南、四川。其中,湖南和四川产区烟叶发酵后细菌和真菌OTU数均有所降低,而海南产区与发酵前相比,OTU数明显增加。
表1 不同产区雪茄烟叶发酵前后细菌Alpha多样性分析
Table 1 Alpha diversity analysis of bacteria in cigar tobacco leaves in different producing areas before and after fermentation
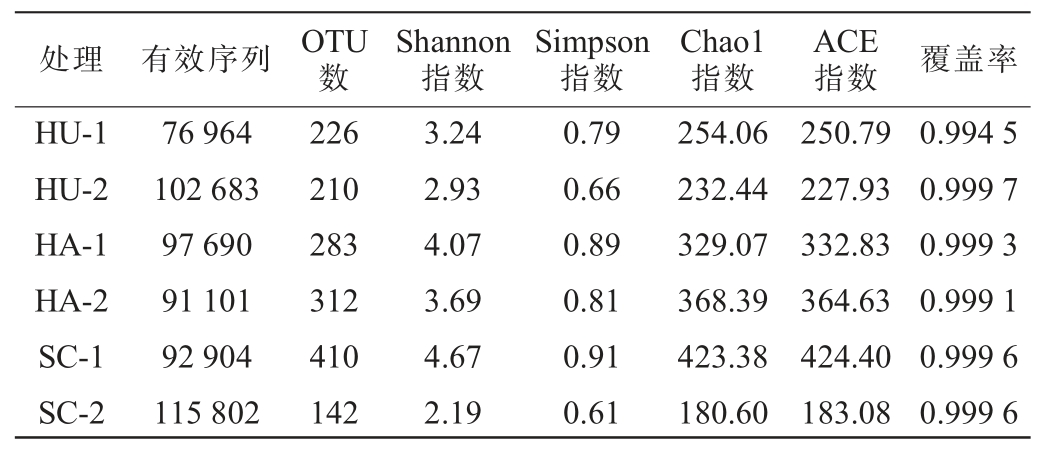
表2 不同产区雪茄烟叶发酵前后真菌Alpha多样性分析
Table 2 Alpha diversity analysis of fungi in cigar tobacco leaves in different producing areas before and after fermentation
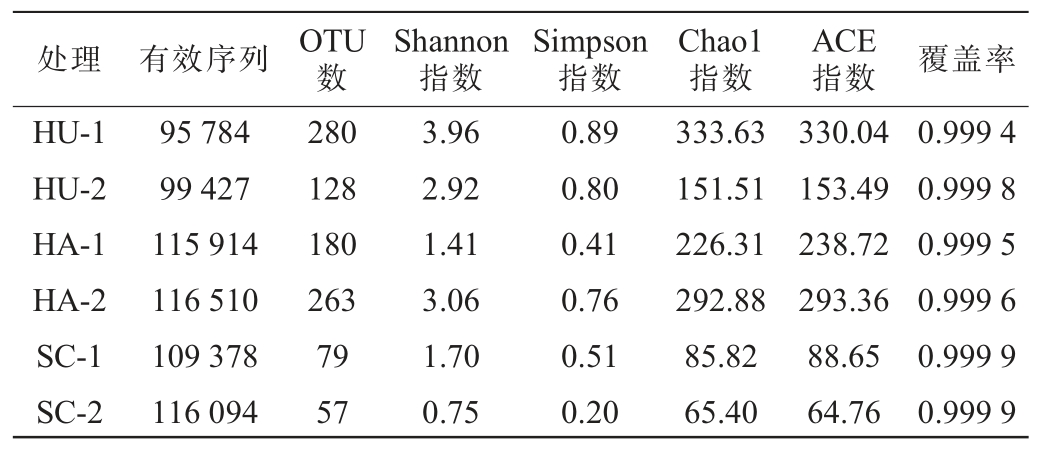
不同产区烟叶细菌和真菌Chao1指数、ACE指数、Shannon指数和Simpson指数值有所差异。这是因为烟叶的微生物群落来源于雪茄烟植烟土壤、周围环境以及环境中微生物群落[15],而不同产区特殊的土壤、气候以及环境微生物条件造成了形态各异的烟叶微生物群落。未发酵烟叶中以四川产区烟叶的细菌群落Chao1指数、ACE指数、Shannon指数和Simpson指数最高,分别为423.38、424.40、4.67和0.91,其次为海南产区,湖南产区最低;而未发酵烟叶中的真菌群落各项指数则以湖南产区最高,分别为333.63、330.04、3.96和0.89,其次为海南产区,四川产区最低。表明发酵前烟叶细菌物种种类和数目以四川产区较高,真菌物种则以湖南产区最高。
同产区烟叶发酵前后比较发现,湖南和四川产区发酵后烟叶细菌和真菌Chao1指数、ACE指数、Shannon指数和Simpson指数均明显下降。海南产区烟叶发酵后细菌Shannon指数和Simpson指数下降,细菌的Chao1、ACE指数和真菌Chao1指数、ACE指数、Shannon指数和Simpson指数均有明显增加。表明海南雪茄烟叶正处于雪茄发酵前期阶段,细菌和真菌物种的丰富度以及多样性增加;而湖南和四川烟叶已经发酵完全,细菌和真菌物种的丰富度以及多样性降低,发酵过程中烟叶表面细菌和真菌群落多样性指标呈先升高后降低趋势。这与林晓路等[16]研究结果相吻合。
2.1.2 OTU分析
不同产区雪茄烟叶发酵前后细菌及真菌OTU数量韦恩图分别见图1和图2。
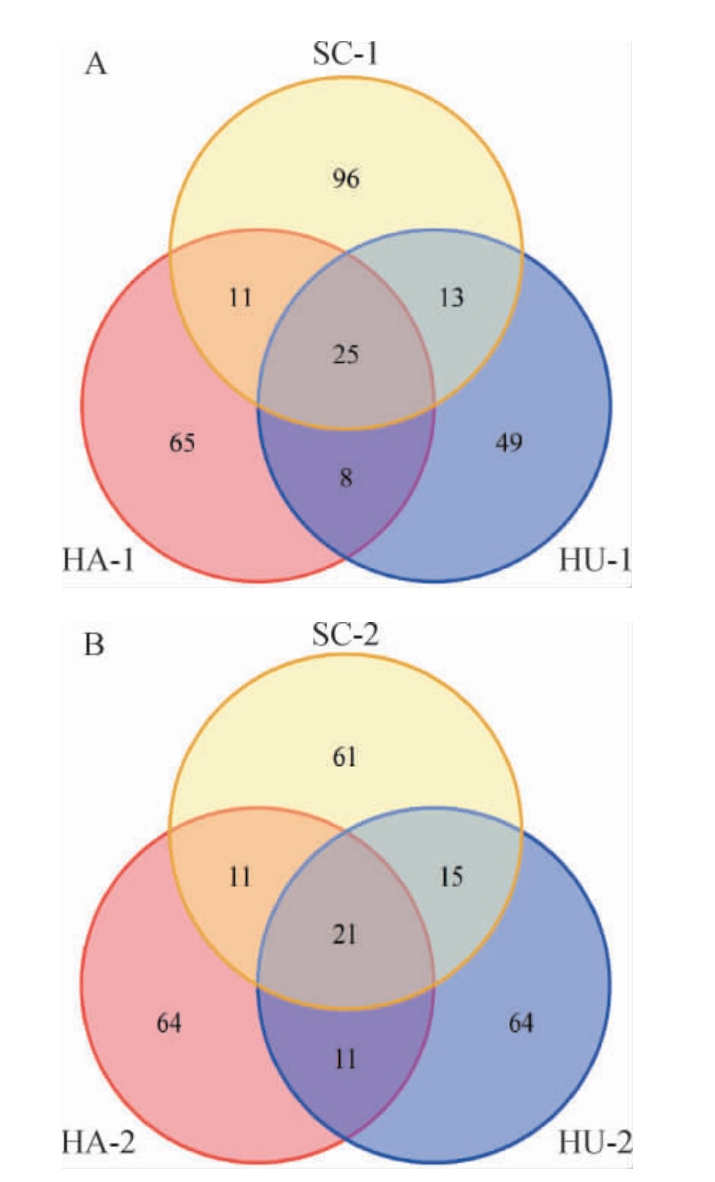
图1 不同产区雪茄烟叶发酵前(A)与发酵后(B)细菌OTU数量韦恩图
Fig.1 Venn diagram of bacteria OTU number in cigar tobacco leaves from different producing areas before (A) and after (B) fermentation
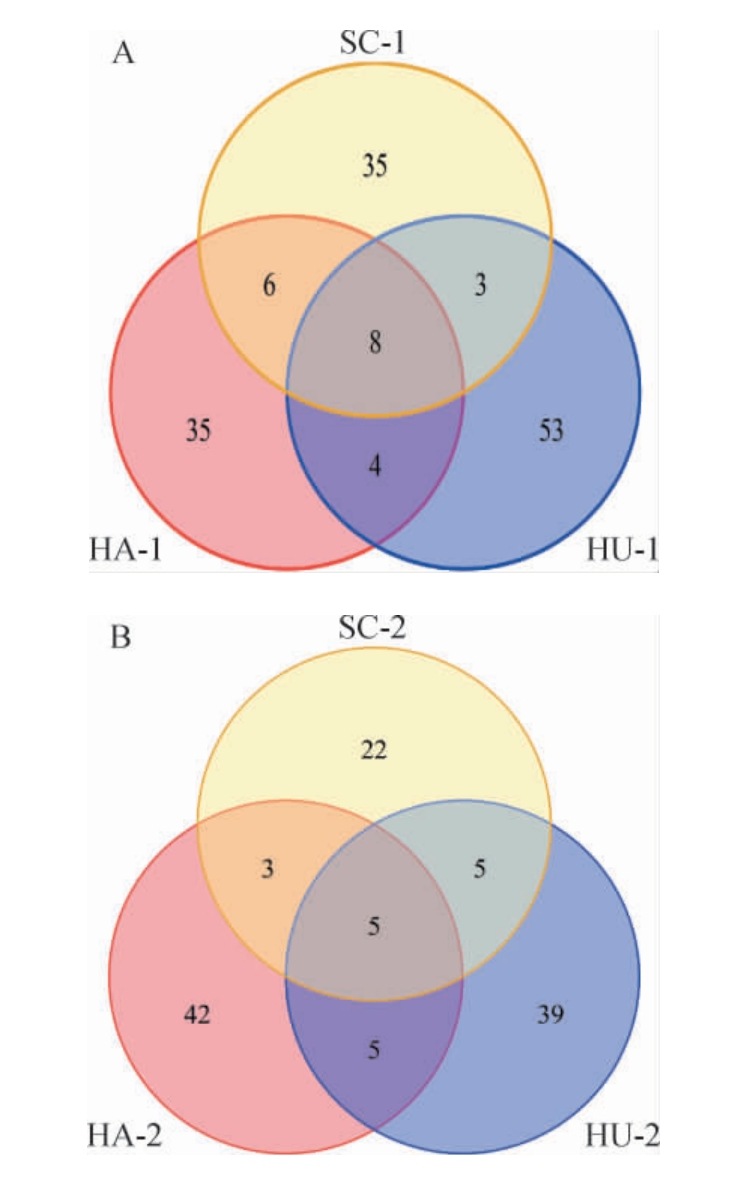
图2 不同产区雪茄烟叶发酵前(A)与发酵后(B)真菌OTU数量韦恩图
Fig.2 Venn diagram of fungi OTU number in cigar tobacco leaves from different producing areas before (A) and after (B)fermentation
由图1可知,发酵前四川产区的细菌OTU总数为145个,明显高于海南产区的OTU总数109个和湖南产区的OTU总数95个;发酵后四川产区的OTU数量为108个,与海南产区的OTU总数107个及湖南产区的OTU总数111个相当。发酵前3个产区烟叶细菌的共有OTU数为25个;而特有OTU数由高到低依次表现为四川、海南、湖南,分别占各自OTU总数的66.21%、59.63%和51.58%。发酵后3个产区的共有细菌OTU数下降至21个,而四川、海南、湖南3个产区的特有细菌OTU数为61个、64个、64个,无明显差异。其中,四川产区特有OTU数与发酵前相比下降最多,由96个下降至61个,表明发酵工序整体上会降低烟叶细菌群落的多样性。
由图2可知,发酵前后3个产区真菌共有OTU数分别为8个、5个,明显低于细菌共有OTU数。发酵前各产区特有OTU数以湖南产区最多,为53个,占其总OTU数的77.94%。发酵后以海南产区特有OTU数最多,为42个。发酵降低湖南和四川产区烟叶真菌多样性,增加海南烟叶真菌多样性,烟叶细菌群落结构与优势菌群改变[12]。海南产区发酵前后烟叶真菌的OTU数增加,这可能与海南产区烟叶身份较厚,油分较足、糖类物质含量较高,发酵时有利于烟叶微生物的繁殖有关[17]。
2.2 不同产区雪茄烟叶发酵前后细菌和真菌群落结构分析
2.2.1 烟叶细菌群落结构分析
不同产区雪茄烟叶发酵前后基于门水平和属水平的细菌群落分析见图3。以相对丰度>1%的菌门(或属)列为优势菌门(属)。由图3A可知,在门水平上,发酵前各产区烟叶的细菌主要为变形菌门(Proteobacteria)、厚壁菌门(Firmicutes)等,这与前人研究结果相吻合[16]。其中,Proteobacteria在3个产区中均占据主导地位,以湖南产区相对丰度最高,为93.19%,其次为海南产区。Firmicutes为四川产区的次优势菌门,相对丰度为25.32%,明显高于湖南和海南产区。说明不同产区特有的微生物和环境因素、微生物之间的互作关系不同,导致了产区间烟叶优势微生物相对丰度的差异[18]。发酵后海南产区细菌物种组成和含量没有明显差异,而四川和湖南产区发酵后烟叶的Proteobacteria相对丰度明显降低,Firmicutes相对丰度明显增加,成为发酵后烟叶的主要优势菌门。这与郑霖霖[19]的研究结果相吻合。
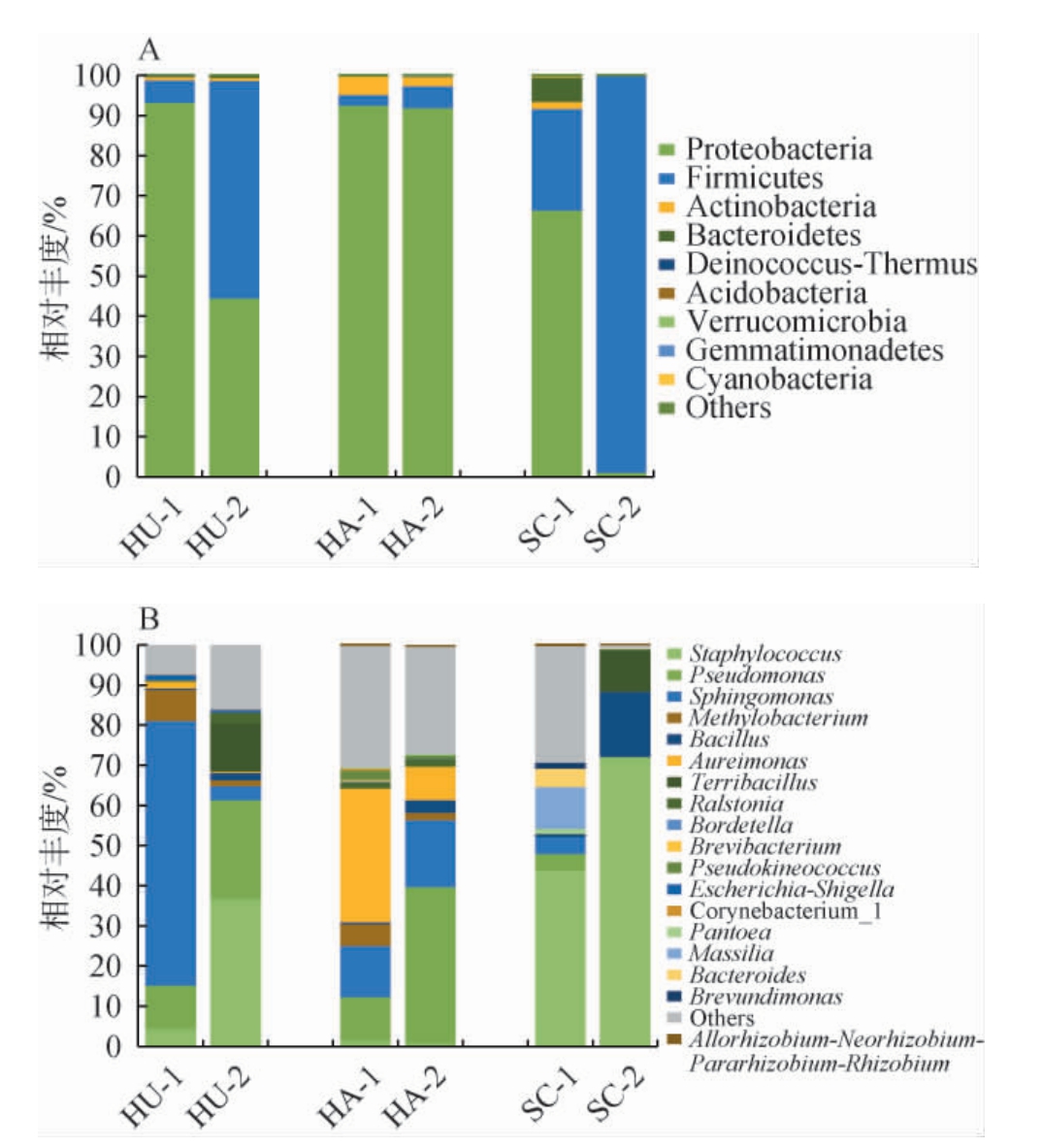
图3 基于门水平(A)和属水平(B)不同产区雪茄烟叶发酵前后细菌群落结构
Fig.3 Bacterial communities structure of cigar tobacco leaves in different producing areas before and after fermentation based on phylum level (A) and genus level (B)
微生物在烟叶发酵过程中不仅能降解烟叶中糖类、烟碱[20]等大分子物质,还能调节脂肪类物质代谢,形成醛酮类致香物质[21],进而改善烟叶吸食品质[22]。由图3B可知,在属水平上,发酵前3个产区烟叶的主要优势菌属有所差异,其中湖南产区以鞘氨醇单胞菌属(Sphingomonas)为主,海南、四川产区的主要优势菌属则分别为金色单胞菌属(Aureimonas)、葡萄球菌属(Staphylococcus)。且发酵前湖南和海南产区烟叶的细菌群落组成较为相似,其次的优势菌属均为假单胞菌属(Pseudomonas)、甲基杆菌属(Methylobacterium),而四川产区以马赛菌属(Massilia)、拟杆菌属(Bacteroides)等为次优势菌属。发酵后3个产区的烟叶细菌群落结构和含量均存在明显差异。湖南和四川产区均以Staphylococcus的相对丰度增加最多,与发酵前相比增加了30个百分点左右;海南产区中Pseudomonas的相对丰度增加了28.12个百分点。这与前人发现烟叶发酵后Staphylococcus倍数级增加,而Pseudomonas丰度增加较不明显的研究结果有所不同[23],这可能与不同产区烟叶本身质量以及发酵工艺参数不同有关。除此之外,3个产区发酵后烟叶的芽孢杆菌属(Bacillus)含量明显增加。这与芽孢杆菌属自身营养需求简单[24],对烟叶发酵过程中温度、水分和pH等外部条件变化的适应性强有关。
2.2.2 烟叶真菌群落结构
不同产区雪茄烟叶发酵前后基于门和属水平的真菌群落分析见图4。由图4A可知,在门水平上,烟叶发酵前后,子囊菌门(Ascomycota)均为各产区烟叶的绝对优势真菌门,相对丰度为86.00%~99.00%,表明Ascomycota在烟叶发酵过程中起主导作用。除此之外,担子菌门(Basidiomycota)在烟叶中也有少量分布,相对丰度为1.00%~14.00%。
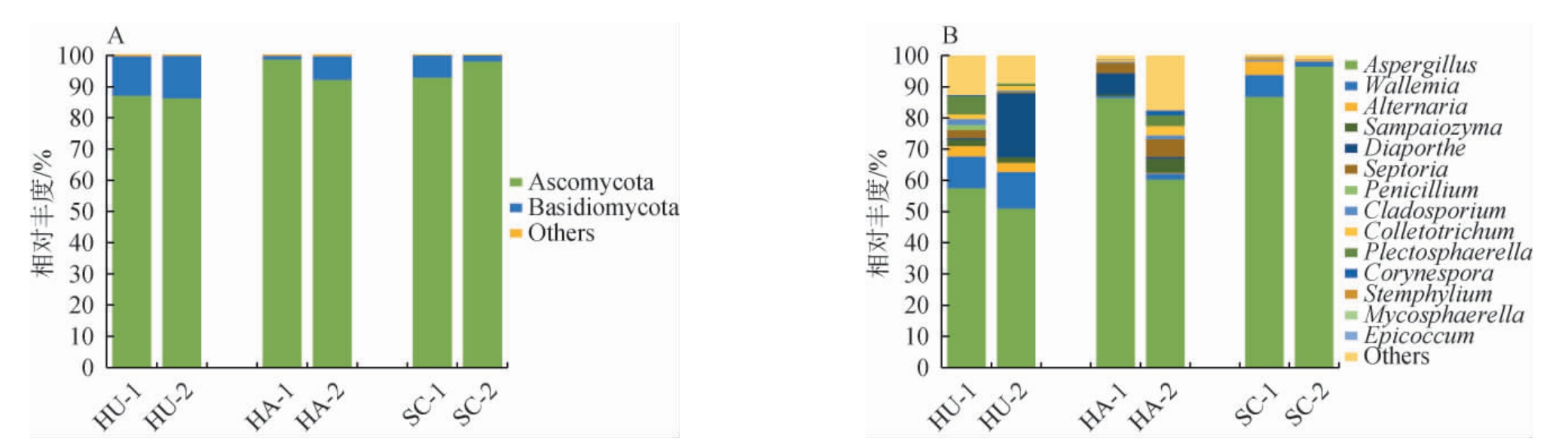
图4 基于门水平(A)和属水平(B)不同产区雪茄烟叶发酵前后真菌群落结构
Fig.4 Fungal communities structure of cigar tobacco leaves in different producing areas before and after fermentation based on phylum level (A) and genus level (B)
由图4B可知,在属水平上,发酵前各产区雪茄烟叶中检测到的主要优势真菌属均为曲霉属(Aspergillus)。表明雪茄烟叶的优势真菌受产区环境、遗传信息和发酵工艺参数等因素的影响基本相同且具有普遍性[25]。发酵后湖南、海南和四川产区烟叶主要真菌属则为曲霉属(Aspergillus)、节担菌属(Wallemia)、链格孢属(Alternaria)和间座壳属(Diaporthe)等。其中,Aspergillus在各产区发酵前后的烟叶中占绝对优势,相对丰度均在50.00%以上,发酵前后不同产区其菌落相对丰度从大到小依次为四川、海南、湖南产区。Wallemia丰度与烟叶酮类物质的积累呈正相关[26]。Wallemia作为湖南产区的次优势菌属,发酵前后相对丰度无明显差异,均在10.00%左右,明显高于其他产区。这与前人研究发现Wallemia是烟叶发酵后的主要差异微生物相一致[27],这可能与湖南产区雪茄烟起步较晚,尚不成熟的发酵工艺影响了烟叶中微生物群落的生长代谢有关[28]。
2.3 不同产区雪茄烟叶发酵后细菌和真菌共现性分析
微生物群落结构和功能都受微生物共生类群因素的调控[28-29]。选择以r>|0.5|和P<0.05为条件,分别建立不同产区雪茄烟叶发酵后细菌和真菌群落的相关性分析图,图中网络节点代表群落中属水平上的物种,节点的大小代表该菌属的相对丰度高低,边代表菌属间的关系,红色为正相关,蓝色为负相关,线条粗细表示相关程度,线条越粗,表明相关系数越高。细菌和真菌群落相关性分析结果见图5和图6。
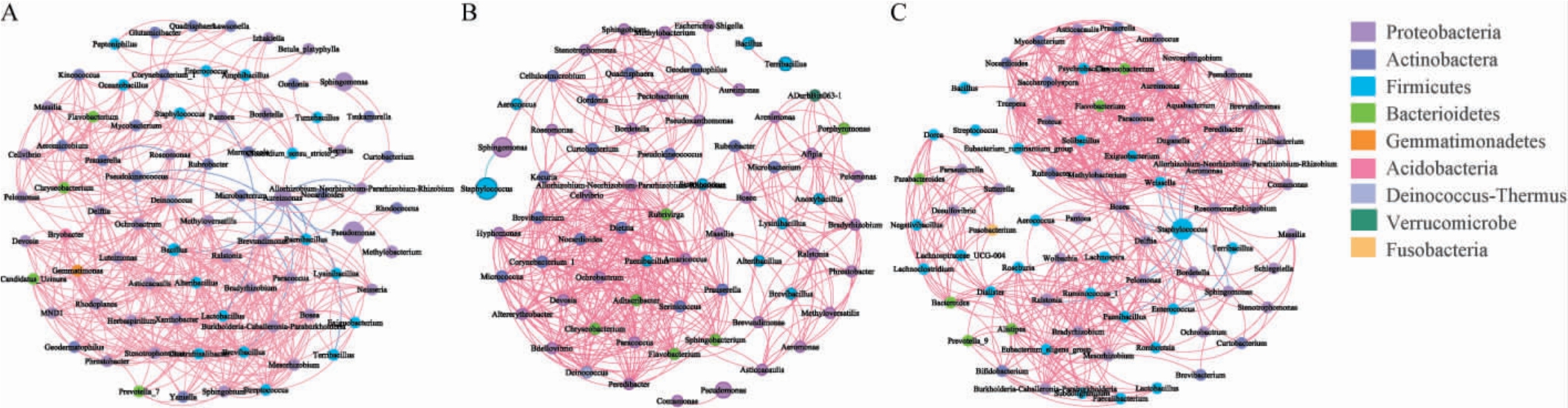
图5 海南(A)、湖南(B)和四川(C)产区雪茄烟叶发酵后细菌群落相关性分析
Fig.5 Correlation analysis of bacterial community of cigar tobacco leaves in Hainan (A),Hunan (B) and Sichuan (C) producing areas after fermentation
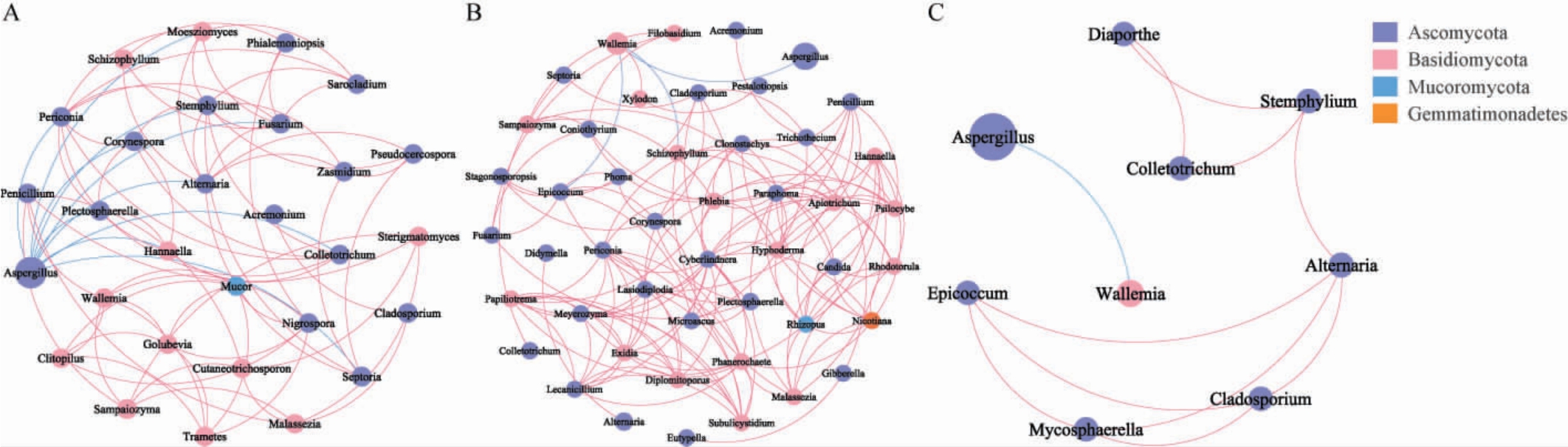
图6 海南(A)、湖南(B)和四川(C)产区雪茄烟叶发酵后真菌群落相关性分析
Fig.6 Correlation analysis of fungal community of cigar tobacco in Hainan (A),Hunan (B) and Sichuan (C) after fermentation
由图5可知,在烟叶细菌群落中,海南、湖南和四川产区分别包含77个、68个和78个节点。其中,细菌网络中的节点按门划分,海南和湖南烟叶的细菌网络节点均以Proteobacteria、Actinobacteria为主,分别占总节点数的45.45%、24.68%和50.00%、23.53%;而四川烟叶细菌网络的节点以Proteobacteria为主,占到总节点数的46.15%,剩下节点中59.5%以上归属于Firmicutes。各产区烟叶细菌网络均以正相关连接为主,表明烟叶中细菌存在较强的共生关系,竞争关系较弱。对比发现,各产区烟叶细菌网络中节点数、边数量、平均度(每个节点平均拥有的连接数)以及聚集系数(节点邻居之间也互相连接的平均程度)均表现为四川>海南>湖南,表明四川烟叶其细菌网络规模更大,群落之间的关系相对复杂,海南次之。四川烟叶主要优势菌属葡萄球菌属(Staphylococcus)与其他菌属呈竞争关系,而海南烟叶中的主要优势菌属假单胞菌属(Pseudomonas),与其他菌属相关性较弱。
由图6可知,不同产区真菌节点数和连接数明显低于细菌,表明在烟叶中细菌较真菌作用更复杂。这与贾云等[28]研究发现不同微生物属间48个细菌节点和45个真菌节点的结果相吻合。按门划分,海南烟叶真菌网络中节点分别属于Ascomycota、Basidiomycota、毛霉门(Mucoromycota),其中Ascomycota为主,占总节点数的58.62%。Aspergillus与其他真菌属之间既有竞争又有合作关系,但竞争关系占主导地位。湖南烟叶节点分属于Ascomycota、Basidiomycota、毛霉门(Mucoromycota),以Ascomycota为主,主要菌属Aspergillus与其他真菌属间相关性较弱,只与Wallemia存在竞争关系。与细菌相反,湖南烟叶真菌网络中节点数、边数量表现为湖南>海南>四川,且平均度以及聚集系数则高于海南和四川产区,表明湖南烟叶中真菌群落之间的连接数最多,菌群最为复杂。四川烟叶中的节点数较其余产区最少,节点所属门只有Ascomycota和Basidiomycota,分别占总节点数的88.89%、11.11%,除Aspergillus外,其余均以正相关连接为主,这是由于微生物通过彼此间的群落演替活动,正向调控了其代谢强度与生存环境,进而推动了相关微生物菌属的共存[30]。网络路径距离反映了物种间传递物质、能量及信息的效率。对比发现,湖南产区烟叶网络平均群聚系数较低,而网络平均路径距离较长,表明湖南烟叶真菌群落结构更为稳定,能更好的适应外部环境变化带来的影响。
3 结论
细菌和真菌在雪茄烟叶发酵过程中扮演着关键角色,而其群落结构和功能直接受产区环境与烟叶自身理化性质的影响。本研究对四川、湖南和海南产区烟叶的微生物群落组成及细菌与真菌间关系进行了分析,初步揭示了不同产区发酵前后烟叶微生物群落的组成差异规律,发酵前烟叶细菌群落多样性以四川产区最高,真菌以湖南产区最高;发酵后除海南外其余产区均有一定程度的下降。湖南、海南、四川产区烟叶发酵前主要优势细菌属分别为鞘氨醇单胞菌属(Sphingomonas)、金色单胞菌属(Aureimonas)和葡萄球菌属(Staphylococcus),海南产区烟叶发酵后优势细菌属为假单胞菌属(Pseudomonas)、湖南、四川产区烟叶发酵后优势细菌属为葡萄球菌属(Staphylococcus);而各产区发酵前后烟叶的优势真菌属均为曲霉属(Aspergillus)。雪茄烟叶中的微生物群落以共生合作关系为主,细菌群落的网络规模和复杂性均高于真菌群落。四川烟叶的细菌网络最复杂且以竞争关系为主;湖南烟叶的真菌网络连接最紧密、结构最稳定。本研究可为企业定向开发利用功能微生物进行烟叶品质提升提供理论依据。但本研究对微生物的研究基于门和属水平上,尚未从科水平上深入分析产区烟叶中微生物菌属含量、分布情况和PICRUSt功能预测,后续将进一步研究。
[1] 周婷,范静苑,邢蕾,等.国产雪茄烟叶原料应用研究的探索和思考[J].现代工业经济和信息化,2021,11(7):140-142,148.
[2] 张倩颖,罗诚,李东亮,等.雪茄烟叶调制及发酵技术研究进展[J].中国烟草学报,2020,26(4):1-6.
[3] 姚芳.海南茄衣叶面微生物鉴定及其在人工发酵过程对雪茄烟叶品质的影响[D].郑州:河南农业大学,2017.
[4]管庆林.大中微量元素配施对雪茄烟叶生理特性及产质量的影响[D].郑州:河南农业大学,2023.
[5] 向东.湖南张家界雪茄烟品种初选及配套生产技术研究[D].郑州:河南农业大学,2022.
[6] 庹有朋,王刚,段旺军,等.利用生物技术对烤烟发酵的研究[J].食品与发酵科技,2020,56(2):69-75.
[7] 赵铭钦,李芳芳.微生物和酶学技术在烟草发酵中的应用及展望[J].中国农学通报,2007(1):314-318.
[8] 张磊,罗泽华,杨明川,等.雪茄烟叶原料发酵微生物多样性及酶活变化研究[J].中国农业科技导报,2021,23(10):171-180.
[9] 张鸽,梁开朝,辛玉华,等.基于高通量测序和传统分离研究雪茄外包皮表面细菌多样性及演替[J].应用与环境生物学报,2018,24(4):783-788.
[10] 叶长文,李璐,贺琛,等.基于高通量测序的雪茄烟微生物群落结构和多样性分析[J].烟草科技,2021,54(8):1-9.
[11] 郑天飞,张倩颖,李东亮,等.不同产地雪茄烟叶的风味特征和微生物群落分析[J].河南农业科学,2022,51(8):45-54.
[12] 陈音,孙贤,郑召君,等.加料发酵对茄芯烟叶化学成分及表面细菌多样性的影响[J].中国烟草学报,2023,29(1):106-115.
[13] 阴耕云,肖冬,王凯,等.基于16S rRNA基因测序分析烟叶发酵过程中表面微生物的多样性[J].食品与生物技术学报,2024,43(3):102-112.
[14] 郑霖霖,赵亮,蔡兴华,等.雪茄茄芯烟叶工业二次发酵过程中细菌与真菌群落多样性变化分析[J].中国烟草学报,2022,28(5):121-128.
[15] LIU S P,HU J,XU Y Z,et al.Combined use of single molecule real-time DNA sequencing technology and culture-dependent methods to analyze the functional microorganisms in inoculated raw wheat Qu[J].Food Res Int,2020,132(5):109062.
[16] 林晓路,杨婷,沈福龙,等.发酵时间对雪茄烟叶化学物质含量及微生物群落结构的影响[J].烟草科技,2025,58(8):28-37.
[17] 潘勇,吴巧茵,李林林,等.国产雪茄烟叶堆积发酵过程中的微生物变化规律及差异分析[J].河南农业科学,2022,51(11):171-180.
[18] ZHOU J,YU L,ZHANG J,et al.Dynamic characteristics and co-occurrence patterns of microbial community in tobacco leaves during the 24month aging process[J].Ann Microbiol,2021,71(1):9.
[19] 郑霖霖.不同发酵工艺下茄芯烟叶的微生物群落与品质变化及相关性分析[D].郑州:河南农业大学,2023.
[20] 徐慧,党立志,杨根华,等.烟碱降解菌的筛选,鉴定及其降解性能的初步研究[J].云南大学学报(自然科学版),2013,35(4):580-586.
[21] OHANAYAC,MATTIAS DH,AGATAJ,et al.Cultivation-independent and cultivation-dependent metagenomes reveal genetic and enzymatic potential of microbial community involved in the degradation of a complex microbial polymer[J].Microbiome,2020,8(1):76.
[22] 赵亮,琚绍煊,时向东,等.芽孢杆菌属在烟叶发酵和醇化中的应用研究进展[J].安徽农业科学,2024,52(21):1-4.
[23] 张鸽,李志豪,邓帅军,等.海南H382雪茄烟叶不同发酵周期细菌群落多样性表征及演替分析[J].中国烟草学报,2021,27(2):117-126.
[24] 徐靖,牛邦彦,张亚南,等.芽孢杆菌属Bacillus分类学研究进展[J].中国土壤与肥料,2022(12):225-237.
[25] ZHENG T F,ZHANG Q Y,WU Q,et al.Effects of inoculation with Acinetobacter on fermentation of cigar tobacco leaves[J].Front Microbiol,2022,13:911791.
[26] 田丽君,荊永锋,郑卜凡,等.浏阳洞库陈化烟叶微生物多样性分析[J].中国烟草学报,2022,28(1):98-107.
[27] 高娅北,李成刚,陈二龙,等.烤烟烟叶类黄酮合成关键酶活性及其调控基因的表达分析[J].中国烟草学报,2019,25(1):86-92.
[28] 贾云,胡婉蓉,吕晋雄,等.雪茄烟叶发酵过程中微生物群落及功能微生物分析[J].轻工学报,2023,38(1):71-78,89.
[29] WANG S L,WU Q,NIE Y,et al.Construction of synthetic microbiota for reproducible flavor compound metabolism in Chinese light-aromatype liquor produced by solid-state fermentation[J]. Appl Environ Microbiol,2019,85(10):e03090-18.
[30] WIDDER S,ALLEN R J,PFEIFFER T,et al.Challenges in microbial ecology: Building predictive understanding of community function and dynamics[J].ISME J,2016,10(11):2557-2568.