新疆吐鲁番是我国重要的葡萄与葡萄酒产区之一,其独特的干旱气候与昼夜温差为葡萄栽培提供了优越的生态条件,同时孕育了多样的本土微生物资源。酵母菌作为果酒发酵的核心微生物,其代谢活动直接影响着发酵产品的品质与风味特征。其中,酯类化合物会赋予果酒更丰富的香气特征,是影响果酒风味品质的关键物质。酵母菌通过代谢调控酯类物质的合成与积累,进而影响产品的香气复杂度、口感及整体品质[1-2]。因此,产酯酵母在果酒发酵中对于塑造产品的独特风味至关重要。
目前,果酒发酵常用的商业酿酒酵母(Saccharomyces cerevisiae)(如EC-1118、安琪系列、QA23等)具有稳定的发酵性能[3],但其同质化的代谢特征导致所酿葡萄酒缺乏地域特征和口味多样化。野生酵母在长期生态适应过程形成了与当地生态环境相匹配的代谢特征,不仅能够分泌多种水解酶(如β-葡萄糖苷酶、蛋白酶、脂肪酶等)[4-6],还能在发酵过程中合成丰富的酯类化合物(如乙酸乙酯、丁酸乙酯等),赋予产品独特的水果香、花香等怡人香气[7-8]。因此,为改善葡萄酒品质,商业酵母往往与野生酵母搭配进行发酵。目前,非酿酒酵母与S.cerevisiae混合发酵已被多项研究证实可显著增强风味的多样性与复杂性。如在Petit Manseng白葡萄酒体系中,戴尔有孢圆酵母(Torulaspora delbrueckii)与S.cerevisiae顺序发酵,显著提升了多种乙醇类物质,整体香气复杂度增强[9]。在新疆以过熟的赤霞珠葡萄为原料,S.cerevisia和毕赤酵母(Pichia)混合发酵的赤霞珠葡萄酒中检出17种气味活性值(odor activity value,OAV)≥1的关键香气化合物,呈现果香、花香等特征[10]。
目前,已有研究对吐鲁番地区的酵母资源进行了初步调查,该地区独特的生境可能蕴藏着具有特殊代谢特性的酵母菌株。吐鲁番葡萄沟位于吐鲁番火焰山西侧,栽培葡萄历史超2000年,为酵母资源提供理想场所。但针对吐鲁番葡萄沟这一特殊生态区域中酵母的多样性及其性能的研究较为有限,酵母资源尚未得到充分挖掘,以及对高糖、高乙醇等条件的耐受性能尚不明确。因此,本研究从该地区分离、筛选优良产酯酵母,并评价其安全性、产酶特性及生长耐受性能,为挖掘本土特色微生物资源提供理论依据,并为今后进一步开展发酵实验、筛选适用于特色发酵食品的优良酵母菌种奠定初步的实验基础。
1 材料与方法
1.1 材料与试剂
1.1.1 材料及菌株
土壤样品:采自新疆吐鲁番葡萄沟(共8个采集点,每点3个平行),将葡萄架下表面土壤去除,挖取葡萄架下土壤(0~20 cm),去除大颗粒杂质,置于无菌采样袋,于4 ℃冷藏保存。
大肠杆菌(Escherichia coli)和金黄色葡萄球菌(Staphylococcus aureus):均由新疆微生物资源保藏管理中心(MicrobiologicalCultureCollectionCenterofXinjiang,MCCCX)提供;商业酵母(XPURE):购自法国LAFFORT公司。
1.1.2 试剂
焦亚硫酸钾、七叶苷、三丁酸甘油酯、对氨基苯磺酸-α-萘胺试液、2,3,5-氯化三苯基四氮唑(2,3,5-triphenyl tetrazolium chloride,TTC)(均为分析纯):山东科源生化有限公司;葡萄糖、酵母浸出粉(均为分析纯):天津市大茂化学试剂厂;溴甲酚紫(指示剂):上海青析化工科技有限公司;MgSO4、KH2PO4、刚果红、对二甲基苯甲醛(均为分析纯):天津市致远化学试剂有限公司;真菌基因组DNA提取试剂盒、引物、2×Es Taq MasterMix:生工生物工程(上海)股份有限公司。
1.1.3 培养基
马铃薯葡萄糖琼脂(potato dextrose agar,PDA)(含氯霉素)培养基、酵母浸出粉胨葡萄糖琼脂(yeast peptone dextrose agar,YPD)培养基、YPD液体培养基、亚硫酸铋葡萄糖甘氨酸酵母琼脂(Bismuth Sulfite Glucose Glycine Yeast Agar,BIGGY)培养基、哥伦比亚血琼脂培养基:青岛高科技工业园海博生物技术有限公司。
产酯筛选培养基[11]:蛋白胨10 g,三丁酸甘油脂7.5 mL,酵母浸出粉5 g,葡萄糖10 g,琼脂20 g,溴甲酚紫0.02 g,蒸馏水1 L。
TTC上层培养基[12]:TTC 0.5 g,葡萄糖5 g,琼脂15 g,蒸馏水1 L;TTC下层培养基[12]:MgSO4 0.4 g,KH2PO4 1.0 g,酵母浸出粉1.5 g,蛋白胨2 g,葡萄糖10 g,琼脂20 g,蒸馏水1 L;调节pH值为5.5。
胰蛋白胨大豆肉汤(tryptone soy broth,TSB)培养基[13]:胰蛋白胨17.0 g,大豆蛋白胨3.0 g,葡萄糖2.5 g,氯化钠5.0 g,磷酸氢二钾2.5 g,蒸馏水加至1 L,调pH值至pH 7.2±0.2。
硝基还原酶检测培养基[14]:蛋白胨10 g,氯化钠10 g,硝酸钾5 g,蒸馏水1 L。
淀粉酶筛选培养基:YPD琼脂培养基中加入10 g/L的可溶性淀粉(加热溶解后加入培养基中)。
脂肪酶筛选培养基:三丁酸甘油酯10 g,酵母膏10 g,蛋白胨5 g,葡萄糖20 g,琼脂20 g,蒸馏水1 L。
蛋白酶筛选培养基:YPD琼脂培养基与10 g/L的脱脂乳粉,分开灭菌,待脱脂乳温度降至50 ℃时与YPD混匀后倒板。
果胶酶筛选培养基:果胶8 g,NH4Cl 1.4 g,KH2PO42.0 g,K2HPO4 6 g,MgSO4 0.1 g,蛋白胨5 g,琼脂18 g,蒸馏水1 L,调pH值至7.0左右。
七叶苷培养基[15]:蛋白胨10 g,酵母粉3 g,氯化钠3 g,七叶苷1 g,柠檬酸铁0.5 g,琼脂粉20 g,蒸馏水1 L。
1.2 仪器与设备
SPX-250BF生化培养箱:上海福玛实验设备有限公司;Biotek Epoch-2酶标仪:美国伯腾仪器有限公司;BSD-250振荡培养箱:上海博讯实业有限公司医疗设备厂;DYY-6C电泳仪:北京六一生物科技有限公司;ABI2720聚合酶链式反应(polymerase chain reaction,PCR)仪:赛默飞世尔科技(中国)有限公司;GelDocG0凝胶成像系统:上海孚约生物科技有限公司。
1.3 方法
1.3.1 酵母菌的分离纯化
8个采样点中,每个采样点取5 g土壤,与45 mL无菌水混合,振荡30 min充分混匀后进行梯度稀释,分别取10-2、10-3、10-4稀释液各100 μL在PDA平板上涂布,28 ℃培养4 d。在PDA平板中挑取部分形态、大小、颜色各异的单菌落在YPD平板中划线2~3次,采用斜面保藏法及甘油保菌法进行保藏。
1.3.2 菌株的形态学观察及分子鉴定
将纯化后的酵母菌株在YPD平板上进行划线,28 ℃培养3~5 d。待YPD平板上长出单菌落后用体视显微镜观察菌落形态并拍照。
利用试剂盒提取菌株DNA,采用标准引物NL1(5'-GCATATCAATAAGCGGAGGAAAG-3')和NL4(5'-GGTCCGTTTCAAGACGG-3')进行PCR扩增反应。PCR扩增体系:酵母菌DNA样品1 μL,正向反向引物各1 μL,SuperMix 25 μL,双蒸水补至50 μL。PCR扩增条件:95 ℃预变性5 min,94 ℃变性30 s,54 ℃退火30 s,72 ℃延伸10 s,循环30次;72 ℃延伸10 min。扩增结束后进行琼脂糖凝胶电泳,选取有明显条带的产物,送往北京诺禾致源生物信息科技有限公司进行测序。
将所测得的序列经拼接和去引物后,在美国国家生物技术信息中心(National Center for BiotechnologyInformation,NCBI)的Genbank数据库中进行基本局部比对搜索工具(basic local alignment search tool,BLAST)比对,选取序列相似度≥99%的模式菌株的26S rRNA基因序列,采用MEGA 11软件中的邻接法(neighbor-joining,NJ)构建系统发育树。
1.3.3 酵母菌发酵性能初筛
将酵母菌株分别接种至BIGGY培养基,28 ℃培养4 d后,观察菌落颜色,判断是否产H2S。酵母菌株产H2S能力不同颜色不同,颜色越深表示产H2S能力越强,以商业酵母为对照。
将酵母菌株分别接种至产酯筛选培养基,28 ℃培养4 d,观察培养基中菌落颜色变化进行判断,颜色越深表示所产酯类物质能力越强。
将TTC下层琼脂培养基在121 ℃条件下灭菌20 min,待培养基冷却到50 ℃左右时,倒入培养皿中,等待培养基冷却凝固,接种酵母菌,28 ℃培养4 d后,再在菌落上覆盖一层TTC上层琼脂培养基,避光培养2 d,观察记录菌株的颜色。酵母会与TTC琼脂培养基发生颜色反应,颜色越深表示产乙醇的能力越强。
1.3.4 酵母菌安全性评价
吲哚试验:将酵母菌株分别接种于胰蛋白胨大豆肉汤培养基,28 ℃、150 r/min振荡培养72 h,加入吲哚试剂8~10滴观察颜色变化。若液面出现玫瑰红色则为阳性结果,否则为阴性结果,以商业酵母XPURE为阳性对照菌株,未接种细菌的胰蛋白胨大豆肉汤培养基为空白对照。
硝基还原酶产生能力测定:参照包怡红等[14]的方法,将菌液以3%的接种量接种至硝基还原酶检测培养基,28 ℃、150 r/min振荡培养72 h,取适量培养液滴入几滴对氨基苯磺酸-α-萘胺试液,混合均匀,静置后观察培养液颜色,以E.coli作为阳性对照组。
挑取菌株单菌落在哥伦比亚血琼脂平板上划线,28 ℃培养48 h,若出现草绿色溶血环,即为α-溶血;若出现无色透明的溶血环,即为β-溶血;若无溶血环,即为γ-溶血。以S.aureus为阳性参照菌株。
1.3.5 酵母菌株产酶特性
将酵母菌株活化后挑取单菌落至YPD液体培养基中,28 ℃、150 r/min培养16~24 h,获得种子液。将吸取50 μL种子液于相应功能酶筛选培养基上,28 ℃培养3~5 d。其中淀粉酶需要用0.1%的碘液对平板进行染色后再观察菌株周围透明圈情况,果胶酶需要用0.1%刚果红对平板进行染色后再观察透明圈情况,其余菌株功能酶筛选可直接通过观察菌落周围是否形成透明圈进行初步判断。
1.3.6 酵母菌耐受性评价
酵母菌SO2耐受试验:将对数生长期的菌株分别以1.0×106 CFU/mL分别接种于含有50 mg/L、150 mg/L、250 mg/L SO2(以H2SO3形式添加)的YPD液体培养基,在28℃、150r/min条件下培养24 h,酶标仪测定OD600nm值。
酵母菌pH耐受试验:将对数生长期的菌株分别以1.0×106CFU/mL分别接种于pH为1.0、3.0、5.0的YPD液体培养基,在28 ℃、150 r/min条件下培养24 h,酶标仪测定OD600nm值。
酵母菌乙醇耐受试验:将对数生长期的菌株分别以1.0×106 CFU/mL分别接种于含有体积分数为6%、12%、18%乙醇的YPD液体培养基,在28 ℃、150 r/min条件下培养24 h,酶标仪测定OD600nm值。
酵母菌葡萄糖耐受试验:将对数生长期的菌株分别以1.0×106 CFU/mL分别接种于含有50 g/L、250 g/L、450 g/L葡萄糖的YPD液体培养基,在28 ℃、150 r/min条件下培养24 h,酶标仪测定OD600nm值。
2 结果与分析
2.1 菌株的形态学特征及分子鉴定
采用梯度稀释法对吐鲁番葡萄沟土壤中的酵母菌进行分离筛选,初步在PDA平板上共挑取大小形态各异的235株酵母菌,部分菌株形态见图1。由图1可知,菌落大小从细小点状至中等菌落不等,颜色多呈乳白至米白色,少数为浅灰白或橙至砖红色,多数菌落表面光滑湿润、有光泽,形态以圆形或椭圆形为主。
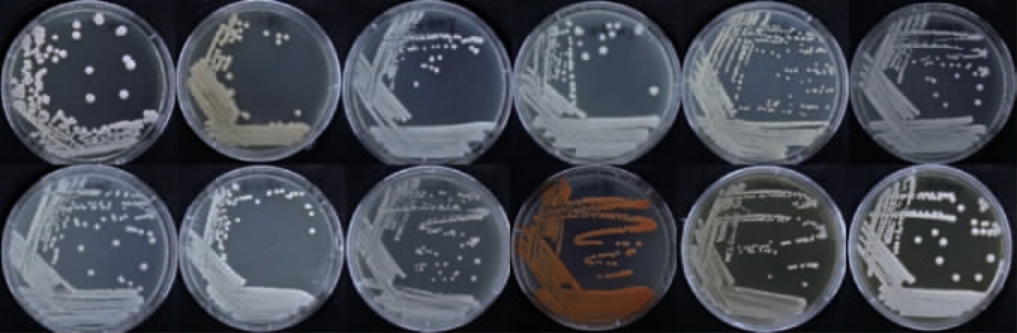
图1 部分酵母在YPD培养基中的菌落形态
Fig.1 Colony morphology of some yeasts in YPD medium
将获得菌株的26S rDNA基因序列在NCBI网站进行序列比对,基于26S rDNA基因序列构建部分代表菌株的系统发育树,结果见图2。由图2可知,在葡萄沟土壤中分离的235株酵母,共涉及15个属。除Saccharomyces外,其余菌株均为非酿酒酵母。有孢圆酵母属(Torulaspora)、长西氏酵母属(Naganishia)、迈耶氏酵母属(Meyerozyma)和假丝酵母属(Candida)4个菌属占比分别是30.2%、21.7%、10.2%、10.2%,为该地区的优势菌群。且获得3株潜在新种TF8-3(98.74%)、TW1-01(96.47%)、TP6-1(98.65%),分别为Suhomyces、Torulaspora和Solicoccozyma属。
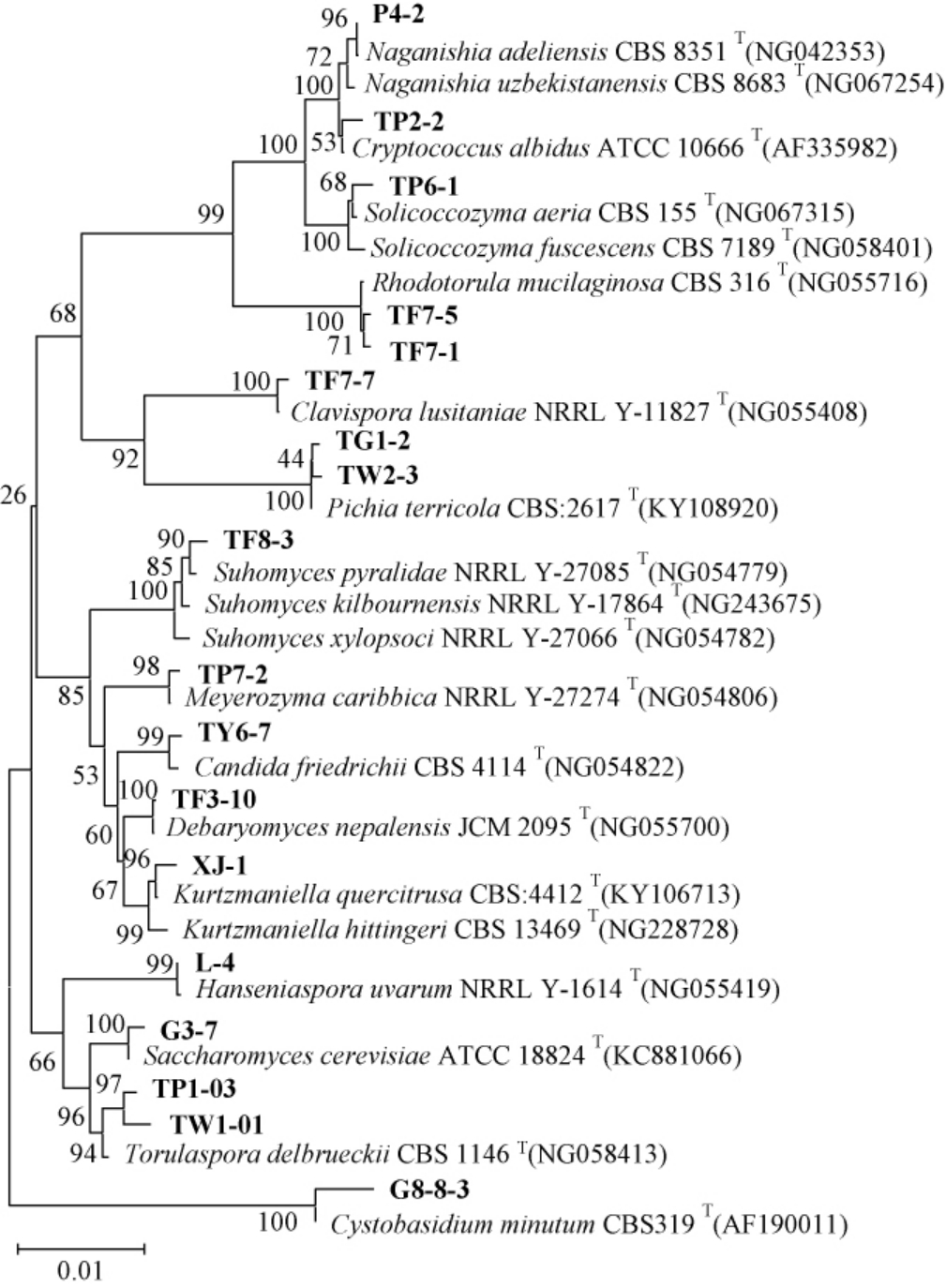
图2 基于26S rDNA D1/D2区基因序列酵母属水平系统发育树
Fig.2 Phylogenetic tree of yeasts at the genus level based on 26S rDNA D1/D2 domain gene sequences
2.2 酵母菌发酵性能初筛结果
出于异味风险、香气能力与发酵力评估的综合考虑,将菌株产H2S能力、产酯能力与产乙醇能力设为发酵性能初筛指标,共选取59株代表性非酿酒酵母菌株进行实验,结果见图3。
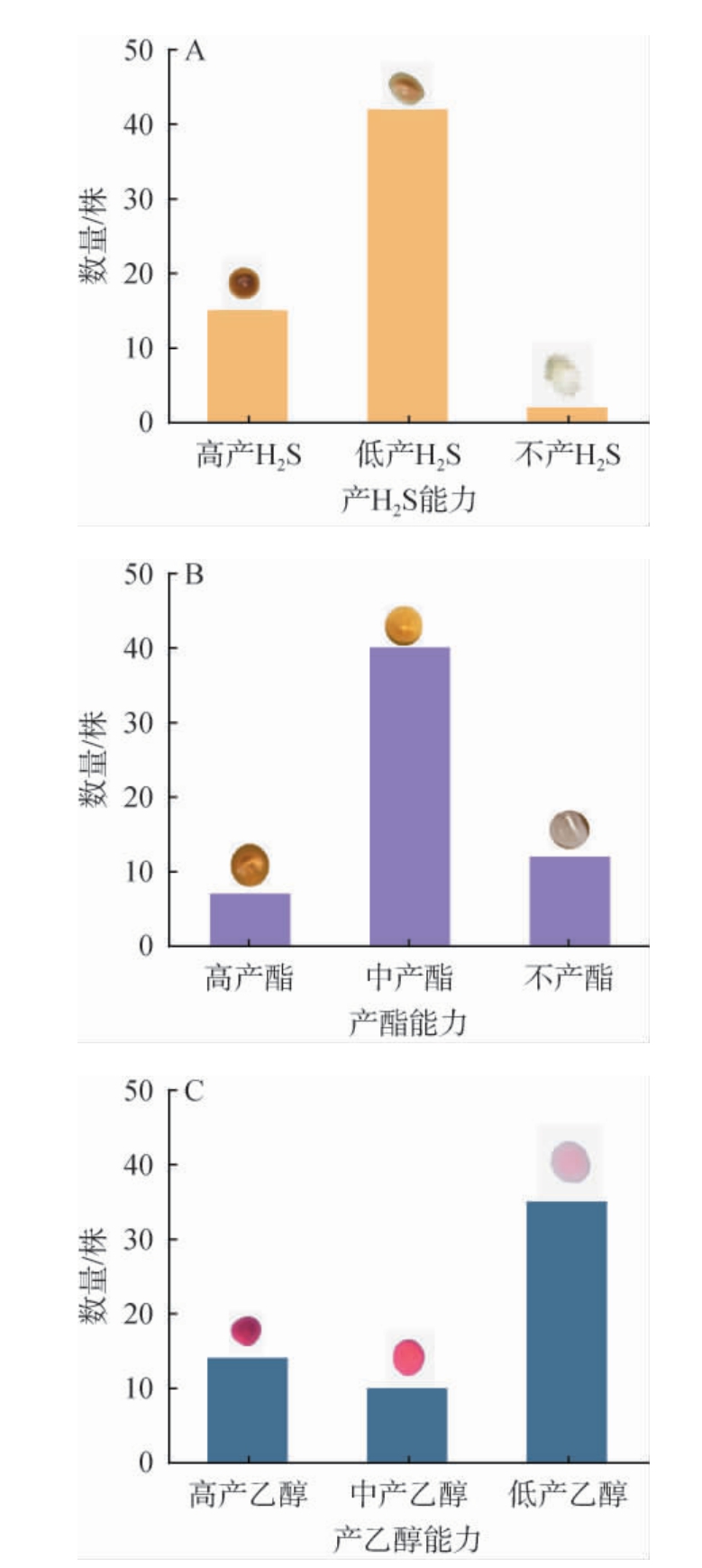
图3 酵母菌产H2S(A)、产酯(B)及产乙醇(C)能力分析
Fig.3 Analysis of H2S production (A),ester production (B) and ethanol production (C) ability of yeast strains
在酵母生长代谢过程中会产生具有臭鸡蛋、大蒜等味道的H2S[16],以商业酵母为对照(呈深棕色),评估酵母菌株的产H2S能力。由图3A可知,15株酵母菌落呈黑色或棕色,表现为高产H2S;42株酵母菌落呈浅咖啡色,低产H2S;2株酵母菌落呈白色,不产H2S。表明多数菌株具备不同水平的H2S生成能力。
优良的酵母菌株应具备产香的能力,因此需要对菌株进行产酯能力测定。由图3B可知,7株酵母菌落呈土黄色,具有高产酯能力;40株酵母菌落呈黄色,具有中产酯能力;12株酵母菌落呈白色,不具有产酯能力。
由图3C可知,14株酵母菌落呈红紫色,可判定为产乙醇能力较强;10株酵母菌落呈红色,可判定为产乙醇能力中等;35株酵母菌落呈浅粉色,可判定为产乙醇能力较低。
综合高产乙醇、低产H2S、高产酯能力,最终筛选TF7-1、TF7-5、TG1-2等8株酵母菌进入后续试验。
2.3 酵母菌安全性评价结果
为确保食品发酵应用安全,对8株酵母菌开展安全性评价,结果见表1。由表1可知,8株酵母菌在吲哚试验、硝基还原酶试验和溶血性试验中的结果均为阴性。说明这些酵母菌未表现出与潜在致病性相关的关键特征,具有一定的安全性。
表1 酵母菌初筛结果及安全性评价
Table 1 Preliminary screening results and safety assessment of yeast strains

注:“+++”表示能力较强;“++”表示能力一般;“+”表示能力较弱;“-”表示无变化。
2.4 酵母菌产功能酶特性
为评估候选产酯酵母在风味与工艺上的潜力,对其功能酶进行初筛。选取与果酒密切相关的5类酶(蛋白酶、果胶酶、β-葡萄糖苷酶、脂肪酶、淀粉酶),将8株酵母菌分别点接至对应指示平板,以透明圈形成判定阳性,8株酵母菌的产功能酶活性结果见表2。
表2 酵母菌产功能酶活性分析
Table 2 Analysis of functional enzyme activity produced by yeast

注:“+”表示有透明圈;“-”表示无透明圈。
由表2可知,具有蛋白酶活性的酵母菌2株,具有淀粉酶活性的酵母菌6株,具有脂肪酶活性的酵母菌3株,具有果胶酶活性和β-葡萄糖苷酶活性的酵母菌分别有5株。其中,菌株TF7-1、TF7-5、TF8-3、TW1-01及TW2-3均具备3种酶活性。菌株TF7-1和TF7-5在蛋白酶和脂肪酶活性方面表现突出,表明其可在酱油等发酵食品中进行应用。菌株TF8-3具有3种水解酶活性,表明其在果蔬加工等方面可能发挥多功能作用。菌株TW1-01和TW2-3在淀粉酶、果胶酶、β-葡萄糖苷酶活性方面表现突出,具有增强原料降解及提升其风味等能力的应用前景,适合应用于果酒酿造。
2.5 酵母菌耐受性评价结果
SO2在果酒酿造过程中具有抑制杂菌的作用,但浓度过高可能会抑制酵母生长。为评估酵母菌株的SO2耐受性,测定8株酵母菌在不同SO2质量浓度下的生长情况(OD600nm值),结果见图4A。由图4A可知,酵母菌株的生长随SO2质量浓度增加而降低,但除菌株TF7-5生长显著受到抑制外,大部分菌株无明显差异。
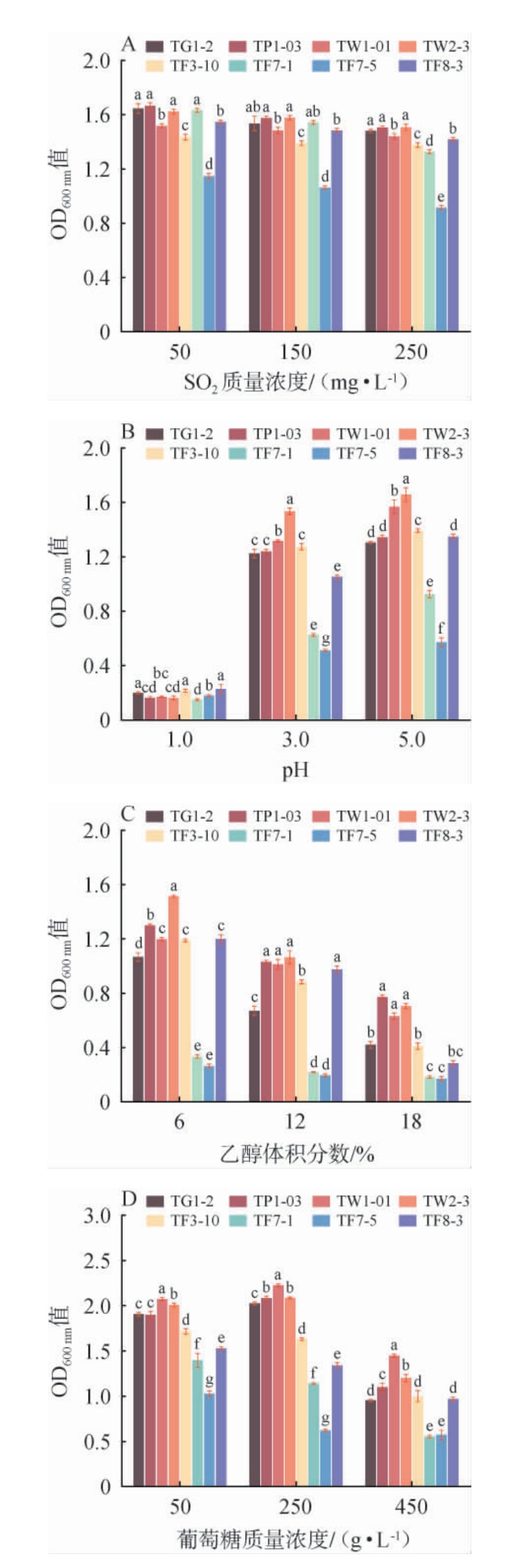
图4 酵母菌对SO2(A)、pH(B)、乙醇(C)及糖含量(D)耐受性评价
Fig.4 Evaluation of the tolerance of yeast to SO2(A),pH (B),ethanol (C) and sugar content (D)
相同条件下不同菌株间小写字母不同代表差异显著(P<0.05)。
果酒发酵过程中,有机酸形成的酸性环境可能影响酵母活性。酵母菌株pH耐受性结果见图4B。由图4B可知,当pH值为3.0和5.0时,大部分菌株生长旺盛,但少部分菌株生长情况较弱。当pH值达到1.0时,菌株生长受到明显抑制,菌株生长微弱(OD600nm值<0.5),菌株TW2-3和TW1-01在pH值3.0和5.0条件下表现出最佳生长能力,表明其对葡萄酒发酵的酸性环境具有较强适应性。
在发酵过程中,乙醇的持续积累会抑制酵母生长[17]。酵母菌株乙醇耐受性结果见图4C。由图4C可知,随着乙醇体积分数的升高,酵母生长速率逐渐降低,但不同菌株的乙醇耐受性存在显著差异。当乙醇体积分数达到18%时,部分菌株仍能维持生长,表现出较强的乙醇耐受能力。其中,菌株TW2-3、TP1-03和TW1-01的耐受性最优,其在高乙醇体积分数(18%)条件下的生长表现显著优于其他菌株。
为探究高糖条件对酵母生长的影响,测定了8株酵母菌株在不同葡萄糖质量浓度下的生长情况(OD600nm值),以分析其葡萄糖耐受性。由图4D可知,当葡萄糖质量浓度从50 g/L增至250 g/L时,OD600nm值显著上升,表明葡萄糖作为碳源促进了细胞生长;但当葡萄糖质量浓度从250 g/L增至450 g/L时,OD600nm值下降,说明过高浓度会抑制酵母生长。在葡萄糖质量浓度250 g/L条件下,酵母生长达到最佳状态。不同菌株的糖耐受性存在差异,其中菌株TW1-01和TW2-3表现最优。
3 讨论
研究发现,新疆葡萄酒重要产区之一的吐鲁番地区蕴藏着丰富多样的酵母资源。其中,Hanseniaspora、Saccharomyces、Naganishia、Candida 4个属在吐鲁番地区广泛分布。杨莹[18]在鄯善县楼兰酒厂发酵汁中分离酵母菌218株,共涉及Hanseniaspora、Saccharomyces、Pichia等5个种属,其优势菌属是Hanseniaspora和Saccharomyces。徐建坤[19]在吐鲁番、鄯善酒庄分离到92株酵母,共涉及Naganishia、Saccharomyces、Hanseniaspora、Candida等9个属,其优势菌属是Naganishia、Saccharomyces、Candida,分别占比17.4%、13%和10.9%。蔡燕丽等[20]在吐鲁番地区葡萄园土壤中共分离13株酵母,共涉及棒孢酵母属(Clavispora)、Candida、隐球酵母属(Cryptococcus)等6个属,其优势菌属是Clavispora,占46.2%。
酵母在代谢过程中合成酯类化合物,如乙酰辅酶A与醇类的酯化反应生成芳香性化合物,赋予产品果香或花香等风味[21]。因此,酵母产酯能力在食品发酵、酿酒、调味品[22]等领域具有应用价值,受到广泛关注。曹恺欣[23]在新疆、西藏等地区特色乳制品中共分离出产香酵母77株,其中NGD43(Torulaspora delbrueckii)产酶能力最强,能大量生成香气物质,如正戊醇、癸酸乙酯等,赋予酒体更多风味。梁斯梅[11] 在白酒样品中分离高产酯酵母菌Y4(Kluyveromyces marxianus),发现其对总酯、乙酸乙酯等风味物质有显著作用,使酒体米香味突出,品质得到提升。WANG X D等[24]用Rhodotorula mucilaginosa和酿酒酵母进行混合发酵果酒,发现果酒中含26种酯类化合物,明显提高了酒体的口感,增强果酒的香味。
在果酒发酵中,优良的产酯酵母不仅具有产酯能力,还应具有较好的发酵性能及较强的耐受性,如耐高糖、耐乙醇、耐低pH等[25],在发酵中协同酿酒酵母起着提高发酵效率、提升产量等作用。周迪等[26]在宁夏贺兰山产区筛选的本土野生酵母(Hanseniaspora、Metschnikowia、Starmerella)均可耐受(葡萄糖450 g/L,pH 1.0,SO2 250 mg/L,乙醇体积分数13%),不仅有优良的发酵性能,还产生了独特的香味物质,可用于酿造产区特色果酒。刘晓柱等[27]从库尔勒香梨中分离的一株非酿酒酵母K6(Metschnikowia),通过耐受性分析发现菌株对乙醇浓度敏感,耐受于体积分数为9%的乙醇,在低酒精果酒生产上具有应用潜力。
4 结论
本实验从吐鲁番葡萄沟分离出235株酵母菌,含15个属,优势菌群为有孢圆酵母属(Torulaspora)、长西氏酵母属(Naganishia)、迈耶氏酵母属(Meyerozyma)和假丝酵母属(Candida),分别占比是30.2%、21.7%、10.2%、10.2%,其中发现3株潜在新种(TF8-3、TW1-01、TP6-1),分别属于Suhomyces、有孢圆酵母属(Torulaspora)和Solicoccozyma。通过产H2S、产酯和产乙醇性能筛选及安全性评估,获得8株无致病性的优良产酯酵母。耐受性试验表明,戴尔有孢圆酵母(Torulaspora delbrueckii)TW1-01和特立科拉毕赤酵母(Pichia terricola)TW2-03在250 g/LSO2、450 g/L葡萄糖、18%乙醇及pH3.0条件下均生长良好,具备用于吐鲁番特色葡萄酒开发的潜力。后续将优化发酵工艺并研究其与商业酵母混合发酵效果。
[1] 袁海珊,刘功良,白卫东,等.产酯酵母在发酵食品中的应用研究进展[J].中国酿造,2023,42(1):15-20.
[2] MARCO M L,SANDERS M E,GÄNZLE M,et al.The international scientific association for probiotics and prebiotics consensus statement on fermented foods[J].Nat Rev Gastroenterol Hepatol,2021,18(3):196-208.
[3] 王琨,张军翔,张毅,等.不同商用酵母对葡萄酒外观品质影响机理研究[J].中外葡萄与葡萄酒,2008(6):32-34.
[4] BORREN E,TIAN B.The important contribution of non-Saccharomyces yeasts to the aroma complexity of wine:A review[J].Foods,2021,10(1):13.
[5] 徐晓裕,吴慧敏,王鑫炜,等.蟠桃表皮产酶非酿酒酵母的分离鉴定及发酵特性研究[J].中国食品添加剂,2023,34(6):48-57.
[6] SUN W,CHEN X,BI P,et al.Screening and characterization of indigenous non-Saccharomyces cerevisiae with high enzyme activity for kiwifruit wine production[J].Food Chem,2024,440:138309.
[7] 刘薇,栾春光,王德良,等.高产酯酵母的筛选、鉴定及其发酵特性研究[J].食品与发酵工业,2021,47(23):311-318.
[8] ŠURANSKÁ H,VRÁNOVÁ D,OMELKOVÁ J.Isolation,identification and characterization of regional indigenous Saccharomyces cerevisiae strains[J].Braz J Microbiol,2016,47(1):181-190.
[9] ZHANG B,TANG C,YANG D,et al.Effects of three indigenous non-Saccharomyces yeasts and their pairwise combinations in cofermentation with Saccharomyces cerevisiae on volatile compounds of Petit Manseng wines[J].Food Chem,2022,368:130807.
[10] ZHU L X,WANG G Q,AIHAITI A.Combined indigenous yeast strains produced local wine from over ripen Cabernet Sauvignon grape in Xinjiang[J].World J Microb Biot,2020,36(8):122.
[11] 梁斯梅,万瑞杰,张龙,等.米香型白酒产酯酵母的分离筛选及推广应用[J].酿酒科技,2025(4):27-32.
[12] 岑涛,岳田利,袁亚宏,等.云南芒果中酵母菌分离鉴定及在芒果酒发酵中的应用[J].食品科学,2015,36(11):119-124.
[13] 孟丹,王丽群,谢国梁,等.一株乳酸乳球菌产γ-氨基丁酸能力及其安全性评价[J].中国酿造,2017,36(4):72-77.
[14] 包怡红,高博,蒋士龙,等.富集钙乳酸菌的筛选、鉴定及安全性评价[J].中国酿造,2023,42(3):115-121.
[15] 孔晓双,黄新新,董应宏,等.一株产β-葡萄糖苷酶甘草内生菌的筛选、全基因组分析及产酶优化[J].微生物学通报,2024,51(1):279-294.
[16] FRANCO-LUESMA E,SAENZ-NAVAJAS M P,VALENTIN D,et al.Study of the effect of H2S,MeSH and DMS on the sensory profile of wine model solutions by Rate-All-That-Apply(RATA)[J].Food Res Int,2016,87:152-160.
[17] QIU Z,JIANG R.Improving Saccharomyces cerevisiae ethanol production and tolerance via RNA polymerase II subunit Rpb7[J].Biotechnol Biofuels,2017,10:125.
[18] 杨莹.新疆地区葡萄酒相关酵母菌的生物多样性研究[D].杨凌:西北农林科技大学,2007.
[19] 徐建坤.产β-葡萄糖苷酶酵母菌的分离鉴定及特性研究[D].石河子:石河子大学,2019.
[20] 蔡燕丽,刘欢,王翀,等.新疆酿酒葡萄园可培养酵母菌多样性分析[J].江苏农业科学,2019,47(2):282-287.
[21] RUIZ-DE-VILLA C,GOMBAU J,POBLET M,et al.Sequential inoculation of Torulaspora delbrueckii and Saccharomyces cerevisiae in rosé wines enhances malolactic fermentation and potentially improves colour stability[J].LWT-Food Sci Technol,2023,190:115540.
[22] 蔡伟琪,钟武杰,周嘉健,等.天然酱醪中产β-苯乙醇酵母菌的分离鉴定、发酵条件优化及其应用[J].食品工业科技,2023,44(17):149-157.
[23] 曹恺欣.产香酵母的分离筛选及其对发酵啤酒香气特性影响的研究[D].沈阳:沈阳农业大学,2022.
[24] WANG X D,CHEN J W,GE X X,et al.Sequential fermentation with indigenous non-Saccharomyces yeasts and Saccharomyces cerevisiae for flavor and quality enhancement of Longyan dry white wine[J].Food Biosci,2023,55:102952.
[25] 闫兴敏,姜娇,高辉,等.优良本土酿酒酵母的酿酒特性及产香能力初析[J].食品与发酵工业,2022,48(4):62-68.
[26] 周迪,卢玲,王岚.贺兰山东麓产区非酿酒酵母筛选及发酵特性研究[J].食品与发酵工业,2025,51(1):72-80.
[27] 刘晓柱,黄元敏,杨筱萱,等.一株库尔勒香梨源非酿酒酵母菌的鉴定及其发酵性能分析[J].中国酿造,2023,42(6):128-134.