浓香型白酒作为中国古老文明的重要传承载体之一,市场占有率稳定在60%以上,具有巨大的市场经济价值[1]。受豫酒振兴政策的影响,白酒的品质要求和科技创新水平不断受到新的挑战。酯类物质尤其是己酸乙酯作为浓香型白酒中重要的香味物质,GB/T 10781.1—2021《白酒质量要求第1部分:浓香型白酒》[2]规定高酒精度优级浓香型白酒总酯含量≥2.00 g/L,且不能通过添加酯类物质等食品添加剂来提高[3]。在当今的白酒酿造行业中,经常会出现酒体总酯含量不达标,以至于酿造出来的白酒品质较差。强化大曲技术是将从浓香型酒曲及窖泥中筛选出产酯酵母,按一定比例重新加入酿造体系中,在提高酒体含酯量的同时还能减少用曲量、增加出酒率[4]。浓香型白酒曲是多年驯化的结果,其中含有丰富的产酯微生物,故从浓香型白酒曲中筛选产酯能力强的酵母菌一直是白酒生产中的重要研究方向。产酯酵母是一类能够产生酯类物质的酵母菌统称,包括汉逊酵母属(Hansenula)、假丝酵母属(Candida)、球拟酵母属(Torulopsis)、酒香酵母属(Brettanomyces)、酿酒酵母属(Saccharomyces)等[5]。其产生的酯类物质因菌种、培养条件和生产工艺的不同而不同,可产生果香、花香、清香、焦糊味和酱香等[6-8]。王鹏昊等[9]从酿酒小曲中分离获得优质产酯菌株Y5,采用正交试验对其产酯条件进行优化,优化后其菌株Y5总酯产量从2.684 g/L提高至4.065 g/L。刘薇[10]以在不同酒厂、醋厂收集的酒醅、醋醅为分离源,筛选出2株高产乙酸乙酯的酵母菌株Y10和Y12,并通过单因素和响应面试验优化菌株Y10和Y12产酶条件,优化后菌株Y10和Y12乙酸乙酯产量分别为13.15 g/L和12.96 g/L,比优化前提高了49.29%和68.5%。刘朋肖等[11]以酿酒酵母Y3401为研究对象,通过单因素和响应面试验对其产己酸乙酯条件进行优化。结果表明,最优产己酸乙酯条件为:糖度14°Brix,初始pH 7,温度25 ℃,转速180 r/min,接种量3.5%,乙醇添加量8%,己酸添加量0.059%,前体添加时机30 h、诱导时间31 h。在此培养条件下己酸乙酯产量达10.1 mg/L。
本研究以新疆雪水坊白酒酒曲为原料,通过稀释涂布平板法分离产酯酵母,通过产气试验、嗅闻法及测定总酯含量进行初筛,利用α-萘酯比色法、气相色谱(gas chromatography,GC)法测定酯化酶活力和己酸乙酯含量进行复筛,并通过形态学观察、生理生化试验及分子生物学技术鉴定优良高产酯酵母。进一步结合单因素试验和响应面法优化其产酯条件。旨在筛选优良产酯酵母,并将其应用于葡萄酒酿造,以期丰富功能酵母的菌种资源,提高酒类产品的风味及品质,对推动葡萄酒产业发展具有重要意义。
1 材料与方法
1.1 材料与试剂
1.1.1 材料
酒曲:万博雪水坊酒业(新疆)有限责任公司;巨峰葡萄:河南信阳超市。
1.1.2 试剂
果胶酶(酶活3万U/g):山东隆科特酶制剂有限公司;酵母膏(生化试剂)、葡萄糖、α-萘酯、α-萘酚、酚酞、硫酸、盐酸、氢氧化钠、氯化钙、酒石酸钾钠、硫酸铜(均为分析纯):天津科密欧化学试剂有限公司;琼脂粉、蛋白胨(均为生化试剂):杭州百思生物技术有限公司;冰乙酸、偏重亚硫酸钾(均为分析纯):郑州派尼化学试剂厂;亚甲基蓝(分析纯):天津巴斯夫化工有限公司。
1.1.3 培养基
酵母膏胨葡萄糖琼脂(yeast peptone dextrose,YPD)培养基[12]:2%葡萄糖,2%蛋白胨,1%酵母膏,2%琼脂。121 ℃灭菌20 min。
含氯霉素马铃薯葡萄糖琼脂(potatodextroseagar,PDA)培养基[13]:氯霉素20 mg/L,200 g/L土豆浸提汁,葡萄糖20 g/L,琼脂20 g/L,蒸馏水1 000 mL。121 ℃灭菌20 min。
基础培养基:在100 mL蒸馏水中加入0.50 g的蛋白胨、0.50 mL的乙醇、0.10 mL的冰乙酸、0.04 g氯化钙、1 g葡萄糖,充分溶解。121 ℃灭菌20 min。
麦芽汁培养基[14]:将大麦芽粉碎,麦芽粉与水按照料液比为1∶4(g∶mL),38 ℃保温2 h,升温至45 ℃保持30 min,再升温至50 ℃保持30 min,再升温至60 ℃,糖化1.0~1.5 h,并用鸡蛋清煮沸澄清,稀释至适当浓度。121 ℃灭菌20 min。
葡萄汁培养基[15]:挑选新鲜完整、无病害的葡萄果实,破碎过滤后分装至100 mL三角瓶中。105 ℃灭菌10 min。
碳源氮源同化基础培养液、糖发酵酵母膏基础液、脲素液体培养基、醋酸钠培养基、产生类淀粉化合物培养液:参照任蓓蕾[16]的方法配制。
1.2 仪器与设备
LDZM-8OL-III型高压灭菌锅:上海申安医疗器械厂;SW-CJ-1D型生化培养箱、LDZM-8OL-III型pH计:上海尚道仪器制造有限公司;XMTD-7000型电热恒温水浴锅:北京永光明医疗仪器有限公司;GC9800型气相色谱(GC)仪:上海科创色谱仪器有限公司;Tprofessional Thermocycler型聚合酶链式反应(polymerase chain reaction,PCR)仪:德国BIOMETRA公司;752型紫外分光光度计:上海精密科学仪器有限公司;16017血球计数板:泰州市育才教学设备有限公司;TD10手持糖度仪:广州融测电子有限公司。
1.3 方法
1.3.1 产酯菌株的分离与纯化
参考王益姝等[17]的方法,对酒曲进行富集培养;参考杜艾明等[18]的方法进行稀释、划线分离及涂布平板培养后,斜面保藏于4 ℃备用。
1.3.2 产酯菌株的筛选
初筛:参照李海营[19]的方法,将斜面保藏菌株分别接种到麦芽汁培养基中,28 ℃恒温培养3 d,观察杜氏管充气情况,参照GB/T 10781.1—2021《白酒质量要求 第1部分:浓香型白酒》中嗅闻法和皂化中和滴定法测定发酵液总酯含量[2],初步筛选产酯菌株。
复筛:测定产酯菌株发酵液中酯化酶活力[20]及己酸乙酯含量,筛选优良产酯酵母。
1.3.3 优良产酯酵母鉴定
1.3.3.1 形态学观察
依据《酵母菌的特征与鉴定手册》[21]中的方法进行酵母菌形态学观察。
1.3.3.2 生理生化试验
糖发酵试验[16,21]:麦芽汁培养基中分别加入2.5%的葡萄糖、半乳糖、蔗糖、麦芽糖、乳糖和棉子糖。将菌落接种于装液量为10 mL/50 mL的YPD培养基中,28 ℃、150 r/min条件下振荡培养36 h,得到种子液。取250 μL种子液分别接种到上述糖发酵培养基中,28 ℃、180 r/min条件下振荡培养3 d,以不接种的培养基作对照,观察产气情况。同理进行碳源同化试验[22]、氮源同化试验及类淀粉产生试验和脲酶试验[23]。
1.3.3.3 分子生物学鉴定[24]
使用酵母基因组DNA提取试剂盒提取目的菌株的基因组DNA并采用通用引物NL1和NL2对26S rDNA的D1/D2区进行特异性扩增。PCR扩增体系(50 μL):DNA模板2 μL、正反引物(10 μmol/L)2 μL、PremixSTAR HS(Takara)25 μL,无菌双蒸水(ddH2O)补齐至50 μL。PCR扩增程序:98 ℃预变性3 min,98 ℃变性10 s,55 ℃退火15 s,72 ℃延伸60 s,35个循环,72 ℃延伸10 min。PCR扩增产物在1%琼脂糖凝胶上进行电泳分析,PCR产物委托生工生物工程(上海)股份有限公司进行测序。将测序结果在美国国家生物技术信息中心(National Center of Biotechnology Information,NCBI)的GeneBank核酸数据库进行基本局部比对搜索工具(basic local alignment search tool,BLAST)序列比对,分析相似性,利用MEGA7.0软件的邻接(neighbor-joining,NJ)法构建系统发育树。
1.3.4 菌株A2产酯条件优化单因素试验
在100 mL基础培养基中分别添加葡萄糖(0、1%、2%、3%、4%、5%),冰乙酸(0、0.05%、0.10%、0.15%、0.20%、0.25%),氯化钙(0、0.02%、0.04%、0.06%、0.08%、0.10%),蛋白胨(0、0.25%、0.50%、0.75%、1.00%、1.25%),乙醇(0、0.50%、1.00%、1.50%、2.00%、2.50%),发酵时间分别为(1.0 d、2.0 d、3.0 d、4.0 d、5.0 d、6.0 d),发酵温度28 ℃,比较不同葡萄糖、冰乙酸、蛋白胨、无水乙醇添加量及发酵时间对筛选酵母产酯能力的影响。
1.3.5 菌株A2产酯条件优化响应面试验
1.3.5.1 Plackett-Burman(PB)试验
以葡萄糖(X1)、蛋白胨(X2)、乙醇(X3)、冰乙酸(X4)、氯化钙(X5)添加量及发酵时间(X6)为自变量,以总酯产量(Y)为响应值,进行Plackett-Burman(PB)试验设计,优化菌株A2产酯条件,Plackett-Burman(PB)试验设计因素与水平见表1。
表1 产酯条件优化Plackett-Burman试验因素与水平
Table 1 Factors and levels of Plackett-Burman experiments for esterification conditions optimization
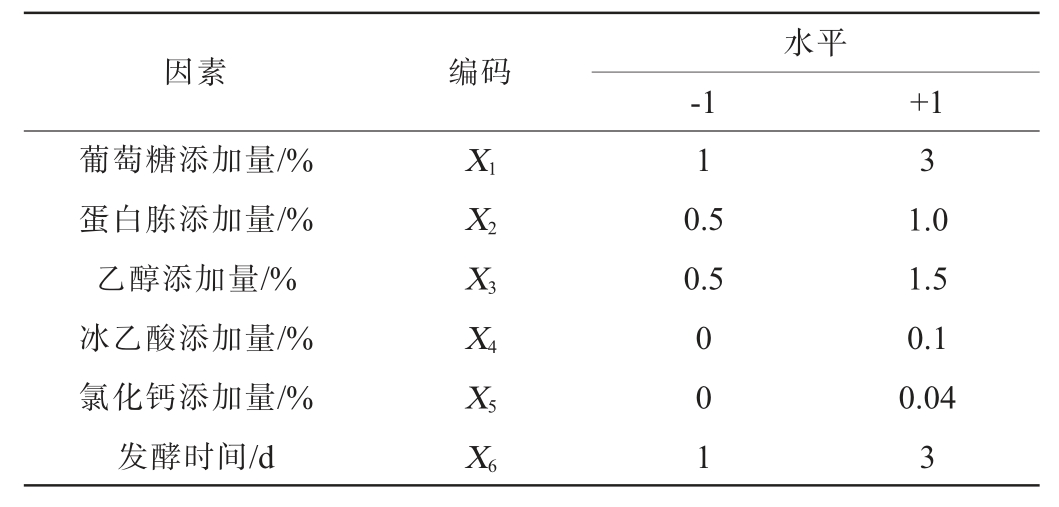
1.3.5.2 最陡爬坡试验
在Plackett-Burman(PB)试验基础上,以各显著因子为中心起点,确定最陡爬坡试验的步长,通过最陡爬坡试验进一步逼近最佳水平,从而确定Box-Behnken设计的中心点,根据各显著因素的效应正负和大小取值,正效应值应逐步增加,负效应值应逐渐减小。
1.3.5.3 Box-Behnken(BB)试验
以葡萄糖添加量(A)、发酵时间(B)及氯化钙添加量(C)为自变量,进行Box-Behnken(BB)试验。以总酯产量(Y)为响应值,优化菌株A2产酶条件,Box-Behnken(BB)试验因素与水平见表2。
表2 产酯条件优化Box-Behnken试验设计因素与水平
Table 2 Factors and levels of Box-Behnken experiments design for esterification conditions optimization
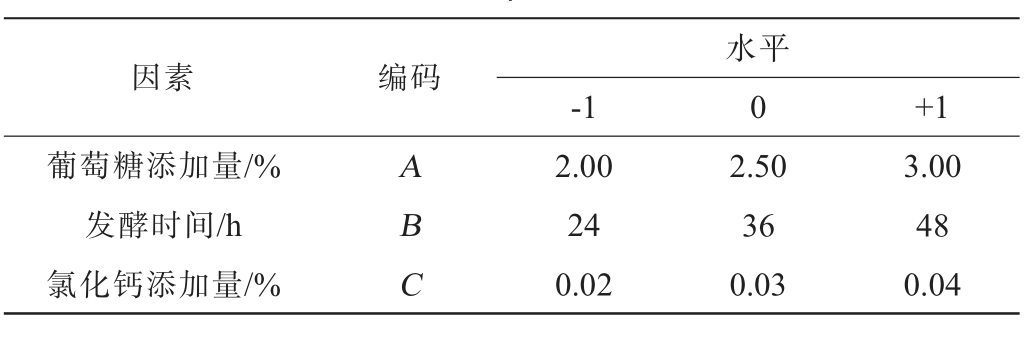
1.3.6 优良产酯酵母在葡萄酒酿造中的应用
种子液制备:YPD液体培养基活化酿酒酵母A2,安琪葡萄酒专用酿酒酵母的活化方式按照产品说明进行活化。活化后菌体种子液按1%接种量至装液量为10 mL/250 mL YPD液体培养基中,置于30 ℃条件下恒温培养24 h,采用血球计数法调整菌体细胞浓度分别为1.4×107 CFU/mL,按1%接种量接种到葡萄汁培养基中,置于30 ℃恒温培养24 h。
葡萄酒酿造[15]:挑选新鲜完整、无病害的葡萄果实,破碎过滤后分装至5 L发酵罐(160 ℃干热灭菌2 h)中,加入50 mg/L的偏重亚硫酸钾和20 mg/L的果胶酶,发酵前葡萄汁初始糖度为15°Brix,添加白砂糖将初始糖度调整为21°Brix。放置2 h后分别接种1%(V/V)的酿酒酵母A2和安琪葡萄酒专用酿酒酵母,置于25 ℃发酵5 d。发酵结束后测定总糖、总酸(以酒石酸计)、总酯含量、pH值、酒精度及主要挥发性香气物质。
1.3.7 分析检测
总糖(以葡萄糖计)、总酸(以酒石酸计)、pH值及酒精度测定:按照GB/T 15038—2006《葡萄酒、果酒通用分析方法》中的方法;总酯含量测定:采用皂化中和法[15]。
葡萄酒中主要酯类测定:采用气相色谱法[25]。气相色谱条件:DB-WAX毛细管柱(0.25 μm×30 m×0.32 mm),氢火焰离子检测器,进样器温度为200 ℃,检测器温度为230 ℃,载气为高纯氮气,流速1.0 mL/min。程序升温为初始温度40 ℃,保持5 min;10 ℃/min升至200 ℃,保持10 min。
定性定量方法:配制含有乙酸乙酯、己酸乙酯、乳酸乙酯、丁酸乙酯的混合标准品溶液,以乙酸丁酯为内标(质量浓度20 mg/L)混匀后进样,根据标准品出峰时间进行物质定性,采用内标法进行定量分析。
1.3.8 数据处理
采用SPSS Statistics 26.0进行单因素方差(analysis of variance,ANOVA)和Duncan检验,Design-Expert 13.0软件设计和分析PB试验、最陡爬坡试验及BB试验结果,使用Origin 2024软件对试验数据统计分析。
2 结果与分析
2.1 酵母菌的分离与纯化
从浓香型白酒酒曲中富集培养液中筛选出具有典型酵母菌形态特征菌株37株,分别编号为A1~A22、B1~B12、BA21、Z1、N1,其在PDA培养基中菌落形态见图1。

图1 筛选酵母菌株菌落形态
Fig.1 Colony morphology of screened yeast strains
由图1可知,菌株A13、A15、B2和B7的菌落质地坚硬、白色、表面粗糙呈绒毛状、边缘不整齐、不易挑取;其余菌株的菌落质地黏稠、白色至乳白色、表面光滑、边缘整齐、易挑取。
2.2 产酯菌株的筛选
2.2.1 产酯菌株的初筛
大部分酵母菌可以产酯产气,且酵母菌产气与产酯有一定正相关性[26]。筛选菌株产气试验及嗅香试验结果见表3。
表3 筛选菌株产气试验及嗅香试验结果
Table 3 Results of gas production tests and aroma tests of screened strains
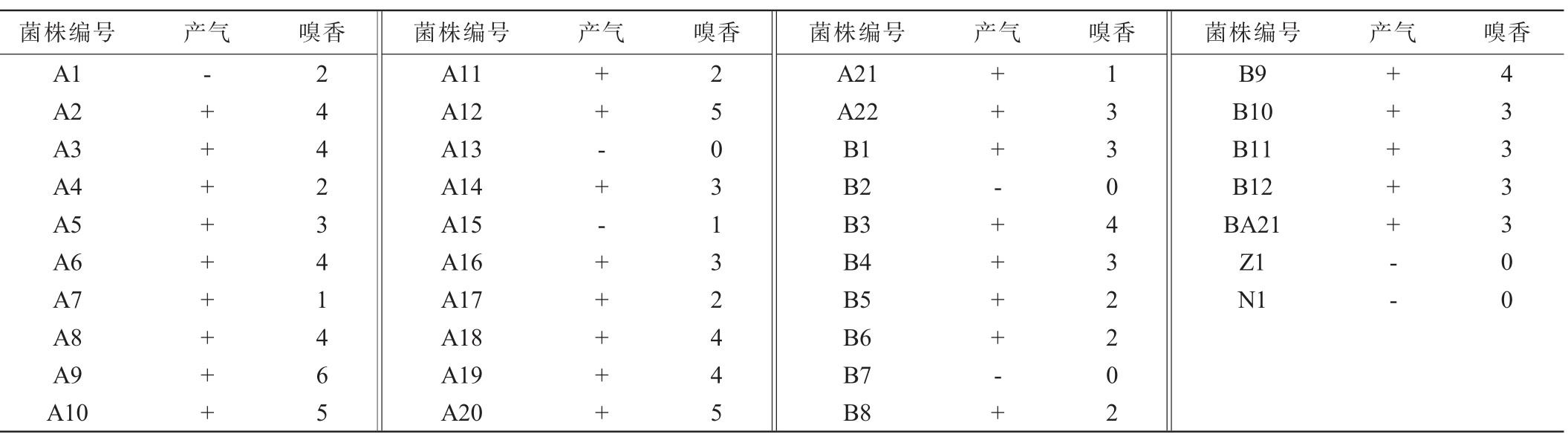
注:“+”表示有产气现象;“-”表示无产气现象;“/”表示无香;“0~6”表示嗅香评分。
由表3可知,共筛选得到产气及产酯(嗅香评分≥4)菌株12株,编号分别为A2、A3、A6、A8、A9、A10、A12、A18、A19、A20、B3和B9。将产气试验与嗅香试验中筛选出的12株菌制备种子液,按1%接种到麦芽汁培养基,30 ℃培养2 d,测定其总酯含量,结果见表4。由表4可知,12株菌发酵液总酯含量在1.37~1.86 g/L,其中菌株A2产酯能力最高,总酯含量为1.86 g/L。这与顾宗珠等[27]研究结果一致。选取产酯效果较好的9株菌进行复筛实验。
表4 筛选菌株发酵液总酯含量测定结果
Table 4 Determination results of total ester contents in fermentation broth of screened strains

注:不同小写字母表示差异显著(P<0.05)。
2.2.2 产酯菌株复筛
酯化酶是白酒酿造过程中很重要的一种酶类,可催化酸醇形成酯类物质。筛选菌株发酵液酯化酶活力测定结果见表5。
表5 筛选酵母菌发酵液酯化酶活力及己酸乙酯含量测定结果
Table 5 Determination results of esterification enzyme activities and ethyl caproate contents in fermentation broth of screened strains
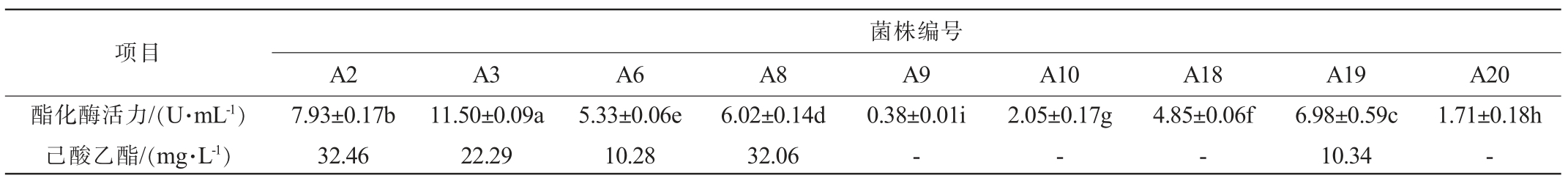
注:“-”表示未检出。
由表5可知,12株筛选菌产酯化酶活力差异较大,其中菌株A3酯化酶活力最高,为11.5 U/mL。筛选出5株酯化酶活力较高的菌株(A2、A3、A6、A8和A19),并采用气相色谱法分析这5株菌发酵液中己酸乙酯含量,结果表明,菌株A2、A3、A6、A8和A19己酸乙酯含量分别为32.46 mg/L、22.29 mg/L、10.28 mg/L、32.06 mg/L、10.34 mg/L,其中,菌株A2己酸乙酯含量最高(32.46 mg/L)。因此,选择优良产酯菌株A2进行鉴定。
2.3 优良产酯酵母A2的鉴定
2.3.1 形态学观察
优良产酯酵母A2菌落形态、显微形态、菌丝及子囊孢子形态见图2。
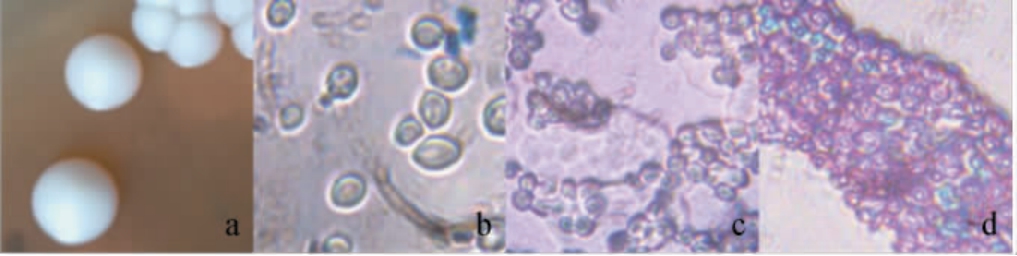
图2 菌株A2菌落(a)、细胞(b)、菌丝(c)及子囊孢子(d)形态
Fig.2 Morphology of colony (a),cells (b),mycelium (c) and ascospores (c) of strain A2
由图2a可知,菌株A2菌落呈白色、圆形、不透明、光滑、整齐、易挑起、凸起。由图2b可知,菌株A2细胞呈椭圆形,可见数个出芽状态的酵母菌,说明菌株A2的无性生殖方式均为出芽生殖。由图2c可知,未见菌株A2有假菌丝生成。由图2d可知,可见被孔雀绿染液染成蓝紫色的子囊孢子,说明酵母菌A2的有性生殖方式为子囊孢子生殖。这与秦立芹等[28]研究结果类似。
2.3.2 生理生化试验
菌株A2生理生化试验结果见表6。由表6可知,菌株A2可利用葡萄糖、半乳糖、蔗糖、麦芽糖和棉子糖进行发酵,不可利用乳糖。其可同化L-赖氨酸和硝酸钾,不可同化可溶性淀粉、D-木糖、海藻糖和柠檬酸。菌株A2脲酶试验、类淀粉产生试验结果均为阴性。依据《酵母菌的特征与鉴定手册》,酵母菌株A2生理生化特征与酿酒酵母基本符合。
表6 菌株A2生理生化试验结果
Table 6 Results of physiological and biochemical experiments of strain A2
注:“+”示为阳性;“-”示为阴性;“+/-”示为阴性或阳性;“w”示为弱阳性。
2.3.3 分子生物学鉴定
为进一步鉴定菌株A2的分类学地位,通过PCR扩增获得菌株A2的26S rDNA序列,将测序结果提交至NCBI,通过BLAST分析,采用MEGA 5.0基于26S rDNA的D1/D2区基因序列构建菌株A2系统发育树,结果见图3。

图3 基于26S rDNA基因序列的菌株A2系统发育树
Fig.3 Phylogenetic tree of strain A2 based on 26S rDNA gene sequence
由图3可知,菌株A2与酿酒酵母(Saccharomyces cerevisiae)聚于同一进化分支,其序列同源性为97%。综合对菌株A2的形态学观察、生理生化试验及基因序列的系统发育分析结果,菌株A2被鉴定为酿酒酵母(Saccharomyces cerevisiae)。
2.4 菌株A2产酯条件优化单因素试验
葡萄糖、冰乙酸、氯化钙、蛋白胨、乙醇添加量及发酵时间对菌株A2总酯产量的影响结果见图4。由图4A可知,总酯含量随葡萄糖添加量在0~5%范围内的增加呈先上升后下降的趋势。当葡萄糖添加量为0~2%时,总酯产量随之增加;当葡萄糖添加量为2%时,总酯产量最高,为1.97 g/L;当葡萄糖添加量>2%之后,总酯产量有所下降。葡萄糖添加量≤2%时,可能是低浓度的葡萄糖提供菌株生长足够的碳源,从而提高的产物代谢速度,产酯能力增强[29]。当葡萄糖添加量>2%时,过高葡萄糖添加量会逐渐增加发酵环境的渗透压,当渗透压大于酵母菌细胞本身的渗透压时,酵母菌细胞内水分被挤出胞外,对酵母菌的细胞形态造成破坏,进而对菌株的生长代谢产生影响[30]。因此,最适葡萄糖添加量为2%。
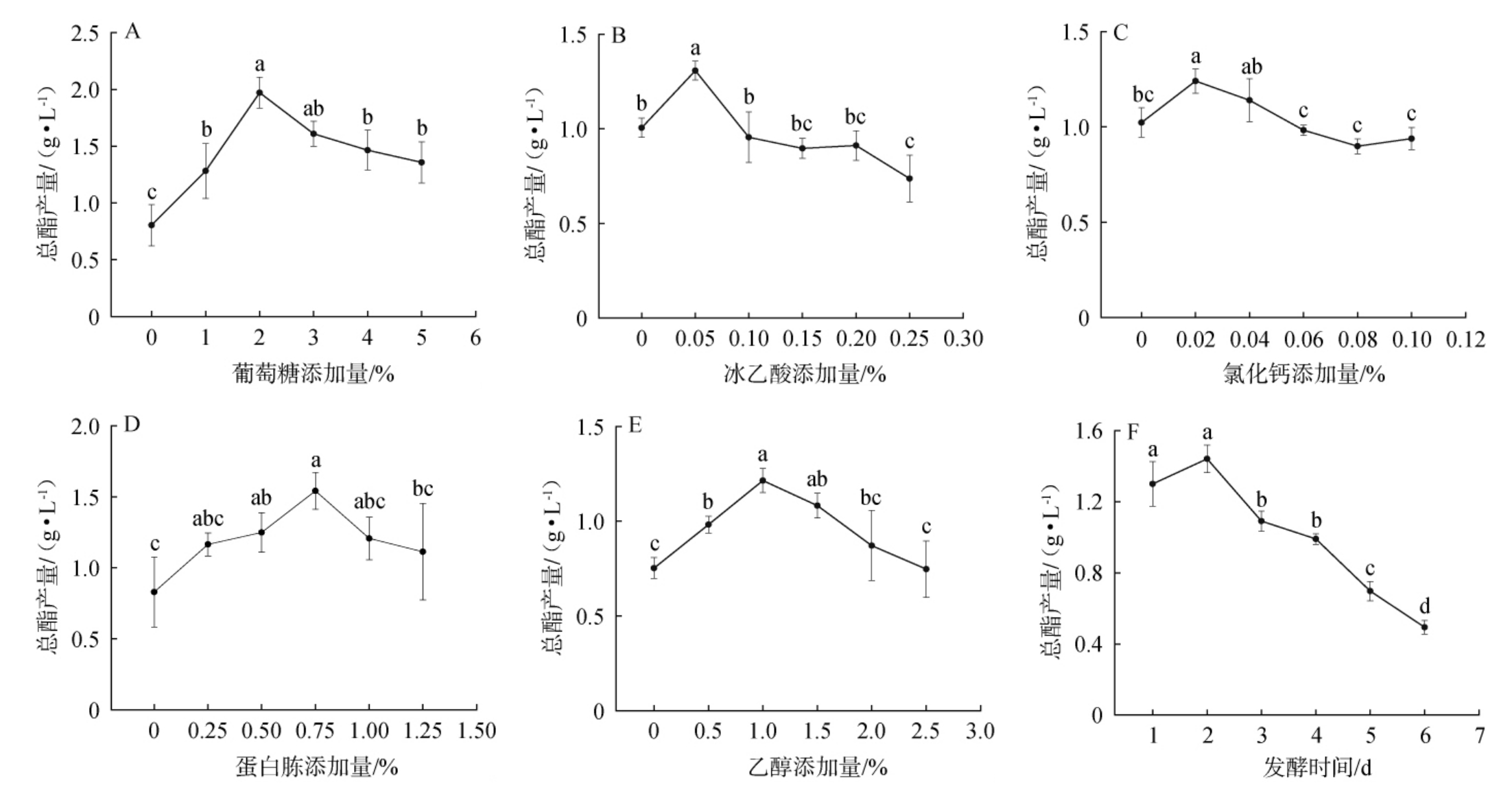
图4 葡萄糖(A),冰乙酸(B),氯化钙(C),蛋白胨(D),乙醇(E)添加量及发酵时间(F)对菌株A2总酯产量的影响
Fig.4 Effect of glucose (A),acetic acid (B),calcium chloride (C),peptone (D),ethanol (E) addition and fermentation time (F) on the total ester production of strain A2
小写字母不同表示差异显著(P<0.05)。
由图4B可知,总酯产量随冰乙酸添加量在0~0.25%范围内的增加呈先上升后下降的趋势。当冰乙酸添加量为0~0.05%时,总酯产量随之增加;当冰乙酸添加量为0.05%时,总酯产量最高,为1.31 g/L;当冰乙酸添加量>0.05%之后,总酯产量有所下降。酵母菌在生长过程中需要代谢一定浓度的冰乙酸,当冰乙酸添加量较低时,冰乙酸含量对酵母菌生长pH造成较小影响;当冰乙酸添加量过高,导致培养基中pH值接近酵母的最低耐受pH值[16],同时降低酵母菌胞内的pH,抑制酵母菌的生长,故冰乙酸添加量越高,总酯含量越低。因此,最适冰乙酸添加量为0.05%。
由图4C可知,总酯产量随氯化钙添加量在为0~0.10%范围内的增加呈先上升后下降至平缓的趋势。当氯化钙添加量0~0.02%时,总酯产量随之增加;当氯化钙添加量为0.02%时,总酯产量最高,为1.24g/L;当氯化钙添加量>0.02%之后,总酯产量有所下降。氯化钙是酵母菌生命活动必不可缺的无机盐类,一定浓度的氯化钙在保持细胞的渗透压、使细胞保持一定形态方面起着关键作用。同时酵母菌体内的缓冲系统对酸和碱都有缓冲作用,这也维持了细胞的酸碱平衡。适量的氯化钙会对酿酒酵母A2的菌体生长速度起到促进作用,如果氯化钙过高,会导致酵母细胞出现失水脱水现象[31]。因此,最适氯化钙添加量为0.02%。
由图4D可知,总酯产量随蛋白胨添加量在0~1.25%范围的增加呈先上升后下降的趋势。当蛋白胨添加量为0~0.75%时,总酯产量随之增加;当蛋白胨添加量为0.75%时,总酯产量最高,为1.54 g/L;当蛋白胨添加量>0.75%之后,总酯产量有所下降。在发酵前期的酵母对数生长期,氮源会被快速利用,含有较高蛋白胨,可以让酵母菌重新获得生长繁殖能力。而当培养基中蛋白胨浓度过高时,会造成渗透压增加,对酵母菌活性产生抑制作用。因此,最适蛋白胨添加量为0.75%。
由图4E可知,总酯产量随乙醇添加量在0~2.5%范围内的增加呈先上升后下降的趋势。当乙醇添加量为0~1.0%时,总酯产量随之增加;当乙醇添加量为1.0%时,总酯产量最高,为1.22 g/L;当无水乙醇添加量>1.0%之后,总酯产量有所下降。乙醇是酵母菌生长代谢的产物,发酵本身会产生乙醇,一定浓度的乙醇对酵母菌生长代谢影响较小。随着乙醇浓度的逐渐增大,在较高的酒精浓度下,会对酵母细胞造成一定的毒害作用。因此,最适乙醇添加量为1.0%。
由图4F可知,总酯产量随发酵时间在1~6 d范围内的增加呈先上升后下降的趋势。当发酵时间为1~2 d时,总酯产量随之增加;当发酵时间为2 d时,总酯产量最高,为1.44 g/L;当发酵时间>2 d之后,总酯产量有所下降。酵母菌消耗营养物质产生酯类的过程需要一定的时间,随着培养时间的延长,菌种的生长繁殖和代谢速率加快,总酯含量上升;发酵时间过长会导致酵母老化,产生的酯类物质挥发,并且培养基中的营养物质慢慢被耗尽。因此,最适发酵时间为2 d。
2.5 产酯条件优化响应面试验
2.5.1 Plackett-Burman试验设计及结果
以葡萄糖、冰乙酸、蛋白胨、无水乙醇添加量及发酵时间为自变量,以总酯产量为响应值,进行Plackett-Burman(PB)试验设计,优化菌株A2产酯条件,Plackett-Burman(PB)试验设计结果见表7,方差分析结果见表8。
表7 产酯条件优化Plackett-Burman试验设计及结果
Table 7 Design and results of Plackett-Burman experiments for esterification conditions optimization
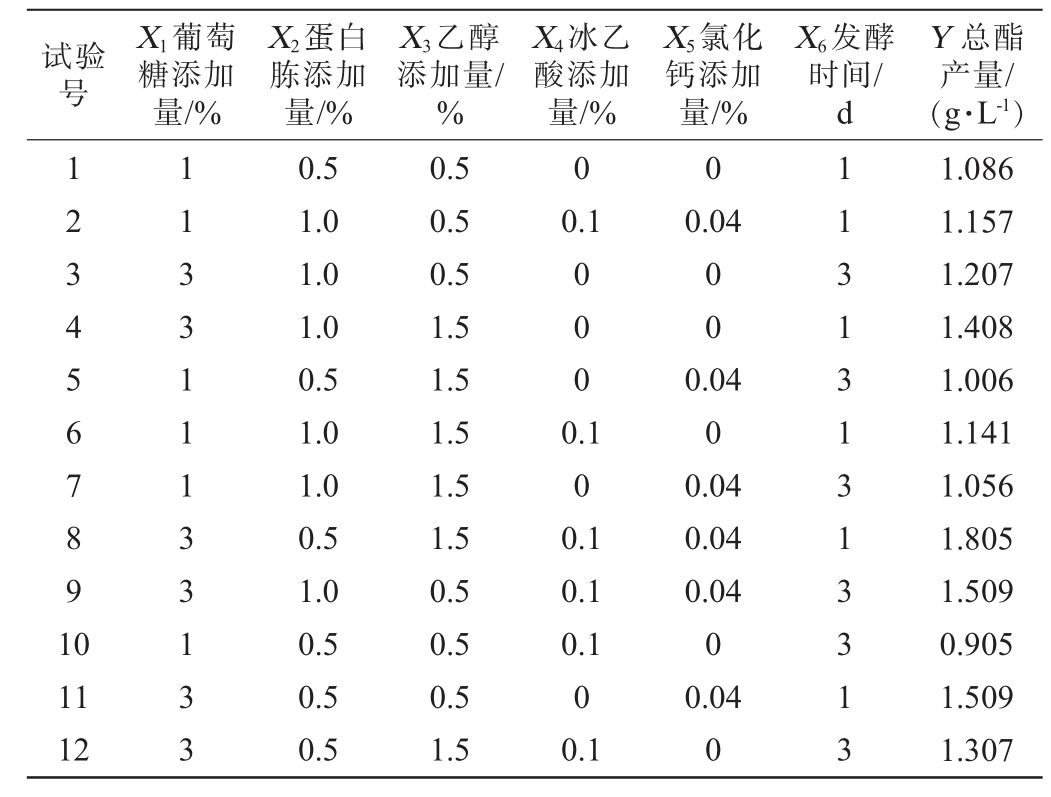
表8 Plackett-Burman试验方差分析结果
Table 8 Variance analysis results of Plackett-Burman experiments
注:“**”表示对结果影响极显著(P<0.01),“*”表示对结果影响显著(P<0.05)。下同。
由表7可知,各因素对总酯产量影响顺序为:葡萄糖添加量>发酵时间>氯化钙添加量>冰乙酸添加量>乙醇添加量>蛋白胨添加量。其中发酵时间和氯化钙添加量对总酯产量有显著影响(P<0.05),葡萄糖添加量对总酯产量有极显著影响(P<0.01)。
2.5.2 最陡爬坡试验结果
根据PB试验中3个显著因素的正负效应,依次增大或减小。其中,葡萄糖添加量和氯化钙添加量是正效应因素,应依次增大;发酵时间为负效应因素,应依次减小。最陡爬坡试验结果见表9。由表9可知,随着葡萄糖添加量和氯化钙添加量的逐渐增大,发酵时间逐渐减小,菌株A2总酯产量先增加后减少。当葡萄糖添加量为2.5%、氯化钙添加量为0.03%、发酵时间为36 h时,菌株A2总酯产量最高,为3个因素的最大响应值。故以第4组试验水平为中心值进行Box-Behnken设计试验。
表9 最陡爬坡试验结果
Table 9 Results of the steepest climbing tests
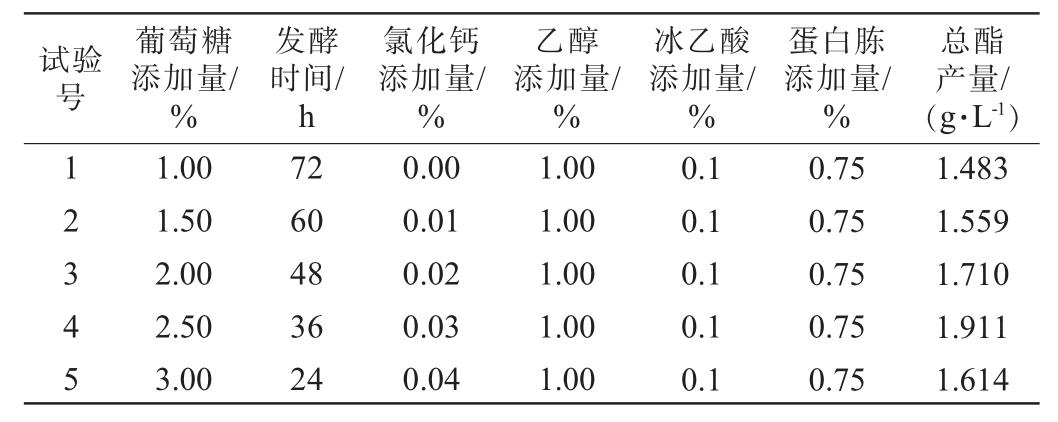
2.5.3 Box-Behnken设计试验
以葡萄糖添加量(A)、发酵时间(B)、氯化钙添加量(C)为自变量,菌株A2总酯产量(Y)为响应值,进行Box-Behnken设计试验,Box-Behnken试验结果见表10,方差分析见表11。
表10 产酯条件优化Box-Behnken试验设计及结果
Table 10 Design and results of Box-Behnken experiments for esterification conditions optimization
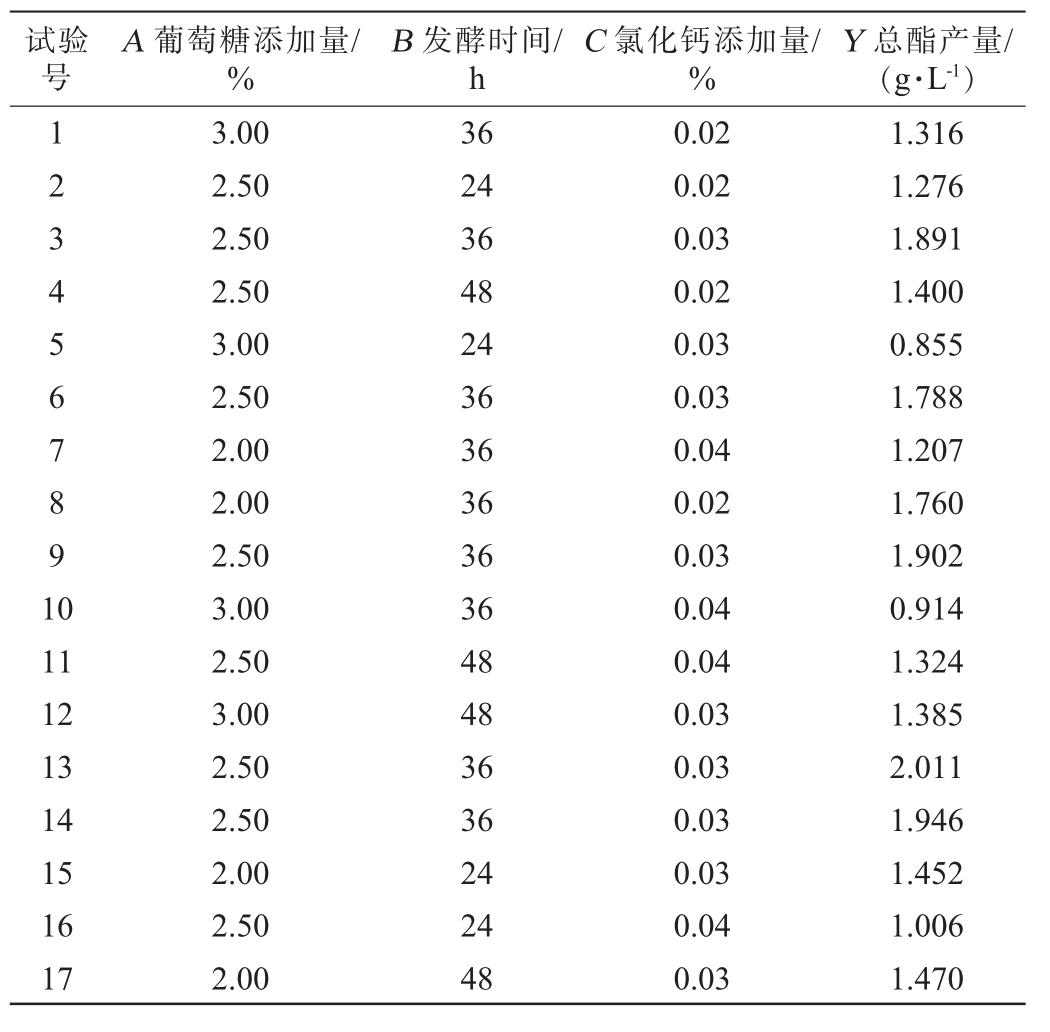
表11 回归模型方差分析
Table 11 Variance analysis of regression model
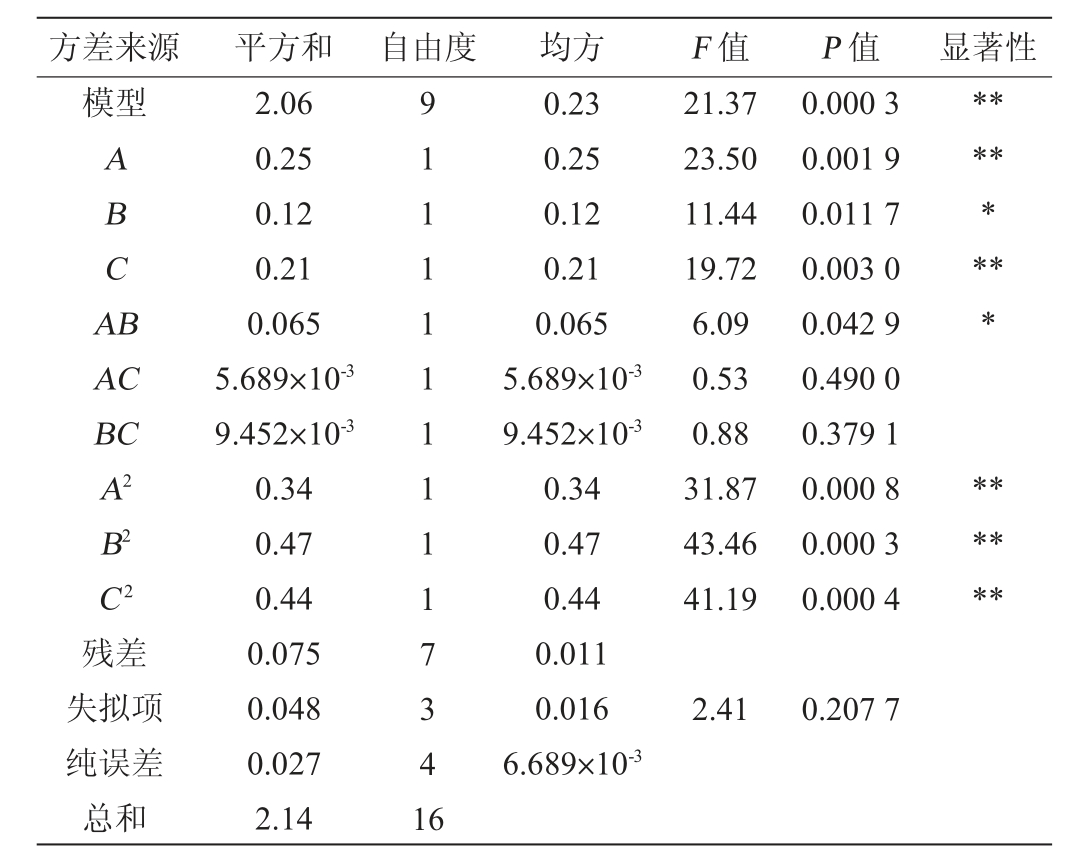
利用Design-Expert 13.0软件对表10数据进行多元二次回归拟合,得到多元二次回归方程为Y=1.91-0.18A+0.12B-0.16C+0.13AB+0.038AC+0.049BC-0.28A2-0.33B2-0.32C2。
由表11可知,该模型P值为0.000 3<0.01,说明该模型显著,失拟项的P值为0.207 7>0.05,不显著,表明模型可靠,该模型拟合方程与实际相符,误差较小。决定系数R2=0.964 9;调整决定系数R2adj=0.919 7,说明该模型拟合良好。由P值可知,一次项B,交互项AB对菌株A2总酯产量影响显著(P<0.05),一次项A、C,二次项A2、B2、C2对菌株A2总酯产量影响极显著(P<0.01)。由F值可知,3个因素对结果影响顺序为葡萄糖添加量(A)>发酵时间(C)>氯化钙添加量(B)。
2.5.4 各因素间交互作用分析
响应曲面越陡峭,等高线越趋于椭圆形,表明二者交互作用对结果影响越强;反之,两因素间交互作用响应面越平缓,等高线越趋于圆形,表明二者交互作用对结果影响越弱。各因素间交互作用对结果影响响应面及等高线见图5。
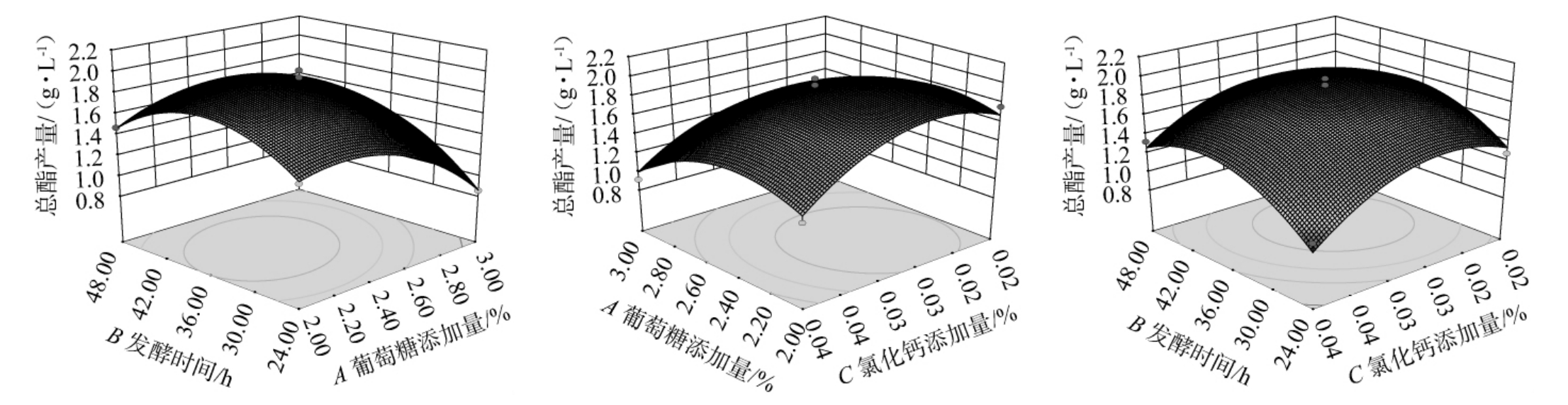
图5 各因素间交互作用对总酯产量影响的响应面及等高线
Fig.5 Response surface plots and contour lines of effect of interaction between various factors on the total ester production
由图5可知,葡萄糖添加量和发酵时间之间的响应面陡峭,且等高线密集,呈椭圆状,表明葡萄糖添加量和发酵时间两个因素的交互作用对酿酒酵母A2总酯产量影响较明显;葡萄糖添加量与氯化钙添加量之间的响应面坡度比较平缓,且等高线较稀疏,表明葡萄糖添加量和氯化钙添加量两个因素的交互作用对酿酒酵母A2总酯产量无显著影响;发酵时间与氯化钙添加量之间的响应面坡度比较平缓,且等高线较稀疏,表明发酵时间和氯化钙添加量两个因素的交互作用对酿酒酵母A2总酯产量影响不显著。
2.5.5 验证试验
利用Design-Expert 13.0软件分析得到酿酒酵母A2最佳产酯条件为:葡萄糖添加量2.35%,发酵时间37.31 h,氯化钙添加量0.03%。在此条件下,总酯产量预测值为1.934 g/L。为考虑到实际操作可行性,将最佳产酯条件修正为:葡萄糖添加量2.4%,发酵时间37 h,氯化钙添加量0.03%。在此条件下进行3次平行验证试验,总酯产量平均实际值为1.996 g/L,与预测值较为接近,表明该模型优化酿酒酵母A2产酶条件可行。
2.6 菌株A2在葡萄酒发酵中的应用
2.6.1 酿酒酵母A2酿造葡萄酒理化指标
以安琪葡萄酒专用酿酒酵母为对照,酿酒酵母A2酿造葡萄酒理化指标测定结果见表12。由表12可知,两种酿酒酵母酿造的葡萄酒总酸为9.47 g/L、10.43 g/L(国标不作要求),总糖含量为1.21 g/L、1.46 g/L(≤4 g/L),酒精度为11.4%vol、12.3%vol(≥7.0%vol),均满足国标GB 15037—2006《葡萄酒》[32]要求。
表12 不同酵母酿造葡萄酒理化指标测定结果
Table 12 Determination results of physicochemical properties of wine brewed by different yeasts

2.6.2 酿酒酵母A2酿造葡萄酒主要酯类
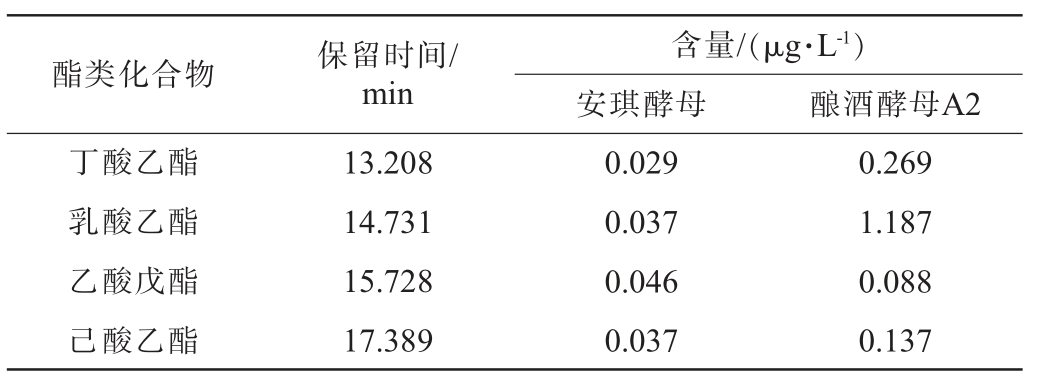
挥发性香气物质是葡萄酒中的重要因素之一,对葡萄酒的风格与品质有重要影响。以安琪葡萄酒专用酿酒酵母为对照,酿酒酵母A2酿造葡萄酒主要酯类测定结果见表13。由表13可知,酿酒酵母A2主要的发酵代谢产物是乳酸乙酯,其次是丁酸乙酯、己酸乙酯、乙酸戊酯;安琪专用酿酒酵母均低于酿酒酵母A2,说明由酿酒酵母A2所酿造的葡萄酒香气物质较优。
表13 不同酵母酿造葡萄酒主要酯类测定结果
Table 13 Determination results of main esters in wine brewed by different yeasts
3 结论
本试验结合产气、嗅香和总酯含量指标,从新疆雪水坊白酒曲中分离出5株产酯酿酒酵母,并结合形态学观察、生理生化试验及分子生物学技术对其进行优良产酯菌种鉴定。结果表明,筛选出一株产酯能力优良菌株A2,其被鉴定为酿酒酵母(Saccharomyces cerevisiae)。通过单因素试验及响应面试验得到酿酒酵母A2的最佳产酯条件为:葡萄糖添加量2.4%,发酵时间37 h,氯化钙添加量0.03%。在此条件下,酿酒酵母A2总酯产量为1.996 g/L。酿酒酵母A2酿造葡萄酒理化指标均符合国标相关要求,且主要酯类含量比对照显著增加,表明其具有应用于葡萄酒实际生产的潜力。
[1] 丁海龙,熊燕飞,沈小娟,等.浓香型白酒微量风味成分研究进展[J].中国酿造,2025,44(11):22-26.
[2] 国家市场监督管理总局,国家标准化管理委员会.GB/T 10781.1—2021白酒质量要求 第1部分:浓香型白酒[S].北京:中国标准出版社,2021.
[3] 国家市场监督管理总局,国家标准化管理委员会.GB/T 17204—2021饮料酒术语和分类[S].北京:中国标准出版社,2021.
[4] 杨磊,穆敏敏,文成兵,等.浓香型白酒提质增香技术研究进展[J].酿酒,2022,49(1):18-21.
[5] 万世旅,李光辉,钟姝霞,等.酒曲中产酯酵母的分离筛选[J].四川理工学院学报(自然科学版),2015,28(6):16-19.
[6] 王益姝,钱超,黄卫宁,等.梅兰春酒醅中生香酵母的分离鉴定及其发酵面包香气成分分析[J].食品发酵与工业,2016,42(9):45-51.
[7] WU W Y,CHEN T,ZHAO M M,et al.Effect of co-inoculation of different halophilic bacteria and yeast on the flavor of fermented soy sauce[J].Food Bioscience,2023,51:102292.
[8] ZUO Y M,XIAO F,GAO J C,et al.Establishing Komagataella phaffii as a cell factory for efficient production of sesquiterpenoid α-santalene[J].JAgr Food Chem,2022,70(26):8024-8031.
[9] 王鹏昊,关统伟,张习超,等.小曲中优质产酯酵母分离鉴定及其产酯条件优化[J].食品与发酵工业,2018,44(2):62-67.
[10] 刘薇.高产乙酸乙酯酵母筛选、特性研究及其应用[D].乌鲁木齐:新疆农业大学,2022.
[11] 刘朋肖,常煦,成柳洁,等.酿酒酵母Y3401产己酸乙酯发酵条件的优化[J].中国食品学报,2022,22(2):178-189.
[12] 王朝阳.清香型大曲白酒产酯酵母的筛选及鉴定[D].太原:山西大学,2019.
[13] 陈田,周佳,汪依萍,等.氯霉素降解菌Pseudoxanthomonas mexicana CC18的筛选、鉴定和降解特性[J].生物学杂志,2024,41(1):94-99.
[14] 姚博,负建民,艾对元,等.浆水中产酯酵母菌菌株的筛选及其增殖培养基优化[J].食品科学,2018,39(6):107-115.
[15] 周桂珍,杨伟明,杨建兴,等.宁夏贺兰山东麓葡萄酒酵母菌的筛选及应用[J].微生物学通报,2023,50(2):553-572.
[16] 任蓓蕾.生香酵母的筛选及真空冷冻干燥法制备其活性干酵母工艺的研究[D].保定:河北农业大学,2014.
[17] 王益姝,钱超,黄卫宁,等.梅兰春酒醅中生香酵母的分离鉴定及其发酵面包香气成分分析[J].食品发酵与工业,2016,42(9):45-51.
[18] 杜艾明,董孝元,李俊薇,等.清香型白酒酿造体系中酵母菌的分离鉴定及生产特性分析[J].食品科技,2021,46(7):29-36.
[19] 李海营.高产酯酿酒酵母的分离筛选与酵母液体曲的制备[D].哈尔滨:黑龙江大学,2013.
[20] 杜春迎.浓香型大酒曲中高产酯化酶菌株的筛选及产酶条件优化[D].哈尔滨:黑龙江大学,2012.
[21] BARNET J A,PENN R W,YARROW D.酵母菌的特征与鉴定手册[M].胡瑞卿译.青岛:青岛海洋大学出版社,1991:394-425.
[22] 刘建学,刘金科,李璇,等.白酒酒醅高产酯酵母筛选鉴定及其发酵性能研究[J].食品与机械,2020,36(6):42-49.
[23] 李晨.一株产酯酵母的筛选鉴定及其产酯条件的优化研究[D].武汉:武汉轻工大学,2019.
[24] 芦红云,刘思宇,娄行行,等.东山老米酒酿造过程中酵母菌的分离鉴定及其品质分析[J].食品安全质量检测学报,2021,12(21):12-19.
[25] 丁银蒙,赵亚惠,柳文媛,等.静态顶空-气相色谱法同时测定葡萄酒中12种挥发性成分[J].食品安全质量检测学报,2021,12(23):8993-8999.
[26] 匡钰,张洪波,沈福英,等.咖啡果酒产酯酵母分离鉴定及遗传稳定性评价[J].生物工程,2019,40(10):14-21.
[27] 顾宗珠,林晓吟,何思娜,等.酒曲中产酯酵母的筛选及培养条件的研究[J].中国酿造,2013,32(10):53-56.
[28] 秦立芹,殷欢,成柳洁,等.一株高产己酸乙酯酵母菌株的筛选鉴定及发酵条件优化[J].食品与发酵工业,2022,48(1):55-61.
[29] 黄小晶.氮源对酿酒酵母发酵特性的影响[D].杨陵:西北农林科技大学,2016.
[30] 黄光建,徐学锋,郭梅君,等.豉香型白酒酒饼中高产乙酸乙酯酵母菌的分离鉴定及发酵性能研究[J].食品工业科技,2015,36(11):153-158.
[31] 陈晓娜,彭加飞,王品美,等.响应面法优化paraherquamide A的发酵工艺[J].天然产物研究与开发,2023,35(6):1049-1057.
[32] 国家质量监督检验检疫总局,中国国家标准化管理委员会.GB 15037—2006葡萄酒[S].北京:中国标准出版社,2006.