乳酸菌(lactic acid bacteria,LAB)是一类广泛应用于食品、医药及农业等领域的有益微生物,具有良好的发酵、保鲜和生物防腐等功能[1]。在传统果蔬发酵中,乳酸菌不仅主导发酵进程与发酵风味物质的产生,还可通过产酸降低pH以及合成抗菌物质抑制腐败菌生长繁殖,从而提高果蔬发酵产品的安全性、风味品质及贮藏稳定性[2-3]。随着功能发酵食品的快速发展,对具有特定发酵特性和应用价值的乳酸菌资源进行系统挖掘与利用,成为当前果蔬发酵研究的重要方向之一。
近年来,国内外学者对泡菜中乳酸菌的菌群结构、优势菌种筛选及其功能特性进行了广泛研究。研究表明,尽管不同地区传统自然发酵泡菜表现出细菌群落多样性与丰度差异性,但是植物乳植杆菌(Lactiplantibacillus plantarum)、短乳杆菌(Lactobacillus brevis)和肠膜明串珠菌(Leuconostoc mesenteroides)等多为泡菜中的常见优势乳酸菌[4]。部分乳酸菌菌株因其良好的益生功能、抑菌作用和环境耐受性,在果蔬发酵产品研制与生产中备受关注[5-7]。然而,传统自然果蔬发酵工艺存在菌群不稳定、品质难以控制、发酵周期长及亚硝酸盐残留风险等问题,亟待开展性能优良的乳酸菌资源分离筛选及其发酵剂制备等研究[8-9]。
芥菜含有辛辣物质异硫氰酸烯丙酯,使得其腌制品呈现独特的风味[10]。水东芥菜(Brassica juncea(L.)Coss.var.foliosa Bailey)作为一种具有代表性的国家地理标志产品,富含维生素与矿物质,其独特风味和营养价值深受消费者青睐[11]。目前,芥菜腌制加工多为传统自然发酵工艺,不仅发酵周期长、效率低,而且难以有效激发芥菜独特的风味物质[12-13]。此外,针对水东芥菜腌制而开展的乳酸菌资源挖掘及其应用研究仍较缺乏。为此,本研究以采购的多份自然发酵泡菜样品为研究对象,分离筛选具有优良发酵、益生性能的乳酸菌,并对筛选菌株进行形态学观察与分子生物学鉴定。利用单因素及响应面试验优化其发酵培养基,提高菌株的产酸能力,以期为水东芥菜腌制发酵剂的开发与应用提供优质的益生菌资源。
1 材料与方法
1.1 材料与试剂
1.1.1 材料
四川泡菜、东北酸菜、广东酸笋、朝鲜族辣白菜、云南腌菜、江西酸豆角、红星酸菜、独山盐酸菜、淅川酸菜、涪陵榨菜:市售。
金黄色葡萄球菌(Staphylococcus aureus)ATCC25923、大肠杆菌(Escherichia coli)ATCC25922、沙门氏菌(Salmonella typhimurium)ATCC14028、单增李斯特菌(Listeria monocytogenes)CMCC(B)54002:均为本实验室购置并保藏。
1.1.2 试剂
过氧化氢、牛胆盐、盐酸、氢氧化钠、对氨基苯磺酸、盐酸萘乙二胺、氯化钠、硝酸钠、硫酸铵、硫酸锰、硫酸锌、钼酸钠、氯化钴、氯化钙、硫酸镁:上海麦克林生化科技有限公司;革兰氏染液、琼脂粉、酵母膏:广东环凯微生物科技有限公司;蛋白胨、牛肉膏:北京陆桥技术股份有限公司;细菌基因组脱氧核糖核酸(deoxyribonucleic acid,DNA)提取试剂盒:北京索莱宝科技有限公司。所用试剂均为分析纯或生化试剂。
1.1.3 培养基
LB肉汤培养基、LB固体培养基:北京陆桥技术股份有限公司。
MRS液体培养基:蛋白胨10 g,牛肉粉8 g,酵母粉4 g,葡萄糖20 g,磷酸氢二钾2 g,柠檬酸氢二铵2 g,乙酸钠5 g,硫酸镁0.2 g,硫酸锰0.04 g,吐温80 1 g,蒸馏水1 000 mL,121 ℃高压蒸汽灭菌20 min。MRS固体培养基:在MRS液体培养基中添加20 g/L琼脂。
1.2 仪器与设备
ZWYR-2102型恒温培养振荡器:上海智城分析仪器制造有限公司;DM500生物显微镜:上海Leica显微系统有限公司;UV-8000紫外分光光度计:上海元析仪器有限公司;BPMJ-150F生化培养箱:上海一恒科学仪器有限公司;3K-15SIGMR台式高速冷冻离心机:扬州离心机有限公司;SW-CJ-2D型净化工作台:苏州净化设备有限公司;HANNA-2210型酸度计:北京信立方科技发展股份有限公司;YXQLS-70A立式压力蒸汽灭菌锅:宁波久兴医疗器械有限公司。
1.3 方法
1.3.1 乳酸菌初筛
取不同的泡菜样品各10 g分别加入90 mL无菌生理盐水中,振荡混匀,制备10-1菌悬液,并采用10倍梯度稀释法逐步稀释。分别取10-3、10-4、10-5梯度稀释液各200 μL,均匀涂布于MRS固体培养基(含1%碳酸钙),在37 ℃生化培养箱中用厌氧袋培养24 h。挑取溶钙圈明显、菌落生长优势突出的单菌落,进行连续划线纯化,37 ℃继续培养24 h,将分离纯化得到的菌株进行革兰氏染色和过氧化氢酶试验,选取疑似乳酸菌菌株并用30%甘油存放在-80 ℃冰箱。
1.3.2 高产酸乳酸菌复筛
取200 μL初筛菌株接种至装有100 mL MRS液体培养基的锥形瓶中,置于恒温振荡培养箱中,37 ℃、160 r/min振荡培养24 h,获得种子液。将种子液以3%(V/V)接种量接种至含不同质量分数NaCl(0、2%、4%、6%、8%)的MRS发酵培养基中,37 ℃、160 r/min振荡培养48 h,于波长600 nm处测量吸光度(OD600nm值),评估菌体的生长情况并测定菌液pH值,筛选产酸能力强、耐盐性良好的菌株。
1.3.3 乳酸菌菌株的鉴定
1.3.3.1 形态学观察
将分离筛选得到的菌株划线接种于MRS固体培养基,37 ℃厌氧培养48 h,观察并记录单菌落的颜色、形状、边缘、表面、透明度、菌落大小和质构特征。取适量菌液进行革兰氏染色,在显微镜下观察菌体形态。利用扫描电子显微镜,对菌株的微观形态结构特征进一步分析。
1.3.3.2 分子生物学鉴定
采用细菌基因组DNA提取试剂盒提取乳酸菌菌株的基因组DNA,提取得到的DNA作为聚合酶链式反应(polymerase chain reaction,PCR)扩增模板。选用细菌通用引物27F(5'-AGAGTTTGATCCTGGCTCAG-3')和1492R(5'-GGTTACCTTGTTACGACTT-3')扩增16S rRNA基因序列。PCR反应体系总量为25 μL,包括10×PCR Buffer(含Mg2+)2.5 μL,脱氧核糖核苷三磷酸(deoxy-ribonucleoside triphosphate,dNTP)混合液(2.5 mmol/L)2 μL,Taq DNA聚合酶(5 U/μL)0.2 μL,27F与1492R引物(10 μmol/L)各0.5 μL,模板DNA(20~50 ng/μL)0.5 μL,ddH2O补足至25 μL。PCR扩增程序:94 ℃预变性5 min;94 ℃变性30 s,55 ℃退火30 s,72 ℃延伸90 s,共30个循环;72 ℃终延伸10 min。PCR扩增产物经1%琼脂糖凝胶电泳检测合格后,送至上海生工生物工程有限公司进行测序。所得测序结果使用ContigExpressv3.0.0软件进行序列拼接和组装,并提交至美国国家生物技术信息中心(National Center for Biotechnology Information,NCBI)的GenBank数据库,利用基本局部比对搜索工具(basic local alignmentsearchtool,BLAST)进行序列同源性比对分析。将目标菌株的16S rRNA基因序列与数据库中相似度较高的参考序列一同导入MEGA 7.0软件,采用邻接法(Neighbor-Joining,NJ)构建系统发育树,并通过Bootstrap自举法(重复次数为1 000次)评估系统发育树的可靠性,以明确菌株的种属归属与系统发育位置。
1.3.4 筛选菌株的益生特性评价
1.3.4.1 生长曲线测定
取甘油冷冻保藏的筛选菌株于MRS液体培养基中进行活化,30 ℃静置培养24 h,取对数生长期菌液(OD600nm值为0.8)按3%(V/V)接种至新鲜MRS液体培养基中,于30 ℃静置培养。在培养过程中,每隔3 h取样一次,测定菌液的OD600nm值和pH值,以菌龄为横坐标,OD600nm值为纵坐标绘制生长曲线。
1.3.4.2 降解亚硝酸盐能力测定
将活化后的筛选菌株接种至添加20 mg/L亚硝酸钠(NaNO2)的MRS液体培养基中,接种量为3%,30 ℃静置培养。分别于0、6、12、24、36、48 h取样,立即离心(6 000×g,10 min,4 ℃)收集上清液,采用重氮盐显色法测定亚硝酸盐残留量[14]。
1.3.4.3 溶血性、自聚集和共聚集
溶血性试验[15]:将活化后的筛选菌株划线接种于5%无菌哥伦比亚血琼脂平板上,37 ℃厌氧培养48 h,观察其溶血类型。其中,α-溶血(部分溶血):菌落周围出现绿色透明带;β-溶血(完全溶血):菌落周围出现清晰透明圈;γ-溶血(无溶血):菌落周围无透明变化。
自聚集率测定[16]:将筛选菌株于MRS液体培养基中培养至对数后期(发酵18~24 h),4 000 r/min离心10 min收集菌体,采用磷酸盐缓冲液(phosphate buffer saline,PBS)(pH 7.20)调节至OD600nm值接近0.8,取4 mL于试管中,静置于30 ℃培养箱,分别于0、2 h、4 h、6 h、8 h测定上清液的OD600nm值。自聚集率计算公式如下:
式中:A0为0 h的OD600nm值,At为t h后的OD600nm值。
共聚集率测定[17]:利用指示菌大肠杆菌ATCC 25922、金黄色葡萄球菌ATCC25923与筛选菌株分别培养,菌液离心后均用PBS调节至OD600nm值接近0.8。各取2 mL等体积混合的两种菌悬液,轻轻混匀,30 ℃静置4 h,取上清液测定OD600nm值。共聚集率计算公式如下:
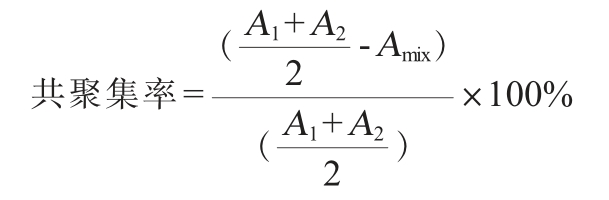
式中:A1为筛选菌株初始OD600nm值,A2为指示菌初始OD600nm值,Amix为混合液静置4 h后的OD600nm值。
1.3.4.4 耐酸与耐胆盐能力测定
参考LIU C等[18]的方法并稍作修改。将筛选菌株活化至对数生长期后,以3%(V/V)的接种量接种至不同pH值(2.0、3.0、4.0、5.0、6.0、7.0)的MRS液体培养基中,于37 ℃条件下培养48 h,分别测定培养0、3 h、6 h、12 h、24 h、36 h、48 h时菌体的OD600nm值,以评估其耐酸性。
菌株的胆盐耐受性测试参考李杰等[19]的方法并稍作修改。将活化至对数生长期的菌株按3%(V/V)的接种量接种至分别含有1 g/L、2 g/L、3 g/L牛胆盐的MRS液体培养基中,37 ℃培养5 h。分别于0 h、5 h取样,进行梯度稀释后接种至MRS固体培养基,37 ℃培养24 h后计数活菌数。使用未加胆盐的MRS液体培养基作为对照组,菌株胆盐耐受能力通过计算存活率评估,存活率计算公式如下:
其中:Nt为胆盐处理后活菌数,N0为初始活菌数。
1.3.4.5 体外抑菌能力测定
为评价筛选菌株的抑菌活性,采用牛津杯扩散法进行测定[20]。将该菌株按3%(V/V)的接种量接种至MRS液体培养基中,于37 ℃静置培养24 h。培养结束后,菌液经4 ℃、6 000 r/min离心5 min,上清液经0.22 μm微孔滤膜无菌过滤,获得无细胞上清液。指示菌株包括大肠杆菌ATCC 25922、金黄色葡萄球菌ATCC 25923、沙门氏菌ATCC 14028和单增李斯特菌CMCC(B)54002。上述菌株接种于LB液体培养基中,37 ℃、160 r/min条件下振荡培养至OD600nm值接近0.5,菌液浓度经无菌生理盐水调整至1.0×106 CFU/mL。将200 μL指示菌液均匀涂布于LB琼脂平板表面,待其表面风干后,将无菌牛津杯垂直置于平板中央,加入200 μL无细胞上清液,以同体积无菌生理盐水为空白对照。平板置于4 ℃预扩散2 h后,37 ℃培养24 h,采用游标卡尺测量抑菌圈直径(mm)以评估抑菌能力,抑菌圈直径越大代表菌株的抑菌能力越强。
1.3.5 筛选菌株发酵培养基条件优化
取250 μL筛选菌株接种到MRS液体培养基中,37 ℃培养24 h,按3%(V/V)接种量接种到初始发酵培养基中培养48 h,测定菌液菌体量、pH值。初始发酵培养基的配制参照周丽君等[21]的方法并略作修改,初始培养基组成为:葡萄糖30 g/L、蛋白胨20 g/L、磷酸氢二钾2 g/L、硫酸镁0.2 g/L、氯化钠5 g/L、碳酸氢钠2 g/L,pH 6.5,在121 ℃条件下灭菌20 min。
1.3.5.1 单因素试验
分别考察不同碳源(葡萄糖、蔗糖、麦芽糖、果糖、糖蜜、可溶性淀粉和糊精)及其添加量(10 g/L、15 g/L、20 g/L、25 g/L、30 g/L、35 g/L、40 g/L)、不同氮源(酵母膏、牛肉膏、蛋白胨、大豆蛋白胨以及硫酸铵)及其添加量(10 g/L、15 g/L、20 g/L、25 g/L、30 g/L、35 g/L、40 g/L)、不同微量元素(钴离子、锰离子、锌离子、钼离子、钙离子、镁离子)及其添加量(0.10 g/L、0.15 g/L、0.20 g/L、0.25 g/L、0.30 g/L、0.35 g/L、0.40 g/L)对菌液pH值及生物量的影响,并以不添加微量元素的组作为对照(CK)。
1.3.5.2 响应面试验
根据上述单因素试验的结果,以糖蜜添加量(A)、蛋白胨添加量(B)、锰离子添加量(C)为自变量,菌液pH值(Y)为响应值,利用Design-Expert 13.0软件设计3因素3水平的响应面试验,探究筛选菌株最优发酵培养基配方,响应面试验因素与水平见表1。
表1 发酵培养基配方优化响应面试验因素与水平
Table 1 Factors and levels of response surface test for fermentation medium formula optimization

1.3.6 数据处理
采用Origin 2021、Design-Expert 13.0、IBM SPSS Statistics 27、Excel 2010、MEGA 6.0等软件进行数据统计及作图分析。
2 结果与分析
2.1 高产酸乳酸菌的初筛与复筛
MRS固体培养基中的CaCO3能与乳酸反应生成可溶性盐,因此透明圈的出现可作为菌株产酸的直观指标。进一步根据菌落透明圈大小、菌体显微镜形态观察、革兰氏染色以及过氧化氢酶试验及气体产量判断(不产气、阴性过氧化氢酶)等生理生化特性检测,筛选出5株符合典型乳酸菌特征的候选菌株,分别编号为XY、XZ、XL、YL、ZL。5株初筛菌株在不同NaCl含量(0、2%、4%、6%、8%)条件下的菌体量(OD600nm值)与发酵pH值见图1。由图1可知,相比于其他菌株,菌株XL在各NaCl梯度下表现出更为优异的菌体生长量以及较低的pH值。尤其是当盐含量提高至6%时,菌株XL仍具有相对较高的OD600nm值(0.7左右),且其发酵液pH值显著低于其他菌株(P<0.05),说明其在高盐胁迫下仍能较好地生长和产酸。综上分析,菌株XL在不同盐浓度条件下均表现出较强的耐盐性和产酸能力,具有作为优势菌株用于高盐环境泡菜发酵的应用潜力,选择其进行后续试验。
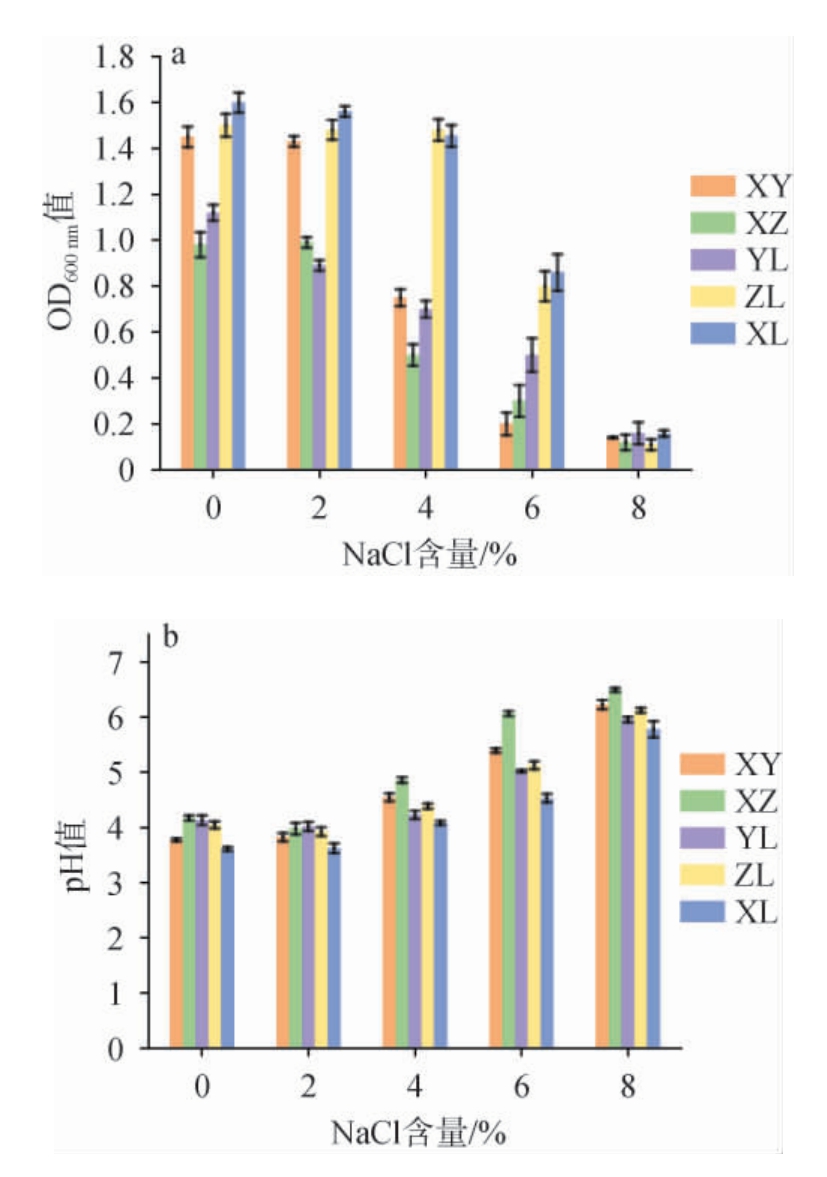
图1 不同NaCl含量对菌株生长量(a)及产酸能力(b)的影响
Fig.1 Effect of different NaCl concentrations on strain biomass (a)and acid-producing ability (b)
2.2 筛选菌株形态学观察及分子生物学鉴定
2.2.1 形态学观察
由图2a可知,菌株XL在MRS平板上形成圆形、乳白色菌落,表面光滑,边缘整齐,略带黏性,菌落质地柔软,透明度较低,具有典型的乳酸菌菌落特征。由图2b可知,经革兰氏染色后在显微镜下观察,该菌株呈阳性,形态为短杆状,两端圆钝,排列多以单个或成对存在,无芽孢,符合乳杆菌属细胞形态特征。采用扫描电子显微镜对其微观结构进行进一步观察,由图2c可知,菌株XL呈杆状,表面光滑,大小均一,表现出良好的细胞结构完整性和形态稳定性。
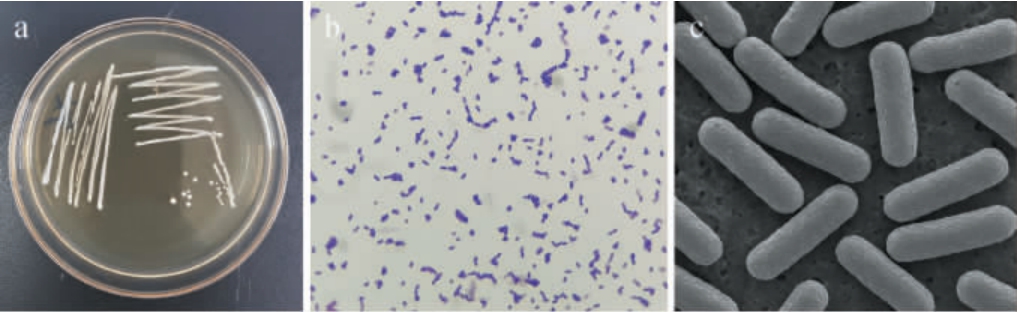
图2 菌株XL的菌落形态(a)、革兰氏染色结果(b)及扫描电镜结果(c)
Fig.2 Colony morphology (a),Gram staining results (b),and scanning electron microscopy images (c) of strain XL
2.2.2 分子生物学鉴定
菌株XL的16S rRNA基因序列在NCBI GenBank数据库中经BLAST同源性比对,与戊糖乳植杆菌(Lactiplantibacillus pentosus)的序列相似性高达99.7%,具有较高的亲缘关系。进一步采用MEGA 6.0软件构建菌株XL的系统发育树,结果见图3。由图3可知,菌株XL与戊糖乳植杆菌聚为同一分支,遗传距离较近。结合其形态学特征和分子水平的鉴定结果,最终菌株XL被鉴定为戊糖乳植杆菌(Lactiplantibacillus pentosus)。
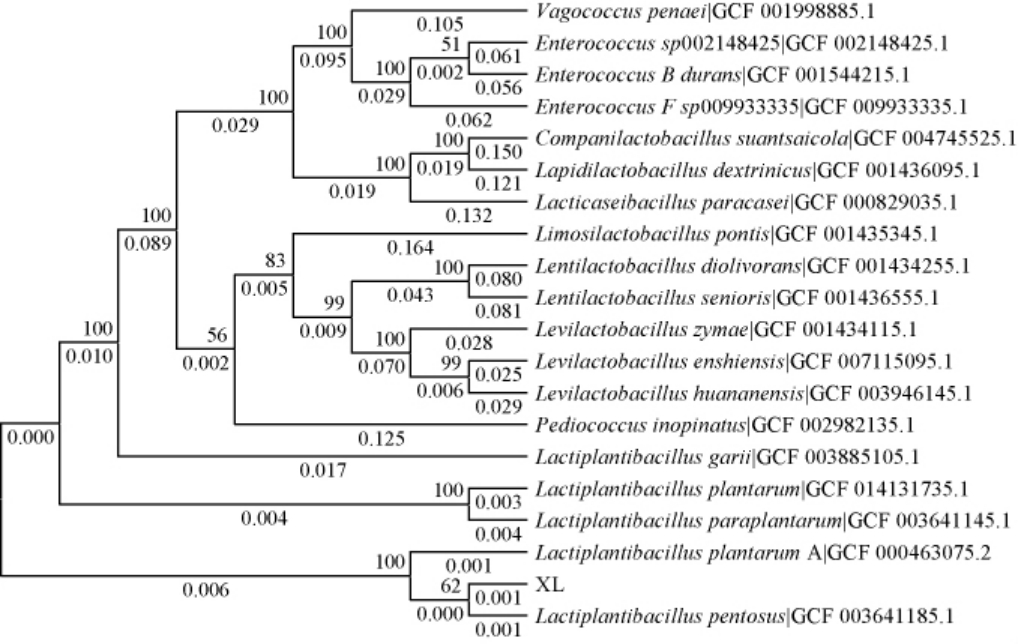
图3 基于16S rRNA基因序列的菌株XL系统发育树
Fig.3 Phylogenetic tree of strain XL based on 16S rRNA gene sequence
2.3 筛选菌株的生长特性和降解亚硝酸盐能力
L.pentosus XL在MRS液体培养基的生长曲线和产酸测定结果见图4A。由图4A可知,菌株XL在发酵初期(0~6 h)处于迟滞期,OD600nm值上升缓慢,pH维持在较高水平(5.35~6.08);随后进入对数生长期(6~30 h),菌体快速增长,OD600nm值迅速上升至(1.388±0.07);从30 h起,菌株XL进入生长稳定期,OD600nm值接近平稳,缓慢增加,并于45 h达到峰值(1.57±0.033);发酵48 h后,OD600nm值下降至(1.563±0.07),表明菌株XL开始进入衰亡期。整个发酵过程的pH值持续下降,由(6.08±0.106)下降至(3.65±0.07),表明菌株XL具有较强的产酸能力。进一步测定了菌株XL降解亚硝酸盐的能力,结果见图4B。由图4B可知,发酵液中NO-2-N含量在30 h内迅速下降后趋于稳定,于36 h降至(1.5±0.5)mg/L,降解率超过85%。这一过程中L.pentosus XL的OD600nm值持续上升,表明亚硝酸盐的降解与菌体生长密切相关,且未对其生长造成明显抑制。综上所述,L.pentosus XL具有良好的生长能力、产酸性能以及显著的亚硝酸盐降解能力,表明其在腌制类食品中具有提升安全性的潜在价值。
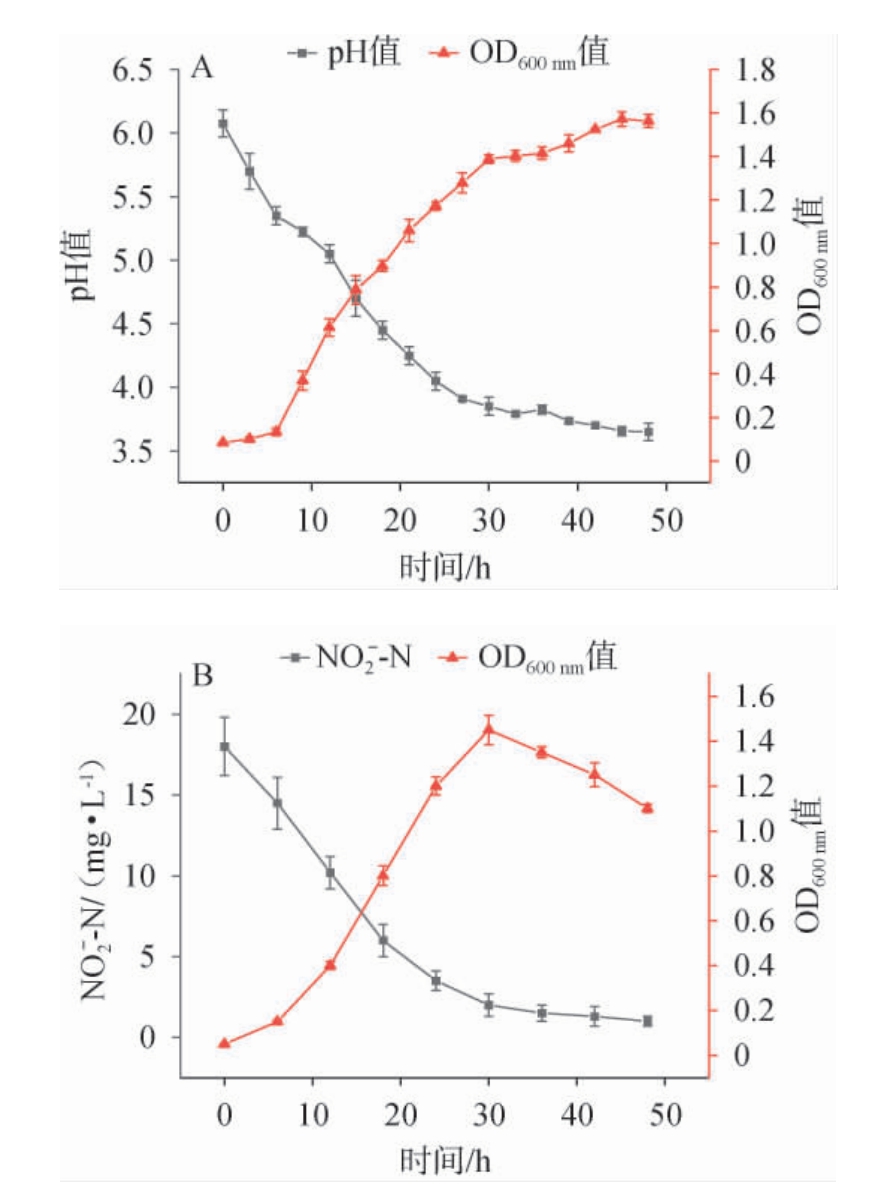
图4 戊糖乳植杆菌XL的生长曲线和产酸曲线(A)及亚硝酸盐降解曲线(B)
Fig.4 Growth curve and acid-producing curve (A),and nitrite degradation curve (B) of Lactiplantibacillus pentosus XL
2.4 筛选菌株的溶血性、自聚集和共聚集
溶血性测试是评估益生菌体外安全性的关键指标之一。根据菌落周围血液琼脂的变化情况,溶血反应可分为3类[22]:若菌落周围出现绿色或棕色环状区域,判定为α-溶血;若形成透明或浅黄色清晰圈,则为β-溶血,提示其具有较强的致病潜力;而若培养基未发生明显改变,则认为该菌株不具备溶血性,即γ-溶血。本研究中菌株XL的溶血情况见图5。由图5A可知,L.pentosus XL培养后其菌落边缘未观察到透明圈或变色现象,表明该菌株为γ-溶血型,不具溶血活性。
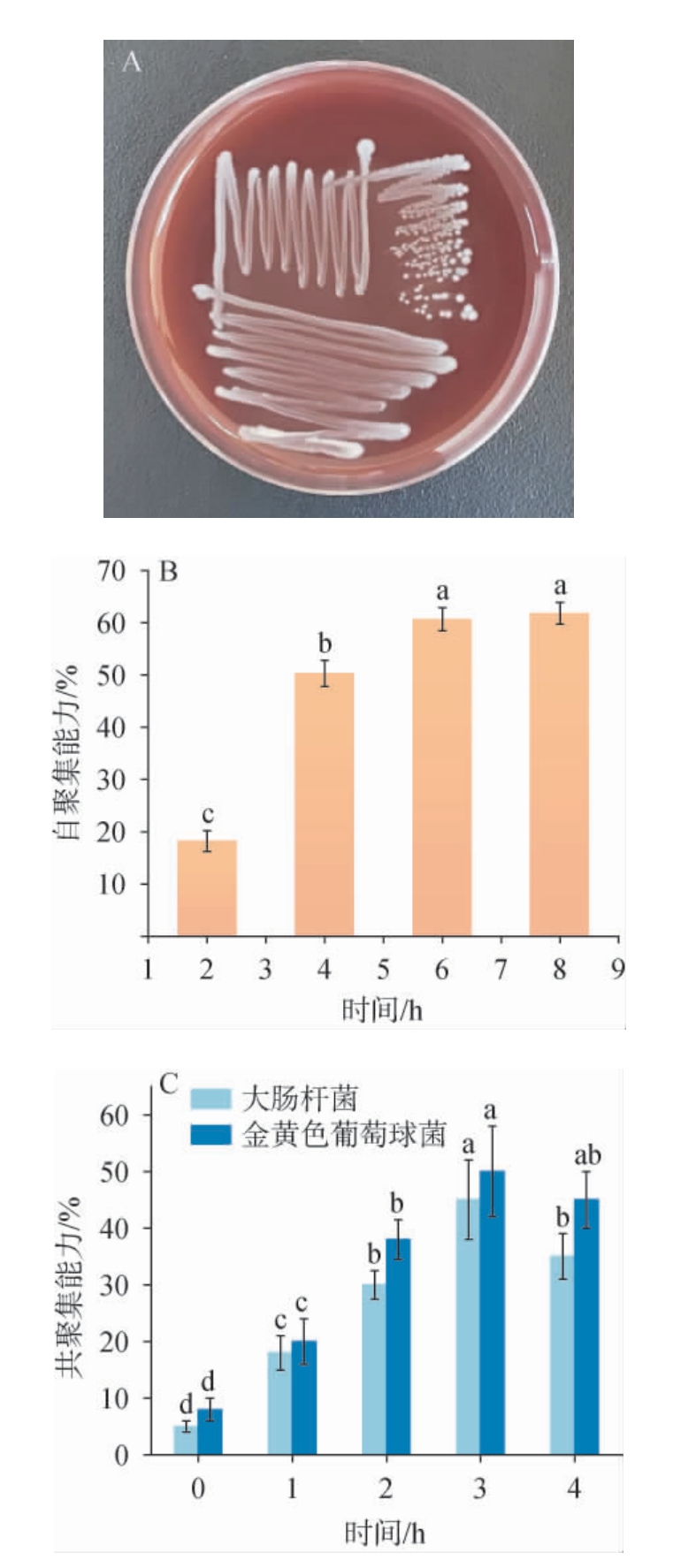
图5 戊糖乳植杆菌XL的溶血性(A)、自聚集率(B)及共聚集率(C)
Fig.5 Hemolysis (A),self-aggregation rate (B) and co-aggregation rate (C) of Lactiplantibacillus pentosus XL
同一指标不同字母表示差异显著(P<0.05)。下同。
由图5B可知,菌株XL的自聚集能力随时间推移呈现出显著的上升趋势。在培养初期(2 h),自聚集能力相对较低,仅为18.2%。随着培养时间的延长,菌体的自聚集能力迅速增强,在第4小时时达到50.3%,并在第6小时后趋于稳定,维持在60%左右。这表明,L.pentosus XL在生长过程中细胞表面的疏水性或电荷特性发生了变化,促进了细胞之间的相互聚集。在肠胃道中,这种聚集体有助于细菌在肠道黏膜表面的黏附,从而增强其定植能力[22]。此外,细胞聚集体还可以减少有害菌的黏附位点,竞争性地阻止病原体的定植,从而在维护肠道微生态平衡方面发挥重要作用[23]。可见,L.pentosus XL的自聚能力有助于其在肠胃环境中能够有效形成细胞聚集体。
由图5C可知,L.pentosus XL对致病菌大肠杆菌、金黄色葡萄球菌均表现出较强的共聚能力,且随着培养时间的延长逐渐增强。培养第3小时时,L.pentosus XL与大肠杆菌、金黄色葡萄球的共聚能力达到最高,分别为45%和50%。这表明菌株XL能够在肠胃环境中与潜在的病原体形成混合聚集体,从而有助于减少病原体在肠道中的数量并降低其致病性。值得注意的是,L.pentosus XL对金黄色葡萄球菌的共聚能力显著高于大肠杆菌,这可能与金黄色葡萄球菌表面的特定化学结构有关[24]。
2.5 菌株XL的耐酸与耐胆盐能力
为评估L.pentosus XL在胃肠环境中的适应能力,对其耐酸性及耐胆盐性进行测定,结果见图6。由图6A可知,菌株XL在pH 2的强酸条件下生长受到明显抑制,OD600nm值仅为(0.09±0.035)。然而在pH 3~7范围内,菌株XL生长情况逐渐改善,尤其在pH 6和pH 7条件下,菌体OD600nm值显著升高,表现出优良的生长性能。此外,菌株XL在pH 5条件下的生长曲线与中性条件相近,表明该菌株在弱酸性环境中仍能维持良好的活性,这一特性对于其通过胃部并进入肠道具有重要意义。由图6B可知,随着胆盐含量的升高,菌株XL的存活率逐渐下降。胆盐含量为1~2 g/L时,菌株XL仍表现出较强的耐受性,存活率为72.19%~98.79%。胆盐含量为3 g/L时,培养5 h菌体的存活率维持在65.39%。综上,菌株XL良好的耐酸与耐胆盐特性有助于其适应胃肠道酸性和胆盐环境[25-26]。
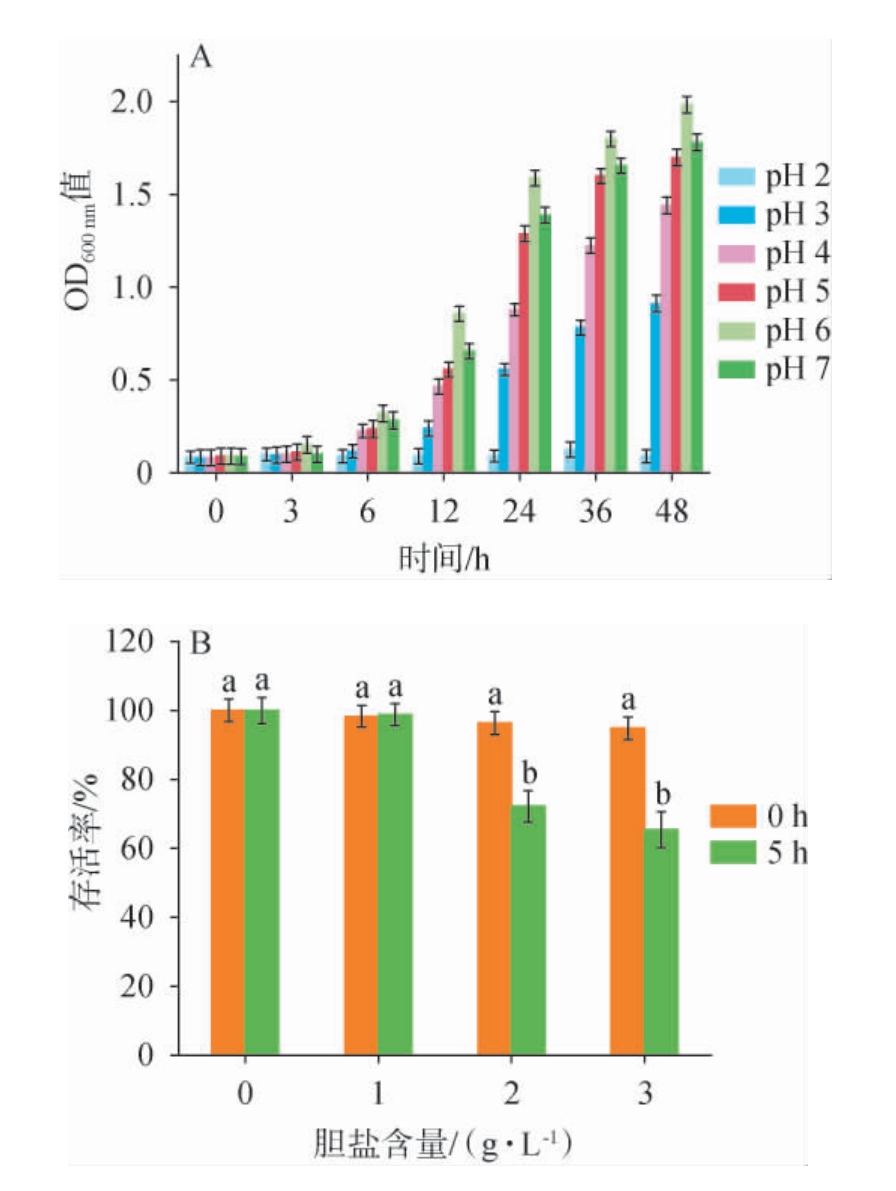
图6 戊糖乳植杆菌XL的耐酸能力(A)及耐胆盐能力(B)
Fig.6 Acid tolerance (A) and bile salt tolerance (B) of Lactiplantibacillus pentosus XL
2.6 菌株XL的抑菌能力
L.pentosus XL对大肠杆菌、金黄色葡萄球菌、沙门氏菌和单增李斯特菌等常见食源性致病菌的抑菌圈直径测定结果见表2。
表2 戊糖乳植杆菌XL对食源性致病菌的抑菌圈直径
Table 2 Inhibition zone diameter of Lactiplantibacillus pentosus XL against foodborne pathogenic bacteria

注:“+”表示抑菌圈直径为1~10 mm,“++”表示抑菌圈直径为10~20 mm,“+++”表示抑菌圈直径>20 mm。
由表2可知,L.pentosus XL对4株致病菌均表现出拮抗能力。与革兰氏阴性菌大肠杆菌和沙门氏菌相比,L.pentosus XL对革兰氏阳性菌金黄色葡萄球菌和单增李斯特菌的拮抗作用更为显著,这一结果与严梦涵等[27]报道的类似。推测其可能原因为L.pentosus XL代谢物更易破坏革兰氏阳性菌的肽聚糖层结构或干扰其胞内代谢过程,从而实现显著抑菌效果[27-28];而革兰氏阴性菌因其外膜中的脂多糖可形成对抗菌因子渗透的屏障,致使L.pentosus XL的抑菌效果相对较弱[29-30]。L.pentosus XL对食源性致病菌的广谱抑菌性能为其在食品防腐和生物保护剂开发中的应用提供了活性物质基础。
2.7 菌株XL发酵培养基优化
2.7.1 碳源及其添加量的优化结果
考察了葡萄糖、蔗糖、麦芽糖、果糖、糖蜜、可溶性淀粉和糊精等常见碳源对L.pentosus XL发酵特性的影响,结果见图7。由图7A可知,糖蜜作为碳源时对菌株XL的生长促进效果最显著,其培养液的OD600nm值达到(1.27±0.014),显著高于其他碳源组(P<0.05),这一现象可能归因于糖蜜本身所含的多种可发酵糖类(如蔗糖、葡萄糖、果糖)以及氨基酸、维生素、矿物质等多种营养成分,能为菌株提供更加全面和均衡的营养物质支持[31]。此外,糖蜜作为碳源时,菌液最终pH值也相对较低。因此,选用糖蜜作为L.pentosus XL发酵的最佳碳源。
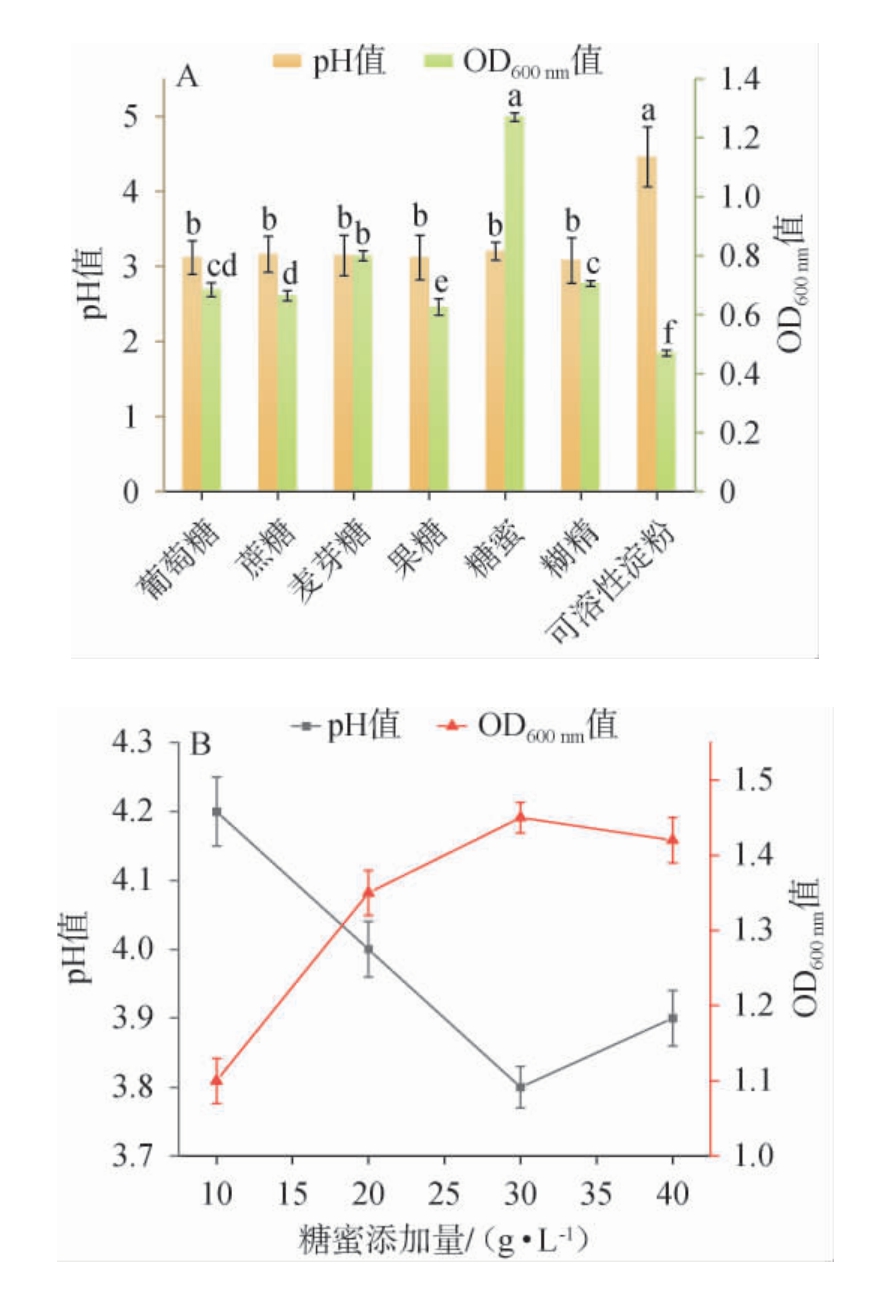
图7 碳源种类(A)及糖蜜添加量(B)对戊糖乳植杆菌XL生物量及产酸能力的影响
Fig.7 Effect of carbon source (A) and molasses addition (B) on biomass and acid-producing ability of Lactiplantibacillus pentosus XL
进一步考察糖蜜添加量对L.pentosus XL发酵特性的影响,结果见图7B。由图7B可知,随着糖蜜添加量由10 g/L增加至30 g/L,菌株XL的OD600nm值逐渐增加,菌液pH逐渐降低,说明营养利用效率较高;当糖蜜添加量为30 g/L时,菌株XL的OD600nm值达到最高,为(1.45±0.02),pH值降至最低,为(3.8±0.03);当糖蜜添加量由30 g/L增加至40 g/L时,菌株XL的OD600nm值逐渐下降,pH逐渐升高,推测可能是由于过高的糖浓度引发渗透压增加,进而对菌体生长产生一定抑制作用[32]。综合菌体量与发酵液pH值,选择糖蜜最佳添加量为30 g/L。
2.7.2 氮源及其添加量的优化结果
酵母膏、牛肉膏、蛋白胨、大豆蛋白胨以及硫酸铵等氮源对L.pentosus XL发酵特性的影响见图8。
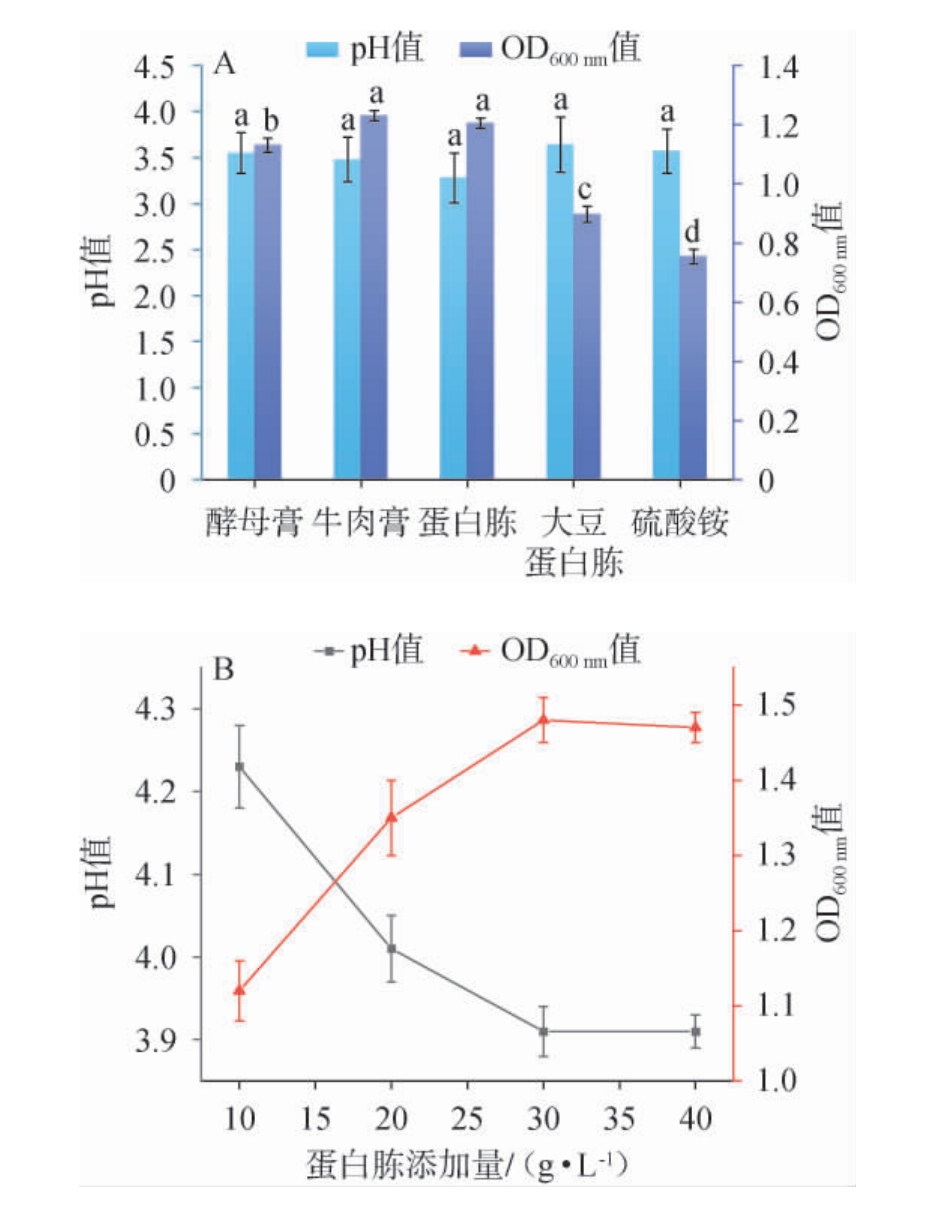
图8 氮源种类(A)及蛋白胨添加量(B)对戊糖乳植杆菌XL生物量及产酸能力的影响
Fig.8 Effect of nitrogen sources (A) and peptone addition (B) on biomass and acid-producing ability of Lactiplantibacillus pentosus XL
由图8A可知,对比其他氮源组,蛋白胨处理组pH值最低,为(3.28±0.27),表明蛋白胨更利于乳酸等酸性代谢物的生成与积累,因此选用蛋白胨作为L.pentosus XL发酵的最佳氮源。硫酸铵组的OD600nm值最低,提示其作为无机氮源对L.pentosus XL的增殖效果不理想,可能与其缺乏维生素、肽类和生长因子等复杂营养成分有关[33]。进一步考察了蛋白胨添加量对菌株XL发酵特性的影响。由图8B可知,随着蛋白胨添加量由10 g/L增加至30 g/L,菌株XL的OD600nm值逐渐增加,菌液pH逐渐降低;当蛋白胨添加量为30 g/L时,菌株XL的OD600nm值达到最高,为(1.48±0.03),pH值降至最低,为(3.91±0.03);当蛋白胨添加量由30 g/L增加至40 g/L时,菌株XL的OD600nm值逐渐下降,pH逐渐升高。综上,选择蛋白胨的最适添加量选为30 g/L。
2.7.3 微量元素及其添加量的优化结果
微量元素(钴离子、锰离子、锌离子、钼离子、钙离子、镁离子)对L.pentosus XL发酵特性的影响见图9。由图9A可知,除锌离子外,各微量元素相比于对照组均能促进菌株XL的菌体生长以及酸性物质积累,其中以锰离子最为显著,其培养液的OD600nm值最高且pH值最低,分别为(0.606±0.017)和(4.7±0.24)。说明锰离子对菌株XL的生长和产酸促进作用最强。张雅丽等[34-35]的研究同样表明,锰离子对于提升乳酸菌的发酵特性具有积极作用。因此,选用锰离子作为L.pentosus XL发酵的最佳微量元素。
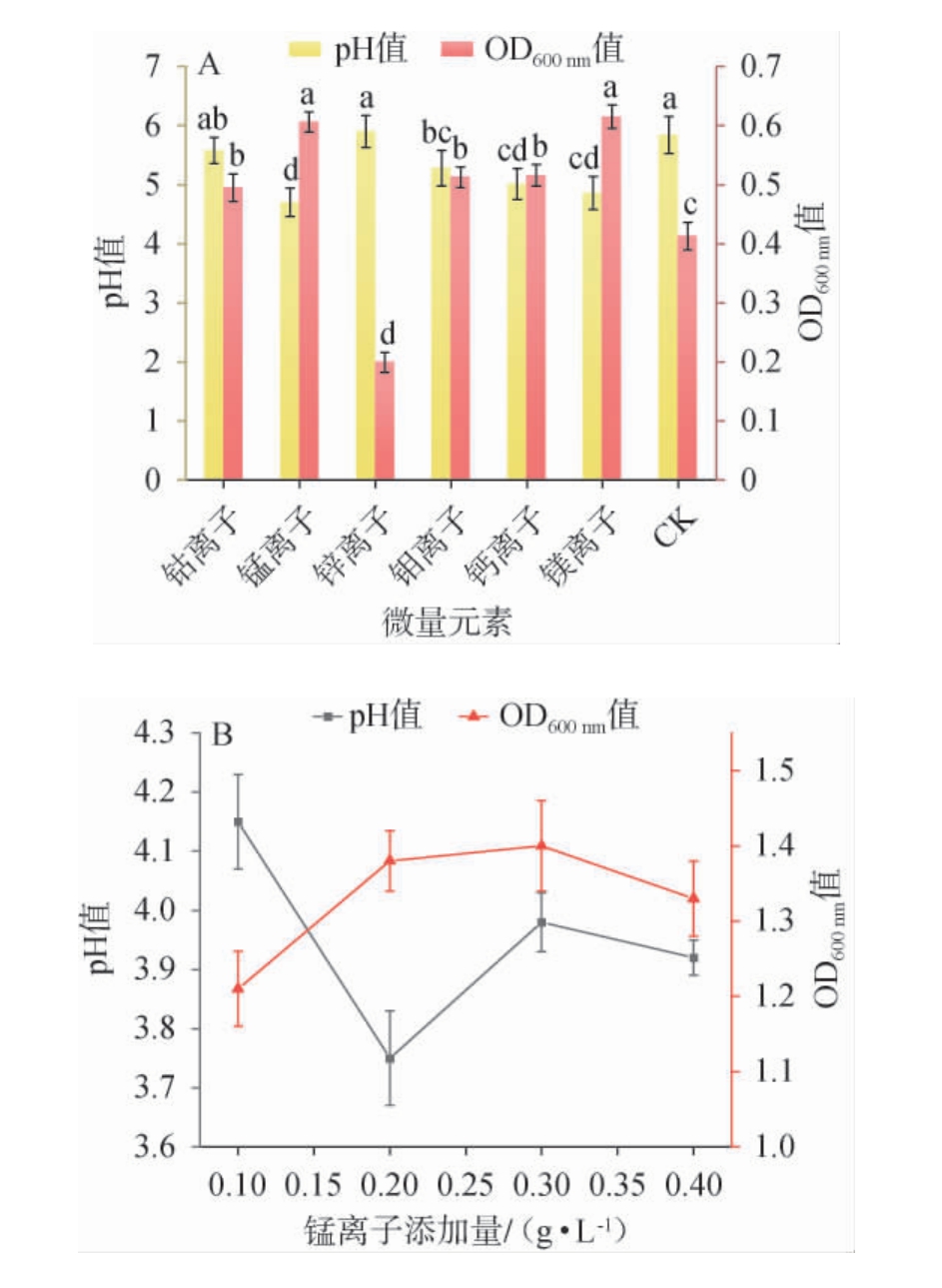
图9 微量元素种类(A)及锰离子添加量(B)对戊糖乳植杆菌XL生物量及产酸能力的影响
Fig.9 Effect of trace elements sources (A) and Mn2+addition (B) on biomass and acid-producing ability of Lactiplantibacillus pentosus XL
进一步考察了锰离子添加量对L.pentosus XL发酵特性的影响。由图9B可知,随着锰离子添加量从0.10 g/L增至0.20 g/L,菌体OD600nm值上升至(1.38±0.04)且发酵液pH值下降至最低,为(3.75±0.08),表明该添加量有利于菌株XL的菌体增殖与有机酸积累。当锰离子添加量进一步升高至0.30 g/L时,菌体OD600nm值虽稍有上升,但发酵液pH值明显升高至(3.98±0.05)。当锰离子添加量由0.30 g/L增加至0.40 g/L时,菌株XL的OD600nm值和pH均有所下降,推测高浓度锰离子可能对菌体XL产生毒性或干扰其正常代谢过程[35]。综上,选择锰离子的最适添加量为0.20 g/L。
2.7.4 响应面试验优化结果
根据上述单因素试验的结果,以糖蜜添加量(A)、蛋白胨添加量(B)、锰离子添加量(C)为试验因素,发酵液pH值(Y)作为考察指标,利用Design-Expert13.0软件设计3因素3水平的响应面试验,试验设计及结果见表3,方差分析结果见表4。
表3 发酵培养基配方优化响应面试验设计及结果
Table 3 Design and results of response surface test for fermentation medium formula optimization
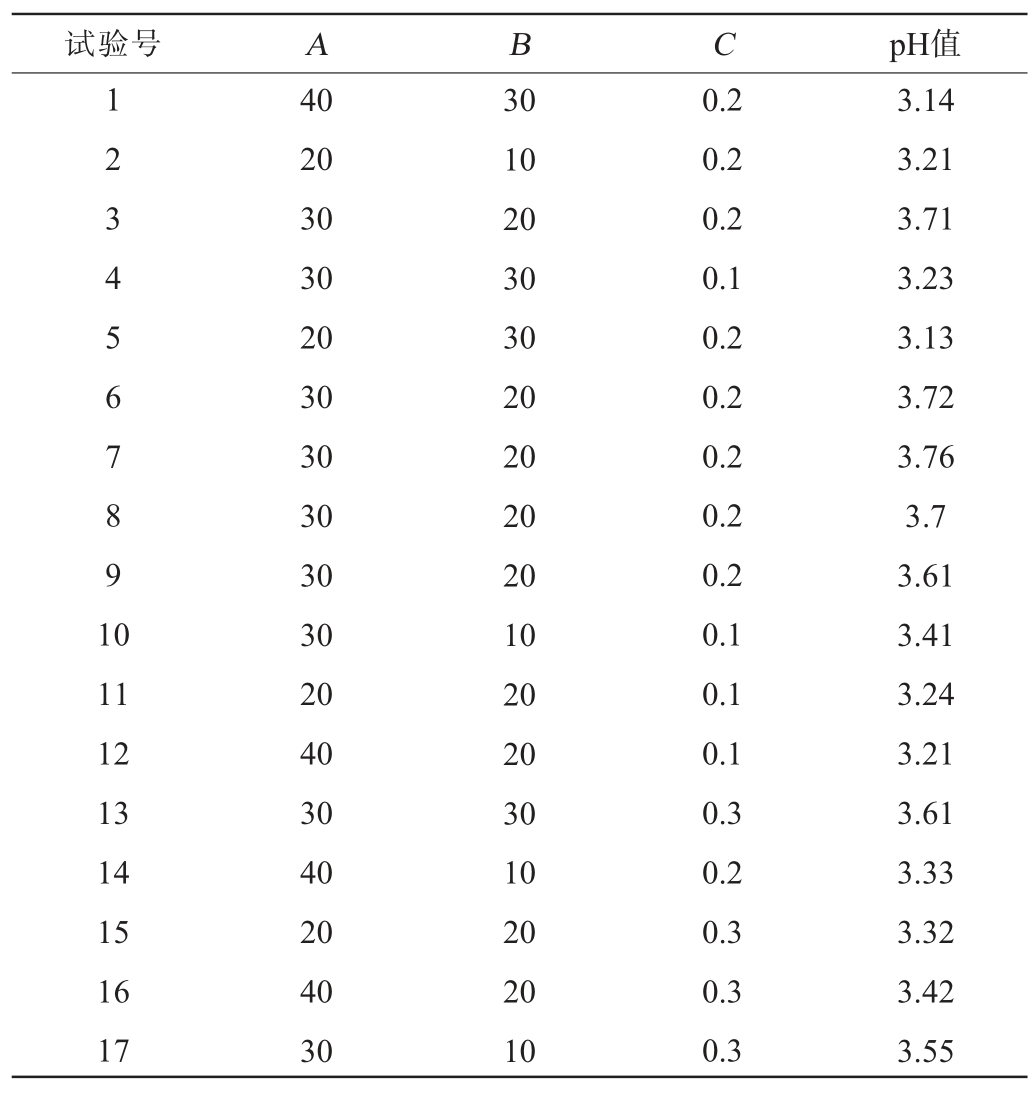
表4 回归模型方差分析
Table 4 Variance analysis of regression model
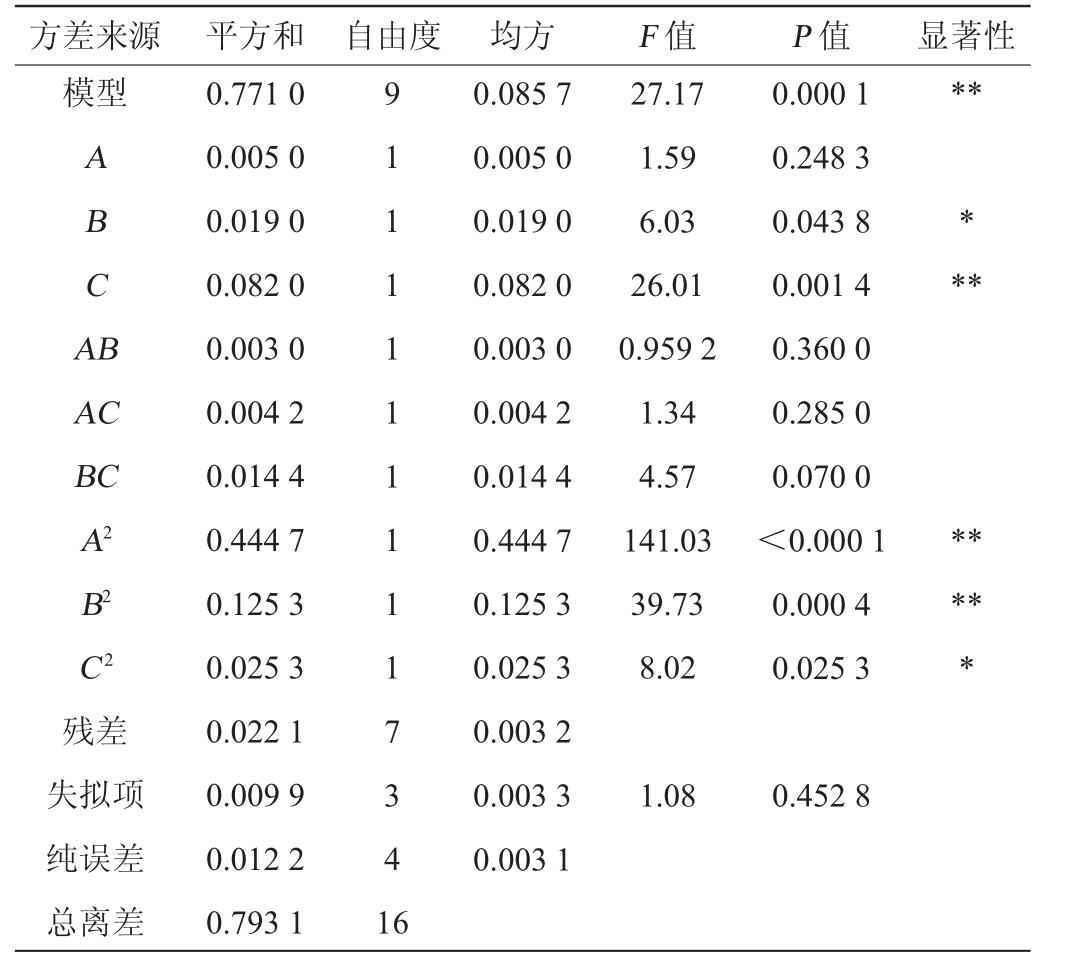
注:“**”代表对结果影响极显著(P<0.01),“*”代表对结果影响显著(P<0.05)。
利用Design-Expert13.0软件对试验数据进行了方差分析,并构建以pH值为响应值的二次回归模型。所得回归方程为:
由表4可知,该模型P值<0.001,呈极显著,而失拟项P值=0.452 8,不显著,回归模型决定系数R2为0.972 2,表明所建立模型可靠,能够准确反映各因素与响应值之间的关系。由P值可知,一次项C,二次项A2、B2对菌液pH值影响极显著(P<0.01),一次项B和二次项C2对菌液pH值影响显著(P<0.05),其余项对菌液pH值影响不显著(P>0.05)。由F值可知,各因素对菌液pH值影响大小顺序为锰离子添加量(C)>蛋白胨添加量(B)>糖蜜添加量(A)。
根据回归方程求导确定了戊糖乳植杆菌XL产酸的最佳发酵培养基配方为糖蜜添加量36.11 g/L,蛋白胨添加量29.90 g/L,锰离子添加量0.10 g/L,该条件下发酵液pH预测值为3.11。为便于实际操作,将各参数修正为糖蜜添加量36 g/L,蛋白胨添加量30 g/L,锰离子添加量0.1 g/L。在此优化条件下进行3次平行验证试验,所得发酵液pH实际值为(3.22±0.1),较优化前的pH值(3.65±0.07)降低了11.78%,且与预测值偏差较小。说明该二次回归模型拟合良好、解释力强,可为L.pentosus XL发酵条件的优化提供理论依据与参数支持。
3 结论
本研究成功从传统泡菜中分离获得一株具有良好应用潜力的优势乳酸菌株XL,经鉴定为戊糖乳植杆菌(Lactiplantibacillus pentosus)。其具有良好的产酸能力、耐酸耐胆盐性、较强的抑菌活性及亚硝酸盐降解能力。经单因素及响应面试验优化得到最佳发酵培养基配方为糖蜜添加量36 g/L,蛋白胨添加量30 g/L和锰离子添加量0.1 g/L,在该条件下发酵液pH值为(3.22±0.1),比优化前降低了11.78%。可见,L.pentosus XL表现出优异的发酵性能、益生功能及安全性,适合作为泡菜等传统发酵食品的功能菌株,并具备开发成直投式发酵剂的应用潜力。后续研究可进一步探索L.pentosus XL的代谢机制、保健功能及在不同食品体系中的适配性,以拓展其产业化应用价值。
[1] 王璐,蒋沙沙,李德海,等.乳酸菌对果蔬产品的抑菌机理及应用[J].中国食品学报,2024,24(2):432-441.
[2] 侯小艺,王建辉,邓娜,等.乳酸菌对发酵蔬菜风味影响研究进展[J].食品与机械,2023,39(4):232-240.
[3] 黄玉立,葛黎红,马思尧,等.乳酸菌与酵母菌互作对萝卜泡菜发酵进程及风味品质的影响[J].中国酿造,2024,43(4):197-202.
[4] 刘巧,罗强,张明,等.利用16S rDNA分析不同地区传统发酵泡菜的细菌多样性[J].食品与发酵工业,2020,46(22):91-97.
[5] KIM H D,SUH H J,CHUNG S H,et al.Sleep-enhancing activity of fermented pea protein hydrolysate with enhanced GABA content by Lactobacillusbrevis SYLB 0016 fermentation[J].J Sci Food Agr,2025,105(8):4297-4305.
[6] 谭仁芩,张曼君,周春丽,等.益生菌对发酵果蔬汁品质影响的研究进展[J].保鲜与加工,2025,25(2):121-133.
[7] 李瑞雪,于江傲,冉军舰,等.发酵果蔬汁功能特性及生物转化研究进展[J].中国酿造,2023,42(2):22-26.
[8] 刘振恒,阴耕云,肖冬,等.泡菜中乳酸菌的筛选鉴定及发酵工艺优化[J].食品与生物技术学报,2024,43(9):125-132.
[9] 史梅莓,伍亚龙,吕鹏军,等.不同乳酸菌接种发酵对泡白菜理化特征及风味的影响[J].食品与发酵工业,2024,50(1):80-88.
[10] 高倩妮,杜传来,邹小欠,等.芥菜加工过程冲味形成机制及其芥子苷酶特性研究[J].食品科技,2018,43(10):90-97.
[11] 邓金兰,李伟华,谢颖琦,等.水东芥菜矿物质元素含量测定及营养评价[J].农产品加工,2023,2023(5):57-60.
[12] 唐睿,邓放明,赵艳玲,等.腌制芥菜细菌多样性的分析及优势乳酸菌的筛选与鉴定[J].食品研究与开发,2023,44(15):168-174.
[13] 李子怡,王锋,赵玲艳,等.基于HS-SPME-GC-MS和多元统计学分析华容芥菜的特征挥发性风味成分[J].中国酿造,2024,43(3):234-242.
[14] 张馨月.干酪乳杆菌LCR 6013降解亚硝酸盐的途径及其亚硝酸盐还原酶的表征[D].广州:华南理工大学,2014.
[15] 杨时雨.乳酸菌发酵花生乳关键技术研究[D].南昌:南昌大学,2024.
[16] KIM H,KIM J S,KIM Y G,et al.Antioxidant and probiotic properties of Lactobacilli and Bifidobacteria of human origins[J].Biotech Biopro Eng,2020,25(3):421-430.
[17] LIN X N,XIA Y J,YANG Y J,et al.Probiotic characteristics of Lactobacillusplantarum AR113 and itsmolecular mechanism of antioxidant[J].LWT-Food Sci Techenol,2020,126:109278.
[18] LIU C,AN C,ZHANG J,et al.Evaluation of safety and probiotic properties of Weissella spp.in fermented vegetables from Xi'an,Shaanxi,China[J].Food Sci Nutr,2025,13(1):e4592.
[19] 李杰,李彦杰,史岩,等.短乳杆菌SLlac-18安全性评价及对高尿酸血症小鼠的益生作用[J].食品与发酵工业,2026,52(1):39-46.
[20] 廖凤平,李昆太,谭明辉,等.脂肽产生菌解淀粉芽孢杆菌HY2-1的发酵条件优化[J].中国酿造,2024,43(7):209-214.
[21] 周丽君,杨苗苗,魏春艳,等.唾液乳杆菌的抗氧胁迫能力及有氧发酵条件[J].食品与发酵工业,2020,46(22):98-105.
[22] ASCANTA P,HANGANU A,MARINAS I C,et al.Probiotic potential and exopolysaccharide characterization of two native lactic acid bacteria for functional applications[J].Food Biosci,2025,68:106600.
[23] 唐曼玉,王晚晴,强敬雯,等.益生菌与肠道菌群、免疫调节的相互作用与机制研究进展[J].食品工业科技,2022,43(16):486-493.
[24]汪宗林,陈建荣,尤忠毓,等.金黄色葡萄球菌生物被膜形成与耐药机制的研究进展[J].生物工程学报,2024,40(7):2038-2051.
[25] RAVINDHIRAN R,SUBRAMANIAN M,RAJALINGAM M,et al.Functional and biological characterization of Lactobacillus plantarum with isatin for use as probiotics for therapeutic options[J]. J Asian Nat Prod Res,2025,27(11):1673-1689.
[26] 汤凯,武运,王雪,等.伊犁地区奶疙瘩中乳酸菌的筛选及其特性研究[J].食品工业科技,2025,46(3):188-195.
[27] 严梦涵,许丽惠,游泽龙,等.乳酸菌素PlnJ第5位氨基酸(赖氨酸)定点突变对其热稳定性的影响[J].福建农林大学学报(自然科学版),2023,52(4):546-553.
[28] 喻冬秀,黎晓华,方梓烨,等.微波辅助离子液体提取余甘子总黄酮及生物活性分析[J].化学研究与应用,2025,37(4):928-937.
[29] 周倩婷,陈虹亮.沙眼衣原体在肠道定殖中的作用机制[J].中国人兽共患病学报,2023,39(4):390-396.
[30] ELSAADANY K,EISAYED A I M,AWAD S.Identification,safetyassessment,and antimicrobial characteristics of cocci lactic acid bacteria isolated from traditional Egyptian dairy products[J].Foods,2024,13(19):3059.
[31] 张菡,陈海军,龙晓宇,等.1株甜菜糖蜜源高产胞外多糖明串珠菌的分离鉴定、发酵工艺优化及抗氧化活性研究[J].轻工学报,2024,39(3):9-20.
[32] ABDEL-RAHMAN M A,HASSAN S E D,AZAB M S,et al.High improvement in lactic acid productivity by new alkaliphilic bacterium using repeated batch fermentation integrated with increased substrate concentration[J].Biomed Res Int,2019,2019(1):7212870.
[33] 衡利冰,夏永军,艾连中,等.植物乳杆菌AR307发酵培养基优化研究[J].工业微生物,2024,54(1):81-86.
[34] 张雅丽,钟华晨,顾悦,等.金属离子对发酵粘液乳杆菌733信号分子AI-2及生物膜的影响[J].中国食品学报,2025,25(3):51-63.
[35] 程新,董英,李昆太.基于iTRAQ技术研究锰离子缺乏对植物乳杆菌的影响[J].中国食品学报,2020,20(9):203-211.