产香微生物是指能够产生具有香味物质的微生物,这些微生物在代谢过程中可以合成各种芳香化合物[1]。产香微生物在多个领域有着广泛应用,常见的产香微生物(如某些酵母菌、乳酸菌等)在发酵食品的生产过程中发挥着重要作用,能赋予食品独特的风味[2-3]。在食品工业中,酿酒时产香微生物可使酒散发迷人香气;制作面包、酸奶时可增添独特风味;在调味品生产方面,产香微生物可协同生产出香味浓郁的酱油、醋等;香料香精行业也得益于它们,通过产香微生物发酵生产天然香料;甚至在烟草行业,产香微生物能提升烟草的香气品质[4];此外,在一些传统发酵食品如奶酪、腐乳等的制作中[5-6],产香微生物更是不可或缺,赋予食品丰富且诱人的味道,为人们的生活增添多样的味觉享受。
利用微生物发酵是获取绿色香气化合物的一种重要途径。如刘小改等[7]从清香型大曲中分离出一株产香细菌并将其应用在麸曲白酒酿造中,发酵酒样中的丁酸乙酯、β-苯乙醇,苯乙醛含量有明显提高。张鹏等[8-9]从烟叶中筛选出一株产果香真菌,并将其应用在烟叶发酵中,其可有效改善烟丝的协调性、香气和余味。周森等[10]从牛栏山酒厂菌库中筛选出一株白地霉,发现其代谢产物为乙酸乙酯,乙酸和一些高级醇,与牛栏山白酒中特征风味物质一致。袁英豪等[11]从以醋醅和醋曲中分离得到一株具有产酯能力的异常威克汉姆酵母,通过产酯工艺优化后其产总酯量达到4.03 g/L。FAN G S等[12]从大曲中分离得到一株高产乙酸乙酯的酵母菌株Y3604,通过产酯条件优化后,其酯产量高达16.92 g/L,该菌株具有显著提高乙酸乙酯含量和增强产品香气特性的潜力。陈嘉等[13]从传统发酵工艺的酒醅中分离筛选得到产酯酵母菌Y14,并将其与大曲混合发酵,发现酿制的山西老陈醋中的总酯含量比对照组提高40.5%,乙酸乙酯含量提高1.3倍。
该研究以绍兴市富盛乡多年生竹林土壤为研究对象,从土壤中分离筛选产酯微生物,以感官闻香实验结果和产酯量为依据,获得了一株具有良好产酯能力的白地霉菌株,旨在为产香微生物在发酵食品香气物质的提升提供微生物来源。
1 材料与方法
1.1 材料与试剂
1.1.1 材料
土壤样品:绍兴市富盛多年生竹林土壤。
1.1.2 试剂
葡萄糖、果糖、乳糖、半乳糖(均为分析纯):天津市试剂材料一厂;蔗糖、麦芽糖、硫酸铵、磷酸二氢钾、磷酸氢二钾、硫酸锰、硫酸镁、硫酸铜、硫酸锌(均为分析纯):天津津东天正精细化学试剂厂;OXOID蛋白胨、OXOID酵母粉(均为生化试剂):赛默飞世尔科技公司;FP318蛋白胨、FP328蛋白胨、FM902酵母粉、FM305酵母粉(均为生化试剂):安琪酵母股份有限公司。
1.1.3 培养基
酵母浸出粉胨葡萄糖(yeast extract peptone dextrose,YEPD)液体培养基:葡萄糖2%,酵母粉1%,蛋白胨2%,pH 6.0,115 ℃灭菌20 min。
YEPD固体培养基:YEPD液体培养基+2%琼脂,115 ℃灭菌20 min。
生理生化鉴定所用培养基:参考《酵母菌的特征与鉴定手册》[14]。
1.2 仪器与设备
752紫外可见分光光度计:天津市华伟科技有限公司;AELTA320 pH计:梅特勒仪器(上海)有限公司;HYG恒温培养振荡器:上海欣蕊自动化设备有限公司;Sorvall ST 8R冷冻高速离心机:赛默飞世尔科技(中国)有限公司;5977C-8890气相色谱-质谱联用(gas chromatography-mass spectrometry,GC-MS)仪:安捷伦科技有限公司。
1.3 实验方法
1.3.1 菌株分离及筛选
称量10 g土壤样品于250 mL锥形瓶中,加30 mL无菌生理盐水后在30 ℃、180 r/min条件下振荡培养24 h,再按10-4,10-5,10-6稀释梯度涂布于含有100 mg/L氯霉素的YEPD琼脂平板中,每个稀释度涂布于2个琼脂平板,在30 ℃条件下恒温培养,选择酵母菌菌落特征明显的单菌落,进一步划线2~3次,获得纯菌落。
将9株疑似酵母的菌株接种到YEPD琼脂平板上,在30 ℃条件培养60 h,挑取平板上菌落直径较大的单菌落到YEPD液体培养基中,在30 ℃、180 r/min条件下培养24 h,并进一步通过感官评价比较其香气特征。最终通过嗅闻法筛选出一株在固体与液体YEPD培养中均能产生浓郁果香味的菌株。
1.3.2 菌株的鉴定
1.3.2.1 形态学鉴定
挑取筛选菌株接种到YEPD琼脂平板上,在30 ℃条件下恒温培养60 h观察其菌落形态。挑取平板上菌落直径较大的单菌落到YEPD液体培养基中,在30 ℃、180 r/min条件下培养24 h,在光学显微镜(10×40倍)下观察细胞形态和菌丝形态。
1.3.2.2 生理生化鉴定
参照《酵母菌的特征与鉴定手册》[14],对菌株进行糖发酵实验、碳源同化实验、尿素水解实验和产类淀粉化合物实验。
1.3.2.3 分子生物学鉴定
将菌株单菌落接到YEPD液体培养基中,30℃、180r/min条件下培养12 h后取1 mL于2 mL EP管中,采用煮沸法提取菌株脱氧核糖核酸(deoxyribonucleic acid,DNA)作为模板。用真菌18S rDNA通用引物NS1(GTAGTCATATGCTTGTCTC)和NS8(TCCGCAGGTTCACCTACGGA)组合,聚合酶链式反应(polymerase chain reaction,PCR)扩增18S rDNA区。PCR扩增体系:ddH2O 21 μL,菌株DNA 1 μL,引物NS1 1.5 μL,引物NS8 1.5 μL,PrimeSTAR Max 25 μL。PCR扩增条件为:95 ℃预变性5 min;95 ℃变性30 s;55 ℃退火30 s,72 ℃延伸30 s;35个循环;72 ℃延伸10 min。扩增后的PCR产物送至金唯智生物科技有限公司进行测序。测序得到的序列用美国国家生物技术信息中心数据库(National Center for Biotechnology Information,NCBI)数据库进行同源序列搜索。对搜索后的结果采用MEGA7软件邻接法(neighbor-joining,NJ)构建系统发育树。
Max 25 μL。PCR扩增条件为:95 ℃预变性5 min;95 ℃变性30 s;55 ℃退火30 s,72 ℃延伸30 s;35个循环;72 ℃延伸10 min。扩增后的PCR产物送至金唯智生物科技有限公司进行测序。测序得到的序列用美国国家生物技术信息中心数据库(National Center for Biotechnology Information,NCBI)数据库进行同源序列搜索。对搜索后的结果采用MEGA7软件邻接法(neighbor-joining,NJ)构建系统发育树。
1.3.3 菌株产酯曲线测定
将活化后的菌株种子液以2%接种量接到YEPD培养基中,25 ℃、180 r/min条件下进行发酵,每隔12 h测定其总酯含量,绘制总酯含量-发酵时间曲线。
1.3.4 菌株产酯条件优化单因素试验
以YEPD培养基为基础产酯发酵培养基,总酯含量为考察指标,通过改变单一变量,考察不同葡萄糖添加量(20g/L、35 g/L、50 g/L、65 g/L、80 g/L、95 g/L),有机氮源种类(OXOID蛋白胨、OXOID酵母粉、FP318蛋白胨、FP328蛋白胨、FM902酵母粉、FM305酵母粉),有机氮源添加量(5 g/L、10 g/L、15 g/L、20 g/L、25 g/L、30 g/L),无机氮源种类(硫酸铵、氯化铵、磷酸二铵、硝酸钠),无机氮源添加量(0.1 g/L、0.2 g/L、0.4 g/L、0.6 g/L、0.8 g/L、1.0 g/L、1.2 g/L),无机盐种类(磷酸二氢钾、磷酸氢二钾、硫酸锰、硫酸镁、硫酸铜、硫酸锌),无机盐添加量(0.01 g/L、0.015 g/L、0.02 g/L、0.025 g/L、0.03 g/L、0.035 g/L、0.04 g/L),不同接种量(2%、4%、6%、8%、10%),不同初始pH(4.5、5.0、5.5、6.0、6.5、7.0、8.0),在发酵温度25 ℃、180 r/min条件下发酵30 h,探究各因素对总酯含量的影响[14]。
1.3.5 菌株产酯条件优化响应面试验
在单因素试验的基础上,选择葡萄糖添加量(A)、蛋白胨添加量(B)、硫酸铵添加量(C)和初始pH(D)为考察因素,以总酯产量为考察指标,设计4因素3水平响应面试验,考察各因素交互作用对总酯产量的影响。响应面试验因素与水平见表1。
表1 菌株产酯条件优化响应面试验因素与水平
Table 1 Factors and levels of response surface experiments for ester-producing conditions optimization of the strain

1.3.6 总酯含量的测定
采用氢氧化钠皂化反应法进行测定。发酵液经7000r/min离心10min,取5mL发酵液上清液于三角瓶中,加入0.1 mol/L的氢氧化钠标准溶液,在70 ℃水浴条件下进行冷凝回流反应60 min后冷却至室温,使用0.1 mol/L的盐酸滴定至无色且保持30 s不变色。总酯含量计算公式如下:
式中:X为总酯含量,g/L;C1为氢氧化钠物质的量浓度,0.1mol/L;V为添加氢氧化钠体积,10 mL;C2为盐酸物质的量浓度,0.1 mol/L;V1为滴定消耗盐酸体积,mL;V0为空白消耗盐酸体积,mL;Vs为取样体积,mL。
1.3.7 挥发性香气物质测定
采用GC-MS法进行测定。
样品前处理:使用最优产酯培养基在25 ℃、180 r/min条件下发酵30 h,发酵液经8 000 r/min离心5 min后取上清液5 mL于20 mL顶空瓶中,装上提前老化后的吸附笔TCBXN(适用沸点-60~450℃),抽真空,在60 ℃、200r/min条件下平衡45 min后进样检测。
GC条件:FFAP色谱柱(60 m,320 μm×0.5 μm),进样口温度260 ℃,载气为高纯氦气(纯度≥99.999%),流速1 mL/min,不分流进样。升温程序:40 ℃保持5 min,1.5 ℃/min升温至55 ℃,保持1 min;再以2 ℃/min升温至75 ℃,保持2 min;再以4 ℃/min升温至125 ℃,保持2.5 min;再以5 ℃/min升温至190 ℃,保持2 min。
MS条件:离子源温度230 ℃,四极杆温度150 ℃,扫描范围40~400 amu,溶剂延迟时间2 min。
定性定量分析:对GC-MS检测得到的质谱图,通过计算机检索并与美国国家标准与技术研究院(National Institute of Standards and Technology,NIST)标准质谱库中的标准质谱图进行比对,仅保留匹配度>80%的鉴定结果。采用峰面积归一化法进行半定量分析。
1.3.8 数据分析
所有试验均设置至少3次重复(n≥3),结果以“平均值±标准差”表示。采用Origin 2024进行基础数据整理与绘图。采用Design-Expert V8.0.6进行响应面试验设计及数据分析。通过该软件的方差分析功能评估实验模型中各因素的显著性,并以P<0.05作为显著性判断标准。
2 结果与分析
2.1 菌株分离鉴定
2.1.1 菌株的分离筛选
土壤样品经过富集后,初筛得到9株具有酵母形态特征的菌株,将9株菌纯化后分别点种于YEPD固体培养基并置于30 ℃条件下恒温培养36~48 h,通过感官闻香法进行复筛,记录香气特征。基于香气浓郁度与持久性,将筛选出的3株菌接种于YEPD液体培养基中,于30 ℃、180 r/min振荡培养24~36 h后,再次进行感官闻香。最终获得1株在固体及液体YEPD培养基中均能产生浓郁且持久果香的菌株,命名为Y3,并进行甘油管保藏以用于后续研究。
2.1.2 菌株的形态学鉴定
菌株Y3在YEPD固体培养基中的菌落形态和经过染色后的菌体在显微镜(10×40倍)下观察,菌落形态和菌体显微观察结果见图1。由图1A可知,菌落成圆形,边缘光滑,表面干燥,白色毛绒状,菌苔较厚,菌落中间突起向外周环状扩散,边缘可见细小绒毛样菌丝。由图1B可知,菌体细胞呈棒状,细胞大小为(2~6)×(1~2)μm,有粗且长的菌丝生成,符合酵母菌的形态特征。
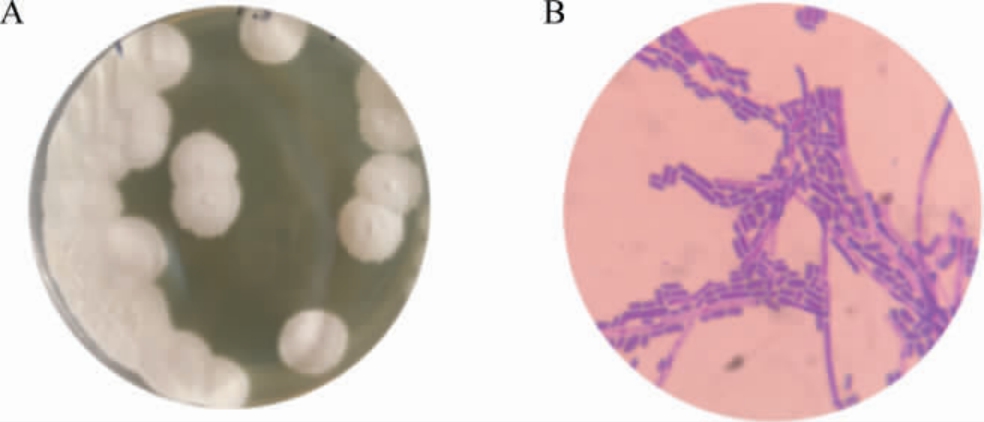
图1 菌株Y3在YEPD培养基中的菌落形态(A)和菌体形态(B)
Fig.1 Colony morphology (A) and cell morphology (B) of strain Y3 in YEPD medium
2.1.3 菌株的Y3生理生化鉴定
菌株Y3的生理生化鉴定结果见表2。由表2可知,菌株Y3只能利用单糖,不能发酵二糖,可发酵D-葡萄糖和D-果糖产酸产气,能同化木糖、甘露醇和山梨醇。产类淀粉化合物实验和尿素水解实验均为阴性。通过对菌株Y3形态观察和生理生化鉴定,初步鉴定为白地霉。
表2 菌株Y3生理生化试验结果
Table 2 Physiological and biochemical test results of strain Y3
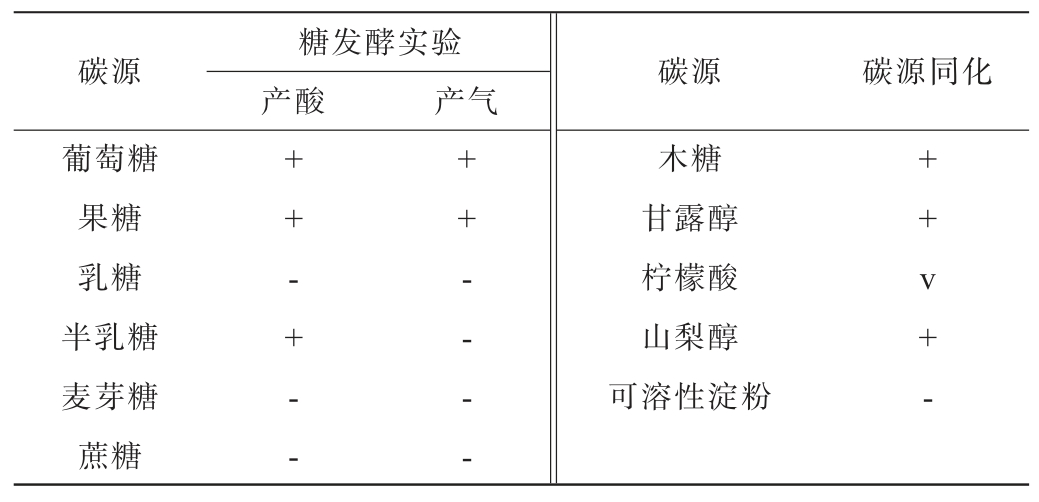
注:(+)为阳性反应,(-)为阴性反应,(v)为可变反应。
2.1.4 菌株分子生物学鉴定
以酵母18SrDNA通用引物克隆菌株Y3相应DNA片段,将PCR产物进行送测,得到一段1 070 bp的序列,将该序列在NCBI官网进行基本局部比对算法的搜索工具(basic local alignment search tool,BLAST)比对,将相似度高于98%的同源序列使用MEGA7软件的邻接法构建系统发育树,结果见图2。由图2可知,菌株Y3与地霉属白地霉(Geotrichum candidum)ON935473在一个分支上,表明与白地霉亲缘关系最近。综合Y3菌株菌落特征、细胞形态、生理生化鉴定结果和分子生物学鉴定结果,确定菌株Y3为白地霉(G.candidum)。
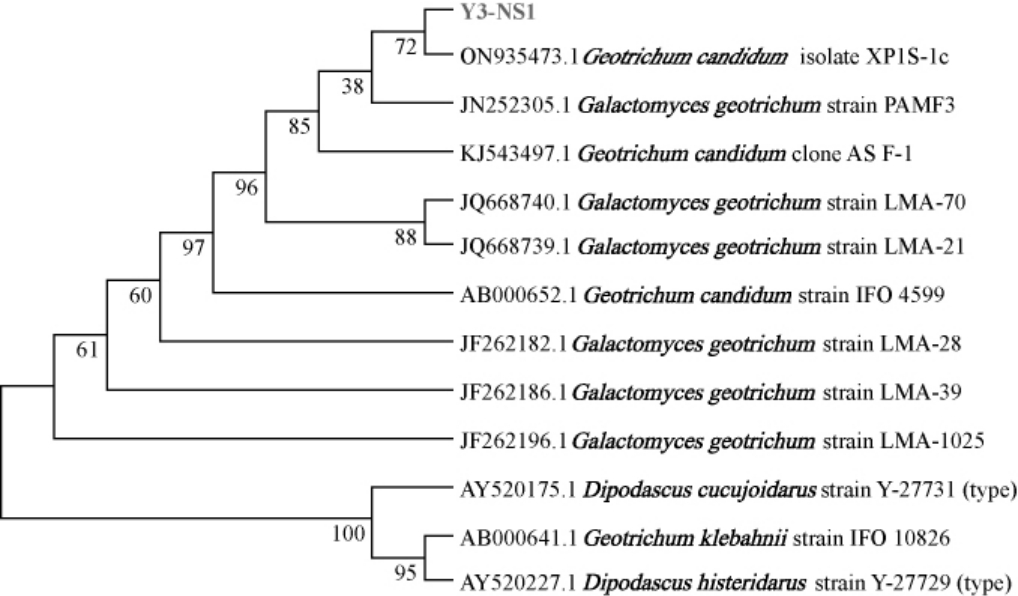
图2 基于18S rDNA基因序列菌株Y3的系统发育树
Fig.2 Phylogenetic tree of strain Y3 based on 18S rDNA gene sequence
2.2 菌株Y3产酯能力分析
根据贾丽艳等[16]的研究,白地霉发酵的总酯含量会随着发酵时间呈现先升高后降低的趋势。本研究中菌株Y3在YEPD培养基中的生长曲线和产酯量随时间的变化情况见图3。由图3可知,菌株Y3的生长过程可分为延滞期、对数生长期、稳定生长期及衰亡期4个阶段,其中0~8 h为延滞期,此阶段OD600nm增长缓慢,菌体处于环境适应阶段,产酯量也极低;8~24 h为对数生长期,OD600nm快速上升,菌体大量增殖,产酯量随菌体生长同步显著增加,表明菌体生长为产酯代谢提供了充足的生物基础;24~30 h接近稳定生长期,OD600nm增长速率放缓并逐渐趋于平稳,而产酯量在此阶段达到最高值(1.84 g/L);30 h后进入衰亡期,OD600nm虽仍有小幅上升(可能与菌体自溶等因素有关),但产酯量开始下降,发酵液中营养成分和pH降低,菌体开始衰老,同时菌体内相关酶对酯类的分解增强所导致[17]。
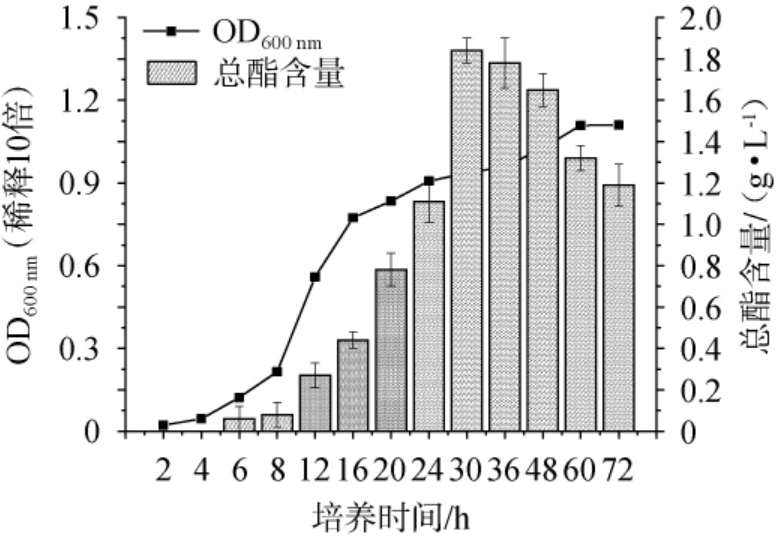
图3 菌株Y3生长曲线和产酯能力分析
Fig.3 Growth curve and ester production capacity analysis of strain Y3
2.3 菌株Y3产酯条件优化单因素试验
2.3.1 葡萄糖添加量对总酯含量的影响
葡萄糖添加量对总酯含量的影响见图4。由图4可知,随着葡萄糖添加量的提高,总酯含量逐渐增大,当葡萄糖添加量为50 g/L时总酯含量达到3.104 g/L,当葡萄糖添加量高于50 g/L时总酯含量逐渐降低。葡萄糖参与菌体生长和乙醇的生成,乙醇是酯类必不可少的前体物质,但是葡萄糖添加量增加导致发酵液渗透压变大,抑制菌体生长[18-19]。因此,最佳葡萄糖添加量为50 g/L。
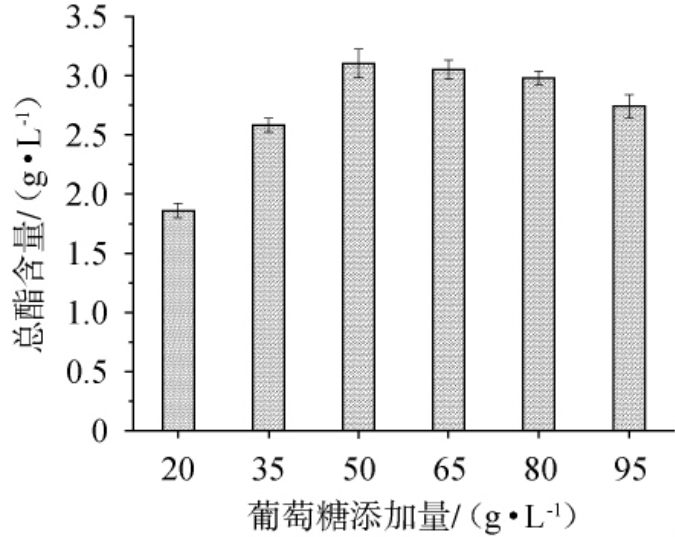
图4 葡萄糖添加量对总酯含量的影响
Fig.4 Effect of glucose addition on total ester content
2.3.2 有机氮源对总酯含量的影响
在50 g/L葡萄糖为培养基碳源的基础上,不同有机氮源对总酯含量的影响见图5。由图5A可知,当使用OXOID蛋白胨为唯一氮源时总酯含量最高达到8.46 g/L,明显高于其他来源的蛋白胨,因此,选择OXOID蛋白胨为最适有机氮源并考察其添加量对总酯含量的影响。由图5B可知,随着OXOID蛋白胨添加量的增大,总酯量表现出缓慢升高再降低的趋势,当蛋白胨添加量为20 g/L时总酯量达到最大值,为8.88 g/L。因此,最适有机氮源为20 g/L OXOID蛋白胨。
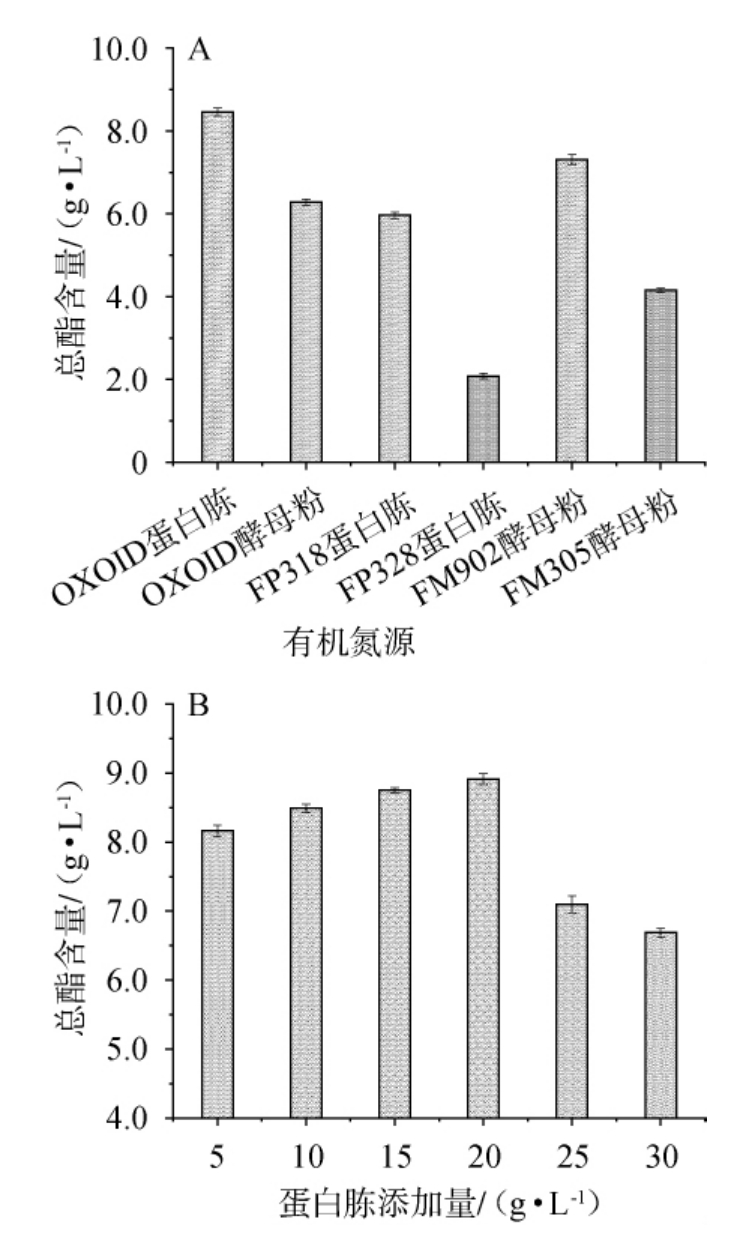
图5 有机氮源种类(A)及蛋白胨添加量(B)对总酯含量的影响
Fig.5 Effect of organic nitrogen sources types (A) and peptone addition (B) on total ester content
2.3.3 无机氮源对总酯含量的影响
不同无机氮源(添加量0.5%)对总酯含量的影响结果见图6。由图6A可知,添加硫酸铵时总酯含量最高达到9.47 g/L,明显高于另外3种无机氮源,因此,实验进一步探究硫酸铵添加量对总酯含量的影响;由图6B可知,总酯含量随硫酸铵添加量的变化呈现先升高后降低的趋势,当硫酸铵添加量为0.2 g/L时,总酯含量达到最高值(10.19 g/L),较未添加硫酸铵的优化基础培养基产酯量(3.104 g/L)有显著提升,这可能是由于在富营养培养基中,微量硫酸铵对产酯代谢的关键酶系合成起到了重要的协同促进作用;当添加量继续升高时,总酯含量均有所下降。综上,最适硫酸铵添加量为0.2 g/L。
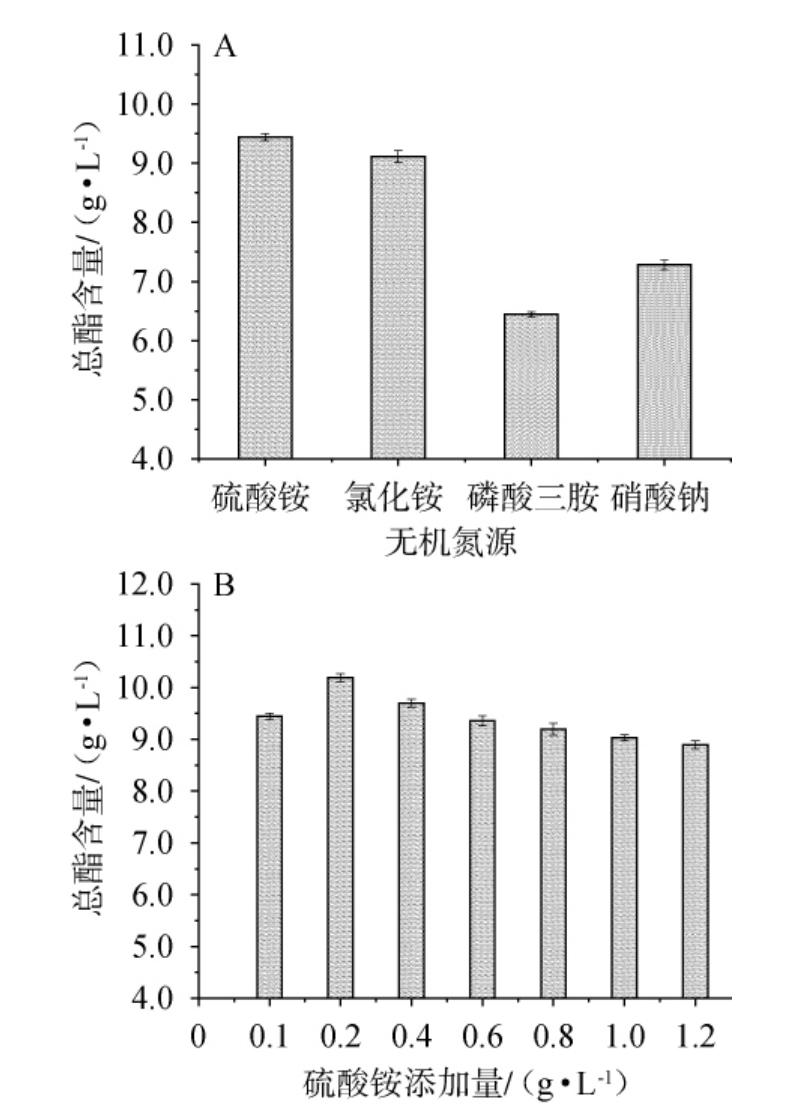
图6 无机氮源种类(A)及硫酸铵添加量(B)对总酯含量的影响
Fig.6 Effect of inorganic nitrogen sources types (A) and ammonium sulphate addition (B) on total ester content
2.3.4 不同无机盐对总酯含量的影响
适量的无机盐能够促进酯类的代谢合成[20],该研究针对不同无机盐对总酯含量的影响进行分析,结果见图7。
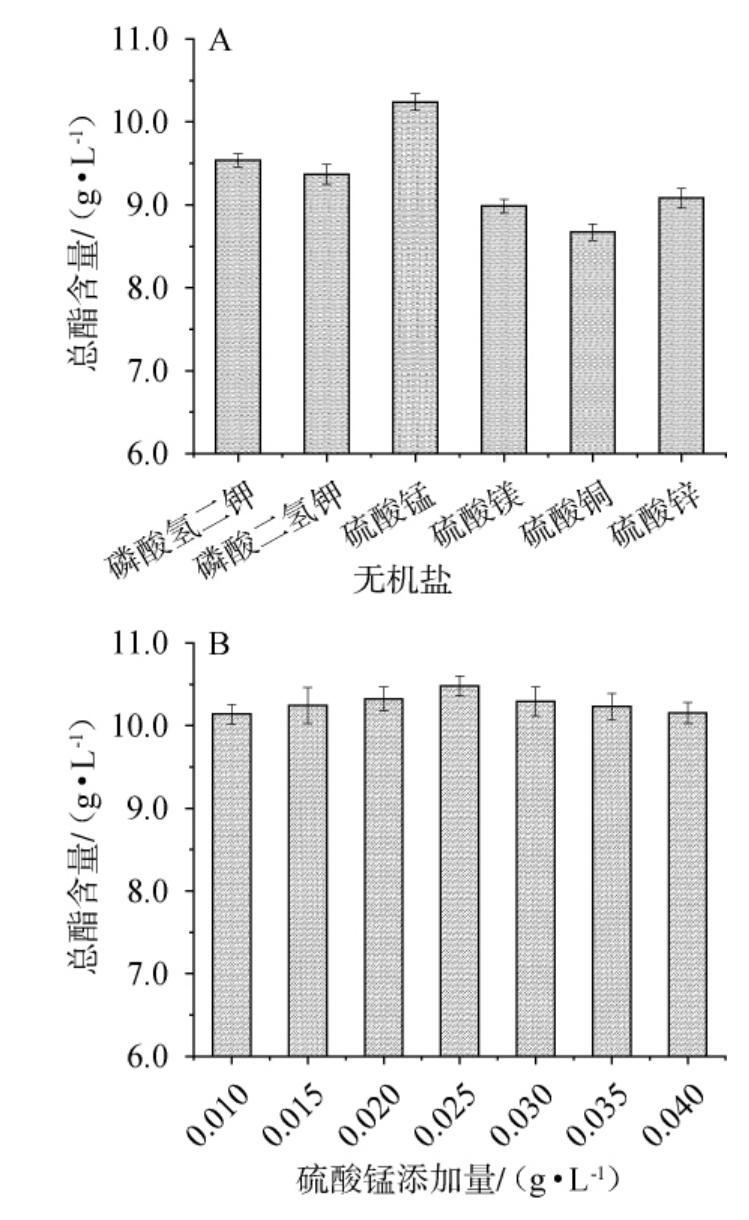
图7 无机盐种类(A)及硫酸锰添加量(B)对总酯含量的影响
Fig.7 Effect of inorganic salts types (A) and manganese sulphate addition (B) on total ester content
由图7A可知,当以硫酸锰为无机盐时,总酯含量最高,达到了10.16 g/L,显著优于其他无机盐。基于该结果进一步探了硫酸锰添加量对总酯含量的影响。由图7B可知,在硫酸锰添加量低于0.025 g/L时,总酯含量随硫酸锰添加量升高而逐渐上升,当硫酸锰添加量为0.025 g/L时总酯含量达到最高值(10.48 g/L);当硫酸锰添加量继续升高时,总酯含量出现下降,推测是过量的锰离子抑制了酯化酶酶活性所致;因此最适无机盐及添加量为0.025 g/L硫酸锰。
2.3.5 接种量对总酯含量的影响
根据梁磊等[21]的研究,在白地霉发酵产乙醇的实验中,较高的接种量对发酵可以起到一定的促进作用。同时在田宇敏等[22]的研究中,接种量显著的影响着白地霉发酵中的总酯含量。考察接种量对总酯产量的影响,结果见图8。
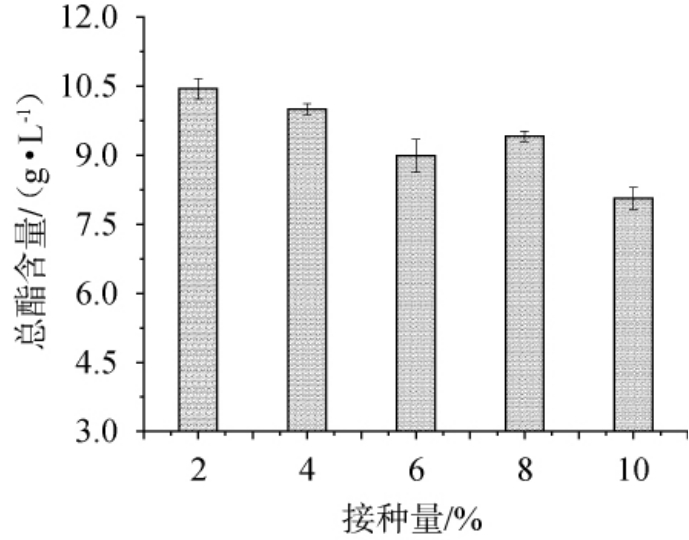
图8 接种量对总酯含量的影响
Fig.8 Effect of inoculum on total ester content
由图8可知,总酯含量随着接种量的上升呈现先上升后下降的趋势,当接种量为2%时发酵液中总酯含量最高,为10.44g/L,继续增加接种量,总酯含量整体呈现下降趋势,推测可能由于菌体浓度增加消耗碳氮源用于菌体生长,导致产酯量减少,最适菌种接种量为2%[22]。
2.3.6 初始pH对总酯含量的影响
pH是发酵过程控制中的重要参数之一,其不仅影响菌体的生长,还会影响到一些酶活性和代谢通路[23-24]。发酵培养基初始pH对总酯含量的影响结果见图9。
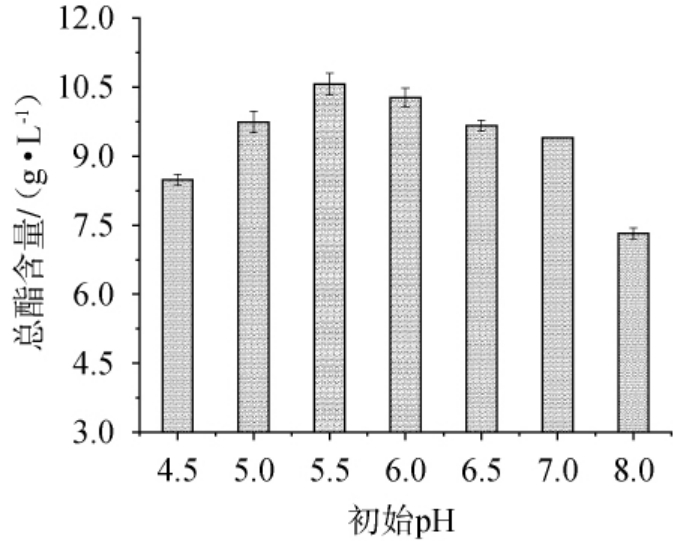
图9 初始pH对总酯含量的影响
Fig.9 Effect of initial pH on total ester content
由图9可知,随着初始pH的升高,总酯含量呈现上升后下降的趋势,初始pH 5.5时发酵液中总酯含量达到最大值10.56 g/L。该趋势表明,白地霉Y3的产酯相关酶系在pH 5.5附近具有最高活性。当初始pH低于5.5时,过酸的环境可能抑制了菌体的正常生长与代谢;而当初始pH高于5.5时,偏中性的环境可能导致关键酶活力下降或代谢途径发生改变,从而不利于酯类的合成与积累。因此,最适发酵培养基初始pH值为5.5。
2.4 菌株Y3产酯条件优化响应面试验
2.4.1 响应面试验设计与结果
通过响应面建立数学模型可以确定影响因素之间的关系,找到最优的工艺条件组合,以实现生产过程或实验结果的最优化。在单因素试验基础上,选择对总酯含量影响较大的4个因素:葡萄糖添加量(A)、蛋白胨添加量(B)、硫酸铵添加量(C)和初始pH(D)为评价因素,以总酯含量为评价指标进行响应面试验优化,试验设计及结果见表3,方差分析结果见表4。
表3 菌株Y3产酯条件优化响应面试验设计与结果
Table 3 Design and results of response surface methodology for ester production conditions optimization of strain Y3
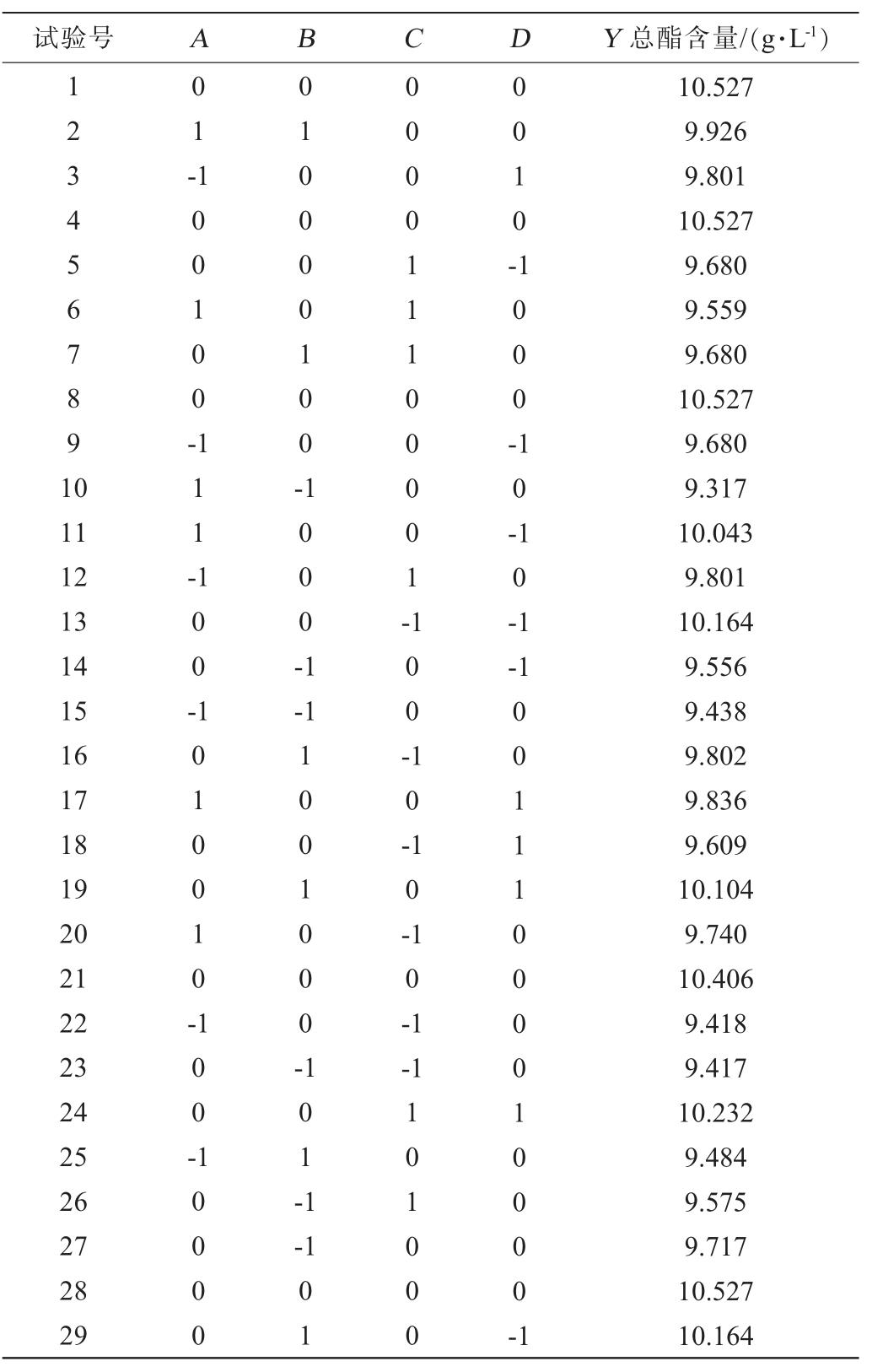
表4 回归模型方差分析
Table 4 Variance analysis of regression model
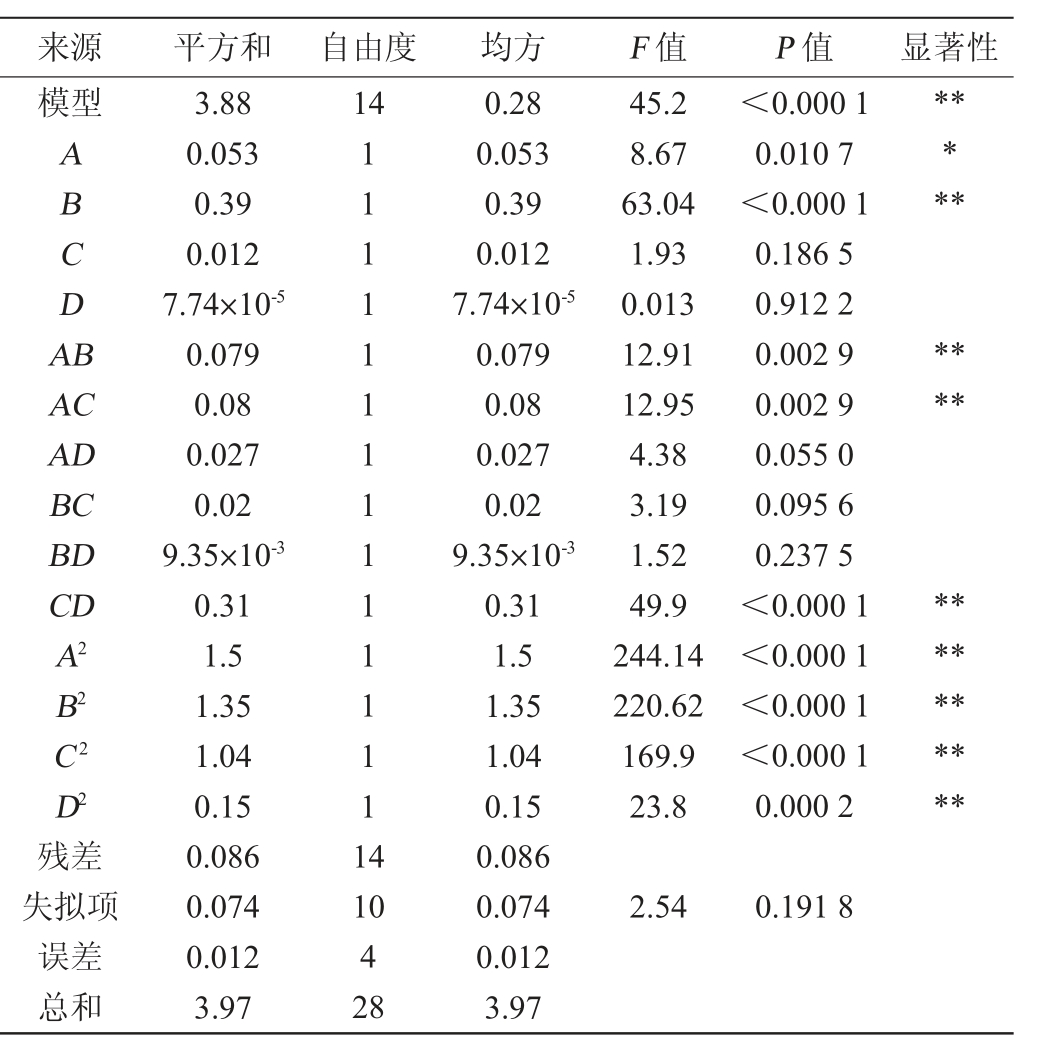
注:“**”表示对结果影响极显著(P<0.01),“*”表示对结果影响显著(P<0.05)。
对响应面试验结果进行多元化回归拟合分析,得出菌株总酯含量(Y)与葡萄糖添加量(A)、蛋白胨添加量(B)、硫酸铵添加量(C)与初始pH(D)4个因素变量的二次方程模型,模型如下:
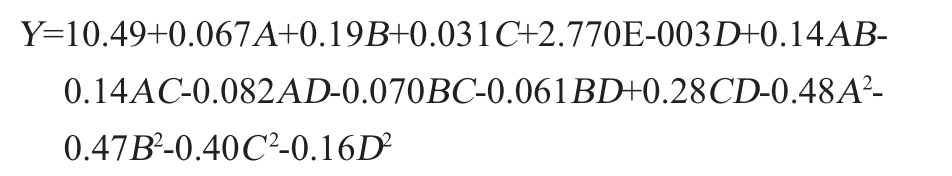
由表3、4可知,该模型的失拟项P=0.191 8>0.05不显著,表明回归方程能够反映出各因素与总酯含量之间的真实关系;回归模型P<0.01,说明该模型极显著,试验设计可靠。模型的回归决定系数R2=0.9784,表明总酯含量的变化有97.84%来源于所选因素的变化。预测决定系数R2Pred=0.8907,也能合理地说明校正决定系数R2adj=0.9567值的变化。各因素对总酯含量的影响顺序为:蛋白胨添加量(B)>葡萄糖添加量(A)>硫酸铵添加量(C)>初始pH(D)。一次项B对总酯含量的影响极显著(P<0.01),一次项A对总酯含量的影响显著(P<0.05);交互项AB、AC、CD对总酯含量的影响极显著(P<0.01);二次项A2、B2、C2、D2对总酯含量的影响极显著(P<0.01)。
2.4.2 各因素间交互作用分析
响应面等高线弧度越大表明两因素间交互作用越显著,若等高线为圆形或类似圆形,则表明两因素间没有交互作用及交互作用不显著。同样,通过响应面陡峭程度来可以判断交互作用对相应值的影响程度。响应面越陡,交互作用对响应值的影响越大,反之影响越小。通过Design-Expert V8.0.6软件绘制产酯量与各因素间三维响应面曲面图,结果见图10。由图10可知,葡萄糖添加量与蛋白胨添加量、葡萄糖添加量与硫酸铵添加量、硫酸铵添加量与pH的交互作用响应面等高线均为椭圆形,曲面较陡峭,响应值变化范围较广,表明对响应值的影响显著,说明交互作用对总酯含量的影响显著,结果与回归模型方差分析结果基本一致。
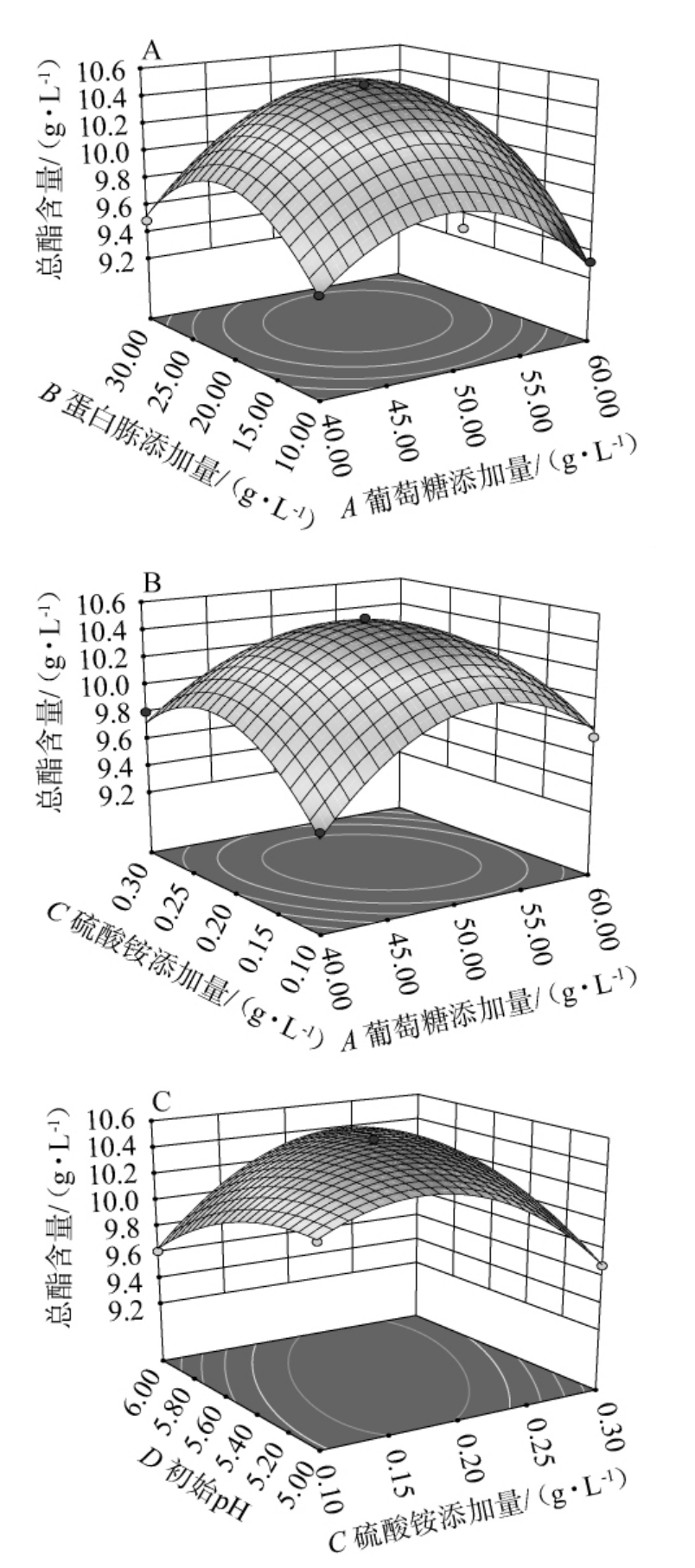
图10 各因素间交互作用对总酯含量影响的响应面和等高线
Fig.10 Response surface plots and contour lines of effects of interaction between various factors on total ester content
2.4.3 最佳产酯条件验证
响应面分析得到最优方案为:葡萄糖51.16 g/L,蛋白胨22.22 g/L,硫酸铵0.20 g/L,pH 5.45,此时最优总酯含量为10.515 g/L,根据实际操作条件,将培养条件修正为葡萄糖51 g/L,蛋白胨22 g/L,硫酸铵0.2 g/L,初始pH 5.5,摇瓶转速180 r/min,接种量2%,温度25 ℃,发酵时间30 h,在此条件下进行3次验证,得到平均总酯产量为10.55 g/L,与预测结果基本一致,因此该模型可行。
2.5 挥发性香气成分测定结果
本研究中菌株Y3在优化产酯培养基中的挥发性香气物质检测结果见图11。由图11可知,发酵液中共检测出18种挥发性风味物质,分别属于酯类、醇类、醛类和酸类,其中酯类物质最多,共12种,其次为醇类,共4种。其中酯类物质在种类和相对含量上均占绝对主导,构成了菌株Y3发酵液果香特征的主体。酯类物质含量为85.90 mg/L,占比76.45%,醇类物质含量为25.63 mg/L,占比22.81%。含量最高的酯类物质异戊酸乙酯22.03 mg/L,其次是乙酸乙酯和2-甲基2-丁烯酸乙酯含量分别为13.75 mg/L和13.08 mg/L,这三种主要香气物质占总酯类的56.88%,形成菌株Y3发酵产香的主体香味,具有明显的水果甜香味。其中异戊酸乙酯在葡萄酒中作为常见的风味物质存在并在部分种类的葡萄酒中具有较高的香气稀释指数,如梅洛红葡萄酒(Merlot red wine)和汝拉弗洛尔雪莉酒(Jura Flor-Sherry)[25-26]。另外,异戊酸乙酯是我国《食品添加剂使用卫生标准》规定允许使用的食品香料,被用于菠萝、苹果、柠檬、葡萄等水果型食用香精的配制。
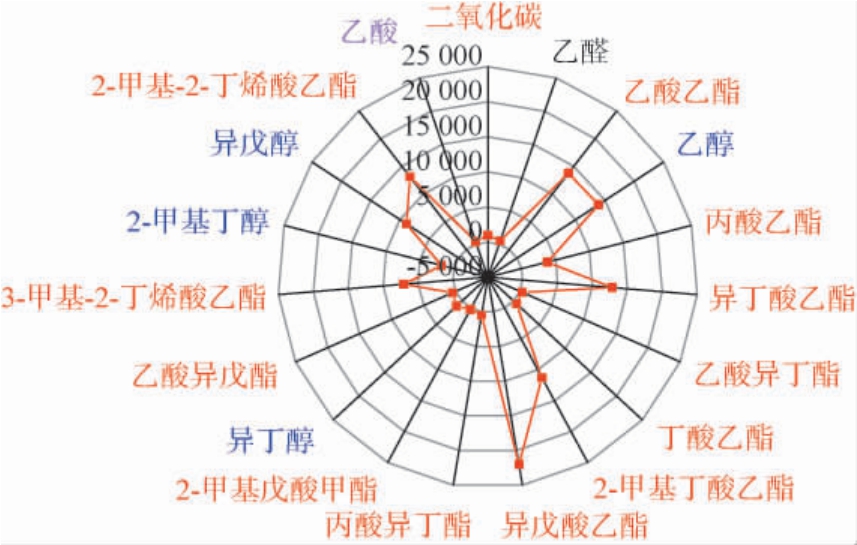
图11 挥发性风味物质含量测定结果雷达图
Fig.11 Radar map of determination results of volatile flavor substance contents
3 结论
本文以多年生竹林土壤为研究对象,筛选出一株能够产浓郁果香味的酵母菌,通过形态和生理生化鉴定,分子生物学鉴定为白地霉(Geotrichum candidum),命名为Y3。通过测定菌株Y3在YEPD培养基中的产酯曲线发现,菌株Y3培养30 h时产酯量能达到1.86 g/L,有较好的产酯能力。以菌株Y3为研究对象,YEPD培养基为基础产酯发酵培养基,总酯含量为考察指标,通过单因素试验和响应面试验确定菌株Y3的最佳产酯条件,发酵30h后总酯含量达到10.55g/L,比初始YEPD培养基总酯含量提高了8.69 g/L。测定其挥发性香气成分发现,18种主要挥发性香气成分为异戊酸乙酯,其次为乙酸乙酯、乙酸异丁酯、2-甲基丁酸乙酯、丙酸乙酯、丁酸乙酯、3-甲基2-丁烯酸乙酯、2-甲基2-丁烯酸乙酯等。本研究为食品发酵工业提供高产酯菌株,在发酵食品和感官提升方面具有一定的意义。同时,为产香白地霉在食品发酵工业中的应用提供理论基础和微生物参考。
[1] 李媚媛,刘安琪,唐道埔,等.产香气化合物微生物的研究进展[J].食品科学,2023,44(19):259-269.
[2] 张安东,贝盏临,张欣,等.产香酵母在食品工业中的应用[J].绿色科技,2015(11):260-264.
[3] 王国良,宋俊梅,曲静然.产香微生物的应用现状[J].食品研究与开发,2007(7):157-160.
[4] 杜飞,喻阑清,周家喜,等.两种产香微生物分离鉴定及其发酵液增香烟草研究[J].山地农业生物学报,2021,40(1):14-21.
[5] 张辉,易彬,任剑波,等.产香微生物及其在传统发酵食品中的应用[J].酿酒,2025,52(3):7-11.
[6] KAGKLI D M,TÂCHE R,COGAN T M,et al.Kluyveromyces lactis and Saccharomyces cerevisiae,two potent deacidifying and volatile-sulphuraroma-producing microorganisms of the cheese ecosystem[J]. Appl Microbiol Biotechnol,2006,73(2):434-442.
[7] 刘小改,李洪媛,周林艳,等.清香型大曲中产香细菌的分离筛选及鉴定[J].中国酿造,2022,41(5):96-100.
[8] 张鹏,李炜,师超,等.一株产果香型真菌的筛选、鉴定及在烟草增香中的应用[J].中国烟草科学,2021,42(5):95-101.
[9] LI H,QU Y,CAO K,et al.Cigarette flavouring regulation by using aromaproducing microorganism isolated from Maotai Daqu[J].E3S Web Conf,2021,271:04031.
[10] 周森,王勇,李艳敏,等.产香白地霉菌株筛选鉴定及其代谢产物分析[J].酿酒科技,2013(7):52-54.
[11] 袁英豪,何梦娇,唐春麟,等.醋源生香酵母的筛选及其特性研究[J].食品与发酵工业,2024,50(15):63-71.
[12] FAN G S,SUN B G,XU D,et al.Isolation and identifation of high-yield ethyl acetate-producing yeast from Gujinggony Daqu and its fermentation characteristics[J].J Am Soc Brew Chem,2018,76(2):117-124.
[13] 陈嘉,邢晓莹,冯志宏,等.山西老陈醋酿造过程中产酯酵母的筛选及产香特性分析(英文)[J].食品科学,2019,40(16):144-151.
[14] 巴尼特,佩恩,亚罗,等.酵母菌的特征与鉴定手册[M].青岛:青岛海洋大学出版社,1991:18-31.
[15] 黄诚,尹红,周金森.食醋中总酸、总酯含量的连续测定[J].食品与发酵工业,2001,27(12):41-43.
[16] 贾丽艳,田宇敏,荆旭,等.果香风味导向白地霉M5的分离鉴定及生物学特性研究[J].中国食品学报,2020,20(3):210-220.
[17] 张阳阳,赵筱岑,王荣荣,等.白地霉S13固态发酵白酒条件优化[J].中国酿造,2023,42(5):196-200.
[18] HOHMANN S.Osmotic stress signaling and osmoadaptation in yeasts[J].Microbiol Mol Biol Rev,2002,66(2):300-372.
[19] 时桂芹,任菲,谢冰宗,等.高糖胁迫对酿酒酵母抗氧化活性及代谢的影响[J].食品工业科技,2019,40(20):94-100.
[20] 雍茜浩,赵婷,刘君,等.酿酒酵母醇酰基转移酶的研究进展[J].中国酿造,2020,39(10):30-36.
[21] 梁磊,张远平,浦跃武,等.高酵母接种量的抑菌特性及其在蔗汁生产乙醇中的应用[J].食品与发酵工业,2007,27(12):1-4.
[22] 田宇敏,贾丽艳,高娟娟,等.基于响应面法对白地霉M5高产酯发酵工艺优化[J].中国调味品,2019,44(1):71-77.
[23] CHANDLER M,STANLEY G A,ROGERS P,et al.A genomic approach to defining the ethanol stress response in the yeast Saccharomyces cerevisiae[J].Ann Microbiol,2004,54(4):427-454.
[24] 范光森,刘朋肖,吴秋华,等.有氧条件下酿酒酵母YF1914产乙醇发酵条件优化及其产香特性[J].食品工业科技,2019,40(13):52-58.
[25] ARCARI S G,CALIARI V,SGANZERLA M,et al.Volatile composition of Merlot red wine and its contribution to the aroma: optimization and validation of analytical method[J].Talanta,2017,174:752-766.
[26] COLLIN S,NIZET S,CLAEYS BOUUAERT T,et al.Main odorants in Jura flor-sherry wines.relative contributions of sotolon,abhexon,and theaspirane-derived compounds[J]. J Agr Food Chem,2012,60(1):380-387.