酱香型白酒翻沙工艺是以7次取酒后的酱香型白酒酒醅为基础,拌入新蒸粮和大曲再次发酵取酒的过程[1-4]。多轮次发酵的酒醅拥有丰富的风味及前体物质,适宜酱香型白酒生产[5]。翻沙工艺利用丢糟再发酵,能够提升原料利用率,并具有周期短、成本低、酒体干净和酱香突出的特点[1-2,6]。
蒸粮是酿酒工艺中重要的工序,其主要目的是使高粱中的淀粉颗粒吸水、膨胀、破裂,进而达到糊化效果[7-8]。糊化后的淀粉更易被微生物转化为可发酵性糖,为酒精发酵提供原料[7,9]。蒸粮工艺主要分为混蒸和清蒸,其中混蒸为粮食和酒糟按一定比例混合后,取酒和蒸粮同时进行[10]。清蒸工艺是将粮食单独蒸煮后再与母糟加曲发酵[11],不仅能够更好地控制高粱的糊化程度,还能有效保留粮食的原始风味。此外,高粱作为白酒酿造的主要原料,其添加量直接影响酒醅微生物的繁殖和发酵,进而对基础酒的产量和质量产生影响。如杨甲平等[12]研究发现,不同投粮量对夏季浓香型白酒的生产有一定影响,适当的投粮量可提高出酒率,同时赋予酒体干净醇厚、香气浓郁、绵甜有粮香的特点。李科发等[13]研究了夏季压窖期间不同投粮量对基酒产量、质量的影响,发现在夏季压窖期间,适当减少投粮量有助于安全度夏,保障生产进行。然而,目前关于投粮量的研究多注重其对酒体品质的影响,对发酵微生物群落结构的研究较少。尤其在酱香型白酒清蒸翻沙工艺中,高粱添加量的影响尚未有系统研究,多依赖酿酒工人的经验,缺乏科学理论指导,难以适应机械化、大规模生产的需求。
本研究以传统清蒸翻沙工艺为基础,以出窖酒醅理化性质、微生物群落,基酒挥发性风味物质及感官特性为评价指标,探讨了不同高粱添加量对翻沙酒酒醅微生物群落结构及基酒品质的影响,旨在确定最佳高粱添加量,为清蒸工艺翻沙酱酒生产提供科学依据。
1 材料与方法
1.1 材料与试剂
酱香型白酒7轮次取酒酒醅、糠壳、大曲、高粱等酿酒原辅料:四川某酒厂提供;DNeasy PowerSoil Pro Kit脱氧核糖核酸(deoxyribonucleic acid,DNA)提取试剂盒:德国Qiagen公司。
1.2 仪器与设备
GZX9070MBE电热鼓风干燥箱:上海博讯实业有限公司医疗设备厂;SX300全自动灭菌锅:日本日立公司;ME204E电子天平:梅特勒-托利多仪器(上海)有限公司;GC-2010Plus气相色谱仪配备氢火焰离子化检测器(gas chromatography-flame ionization detector,GC-FID):岛津企业管理(中国)有限公司;DB-WAX毛细管色谱柱(60 m×0.25 mm×0.25 μm):美国Agilent公司;S0200-230V-EV涡旋仪:美国Labnet公司;PC-2RP-EDI集中供水装置:成都品成科技有限公司;5810R冷冻离心干燥机:德国Eppendorf公司。
1.3 方法
1.3.1 酱香型白酒清蒸翻沙工艺流程及取样方法
以第7次取酒后的酱香型白酒酒醅为基础进行酱香型白酒清蒸翻沙工艺实验,选取4口窖池,每个窖池25甑酒醅,设计高粱添加量分别为50 kg/甑、75 kg/甑、100 kg/甑、125 kg/甑(编号为Q_50、Q_75、Q_100、Q_125),每甑酒醅约为1 t。酱香型白酒清蒸翻沙工艺流程如下:

取样方法:出窖酒醅分层取样,酒醅总深度2.0 m(上层:0~0.5 m;中层:0.5~1.5 m;下层:1.5~2.0 m)。每层5点各取100 g混成500 g层样;再将各层500 g层样混匀后取出500 g为最终检测样。部分用于微生物检测的样品置于-80 ℃条件下保存,其余样品置于-20 ℃条件下保存。
1.3.2 酒醅理化指标检测
酒醅可滴定酸度、水分、还原糖和淀粉含量:参照DB 34/T 2264—2014《固态发酵酒醅分析方法》[14]进行分析测定;还原糖和淀粉含量均以酒醅干质量计算。
1.3.3 酒醅微生物检测分析
按试剂盒提取说明对出窖酒醅进行DNA提取。完成DNA提取后,检测DNA的浓度和纯度,并利用1%琼脂糖凝胶电泳检测DNA的完整性。将DNA样品送至上海美吉生物医药科技有限公司完成宏基因组Illumina NovaSeq测序。
1.3.4 基酒感官评价
参考GB/T 10220—2012《感官分析方法学总论》[15]和GB/T 15549—2022《感官分析 方法学 检测和识别气味方面评价员的入门和培训》[16],由5人(包括1名国家级品酒师,2名省级品酒师,2名研究人员)组成感官评价小组,采用盲评的方式对基酒样品的香气(包括曲香、粮香、酱香、陈香、果香、花香、酸香、烘焙香、焦香和青香),口味(包括柔和度、丰满度、协调度、纯净度、持久度、酸味、甜味、苦味、鲜味和咸味)进行感官评定打分,评分区间为1~10分,并对最终评分结果进行统计分析。
1.3.5 基酒挥发性风味物质检测
使用GC-FID对基酒的挥发性风味物质进行检测,取1mL基酒,加入内标(10 μL叔戊醇(20 g/L)、乙酸正戊酯(20 g/L)和2-乙基丁酸(20 g/L))。
气相色谱条件:进样口和检测器温度为250 ℃,分流比为40∶1。升温程序为初始温度35 ℃,保持3 min;以3 ℃/min升温至80 ℃,保持1 min;以5 ℃/min升温至100 ℃,保持3min;再以5 ℃/min升温至160 ℃,保持2 min;以10 ℃/min升温至230 ℃,保持18 min。检测器为FID,载气为高纯氦气,流速为0.8 mL/min,分流比20∶1,进样量1 μL。
定性定量方法:采用GC-FID与配制的挥发性风味物质标准品保留时间进行定性分析;采用内标法进行定量,配制5个浓度梯度的挥发性风味物质标准品的混合溶液,以标准溶液各组分质量浓度与内标物质量浓度的比值(x)为横坐标,各组分峰面积与内标物质峰面积比值(y)为纵坐标,绘制内标定量法校准曲线。为验证方法的精密度,参照GB/T 27404—2008《实验室质量控制规范食品理化检测》方法,设计精密度实验。精密度实验用配制标准曲线第2浓度点的混合标准溶液在相同色谱条件下重复测定6次,计算各组分的精密度相对标准偏差(relative standard deviation,RSD)[17]。
1.3.6 香气活度值的计算
通常认为香气活度值(odor activity value,OAV)>1的挥发性风味物质对白酒香气具有贡献作用,是关键香气物质。OAV计算公式如下:
1.3.7 数据分析
酒醅理化指标使用R语言包进行显著性分析。利用Origin 2021进行柱形图、雷达图绘制。利用Fastpv0.20.0对原始数据进行质控。利用软件BWA将reads比对宿主DNA序列,并去除比对相似性高的污染reads。通过美吉平台工具进行热图和相关性热图绘制。
2 结果与分析
2.1 不同高粱添加量出窖酒醅理化指标分析
水分、酸度、还原糖和淀粉含量等是评估白酒生产质量的重要指标[18-19],可以反映酿酒工艺要点和微生物生长等情况[20]。由表1可知,不同高粱添加量出窖酒醅水分含量为53.11%~55.25%,组间差异不显著(P>0.05),适宜的水分有利于酒醅的糖化过程,保证微生物的生长代谢[21]。出窖酒醅酸度随高粱添加量的增加而显著下降(P<0.05),这可能是由于高粱添加量的增大稀释调节了酒醅酸度。不同高粱添加量出窖酒醅还原糖含量为1.68%~5.35%,其中Q_100组酒醅还原糖含量(5.35%)显著高于其他组(P<0.05),可能是糖转化率低所致。淀粉是微生物生长代谢和各类风味物质的物质基础。4组酒醅的淀粉含量为32.04%~39.84%,其中Q_50组酒醅淀粉含量(32.03%)显著低于其余3组(P<0.05),而Q_75(36.68%)、Q_100(37.92%)和Q_125组(39.84%)间差异不显著(P>0.05)。Q_50组淀粉含量最低,可能是因为初始高粱添加总量最小,同时较低的高粱添加量可能通过优化酒醅的碳氮比与微生态环境,使发酵效率提高。相比之下,Q_75、Q_100和Q_125组的淀粉添加量虽然递增,但其残留淀粉含量无显著差异,表明超出某一阈值后,单纯增加投料量并不能有效提升转化率,这进一步说明Q_50组淀粉残留的显著降低部分是源于其较高的生物转化效率,而不仅是初始投料差异导致。以上结果表明,不同高粱添加量的酒醅理化指标存在显著差异。有研究表明,酒醅微生物与理化性质具有相关性[22-23],推测这些理化性质的差异可能是由于酒醅中微生物生长代谢所引起的。
表1 不同高粱添加量出窖酒醅理化指标
Table 1 Physicochemical indexes of outpit fermented grains with different sorghum additions
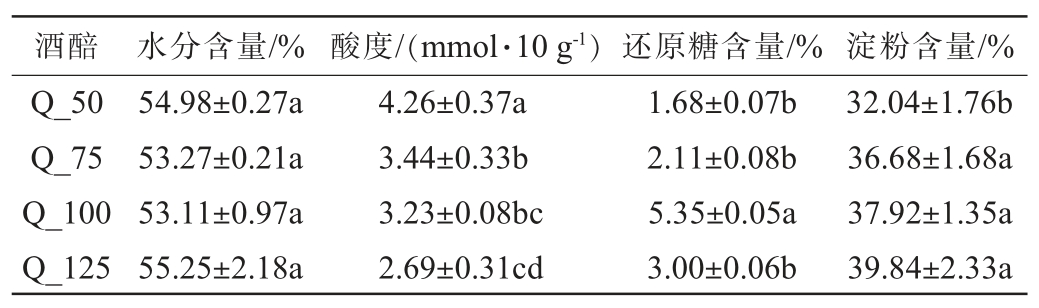
注:同列数据后不同小写字母表示差异显著(P<0.05)。下同。
2.2 不同高粱添加量出窖酒醅微生物群落分析
2.2.1 多样性分析
由表2可知,酒醅微生物群落的α多样性对高粱添加量的响应呈现出非线性特征。细菌与真菌的物种丰富度(Chao1指数)均随高粱添加量增加呈先升后降趋势,并在Q_100组达到峰值,表明该高粱添加量为绝大多数微生物类群的定殖与生长提供了最优的营养环境。在群落均匀度(Shannon指数)方面,真菌Shannon指数随高粱添加量增加而持续下降,反映出资源向部分优势真菌类群集中的趋势;细菌Shannon指数则呈现明显的先升后降格局,并在Q_100组达到最高。过量添加高粱(Q_125)可能导致酒醅微环境中的营养丰富[24],从而激化了微生物之间对资源的激烈竞争;这种竞争会筛选出少数适应性强的优势菌种,使其占据主导生态位,最终导致群落结构简化,物种丰富度与多样性同步衰退。该结果表明翻沙工艺中高粱添加量存在一个关键阈值,超越此阈值将破坏微生物群落结构的稳定性。
表2 不同高粱添加量出窖酒醅微生物群落多样性分析
Table 2 Analysis of microbial community diversities of outpit fermented grains with different sorghum additions
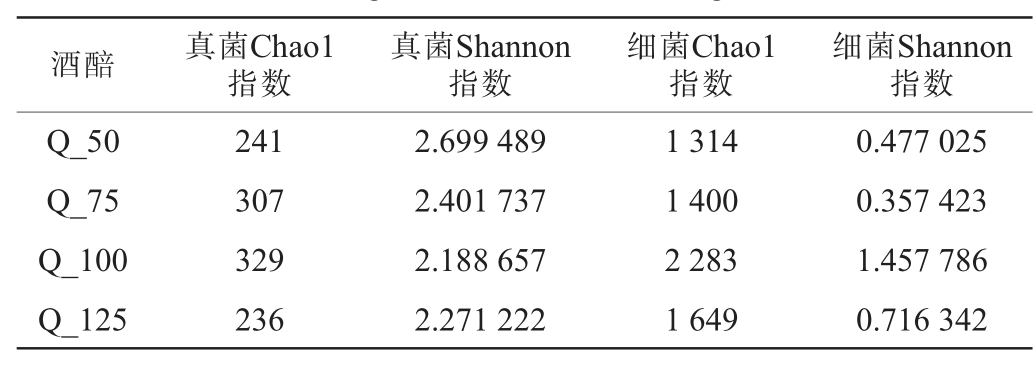
2.2.2 微生物群落结构分析
酒醅微生物群落结构是决定酱香型白酒风味品质的核心。为解析其受工艺调控机制,本研究通过高通量测序分析了不同高粱添加量下的群落结构,发现其整体结构存在显著差异。由图1A、B可知,在属水平上,4组不同高粱添加量出窖酒醅真菌属中平均相对丰度>1%的有9种,包括酵母属(Saccharomyces)、毕赤酵母属(Pichia)、哈萨克斯坦酵母属(Kazachstania)、裂殖酵母属(Schizosaccharomyces)、曲霉属(Aspergillus)、接合酵母属(Zygosaccharomyces)、篮状菌属(Talaromyces)、拟青霉属(Paecilomyces)、酒香酵母属(Brettanomyces)。Q_50组酒醅中Saccharomyces占比最高(40%),酵母菌是白酒酿造过程中乙醇代谢的核心功能菌群,对于酒醅发酵产生酒精和生香具有一定作用[25];Q_75组、Q_100组酒醅中Kazachstania占比最高(43%、56%),Kazachstania主要产异戊醇和乙酸异戊酯等[26-28];Q_125组酒醅中Pichia占比最高(47%),Pichia对酒醅发酵生香具有重要作用,可产生花果香气的风味物质[29]。不同高粱添加量出窖酒醅细菌属中,相对丰度>1%的细菌属有7种,包括醋乳杆菌属(Acetilactobacillus)、半生乳杆菌属(Companilactobacillus)、迟缓乳杆菌属(Lentilactobacillus)、乳酸杆菌属(Lactobacillus)、克罗彭斯特菌属(Kroppenstedtia)、魏斯氏菌属(Weissella)、Secundilactobacillus和unclassfied_D_Bacteria,其中Acetilactobacillus为绝对优势菌属,在Q_50组、Q_75组、Q_100组、Q_125组酒醅中占比均最高,分别为92%、94%、88%、73%。Acetilactobacillus是酱香型白酒发酵过程脂肪酸合成的核心微生物[30]。
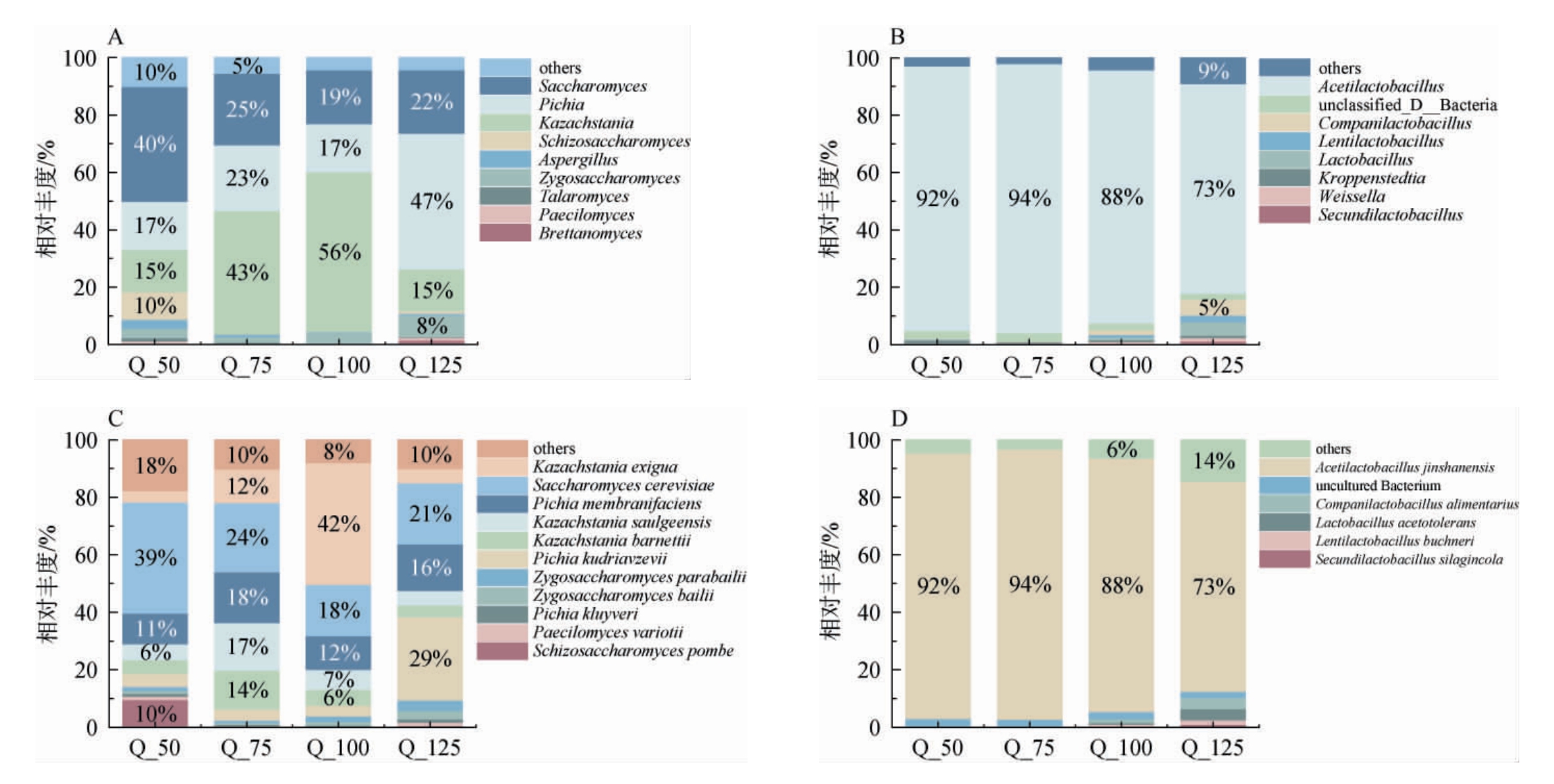
图1 基于属水平(A、B)与种水平(C、D)不同高粱添加量出窖酒醅真菌及细菌群落结构分析
Fig.1 Analysis of fungal and bacterial community structure of outpit fermented grains with different sorghum additions based on genus level (A,B) and species level (C,D)
由图1C、D可知,在种水平上真菌群落中平均相对丰度>1%有11种,包括粟酒裂殖酵母(Schizosaccharomyces pombe)、宛氏拟青霉(Paecilomyces variotii)、克鲁维毕赤酵母(Pichia kluyveri)、拜耳接合酵母(Zygosaccharomyces bailii)、拜氏接合酵母(Zygosaccharomyces parabailii)、库德里阿兹威毕赤酵母(Pichia kudriavzevii)、巴奈特哈萨克斯坦酵母(Kazachstania barnettii)、德兰士瓦哈萨克斯坦酵母(Kazachstania saulgeensis)、膜醭毕赤酵母(Pichia membranifaciens)、酿酒酵母(Saccharomyces cerevisiae)、少孢哈萨克斯坦酵母(Kazachstania exigua)。Q_50组酒醅中S.cerevisiae(39%)占比最大;Q_75组酒醅中相对丰度>10%的菌有5种,且占比相对较均衡,分别为S.cerevisiae(24%)、P.membranifaciens(18%)、K.saulgeensis(17%)、Kazachstania barnettii(14%)、K.exigua(12%);Q_100组酒醅中K.exigua(42%)占比最大;Q_125组酒醅中P.kudriavzevii(29%)和S.cerevisiae(21%)占比最大。细菌群落丰度占比>1%的物种共注释到6种,其中Acetilactobacillus中的金山醋乳杆(Acetilactobacillus jinshanensis)是该属的唯一种,在Q_50组、Q_75组、Q_100组、Q_125组酒醅中占比均最高,分别为92%、94%、88%、73%,该菌在发酵过程中可产生多种风味物质,如醋酸、乳酸等,赋予酱香型白酒独特的酸香和复杂口感[31]。
2.3 不同高粱添加量清蒸翻沙工艺酱香型白酒基酒挥发性风味物质分析
2.3.1 挥发性风味物质含量分析
采用GC-FID检测技术对不同高粱添加量清蒸翻沙工艺酱香型白酒基酒挥发性风味物质进行定量检测。由表3可知,4组基酒样品共靶向定量检测了56种物质,在Q_50组、Q_75组、Q_100组、Q_125组总含量分别为10 701.5 mg/L,9 388.20 mg/L,8 719.37 mg/L和10 043.82 mg/L,差异显著(P<0.05)。56种物质可以分为6大类,包括酯类18种、醇类14种、酮类3种、醚类1种、酸类11种、醛类9种,其中酯类、醇类物质含量最高。
表3 不同高粱添加量清蒸翻沙工艺酱香型白酒基酒挥发性风味物质含量检测结果及香气活性值
Table 3 Determination results of volatile flavor compounds contents and odor activity values in Qingzheng Fansha-processed sauce-flavor Baijiu with different sorghum additions
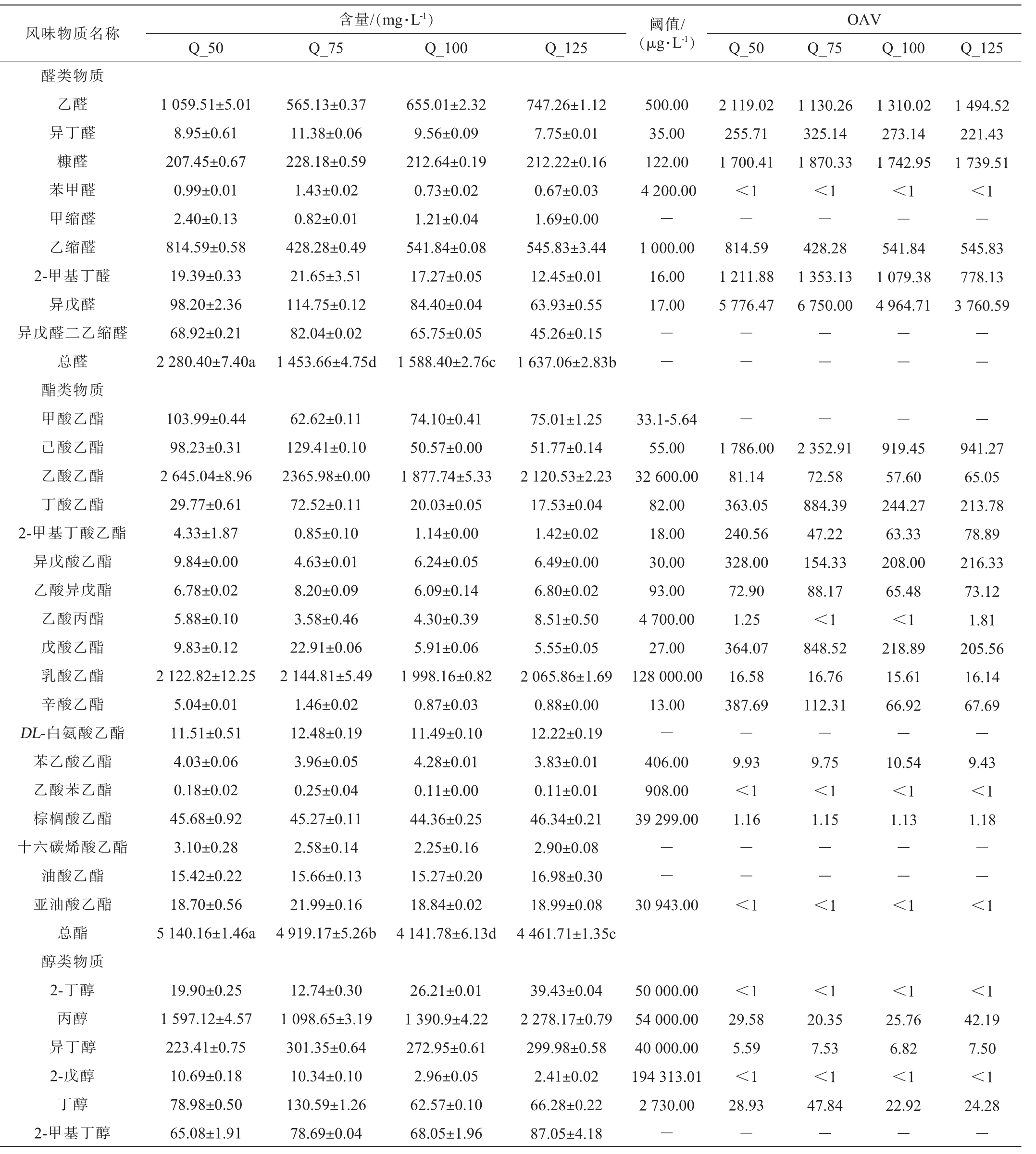
续表
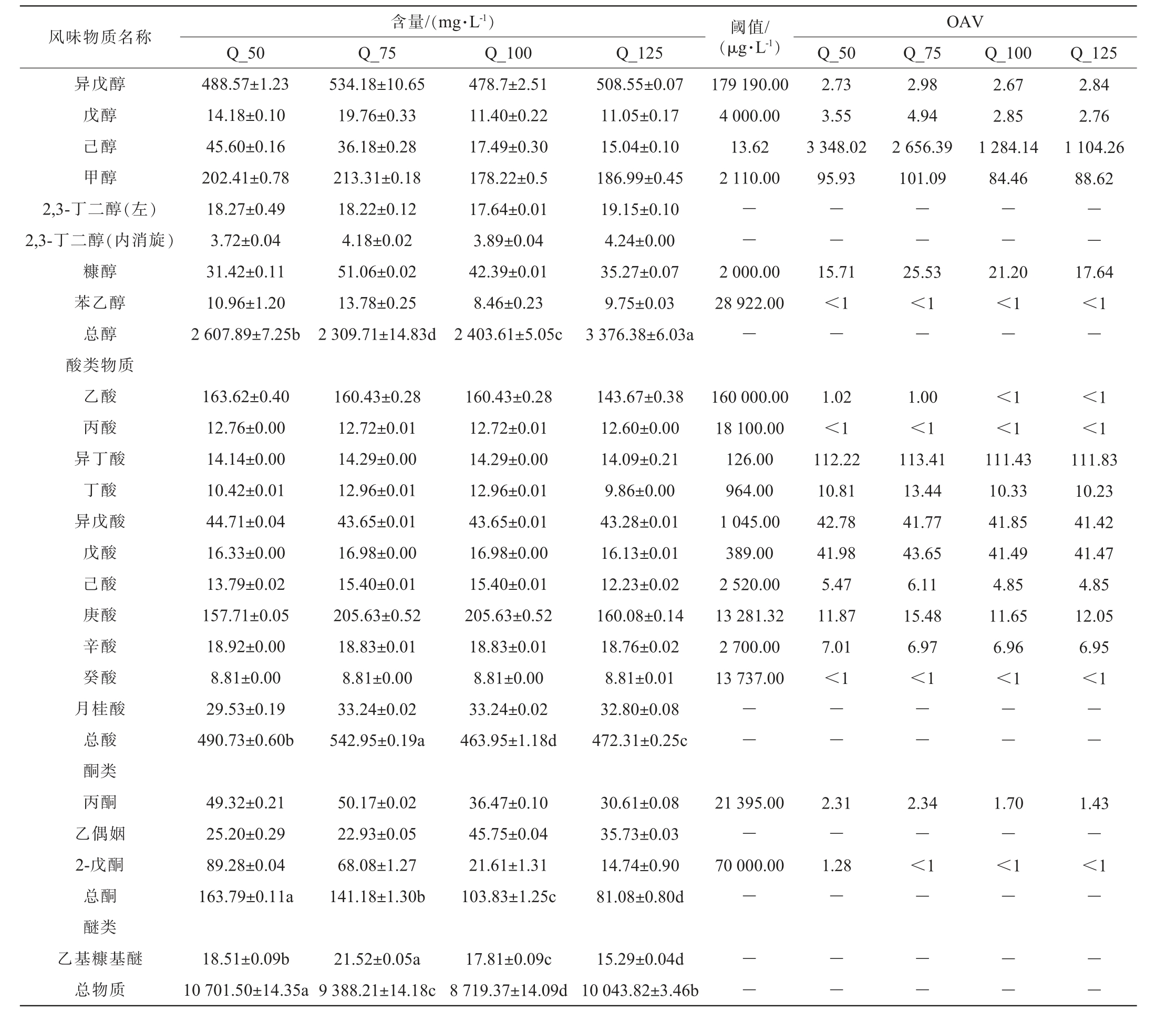
酯类物质是基酒中重要的呈香风味物质,能够赋予酒体柔和、醇厚的口感,可由醇和酸酯化产生,同时也可由微生物直接代谢产生[17,32]。Q_50组基酒酯类物质含量最高,为5 140.16 mg/L,主要为乙酸乙酯、乳酸乙酯、甲酸乙酯、己酸乙酯等。
醇类物质在酱香型白酒中主要起辅助作用,能够提升其他香味物质的观感,具有“助香”和“提扬”的作用[3,33]。Q_125组基酒醇类物质含量最高,为3 412.11 mg/L。醇类是酯类的前体物质,对酒体有助香作用,含量较高的有丙醇、异戊醇、异丁醇等。
醛类物质是酱香型白酒香气的重要组成部分,适量的醛类物质可以使酒体香气更加浓郁、优雅,可以增加酒体的醇厚感和柔和度[34]。Q_50组基酒醛类物质含量最高,为2 280.4 mg/L,主要为乙醛、乙缩醛、糠醛等。
酱香型白酒的典型酸味(如乙酸、乳酸、己酸等)与酯类、醇类物质协同,形成“酸甜苦咸鲜”的复杂层次感[34]。Q_75组基酒酸类物质含量最高,为542.95 mg/L。主要为庚酸、乙酸、异戊酸和月桂酸等。
酮类物质具有独特的香气,如醇香、微甜的味道,能够带来花香和水果香味[34]。其生成途径有很多种,醇类氧化和脱氢、氨基酸脱氨脱羧、酮酸脱羧等都可生成相应的酮类物质。Q_50组基酒酮类物质含量最高,为138.6 mg/L。主要为丙酮和2-戊酮等。
醚类物质检出的为乙基糠基醚,Q_75组基酒醚类物质含量最高,为21.52 mg/L。乙基糠基醚具有独特的甜辣气味,与其他风味物质具有协同作用。
2.3.2 风味物质差异分析
对OAV>1的33种挥发性风味物质绘制聚类分析热图,结果见图2。由图2可知,聚类树将风味物质分为两类:Q_75组基酒中含量较高的2-甲基丁醛、糠醇、糠醛、乙酸异戊酯等18种物质聚为一类,其他3组基酒中含量较高的2-甲基丁酸乙酯、乙缩醛、苯乙酸乙酯、乙酸丙酯等15种物质聚为一类。其中2-甲基丁醛具有可可、咖啡等气味[35];糠醇具有淡淡的酸香气[36];糠醛具有杏仁味,是酱香型白酒中呋喃类中含量较高的物质,也是酱香型白酒的标志性物质之一[37];乙酸异戊酯具有香蕉气味,是优级酒中的重要标志物[37]。
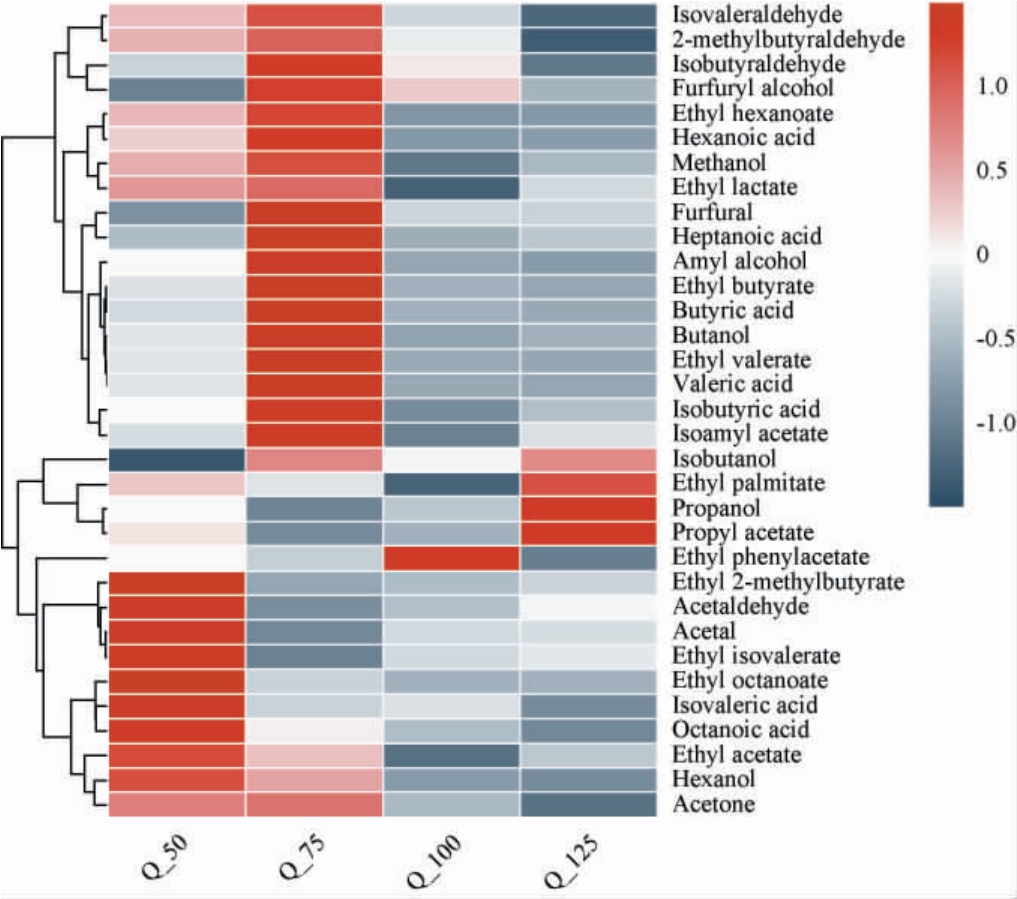
图2 不同高粱添加量清蒸翻沙工艺酱香型白酒基酒挥发性风味物质聚类分析热图
Fig.2 Cluster analysis heatmap of volatile flavor compounds of base liquor of Qingzheng Fansha-processed sauce-flavor Baijiu with different sorghum additions
2.4 基酒感官品质分析
对不同高粱添加量清蒸翻沙工艺酱香型白酒基酒酒体进行感官评定,结果见图3。由图3可知,4组基酒样品的曲香、粮香、酱香风味比较浓郁,在持久度、纯净度、协调度、丰满度、甜味口感上得分均高于5分。Q_50组基酒感官评价在花香、果香、酸香等方面得分最高,这可能与Q_50组基酒风味物质中酸类风味物质和乙酸壬酯含量高有关;Q_75组基酒感官评价在曲香、粮香、酱香、焦香、柔和度、甜味上得分最高,这与上述分析Q_75组基酒风味物质中的糠醛、糠醇、乙酸异戊酯、庚酸等物质含量高有关;Q_100组基酒在鲜味得分比较明显;Q_125组基酒在烘焙香、持久度、丰满度上得分相对较高。Q_50、Q_75、Q_100和Q_125组的感官总得分分别为95.5分、102.9分、96.6分和101.8分,综合比较,Q_75组基酒感官得分最高,曲香、酱香最为明显。
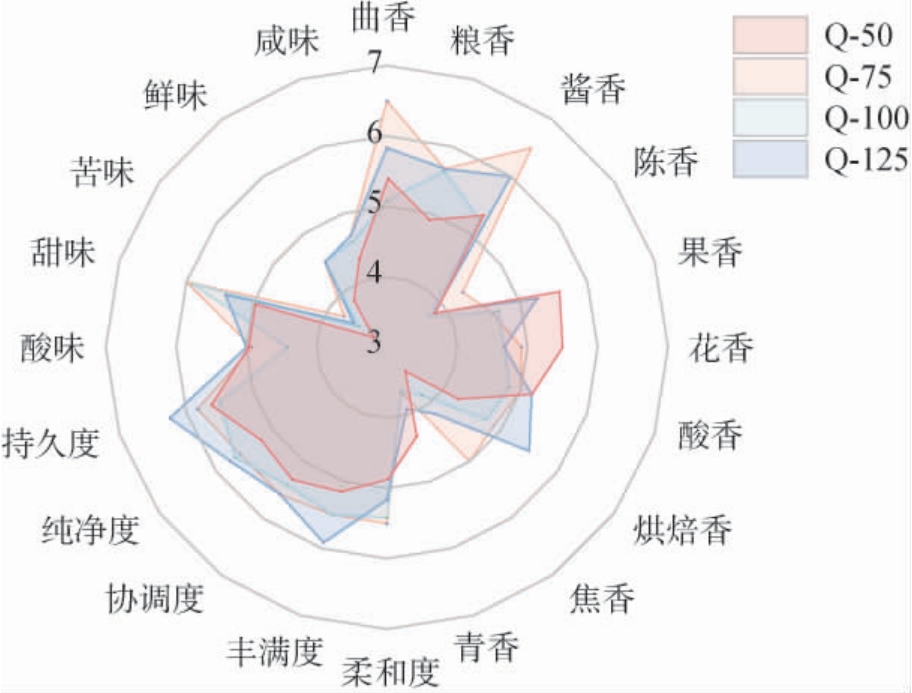
图3 基酒感官评定雷达图
Fig.3 Radar chart of sensory evaluation for base liquor
2.5 不同高粱添加量酒醅微生物与关键香气物质相关性分析
由图4A可知,相对丰度前9的真菌与辛酸乙酯、乙酸乙酯、己醇、辛酸、异戊酸、苯乙酸乙酯6种风味物质呈负相关,与异丁醇呈正相关。其中K.barnettii 和K.saulgeensis与异丁醇呈非常显著正相关(P<0.001);K.exigua 与辛酸乙酯、乙酸乙酯呈非常显著负相关(P<0.001);P.kluyveri、P.kudriavzevii、P.membranifaciens和Z.bailii与异戊酸呈非常显著负相关(P<0.001);S.cerevisiae与苯乙酸乙酯呈非常显著负相关(P<0.001);Z.bailii与己醇、辛酸呈非常显著负相关(P<0.001)。Q_50组以S.cerevisiae为绝对优势菌(39%),其与苯乙酸乙酯显著负相关与该组苯乙酸乙酯较低含量(4.03 mg/L)相符;Q_75组具有最为均衡的真菌群落分布,其中相对丰度较高的K.barnettii和K.saulgeensis与异丁醇显著正相关与该组异丁醇含量最高的结果一致;Q_100组以K.exigua为绝对优势菌,其与辛酸乙酯、乙酸乙酯显著负相关与该组辛酸乙酯含量最低及乙酸乙酯含量较低相吻合,整体风味强度最弱(总质量浓度8 719.37 mg/L);而Q_125组中P.kudriavzevii和S.cerevisiae共同主导,该组总醇含量最高(3 376.38 mg/L)但总醛、总酮含量较低,S.cerevisiae与苯乙酸乙酯的负相关关系在该组苯乙酸乙酯含量最低中得到体现。这些结果表明,不同高粱添加量通过塑造特定的真菌群落结构,与基酒中风味物质的组成和含量建立了关联。
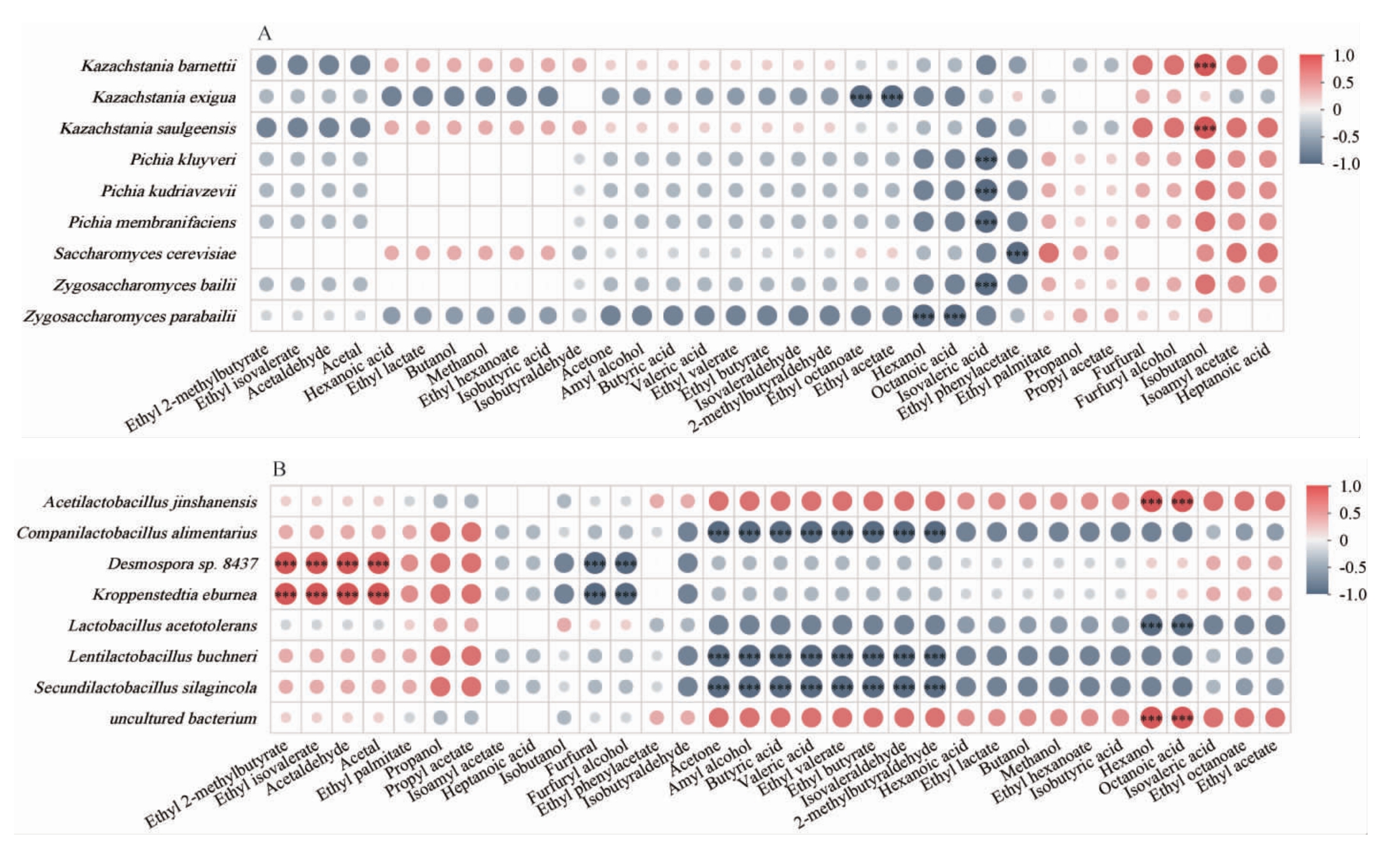
图4 酒醅微生物与基酒挥发性风味物质的相关性分析
Fig.4 Correlation analysis between microorganisms in fermented grains and volatile flavor compounds in base liqour
A为真菌;B为细菌。“***”表示相关性非常显著(P<0.001)。
由图4B可知,相对丰度前8的细菌与OVA>1的风味物质形成了42对相关性,4种细菌与乙醛、乙缩醛、2-甲基丁酸乙酯等6种风味物质呈显著正相关,6种细菌与糠醛、糠醇、丁酸、戊酸等12种风味物质负相关。绝对优势菌种A.jinshanensis与己醇和辛酸呈非常显著正相关(P<0.001)。K.eburnea和Desmospora sp.8437与2-甲基丁酸乙酯、异戊酸乙酯、乙醛和乙缩醛呈非常显著正相关(P<0.001),与糠醛和糠醇呈非常显著负相关(P<0.001)。C.alimentarius、L.buchneri和S.silagincola与丙酮、戊醇、丁酸、戊酸、戊酸乙酯、丁酸乙酯、乙酸异戊酯和2-甲基丁醛呈非常显著负相关(P<0.001)。L.acetotolerans与己醇和辛酸呈非常显著负相关(P<0.001)。随着添加量从Q_50增至Q_125,绝对优势菌A.jinshanensis的相对丰度从92%降至73%,与其呈正相关的己醇和辛酸含量也随之变化。Q_75和Q_100组中具有正向产香功能的K.eburnea和Desmospora sp.8437相对活跃,这些组中2-甲基丁酸乙酯、异戊酸乙酯等酯类及乙醛、乙缩醛含量相应较高。而在Q_125高添加量组中,具有广泛负相关性的C.alimentarius等菌属相对丰度上升,与其显著负相关的丙酮、戊醇、丁酸等12种风味物质含量则呈现下降趋势。这些关联表明,不同高粱添加量通过改变细菌群落结构,进而影响风味物质的组成特征,其中Q_75组展现出相对均衡的细菌群落分布和协调的风味物质谱。
3 结论
本研究系统解析了高粱添加量对酱香型白酒清蒸翻沙工艺中酒醅微生态及基酒风味品质的调控作用。结果表明,不同高粱添加量(50~125 kg/甑)通过显著影响酒醅微生物群落结构与代谢功能,进而调控基酒风味品质。其中,75kg/甑添加量(Q_75)展现出最佳的综合效果:其酒醅微生物群落结构最为均衡,真菌中酿酒酵母、膜醭毕赤酵母与两种哈萨克斯坦酵母协调分布,细菌中优势菌金山醋乳杆菌保持较高丰度(94%);该组基酒中异丁醇、糠醛、糠醇、乙酸异戊酯等关键风味物质含量较高,风味协调性最佳,感官评价得分最高(102.9),兼具突出的曲香、粮香、酱香特征及良好的柔和度与甜味。过高添加量(100~125 kg/甑)会导致真菌群落结构失衡,细菌多样性下降,进而影响风味协调性。本研究确定75 kg/甑为清蒸翻沙工艺的较佳高粱添加量,为酱香型白酒机械化、标准化生产提供了科学依据。
[1] 郭世鑫,张小娜,姚孟琦,等.不同工艺酱香型白酒成分分析[J].食品与发酵工业,2022,48(1):241-246.
[2] 谭军辉,左垚.简述酱香型白酒新型生产工艺[J].酿酒,2020,47(4):32-35.
[3] 张晓婕,邱树毅,曾庆军,等.不同工艺酱香型白酒挥发性物质差异分析[J].食品科学,2022,43(18):279-285.
[4] 穆建科.以地面不锈钢窖箱生产酱香翻、碎沙白酒的研究[J].轻工科技,2020,36(5):10-11.
[5] 李芳香,徐丽娜,宋露露,等.酱香型白酒丢糟中多酚提取工艺优化及抗氧化活性分析[J].中国酿造,2023,42(9):175-179.
[6] 张晓婕.不同工艺酱香白酒品质差异分析[D].贵阳:贵州大学,2022.
[7] 卢君,唐平,山其木格,等.一种评价酱香型白酒酿造过程高粱蒸煮程度的技术研究[J].中国酿造,2021,40(3):73-78.
[8] LI E P,YANG C T,WANG J P,et al.Leached starch content and molecular size during sorghum steaming for Baijiu production is not determined by starch finemolecularstructures[J].Int J Biol Macromol,2021,184(1):50-56.
[9]SHI X,FAN C M,PAN C M,et al.Analysis of differences in physicochemical properties of different sorghum varieties and their influence on the selection of raw materials for winemaking[J].Food Chem,2024,23:101517.
[10] 马浩,明红梅,郑佳,等.同时蒸馏萃取结合气相色谱-质谱联用解析不同酿酒原料蒸煮香气成分[J].食品与发酵工业,2024,56(6):247-253.
[11] 李晨阳,杨平,秦辉,等.清蒸高粱糊化度检测及其蒸粮效果评价方法研究[J].食品与发酵工业,2025,51(17):150-158.
[12] 杨甲平,王孝荣,蔡小波,等.夏季不同投粮量对酿酒生产的影响研究[J].酿酒科技,2021(8):76-80,92.
[13] 李科发,胡贤民,付毅华,等.关于夏季压窖期间不同投粮量对基酒产质量的影响研究[J].酿酒,2016,43(3):41-43.
[14] 安徽省质量技术监督局.DB 34/T 2264—2014固态发酵酒醅分析方法[S].合肥:安徽人民出版社,2014.
[15] 国家质量监督检验检疫总局,国家标准化管理委员会.GB/T 10220—2012感官分析方法学总论[S].北京:中国标准出版社,2012.
[16] 国家市场监督管理总局,国家标准化管理委员会.GB/T 15549—2022感官分析方法学检测和识别气味方面评价员的入门和培训[S].北京:中国标准出版社,2022.
[17] 郑蕾,马龙,牛曼思,等.不同产地酱香型白酒感官特征与重要挥发性成分差异分析[J].酿酒科技,2023(5):54-64.
[18] 李潮云,卢君,冯海燕,等.酱香型白酒二轮次堆积酒醅酵母菌数量与理化指标变化分析[J].中国酿造,2024,43(2):48-52.
[19] ZHANG Q M,DU G C,CHEN J,et al.Systematic analysis of Baobaoqu fermentation starter for Wuliangye Baijiu by the combination of metagenomics and metabolomics[J].Front Microbiol,2022,4(13):1062547.
[20] 史琳铭,杜艳红,聂建光,等.不同品种高粱理化品质与清茬大曲白酒风味品质的相关性研究[J].食品工业科技,2025,34(2):1-17.
[21] 王清龙,刘延波,任晓萌,等.赊店老酒新老窖池酒醅理化指标、细菌菌群多样性及风味物质分析[J].中国酿造,2023,42(8):122-128.
[22] HAO F,TAN Y W,LV X B,et al.Microbial community succession and its environment driving factors during initial fermentation of maotai-flavor Baijiu[J].Front Microbiol,2021,3(12):1-8.
[23] 黄廷财,柴丽娟,时伟,等.酱香型白酒第、轮次堆积发酵有机酸代谢规律与菌群结构及其相关性解析[J].食品科学,2024,45(18):106-115.
[24] DAI T,WEN D,BATES C T,et al.Nutrient supply controls the linkage between species abundance and ecological interactions in marine bacterial communities[J].Nat Commun,2022,13(1):175.
[25] 张恩华,柏永昊,范培文,等.酵母菌种类及发酵条件对白酒正丙醇含量的影响[J].武汉轻工大学学报,2024,43(3):46-52.
[26] 游玲,周荣清,谭壹,等.Kazachstania属酵母在浓香型白酒糟醅中的分布特征及发酵功能[J].生物技术通报,2021(6):108-116.
[27] 肖辰.泸型酒中温大曲微生物群落的演替及其对酒醅发酵的贡献[D].无锡:江南大学,2018.
[28] YANG Y,WANG S T,LU Z M,et al.Metagenomics unveils microbial roles involved in metabolic network of flavor development in mediumtemperature daqu starter[J].Food Res Int,2021,140:110037.
[29] 倪冰倩,夏韩硕,闵伟红,等.生物强化对酱香型白酒酒醅微生物群落结构及挥发性风味组分的影响[J].食品科学技术学报,2024,42(2):93-108.
[30] 张晶.酱香型白酒发酵过程脂肪酸合成核心微生物及其影响因素解析[D].无锡:江南大学,2023.
[31] 孙佳,陆震鸣,张晓娟,等.实时荧光定量PCR检测金山醋酸乳杆菌的方法与应用[J].微生物学报,2021,48(10):3211-3221.
[32] 王金龙,尹延顺,田栋伟,等.不同质量等级酱香白酒中风味物质及差异性分析[J].中国酿造,2024,43(1):41-49.
[33] 张晓婕,邱树毅,王晓丹,等.不同质量酱香型白酒的挥发性物质差异分析[J].中国食品学报,2022,35(10):340-351.
[34] 何艳艳,刘俊男,李瑞杰,等.酱香型白酒风味及其关键物质分析技术研究进展[J].中国酿造,2024,43(11):1-7.
[35] 陈旭露,李明宇,王静,等.酱油中特征醛类风味物质的微生物生成途径研究进展[J].中国调味品,2025,50(10):217-224.
[36] 杨婷婷,黄永光,左乾程,等.酱香白酒酿造过程糠醛及糠醇的时空分布规律及溯源分析[J].食品科学,2025,46(5):38-47.
[37] 王凡,张文娟,李国辉,等.近红外光谱技术用于酱香型白酒基酒关键成分的快速定量分析[J/OL].现代食品科技,1-10[2025-11-03].https://doi.org/10.13982/j.mfst.1673-9078.2026.2.1673.