甲壳素是自然界储量最丰富的氨基多糖之一,广泛存在于虾蟹壳中[1-2]。我国是水产养殖大国,每年产生虾蟹壳废弃物约200~400万t,其高值化利用对资源循环和环境保护具有重要意义[3-4]。甲壳素可通过脱乙酰转化为壳聚糖,再进一步降解得到壳寡糖。相较于壳聚糖,壳寡糖因具有更好的水溶性、生物相容性[5-6]以及独特的抗菌[7]、抗氧化[8-9]、抗肿瘤[10-11]、促生长[12-13]等生物活性,成为当前甲壳资源高值化利用的核心产物,这些特性使其在医药、农业、食品等领域展现出广阔的应用前景。
壳聚糖酶是一种特异性催化壳聚糖中D-氨基葡萄糖之间的β-1,4-糖苷键断裂的水解酶,主要来源于细菌、真菌等微生物,因为其酶解条件温和、绿色高效、产物可控等优势[14-15],已成为当前酶法制备壳寡糖的最理想方法。不同来源的壳聚糖酶在性能上存在显著差异,与细菌壳聚糖酶相比,真菌来源的壳聚糖酶最适作用pH多为酸性环境(pH 4~6),而其作用底物壳聚糖也需要在酸性条件下(pH<6.5)发生质子化溶解[16],才能充分暴露活性位点,这种酶与底物对酸性环境的协同适应性,使得真菌壳聚糖酶能够更高效地发挥催化降解作用。再者,真菌壳聚糖酶的底物专一性更强,严格识别高脱乙酰的壳聚糖,而对几丁质、纤维素等不产生作用,从而避免了副产物的干扰[17];此外,利用真菌发酵产壳聚糖酶在分离纯化方面优势显著,真菌分泌的壳聚糖酶多为胞外酶,发酵液成分简单,无需破碎细胞即可通过离心、过滤获取含酶上清液,极大简化酶的纯化工艺[17-18]。同时,真菌还可以更高效的利用廉价的工农业废弃物,降低生产成本[19]。然而,目前关于真菌壳聚糖酶研究较细菌少,菌种资源相对匮乏,产酶菌株主要集中于曲霉属、青霉属、木霉属和毛霉属等少数菌属[20-25];并且菌株普遍存在产酶效率低、发酵周期长[16]等问题,严重制约了产业化进程。因此,筛选高产壳聚糖酶的真菌菌株并挖掘具有工业化潜力的新型酶源,仍然是当前研究的重要方向,具有显著的应用价值和产业化前景。
淡紫紫孢菌(Purpureocillium lilacinum)是一种广泛分布于土壤的丝状真菌,1979年,Jatala首次从南方根结线虫卵中分离[26],目前关于P.lilacinum的研究主要集中于害虫生物防控[27-29]及环境修复(农药降解)[30-31]等领域,关于其壳聚糖酶领域的研究较少,CHAO C F等[32]从淡紫紫孢菌中分纯化出外切型D-氨基葡萄糖苷酶;赵有玺等[33]采用紫外和亚硝基胍诱变淡紫紫孢菌BJ2获得产壳聚糖酶突变菌株BJ2-3,其酶活可达7.48 U/mL;张馨月等[34]从土壤中筛选获得一株产壳聚糖酶的淡紫紫孢菌菌株M7a,对其固体产壳聚糖酶条件进行了优化,优化后酶活可达16.8 U/mL。总体来说,淡紫紫孢菌壳聚糖酶的生产潜力尚未得到充分挖掘,针对菌株的产酶条件优化及工业化应用潜力仍有待探索。
本研究从拓展优良壳聚糖酶资源的角度出发,以填埋虾蟹壳的土壤为样本筛选具有高产壳聚糖酶能力、遗传稳定性强且具有工业应用潜力的真菌菌株,通过Plackett-Burman试验和Box-Behnken响应面设计试验优化其产酶条件,以期为甲壳类废弃物的高效生物降解及资源化利用提供优良菌种资源和理论参考。
1 材料与方法
1.1 材料与试剂
1.1.1 试验材料
试验土壤样品:采集自潍坊科技学院农学院水产所旁一处长期填埋虾蟹壳(填埋时间>1年)的场地。采用五点采样法采样,采集后的样品立即置于无菌密封袋中,于4 ℃冰箱内低温保存。
1.1.2 试剂
壳聚糖(脱乙酰度≥90%):浙江普陀兴业药业有限公司;脱乙酰蟹壳(脱乙酰度≥80%):寿光奥康生物制品有限公司;酵母粉(LP0021):英国OXOID公司;氨基葡萄糖盐酸盐(glucosamine hydrochloride,GAH):美国Sigma公司;3,5-二硝基水杨 酸(3,5-dinitrosalicylic acid,DNS):国药集团药业股份有限公司;壳寡糖标样(聚合度(degree of polymerization,DP)3~7):青岛博智汇力生物有限公司;Ezup柱式真菌基因组脱氧核糖核酸(deoxyribonucleic acid,DNA)抽提试剂盒:上海生工生物工程有限公司;其他试剂均为国产分析纯。
1.1.3 培养基
富集培养基:胶体壳聚糖5 g/L、磷酸二氢钾0.5 g/L、酵母粉1 g/L、硫酸镁0.25 g/L、氯化钠0.5 g/L、硫酸铵1 g/L,pH 6.0。
初筛平板:胶体壳聚糖5 g/L、酵母粉1.0 g/L、葡萄糖0.7 g/L、硫酸镁0.25 g/L、氯化钠1 g/L、磷酸二氢钾0.7 g/L、磷酸氢二钾0.3 g/L、硫酸铵2 g/L,琼脂20.0 g/L,pH 6.0。
种子培养基:葡萄糖10 g/L、酵母粉1 g/L、蛋白胨2.5 g/L、氯化钠1 g/L。
发酵培养基:胶体壳聚糖10 g/L、硫酸铵2 g/L、硫酸镁0.5 g/L、磷酸二氢钾1 g/L,pH 6.0。以上培养基均采用121 ℃高压蒸汽灭菌20 min。
1.2 仪器与设备
721可见分光光度计:上海佑科仪器仪表有限公司;HC-2517高速离心机:安徽中科中佳科学仪器有限公司;DXY-12L数显恒温水浴锅:深圳市鼎鑫宜实验设备有限公司;ZD-85A恒温振荡器:常州国华仪器制造有限公司;SWCJ-1C超净工作台:苏州净化设备有限公司;SPX-250BS-II生化培养箱:上海新苗医疗器械制造有限公司。
1.3 方法
1.3.1 菌株筛选
富集:采集10 g土样加入90 mL无菌去离子水中,振荡均匀,吸取上清液,按10%(V/V)的接种量接种至富集培养基中,30 ℃、160 r/min富集培养48 h。
初筛:对富集培养液梯度稀释(10-1~10-7),吸取不同稀释度富集液各100 μL涂布至初筛平板,30 ℃温箱静置培养,待长出菌落后,挑选透明圈明显的菌落至空白平板划线分离纯化,挑选生长茁壮的纯化菌株接种到种子培养基中制成种子液。
复筛:将初筛得到的壳聚糖分解菌的种子液按照2%(V/V)的接种量接种于装有100 mL发酵培养基的250 mL三角瓶中,30 ℃、160 r/min条件下培养72 h,测定发酵液中的壳聚糖酶的活力,选择酶活最高的菌株进行下一步研究。
1.3.2 菌种鉴定
形态观察:菌株在筛选平板上培养5~7 d后,观察菌落生长情况,挑取菌落边缘菌丝,乳酸石炭酸棉蓝染液染色后,在油镜下观察菌丝以及分生孢子等形态特征,参照《真菌鉴定手册》[35]进行形态学鉴定。
分子生物学鉴定:依照真菌基因组脱氧核糖核酸(deoxyribonucleic acid,DNA)抽提试剂盒说明提取DNA,利用真菌18S rDNA通用引物(NS1/NS7)进行聚合酶链式反应(polymerase chain reaction,PCR)扩增,扩增产物送至生工生物工程(上海)股份有限公司测序。测序结果在美国国家生物技术信息中心(nationalcenter for biotechnology information,NCBI)网站中进行基于局部比对算法的搜索工具(basic local alignment search tool,BLAST)比对,利用MEGA7.0软件邻接(Neighbor-Joining,NJ)法构建系统发育树。
1.3.3 粗酶液的制备
菌株在种子培养基中培养48 h后,以2%接种量接种至装有100 mL发酵培养基的250 mL摇瓶中,30 ℃、160 r/min摇床培养72 h后,发酵液12 000 r/min离心10 min,上清液即为粗酶液。
1.3.4 壳聚糖酶活测定
取1 mL适当稀释的粗酶液,加3 mL 1%胶体壳聚糖底物,记作实验组;另取1 mL粗酶液沸水浴灭活10 min后,加入3 mL 1%胶体壳聚糖,记作灭酶组。两组同时置于50 ℃恒温水浴锅中反应20 min后,于沸水浴中10 min终止酶解反应,分别加入3 mL DNS试剂,摇匀,沸水浴10 min显色,冷却至室温后,8 000 r/min离心10 min,取上清液定容至25 mL,于波长540 nm处测吸光度值A540nm,以蒸馏水加DNS为空白。以氨基葡萄糖盐酸盐含量为横坐标(x),吸光度值A540nm为纵坐标(y)绘制标准曲线,得到标准曲线方程y=0.033 5x+0.024 2(R2=0.990 4),计算壳寡糖含量。酶活定义:每分钟催化产生1 μmol氨基葡萄糖所需的酶量为一个酶活力单位(U/mL)。酶活计算公式:
式中:N为稀释倍数;n为氨基葡萄糖盐酸盐物质的量,μmol;t为反应时间,min;V为发酵液体积,mL。
1.3.5 产壳聚糖酶培养基组成和培养条件优化单因素试验
1.3.5.1 碳源种类及碳源添加量
以发酵培养基为基础,分别以10 g/L的胶体壳聚糖、胶体几丁质、葡萄糖、蔗糖及5 g/L胶体壳聚糖+5 g/L葡萄糖作为培养基中的碳源,考察碳源种类对发酵产壳聚糖酶的影响。在确定最适碳源种类为复合碳源的基础上,固定胶体壳聚糖添加量为5 g/L,考察不同葡萄糖添加量(1 g/L、3 g/L、5 g/L、7 g/L、9 g/L)对发酵产壳聚糖酶的影响。
1.3.5.2 氮源及氮源添加量
在确定最佳碳源的基础上,分别以2 g/L的硫酸铵、硝酸钠、牛肉膏、尿素、蛋白胨作为培养基中的氮源,考察氮源种类对发酵产壳聚糖酶的影响。在确定最适碳源为尿素的基础上,考察不同尿素添加量(1 g/L、1.5 g/L、2 g/L、2.5 g/L、3 g/L)对发酵产壳聚糖酶的影响。
1.3.5.3 培养基初始pH
在确定培养基最佳碳源、氮源的基础上,分别调节发酵培养基的初始pH为4.0、5.0、6.0、7.0、8.0,考察培养基初始pH对发酵产壳聚糖酶的影响。
1.3.5.4 发酵温度
在确定最适初始pH的基础上,分别在20 ℃、25 ℃、30 ℃、35 ℃、40 ℃的条件下发酵培养,考察发酵温度对发酵产壳聚糖酶的影响。
1.3.5.5 摇床转速
在确定最适培养基初始pH、发酵温度的基础上,分别调整摇床转速为120 r/min、140 r/min、160 r/min、180 r/min、200 r/min,考察摇床转速对发酵产壳聚糖酶的影响。
1.3.5.6 发酵时间
在确定最适培养基初始pH、发酵温度、摇床转速的基础上,分别调整菌株发酵时间为24 h、48 h、72 h、96 h、120 h,考察发酵时间对发酵产壳聚糖酶的影响。
1.3.6 产壳聚糖酶培养基组成和培养条件优化响应面试验
1.3.6.1 Plackett-Burman(PB)试验
在单因素试验结果的基础上,以壳聚糖酶活力(Y)为响应值,以葡萄糖添加量(A)、尿素添加量(B)、培养基初始pH值(C)、发酵温度(D)、摇床转速(E)、发酵时间(F)为考察因素,利用Design-Expert 13软件进行PB试验设计,筛选影响壳聚糖酶活的重要变量,PB试验因素与水平见表1。
表1 Plackett-Burman试验设计因素与水平
Table 1 Factors and levels of Plackett-Burman experimental design

1.3.6.2 最陡爬坡试验
根据PB试验筛选出3个最显著因素,利用拟合方程中3因素的变量系数确定爬坡方向和变化步长,进行最陡爬坡试验,根据最陡爬坡试验确定Box-Behnken试验中心点及最陡爬坡方向。
1.3.6.3 Box-Behnken(BB)试验
在单因素试验和PB试验的基础上,选取对壳聚糖酶活影响最显著的3个因素葡萄糖添加量(A)、培养基初始pH(B)、发酵温度(C)为自变量,以壳聚糖酶活力(Y)为响应值,设计3因素3水平的Box-Behnken试验优化培养基组成及培养条件,BB试验因素与水平见表2。
表2 Box-Behnken试验设计因素与水平
Table 2 Factors and levels of Box-Behnken experimental design

1.3.7 酶解产物分析
采用薄层层析法(thin-layer chromatography,TLC)进行酶解产物分析,以脱乙酰蟹壳制备的10%胶体壳聚糖(pH 5.5)为底物,与粗酶液按体积比3∶1混合,于55 ℃分别反应30 min、40 min、50 min、60 min。反应终止后,沸水浴处理10 min,随后以8 000 r/min离心10 min,取上清液作为点样样品,以乙酸∶水∶正丁醇∶氨水体积比10∶10∶20∶1.5为展层剂,0.5%茚三酮(乙醇溶液)为显色剂,壳寡糖标准品(聚合度3~7)为标样,通过比较酶解产物与壳寡糖标准品的比移值(Rf值),判断酶切产物壳寡糖的聚合度。比移值计算公式为:Rf=样品斑点中心移动的距离/展层剂前沿移动的距离。
1.3.8 数据处理
本研究采用Excel 2019进行数据处理,利用Design-Expert 13软件进行PB试验、最陡爬坡试验及Box-Behnken试验设计,用SPSS 20.0对试验结果进行方差分析,MEGA7.0软件构建系统发育树。
2 结果与分析
2.1 产壳聚糖酶菌株的筛选与鉴定
以胶体壳聚糖作为唯一碳源,以透明圈法从掩埋虾蟹壳的土壤中筛选出1株产壳聚糖酶酶活最高的菌株WK005,菌株WK005菌落特征及分生孢子见图1。由图1a可知,菌落初期为白色棉絮状菌丝,质地致密,3~5 d时,菌落出现淡紫色同心轮纹,边缘整齐,随培养时间延长,同心环纹色泽加深,范围扩大;由图1b可知,分生孢子为卵圆形或椭圆形,呈链状,着生于帚状分生孢子梗。
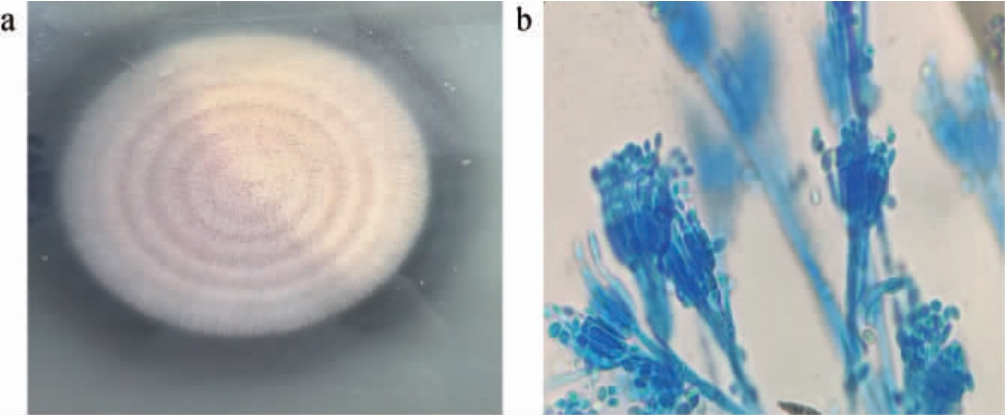
图1 菌株WK005菌落特征(a)及分生孢子油镜图(100X)(b)
Fig.1 Colony characteristics of strain WK005 (a) and oil microscope image of conidiospores (100X) (b)
基于菌株18SrDNA序列,利用MEGA7.0软件绘制系统发育树,结果见图2。

图2 基于18S rDNA基因序列菌株WK005的系统发育树
Fig.2 Phylogenetic tree of strain WK005 based on 18S rDNA gene sequence
由图2可知,菌株WK005与Purpureocillium lilacinum AH20的亲缘关系最近,位于同一分支,综合形态学特征,鉴定菌株WK005为淡紫紫孢菌(Purpureocillium lilacinum)。
2.2 产壳聚糖酶培养基组成和培养条件优化单因素试验
2.2.1 不同碳源种类及碳源添加量对菌株产壳聚糖酶的影响
不同碳源种类及碳源添加量对菌株产壳聚糖酶的影响见图3。由图3A可知,培养基碳源为5 g/L胶体壳聚糖+5 g/L葡萄糖时,菌株产壳聚糖酶活最高,为7.12 U/mL,其次为10 g/L胶体壳聚糖组,壳聚糖酶活为6.09 U/mL,二者酶活显著高于其他组(P<0.05),且均含有胶体壳聚糖,说明淡紫紫孢菌WK005所产壳聚糖酶为诱导酶,需要底物壳聚糖的诱导才能大量合成。复合碳源酶活最高,可能是因为葡萄糖是快速碳源,能够为菌株提供能量(腺苷三磷酸(adenosine triphosphate,ATP))和碳骨架,促进菌体生长繁殖,从而增强产壳聚糖酶能力[36]。因此,选择复合碳源(胶体壳聚糖+葡萄糖)为最佳碳源种类。
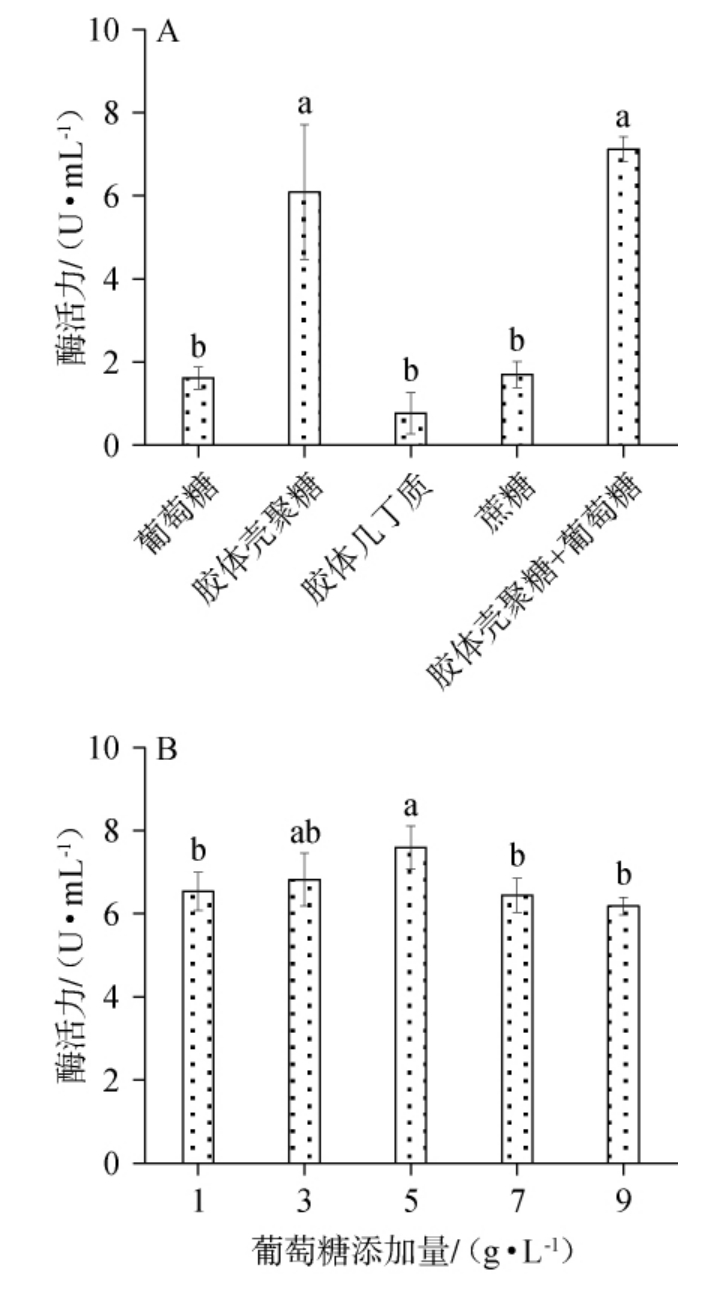
图3 不同碳源种类(A)及葡萄糖添加量(B)对菌株产壳聚糖酶的影响
Fig.3 Effect of different carbon source types (A) and glucose addition (B) on chitosanase production by the strain
相同指标不同小写字母表示差异显著(P<0.05)。下同。
由图3B可知,在固定胶体壳聚糖添加量为5 g/L的基础上,随葡萄糖添加量的增加,菌株WK005产壳聚糖酶活性呈先上升后下降的趋势,葡萄糖添加量为5 g/L时,壳聚糖酶活最高,为7.59 U/mL,当葡萄糖添加量>5 g/L时,壳聚糖酶活呈下降趋势。可能是因为过多的葡萄糖因为分解代谢产物阻遏作用而抑制菌株的产酶活力[37],因此,选择5 g/L胶体壳聚糖+5 g/L葡萄糖为最佳碳源。
2.2.2 不同氮源种类及氮源添加量对菌株产壳聚糖酶的影响不同氮源种类及氮源添加量对菌株产壳聚糖酶的影响见图4。由图4A可知,菌株对氮源的利用范围较广,有机氮和无机氮均可被其利用,以尿素作为氮源时菌株产壳聚糖酶最高,为8.61 U/mL,这与多数真菌对氮源的利用偏好存在差异[33-34,38],推测可能是该菌株对尿素的吸收利用效率较高,可快速分解尿素为 等可利用氮源,为菌体生长及壳聚糖酶合成提供充足的氮代谢前体。因此选择尿素作为培养基最佳氮源种类。
等可利用氮源,为菌体生长及壳聚糖酶合成提供充足的氮代谢前体。因此选择尿素作为培养基最佳氮源种类。
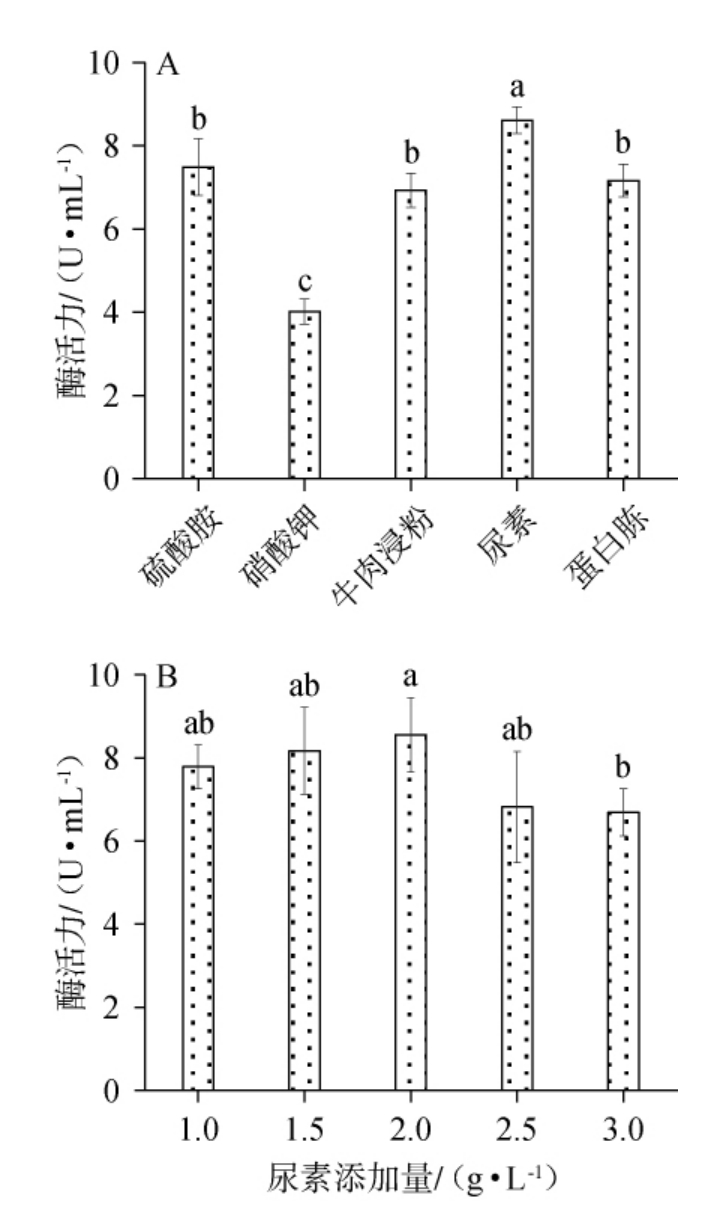
图4 不同氮源种类(A)及尿素添加量(B)对菌株产壳聚糖酶的影响
Fig.4 Effect of different nitrogen source types (A) and urea addition(B) on chitosanase production by the strain
由图4B可知,随着尿素添加量的增加,菌株WK005产壳聚糖酶活性呈先上升后下降的趋势,尿素添加量为2 g/L时壳聚糖酶活最高,为8.56 U/mL,显著高于其他组(P<0.05);继续增大尿素添加量,酶活开始下降,可能是因为高浓度NH4+的积累对菌株产生了代谢抑制作用[39]。因此,选取2 g/L尿素作为最佳氮源。
2.2.3 培养基初始pH对菌株产壳聚糖酶的影响
培养基初始pH值是影响壳聚糖酶合成的重要因素。培养基初始pH对菌株产壳聚糖酶的影响见图5。由图5可知,随着培养基初始pH值的升高,菌株WK005产壳聚糖酶活性呈先上升后下降的趋势,在初始pH为5时,壳聚糖酶活最高为10.19 U/mL。当pH偏离该适宜范围时,酶活均出现明显下降:在pH4和pH8条件下,酶活分别降低了37.1%和49.5%。这可能是因为过高或过低的pH会影响酶蛋白或底物的构象,影响其相互作用,从而抑制酶的合成与功能。因此选取pH 5为培养基最适初始pH。
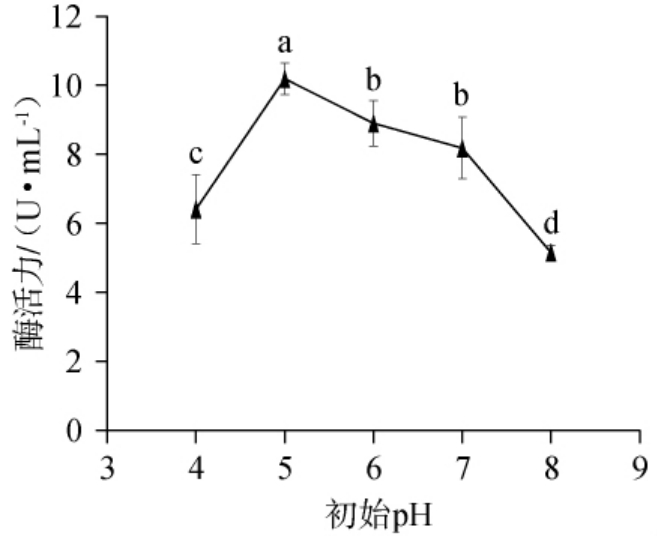
图5 培养基初始pH对菌株产壳聚糖酶的影响
Fig.5 Effect of initial pH of medium on chitosanase production by the strain
2.2.4 发酵温度对菌株产壳聚糖酶的影响
温度是影响微生物生长和代谢产物合成的重要环境因素之一,温度变化对酶活性具有显著影响。发酵温度对菌株产壳聚糖酶的影响见图6。由图6可知,随着发酵温度的升高,壳聚糖酶活力呈先升高后下降的趋势,当发酵温度为30 ℃时,壳聚糖酶活最高为11.66 U/mL,显著高于其他温度条件组(P<0.05)。发酵温度高于35 ℃时,酶活下降显著,在发酵温度40 ℃时只有最高酶活的20.6%。这表明在适宜范围内,温度升高,有助于促进菌体代谢和酶合成速率;当温度过高时,菌体蛋白质及核酸结构易受损,从而导致生长受限及酶合成能力下降[40]。因此选择30 ℃为最佳发酵温度。
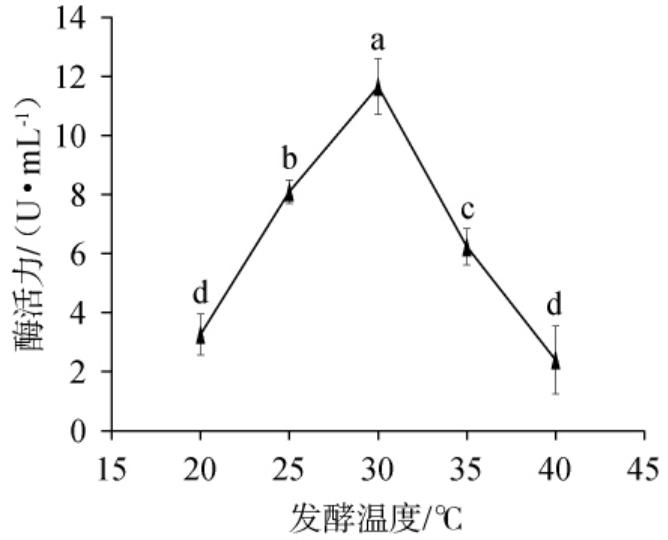
图6 发酵温度对菌株产壳聚糖酶的影响
Fig.6 Effect of fermentation temperature on chitosanase production by the strain
2.2.5 摇床转速对菌株产壳聚糖酶的影响
摇床转速是影响溶氧水平、底物利用率和菌体生理状态的重要参数。由图7可知,随着摇床转速的升高,壳聚糖酶酶活呈现先升高后下降的趋势,在摇床转速为180 r/min时酶活最高,为13.30 U/mL,之后酶活开始下降。可能是因为在较低转速下,溶氧不足限制了菌体生长与酶的合成;而过高转速时,液体剪切力增大,易损伤菌体,破坏酶蛋白结构,同时过多的泡沫会降低实际有效溶氧量,从而抑制酶的合成[41]。因此选择180 r/min为最优转速。
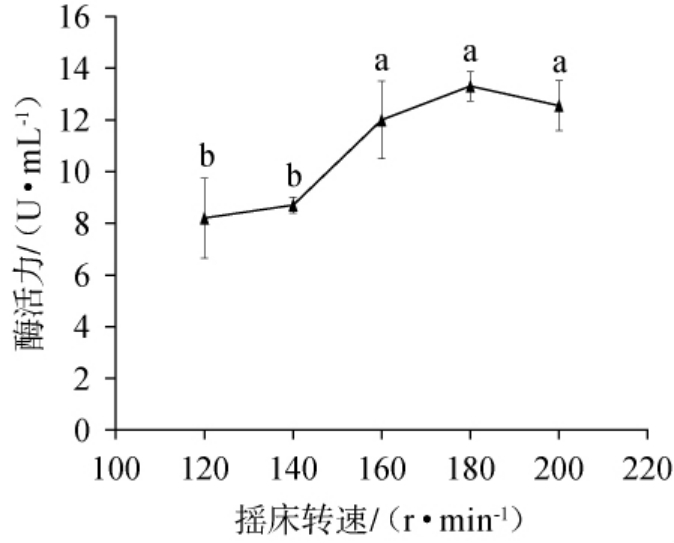
图7 摇床转速对菌株产壳聚糖酶的影响
Fig.7 Effect of shaking speed on chitosanase production by the strain
2.2.6 发酵时间对菌株产壳聚糖酶的影响
发酵时间对菌株产壳聚糖酶的影响见图8。由图8可知,随发酵时间延长,壳聚糖酶酶活呈现先升高后下降的趋势,发酵时间低于96 h时,酶活随着发酵时间的延长逐步提升,24~48 h时,菌株处于适应期,相对酶活较低;在48~72 h,酶活增加迅速,此时菌株处于生长累积期,底物诱导效应明显,发酵96 h时酶活达到最高,为15.65 U/mL,之后酶活开始下降。可能是随着培养时间的延长,发酵培养基中营养物质损耗,代谢废物累积,菌体老化,导致产酶能力下降。因此选择96 h为最优发酵时间。
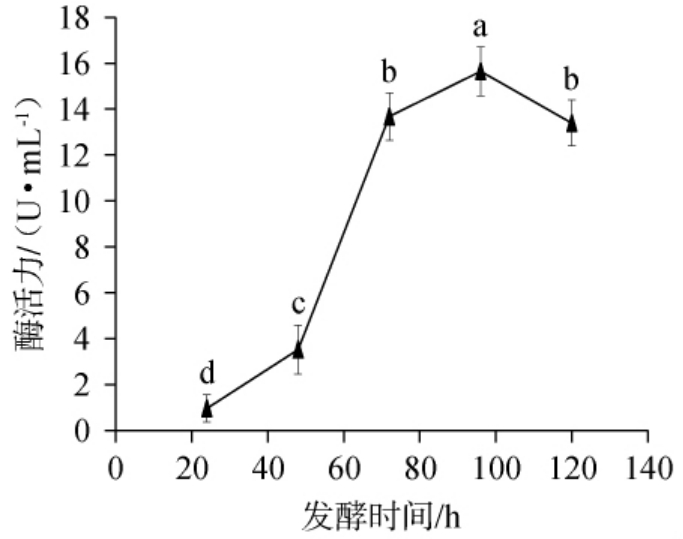
图8 发酵时间对菌株产壳聚糖酶的影响
Fig.8 Effect of fermentation time on chitosanase production by the strain
2.3 产壳聚糖酶培养基组成和培养条件优化响应面试验
2.3.1 Plackett-Burman试验
在单因素试验的基础上,以壳聚糖酶酶活为响应值(Y),以葡萄糖添加量(A)、尿素添加量(B)、初始pH(C)、发酵温度(D)、摇床转速(E)和发酵时间(F)为考察因素设计Plackett-Burman试验,Plackett-Burman试验设计及结果见表3,方差分析结果见表4。
表3 Plackett-Burman试验设计及结果
Table 3 Design and results of Plackett-Burman experiment
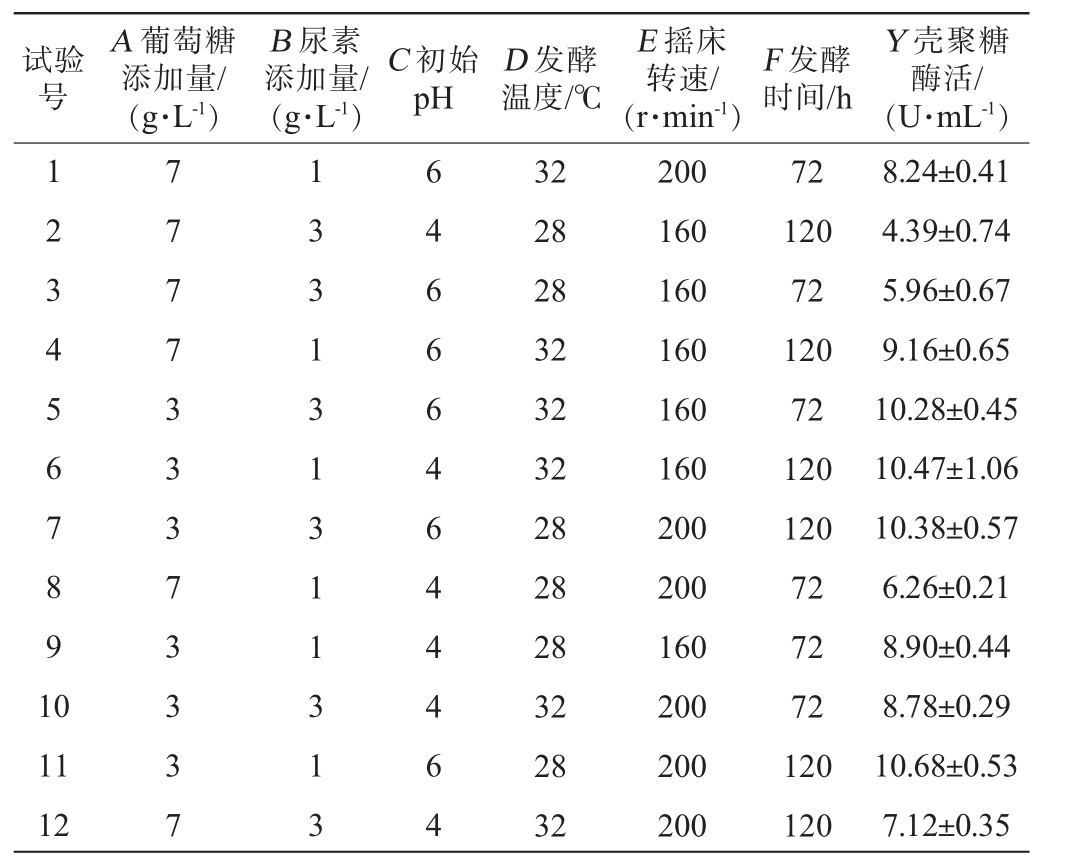
表4 Plackett-Burman试验回归模型方差分析
Table 4 Variance analysis of regression model of Plackett-Burman experiment
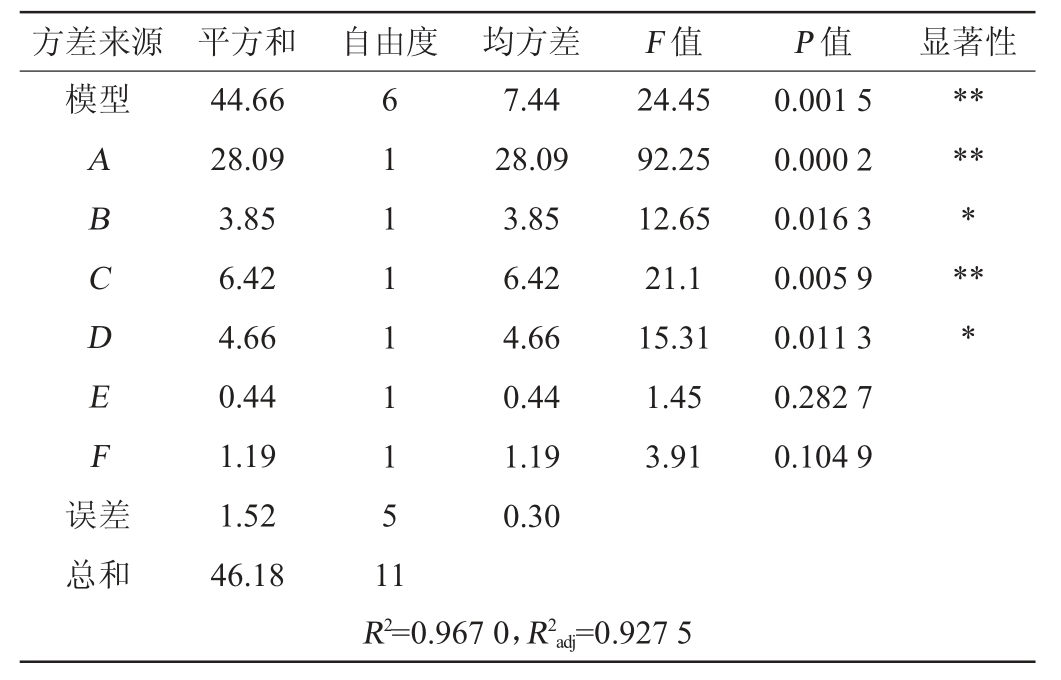
注:“**”表示对结果影响极显著(P<0.01);“*”表示对结果影响显著(P<0.05)。
采用Design Expert 13软件对表3数据进行回归分析,得到各变量与壳聚糖酶活之间的模型拟合方程:Y=8.39-1.53A-0.566 7B+0.731 7C+0.623 3D+0.191 7E+0.315 0F。
拟合方程中葡萄糖添加量(A)和尿素添加量(B)的系数为负值,具有负效应,增加其水平会降低酶活;初始pH(C)、发酵温度(D)、摇床转速(E)和发酵时间(F)的系数为正值,具有正效应,提高其水平会升高酶活。
由表4可知,该回归模型极显著(P=0.001 5<0.01),说明所选因素对酶活的影响具有统计学意义。模型的决定系数R2=0.967 0,调整决定系数R2adj=0.927 5,表明该模型能解释96.7%的响应值变异,拟合效果良好。对各因素的显著性分析表明,葡萄糖添加量(A)、初始pH(C)对壳聚糖酶活的影响极显著(P<0.01);尿素添加量(B)和温度(D)对壳聚糖酶活的影响显著(P<0.05);摇床转速(E)和发酵时间(F)对壳聚糖酶活的影响不显著(P>0.05)。根据F值大小(表4),各因素对酶活的影响程度排序为:葡萄糖添加量(A)>初始pH(C)>发酵温度(D)>尿素添加量(B)。综合回归方程系数和方差分析结果,最终选取葡萄糖添加量(A)、初始pH(C)和发酵温度(D)作为关键影响因素,用于后续响应面优化试验。
2.3.2 最陡爬坡试验
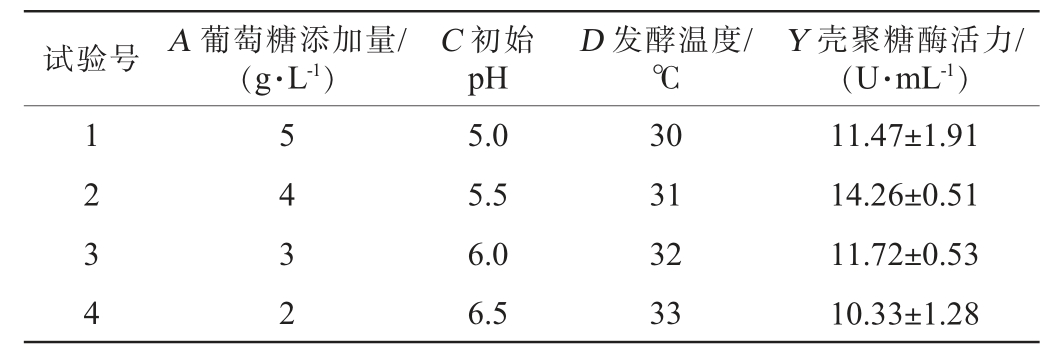
在PB试验基础上进行最陡爬坡试验,以PB试验设计的中心点作为步移的起点,最陡爬坡试验设计及结果见表5。由表5可知,第2组试验产壳聚糖酶活最高,因此采用葡萄糖添加量为4 g/L,初始pH 5.5,发酵温度31 ℃作为Box-Behnken试验的中心点。
表5 最陡爬坡试验设计及结果
Table 5 Design and results of the steepest ascent experiment
2.3.3 响应面试验
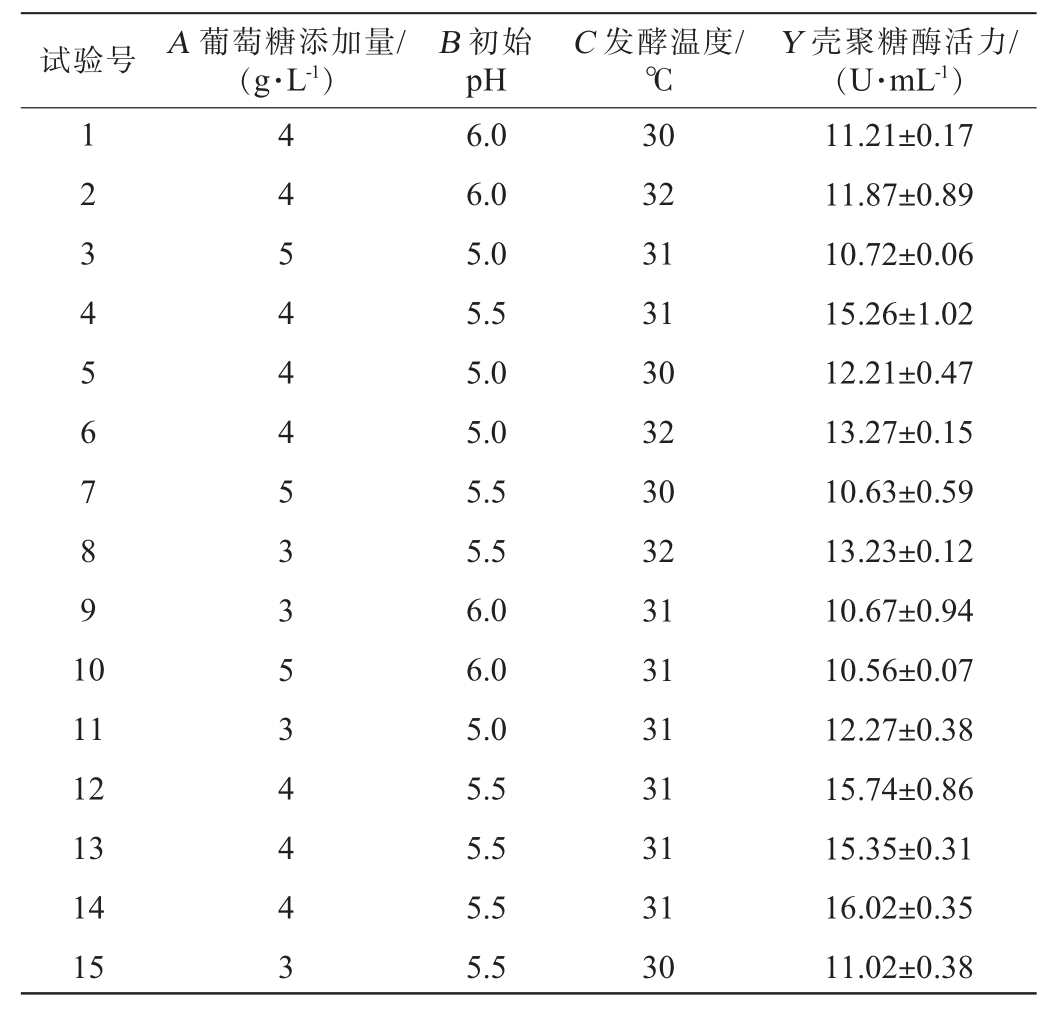
Box-Behnken试验设计及结果见表6,方差分析见表7。
表6 Box-Behnken响应面试验设计及结果
Table 6 Design and results of Box-Behnken response surface experiment
续表
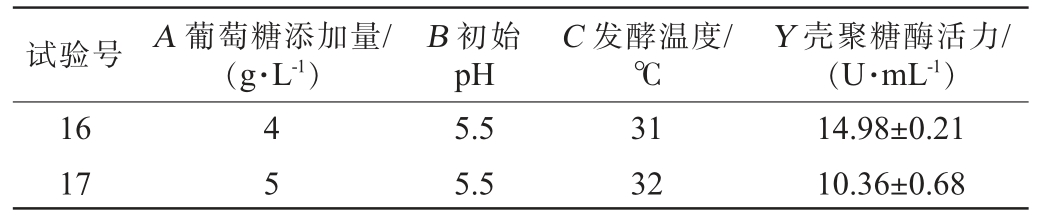
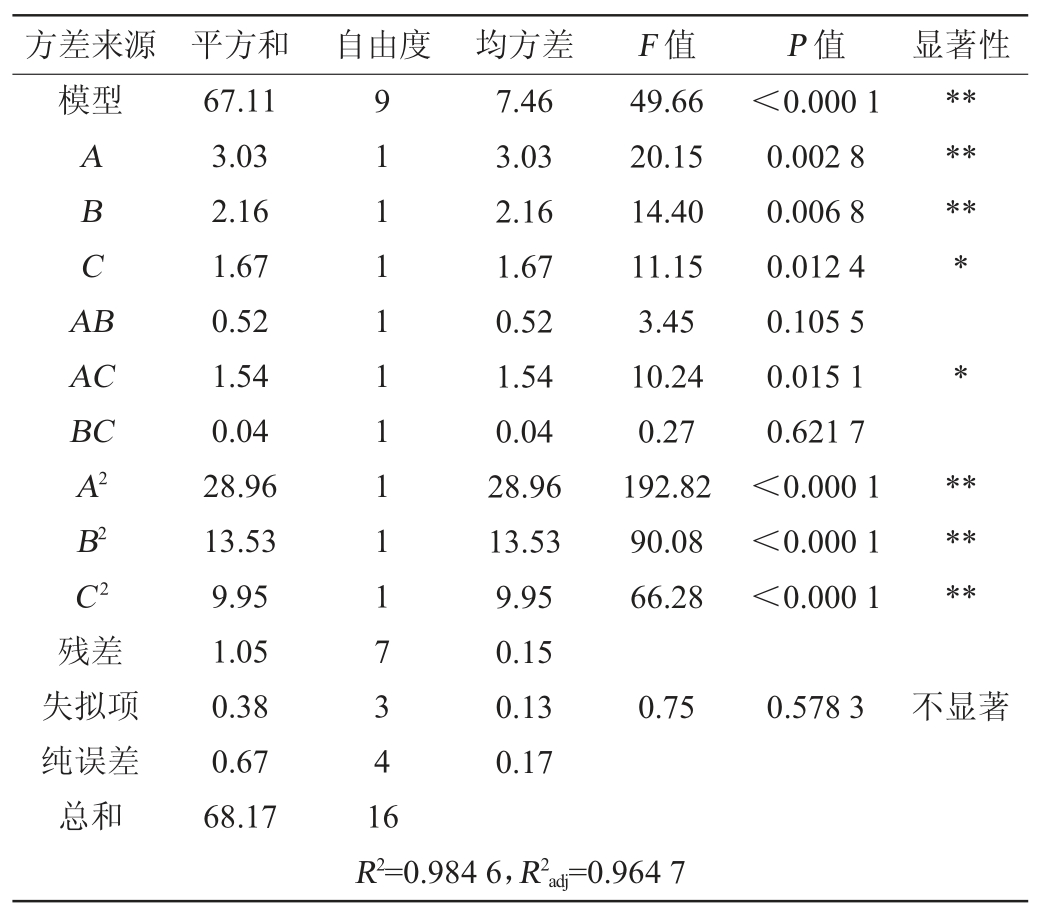
表7 Box-Behnken响应面试验回归模型方差分析
Table 7 Variance analysis of regression model of Box-Behnken response surface experiment
注:“**”表示对结果影响极显著(P<0.01);“*”表示对结果影响显著(P<0.05)。
应用Design Expert 13软件对表6数据拟合得到菌株发酵产壳聚糖酶活力(Y)对试验因素葡萄糖添加量(A)、初始pH(B)、发酵温度(C)的三元二次多项回归方程:
由表7可知,回归模型极显著(P<0.01),失拟项P=0.578 3不显著(P>0.05),模型拟合度良好,相关系数R2=0.984 6,调整决定系数R2adj=0.964 7,表明模型可信度较高,可用于对试验结果进行分析和预测。
由表7中的F值可知,各因素影响菌株产酶活力的主次顺序为A>B>C。根据P值可知,一次项A、B,二次项A2、B2、C2对菌株产酶活力影响极显著(P<0.01),一次项C、交互项AC对结果影响显著(P<0.05),其他项对结果影响不显著(P>0.05)。
用Design-Expert 13软件绘制拟合3个因素间交互作用对壳聚糖酶活影响的响应曲面图,结果见图9。由图9可知,葡萄糖添加量与发酵温度(AC)的交互作用对酶活力影响显著(P<0.05),其响应面图较为陡峭;而葡萄糖添加量和发酵初始pH(AB)、发酵初始pH和发酵温度(BC)间交互作用对酶活力影响不显著(P>0.05),其对应的响应面图相对平缓,这与表7中的方差分析结果一致。
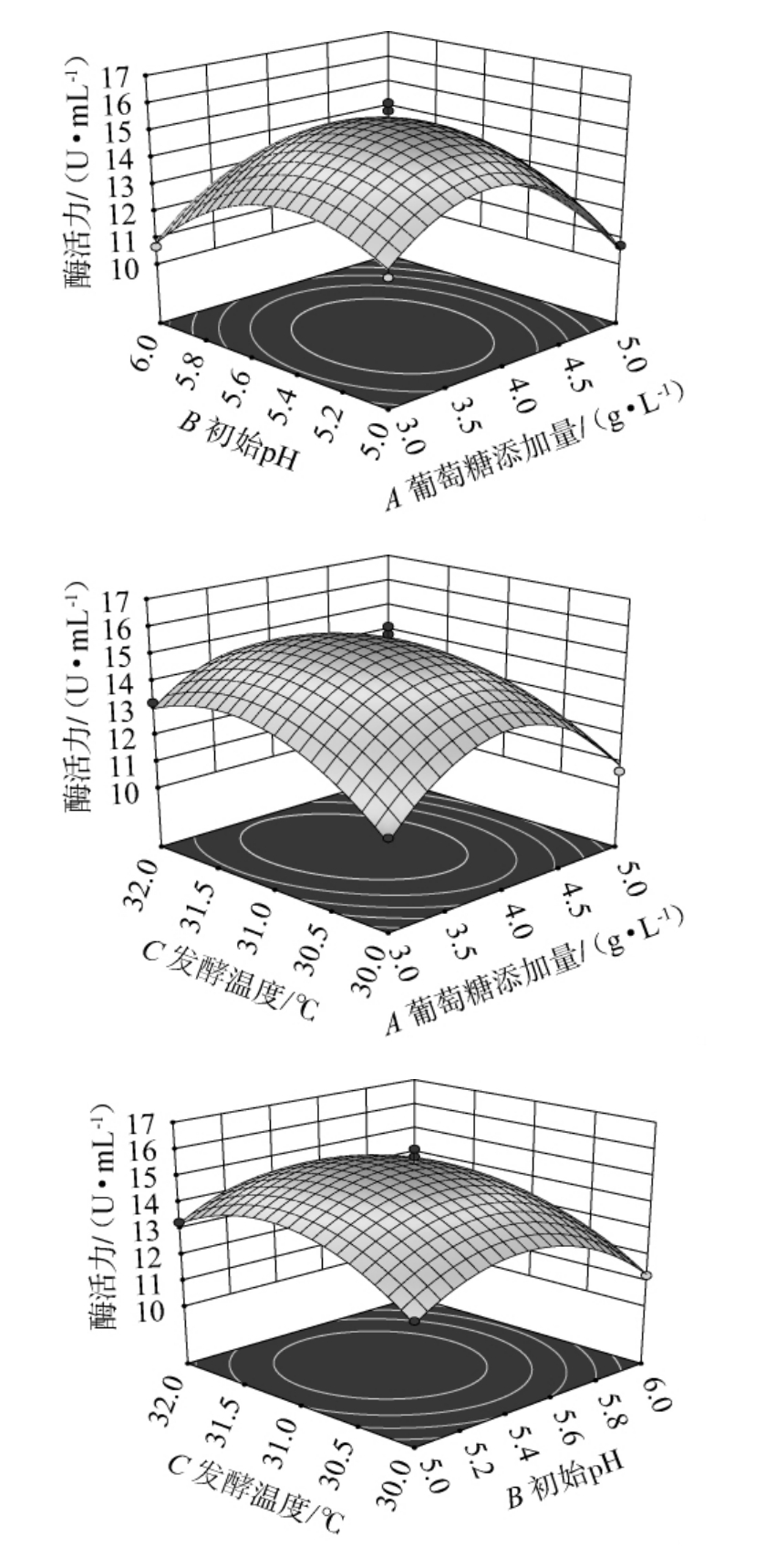
图9 各因素交互作用对壳聚糖酶活影响的响应曲面图
Fig.9 Response surface polts of the effect of the interaction of various factors on chitosanase activity
2.4 验证试验
由软件Design-Expert 13获得最优工艺条件:葡萄糖添加量为3.85 g/L、发酵温度为31.2 ℃、培养基初始pH为5.4,在此条件下壳聚糖酶活力预测值为15.60 U/mL。考虑到实际操作的可行性,将最佳条件调整为葡萄糖添加量3.9 g/L、发酵温度31 ℃、初始pH 5.5,在此条件下进行3次平行验证试验,结果所得壳聚糖酶活为16.29 U/mL,与预测值接近,表明此模型可以较好的预测淡紫紫孢菌WK005菌株产壳聚糖酶活力。
2.5 壳聚糖酶粗酶液水解特性及产物
以脱乙酰基蟹壳(脱乙酰度≥85%)制备的10%胶体壳聚糖为底物,通过薄层层析分析不同酶解时间(30~60 min)条件下壳聚糖酶的水解产物特征,结果见图10。由图10可知,该酶能够高效且特异性地水解壳聚糖,主要生成聚合度(DP)为4~6的壳寡糖,并且随着酶解时间的延长,产物中始终未检测到单糖或二糖,表明该壳聚糖酶属于典型的内切酶。

图10 壳聚糖酶酶解产物薄层层析结果
Fig.10 Thin-layer chromatography results of the enzymatic hydrolysis products of chitosanase
a为聚合度3~7壳寡糖标准样;1为反应30 min;2为反应40 min;3为反应50 min;4为反应60 min。
3 结论
本研究采用透明圈初筛和摇瓶复筛的方法从长期掩埋虾蟹壳的土壤中分离获得一株产壳聚糖酶的真菌WK005,结合形态学观察和18S rRNA基因序列分析,鉴定该菌株为淡紫紫孢菌(Purpureocillium lilacinum)。利用单因素试验和响应面试验对发酵产酶条件进行优化,确定其产壳聚糖酶最佳条件为:培养基组成为5 g/L胶体壳聚糖,3.9 g/L葡萄糖,2 g/L尿素,0.5 g/L硫酸镁,1 g/L磷酸二氢钾,培养基初始pH值5.5,发酵温度31 ℃,发酵时间96 h,摇床转速180 r/min。在此条件下,其产壳聚糖酶活最高可达16.29 U/mL,较优化前(6.09 U/mL)提高了1.67倍。薄层层析结果表明,该菌株所产壳聚糖酶为内切型酶,其酶解产物主要为聚合度4~6的壳寡糖。本研究为壳聚糖酶的低成本工业化生产提供了具有应用潜力的候选菌株。
[1] MENEGAZZO F,GHEDINI E,SIGNORETTO M.5-Hydroxymethylfurfural(HMF)production from real biomasses[J].Molecules,2018,23(9):2201.
[2] YANG H,GOZAYDIN G,NASARUDDIN R R,et al.Toward the shellbiorefinery:processing crustacean shell waste using hot water and carbonic acid[J].Acs Sust Chem Eng,2019,7(5):5532-5542.
[3] 邱月,岳澳冬,张建友.基于超声辅助深共晶溶剂法的废弃虾蟹壳中虾青素高效提取[J].食品与发酵工业,2025,51(23):277-285.
[4] BOENISH R,KRITZER J P,KLEISNER K,et al.The global rise of crustacean fisheries[J].Front Ecology Environ,2022,20(2):102-110.
[5] MUKHTAR AHMED K B,KHAN M M A,SIDDIQUI H,et al.Chitosan and its oligosaccharides,a promising option for sustainable crop production-a review[J].Carbohydr Polym,2020,227:115331.
[6]章晔敏,邵一凡,熊妍妍,等.响应面法优化鹿皮曲霉ZJOU-AC1产壳聚糖酶的发酵条件[J].中国酿造,2016,35(11):93-98.
[7] SUN T,QIN Y Y,XU H L,et al.Antibacterial activities and preservative effect of chitosan oligosaccharide Maillard reaction products on Penaeus vannamei[J].Int J Biol Macromol,2017,105(Pt 1):764-768.
[8] LIANG T W,CHEN W T,LIN Z H,et al.An amphiprotic novel chitosanase from Bacillus mycoides and its application in the production of chitooligomers with their antioxidant and anti-inflammatory evaluation[J].Int J Mol Sci,2016,17(8):1302.
[9] LU B,CHEN X,OUYANG X,et al.The roles of novel chitooligosaccharide-peanut oligopeptide carbon dots in improving the flavor quality of Chinese cabbage[J].Food Chem: X,2023,20:100963.
[10] 季珂,李恒,龚劲松,等.酶法制备壳寡糖及其抗肿瘤活性评价[J].食品与生物技术学报,2021,40(6):93-99.
[11] MAEDA Y,KIMURA Y.Antitumor effects of various low-molecularweight chitosans are due to increased natural killer activity of intestinal intraepithelial lymphocytes in sarcoma 180-bearing mice[J]. J Nutrit,2004,134(4):945-950.
[12] LIU Y,XING R,LIU S,et al.Effects of chitooligosaccharides supplementation with different dosages,molecular weights and degrees of deacetylation on growth performance,innate immunity and hepatopancreas morphology in Pacific white shrimp (Litopenaeus vannamei)[J].Carbohydr Polym,2019,226:115254.
[13] XU Q,AZZAM M M M,ZOU X,et al.Effects of chitooligosaccharide supplementation on laying performance,egg quality,blood biochemistry,antioxidant capacity and immunity of laying hens during the late laying period[J].Ital J Anim Sci,2020,19(1):1180-1187.
[14] 薛萍红,邓运鸿,田学琴,等.生物法制备壳寡糖的研究进展[J].微生物学报,2025,65(5):453-466.
[15] 张沛尧,赵宁,席军,等.壳寡糖的制备及应用的研究进展[J].中国调味品,2024,49(11):205-212.
[16] 龚香艺,吴静,邬敏辰.真菌壳聚糖酶研究进展[J].食品科学,2012,33(17):308-311.
[17] 史凤玉,蔡爱军,田辉,等.来自拟青霉属真菌的壳聚糖酶的分离纯化、理化性质及降解产物的分析(英文)[J].菌物学报,2013,32(4):721-728.
[18] BANERJEE G,RAY A K.Impact of microbial proteases on biotechnological industries[J]. Biotechnol Genetic Eng Rev,2017,33(2): 119-143.
[19] 姚炎,李菁菁,张雨萌,等.溜曲霉M3b产壳聚糖酶的固体发酵工艺优化及酶学性质[J].华中农业大学学报,2022,41(5):215-222.
[20] 阎贺静,刘畅,时月,等.碳源对烟曲霉WHSW-01产壳聚糖酶的诱导条件优化[J].食品与发酵工业,2015,41(5):110-115.
[21] SINHA S,CHAND S,TRIPATHI P.Enzymatic production of glucosamine and chitooligosaccharides using newly isolated exo-β-d-glucosaminidase having transglycosylation activity[J].Biotech,2016,6(1):1036-1041.
[22] AKTUGANOV G E,GALIMZIANOVA N F,GILVANOVA E A,et al.Purification and characterization of exo-β-1,4-glucosaminidase producedby chitosan-degrading fungus,Penicillium sp.IB-37-2A[J].World J Microb Biot,2019,35(2):331-337.
[23] SILVA L,HONORATO T L,FRANCO T T,et al.Optimization of chitosanase production by Trichoderma koningii sp.under solid-state fermentation[J].Food Bioproc Technol,2012,5(5):1564-1572.
[24] 何灏彦.卷枝毛霉发酵产壳聚糖酶的条件优化[J].化学与生物工程,2012,29(12):89-91.
[25] STRUSZCZYK K,SZCZ SNA-ANTCZAK M,WALCZAK M,et al.Isolation and purification of Mucor circinelloides intracellular chitosanolytic enzymes[J].Carbohydr Polym,2009,78(1):16-24.
[26] JATALA P,KALTENBACH R,BOCANGEL M.Biological control of Meloidogyne incognita acrita and Globodera pallida on potatoes[J]. J Nematol,1979,11(4):303.
[27] 袁梦蕾,范乐乐,赵雪,等.淡紫紫孢菌微菌核防治黄瓜根结线虫病及土壤环境对其定殖的影响[J].中国生物防治学报,2022,38(4):831-839.
[28] 杨凡,蔡毓新,贾文华,等.淡紫紫孢菌对黄瓜根结线虫的防治效果[J].中国瓜菜,2018,31(7):35-38.
[29] 邓嘉茹,孙龙华,毕可可,等.一株淡紫紫孢菌12ID-1的分离及其对埃及吹绵蚧的致病性[J].林业与环境科学,2019,35(3):63-70.
[30] SHARMA A,SHARMA S,DALELA M.Nematicidal activity of Paecilomyces lilacinus 6029 cultured on Karanja cake medium[J].Microb Pathog,2014,75:16-20.
[31] 韩娜,陶宗娅,代文秀,等.淡紫拟青霉A10的促生特性及其发酵液对印度芥菜幼苗蓄积Cs+的影响[J].农业环境科学学,2019,38(3):485-493.
[32] CHAO C F,CHEN Y Y,CHENG C Y,et al.Catalytic function of a newly purified exo-β-d-glucosaminidase from the entomopathogenic fungus Paecilomyces lilacinus[J].Carbohydr Polym,2013,93(2):615-621.
[33] 赵有玺,龚平,王科力,等.产壳聚糖酶菌株选育及产酶条件研究[J].食品科技,2014,39(5):2-5.
[34] 张馨月,岳晓洁,李铮峥,等.淡紫紫孢菌的筛选、鉴定及产壳聚糖酶固体发酵条件优化[J].中国食品学报,2020,20(4):160-169.
[35] 魏景超.真菌鉴定手册[M].上海:上海科学技术出版社,1979:487-503.
[36] JANTZEN E,JENSEN P R,MOLIN S,et al.Glucose becomes one of the worst carbon sources for E.coli on poor nitrogen sources due to suboptimal levels of cAMP[J].Sci Rep,2016,6:29758.
[37] ADNAN M,ZHENG W,ISLAM W,et al.Carbon catabolite repression in filamentous fungi[J].In J Mol Sci,2017,19(1):48.
[38] 张朝正,李意,赵华.响应面法优化壳聚糖酶发酵培养基[J].中国酿造,2022,41(1):197-203.
[39] GUO W,HE R,ZHAO Y,et al.Imbalanced metabolism induced NH4+accumulation and its effect on the central metabolism of Methylomonas sp.ZR1[J].Int Microbiol,2024,27(1):49-66.
[40] RUSSELL A D.Lethal effects of heat on bacterial physiology and structure[J].Science Progress,2003,86(1-2):115-137.
[41] 黄建平,郑燕.阿卡波糖发酵代谢阶段性溶氧控制的研究与应用[J].中国现代应用药学,2020,37(17):2114-2118.