小曲清香型白酒是我国历史悠久的酒种之一[1],其以高粱、玉米、小麦等粮谷类为原料,采用固态发酵工艺酿制而成,具有酒体清香纯净、自然协调的特点[2]。该酒种符合现代消费者低度化、纯净化需求,有望成为中国白酒国际化的先锋酒品[3]。然而,传统小曲清香型白酒多采用手工操作的单粮固态发酵方式,虽然保持了独特的工艺特色,但也存在设备简单、劳动强度大、生产效率低、产品质量不稳定等问题,严重制约了产业的规模化发展[4-5]。近年来,随着智能化技术的快速发展,众多企业积极引进自动化生产设备,通过板链输送机、自动摊晾机、可移动发酵池等设备实现了对生产过程的精确控制,为小曲清香型白酒的现代化生产提供了典型范例[6-9]。
微生物群落是白酒发酵的核心驱动力,其结构演替直接影响风味物质的合成与积累[10]。随着高通量测序技术的发展,研究者对传统白酒酿造微生物进行了深入解析[11]。针对小曲清香型白酒发酵体系具有微生物多样性高、演替复杂的特征,核心功能菌群主要包括霉菌(如根霉属(Rhizopus))、酵母菌(如酿酒酵母属(Saccharomyces))以及乳酸菌(如乳酸杆菌属(Lactobacillus))等。已有研究者开始关注小曲清香型白酒酿造中不同批次发酵、手工与机械化生产之间微生物群落的差异。晏培等[12]研究表明,小曲清香型白酒手工和机械化酿造过程中乳酸菌均为丰度最高的细菌,核心真菌均为酿酒酵母属(Saccharomyces)、根霉属(Rhizopus)和伊萨酵母属(Issatchenkia)。然而,自动化小曲清香型白酒酿造过程中微生物类群间复杂关系尚不清晰,制约了机械化白酒品质的快速提升[13-14]。尽管自动化酿造工艺与传统工艺相似,但其独特的设备和环境条件(如机械化物料转运、控温糖化等)导致基酒风味组成存在显著差异,这些工艺环节可能改变微生物的定植与代谢路径[15]。因此,研究小曲清香型白酒自动化发酵过程中微生物群落演替规律具有重要意义。
本研究以小曲清香型白酒自动化发酵过程中酒醅为研究对象,采用常规分析方法对其理化指标进行分析,并基于高通量测序技术解析发酵过程中微生物群落组成,对理化指标及微生物菌群进行相关性分析,并结合京都基因与基因组百科全书(KyotoEncyclopediaofGenesandGenomes,KEGG)和碳水化合物活性酶(carbohydrate active enzyme database,CAZy)数据库对功能基因进行注释。旨在揭示自动化酿造中微生物群落的演替规律及关键驱动因素,阐明“自动化工艺-微生物群落-风味物质”的作用机制,为白酒智能化、标准化生产提供理论依据和技术支撑。
1 材料与方法
1.1 材料与试剂
酒醅样品采集自四川泸州一家自动化酿造白酒生产工厂,选取了同一批次的3个独立发酵槽车,分别在发酵第3天、第5天、第7天、第12天和第15天取样(编号分别为D3、D5、D7、D12、D15)。取样时从每个发酵槽车的上部、中部和下部采集取样,并充分混合均匀,立即装入无菌袋中于-20 ℃冷冻保存,备用。
氢氧化钠、酒石酸钾钠、无水硫酸铜、盐酸、硫酸、葡萄糖、亚甲基蓝、无水乙醇、碘、甲醛、邻苯二甲酸氢钾(均为分析纯):成都市科隆化学品有限公司;土壤基因组脱氧核糖核酸(deoxyribonucleic acid,DNA)提取试剂盒:天根生化科技(北京)有限公司。
1.2 仪器与设备
CHG-9090B智能型电热恒温鼓风干燥箱:上海琅玕实验设备有限公司;YP20002B电子分析天平(精度0.1 mg):上海力辰邦西仪器科技有限公司;HC-2517高速离心机、HC-3018R高速冷冻离心机:安徽中科中佳科学仪器有限公司;NanoDrop2000超微量分光光度计:Thermo Fisher Scientific;DHG-9075A电热炉:上海齐欣科学仪器有限公司;Illumina NovaSeq高通量测序平台:美国Illumina公司;Gene Amp 9700型聚合酶链式反应(polymerase chain reaction,PCR)仪:美国ABI公司。
9700型聚合酶链式反应(polymerase chain reaction,PCR)仪:美国ABI公司。
1.3 方法
1.3.1 理化指标测定
水分的测定:参考GB/T 5009.3—2016《食品中水分的测定》;pH和酸度测定:参考DB 34/T 2264—2014《固态发酵酒醅分析方法》;淀粉的测定:参考GB/T 5009.9—2023《食品中淀粉的测定》;还原糖的测定:参考GB/T 5009.7—2016《食品中还原糖的测定》[16]。
1.3.2 DNA提取、PCR扩增及高通量测序
采用土壤基因组脱氧核糖核酸(DNA)提取试剂盒提取酒醅样本的宏基因组DNA。以提取的DNA为模板,其中,采用引物338F(5'-ACTCCTACGGGAGGCAGCAG-3')和806R(5'-GGACTACHVGGGTWTCTAAT-3')对细菌16S rRNA基因序列中的V3~V4区进行扩增[17];采用通用引物ITS1F(5'-CTTGGTCATTTAGAGGAAGTAA-3')和ITS2(5'-GCTGCGTTCTTCATCGATGC-3')对真菌ITS区进行扩增。PCR扩增体系(25 μL):10×PCR Buffer 2.5 μL,脱氧核糖核苷三磷酸(deoxy-ribonucleoside triphosphate,dNTP)Mixture(2.5mmol/L)2μL,上下游引物(10μmol/L)各0.5 μL,Taq DNA聚合酶(5 U/μL)0.2 μL,模板DNA 1 μL,双蒸水(ddH2O)18.3 μL。PCR扩增条件:95 ℃预变性5 min;95 ℃变性30 s,55 ℃退火30 s,72 ℃延伸45 s,30个循环;72 ℃终延伸10 min。扩增结束后,将检测合格的PCR产物送往上海美吉生物医药科技有限公司进行Illumina NovaSeq高通量测序。
1.3.3 序列质控和数据分析
为确保后续分析的准确性和可靠性,首先利用Fastp v0.23.0软件对原始测序数据进行严格的质量控制(quality control,QC)。该步骤去除序列长度低于50 bp、平均质量值(Phred score)低于20,含有未知碱基(N)的reads,最终保留高质量的配对末端reads(pair-end reads)和单末端reads(single-end reads)。随后,利用拼接软件MEGAHIT v1.1.2对不同样本的高质量序列进行重叠群(Contig)组装,并保留最短长度不低于300 bp的Contig。接着,采用Prodigal v2.6.3软件对组装得到的Contig进行开放阅读框(Open Reading Frame,ORF)预测。ORF是指一段由起始密码子和终止密码子界定的、具有编码蛋白质潜能的核酸序列。在此基础上,筛选出核酸长度≥100 bp的基因序列,并将其翻译为氨基酸序列。使用CD-HIT v4.7软件对所有样本预测出的基因序列进行聚类,构建非冗余基因集(Non-redundant Gene Catalog),并获取其碱基序列。最后,利用短序列比对软件SOAPaligner将每个样本的高质量reads与构建的非冗余基因集进行比对,进而统计基因在对应样品中的丰度信息,基于“美吉云分析平台”完成上述所有生物信息学分析。
1.3.4 数据处理
采用Excel 2010软件处理实验数据,Origin 7.5和R软件作图,采用Kruskal-Wallis秩和检验方法进行京都基因与基因组百科全书(KEGG)和碳水化合物活性酶(CAZy)分析。
2 结果与分析
2.1 发酵过程中酒醅理化指标分析
发酵过程中酒醅理化指标测定结果见表1。由表1可知,水分含量呈“升-降-升”的波动变化趋势:发酵初期(3~7 d),水分含量由66.16%上升至67.62%,增加1.46%,其原因可能是微生物呼吸代谢和乙醇发酵过程中产生了代谢水[16,20];发酵中期(7~12 d),水分含量略有下降,由67.62%降至67.06%,这可能与发酵产热导致的水分蒸发以及酒精挥发、微生物细胞失水等因素有关[17];发酵后期(12~15 d),水分含量再次回升至68.83%,这与发酵后期微生物2次代谢产水及蛋白质分解释放结合水密切相关[21]。在发酵3~5 d期间内淀粉含量由12.12 g/100 g增加至14.47 g/100 g,可能是由于发酵温度升高促进了淀粉颗粒溶胀和α-淀粉酶活性增强,使不溶性淀粉转化为可溶性淀粉[17];发酵5~15 d期间内,淀粉含量由14.47 g/100 g降低至8.61 g/100 g,淀粉利用率达40.5%,其原因可能是根霉产生的糖化酶和细菌淀粉酶协同作用下,淀粉持续水解为可发酵性糖[17]。在发酵3~12 d期间内,还原糖含量总体呈下降趋势,由0.090 mg/g降低至0.050 mg/g,表明此阶段酵母菌代谢较旺盛;在发酵12~15 d期间内,还原糖含量有所增加,增加至0.058 mg/g。pH值和总酸的变化体现了发酵过程中酸代谢的平衡[21]。在发酵过程(3~15 d)中,pH值由3.38逐渐降低至3.33,而酸度由2.13 mmol/10 g逐渐增加至2.24 mmol/10 g。其原因可能是乳酸菌在发酵后期大量繁殖,通过同型和异型乳酸发酵途径产生乳酸、乙酸等有机酸,为后续酯化反应提供酸性前体物质[21]。
表1 发酵过程中酒醅理化指标测定结果
Table 1 Determination results of physicochemical indicators of fermented grains during fermentation process
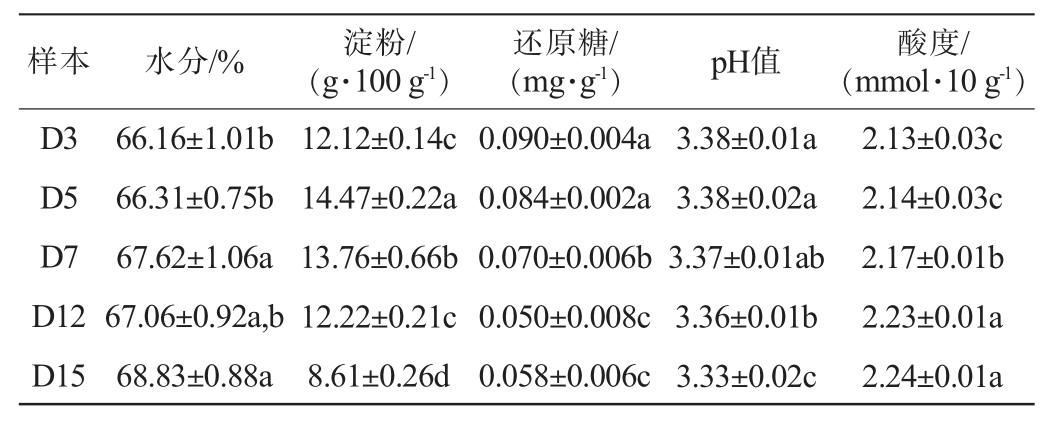
注:同列不同小写字母表示差异显著(P<0.05)。
2.2 发酵过程中酒醅微生物多样性分析
2.2.1 微生物Alpha多样性分析
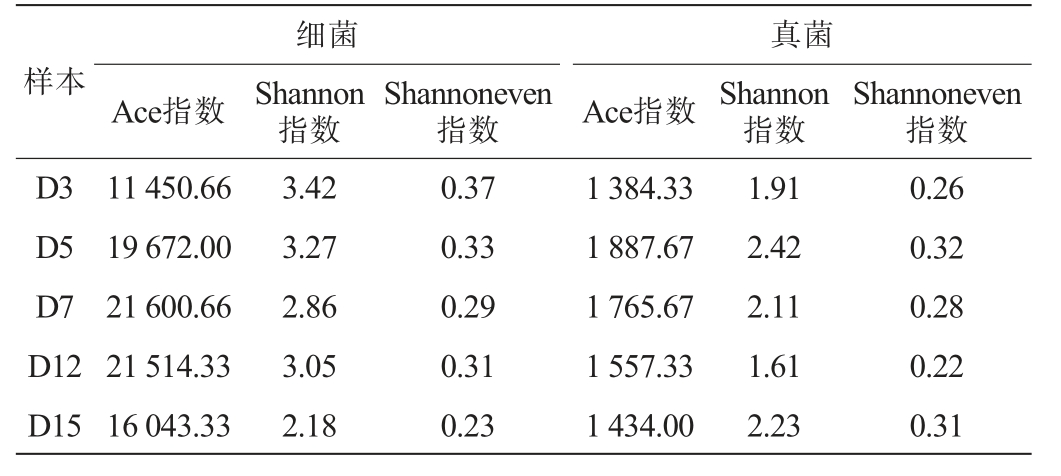
ACE指数反映群落丰富度,即物种数量,Shannon指数反映群落多样性,即物种丰富度与均匀度的综合指标,Shannoneven指数反映群落中物种分布的均匀性(越接近1越均匀)[21]。发酵过程中酒醅微生物群落Alpha多样性分析结果见表2。由表2可知,在发酵3~15 d期间内,细菌群落及真菌群落的Ace指数均呈先上升后下降的趋势,且细菌群落Ace指数高于真菌;细菌群落及真菌群落的Ace指数分别在发酵7 d、5 d时,Ace指数最高,为21 600.66、1 887.67,其原因可能是,发酵前期适宜的温度、湿度和营养条件促进了细菌种类的增加,而发酵后期pH降低、营养竞争加剧导致部分细菌种群淘汰[18]。细菌Shannon指数在发酵3~15 d期间内呈下降趋势,由3.42降低至2.18,表明随着发酵的进行微生物群落多样性下降[18],真菌Shannon指数呈“升-降-升”波动趋势。这可能与发酵过程中糖化菌与酒精发酵菌等关键功能类群交替占据生态位相关[19],细菌群落Shannon指数高于真菌,表明细菌多样性优于真菌。细菌群落Shannoneven指数整体呈下降趋势,由0.37降低至0.23;真菌群落Shannoneven指数亦呈“升-降-升”波动趋势,发酵5 d时,Shannoneven指数最高(0.32),表明真菌群落分布相对均匀;发酵12 d时有所下降,表明真菌群落均匀度降低;发酵结束(15 d)略有回升(0.31),表明群落多样性趋于稳定,与优势真菌种群的周期性更替和竞争强度变化一致[18]。结果表明细菌丰富度及多样性高于真菌群落。
表2 发酵过程中酒醅微生物群落Alpha多样性分析结果
Table 2 Alpha diversity analysis results of microbial community in fermented grains during fermentation process
2.2.2 细菌菌群结构分析
基于门水平和属水平发酵过程中酒醅细菌菌群结构进行分析,结果见图1。由图1a可知,发酵过程中酒醅共检出4个优势菌门(相对丰度>1%),其中,厚壁菌门(Firmicutes)在发酵3~15 d期间相对丰度逐渐增加,由56.9%增加至88%,其原因可能是其在酸性环境(pH 3.0~4.0)中具有竞争优势,其耐酸性和快速繁殖能力使其逐步建立生态优势[24];变形菌门(Proteobacteria)相对丰度逐渐降低,由25.3%降至5.1%;拟杆菌门(Bacteroidota)在发酵3~12 d期间相对稳定(平均相对丰度为12.4%),但在发酵15 d时相对丰度明显下降至2.1%,可能与发酵后期极端酸性环境(pH 3.33)的选择压力有关[23];放线菌门(Actinobacteria)在3~12 d期间内平均相对丰度较高(3.2%),发酵15 d时相对丰度为0.1%,表明其在小曲清香型白酒发酵环境中缺乏竞争力[2]。
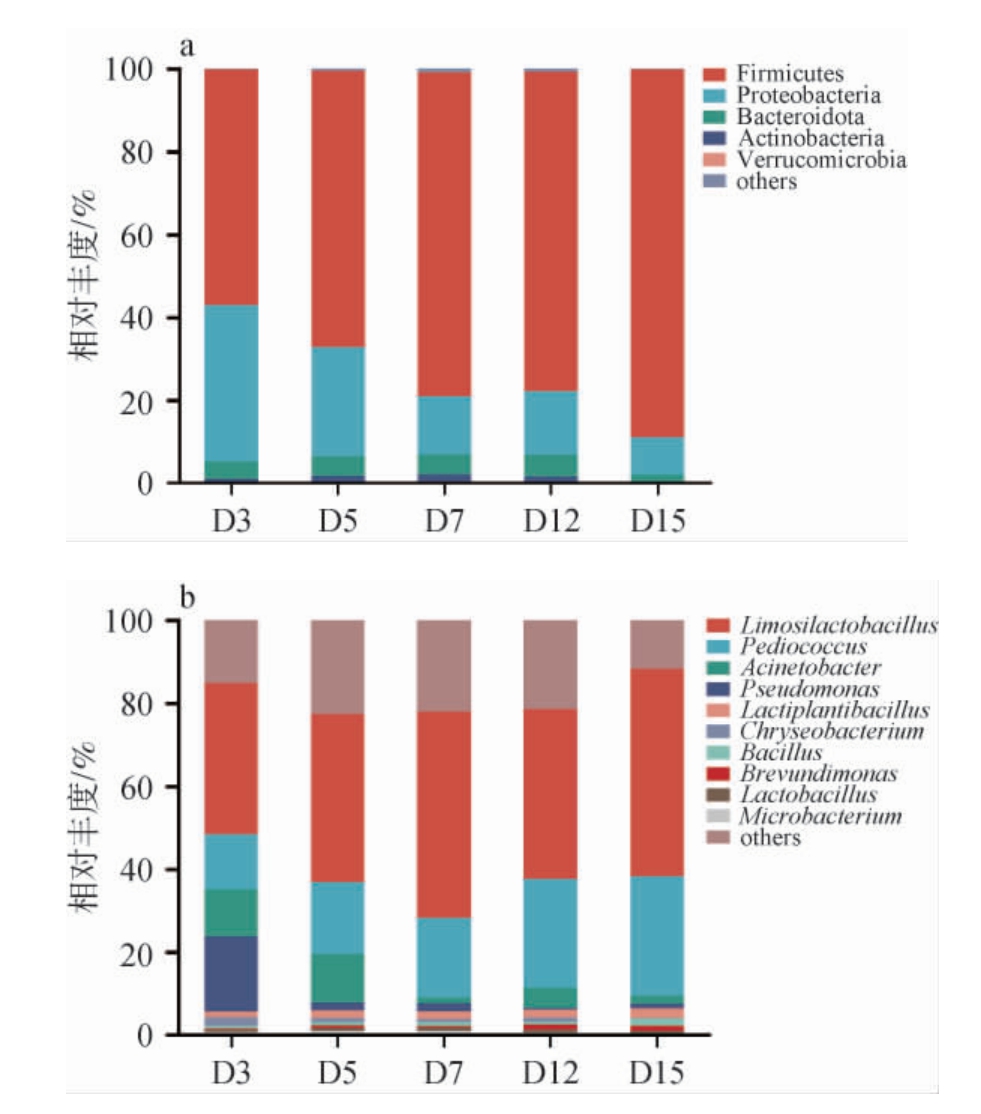
图1 基于门水平(a)和属水平(b)发酵过程中酒醅细菌菌群结构分析
Fig.1 Analysis of bacterial community structure of fermented grains during fermentation process based on phylum level (a) and genus level (b)
由图1b可知,发酵过程中酒醅中共检出7个优势细菌属(相对丰度>1%),分别为柠檬乳杆菌属(Limosilactobacillus)、片球菌属(Pediococcus)、不动杆菌属(Acinetobacter)、假单胞菌属(Pseudomonas)、乳球菌属(Lactococcus)、魏斯氏菌属(Weissella)和芽孢杆菌属(Bacillus)。其中,柠檬乳杆菌属为主要优势菌属,其相对丰度在发酵3~15 d呈先上升后稳定趋势,发酵7 d时达到最高值(45.3%),随后保持在较高水平(15 d时为43.6%)。该菌属具有较强的同型发酵能力,其产酸速率约为0.5 g/(L·h),能够快速降低体系pH并抑制杂菌生长,是维持发酵体系稳定性的关键功能菌群[24]。
片球菌属的相对丰度在发酵过程中持续上升,发酵15 d时达28.7%,与柠檬乳杆菌属共同构成了中后期的优势发酵菌群。不动杆菌属和假单胞菌属在发酵3 d时相对丰度最高(分别为18.7%和15.2%),但随后迅速下降,发酵15 d时分别仅为2.3%和1.2%,表明其在厌氧环境和酸性条件下的适应性较弱,对发酵环境变化具有较高敏感性[23]。此外,乳球菌属、魏斯氏菌属和芽孢杆菌属在发酵后期仍维持一定比例,其相对丰度分别为3.1%、5.8%和2.6%,在风味前体生成及发酵体系稳定方面亦可能发挥重要作用。
2.2.3 真菌菌群结构分析
基于门水平和属水平发酵过程中酒醅真菌菌群结构分析见图2。由图2a可知,在发酵过程中酒醅共检出3个优势真菌门(相对丰度>1%)。其中,子囊菌门(Ascomycota)和毛霉菌门(Mucoromycota)为绝对优势类群,其相对丰度之和>90%。在发酵3~12 d期间内,Ascomycota的相对丰度呈上升趋势,发酵结束时有所下降;与之相反,Mucoromycota的相对丰度变化趋势相反。链型植物门(Streptophyta)在整个发酵周期内保持稳定(相对丰度为1.5%~3.0%)。
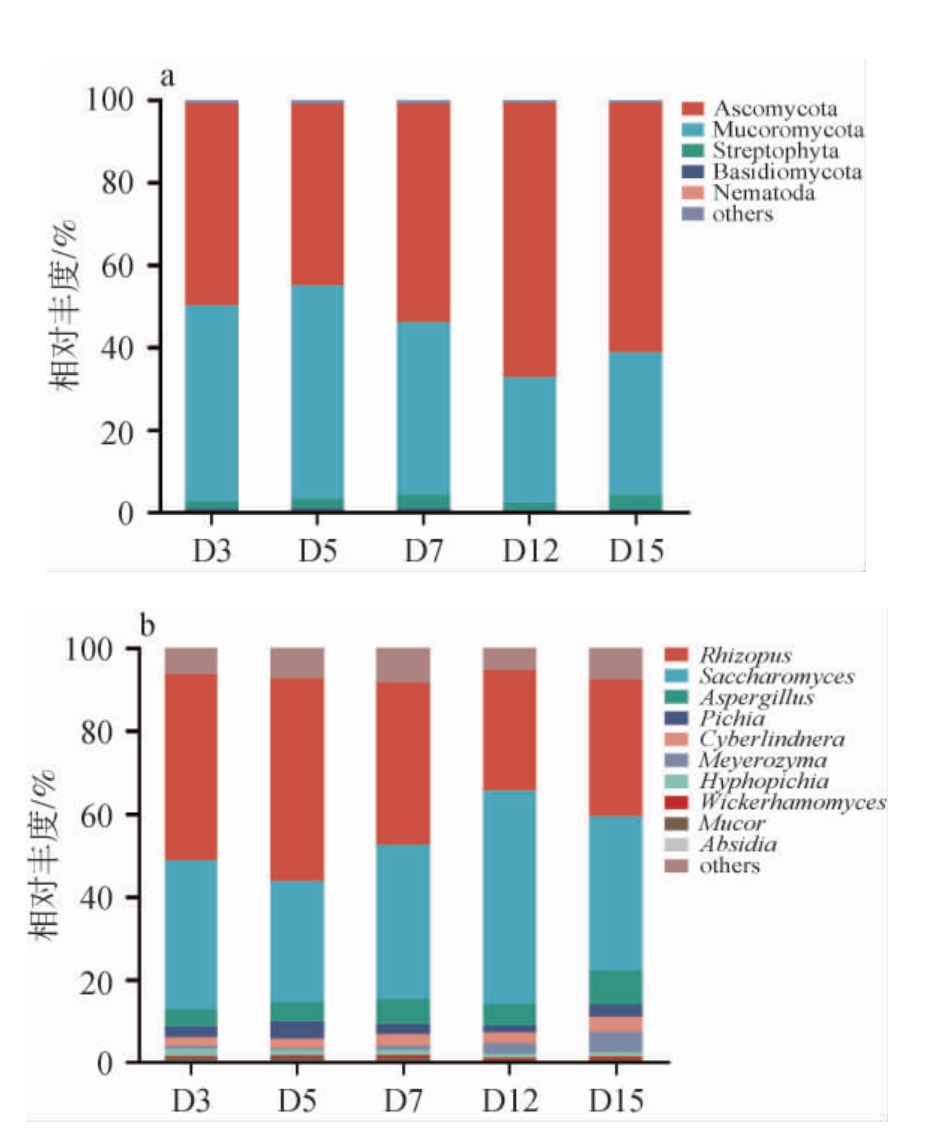
图2 基于门水平(a)和属水平(b)发酵过程中酒醅真菌菌群结构分析
Fig.2 Analysis of fungal community structure of fermented grains during fermentation process based on phylum level (a) and genus level (b)
由图2b可知,酒醅真菌群落共检测到7个优势真菌属(相对丰度>1%)分别为根霉属(Rhizopus)、酿酒酵母属(Saccharomyces)、曲霉属(Aspergillus)、毛霉属(Mucor)、毕赤酵母属(Pichia)、塞伯林德纳氏酵母属(Cyberlindnera)和梅耶酵母属(Meyerozyma)。作为毛霉菌门的主要代表,Rhizopus的相对丰度在发酵3~5 d显著富集,发酵5 d时相对丰度最高(43.78%),随后其相对丰度随着发酵的进行逐渐降低。Rhizopus因其高效的淀粉酶系统,在发酵前期主导淀粉的水解过程,为后续酒精发酵提供可发酵糖底物[25]。同属毛霉菌门的Mucor在发酵7 d时,相对丰度最高,与Rhizopus共同参与酒醅初期的糖化功能。Saccharomyces的相对丰度在发酵5~12 d期间内逐渐增加,并于第12天达到最高值(49.01%),表明其在酒醅中承担主要的酒精发酵功能。Rhizopus主导糖化、Saccharomyces主导发酵的动态演替,体现了传统固态发酵中典型的“糖化-发酵”功能分工。Aspergillus在整个发酵周期内保持相对恒定的丰度(3.41%~7.10%),作为重要的辅助微生物群,主要参与蛋白质降解和次级代谢产物生物合成等过程[26]。Pichia和Cyberlindnera的相对丰度虽处于较低水平,但在发酵后期显示出微弱的增长趋势,这可能与其在极端环境胁迫下的生存优势密切相关[27]。Meyerozyma的相对丰度较低(约为1%~2%),且其富集主要出现在发酵的后期阶段,推测这类耐逆性酵母可能在酒精高浓度、营养受限的发酵后期环境中发挥潜在的功能作用[28]。
2.4 理化指标与细菌、真菌的相关性分析
2.4.1 理化指标与细菌属的相关性分析
理化指标与细菌属聚类相关性分析热图见图3。由图3可知,水分含量与乳酸菌类群(如布氏迟缓乳杆菌属(Lentilactobacillus)、片球菌属(Pedicoccus)、乳酸杆菌属(Lactobacillus)和植物乳植杆菌属(Lactiplantibacillus))呈正相关,反映出乳酸菌对高湿度环境的依赖性,水分有利于维持其细胞活性和发酵进程。相反,水分含量与不动杆菌属(Acinetobacter)呈极显著负相关(P<0.01),显示该菌属偏好相对干燥的环境的生态特性。
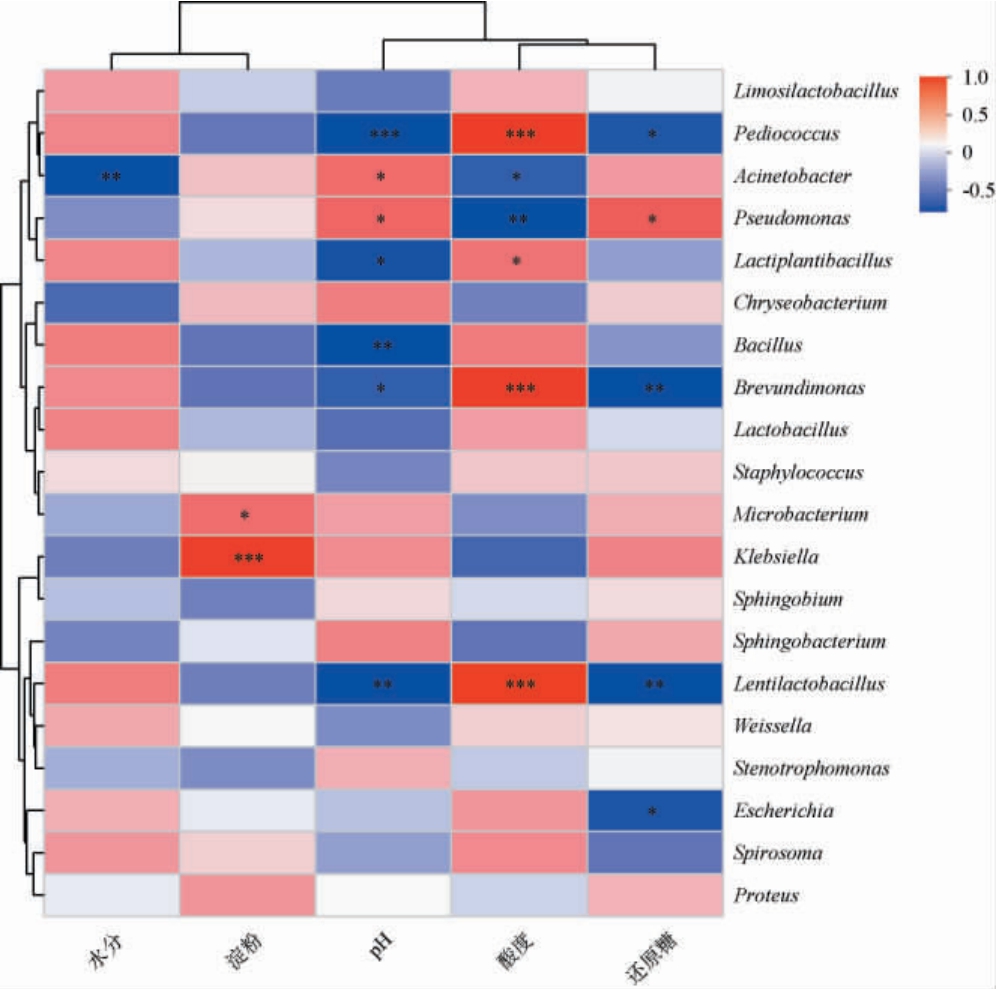
图3 理化指标与细菌属相关性聚类分析热图
Fig.3 Cluster analysis heatmap of correlation between physicochemical indicators and bacterial genera
“*”表示相关性显著(P<0.05),“**”表示相关性极显著(P<0.01),“***”表示相关性高度显著(P<0.001)。下同。
pH值与片球菌属(Pedicoccus)呈高度显著负相关(P<0.001),与芽孢杆菌属(Bacillus)、布氏迟缓乳杆菌属(Lentilactobacillus)呈极显著负相关(P<0.01),与植物乳植杆菌属(Lactiplantibacillus)、短杆菌属(Brevibacterium)呈显著负相关(P<0.05),表明乳酸菌通过同型或异型乳酸发酵产生有机酸,迅速降低环境pH,进而抑制腐败菌生长并强化自身竞争优势。pH值与不动杆菌属(Acinetobacter)、假单胞菌属(Pseudomonas)呈显著正相关(P<0.05),与其他菌属相关性不显著(P>0.05),显示高酸环境对不动杆菌属(Acinetobacter)等的生长具有明显的抑制作用,其主要活跃于发酵早期的弱酸或中性偏酸环境中;酸度与不动杆菌属(Acinetobacter)、假单胞菌属(Pseudomonas)分 别呈显著和极显著负相关(P<0.05,P<0.01),与片球菌属(Pedicoccus)、短杆菌属(Brevibacterium)、布氏迟缓乳杆菌属(Lentilactobacillus)呈高度显著正相关(P<0.001),与其他菌属相关性不显著(P>0.05)。
淀粉与克雷伯氏菌属(Klebsiella)呈高度显著正相关(P<0.001),与微杆菌属(Microbacterium)呈显著正相关(P<0.05),反映其具备一定的淀粉降解潜力,与其他菌属相关性不显著(P>0.05)。还原糖与短杆菌属(Brevibacterium)、布氏迟缓乳杆菌属(Lentilactobacillus)呈极显著负相关(P<0.01),与片球菌属(Pedicoccus)、埃希氏菌属(Escherichia)呈显著负相关(P<0.05),并与假单胞菌属(Pseudomonas)呈显著正相关(P<0.05),表明该菌属倾向于利用小分子糖类,但其优势受到乳酸菌的竞争和酸性环境的抑制,还原糖与其他菌属相关性不显著(P>0.05)。
综上,pH和总酸是决定白酒酒醅细菌群落演替的关键驱动因子[24,29],它们通过酸性抑制作用筛选出以片球菌属(Pedicoccus)和布氏迟 缓乳杆菌属(Lentilactobacillus)为代表的耐酸乳酸菌群,从而主导发酵进程。淀粉与还原糖作为核心碳源,主要影响如克雷伯氏菌属(Klebsiella)等菌群的代谢潜力[23],并确保了乳酸菌能够快速利用单糖并形成产酸优势。水分含量则通过对细胞渗透压的影响,间接体现了对乳酸菌活性和腐败菌抑制的作用。功能乳酸菌群与环境理化指标在发酵体系中形成了相互促进的稳定正向反馈。
2.4.2 理化指标与真菌属的相关性分析
理化指标与真菌属聚类分析热图见图4。由图4可知,水分含量与梅耶酵母属(Meyerozyma)、腐食螨属(Tyrophagus)呈显著正相关(P<0.05),与犁头霉属(Absidia)呈显著负相关(P<0.05),与其他菌属相关性不显著(P>0.05)。这表明适宜的水分条件有利于酵母类群的生长与代谢,而可能对部分霉菌的繁殖起到抑制作用。
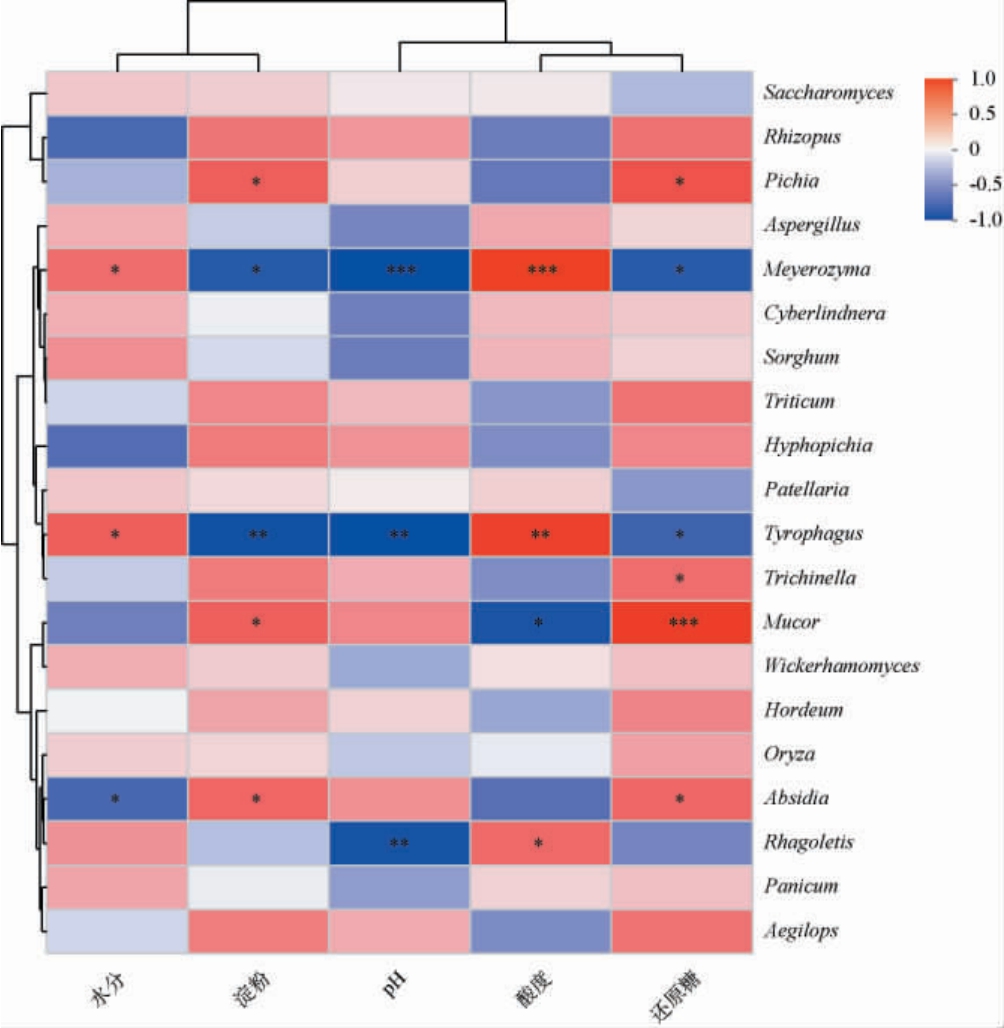
图4 理化指标与真菌属相关性聚类分析热图
Fig.4 Cluster analysis heatmap of correlation between physicochemical indicators and fungal genera
梅耶酵母属(Meyerozyma)与酸度呈高度显著正相关(P<0.001),与pH呈高度显著负相关(P<0.001),表明其是典型的耐酸菌属,适应发酵中后期低pH环境,并能在极端酸性条件下保持代谢优势。腐食螨属(Tyrophagus)与酸度呈极显著正相关(P<0.01),与pH呈极显著负相关(P<0.01),显示其对酸性环境较为敏感,偏好在发酵早期的弱酸性环境中进行糖化作用。此外,毛霉属(Mucor)与酸度呈显著负相关(P<0.05),表明该菌属可能更适应发酵早期的中性偏弱酸性环境,酸度、pH与其他菌属相关性不显著(P>0.05)。
毕赤酵母属(Pichia)、犁头霉属(Absidia)均与淀粉和还原糖均呈显著正相关(P<0.05),而梅耶酵母属(Meyerozyma)与淀粉和还原糖均呈显著负相关(P<0.05),可能是其作为耐酸发酵菌,主要在糖原被大量利用后的发酵后期发挥作用。此外,腐食螨属(Tyrophagus)与淀粉呈极显著负相关(P<0.01),与还原糖呈显著负相关(P<0.05)。毛霉属(Mucor)与淀粉呈显著正相关(P<0.05),但与还原糖呈高度显著正相关(P<0.001),表明毛霉属(Mucor)倾向于利用酶解产生的小分子还原糖进行代谢,而淀粉与还原糖与其他菌属相关性不显著(P>0.05)。
综上,pH和总酸是影响真菌群落结构的关键理化因子[29],决定了不同功能类群的代谢阶段分布(耐酸型和非耐酸型)。水分含量影响真菌的细胞活性和代谢强度[30],而淀粉与还原糖等核心碳源,则决定了糖化真菌(如根霉属(Rhizopus)和毛霉属(Mucor))与发酵真菌(如酿酒酵母属(Saccharomyces)、梅耶酵母属(Meyerozyma))的功能分配与能量转化效率[31]。总体来看,发酵前期以糖化真菌为主,中后期则以发酵型真菌占优势,二者形成稳定的功能互补关系。
2.5 KEGG数据库代谢通路功能注释
发酵过程中酒醅微生物的KEGG代谢通路功能注释结果见图5。由图5可知,根据KEGG数据库的一级分类注释,共包括代谢(Metabolism)、遗传信息处理(Genetic Information Processing)、人类疾病(Human Diseases)、环境信息处理(Environment Information Processing)、细胞过程(Cellular Processes)和生物体系统(Organismal Systems)共6类功能通路。其中,代谢(Metabolism)通路注释到的基因数量最多,其次为遗传信息处理和人类疾病(HumanDiseases),注释到生物体系统(Organismal Systems)的基因数量最少。
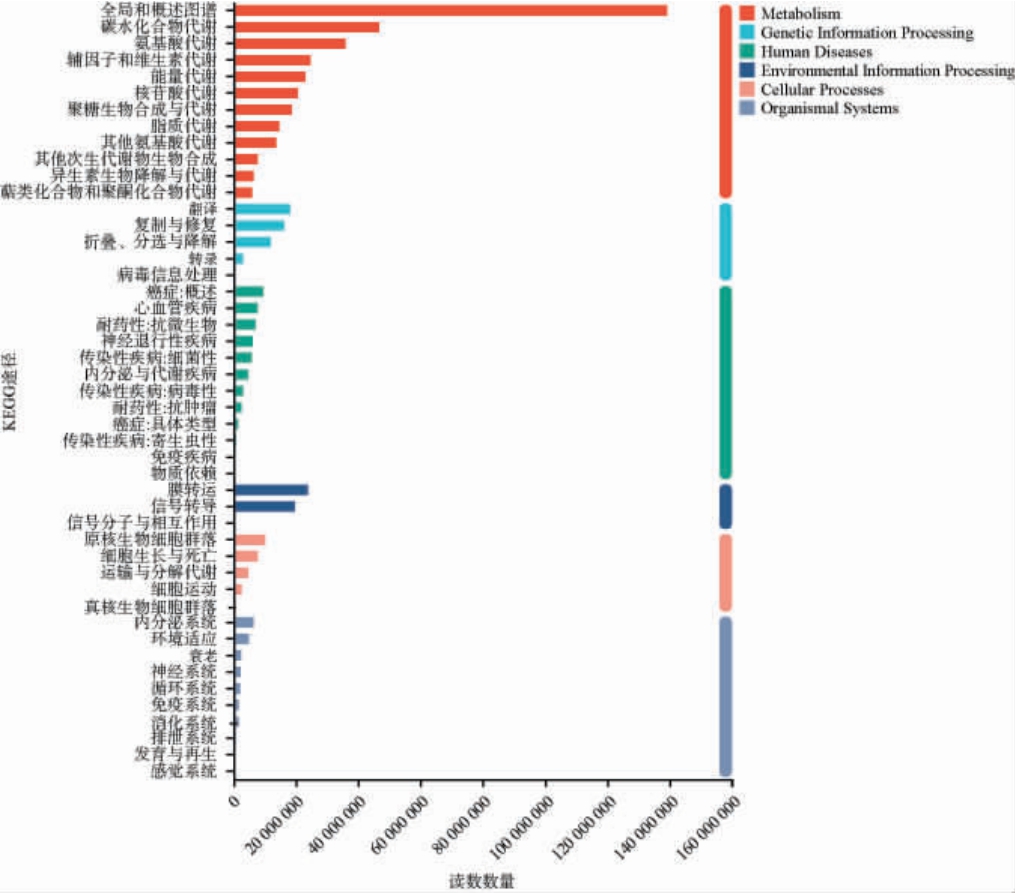
图5 发酵过程中酒醅微生物菌群的KEGG代谢通路功能注释
Fig.5 Functional annotation of KEGG metabolic pathways in the microbial community of fermented grains during fermentation process
KEGG注释到47类的2级代谢通路,其平均相对丰度排名前5的通路及其占比为:全局和概述图谱(Global and overview maps)(32.75%)、碳水化合物代谢(Carbohydrate metabolism)(10.97%)、氨基酸代谢(Amino acid metabolism)(8.66%)、膜转运(Membrane transport)(5.86%)和辅因子和维生素的代谢(Metabolismofcofactorsandvitamins)(5.78%)。排名前三的代谢功能均属于代谢过程(Metabolism)的一级通路,说明在酒醅发酵过程中,碳水化合物、氨基酸等核心物质存在着较为旺盛的代谢活动。碳水化合物作为生命细胞结构的主要成分及主要供能物质,具有调节细胞活动的重要功能[32]。大量研究表明,在小曲清香型白酒发酵过程中,还原糖与氨基酸可通过美拉德反应生成一系列风味物质[33],对白酒独特风味的形成作出了重要贡献[22]。
2.6 CAZy数据库代谢通路功能注释
发酵过程中酒醅微生物CAZy代谢通路功能注释结果见图6。由图6可知,发酵过程中酒醅微生物基因组中共检出7类碳水化合物活性酶,构成了复杂而高效的碳水化合物代谢酶系。发酵过程中,糖苷水解酶(Glycoside Hydrolases,GHs)平均相对丰度较高(38.7%),其次为糖基转移酶(Glycosyl Transferases,GTs)(28.4%)和碳水化合物酯酶(Carbohydrate Esterases,CEs)(15.2%),三者构成碳水化合物代谢的核心酶系,平均相对丰度之和为82.3%。酒醅的发酵离不开糖类的合成与分解。GHs是水解糖苷键的关键酶,其活性在发酵过程中起着至关重要的作用。酒醅中含有大量的多糖类物质,GHs通过水解酒醅中的多糖类物质,将其分解为可被微生物利用的营养物质,从而为微生物发酵过程提供能量和碳源[29]。GTs在酒醅发酵中有助于调节糖代谢通路、合成生物活性分子,促进微生物在发酵过程中正常生长和代谢,影响发酵产物的组成和产率[30-31]。在酒醅发酵中,CEs主要参与碳水化合物酯键的水解过程,可以将这些酯类底物分解为可供微生物利用的碳源,促进微生物的生长和发酵过程[27]。
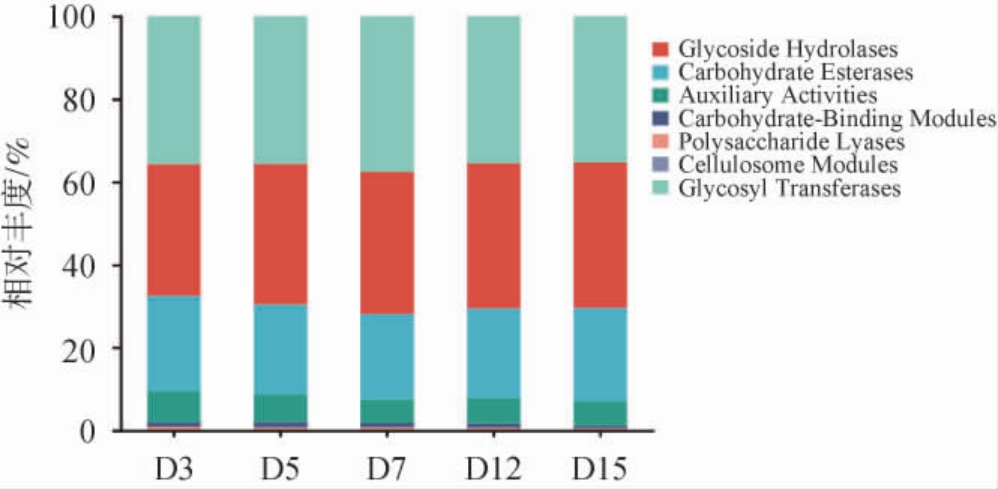
图6 发酵过程中酒醅微生物菌群CAZy代谢通路功能注释
Fig.6 Functional annotation of CAZy metabolic pathways in the microbial community of fermented grains during fermentation process
此外,碳水化合物结合模块(Carbohydrate-BindingModules,CBMs)、多糖裂解酶(Polysaccharide Lyases,PLs)和辅助氧化还原酶(Auxiliary Activities,AAs)在酒醅发酵过程中也发挥着重要作用。CBMs能够促进酶与底物结合,增强纤维素等大分子物质的降解效率[33];PLs主要作用于果胶和硫酸软骨素等多糖类物质,对糖化过程有辅助作用;AAs则主要参与氧化还原反应,协助酶促反应的进行[33]。由此可知,完整的CAZy碳水化合物活性酶系在酒醅发酵过程中起到了关键的生物催化作用。
3 结论
本研究采用常规分析法及高通量测序技术分析其理化指标及微生物菌群结构,对理化指标及微生物菌群进行相关性分析,并结合京都基因与基因组百科全书(KEGG)和碳水化合物活性酶(CAZy)数据库对功能基因进行注释。结果表明,发酵过程中水分含量呈“升-降-升”的波动变化趋势(66.16%~68.83%),pH、淀粉含量分别从3.38、14.47 g/100 g降低至3.33、8.61 g/100 g,酸度从2.13 mmol/10 g增加至2.24 mmol/10 g;发酵过程中酒醅分别检出4个优势细菌门(相对丰度>1%)、3个优势真菌门及7个优势细菌属、7个优势真菌属;片球菌属(Pedicoccus)、梅耶酵母属(Meyerozyma)与pH值呈高度显著负相关(P<0.001),与总酸呈高度显著正相关(P<0.001),淀粉与克雷伯氏菌属(Klebsiella)、毛霉属(Mucor)呈高度显著正相关(P<0.001),这表明pH与总酸是调控耐酸菌群建立与稳定的关键驱动力,淀粉与还原糖则决定了糖解菌群的代谢潜力与发酵效率。KEGG功能注释结果显示,发酵微生物群落的功能主要富集于代谢相关通路,其中碳水化合物代谢(10.97%)和氨基酸代谢(8.66%)是核心代谢途径。CAZy功能注释结果显示,糖苷水解酶(GHs)、糖基转移酶(GTs)及碳水化合物酯酶(CEs)等关键酶系共同构建了高效的碳水化合物转化体系,为酒醅发酵提供酶学基础。本研究为自动化发酵条件下微生物群落与代谢功能的协同调控机制提供了理论支撑,对小曲清香型白酒的智能化酿造工艺优化具有重要的指导意义。
[1] 黄志久,赵金松,刘莎,等.小曲清香白酒生产工艺现状及发展趋势[J].酿酒,2018,45(6):17-19.
[2] 韩冰玙,陈辉太,李宗军.酱、浓、清香型白酒酿造过程中真菌及其功能特性研究进展[J].中国酿造,2024,43(3):27-32.
[3] 邓世彬.小曲清香型白酒研究与概述[J].现代食品,2023,29(6):29-31.
[4] 吴赫川,马莹莹,杨建刚,等.川法小曲白酒发展现状及其瓶颈问题分析[J].安徽农业科学,2014,42(33):11850-11853,11856.
[5] 陈申习,唐洁,张龙,等.清香型小曲白酒机械化生产中微生物动态变化研究[J].中国酿造,2018,37(6):68-72.
[6] 蒲刚,栗伟,李健.小曲清香白酒发展创新之路[J].酿酒,2024,51(1):24-26.
[7] 蔡凤娇.固态法小曲白酒机械化酿造工艺技术研究[D].武汉:湖北工业大学,2013.
[8] 张杰,程伟,彭兵,等.小曲清香型白酒研究概述[J].酿酒科技,2017(9):91-95.
[9] 郭小燕.白酒酿造设备的机械化发展现状与展望[J].山东工业技术,2018(10):26.
[10] 时伟,郑红梅,黄婷,等.中国白酒酿造核心微生物相互作用研究进展[J].食品与发酵工业,2025,51(20):427-436.
[11] 骆红波,孙优兰,范奇高,等.组学技术在白酒酿造微生物中的应用进展[J].中国酿造,2023,42(12):13-21.
[12] 晏培,谭壹,李登勇,等.小曲清香型白酒手工和机械化酿造过程中酒醅理化及微生物群落演变的差异性分析[J].酿酒科技,2022(4):65-70.
[13] JING Z,ZHU Y,XU Y.Mystery behind Chinese liquor fermentation[J].Trend Food Sci Technol,2017,63:18-28.
[14] 杨强.劲牌公司白酒生产机械化发展历程与体会——在全国第四届清香型白酒高峰论坛上的发言[J].酿酒,2011,38(5):12-13.
[15]童文华,王燕,李依芸,等.小曲清香型白酒自动化酿造技术的研究与优化[J].当代化工研究,2025(1):182-184.
[16] 韩韶.清香型酒醅发酵过程理化性质变化规律研究[J].中国食品工业,2024(10):104-106.
[17] 陈佩,翟彩宁,刘莹,等.白水地区清香型大曲理化指标及真菌多样性分析[J].食品与发酵工业,2024,50(10):197-204.
[18] 赵亮,王莉,汪地强,等.白酒微生物群落研究技术现状与二代测序数据分析方略[J].酿酒科技,2016(7):88-96.
[19] 贾丽艳,田宇敏,王晓勇,等.传统清香型白酒发酵过程中真菌群落结构及其动态演替[J].中国食品学报,2020,20(10):303-308.
[20] 张霞,王中凯,郑佳,等.浓香型白酒发酵过程中酒醅理化指标变化规律研究[J].酿酒科技,2021(10):53-56.
[21] 杜艾明,李良,李俊薇,等.清香型白酒酿造核心功能微生物的研究与应用[J].中国酿造,2021,40(2):16-19.
[22] 田德雨,闫子茹,危晶晶,等.清香型白酒酿造微生物和风味物质的研究进展[J].中国酿造,2021,40(4):20-25.
[23] 谢再斌,常煦,何国庆,等.清香型白酒酿造过程中功能微生物及应用研究[J].中国酿造,2024,43(7):27-32.
[24] 马丹,张秋波,王涵,等.小曲清香型白酒酿造中乳酸杆菌的演替及优势乳酸杆菌发酵特性分析[J].微生物学报,2025,65(10):4667-4683.
[25] 王瑞鑫,高宇迪,刘晓妹,等.根霉菌添加量对小曲清香型白酒酒醅理化指标及基酒风味成分的影响[J].中国酿造,2025,44(5):161-168.
[26] 王兆华.清香型白酒酒曲核心真菌发酵的特性分析[J].酿酒,2024,51(4):107-109.
[27] 尚玮璇,刘璐,雷素珍,等.功能性碳水化合物通过调节肠道菌群和代谢物改善非酒精性脂肪肝的作用机制[J].食品与发酵工业,2022,48(14):311-318.
[28] DONG W,YU X,WANG L,et al.Unveiling the microbiota of sauceflavor Daqu and its relationships with flavors and color during maturation[J].Front Microbiol,2024,15:1345772.
[29] ZOU Y,YUAN Y,LIU M,et al.Metagenomics reveal the role of microorganism and GH genes contribute to Sichuan South-road dark tea quality formation during pile fermentation[J].LWT-Food Sci Technol,2023,178:114618.
[30] BRETON C,MUCHA J,JEANNEAU C.Structural and functional features of glycosyltransferases[J].Biochimie,2001,83(8):713-718.
[31] WANG J,HOU B.Glycosyltransferases: key players involved in the modification of plant secondary metabolites[J].Front Biol China,2009,4:39-46.
[32] MA S,SHANG Z,CHEN J,et al.Differences in structure,volatile metabolites,and functions of microbial communities in Nongxiangxing Daqu from different production areas[J].LWT-Food Sci Technol,2022,166:113784.
[33] BARBA-CEDILLO V,MONTANIER C Y.Effect of multimodularity and spatial organization of glycoside hydrolases on catalysis[J]. Essays Biochem,2023,67(3):629-638.