海藻糖由两个葡萄糖分子以α,α-1,1糖苷键连接而成,是一种性质稳定的非还原性糖,能耐受高温,无旋光性[1]。海藻糖作为一种重要的贮藏碳水化合物和能量来源,广泛分布于除脊椎动物外的昆虫、真菌、细菌以及植物等众多生物体内[2]。病原体产生的海藻糖可能导致顽固性生物膜的形成和发展,使其对微生物杀菌剂的抵抗力增强,并通过引起多重感染、污染组织植入物和医疗器械对接受手术的患者构成极大威胁[3]。
海藻糖酶(EC3.2.1.28)是一种葡萄糖苷水解酶,可以催化一分子海藻糖水解生成两分子葡萄糖[4]。根据氨基酸序列分析,在碳水化合物活性酶(Carbohydrate-Active enzymes,CAZy)数据库中,海藻糖酶主要归属于糖苷水解酶(glycoside hydrolase,GH)第15、37和65家族[5],这些海藻糖酶催化结构域(catalytic domain,CD)通常具有(α/α)_6桶状结构,并且有两个氨基酸残基[天冬氨酸(aspartic acid,Asp)和/或谷氨酸(glutamic acid,Glu)]在反转机制中起催化残基的作用[6]。LIN M G等[7]在GH13家族中也发现来源于地衣芽孢杆菌(Bacillus licheniformis)的海藻糖酶磷酸化酶TreA,通过蛋白质结构分析,确定其催化残基为Asp和Glu。
在发酵工业中,海藻糖是酿酒酵母(Saccharomyces cerevisiae)在乙醇胁迫下产生的重要应激产物,但酿酒酵母不能利用海藻糖,因此添加海藻酸酶可以提高最后的乙醇产量[8]。DONG L等[9]在30%的淀粉糖化液中,添加海藻糖酶MthT,使乙醇转化率(乙醇产量/总葡萄糖)从34.38%提高到51.88%。在谷氨酸发酵过程中同样会产生较多的海藻糖,在发酵过程中添加海藻糖酶能通过降低发酵液中海藻糖的浓度,进而提高谷氨酸得率,减小海藻糖对下游谷氨酸提取的影响[10]。因为海藻糖对发酵过程有显著的负面影响,因此发掘高活性、高稳定性海藻糖酶对于发酵工业意义重大。
目前为止,已分离并表征了源于细菌、真菌、昆虫、古菌等生物的海藻糖酶,但仍不能完全满足生产需求[3,11]。基于此,本研究以分离自云南洱源牛街热泉的无氧芽孢杆菌属(Anoxybacillus sp.)YHS0032为研究对象,采用人工合成技术合成其基因组中的嗜热海藻糖酶Adb1332基因,并通过基因重组技术将其在大肠杆菌(Escherichia coli)中进行异源表达。通过镍柱亲和层析对嗜热海藻糖酶Adb332粗酶液进行分离纯化后,对其酶学性质进行表征,以期为嗜热海藻糖酶Adb1332在发酵工业中的应用提供参考。
1 材料与方法
1.1 材料与试剂
1.1.1 基因、质粒与菌株
海藻糖酶Adb1332基因:来源于分离自云南洱源牛街热泉的无氧芽孢杆菌属(Anoxybacillus sp.)YHS0032的基因组,由上海生工生物技术有限公司合成;大肠杆菌BL21(DE3)感受态细胞、表达质粒pET28a:上海生工生物技术有限公司。
1.1.2 化学试剂
海藻糖(纯度>98%):上海源叶生物科技有限公司;昆布多糖(纯度>96%)、木聚糖(纯度>95%)、水苏糖(纯度>80%)、葡萄糖(分析纯):上海麦克林生化科技股份有限公司;普鲁兰多糖(纯度>98%)、甘氨酸(分析纯)、盐酸(分析纯)、异丙基-β-D-硫代半乳糖苷(isopropyl β-D-1-thiogalactopyranoside,IPTG)(分析纯)、硫酸卡那霉素(分析纯):上海阿拉丁生化科技股份有限公司;β-葡聚糖(纯度>85%):北京普西唐生物科技有限公司;十二烷基硫酸钠(sodium dodecyl sulfate,SDS)(分析纯):北京兰杰柯科技有限公司:Tris(分析纯):上海贝外塔生物科技有限公司;咪唑、氯化钠、柠檬酸、磷酸二氢钠、氢氧化钠、3,5-二硝基水杨酸(3,5-dinitrosalicylic acid,DNS)(均为分析纯):北京化工厂;甲醇、无水乙醇、异丙醇(均为分析纯):天津市大茂化学试剂厂;HyPur T Ni-NTA 6FF(His-Tag)预装重力柱纯化试剂盒:上海生工生物技术有限公司。
1.1.3 培养基
LB液体培养基[12]:胰蛋白胨10.0 g/L,酵母提取物5.0 g/L,NaCl 10.0 g/L,pH 7.2,121 ℃高压蒸汽灭菌20 min。LB固体培养基:在LB液体培养基中添加琼脂20 g/L。
1.2 仪器与设备
H2-16KR台式高速离心机:湖南可成仪器设备有限公司;HC-2517高速离心机:安徽中科中佳科学仪器有限公司;JY96-IIN超声波细胞粉碎机:宁波新芝生物技术有限公司;MZB-25ZS制冰机:长虹美菱股份有限公司;MULTISKAN FC酶标仪:昆明友宁科技有限公司;WB100-1恒温水浴锅:宁波市鄞州群安实验仪器有限公司;DYY-12型电泳仪:北京市六一仪器厂。
1.3 方法
1.3.1 海藻糖酶Adb1332氨基酸序列分析
将海藻糖酶Adb1332的氨基酸序列提交至美国国家生物技术信息中心(National Center for Biotechnology Informa tion,NCBI),采用蛋白质基本局部比对搜索工具(basic local alignment search tool for proteins,BLASTP)与非冗余蛋白质序列(non-redundant protein sequence,NR)数据库、通用蛋白质知识数据库(universal protein knowledgebase,UniProtKB)和蛋白质数据库(protein data bank,PDB)中的蛋白质氨基酸序列进行序列相似性检索,并基于邻接法(neighbor-joining,NJ)采用MEGA11软件构建系统发育树。
1.3.2 海藻糖酶Adb1332的异源表达
根据参考文献[13],基于E.coli表达宿主对海藻糖酶Adb1332基因进行密码子优化,再由生工生物工程(上海)股份有限公司合成。采用NdeI和XhoI内切酶将合成的海藻糖酶Adb1332基因与pET28a质粒进行双酶切后连接,并构建重组质粒pET28a-Adb1332。将重组质粒pET28a-Adb1332导入感受态细胞E.coli BL21中,加入500 μL LB液体培养基,于37 ℃、180 r/min条件下培养2 h;将培养液涂布于含有50 μg/mL卡那霉素抗性的LB固体培养基平板上,于37 ℃条件下过夜培养。挑取单菌落,接种到含有50 μg/mL卡那霉素的5 mL LB液体培养基中,于37 ℃、220 r/min条件下培养12h作为种子液。将种子液按3%的接种量接种于含50μg/mL卡那霉素的LB液体培养基中,于37 ℃、220 r/min条件下培养至OD600nm值为0.6。随后加入150 μL IPTG诱导剂(0.5 mol/L),于16 ℃、220 r/min条件下培养20 h。
发酵液在8 000 r/min条件下离心10 min收集菌体,用无菌水重悬菌体,8 000 r/min离心10 min收集菌体,重复清洗3次,除去残留的还原糖。采用20 mL pH 7.5的非变性裂解液重悬细胞,加入2 μL溶菌酶(50 mg/mL),混匀,于冰上酶解30 min后,超声破碎细胞(150 W,1 h,开3 s,关6 s),在8 000 r/min条件下离心20 min,收集上清液即为粗酶液。以E.coli BL21 pET28a为对照,采用十二烷基硫酸钠聚丙烯酰胺凝胶电泳(sodium dodecyl sulfate polyacrylamide gel electrophoresis,SDS-PAGE)检测粗酶液。
1.3.3 海藻糖酶Adb1332的分离纯化
选择10 mL镍柱,用结合液(10 mmol/L咪唑的磷酸缓冲液)平衡镍柱,取破碎上清液过柱,以1倍柱体积的结合液洗脱杂蛋白,然后依次用1倍柱体积不同浓度(30、50、100、150、200和250 mmol/L)的咪唑洗脱液洗脱重组蛋白,分别收集不同浓度的洗脱液。将收集到的液体用于酶活检测和SDS-PAGE分析[14]。不同浓度的咪唑洗脱缓冲液及SDSPAGE凝胶的配制参照文献[15-16]。
1.3.4 海藻糖酶活力的测定
采用DNS比色法测定海藻糖酶活力[17]。海藻糖酶活力定义:1 min催化海藻糖水解产生1 μmol葡萄糖所需要的酶量。
1.3.5 海藻糖酶Adb1332酶学性质研究
温度对海藻糖酶Adb1332活力的影响:在pH 6.0及不同温度(40 ℃、50 ℃、55 ℃、60 ℃、65 ℃、70 ℃、80 ℃和90 ℃)条件下测定酶活力,以确定该酶的最适反应温度。将最高酶活力定义为100%,计算相对酶活。将海藻糖酶Adb1332纯酶液在不同温度(40 ℃、50 ℃、55 ℃、60 ℃和70 ℃)条件下孵育48 h,分别在1 h、2 h、4 h、6 h、8 h、12 h、24 h、36 h和48 h后采用最适条件测定酶活力,并以未进行温度处理酶液的酶活力定义为100%,计算相对酶活,考察该酶的热稳定性。
pH对海藻糖酶Adb1332活力的影响:配制柠檬酸-磷酸氢二钠缓冲液(200 mmol/L,pH 3.0~7.0)和甘氨酸-NaOH缓冲液(200 mmol/L,pH 7.5~9.0),在最适温度及不同pH值(4.0、5.0、5.5、6.0、6.5、7.0、8.0和9.0)条件下测定酶活力,以确定该酶的最适反应pH。将最高酶活力定义为100%,计算相对酶活。将海藻糖酶Adb1332纯酶液置于不同pH的(4.0、5.0、5.5、6.0、6.5、7.0、8.0和9.0)缓冲液中,60 ℃条件下放置24 h后,采用最适条件测定酶活力,并以未进行pH处理酶液的的酶活力定义为100%,计算相对酶活,考察该酶的pH稳定性。
金属离子与化学试剂对海藻糖酶Adb1332活力的影响:在海藻糖酶Adb1332纯酶液中分别添加终浓度为0.2 mmol/L、1 mmol/L和5 mmol/L的Fe2+、Mg2+、Ni2+、Co2+、K+、Hg2+、Mn2+、Cu2+、Al3+、Na+和Zn2+以及终体积分数为1%、3%、5%和7%的β-巯基乙醇、SDS、吐温20、尿素,在最适反应条件下测定酶活力,并以不添加金属离子或化学试剂的酶活力定义为100%,计算相对酶活,考察不同金属离子及化学试剂对海藻糖酶Adb1332活力的影响。
有机溶剂对海藻糖酶Adb1332活力的影响:在最适反应条件下,考察不同体积分数(5%、10%、20%、30%和50%)的有机溶剂甲醇、无水乙醇和异丙醇对该酶酶活力的影响,以不添加有机溶剂的酶活力定义为100%,计算相对酶活,考察该酶对有机溶剂的耐受情况。
底物特异性分析:在最适反应条件下,分别测定海藻糖酶Adb1332对2%的β-葡聚糖、水苏糖、海藻糖、木聚糖、昆布多糖和普鲁兰多糖溶液的水解能力。以水解海藻糖的酶活力定义为100%,计算水解其他底物的相对酶活。
动力学参数:采用pH 6.0的缓冲液分别配制浓度为1 mmol/L、5 mmol/L、10 mmol/L、30 mmol/L、50 mmol/L、70mmol/L、90mmol/L、110mmol/L、130mmol/L、150mmol/L、200 mmol/L、258 mmol/L、516 mmol/L、775 mmol/L和1 033 mmol/L的海藻糖溶液。在最适反应条件下,测定海藻糖酶Adb1332的活力,并结合葡萄糖标准曲线计算酶的水解反应速率。以底物浓度(x)为横坐标,反应速率(y)为纵坐标,绘制酶促动力学曲线,求米氏常数Km和最大反应速率Vmax。
1.3.6 海藻糖酶Adb1332的分子对接
采用LeDock软件预测海藻糖酶Adb1332的催化过程[18]。将海藻糖与海藻糖酶Adb1332进行分子对接,结果用PyMOL 2.3.0软件进行可视化。
2 结果与分析
2.1 海藻糖酶Adb1332的氨基酸序列分析
基于氨基酸序列海藻糖酶Adb1332的系统发育树见图1。由图1可知,海藻糖酶Adb1332与GH13糖苷水解酶家族29亚家族的氨基酸序列具有最高的相似性且聚为一个分支,表明海藻糖酶Adb1332归属于GH13_29亚家族。

图1 基于氨基酸序列海藻糖酶Adb1332的系统发育树
Fig.1 Phylogenetic tree of trehalase Adb1332 based on amino acid sequence
2.2 海藻糖酶Adb1332的异源表达及分离纯化
将粗酶液经Ni柱分离纯化后,采用SDS-PAGE进行检测,结果见图2。由图2可知,与泳道2相比,泳道3在55~70 kDa之间存在一个明显的条带,与海藻糖酶Adb1332的理论分子质量66 kDa相符,说明异源表达成功;泳道4在55~70 kDa之间也存在明显的单一条带,说明得到了纯海藻糖酶Adb1332。
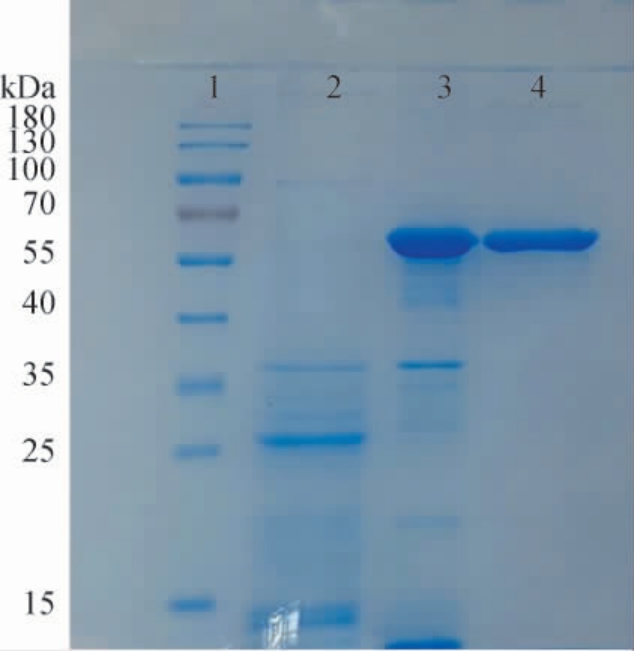
图2 海藻糖酶Adb1332的十二烷基硫酸钠-聚丙烯酰胺凝胶电泳图
Fig.2 Sodium dodecyl sulfate-polyacrylamide gel electropherogram of trehalase Adb1332
1:蛋白Marker;2:E.coli BL21 pET28a发酵液;3:粗酶液;4:纯化后的酶液。
2.3 海藻糖酶Adb1332的酶学性质
2.3.1 温度对海藻糖酶Adb1332活力的影响
温度对海藻糖酶Adb1332活力的影响见图3。由图3a可知,在40~90 ℃范围内,随着温度的升高,海藻糖酶Adb1332活力总体呈现出先升高后下降的趋势;当温度为60 ℃时,相对酶活最高,说明其最适反应温度为60 ℃。尽管海藻糖酶Adb1332的最适反应温度低于海洋红嗜热菌(Rhodothermus marinus)(88 ℃)[19]和嗜酸热硫化叶菌(Sulfolobus acidocaldarius)(85 ℃)[20]来源的海藻糖酶,但仍然高于大多数的酶[3,21-28],属于典型的耐高温海藻糖酶。
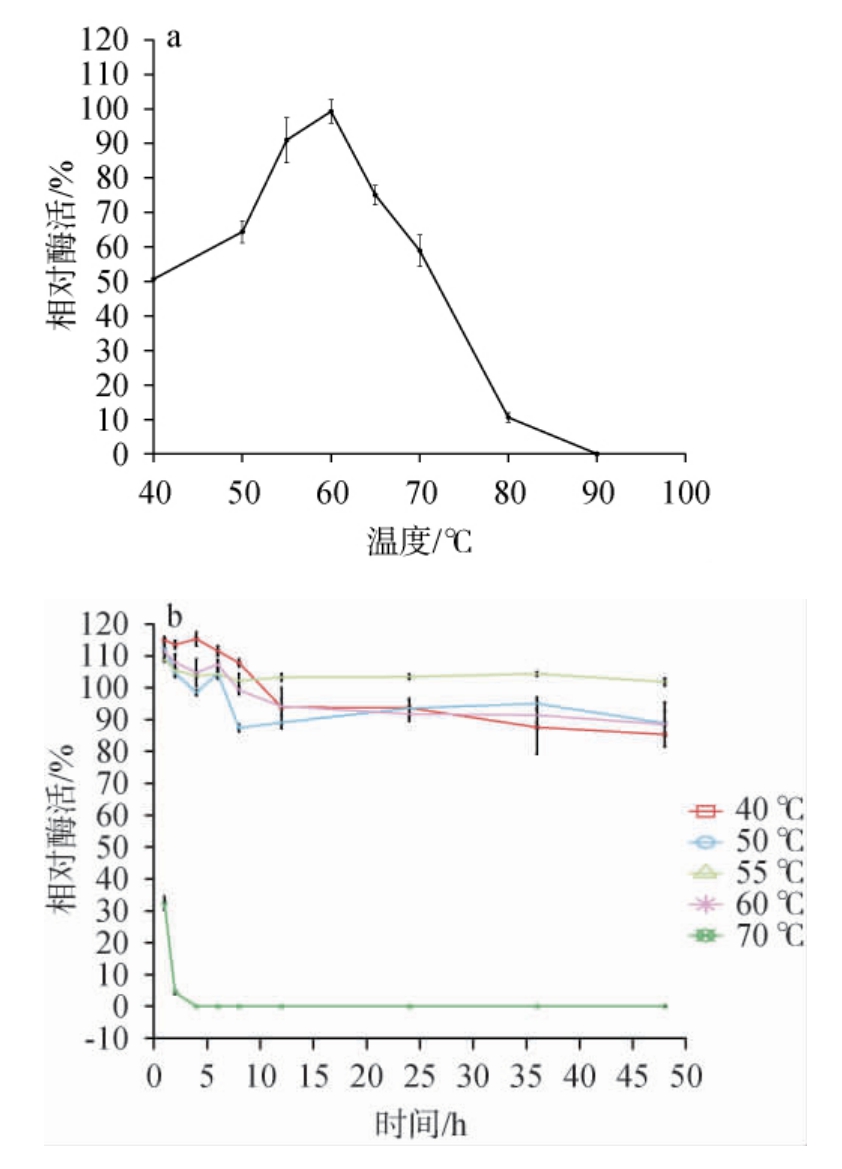
图3 海藻糖酶Adb1332的最适反应温度(a)及温度稳定性(b)
Fig.3 Optimum reaction temperature (a) and temperature stability (b)of trehalase Adb1332
由图3b可知,在40~60 ℃条件下孵育48 h,海藻糖酶Adb1332的相对酶活>50%。然而,海藻糖酶Adb1332在70℃条件下孵育1 h后,相对酶活迅速下降,相对酶活<30%;在60 ℃条件下孵育48 h时,海藻糖酶Adb1332的相对酶活仍>80%,其热稳定性强于嗜热毁丝菌(Myceliophthora thermophila)来源的海藻糖酶MthT(60 ℃孵育3 h后,仅保留60%的相对酶活)[9]和瘤孢梭孢壳(Myceliophthra sepedonium)来源的海藻糖酶TreM(55 ℃孵育3 h后,仅保留70%的相对酶活)[22]。结果表明,海藻糖酶Adb1332显示了良好的热稳定性,具有较强的工业应用潜力[9,29]。
2.3.2 pH对海藻糖酶Adb1332活力的影响
pH对海藻糖酶Adb1332活力的影响见图4。
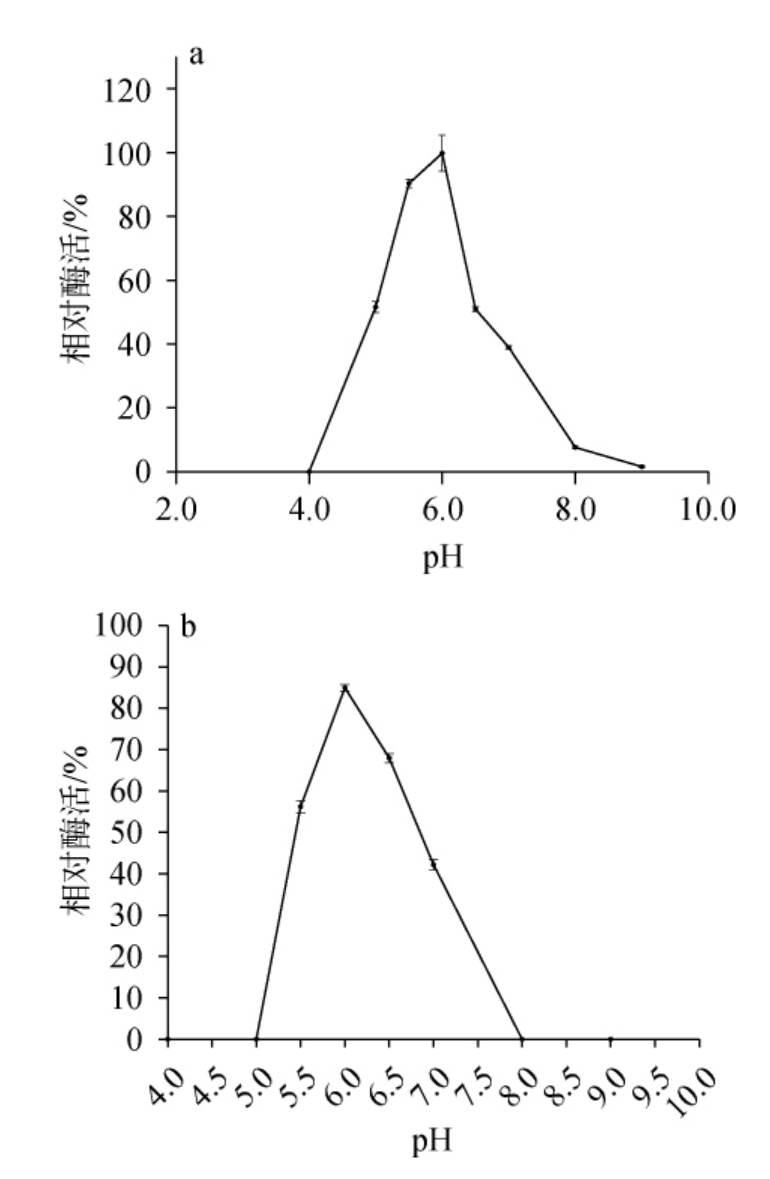
图4 海藻糖酶Adb1332的最适反应pH(a)及pH稳定性(b)
Fig.4 Optimum reaction pH (a) and pH stability (b) of trehalase Adb1332
由图4a可知,随着pH在4.0~6.0范围内的升高,海藻糖酶Adb1332活力呈先升高后下降的趋势,当pH为6.0时,海藻糖酶Adb1332活力最高,说明海藻糖酶Adb1332的最适pH为6.0。由图4b可知,在温度60 ℃、pH 6.0条件下孵育24 h,海藻糖酶Adb1332的相对酶活>80%;在温度60 ℃、pH 5.5~7.0条件下孵育24h,海藻糖酶Adb1332的相对酶活均>40%,说明海藻糖酶Adb1332在pH 5.5~7.0之间酶活比较稳定。
2.3.3 有机溶剂对海藻糖酶Abd1332活力的影响
不同有机溶剂对海藻糖酶Adb1332活力的影响见图5。由图5可知,不同体积分数的有机溶剂对海藻糖酶Adb1332的活力均有抑制作用,且体积分数越大,抑制作用越大。采用5%的甲醇和无水乙醇处理时,海藻糖酶Adb1332的相对酶活>60%,而采用5%的异丙醇处理时,海藻糖酶Adb1332的相对酶活<40%;当采用10%的甲醇或无水乙醇处理时,海藻糖酶Adb1332的相对酶活仍>40%,而分别采用体积分数>20%的甲醇、体积分数>10%的无水乙醇、异丙醇进行处理时,海藻糖酶Adb1332的酶活完全被抑制。结果表明,海藻糖酶Adb1332可分别耐受20%的甲醇、10%的无水乙醇及10%的异丙醇,且海藻糖酶Adb1332在体积分数为10%的甲醇或无水乙醇的环境中,仍保持了40%以上的酶活,使其在乙醇和谷氨酸的发酵等工业生产中具有一定的应用潜力[9-10]。
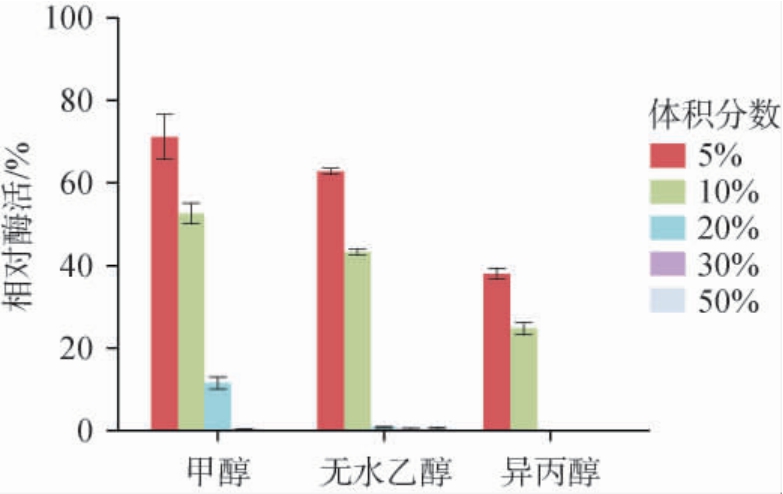
图5 不同有机溶剂对海藻糖酶Adb1332活力的影响
Fig.5 Effect of different organic reagents on trehalase Adb1332 activity
2.3.4 金属离子和化学试剂对海藻糖酶Adb1332活力的影响
不同金属离子和化学试剂对海藻糖酶Adb1332活力的影响见图6。由图6a可知,Hg2+对海藻糖酶Adb1332具有明显的抑制作用,当浓度为5 mmol/L时酶几乎失活;当Co2+浓度为0.2 mmol/L和1 mmol/L时,海藻糖酶Adb1332的相对酶活均>100%,而当浓度达到5 mmol/L时,相对酶活明显下降,说明低浓度的Co2+会促进海藻糖酶Adb1332的活性,高浓度抑制其活性;Mg2+、Ni2+、K+、Na+、Zn2+在浓度为0.2~5 mmol/L时,海藻糖酶Adb1332的相对酶活均保持在90%左右,说明Mg2+、Ni2+、K+、Na+、Zn2+对海藻糖酶Adb1332的活性影响较小;Al3+在浓度为0.2 mmol/L和1 mmol/L时对海藻糖酶Adb1332的活性影响较小,当浓度达到5 mmol/L时,相对酶活明显上升,说明增加一定浓度的Al3+可以促进海藻糖酶Adb1332的活性;Fe2+、Mn2+、Cu2+在浓度为0.2~5 mmol/L时,海藻糖酶Adb1332的相对酶活均>100%,有明显的促进作用,说明Fe2+、Mn2+、Cu2+可以促进海藻糖酶Adb1332的活性。
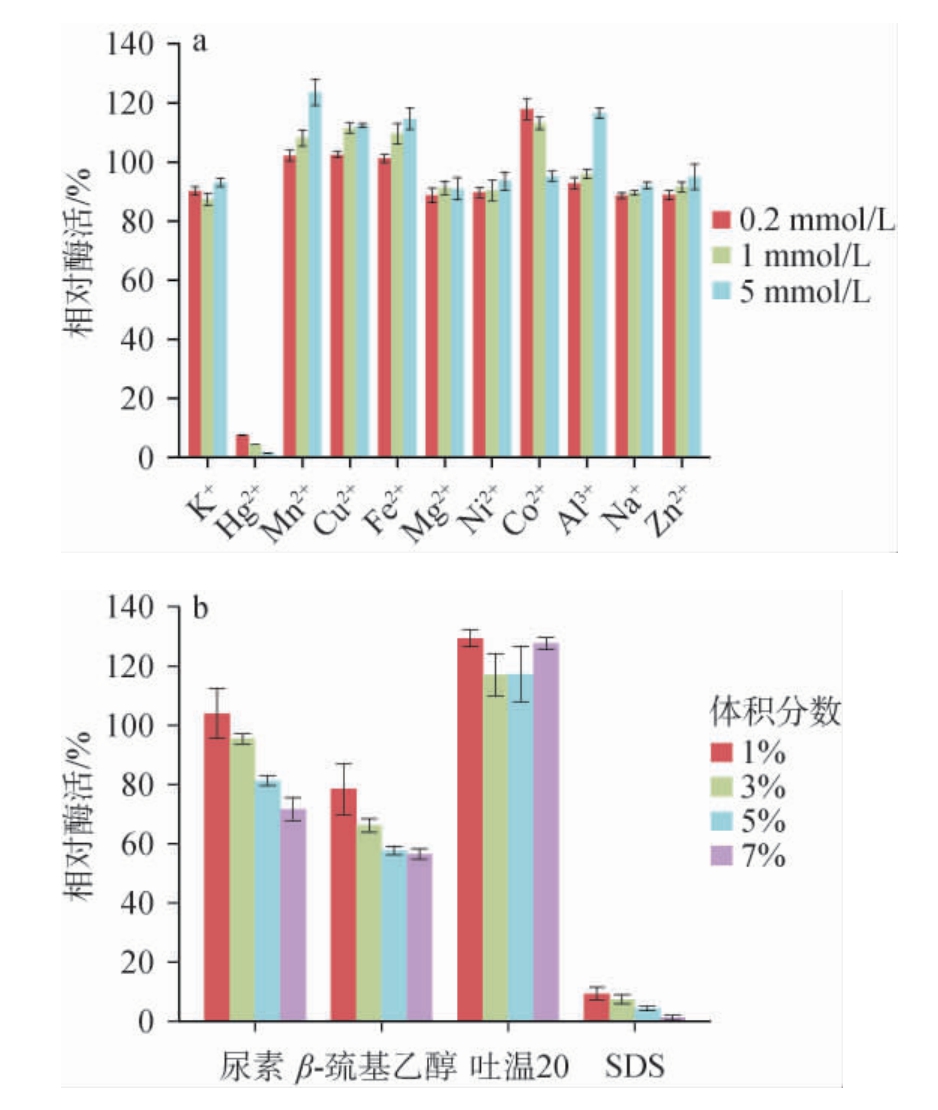
图6 金属离子(a)和化学试剂(b)对海藻糖酶Adb1332活力的影响
Fig.6 Effect of mental ions (a) and chemical reagents (b) on trehalase Adb1332 activity
由图6b可知,吐温20能够促进海藻糖酶Adb1332的活性;SDS对海藻糖酶Adb1332的活力具有明显的抑制作用,当SDS体积分数为1%时,相对酶活力<10%;随着尿素和β-巯基乙醇浓度的升高,对海藻糖酶Adb1332活性的抑制作用越明显,当尿素或β-巯基乙醇的体积分数为7%时,海藻糖酶Adb1332的相对酶活<70%。
综上,Fe2+、Mn2+和Cu2+能促进酶活,浓度≤1 mmol/L的Co2+能提高酶活,浓度为5 mmol/L的Al3+能提高酶活,而Hg2+则抑制酶活,其他金属离子对酶活影响较小。吐温20能提高海藻糖酶Adb1332的酶活,SDS对海藻糖酶Adb1332的酶活具有明显的抑制作用,高浓度的尿素和β-巯基乙醇能抑制海藻糖酶Adb1332酶活。
2.3.5 海藻糖酶Adb1332的底物特异性和动力学研究
在最适反应条件下测定海藻糖酶Adb1332对不同底物的水解效率及酶促反应动力学,结果见图7。由图7a可知,海藻糖酶Adb1332对海藻糖的水解活性最高,对水苏糖具有轻微的水解活性,而对β-葡聚糖、普鲁兰多糖、木聚糖和昆布多糖几乎没有水解活性。结果表明,海藻糖酶Adb1332对海藻糖具有专一性。由图7b可知,利用米氏方程进行拟合得到米氏常数Km值为(284.06±28.58),表明酶与底物的亲和力较高,最大反应速率(Vmax)为(0.30±0.01)mmol/(L·min)。
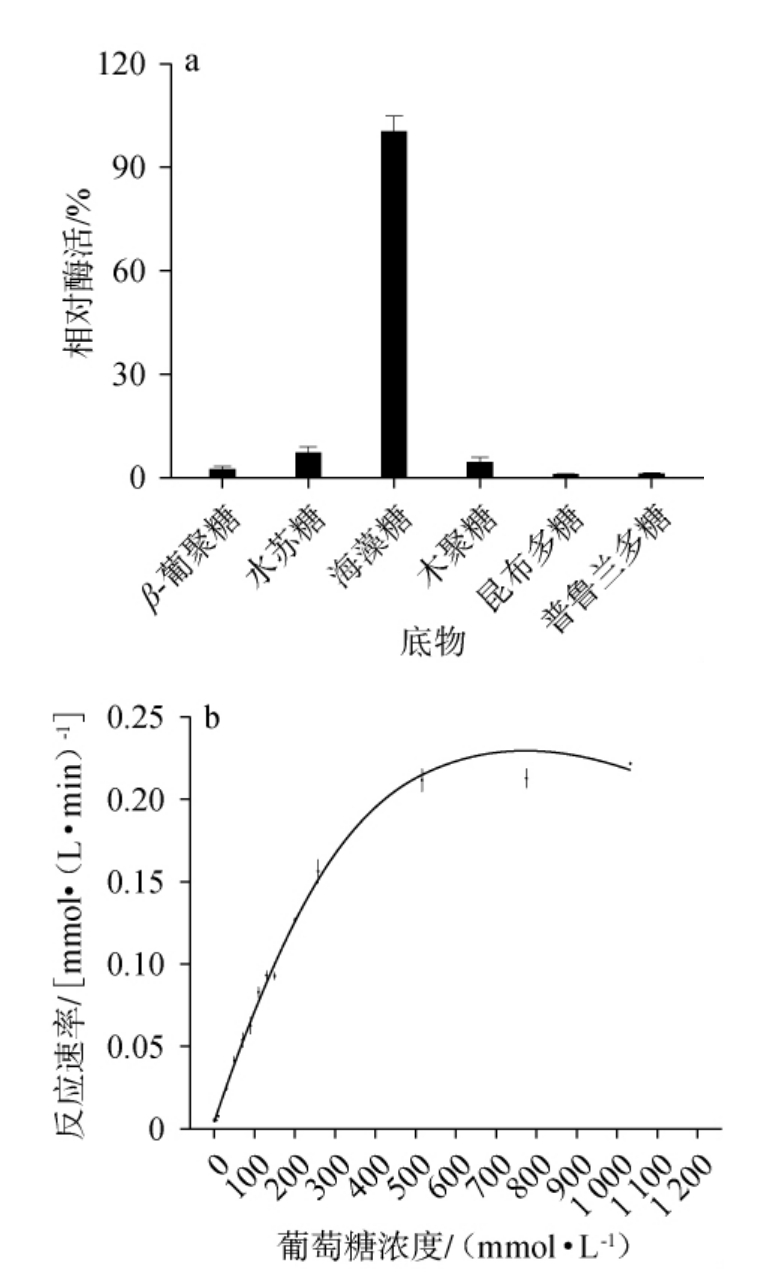
图7 海藻糖酶Adb1332的底物特异性(a)及酶促反应动力学曲线(b)
Fig.7 Substrates specificity (a) and enzymatic reaction kinetics curve (b) of trehalase Adb1332
2.4 海藻糖酶Adb1332与海藻糖的分子对接
具有最低结合能的海藻糖酶Adb1332与海藻糖的对接模型见图8。
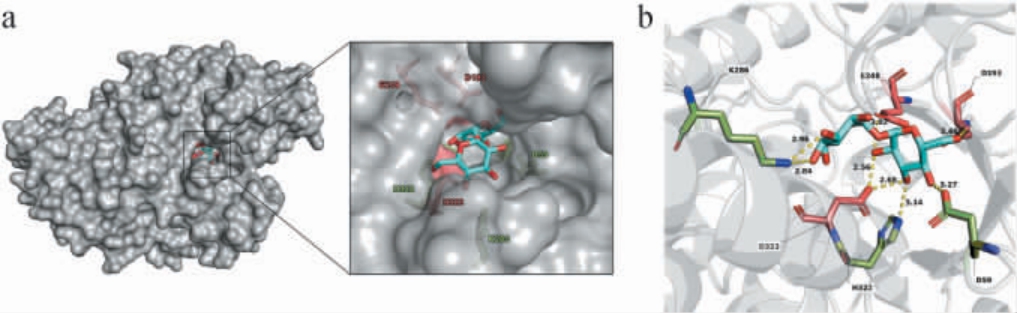
图8 海藻糖酶Adb1332与海藻糖的分子对接结果(a)及作用力(b)
Fig.8 Molecular docking result (a) and reaction force (b) of trehalase Adb1332 and trehalose
由图8a可知,海藻糖分子对接到海藻糖酶Adb1332的活性口袋中,与天冬氨酸(aspartic acid,Asp)193、Asp323和谷氨酸(glutamate,Glu)248相互作用,催化海藻糖分子水解为2分子葡萄糖。Asp193、Asp323和Glu248三联体构成了海藻糖酶的催化活性位点,在GH13家族中具有高度的保守性[7]。Asp193作为亲和催化残基,Glu248作为酸碱催化残基,而Asp323具有稳定酶与底物形成的过渡态复合物的功能,以双交换机制实现底物的催化水解[7]。由图8b可知,Asp59、组氨酸(histidine,His)332和赖氨酸(lysine,Lys)286与海藻糖通过氢键连接,有助于底物的识别和催化中间体的稳定。
3 结论
本研究首次从云南热泉无氧芽孢杆菌(Anoxybacillus sp.)YHS0032中克隆表达新型嗜热海藻糖酶Adb1332(GH13_29家族),分子质量为66 kDa。该酶具有高效嗜热性,最适反应温度为60 ℃,在此温度下孵育48 h,相对酶活仍>80%,并在40~60 ℃范围内维持高催化效率;其最适pH为6.0,在pH 5.5~7.0条件下孵育24 h,相对酶活维持在40%以上,显示出广泛的酸碱适应性。此外,Adb1332具有良好的有机溶剂耐受性,可耐受体积分数20%甲醇、10%无水乙醇及10%异丙醇,且在体积分数为10%甲醇或无水乙醇溶液中相对酶活>40%,使其在甲醇或乙醇的工业生产中具有潜在的应用价值。金属离子Fe2+、Mn2+和Cu2+可明显激活海藻糖酶Adb1332活力,而Hg2+则明显抑制其活力;吐温20能促进酶活,而SDS抑制酶活。底物动力学分析证实海藻糖酶Adb1332对海藻糖具有底物专一性,Km值为(284.06±28.58),Vmax为(0.30±0.01)mmol/(L·min),其主要通过氢键与底物连接,催化位点为天冬氨酸(Asp)193、Asp323和谷氨酸(Glu)248。本研究结果证实了海藻糖酶Adb1332具有在燃料乙醇和谷氨酸发酵应用的潜力,为生物能源和食品工业提供了高效、稳定的生物催化剂。
[1] ADHAV A,HARNE S,BHIDE A,et al.Mechanistic insights into enzymatic catalysis by trehalase from the insect gut endosymbiont Enterobacter cloacae[J].FEBS J,2009,286(9):1700-1716.
[2] 王一雯,马焕,权淑静,等.昆明假单胞菌HL22-2海藻糖合酶基因的克隆、表达及酶学性质研究[J].中国酿造,2020,39(1):154-159.
[3] SU C,GONG J S,DONG Q,et al.Efficient production and characterization of a newly identified trehalase for inhibiting the formation of bacterial biofilms[J].Int J Bio Macromol,2024,262:129928.
[4] GAO H,GONG J S,SU C,et al.Characterization,heterologous expression and engineering of trehalase for biotechnological applications[J].SMAB,2022,2(3):445-460.
[5] 师东梅,蒋志洋,邹雪君,等.海藻糖酶结构及其抑制剂的农用活性研究进展[J].农药学学报,2022,24(5):1017-1033.
[6] SAKAGUCH M.Diverse and common features of trehalases and their contributions to microbial trehalose metabolism[J].Appl Microbiol Biotechnol,2020,104(5):1837-1847.
[7] LIN M G,CHI M C,NAVEEN V,et al.Bacillus licheniformis trehalose-6-phosphate hydrolase structures suggest keys to substrate specificity[J].Acta Crystallogr D Struct Biol,2016,72(1):59-70.
[8] 何迎粉,何荣荣,刘敦华,等.海藻糖与酿酒酵母乙醇耐受性相关性的研究进展[J].中国酿造,2020,39(11):1-4.
[9]DONG L,LIN X,YU D,et al.High-level expression of highly active and thermostable trehalase from Myceliophthora thermophila in Aspergillus niger by using the CRISPR/Cas9 tool and its application in ethanol fermentation[J].J Ind Microbiol Biotechnol,2020,47(1):133-144.
[10] 满在伟,崔慧慧,李锦,等.谷氨酸棒杆菌表达大肠杆菌来源海藻糖酶[J].食品研究与开发,2022,43(24):181-187.
[11] SHRESTHA P,KARMACHARYA J,KIM K H,et al.Exploration of novel trehalases from cold-adapted Variovorax sp.PAMC28711: Functional characterization[J].Int J Bio Macromol,2024,271(1):132503.
[12] JIRA J,REZEK B,KRIHA V,et al.Inhibition of E.coli growth by nanodiamond and graphene oxide enhanced by Luria-Bertani medium[J].Nanomaterials,2018,8(140):1-13.
[13] BLATTNER F R,PLUNKETT G,BLOCH C A,et al.The complete genome sequence of Escherichia coli K-12[J].Science,1997,277(5331):1453-1462.
[14] 高涵.高活性海藻糖酶的克隆表达及其应用研究[D].无锡:江南大学,2022.
[15] 申欢欢.猪圆环病毒Ⅱ型Cap蛋白的原核表达、纯化和酶活性探索[D].郑州:河南农业大学,2017.
[16] 白茹.白酒酿造用真菌酯化酶的挖掘、表达及催化性质研究[D].天津:天津科技大学,2022.
[17] 王俊刚,张树珍,杨本鹏,等.3,5-二硝基水杨酸(DNS)法测定甘蔗茎节总糖和还原糖含量[J].甘蔗糖业,2008(5):45-49.
[18] WANG Z,SUN H,YAO X,et al.Comprehensive evaluation of ten docking programs on a diverse set of protein-ligand complexes:the prediction accuracy of sampling power and scoring power[J].Phys Chem Chem Phys,2016,18:12964-12975.
[19] JORGE C D,SAMPAIO M M,HREGGVIDSSON G O,et al.A highly thermostable trehalase from the thermophilic bacterium Rhodothermus marinus[J].Extremophiles,2007,11(1):115-122.
[20] MOON J H,LEE W,PARK J,et al.Characterization of a trehalose-degrading enzyme from the hyperthermophilic archaeon Sulfolobus acidocaldarius[J].J Biosci Bioeng,2016,122:47-51.
[21] ALMEID F M D,BONINI B M,BETON D,et al.Heterologous expression in Escherichia coli of Neurospora crassa neutral trehalase as an active enzyme[J].Protein Expre Purif,2009,65:185-189.
[22] DONG L B,YU D,LIN X T,et al.Improving expression of thermostable trehalase from Myceliophthora sepedonium in Aspergillus niger mediated by the CRISPR/Cas9 tool and its purification,characterization[J].Protein Expres Purif,2020,165:105482.
[23] WANG Q T,FANG K,QI L,et al.Purification and functional characterization of a soluble trehalase in Lissorhoptrus oryzophilus (Coleoptera:Curculionidae)[J].Insects,2022,13:867.
[24] DONG C,FAN Q,LI X,et al.Expression and characterization of a novel trehalase from Microvirga sp.strain MC18[J].Protein Expres Purif,2021,182:105846.
[25] NEYMAN V,FRANCIS F,MATAGNE A,et al.Purifcation and characterization of trehalase from Acyrthosiphon pisum,a target for pest control[J].Protein J,2022,41:189-200.
[26] WEN Z H,YAN S P,AMUJILATA,et al.Characterization of the trehalase function of Haemonchus contortus and its immunomodulatory effect on host PBMCs[J]. Int J Bio Macromol,2025,309:143102.
[27] ZHANG J,YU X,GUAN B,et al.Identification and characterization of a novel cold-adapted GH15 family trehalase from the psychrotolerant Microbacterium phyllosphaerae LW106[J].Fermentation,2022,8:471.
[28] AI D,CHENG S,CHANG H,et al.Gene cloning,prokaryotic expression,and biochemical characterization of a soluble trehalase in Helicoverpa armigera Hübner(Lepidoptera:Noctuidae)[J]. J Insect Sci,2018,18(3):1-8.
[29] FEOFILOBA E P,USOV A L,MYSYAKINA I S.Trehalose: chemical structure,biological functions,and practical application[J]. Microbiol,2014,83(3):184-194.