白酒是中国传统的酒精饮料,是中国传统文化的重要构成部分,也是世界上消费最多的蒸馏酒之一[1]。根据国家统计局(https://data.stats.gov.cn/)数据显示,近20年白酒产量呈现先增加后减少的趋势,2024年规模以上企业产量达到414.5万kL(折65%vol),当前行业面临产能过剩与供需失衡压力。在此背景下,白酒行业通过持续深化微生物在白酒生产中的作用机制研究,以指导生产工艺优化,推动高质量发展转型。 白酒以谷物为主要原料,以大曲、小曲、麸曲、酶制剂及酵母等为糖化发酵剂,经蒸煮、糖化、发酵、蒸馏、陈酿、勾调成的蒸馏酒,按香型可分为酱香型,浓香型,清香型,米香型等12种[2]。其中,优质大曲白酒的生产以固态纯粮发酵法为主,采用自然接种的多菌种混菌发酵。生产过程涉及环境微生物与大曲、酒醅、窖泥等载体中富集的酵母菌、细菌和霉菌等多菌系的共同作用[3]。这些微生物通过微生物相互作用起到调整群落结构和代谢产物的生成,最终影响构成了各种白酒独特的风味的生成[4-6]。
该文对相关文献进行分析,总结了微生物相互作用的研究方法及局限,总结了优势微生物菌属与其他微生物的相互作用,并阐明其作用机制,旨在深化对白酒微生物功能的认识,为酿酒过程微生物与风味物质形成机理的理解提供更多的参考。
1 白酒中的优势微生物
白酒生产过程中微生物间的相互作用影响生产效率、品质与安全[7]。 研究者通常会着重关注某些优势或核心微生物。SHEN S等[8]认为在酒醅中相对丰度>20%的微生物为核心微生物,相对丰度在1%~20%的微生物为优势微生物。HU X等[9]定义的核心微生物属在样品中平均相对丰度>1.00%,刘兰兰[10]将样品中平均丰度>1%且在至少两个样品中出现的微生物定义为核心微生物。本文对相对丰度>1%的主要优势微生物进行统计分析,并将其作为后续深入研究的重点对象。
考虑到不同香型白酒在生产过程中微生物群落构成存在显著差异,为使研究具有较高的代表性和应用价值,本文从Web of Science数据库检索了与制曲和发酵相关的文献并进行了统计,结果见图1。
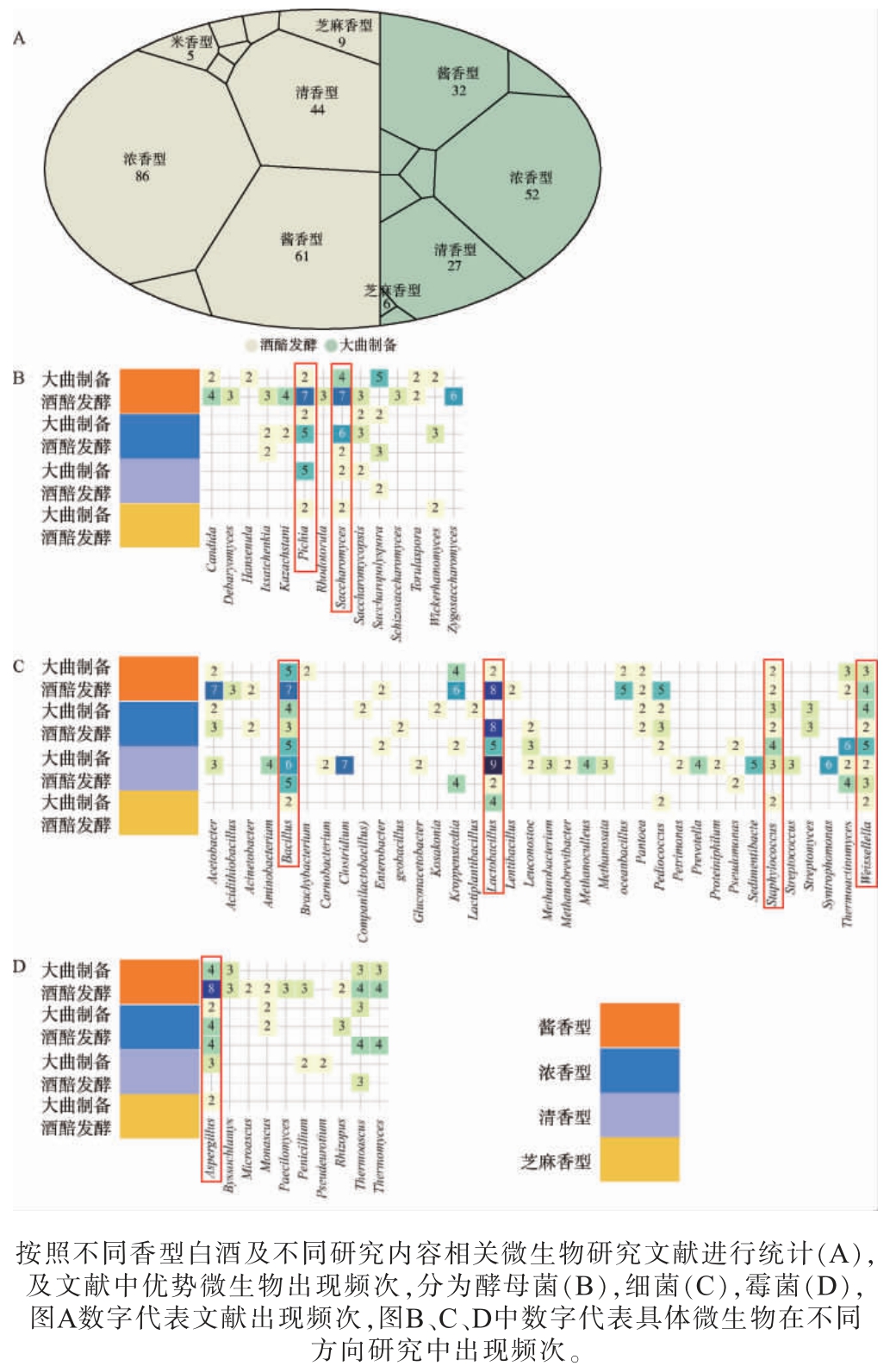
图1 源于Web of Science数据库不同香型白酒研究文献数量统计结果
Fig. 1 Statistical results of the number literatures on different types of Baijiu from Web of Science database
图1A展示了不同香型白酒研究的文献数量(以不同颜色区分不同研究内容,香型下数字代表文献数量),结果显示酱香型、浓香型、清香型及芝麻香型白酒的研究占比较高,因此重点分析统计这些香型白酒文献中出现的微生物。本文通过选取不同香型白酒及其生产过程中普遍出现且频次较高的优势微生物,从酱香型白酒,浓香型白酒,清香型白酒,芝麻香型白酒中发现了相对丰度>1%的优势微生物,见图1B~图1D。 其中数字代表着其在相关文献中出现频次。其中酵母菌(图1B)中的酵母属(Saccharomyces)和毕赤酵母属(Pichia),细菌(图1C)中的芽孢杆菌属(Bacillus)、乳酸杆菌属(Lactobacillus)、葡萄球菌属(Staphylococcus)和魏斯氏菌属(Weissella),霉菌(图1D)中的曲霉属(Aspergillus)为在多篇文献及多个不同生产过程中为重点关注的优势微生物。因此该文将针对上述优势微生物,综述其相互间的作用类型、研究方法及具体作用机制。
2 微生物相互作用机制及研究方法
2.1 微生物相互作用的类型和机制
优势微生物与其他微生物间存在多种互作类型,包括竞争、互利共生、偏利共生、偏害共生和寄生等。 这些相互作用包括营养互作和细胞信号传导机制两大类,前者包括营养竞争,交叉喂养等,后者以群体感应系统为代表[11]。交叉喂养作为典型机制,表现为某菌株分泌的代谢产物(如碳氮源、氨基酸、维生素等)被其他菌株作为生长基质利用[12]。在葡萄汁中观察到酿酒酵母释放的氨基酸和其他代谢产物能够刺激植物乳植杆菌(Lactiplantibacillus plantarum)的生长[12]。群体感应方面,AVBELJ M等[13]研究了葡萄酒酿酒酵母中的群体感应,群体感应分子被鉴定为2-苯基乙醇、色氨酸和酪醇。这些群体响应分子提升了酵母在面对乙醇和重金属等压力时的耐受性,并促进了芳香醇的合成,从而改善了食品的风味。
另一方面,微生物互作网络呈现复杂特征。 单一微生物可能受多种微生物互作影响,或某种互作受第三方微生物调控[14]。 这种动态关系影响了代谢产物,但同时也为机制解析带来挑战。
2.2 微生物相互作用的研究方法及局限
2.2.1 相关研究方法
阐明微生物相互作用机制已成为白酒发酵研究的关键环节之一。研究者主要采用统计分析与纯种共培养实验验证相结合的研究范式,基于高通量测序获得的微生物丰度数据,通过采用统计学相关性分析揭示微生物间的潜在互作关系。研究者通过皮尔逊(Pearson)相关系数、斯皮尔曼(Spearman)等级相关系数等统计方法,将相关系数矩阵中显著性较高的节点连接形成互作网络,为白酒发酵过程中复杂的微生物群落关系提供了直观视角[15-17]。 同时针对微生物群落数据具有高维度、高稀疏性特征,可以采用SparCC、CCLasso等优化算法以降低假阳性,这些改进算法在肠道微生物等复杂群落研究中已展现出应用潜力[18-20]。
在实验验证微生物互作方法中,通过分离优势菌属并进行纯种共培养实验的方法可通过构建简化群落模型揭示特定微生物间的相互作用机制,并通过结合基因组学与代谢组学等组学联用技术,系统解析互作过程中相关的基因表达和代谢产物形成之间的关系。SUN H等[21]探究从窖泥中分离的两种梭菌菌株,通过结合代谢组学和基因组学证实了其基于代谢物交换促进丁酸,己酸积累的互作机制。
另外一种方法是通过微生物群落模型分析,该方法通过结合组学数据、实验数据与数学建模,来模拟并解析微生物群落内相互作用[22]。两种常用方法来模拟群落动态:以物种或细胞为基本单位并以它们之间的相互作用为重点的生态模型,包括Lotka-Volterra模型、MacAuther消费者-资源模型、基于性状的模型、基于个体的模型,该模型使用生态参数(如生长率等)描述群落,相互作用缺乏对代谢通路的机制解析;另一种模型是以细胞内反应为主要单位并以营养生成/消耗为重点的基因组规模代谢模型,该模型可以预测代谢背景下的相互作用,同时提供群落动态描述[23-24]。其中基因组规模代谢模型在近10年来被广泛应用[25]。基于生物体特定数据库、高通量数据和科学文献基础上,该模型将目标生物体的所有代谢反应和代谢基因整合,构成基因-蛋白质-反应相关联的单细胞模型[26]。在假设群落处于稳态的情况下,根据群落使用基于通量平衡分析的方法从单物种扩展到多物种系统,从而完成对微生物群落建模[25]。目前常用工具有RAVEN 2.0[27]、KBase[28]、ModelSEED[29]、CarveMe[30]等。BASKARAN D K K等[31]利用CarveMe工具基于宏基因组学数据构建基因组规模的代谢模型,通过整合多种组学数据集和机器学习方法,更全面地代表基因型-表型关系,减少了假阴性和假阳性结果,揭示了古菌-细菌间非对称的代谢依赖关系。KUMAR R K等[32]使用ModelSEED工具为52种微生物构建了基因组规模的代谢模型并分析微生物之间的代谢依赖性和相互作用类型,并通过共培养实验验证了肺炎克雷伯菌细胞破坏曲霉菌的形态结构和生物膜形成能力。基因组规模代谢模型在微生物互作机制研究上存在显著优势,为研究白酒发酵体系中微生物相互作用提供了参考。
此外,机器学习在分析微生物间相互作用方面也有所应用,并且可以在一定程度上弥补基因组规模代谢模型在面对基因组注释不足和菌种数量过多难求解的劣势。该方法可以以多种类型的数据作为基础,LEE J Y等[33]利用深度残差网络,成功从显微图像中预测了微生物底物依赖性的互作关系。NESTOR E等[34]基于7 500多种土壤细菌共培养数据构建XGBoost模型,通过物种单一培养生长能力与系统发育信息预测成对相互作用方向,准确率达88%,强度预测相关系数R2值达0.87。DIMUCCI D等[35]整合了随机森林和基因组规模代谢模型,通过基因的存否、代谢功能、系统发育分类等其中一组数据作为特征向量,预测和验证复杂微生物群落中微生物相互作用,该研究在模拟人类肠道微生物群落(使用动态通量平衡代谢模型模拟获得)、营养缺陷型大肠杆菌以及土壤微生物群落的数据集上均取得了约80%至90%的预测准确率。这些结果证明,机器学习模型能够从有限的实验数据中高效推断出微生物间潜在的相互作用。
2.2.2 研究方法的局限
尽管上述方法在解析优势微生物互作关系方面已获得一定的成效,但仍有一定的局限性。 基于统计分析的相关性研究方法,如皮尔逊相关系数和斯皮尔曼等级相关系数,常用于从高通量测序数据中计算微生物间的相关性程度,进而推断其潜在相互作用。然而,此类方法难以区分直接互作与间接关联,且存在较高的误判风险。 通过分离优势菌属并进行纯种共培养实验的方法,虽可深入揭示微生物间的互作机制,但受限于微生物的可培养性,能够系统研究的互作组合较为有限,且难以全面反映多物种共存环境下复杂的群落交互效应。在微生物群落建模方面,生态模型因缺乏明确的机制解释及参数不确定性较高而应用受限;基因组尺度代谢模型则面临计算复杂度高和对高质量输入数据依赖性强等挑战。 此外,机器学习模型的预测性能与结果可靠性高度依赖于训练数据的数量与质量,数据不足或偏差较大易导致模型泛化能力下降。
因此,将多种方法结合探究微生物互作机制成为一种潜在发展方向,目前已经使用统计分析与共培养实验验证结合,发现了微生物互作。而在下一步研究中,将基因组规模代谢模型与机器学习相结合被认为是代谢建模中重要的发展方向,通过两者结合弥补基因组规模代谢模型对基因组注释不足及求解难题和机器学习黑箱的缺陷[24]。因此使用多种方法相结合将深化对微生物互作机制的探索研究。
3 优势微生物的相互作用
基于现有微生物相互作用研究方法,总结了部分优势微生物之间的互作关系,相关性分析结果见表1。 由表1可知,乳酸杆菌属和芽孢杆菌属与其他微生物表现出较多的正负相关性。 乳酸杆菌属与其他微生物存在20种正相关和21种负相关关系,芽孢杆菌属则具有15种正相关和15种负相关关系,表明这两类微生物可能处于较为复杂的生态位中,参与多样化的种间相互作用。而葡萄球菌属和魏斯氏菌属的正相关数量显著高于负相关,提示其更倾向于形成互利共生的协作关系。而酵母属、毕赤酵母属及曲霉属的正负相关性数量相对均衡,反映出它们在微生物群落中可能同时维持着合作与竞争的动态平衡。需注意的是,这些关联性结果源于统计学相关方法推断,其具体作用机制仍有待阐明。
表1 优势微生物与其他微生物间的相关性分析
Table 1 Correlation analysis between dominant microorganisms and other microorganisms
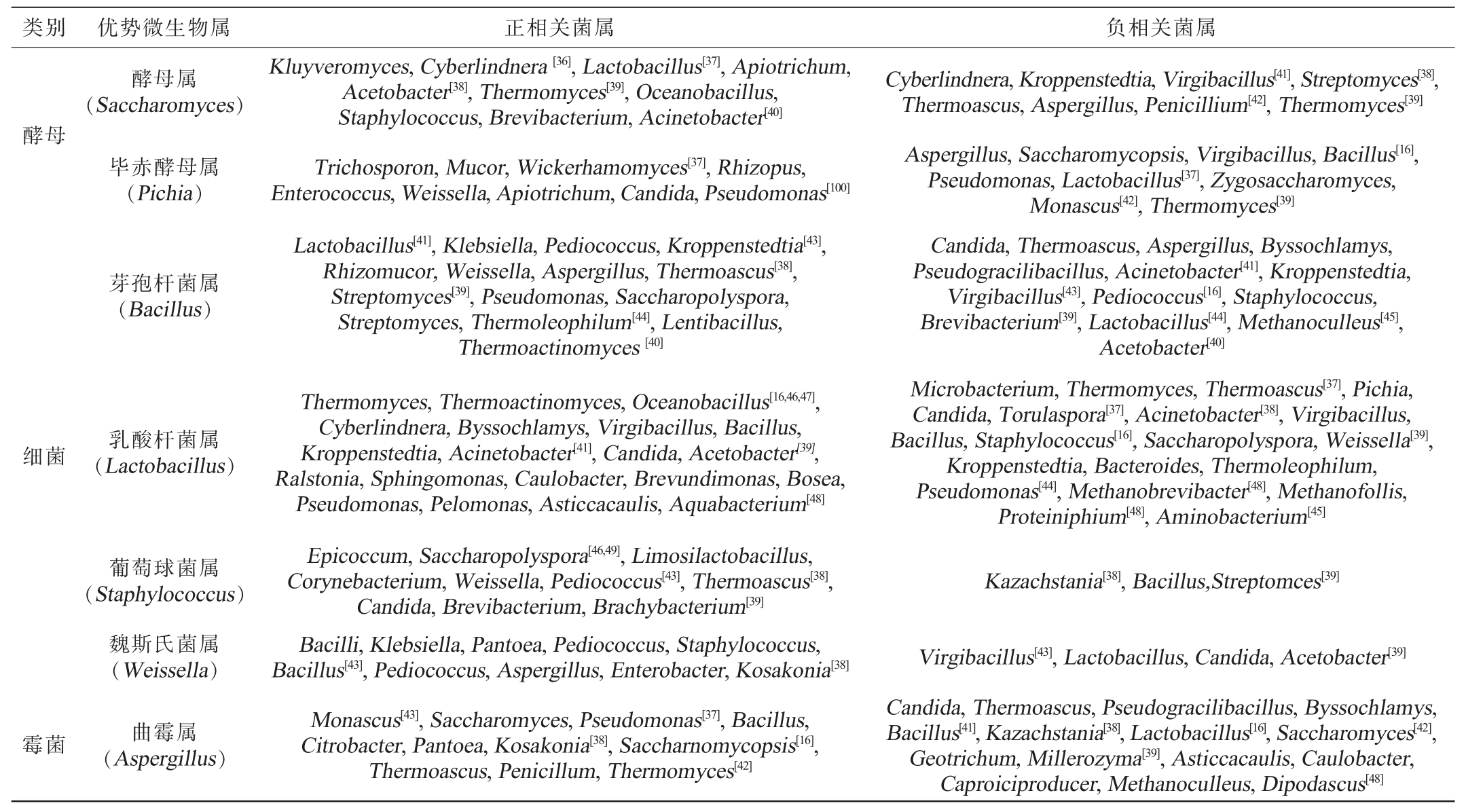
类别优势微生物属正相关菌属负相关菌属酵母细菌霉菌酵母属(Saccharomyces)毕赤酵母属(Pichia)芽孢杆菌属(Bacillus)乳酸杆菌属(Lactobacillus)葡萄球菌属(Staphylococcus)魏斯氏菌属(Weissella)曲霉属(Aspergillus)Kluyveromyces,Cyberlindnera [36],Lactobacillus[37],Apiotrichum,Acetobacter[38],Thermomyces[39],Oceanobacillus,Staphylococcus,Brevibacterium,Acinetobacter[40]Trichosporon,Mucor,Wickerhamomyces[37],Rhizopus,Enterococcus,Weissella,Apiotrichum,Candida,Pseudomonas[100]Lactobacillus[41],Klebsiella,Pediococcus,Kroppenstedtia[43],Rhizomucor,Weissella,Aspergillus,Thermoascus[38],Streptomyces[39],Pseudomonas,Saccharopolyspora,Streptomyces,Thermoleophilum[44],Lentibacillus,Thermoactinomyces [40]Thermomyces,Thermoactinomyces,Oceanobacillus[16,46,47],Cyberlindnera,Byssochlamys,Virgibacillus,Bacillus,Kroppenstedtia,Acinetobacter[41],Candida,Acetobacter[39],Ralstonia,Sphingomonas,Caulobacter,Brevundimonas,Bosea,Pseudomonas,Pelomonas,Asticcacaulis,Aquabacterium[48]Epicoccum,Saccharopolyspora[46,49],Limosilactobacillus,Corynebacterium,Weissella,Pediococcus[43],Thermoascus[38],Candida,Brevibacterium,Brachybacterium[39]Bacilli,Klebsiella,Pantoea,Pediococcus,Staphylococcus,Bacillus[43],Pediococcus,Aspergillus,Enterobacter,Kosakonia[38]Monascus[43],Saccharomyces,Pseudomonas[37],Bacillus,Citrobacter,Pantoea,Kosakonia[38],Saccharnomycopsis[16],Thermoascus,Penicillum,Thermomyces[42]Cyberlindnera,Kroppenstedtia,Virgibacillus[41],Streptomyces[38],Thermoascus,Aspergillus,Penicillium[42],Thermomyces[39]Aspergillus,Saccharomycopsis,Virgibacillus,Bacillus[16],Pseudomonas,Lactobacillus[37],Zygosaccharomyces,Monascus[42],Thermomyces[39]Candida,Thermoascus,Aspergillus,Byssochlamys,Pseudogracilibacillus,Acinetobacter[41],Kroppenstedtia,Virgibacillus[43],Pediococcus[16],Staphylococcus,Brevibacterium[39],Lactobacillus[44],Methanoculleus[45],Acetobacter[40]Microbacterium,Thermomyces,Thermoascus[37],Pichia,Candida,Torulaspora[37],Acinetobacter[38],Virgibacillus,Bacillus,Staphylococcus[16],Saccharopolyspora,Weissella[39],Kroppenstedtia,Bacteroides,Thermoleophilum,Pseudomonas[44],Methanobrevibacter[48],Methanofollis,Proteiniphium[48],Aminobacterium[45]Kazachstania[38],Bacillus,Streptomces[39]Virgibacillus[43],Lactobacillus,Candida,Acetobacter[39]Candida,Thermoascus,Pseudogracilibacillus,Byssochlamys,Bacillus[41],Kazachstania[38],Lactobacillus[16],Saccharomyces[42],Geotrichum,Millerozyma[39],Asticcacaulis,Caulobacter,Caproiciproducer,Methanoculleus,Dipodascus[48]
部分微生物间的相互作用关系如图2所示,其中一些微生物相互作用的机理已经通过实验得到了一定程度验证,经实验验证的互作机制主要包括:生物量调控(促进/抑制生长)、代谢产物调控(激活/抑制合成)等典型作用模式。
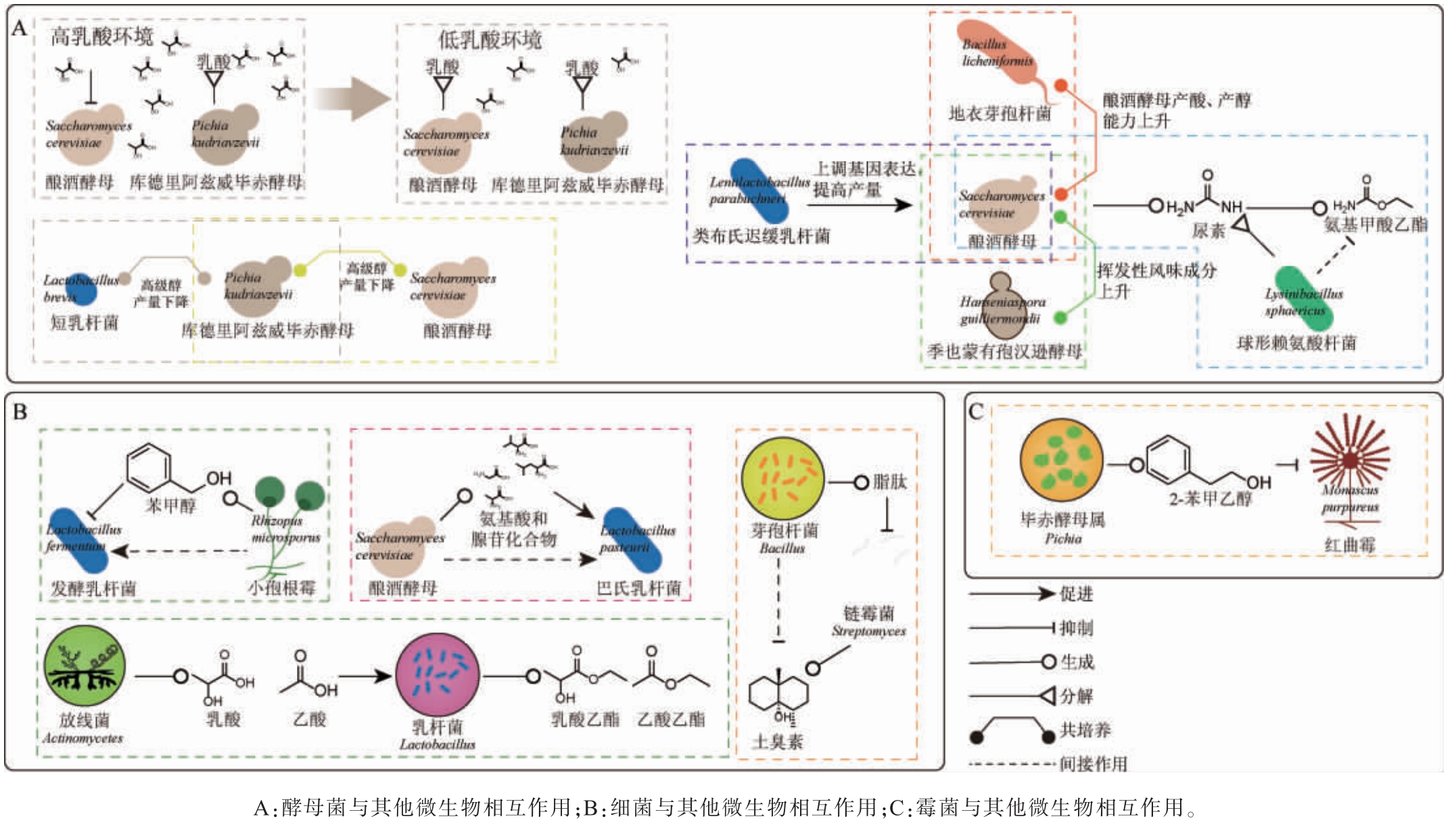
图2 部分微生物相互作用示意图
Fig. 2 Schematic diagram of some microbial interactions
3.1 酵母菌与其他微生物相互作用
酵母菌与其他微生物互作机制如图2A所示,酵母可以通过代谢产酸和产乙醇抑制其他微生物如芽孢杆菌的生长[50],但适量的乙醇可以为己酸菌生长代谢提供碳源促进其生长[51]。 在高乳酸环境中,酿酒酵母的生长受到库德里亚毕赤酵母的促进作用,这是因为酿酒酵母在乳酸较高的发酵环境受抑制,而库德里亚毕赤酵母具有较强的乳酸适应能力[52]。当两种菌共培养时,库德里亚毕赤酵母可以通过丙酮酸代谢途径分解高浓度的乳酸,当乳酸降低到一定程度时,酿酒酵母恢复分解乳酸的能力并将其作为碳源[53]。同样,粟酒裂殖酵母(Schizosaccharomyces pombe)也可以通过消耗乙酸来增强其他酵母菌的生长繁殖[54]。除此之外,酵母属与其他微生物的相互作用影响其代谢产物的生成。JIANG J等[55]研究发现,当酿酒酵母与库德里亚毕赤酵母共培养时,培养液中高级醇的产量下降。酿酒酵母与异常威克汉姆酵母(Wickerhamomyces anomalus)共培养时,其乙酸乙酯,β-苯乙醇,乙酸苯乙酯,甲基丁酸,己酸,乙烯愈创木酚等代谢产物的含量发生变化[56-58]。XU A等[59]研究发现,酿酒酵母与季也蒙有孢汉逊酵母(Hanseniaspora guilliermondii)共培养时,其挥发性风味成分更为丰富。MENG X等[60]研究发现,在酿酒酵母与地衣芽孢杆菌共培养时,酿酒酵母产醇、产酸能力显著提升,特别是丙酮酸、柠檬酸、琥珀酸、乳酸、苹果酸和酒石酸的产量均高于纯培养。另外一项研究中表明,通过在白酒发酵中共培养酿酒酵母和布氏迟缓乳杆菌(Lentilactobacillus buchneri),提高了3-(甲硫基)-1-丙醇和二甲基二硫醚的产量[7]。这是因为在布氏乳杆菌存在的情况下,酿酒酵母会上调生成3-(甲硫基)-1-丙醇和二甲基二硫醚的基因表达[7]。白酒生产中酿酒酵母会产生尿素,并进一步生成氨基甲酸乙酯(ethyl carbamate,EC),EC是一种致癌性化合物,而球形赖氨酸杆菌(Lysinibacillus sphaericus)通过分解尿素,可减少EC的生成[61]。
3.2 细菌与其他微生物相互作用
白酒生产相关的细菌受其它微生物代谢物调节,这些细菌与其它微生物互作机制如图2B所示,小孢根霉(Rhizopusmicrosporus)产生的苯甲醇可促进发酵乳杆菌的生长[36]。 泛氏乳杆菌(Lactobacillus panis)的生长会受到酿酒酵母分泌的氨基酸和腺苷化合物来调节[62]。细菌间的相互作用也会影响代谢物的产生,如芽孢杆菌和葡萄球菌可以调节白酒醇厚甜味的2,3-丁二醇的产生[8]。 除此之外,乳杆菌与酵母菌的相互作用也可以调节发酵中代谢产物的产生,酯类,硫化物,杂环风味物质等[63]可促进杂环化合物的代谢,如2-乙酰吡咯、2,3,5-三甲基吡嗪和2-乙酰呋喃[64]。张华东[65]研究了3种乳杆菌对酿酒酵母产代谢产物抑制作用,发现地衣芽孢杆菌会降低高产酯酿酒酵母产乙酸异戊酯的产量,枯草、解淀粉芽孢杆菌会抑制其产乙酸酯代谢。席博[66]研究发现,植物乳植杆菌的生长和乳酸发酵会受到酿酒酵母抑制,这与其影响糖酵解途径、核糖体和氨基酰t-RNA生物合成相关的蛋白表达水平下降相关。
乳杆菌与放线菌共培养会提升乳酸乙酯和乙酸乙酯的产量,这是因为放线菌能够产生乙酸,乳酸供乳杆菌利用[67]。 芽孢杆菌可以通过产生脂肽抑制链霉菌,进而降低链霉菌产生的土臭素的浓度,从而降低白酒中的异味[68]。而且大曲中芽孢杆菌通过合成表面活性素来抑制链霉菌等菌属,以及作为信号分子诱导产酶芽孢杆菌生物膜形成[69]。
3.3 霉菌与其他微生物相互作用
霉菌通常通过产生酶类影响其他微生物,例如在混合培养体系中,米曲霉(Aspergillus oryzae)能够通过分泌多种水解酶(淀粉酶、蛋白酶和脂肪酶)来降解复杂的大分子[7]。费比恩塞伯林德纳氏酵母(Cyberlindnera fabianii)和葡萄牙棒孢酵母(Clavispora lusitaniae)利用米曲霉的产酶优势,在混菌培养中提高了挥发性风味物质、氨基酸等代谢物产量[70]。霉菌也受到其它微生物影响,如图2C所示,红曲霉受到枝芽孢菌属(Virgibacillus)产生的2-苯基乙醇等代谢物抑制,并可能对整个发酵群落产生积极的影响[42,59]。
4 总结
一直以来,白酒中优势微生物及其微生物互作关系是研究白酒的重点,该研究通过对不同香型白酒文献进行分析,发现在白酒制曲和发酵过程中酵母属(Saccharomyces)、毕赤酵母属(Pichia)、芽孢杆菌属(Bacillus)、乳酸杆菌属(Lactobacillus)及曲霉属(Aspergillus)为共有的优势微生物。这些微生物与其他微生物间互作关系主要受到营养相互作用(如交叉喂养)和细胞信号(如群体感应)机制影响,这些相互作用影响着优势微生物的生物量,也调控着代谢产物的合成。为更好的深入解析微生物之间复杂的互作关系,下一步研究可以围绕下面几方面进行。首先,对微生物相互作用的进一步挖掘,通过相关性或其他方法得到潜在互作关系后,应当结合共培养实验验证与组学等技术验证得到更多优势微生物互作关系;其次,应将更多的新的方法或将现有的方法进行组合,多角度描述优势微生物间的互作关系,将微生物群落模型、机器学习方法及其联用方法分析微生物互作在其他研究领域的成功经验应用于本领域;最后,研究需聚焦白酒发酵动态演变过程,通过高分辨率传感器与实时监测技术,对白酒发酵环境参数进行实时监测,结合组学检测发酵过程动态变化,从而对白酒发酵进行实时表征,捕捉微生物动态发酵过程中互作关系。
[1] SAKANDAR H A,HUSSAIN R,FARID KHAN Q,et al.Functional microbiota in Chinese traditional Baijiu and Mijiu Qu(starters):A review[J] .Food Res Int,2020,138:109830.
[2] TU W, CAO X, CHENG J, et al. Chinese Baijiu:The perfect works of microorganisms[J] .Front Microbiol,2022,13:919044.
[3] 李安军,孟雅静,汤有宏,等. 白酒酿造微生态的研究进展[J] . 酿酒,2024,51(4):5-13.
[4] 王一然,程寒,孙敏,等.白酒酿造过程中微生物多样性的研究进展[J] .中国酿造,2024,43(1):1-6.
[5] HONG J,TIAN W,ZHAO D.Research progress of trace components in sesame-aroma type of Baijiu[J] .Food Res Int,2020,137:109695.
[6] WU J,CHEN R,LI X,et al.Comprehensive identification of key compounds in different quality grades of soy sauce-aroma type Baijiu by HS-SPME-GCMS coupled with electronic nose[J] .Front Nutr,2023,10:1132527.
[7] GAO L,ZHOU J,HE G.Effect of microbial interaction on flavor quality in Chinese Baijiu fermentation[J] .Front Nutr,2022,9:960712.
[8] SHEN S, LIU J, LUO R, et al. Analysis of the influence of microbial community structure on flavor composition of Jiang-flavor liquor in different batches of pre-pit fermented grains[J] .Fermentation,2022,8(12):671.
[9] HU X,DU H,REN C,et al.Illuminating anaerobic microbial community and cooccurrence patterns across a quality gradient in Chinese liquor fermentation pit muds[J] .Appl Environ Microbiol,2016,82(8):2506-2515.
[10] 刘兰兰.酱香型白酒糟醅核心微生物菌群的解析及分离筛选研究[D] .贵阳:贵州大学,2023.
[11] IVEY M, MASSEL M, PHISTER T G. Microbial interactions in food fermentations[J] .Ann Rev Food Sci Technol,2013,4:141-162.
[12] 慕婷婷,荣良燕,吴建军,等.发酵食品群落生态系统微生物相互作用的研究进展:聚焦交叉喂养[J] . 食品与发酵工业,2023,49(18):332-339.
[13] AVBELJ M, ZUPAN J, RASPOR P. Quorum-sensing in yeast and its potential in wine making[J] .Appl Microbiol Biotechn,2016,100(18):7841-7852.
[14] BAIREY E,KELSIC E D,KISHONY R.High-order species interactions shape ecosystem diversity[J] .Nature Commun,2016,7(1):12285.
[15] ZHU C,CHENG Y,ZUO Q,et al.Exploring the impacts of traditional crafts on microbial community succession in Jiang-flavored Daqu[J] .Food Res Int,2022,158:111568.
[16] ZHANG H,WANG L,TAN Y,et al.Effect of Pichia on shaping the fermentation microbial community of sauce-flavor Baijiu[J] . Int J Food Microbiol,2021,336:108898.
[17] HAO F, TAN Y, LV X, et al. Microbial community succession and its environment driving factors during initial fermentation of Maotai-flavor Baijiu[J] .Front Microbiol,2021,12:669201.
[18] FRIEDMAN J,ALM E J. Inferring correlation networks from genomic survey data[J] .PLOS Computat Biol,2012,8(9):e1002687.
[19] MATCHADO M S,LAUBER M,REITMEIER S,et al.Network analysis methods for studying microbial communities:A mini review[J] .Comput Struct Biotechn J,2021,19:2687-2698.
[20] FANG H, HUANG C, ZHAO H, et al. CCLasso:Correlation inference for compositional data through lasso[J] .Bioinformatics,2015,31(19):3172-3180.
[21] SUN H, CHAI L J, FANG G Y, et al. Metabolite-based mutualistic interaction between two novel Clostridial species from pit mud enhances butyrate and caproate production[J] . Appl Environ Microbiol, 2022,88(13):e00484-22.
[22] ANG K S,LAKSHMANAN M,LEE N R,et al.Metabolic modeling of microbial community interactions for health,environmental and biotechnological applications[J] .Curr Genom,2018,19(8):712-722.
[23] VAN DEN BERG N I, MACHADO D, SANTOS S, et al. Ecological modelling approaches for predicting emergent properties in microbial communities[J] .Nat Ecol Evolut,2022,6(7):855-865.
[24] GARCÍA-JIMÉNEZ B,TORRES-BACETE J,NOGALES J. Metabolic modelling approaches for describing and engineering microbial communities[J] .Comput Struct Biotechnol J,2021,19:226-246.
[25] COLARUSSO A V,GOODCHILD-MICHELMAN I, RAYLE M, et al.Computational modeling of metabolism in microbial communities on a genome-scale[J] .Curr Opin Syst Biol,2021,26:46-57.
[26] O'BRIEN E J,MONK J M,PALSSON B O.Using genome-scale models to predict biological capabilities[J] .Cell,2015,161(5):971-987.
[27] WANG H,MARCIŠAUSKAS S,SÁNCHEZ B J,et al.RAVEN 2.0:A versatile toolbox for metabolic network reconstruction and a case study on Streptomyces coelicolor[J] .PLoS Comput Biol,2018,14(10):e1006541.
[28] ARKIN A P,COTTINGHAM R W,HENRY C S,et al.KBase:The United States department of energy systems biology knowledgebase[J] .Nat Biotechnol,2018,36(7):566-569.
[29] SEAVER S M D,LIU F,ZHANG Q,et al.The ModelSEED Biochemistry Database for the integration of metabolic annotations and the reconstruction, comparison and analysis of metabolic models for plants,fungi and microbes[J] .Nucleic Acids Res,2021,49(D1):D575-D588.
[30] MACHADO D, ANDREJEV S, TRAMONTANO M, et al. Fast automated reconstruction of genome-scale metabolic models for microbial species and communities[J] .Nucleic Acids Res,2018,46(15):7542-7553.
[31] BASKARAN D K K, UMALE S, ZHOU Z, et al. Metagenome-based metabolic modelling predicts unique microbial interactions in deep-sea hydrothermal plume microbiomes[J] .ISME Commun,2023,3:42.
[32] KUMAR R K,SINGH N K,BALAKRISHNAN S,et al.Metabolic modeling of the International Space Station microbiome reveals key microbial interactions[J] .Microbiome,2022,10(1):102.
[33] LEE J Y, SADLER N C, EGBERT R G, et al. Deep learning predicts microbial interactions from self-organized spatiotemporal patterns[J] .Comput Struct Biotechnol J,2020,18:1259-1269.
[34] NESTOR E,TOLEDANO G,FRIEDMAN J.Interactions between culturable bacteria are predicted by individual species'growth[J] . mSystems,8(2):e00836-22.
[35] DIMUCCI D, KON M, SEGRÈ D. Machine learning reveals missing edges and putative interaction mechanisms in microbial ecosystem networks[J] .mSystems,2018,3(5):e00181-18.
[36] HAO H,YAN R,MIAO Z,et al.Volatile organic compounds mediated endogenous microbial interactions in Chinese Baijiu fermentation[J] .Int J Food Microbiol,2022,383:109955.
[37] TAN Y,ZHONG H,ZHAO D,et al.Succession rate of microbial community causes flavor difference in strong-aroma Baijiu making process[J] .Int J Food Microbiol,2019,311:108350.
[38] GUAN T,LIN Y,CHEN K,et al.Physicochemical factors affecting microbiota dynamics during traditional solid-state fermentation of Chinese strong-flavor Baijiu[J] .Front Microbiol,2020,11:2090.
[39] HU Y,HUANG X,YANG B,et al.Contrasting the microbial community and metabolic profile of three types of light-flavor Daqu[J] .Food Biosci,2021,44:101395.
[40] YANG L,XIAN C,LI P,et al.The spatio-temporal diversity and succession of microbial community and its environment driving factors during stacking fermentation of Maotai-flavor Baijiu[J] .Food Res Int,2023,169:112892.
[41] WANG C,BIN Z,WANG L,et al.Metagenomic and metabolomic profiling analyses to unravel the formation mechanism of n-propanol during the first and second round of Jiangxiangxing Baijiu fermentation[J] .Food Res Int,2025,200:115459.
[42] ZHANG H,DU H,XU Y.Volatile organic compound-mediated antifungal activity of Pichia spp.and its effect on the metabolic profiles of fermentation communities[J] .Appl Environ Microbiol,2021,87(9):e02992-20.
[43] NIU J,LI W,DU B,et al.Temporal heterogeneity of microbial communities and flavor metabolism during storage of high-temperature Daqu[J] .Food Chem,2025,464:141577.
[44] XUE Y,TANG F,CAI W,et al.Bacterial diversity,organic acid,and flavor analysis of Dacha and Ercha fermented grains of Fen flavor Baijiu[J] .Front Microbiol,2022,12:769290.
[45] HOU Q, WANG Y, NI H, et al. Deep sequencing reveals changes in prokaryotic taxonomy and functional diversity of pit muds in different distilleries of China[J] .Ann Microbiol,2022,72(1):12.
[46] ZHU M,ZHENG J,XIE J,et al.Effects of environmental factors on the microbial community changes during medium-high temperature Daqu manufacturing[J] .Food Res Int,2022,153:110955.
[47] LUO A,YANG N,YANG J,et al.Effects of microbial interspecies relationships and physicochemical parameters on volatile flavors in sorghumbased fermented grains during the fermentation of Shanxi light-flavored liquor[J] .Food Sci Nutr,2023,11(3):1452-1462.
[48] MU Y, HUANG J, ZHOU R, et al. Exploring the response patterns of strong-flavor Baijiu brewing microecosystem to fortified Daqu under different pit ages[J] . Food Res Int,2022,155:111062.
[49] LI W, ZHANG H, WANG R, et al. Temporal profile of the microbial community and volatile compounds in the third-round fermentation of sauce-flavor Baijiu in the Beijing region[J] .Foods,2024,13(5):670.
[50] 杨宁. 产酱香芽孢杆菌与酵母菌在堆积发酵过程中相互作用的研究[D] .长沙:中南林业科技大学,2023.
[51] 殷想想,王欣蕊,冯文聪,等. 己酸菌的筛选及其在浓香型白酒生产中应用的研究进展[J] .中国酿造,2023,42(9):14-18.
[52] JI H,XU K,DONG X,et al.Transcriptional profiling reveals molecular basis and the role of arginine in response to low-pH stress in Pichia kudriavzevii[J] .J Biosci Bioeng,2020,130(6):588-595.
[53] DENG N, DU H, XU Y. Cooperative response of Pichia kudriavzevii and Saccharomyces cerevisiae to lactic acid stress in Baijiu fermentation[J] .J Agr Food Chem,2020,68(17):4903-4911.
[54] CHEN E S.Application of the fission yeast Schizosaccharomyces pombe in human nutrition[J] .FEMS Yeast Res,2023,23:foac064.
[55] JIANG J,LIU Y,LI H,et al.Modeling and regulation of higher alcohol production through the combined effects of the C/N ratio and microbial interaction[J] .J Agr Food Chem,2019,67(38):10694-10701.
[56] FAN G,TENG C,XU D,et al.Enhanced production of ethyl acetate using co-culture of Wickerhamomyces anomalus and Saccharomyces cerevisiae[J] .J Biosci Bioeng,2019,128(5):564-570.
[57] MENG W,DING F,WANG R M,et al.Enhanced production of tetramethylpyrazine in Bacillus licheniformis BL1 through aldC over-expression and acetaldehyde supplementation[J] .Sci Rep,2020,10(1):3544.
[58] ZHA M,SUN B,WU Y,et al.Improving flavor metabolism of Saccharomyces cerevisiae by mixed culture with Wickerhamomyces anomalus for Chinese Baijiu making[J] .J Biosci Bioeng,2018,126(2):189-195.
[59] XU A, XIAO Y, HE Z, et al. Use of Non-Saccharomyces yeast co-fermentation with Saccharomyces cerevisiae to improve the polyphenol and volatile aroma compound contents in Nanfeng tangerine wines[J] . J Fungi,2022,8(2):128.
[60] MENG X,WU Q,WANG L,et al.Improving flavor metabolism of Saccharomyces cerevisiae by mixed culture with Bacillus licheniformis for Chinese Maotai-flavor liquor making[J] . J Ind Microbiol Biotechnol,2015,42(12):1601-1608.
[61] CUI K,WU Q,XU Y.Biodegradation of ethyl carbamate and urea with Lysinibacillus sphaericus MT33 in Chinese liquor fermentation[J] .J Agr Food Chem,2018,66(6):1583-1590.
[62] DUAN Z,WU Y,ZHANG C,et al.Comparison of fungal communities and flavor substances in surface and inner layers of fermented grains during stacking fermentation of sauce-flavor Baijiu[J] .J Biosci Bioeng,2023,136(4):295-303.
[63] PANG Z,HAO J,LI W,et al.Investigation into spatial profile of microbial community dynamics and flavor metabolites during the bioaugmented solid-state fermentation of Baijiu[J] .Food Biosci,2023,56:103292.
[64] TAN Y,DU H,ZHANG H,et al.Geographically associated fungus-bacterium interactions contribute to the formation of geography-dependent flavor during high-complexity spontaneous fermentation[J] . Microbiol Spectrum,2022,10(5):e01844-22.
[65] 张华东. 白酒发酵过程中主要微生物对酿酒酵母酯醇代谢的影响[D] .天津:天津科技大学,2020.
[66] 席博.混合发酵体系中酿酒酵母和植物乳植杆菌相互作用机制的研究[D] .太原:山西大学,2024.
[67] CHEN C,YANG H,LIU J,et al.Systematic review of Actinomycetes in the Baijiu fermentation microbiome[J] .Foods,2022,11(22):3551.
[68] 赵亮亮,盛伟喜,时晓,等. 浓香型白酒酿造生境中微生物群落多样性及群落间相互作用[J] .中国酿造,2023,42(11):15-21.
[69] 郅岩. 芽孢杆菌高效合成表面活性素的代谢机制及功能研究[D] . 无锡:江南大学,2017.
[70] 汪继伟,阎春悦,马春蕾,等.两种非酿酒酵母与米曲霉互作特性研究[J] .食品工业科技,2023,44(4):171-180.