大豆异黄酮是一类与人体雌激素17-β-雌二醇结构高度相似的天然植物雌激素[1],可缓解乳腺癌、前列腺癌、心血管疾病、骨质疏松症、肥胖以及糖尿病等多种慢性疾病[2]。大豆中的异黄酮含量一般为1~3 mg/g[3],约90%的大豆异黄酮以结合型糖苷的形式存在,其中包括以葡萄糖苷形式存在的染料木苷(genistin)、大豆苷(daidzin)和黄豆苷(glycitin),其余少数以游离形式存在[4]。由于大豆异黄酮的生物学效应主要由游离形式的苷元决定[5],所以糖苷需要转化为其相应的苷元才能提高生物利用度,使其吸收速度更快,吸收量更大[2,6],即转化为染料木素、大豆苷元和黄豆黄素。目前,转化大豆苷的方法主要包括酸水解、碱水解和酶水解等。酸水解技术简单且成本低,易导致产物不稳定,且强酸会腐蚀设备[7]。酶水解反应条件温和,特异性作用于β-葡萄糖苷键,不会产生毒性副产物,较为环保[8]。β-葡萄糖苷酶(E.C.3.2.1.21)是一种水解糖苷键以从糖苷和低聚糖中释放非还原末端葡萄糖基残基的酶[9],在再生能源、制药和食品行业有广泛应用[9-11]。 在碳水化合物活性酶数据库(carbohydrate-active enzymes database,CAZy)中,β-葡萄糖苷酶分布在糖苷水解酶(glycoside hydrolases,GH)家族1、2、3、5、9、16、30、39和116中[12]。 其中GH1家族为研究最多的β-葡萄糖苷酶家族,其催化结构域通常具有(β/α)8桶形结构[13]。
关于β-葡萄糖苷酶转化大豆异黄酮糖苷制备苷元的研究已有报道,来源于嗜热拟青霉(Paecilomyces thermophila)的β-葡萄糖苷酶在50 ℃条件下非常稳定,能够在4 h内水解超过93%的大豆异黄酮糖苷(如大豆苷、染料木苷和黄豆苷)[14];来源于球托霉属(Gongronella sp.)的β-葡萄糖苷酶BglW5在60 ℃条件下半衰期为20 h,能够高效水解大豆苷和染料木苷,水解率分别为96.2%和96.7%[15];来源于土曲霉(Aspergillus terreus)的β-葡萄糖苷酶的最适反应pH和温度分别为5.0和65 ℃,能够高效水解大豆异黄酮糖苷[16];来源于蓝状菌(Talaromyces leycettanus)的β-葡萄糖苷酶Bgl3B在37 ℃条件下处理大豆粉提取物10 min时,0.05 U的Bgl3B水解了95.1%的大豆苷[17]。然而,常温酶处理过程中容易造成微生物污染且酶的成本较高[8]。高活性的嗜热β-葡萄糖苷酶是解决这一问题的关键,高温条件可降低微生物污染的风险[18]、加速底物扩散和提高酶促反应速率[19]。来源于费希新萨托菌(Neosartorya fischeri)P1的β-葡萄糖苷酶NfBGL1的最适反应温度为80 ℃,该酶具有很高的比活性和热稳定性,能高效转化大豆异黄酮糖苷(如染料木苷、大豆苷和黄豆苷)为游离型异黄酮[20]。
本研究通过生物信息学技术从云南省玉溪市元江哈尼族彝族傣族自治县94℃热泉泥水样中提取微生物宏基因组,挖掘β-葡萄糖苷酶基因,将其转化到大肠杆菌(Escherichia coli)BL21(DE3)中进行异源表达,得到重组酶。 对重组酶进行纯化并表征其酶学性质,并考察其在转化大豆苷制备大豆苷元的应用效果,以期为制备富含大豆苷元的豆制品提供新的嗜热β-葡萄糖苷酶选择。
1 材料与方法
1.1 材料与试剂
94 ℃热泉泥水样:云南省玉溪市元江哈尼族彝族傣族自治县。
1.1.2 试剂
硫酸卡那青霉素、异丙基-β-D-硫代半乳糖苷(isopropylβ-D-thiogalacto-pyranoside,IPTG)(均为分析纯)、大肠杆菌(Escherichia coli)BL21(DE3)、质粒小提试剂盒、十二烷基硫酸钠聚丙烯酰胺凝胶电泳(sodium dodecyl sulfate-polyacrylamide gel electrophoresis,SDS-PAGE)制备试剂盒:上海生工生物技术有限公司;对硝基苯基β-D-吡喃葡萄糖苷(p-nitrophenyl-β-D-glucopyranoside,p-NPGlu)、对硝基苯基β-D-吡喃半乳糖苷(p-nitrophenyl-β-D-galactopyranoside,p-NPGal)、对硝基苯基β-D-吡喃木糖苷(p-nitrophenyl-β-Dxylopyranoside,p-NPXyl)、对硝基苯α-D-吡喃葡萄糖苷(pnitrophenyl-α-D-glucopyranoside,p-NPαGlu)(纯度均为99%):上海源叶生物科技有限公司;无水葡萄糖、对硝基苯酚(pnitrophenol,p-NP)、β-巯基乙醇、吐温20(均为分析纯):上海麦克林生化有限公司;其他试剂均为分析纯。
1.1.3 培养基
LB液体培养基、LB固体培养基:上海生工生物技术有限公司。
1.2 仪器与设备
MultiskanTM FC型酶标仪:赛默飞世尔(上海)仪器有限公司;ZWY-2112B恒温培养振荡器:上海智城分析仪器制造有限公司;JY96-IIN超声破碎仪:宁波新芝生物科技股份有限公司;DYY-12型电泳仪:北京六一仪器厂;Agilent 1100 serise高效液相色谱(high performance liquid chromatography,HPLC)仪:美国Agilent公司。
1.3 方法
1.3.1 β-葡萄糖苷酶的基因挖掘和序列分析
采用Illumina测序平台对源自云南省玉溪市元江哈尼族彝族傣族自治县94 ℃热泉泥水样中微生物宏基因组(登录号:NO.SRP448733)进行测序,利用MetaGeneMark v3.38软件对热泉微生物宏基因组数据进行组装和基因预测,并合所有基因并去冗余后,利用直系同源蛋白分组比对(evolutionary genealogy of genes:Non-supervised Orthologous Groups,eggNOG)数据库进行功能注释,基于此挖掘β-葡萄糖苷酶基因。 将筛选出的β-葡萄糖苷酶基因命名为BglYJ446,将其编码的蛋白质(重组酶)命名为BglYJ446。将BglYJ446的氨基酸序列提交至美国国家生物技术信息中心(National Center of Biotechnology Information,NCBI)的非冗余蛋白质序列数据库(non-redundant protein database,NR)中,获得NCBI登录号,同时采用基本局部比对搜索工具(Basic Local Alignment Search Tool,BLAST)进行序列比对,并用MEGA 11.0软件中的邻接法(neighbor-joining,NJ)构建系统发育树。通过AlphaFold2预测BglYJ446的3D结构,进一步在NCBI蛋白质数据库(protein data bank,PDB)中下载与BglYJ446氨基酸序列同源性最高的5个GH1家族的β-葡萄糖苷酶的氨基酸序列,采用MEGA11软件进行多重序列比对,将BglYJ446的3D结构及序列比对结果提交至ESPript 3.0,输出带有二级结构的多序列比对结果。
1.3.2 β-葡萄糖苷酶的异源表达
以大肠杆菌作为宿主,对获得的β-葡萄糖苷酶BglYJ446的氨基酸序列进行密码子优化,并在其N端加上组氨酸(histidine,His)标签,由生工生物工程(上海)股份有限公司进行全基因合成。 将合成的基因BglYJ446与pET-28(a)载体连接,最终获得重组质粒pET-28(a)-BglYJ446。将重组质粒pET-28(a)-BglYJ446转化至大肠杆菌BL21(DE3)中,加入500μLLB液体培养基,37℃、180r/min条件下培养45min,将100 μL培养液涂布于含有硫酸卡那霉素(终质量浓度50 μg/mL)的LB固体培养基平板上,在37 ℃条件下正置培养30 min后倒置培养12~16 h,挑取单菌落委托生工生物工程(上海)股份有限公司进行测序验证。将转化成功的重组菌株E. coli BL21(DE3)pET-28(a)-BglYJ446的单菌落接种于含有硫酸卡那霉素(终质量浓度50 μg/mL)的LB液体培养基中,37 ℃、180 r/min条件下培养至OD600 nm值达到0.4~0.6之后,加入终浓度为0.5 mmol/L的IPTG,在16 ℃、220 r/min条件下培养20 h。
1.3.3 β-葡萄糖苷酶的纯化
将诱导后的发酵液8 000×g离心5 min,收集菌体,并用纯净水清洗3次,每5 g湿质量菌体加入20 mL非变性裂解液(20 mmol/L Tris-HCl,500 mmol/L NaCl,pH 8.0)重新悬浮。在冰浴条件下超声处理(功率40 W,时间2 s,间隔8 s)30 min。4 ℃,8 000×g离心15 min,收集上清液,即得到β-葡萄糖苷酶BglYJ446的粗酶液。通过His-Tag标签蛋白纯化试剂盒对目的蛋白进行纯化,并采用十二烷基硫酸钠-聚丙烯酰胺凝胶电泳(SDS-PAGE)对BglYJ446粗酶液、空载大肠杆菌BL21(DE3)发酵液、重组菌株加诱导剂不破碎上清液、重组菌株不加诱导剂破碎上清液、重组菌株不加诱导剂不破碎上清液以及BglYJ446纯酶液进行检测。
1.3.4 β-葡萄糖苷酶活力的测定
采用对硝基苯酚法测定β-葡萄糖苷酶BglYJ446的活力[21]。 单位酶活力定义为:在酶的最适反应条件下每分钟生成1 μmol p-NP为1个酶活力单位(U)。
1.3.5 β-葡萄糖苷酶的酶学性质研究
最适反应温度及温度稳定性:在pH值为7.5及不同反应温度(30℃、40℃、50℃、60℃、70℃、75℃、80℃、85℃和90 ℃)下测定β-葡萄糖苷酶BglYJ446的活力,以确定其最适反应温度。 将最高酶活力作为100%,计算其相对酶活。 将β-葡萄糖苷酶BglYJ446粗酶液分别在70 ℃、80 ℃和85 ℃条件下进行孵育,并在孵育1 h、2 h、4 h、6 h、8 h、12 h、24 h、36 h和72 h后测定酶活力,以未处理的酶液的酶活力作为100%,计算相对酶活力,分析β-葡萄糖苷酶BglYJ446的热稳定性。
最适反应pH及pH稳定性:配制不同pH的缓冲液,包括柠檬酸-磷酸氢二钠缓冲液(100 mmol/L,pH 3.0~7.0)和甘氨酸-NaOH缓冲液(100 mmol/L,pH 7.5~9.0),在最适反应温度及不同pH值(3.0、4.0、5.0、6.0、6.5、7.0、7.5、8.0、8.5、9.0)条件下测定β-葡萄糖苷酶BglYJ446的活力,以确定其最适反应pH。以最高酶活力作为100%,计算相对酶活。将β-葡萄糖苷酶BglYJ446粗酶液分别置于不同pH的缓冲液中,4 ℃条件下放置24 h后,在最适温度及pH条件下测定酶活力,以未处理的酶液的酶活力作为100%,计算相对酶活,分析β-葡萄糖苷酶BglYJ446的pH稳定性。
金属离子与化学试剂对β-葡萄糖苷酶BglYJ446活力的影响:在最适反应条件下,考察终浓度为0.1mmol/L、1mmol/L和10 mmol/L的CoCl2、NiCl2、NaCl等金属离子以及终质量分数为0.1%、1.0%、10.0%的β-巯基乙醇、SDS、吐温20、尿素对β-葡萄糖苷酶BglYJ446活力的影响。以相同反应条件下不添加金属离子或化学试剂的酶活力作为100%,计算相对酶活。
有机溶剂对β-葡萄糖苷酶BglYJ446活力的影响:在最适反应条件下,考察终体积分数分别为5%、10%、20%、30%和50%的甲醇、乙醇和异丙醇对β-葡萄糖苷酶BglYJ446活力的影响,以相同反应条件下不添加有机溶剂的酶活力作为100%,计算相对酶活。
葡萄糖对β-葡萄糖苷酶BglYJ446活力的影响:在最适反应条件下,考察终浓度为100 mmol/L、200 mmol/L、500 mmol/L、1 000 mmol/L和2 000 mmol/L的葡萄糖对β-葡萄糖苷酶BglYJ446活力的影响。以相同反应条件下不添加葡萄糖的酶活力作为100%,计算相对酶活。
底物特异性:分别以人工底物(p-NPGlu、p-NPGal、p-NPXyl和p-NPαGlu)以及天然底物(大豆苷、染料木苷、水杨苷、熊果苷和羧甲基纤维素钠)为底物,参照方法1.3.4测定酶活力,以最高酶活力作为100%,计算相对酶活,考察β-葡萄糖苷酶BglYJ446的底物特异性。
酶促反应动力学:以不同浓度(0.25mmol/L、0.50mmol/L、1.00 mmol/L、2.00 mmol/L、3.00 mmol/L、4.00 mmol/L、5.00 mmol/L、6.00 mmol/L)的pNPGlu为底物,参照方法1.3.4测定酶活力,以p-NPGlu浓度为横坐标,以反应速率为纵坐标,采用Origin v9.9.0.225软件拟合得到米氏方程,得到米氏常数(Km)和最大反应速率(Vmax)。
1.3.6 β-葡萄糖苷酶水解大豆苷的活性测定
采用pH为7.5的甘氨酸-NaOH缓冲液配制质量浓度为1 mg/mL的大豆苷,取200 μL大豆苷溶液加入125 μL酶液(0.15 U),在80 ℃条件下进行水解不同时间(10 min、20 min、30 min、40 min、50 min、60 min),并采用HPLC测定大豆苷及大豆苷元的含量[22],计算大豆苷的转化率,其计算公式:大豆苷转化率=(酶解前大豆苷质量浓度-酶解后大豆苷质量浓度)/酶解前大豆苷质量浓度×100%。
1.3.7 β-葡萄糖苷酶与大豆苷的分子对接
通过Autodock vina1.2.5将β-葡萄糖苷酶BglYJ446与配体大豆苷进行分子对接,探究β-葡萄糖苷酶BglYJ446水解大豆苷的催化机制。并用LigPlot+2.2.8成像,对接结果通过PyMOL 2.6.0a0.展示。
1.3.8 数据处理
每个试验重复3次,采用Microsoft Excel 2023处理数据,结果用“平均值和标准偏差”表示,并用Origin v9.9.0.225软件绘制图表。
2 结果与分析
2.1 β-葡萄糖苷酶的基因挖掘与序列分析
从云南省元江县热泉宏基因组中挖掘到了β-葡萄糖苷酶基因BglYJ446(NCBI登录号:WOR08337),将其编码的蛋白质命名为BglYJ446,其由455个氨基酸组成。以BglYJ446的氨基酸序列为模板,在NCBI的NR数据库进行检索,并构建系统发育树,结果见图1。由图1可知,BglYJ446的氨基酸序列与来源于热曲菌纲(Thermoflexia)的GH1家族的β-葡萄糖苷酶(RME39878.1)聚于一支,序列同源性最高为93.88%,说明本研究从云南省元江县94 ℃热泉泥水样中提取微生物宏基因组中挖掘的β-葡萄糖苷酶基因BglYJ446,其编码的重组酶BglYJ446为GH1家族的β-葡萄糖苷酶。
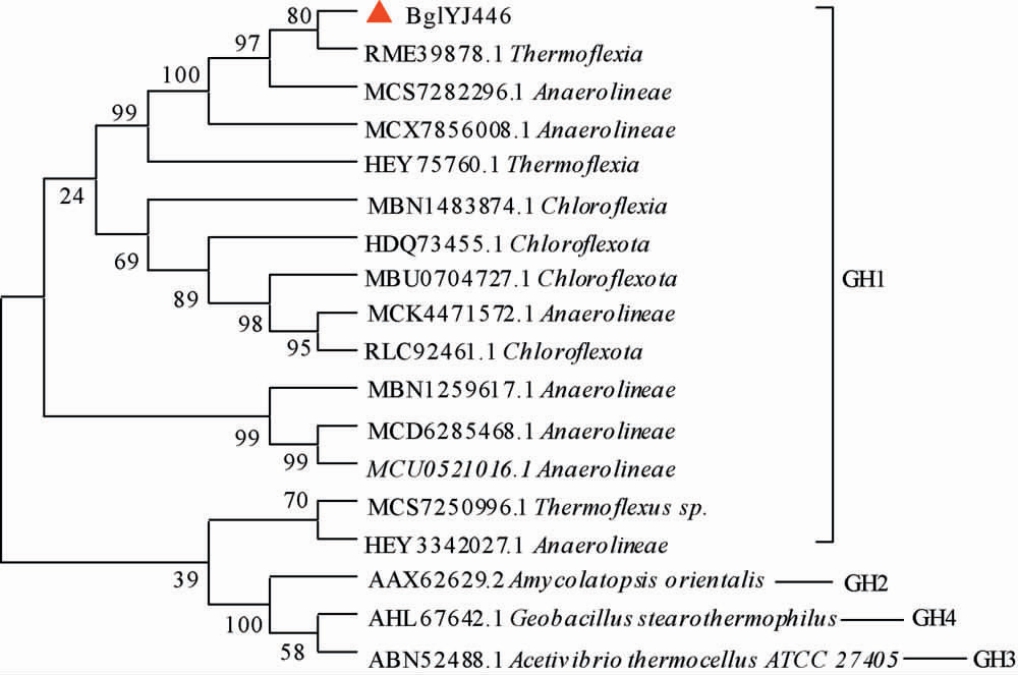
图1 基于氨基酸序列β-葡萄糖苷酶BglYJ446的系统发育树
Fig. 1 Phylogenetic tree of β-glucosidase BglYJ446 based on amino acid sequence
5个GH1家族的β-葡萄糖苷酶与BglYJ446的氨基酸序列比对结果见图2。
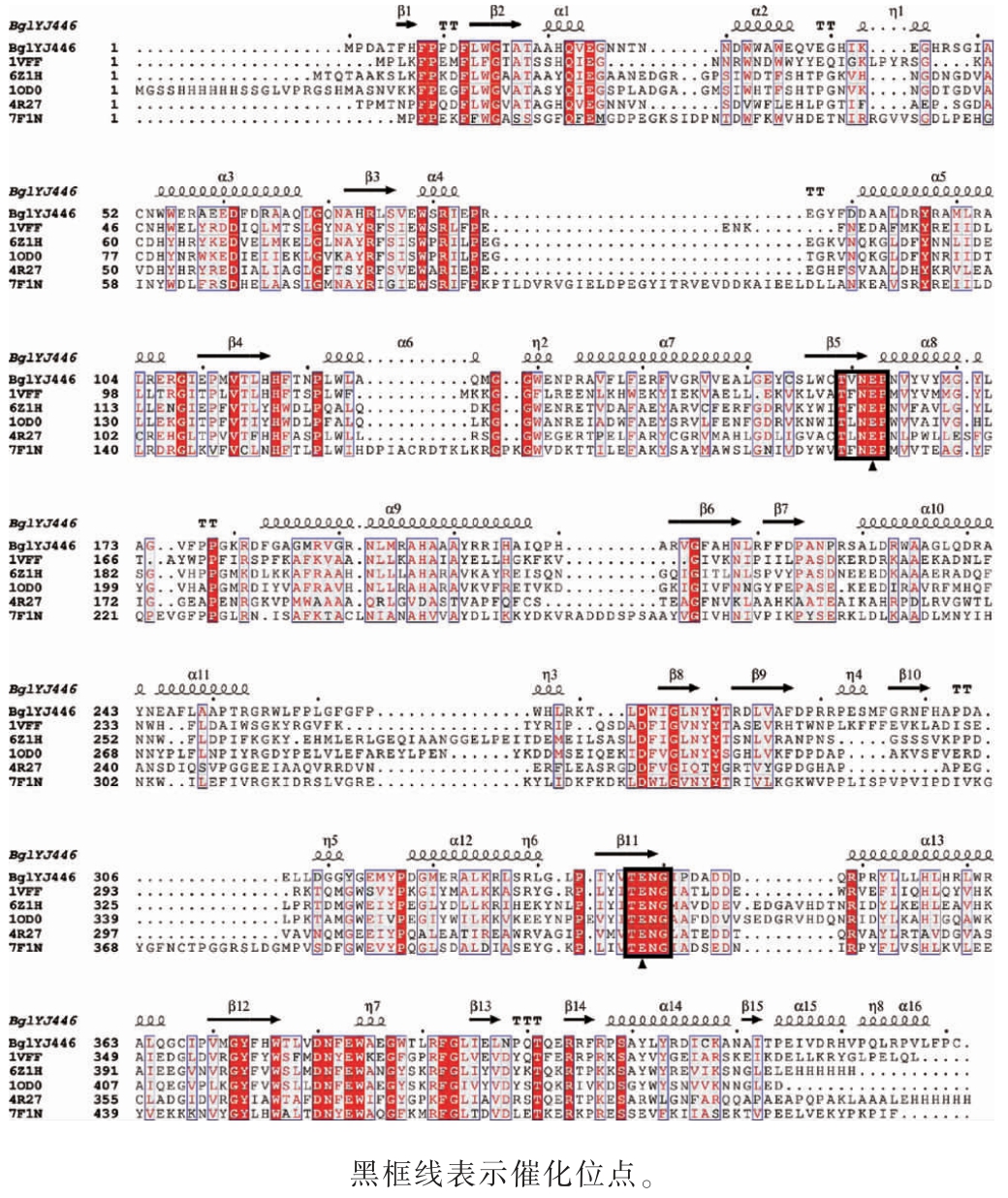
图2 β-葡萄糖苷酶BglYJ446与5个GH1家族的β-葡萄糖苷酶氨基酸序列比对结果
Fig. 2 Amino acid sequence alignment results of β-glucosidase BglYJ446 and 5 β-glucosidases from GH1 family
由图2可知,BglYJ446与来源于掘越氏火球菌(Pyrococcus horikoshii)的β-葡萄糖苷酶(PDB登录号:1VFF)[23]的氨基酸序列同源性最高为40.60%,与合成构建的β-葡萄糖苷酶(PDB登录号:6Z1H)[24]的序列同源性为37.53%,与来源于微杆菌属(Microbacterium sp.)的β-葡萄糖苷酶(PDB登录号:4R27)[25]的序列同源性为36.66%,与来源于海栖热袍菌(Thermotoga maritima)的β-葡萄糖苷酶(PDB登录号:1OD0)[26]的序列同源性为32.44%,与来源于热丝菌属(Thermofilum sp.)的β-葡萄糖苷酶(PDB登录号:7F1N)[27]的序列同源性为31.88%。BglYJ446与所对比的序列都具有GH1家族特有的高度保守催化位点基序,为161-NEP-163和337-TENG-340。
2.2 β-葡萄糖苷酶BglYJ446的表达及纯化
经酶活测定,发酵液中β-葡萄糖苷酶BglYJ446的酶活为1.22 U/mL,进一步对其纯化,结果见图3。
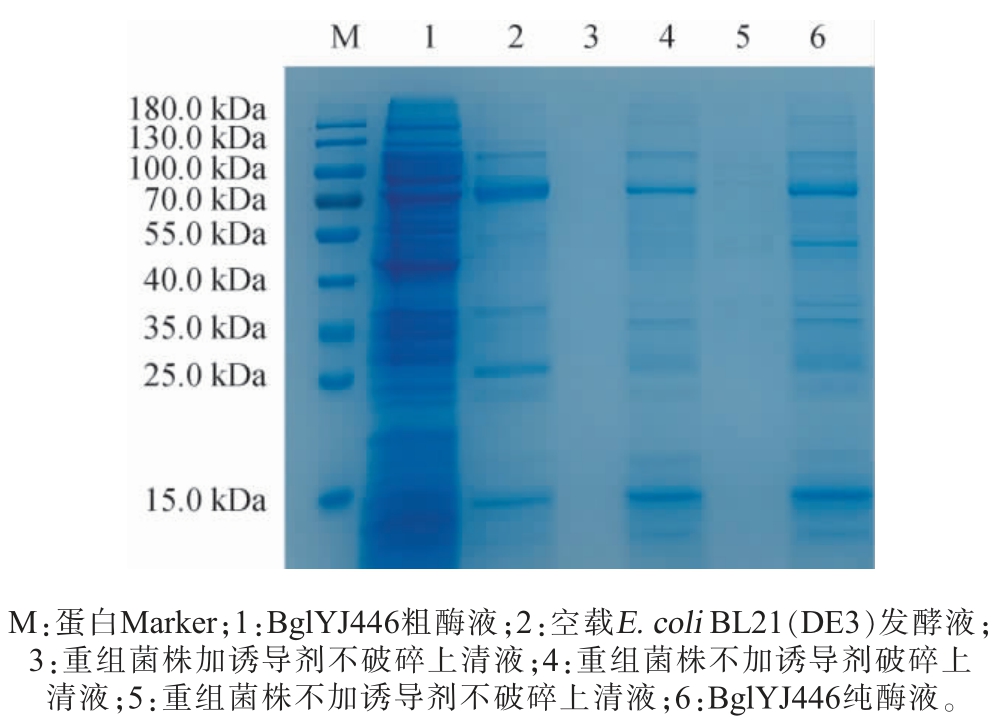
图3 β-葡萄糖苷酶BglYJ446的十二烷基硫酸钠-聚丙烯酰胺凝胶电泳结果
Fig. 3 Sodium dodecyl sulfate-polyacrylamide gel electrophoresis results of β-glucosidase BglYJ446
β-葡萄糖苷酶BglYJ446的理论分子质量为52.11 kDa,由图3可知,在BglYJ446粗酶液中含有目的条带,空载E.coli BL21(DE3)发酵液中无目的条带,说明β-葡萄糖苷酶BglYJ446由重组质粒诱导表达得到;重组菌株中加诱导剂不破碎的上清液中无目的条带,表明表达的目的蛋白是胞内酶;经过His标签纯化后,虽然未能得到单一条带但在分子质量40~55 kDa间观察到清晰条带,该条带与β-葡萄糖苷酶BglYJ446的理论分子质量52.11 kDa相符,即确定为BglYJ446蛋白表达的条带。
2.3 β-葡萄糖苷酶BglYJ446酶学性质研究
2.3.1 温度和pH对β-葡萄糖苷酶BglYJ446活力的影响
温度和pH对β-葡萄糖苷酶BglYJ446活力的影响见图4。由图4a可知,随着反应温度的升高,β-葡萄糖苷酶BglYJ446的酶活力呈先升高后下降的趋势,当反应温度为85 ℃时,β-葡萄糖苷酶BglYJ446活力最高,说明该酶的最适反应温度为85 ℃。由图4b可知,β-葡萄糖苷酶BglYJ446在70 ℃处理72 h后,相对酶活为49.40%;80 ℃处理了8 h后相对酶活为57.77%,在85 ℃处理2 h后,相对酶活仅为18.75%。目前,用于水解大豆异黄酮糖苷的β-葡萄糖苷酶中仅有两个酶的最适温度和热稳定性高于BglYJ446,分别是来源于酸叶菌属(Acidilobus sp.)的β-葡萄糖苷酶BglAc,该酶最佳反应条件为100 ℃,在90 ℃下孵育6 h还有50%的剩余酶活[28];以及来源于激烈火球菌(Pyrococcus furiosus)的β-葡萄糖苷酶,95 ℃下孵育59 h还有50%的剩余酶活[29]。相比大多数用于大豆异黄酮糖苷水解的β-葡萄糖苷酶,β-葡萄糖苷酶BglYJ446表现出较高的最适反应温度和较好的热稳定性。综上,BglYJ446为嗜热β-葡萄糖苷酶。
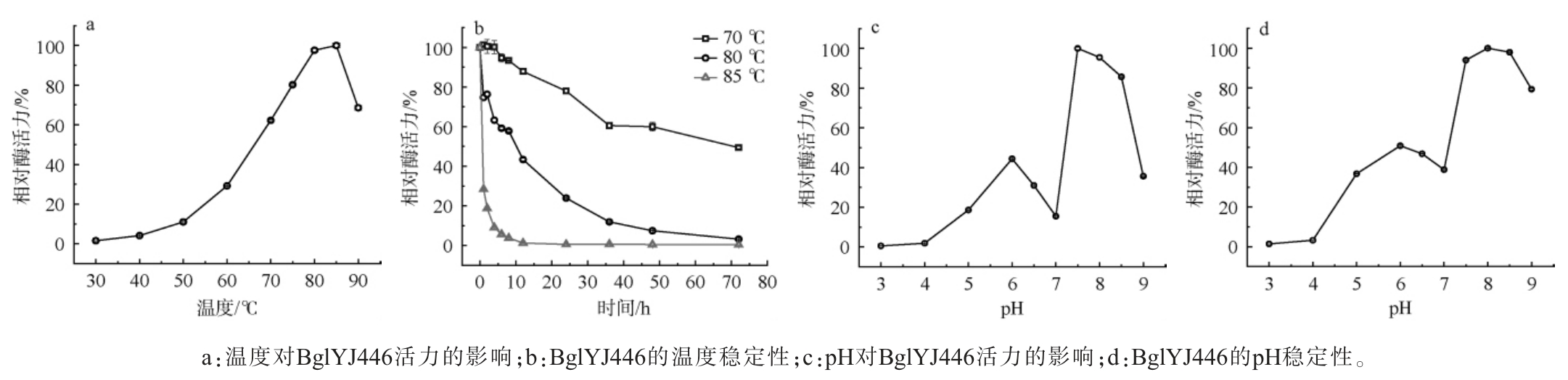
图4 温度和pH对β-葡萄糖苷酶BglYJ446相对酶活的影响
Fig. 4 Effects of temperature and pH on the relative enzyme activities of β-glucosidase BglYJ446
由图4c可知,当pH为3.0~4.0时,几乎未检测到酶活,pH值为7.5时,该酶有最高酶活力,在pH 7.5~8.5的范围内,相对酶活>80%,说明该酶的最适反应pH为7.5。由图4d可知,在不同pH条件下4 ℃处理24 h,当pH值为7.5~8.5时,相对酶活>90%,当pH值为9.0时,相对酶活为79.3%,说明该酶在pH值为7.5~9.0的范围内稳定性较好。
2.3.2 金属离子、化学试剂及有机溶剂对嗜热β-葡萄糖苷酶BglYJ446活力的影响
金属离子、化学试剂及有机溶剂对嗜热β-葡萄糖苷酶BglYJ446活力的影响分别见表1和表2。由表1可知,0.1mmol/L的金属离子对嗜热β-葡萄糖苷酶BglYJ446活力基本无影响,1 mmol/L的K+、Na+、Mn2+、Mg2+、Ni2+和Co2+对嗜热β-葡萄糖苷酶BglYJ446活力基本无影响。 除了不同浓度的K+、Na+对嗜热β-葡萄糖苷酶BglYJ446的酶活力没有明显影响外,其余金属离子在10 mmol/L的终浓度下,对嗜热β-葡萄糖苷酶BglYJ446呈现不同程度的抑制作用,但Mg2+、Co2+和Mn2+还保留了50%及以上的酶活性,Ni2+、Fe2+、Cu2+、Al3+的相对酶活均<50%。 与报道的金属离子对来源于糖单孢菌属(Saccharomonospora sp.)NB11的GH1家族的β-葡萄糖苷酶BglNB11[30]的作用趋势相似,高浓度Co2+、Cu2+抑制酶活力,但10 mmol/L的K+和Na+对BglNB11呈现出不同程度的抑制作用,而对嗜热β-葡萄糖苷酶BglYJ446无明显抑制作用。此外,嗜热β-葡萄糖苷酶BglYJ446与来源于烟曲霉(Aspergillus fumigatus)的β-葡萄糖苷酶nBgl3[31]相似,它们在1 mmol/L的Mg2+作用下表现为促进作用,1 mmol/L的Cu2+作用下表现为抑制作用。
表1 金属离子和有机物对嗜热β-葡萄糖苷酶BglYJ446相对酶活的影响
Table 1 Effects of metal ions and organic compounds on the relative enzyme activities of thermophilic β-glucosidase BglYJ446%

注:“ND”表示未检出。下同。
金属离子有机物添加量/(mmol·L-1)0.11100.1 K+Na+Mn2+Mg2+Ni+Co2+Fe2+Cu2+Al3+105.2±0.77 100.5±0.74 106.8±0.60 110.4±0.06 100.7±0.66 100.5±0.62 94.9±0.75 96.4±0.29 103.0±0.29 103.0±0.05 106.2±0.50 93.4±0.50 108.3±0.47 676.4±0.24 115.0±0.60 49.2±0.32 3.4±0.07 5.0±0.06 103.5±0.26 104.1±0.16 50.4±0.33 88.3±0.24 4.1±0.01 67.9±0.21 10.0±0.96 0.1±0.02 1.5±0.12 SDS尿素吐温20 β-巯基乙醇ND 103.2±0.50 69.4±0.21 110.6±0.41添加量/%1 ND 102.0±0.34 50.4±0.45 168.8±0.52 10 ND 87.0±0.48 2.4±0.05 10.0±0.07
表2 有机溶剂对嗜热β-葡萄糖苷酶BglYJ446相对酶活的影响
Table 2 Effect of organic solvents on the relative enzyme activities of thermophilic β-glucosidase BglYJ446%
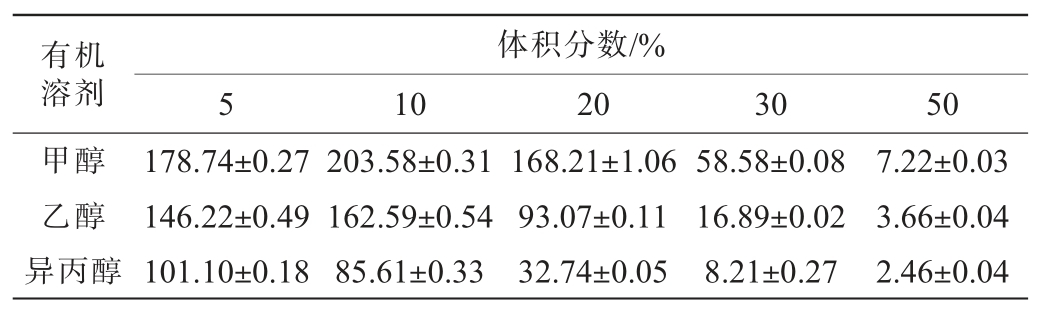
有机溶剂甲醇乙醇异丙醇体积分数/%5 10203050 178.74±0.27 146.22±0.49 101.10±0.18 203.58±0.31 162.59±0.54 85.61±0.33 168.21±1.06 93.07±0.11 32.74±0.05 58.58±0.08 16.89±0.02 8.21±0.27 7.22±0.03 3.66±0.04 2.46±0.04
不同质量分数的SDS均完全抑制嗜热β-葡萄糖苷酶BglYJ446的活力;尿素对嗜热β-葡萄糖苷酶BglYJ446活力影响较小;0.1%的吐温20对嗜热β-葡萄糖苷酶BglYJ446活力有一定抑制作用,10%的吐温20的抑制作用更明显;1%的β-巯基乙醇对嗜热β-葡萄糖苷酶BglYJ446活力有明显促进作用,但10%的β-巯基乙醇对该酶有明显抑制作用。
综上,K+、Na+对嗜热β-葡萄糖苷酶BglYJ446活力影响较小,但高浓度的其他金属离子抑制其酶活力;低浓度的β-巯基乙醇能提高嗜热β-葡萄糖苷酶BglYJ446活力,但高浓度的β-巯基乙醇及SDS、吐温20抑制其酶活力,说明该酶具有适应严苛工业环境应用的潜能。
由表2可知,体积分数为5%和10%的甲醇和乙醇以及体积分数为20%的甲醇均对嗜热β-葡萄糖苷酶BglYJ446活力产生促进作用,但随着甲醇和乙醇体积分数的增加,该酶出现不同程度的抑制作用,说明低体积分数的甲醇和乙醇对该酶呈现激活作用。体积分数为5%的异丙醇对β-葡萄糖苷酶BglYJ446酶活力无明显影响,随着异丙醇体积分数的增加,该酶出现不同程度的抑制作用,说明高体积分数的异丙醇对该酶有抑制作用。来自极端热泉(98 ℃)宏基因组中的GH1家族的β-葡萄糖苷酶BglM[32],在20%的乙醇体积分数下仅保留40%的活性,而BglYJ446在20%的乙醇体积分数下可保持93.07%的酶活力。 综上,嗜热β-葡萄糖苷酶BglYJ446对有机溶剂有较好的耐受性,能够在低体积分数的有机溶剂环境中进行反应。
2.3.3 葡萄糖含量对嗜热β-葡萄糖苷酶BglYJ446活力的影响
葡萄糖含量对嗜热β-葡萄糖苷酶BglYJ446活力的影响见图5。
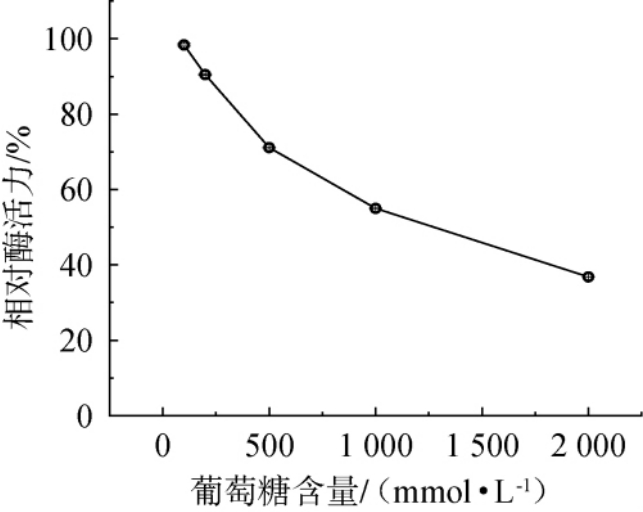
图5 葡萄糖含量对嗜热β-葡萄糖苷酶BglYJ446相对酶活的影响
Fig. 5 Effect of glucose content on the relative enzyme activities of thermophilic β-glucosidase BglYJ446
由图5可知,随着葡萄糖含量的升高,嗜热β-葡萄糖苷酶BglYJ446的活力逐渐降低,显示出葡萄糖抑制作用。 但当葡萄糖含量为1 000 mmol/L时,还保持有55.01%的酶活力,当葡萄糖含量为2 000 mmol/L时,还保持有36.83%的酶活力,说明嗜热β-葡萄糖苷酶BglYJ446可以催化高浓度的底物进行反应。 已报道的来源于戊糖嗜热厌氧杆菌(Thermoanaerobacteriumaotearoense)的β-葡萄糖苷酶P8G3#4在1 500 mmol/L葡萄糖浓度下剩余酶活<40%[33]。大多数β-葡萄糖苷酶有产物抑制现象,会造成催化效率降低,葡萄糖耐受β-葡萄糖苷酶在工业应用中更具优势[34]。
2.3.4 嗜热β-葡萄糖苷酶BglYJ446的底物特异性和酶促反应动力学研究
嗜热β-葡萄糖苷酶BglYJ446的底物特异性及酶促反应动力学研究结果分别见表3和图6。
表3 嗜热β-葡萄糖苷酶BglYJ446的底物特异性分析结果
Table 3 Substrate specificity analysis results of thermophilic β-glucosidase BglYJ446

人工底物相对酶活/%天然底物相对酶活/%p-NPGlu p-NPGal p-NPXyl p-NPαGlu p-NPαGal 100.0±2.28 34.57±0.28 ND ND ND大豆苷染料木苷水杨苷熊果苷羧甲基纤维素钠100.0±0.21 10.46±0.04 6.15±0.12 8.75±0.15 ND
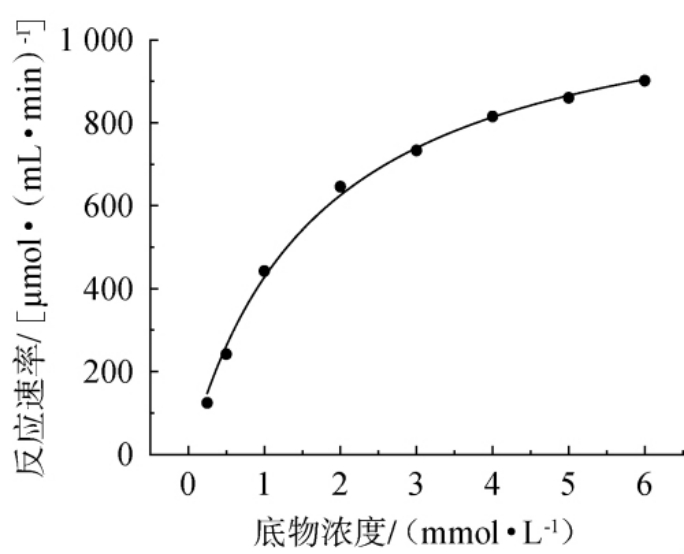
图6 以p-NPGlu为底物嗜热β-葡萄糖苷酶BglYJ446的酶促反应动力学曲线
Fig. 6 Enzymatic reaction kinetics curve of thermophilic β-glucosidase BglYJ446 with p-NPGlu as substrate
由表3可知,嗜热β-葡萄糖苷酶BglYJ446可以和人工底物p-NPGlu、p-NPGal以及天然底物大豆苷、染料木苷等进行反应,其中嗜热β-葡萄糖苷酶BglYJ446对p-NPGlu及大豆苷表现出最高活性。
由图6可知,以p-NPGlu为底物,根据米氏方程得到嗜热β-葡萄糖苷酶BglYJ446的Km值为1.72 mmol/L,Vmax为1 164.56 μmol/(mL·min),表明嗜热β-葡萄糖苷酶BglYJ446与底物p-NPGlu的亲和力较高。
2.4 嗜热β-葡萄糖苷酶BglYJ446水解大豆苷的研究
利用嗜热β-葡萄糖苷酶BglYJ446对大豆苷进行水解,大豆苷的转化率见图7。由图7可知,在80 ℃条件下,随着反应时间的延长,大豆苷的转化率逐渐上升,60 min时大豆苷的转化率达到98.87%,说明嗜热β-葡萄糖苷酶BglYJ446对大豆苷具有较高的水解效率。来源于Acidilobussp.的β-葡萄糖苷酶BglAc,在90 ℃加入27.54 U β-葡萄糖苷酶BglAc水解15 min后,大豆异黄酮糖苷完全转化为游离苷元大豆苷元,水解率接近100%[28]。来源于P.furiosus的β-葡萄糖苷酶,在95 ℃添加1.65 U/mL酶,将1.0 mmol/L大豆苷在140 min内完全水解为大豆苷元[29]。
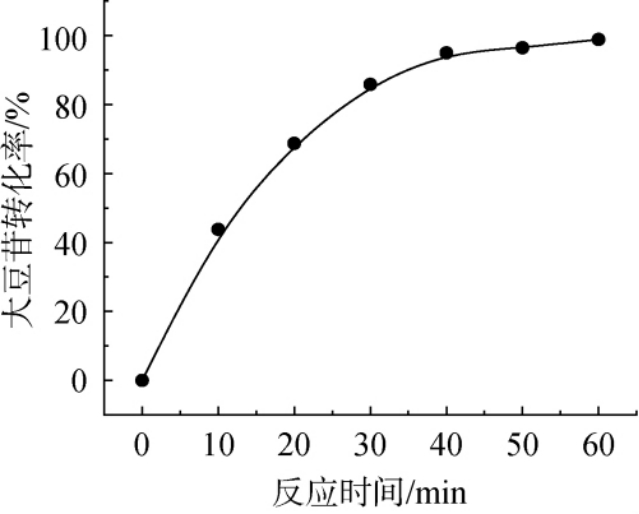
图7 嗜热β-葡萄糖苷酶BglYJ446对大豆苷的转化率
Fig. 7 Conversion rate of daidzin by thermophilic β-glucosidase BglYJ446
在大豆异黄酮的工业生产中,大豆异黄酮的溶解度低、β-葡萄糖苷酶稳定性差、产物抑制、酶解效率有限等科学问题降低了大豆异黄酮苷元的转化效率[35]。嗜热β-葡萄糖苷酶BglYJ446具有较好的热稳定性、葡萄糖耐受性及较高的水解效率,可作为生产大豆异黄酮和富含大豆异黄酮的豆制品的候选酶。
2.5 嗜热β-葡萄糖苷酶BglYJ446与大豆苷的分子对接
通过Autodock vina1.2.5对嗜热β-葡萄糖苷酶BglYJ446和大豆苷进行分子对接,结果见图8。 由图8可知,底物结合位点位于该酶中央的β折叠形成的桶状结构中。嗜热β-葡萄糖苷酶BglYJ446具有两个保守基序NEP和TENG,包含参与催化的谷氨酸(glutamic acid,Glu)162和Glu338残基,它们相对位于活性位点的底部。 对接还包含了组氨酸(histidine,His)117、酪氨酸(tyrosine,Tyr)280、Tyr312和Glu383残基,这些残基通过氢键与配体相互作用,在酶底物水解中起到重要作用。GH1家族的催化机制是使用两种氨基酸残基,一种作为酸/碱催化,另一种作为亲核试剂,与底物形成共价中间体[36]。 来源于Jeotgalibacillus malaysiensis的β-葡萄糖苷酶BglD5中Glu162残基为酸碱催化剂,Glu348残基为亲核试剂[37],它和BglYJ446都存在双谷氨酸作为催化位点,表明BglYJ446与GH1家族β-葡萄糖苷酶的催化机制是相似的,都是两个谷氨酸参与的酸碱催化。
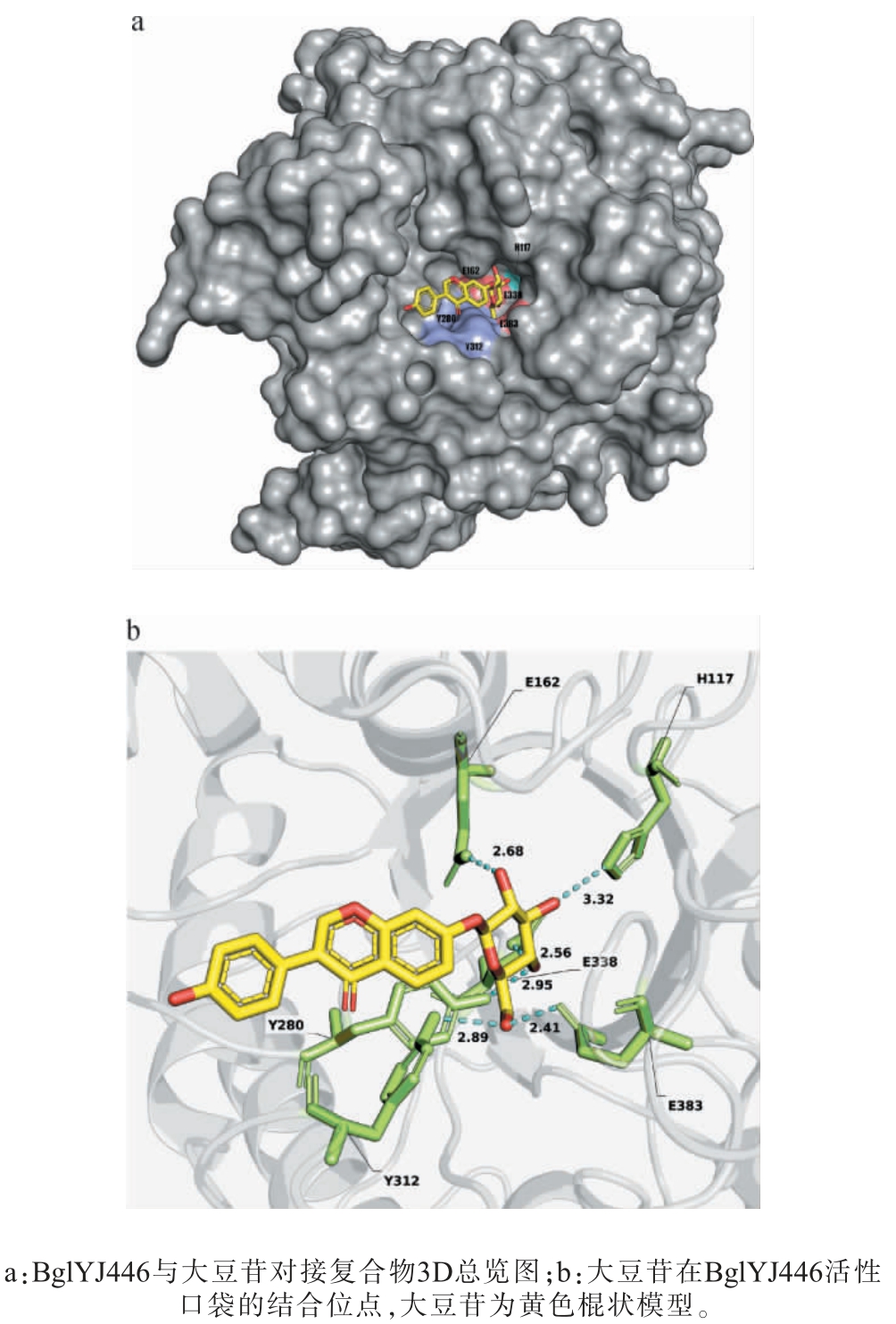
图8 嗜热β-葡萄糖苷酶BglYJ446与大豆苷的分子对接结果
Fig. 8 Molecular docking results of thermophilic β-glucosidase BglYJ446 and daidzin
3 结论
本研究从云南省玉溪市元江哈尼族彝族傣族自治县94 ℃热泉泥水样中提取微生物宏基因组中挖掘到了一个新型GH1家族的嗜热β-葡萄糖苷酶BglYJ446,其最适反应温度为85 ℃,最适反应pH为7.5;在80 ℃处理8 h,相对酶活为57.77%,表现出较好的热稳定性;且在pH 7.5~9.0的范围内稳定性较好(相对酶活>70%)。K+、Na+对BglYJ446活性影响较小,高浓度(10 mol/L)的Ni+、Cu2+等其他金属离子、十二烷基硫酸钠(SDS)、吐温20及10%β-巯基乙醇抑制其酶活;BglYJ446BglYJ446在体积分数均为20%的甲醇和乙醇、2 000 mmol/L葡萄糖条件下相对酶活分别为168.21%、93.07%、36.83%。 BglYJ446对人工底物p-NPGlu及天然底物大豆苷酶解活性最高,且以p-NPGlu为底物时,米氏常数(Km值)为1.72 mmol/L,最大反应速率(Vmax)为1 164.56 μmol/(mL·min)。 在80 ℃条件下,采用BglYJ446(0.15 U)可在反应时间60 min时转化98.87%大豆苷。 通过分子对接发现其通过Glu162和Glu338参与的酸碱催化机制进行催化。综上,BglYJ446具有较好的热稳定性、葡萄糖耐受性及较高的水解效率,可作为提高大豆苷元含量,制备富含大豆异黄酮游离苷元豆制品应用中有潜力的酶。未来研究可进一步通过酶工程定向改造提升其特定性能,并拓展其在其他糖苷类化合物生物转化中的应用。
[1] KURZER M S,XU X.Dietary phytoestrogens[J] .Annu Rev Nutr,1997,17:353-381.
[2] ZAHEER K,AKHTAR M H. An updated review of dietary isoflavones:Nutrition, processing, bioavailability and impacts on human health[J] .Crit Rev Food Sci,2017,57(6):1280-1293.
[3] SONG T T,HENDRICH S,MURPHY P A.Estrogenic activity of glycitein,a soy isoflavone[J] .J Agr Food Chem,1999,47(4):1607-1610.
[4] 李珊珊.大豆胚芽中异黄酮提取研究[D] .杭州:浙江大学,2004.
[5] 梁文欧,赵力超,方祥,等.大豆异黄酮与肠道微生物相互作用研究进展[J] .食品科学,2019,40(9):283-289.
[6] TORU I,SACHIKO O,AKIO O,et al.Soy isoflavone aglycones are absorbed faster and in higher amounts than their glucosides in humans[J] .J Nutr,2000,130(7):1695-1699.
[7] 李参参,张淦,常徽. 微生物发酵法转化大豆异黄酮研究进展[J] . 食品研究与开发,2023,44(12):218-224.
[8] 周文红,郭咪咪,李秀娟,等.大豆异黄酮提取及其生物转化的研究进展[J] .粮油食品科技,2019,27(5):37-42.
[9] CAIRNS J R K,ESEN A.β-glucosidases[J] .Cell Mol Life Sci,2010,67:3389-3405.
[10] SUPRIYADI S,NARESWARI A R,FITRIANI A,et al.Enhancement of black tea aroma by adding the β-glucosidase enzyme during fermentation on black tea processing[J] .Int J Food Sci,2021,2021:5542109.
[11] MAGWAZA B,AMOBONYE A,PILLAI S.Microbial β-glucosidases:Recent advances and applications[J] .Biochimie,2024,225:49-67.
[12] HENRISSAT B,DAVIES G.Structural and sequence-based classification of glycoside hydrolases[J] .Curr Opin Struct Biol,1997,7(5):637-644.
[13] DAVIES G,HENRISSAT B.Structures and mechanisms of glycosyl hydrolases[J] .Structure,1995,3(9):853-859.
[14] YANG S Q,WANG L J,YAN Q J,et al.Hydrolysis of soybean isoflavone glycosides by a thermostable β-glucosidase from Paecilomyces thermophila[J] .Food Chem,2009,115(4):1247-1252.
[15] FANG W, SONG R, ZHANG X B, et al. Characterization of a novel β-glucosidase from Gongronella sp W5 and its application in the hydrolysis of soybean isoflavone glycosides[J] .J Agr Food Chem,2014,62(48):11688-11695.
[16] YAN F Y,XIA W,ZHANG X X,et al.Characterization of β-glucosidase from Aspergillus terreus and its application in the hydrolysis of soybean isoflavones[J] .J Zhejiang Univ Sci B,2016,17:455-464.
[17] LI X X,XIA W,BAI Y G,et al.A novel thermostable GH3 β-glucosidase from Talaromyce leycettanus with broad substrate specificity and significant soybean isoflavone glycosides-hydrolyzing capability[J] . Biomed Res Int,2018,2018(1):4794690.
[18] HAKI G D, RAKSHIT S K. Developments in industrially important thermostable enzymes:a review[J] .Bioresource Technol,2003,89(1):17-34.
[19] LI D, LI X L, DANG W, et al. Characterization and application of an acidophilic and thermostable β-glucosidase from Thermofilum pendens[J] .J Biosci Bioeng,2013,115(5):490-496.
[20] YANG X Z,MA R,SHI P J,et al.Molecular characterization of a highlyactive thermophilic β-glucosidase from Neosartorya fischeri P1 and its application in the hydrolysis of soybean isoflavone glycosides[J] . PloS ONE,2014,9(9):1.
[21] MO H Y, CHEN X, TANG M W, et al. Expression of a thermostable glucose-stimulated β-glucosidase from a hot-spring metagenome and its promising application to produce gardenia blue[J] .Bioorg Chem,2024,143:107036.
[22] 张永忠,李木子,孙艳梅,等.“Amano”β-糖苷酶水解大豆异黄酮技术的研究[J] .食品科学,2008,29(5):254-258.
[23] AKIBA T,NISHIO M,MATSUI I,et al.X-ray structure of a membranebound β-glycosidase from the hyperthermophilic Archaeon Pyrococcus horikoshii[J] .Proteins,2004,57(2):422-431.
[24] GAMIZ-ARCO G, GUTIERREZ-RUS L I, RISSO V A, et al. Hemebinding enables allosteric modulation in an ancient TIM-barrel glycosidase[J] .Nat Commun,2021,12(1):380.
[25] PARK S J,CHOI J M,KYEONG H H,et al.Rational design of a β-glycosidase with high regiospecificity for triterpenoid tailoring[J] .Chem Bio Chem,2015,16(5):854-860.
[26] ZECHEL D L, BORASTON A B, GLOSTER T, et al. Iminosugar glycosidase inhibitors:Structural and thermodynamic dissection of the binding of isofagomine and 1-deoxynojirimycin to β-glucosidases[J] .J Am Chem Soc,2003,125(47):14313-14323.
[27] CHEN A K,WANG D,JI R,et al.Structural and catalytic characterization of TsBGL,a β-glucosidase from Thermofilum sp.ex4484_79[J] .Front Microbiol,2021,12:723678.
[28] HE J J,LI Y Y,SUN X H,et al.Characterization of a novel hyperthermophilic GH1 β-glucosidase from Acidilobus sp.and its application in the hydrolysis of soybean isoflavone glycosides[J] .Microorganisms,2024,12(3):533.
[29] YEOM S J,KIM B N,KIM Y S,et al.Hydrolysis of isoflavone glycosides by a thermostable β-glucosidase from Pyrococcus furiosus[J] .J Agr Food Chem,2012,60(6):1535-1541.
[30] ZADA N S,BELDUZA O,GULER H I,et al.Cloning,expression,biochemical characterization,and molecular docking studies of a novel glucose tolerant β-glucosidase from Saccharomonospora sp.NB11[J] .Enzyme Microb Technol,2021,148:109799.
[31] LIU D Y, ZHANG R F, YANG X M, et al. Characterization of a thermostable β-glucosidase from Aspergillus fumigatus Z5, and its functional expression in Pichia pastoris X33[J] .Microb Cell Fact,2012,11:25.
[32] KAUSHAL G,RAI A K,SINGH S P.A novel β-glucosidase from a hotspring metagenome shows elevated thermal stability and tolerance to glucose and ethanol[J] .Enzyme Microb Technol,2021,145:109764.
[33] YANG F,YANG X F,LI Z,et al.Overexpression and characterization of a glucose-tolerant β-glucosidase from T.aotearoense with high specific activity for cellobiose[J] . Appl Microbiol Biotechnol, 2015, 99(21):8903-8915.
[34] KROGH K B R M,HARRIS P V,OLSEN C L,et al.Characterization and kinetic analysis of a thermostable GH3 β-glucosidase from Penicillium brasilianum[J] .Appl Microbiol Biotechnol,2010,86(1):143-154.
[35] GODSE R, BAWANE H, TRIPATHI J, et al. Unconventional β-glucosidases:A promising biocatalyst for industrial biotechnology[J] .Appl Biochem Biotechnol,2021,193(9):2993-3016.
[36] CAIRNS J R K,KARUNAMBIGAI A,JEON J S,et al.Functions of rice beta-glucosidases and transglucosidases[J] .Scienceasia,2023,49(5):635-645.
[37] LIEW K J,LIM L,WOO H Y,et al.Purification and characterization of a novel GH1 beta-glucosidase from Jeotgalibacillus malaysiensis[J] .Int J Biol Macromol,2018,115:1094-1102.