单核细胞增生性李斯特菌,即单增李斯特菌(Listeria monocytogenes)是一种革兰氏阳性菌,在自然界中广泛存在,能够适应多种不利的环境条件,如不同的温度、pH值及较高盐浓度,表现出较强的生存能力和环境耐受性。 该菌细胞形态多为球状或短杆状,其表面分布的多种膜蛋白在感染宿主的过程中起到重要作用[1-2]。单增李斯特菌感染可引起多种临床疾病,包括发热、胃肠炎、局部组织肿胀、菌血症以及脑膜炎等症状[3]。由于该菌能够穿越血脑屏障和血胎屏障,其感染可能进一步导致中枢神经系统损伤、胎儿流产及新生儿感染等严重并发症[4-5],抗生素治疗对于免疫力低下人群的作用也微乎其微,这使其成为食品安全与公共卫生领域亟需关注的致病菌之一。
在食品加工与储藏过程中,生物或非生物表面都可能存在单增李斯特菌生物膜[6]。与浮游状态的细胞相比,生物膜内的细菌对消毒剂、抗生素及不良环境的抵抗力显著增强,因而更难被清除[7-8]。生物膜的形成是一个多阶段、动态演变的过程,通常经历初始黏附、微菌落聚集、生物膜结构成熟以及最终的分散或解体等环节。细菌具有一定的黏附性,在表面逐渐生长。随着生物膜的发育成熟,内部细胞的代谢活动逐渐改变,部分细菌会脱离生物膜重新进入游离状态,从而启动新的定植与感染循环[9]。此外,即使部分菌群处于休眠状态,抗生素耐受性依然存在,进一步增加了感染的可能[10]。因此,针对生物膜形成机制寻找有效的抑制策略,对于控制单增李斯特菌的传播与危害具有重要意义。
细菌素具有良好的抑菌活性,且通常具有高效性和低毒性等优点[11-15]。大量研究表明,来源于乳酸菌或肠球菌的细菌素(如IIa类、nisin/类nisin细菌素以及多组分细菌素)对单增李斯特菌具有明确的抑制活性,可弱化其生物膜形成与黏附能力[16-20]。乳酸菌素LLC518可通过破坏细胞膜结构显著抑制单增李斯特菌的生长[21];SARAOUI T等[22]研究发现,乳球菌CNCM I-4031能够有效抑制去皮及熟虾制品中单增李斯特菌的繁殖;WANG Y等[23]研究进一步指出,植物乳杆菌素LPL-1不仅可显著降低单增李斯特菌的活菌数量,还能下调与毒力及生物膜形成相关基因的表达水平。这些研究表明,细菌素在抑制单增李斯特菌及其生物膜形成方面具有潜在应用价值。GL肠球菌素是从奶酪中分离出来的一个由43个氨基酸组成的新型细菌素,其具有较窄的抑菌谱,主要靶向抑制单增李斯特菌生长,因此本研究以GL肠球菌素为对象开展实验。
为了探讨GL肠球菌素对单增李斯特菌生物膜形成的抑制作用及其机制,该研究通过测定单增李斯特菌的生长曲线,确定GL肠球菌素的亚致死浓度;随后采用平板计数法评价其对浮游菌的杀灭效果;再利用结晶紫法测定单增李斯特菌生物膜生成量;最后,从生物膜内活菌数、代谢活性、鞭毛相关基因及胞外多糖分泌等方面进行分析,系统评估GL肠球菌素对单增李斯特菌的抑菌作用及其机制,为细菌素在食品防腐及微生物控制中的应用提供理论依据,同时为单增李斯特菌的防治提供思路。
1 材料与方法
1.1 材料与试剂
1.1.1 材料和菌株
单增李斯特菌(Listeria monocytogenes)ATCC 19115:由本实验室保存;GL肠球菌素:合肥国肽生物科技有限公司。
1.1.2 化学试剂
磷酸缓冲盐溶液(phosphate buffer saline,PBS)、结晶紫:北京索莱宝科技有限公司;钌红(生化试剂):上海懋康生物科技有限公司;氯仿(分析纯):美国Sigma-Aldrich公司;异丙醇(分析纯)、Trizol试剂(生化试剂):上海生工股份有限公司;逆转录试剂盒、荧光定量试剂盒、细胞计数试剂盒(cell counting kit,CCK)-8:南京诺唯赞生物科技股份有限公司。
1.1.3 培养基
脑心浸液肉汤(brain heart infusion broth,BHI)培养基、BHI固体培养基:青岛海博生物技术有限公司。
1.2 仪器与设备
Synergy H1全波长酶标仪:美国伯腾仪器有限公司;FA6103C电子分析天平:上海天平仪器技术有限公司;Octet Red 96分子相互作用分析仪:美国Pall 公司;CJ-2D超净工作台、BSC-250隔水式恒温培养箱:上海三发科学仪器有限公司;THZ-D台式恒温振荡器:太仓市强乐实验设备有限公司;ND ONE 超微量分光光度计、7500实时荧光定量聚合酶链式反应(real time fluorescence quantative polymerase chain reaction,RT-fqPCR)仪:赛默飞世尔(中国)科技有限公司。
1.3 方法
1.3.1 亚抑菌浓度的选择
亚抑菌浓度指低于最小抑菌浓度(minimal inhibit concentration,MIC)而对细菌有选择作用的抗菌药物浓度,表明药物浓度低于MIC时细菌耐药性仍可增强。在实验室先前研究中确定了GL肠球菌素抑制单增李斯特菌的MIC为(2.5±0.2)μg/mL[24],以MIC测定单增李斯特菌的生长曲线和杀菌曲线。首先将活化的单增李斯特菌重新接种于新配制的BHI培养基中,并将菌液在波长600 nm处测定的吸光度值(OD600 nm值)调节至0.1[25],将GL肠球菌素分别加入菌悬液中,使其终浓度依次为0、1/32 MIC、1/16 MIC、1/8 MIC、1/4 MIC、1/2 MIC、1 MIC、2 MIC及4 MIC。培养过程中在不同时间点测定菌液的OD600 nm值。 将0、1 h、2 h和3 h时的0、2 MIC和4 MIC样品取样,按梯度稀释后均匀涂布于BHI固体培养基上,经过培养后进行菌落计数[26]。
1.3.2 单增李斯特菌生物膜相对形成量测定
单增李斯特菌生物膜相对形成量:采用结晶紫染色法测定。结晶紫为带正电荷的碱性染料,可与细菌细胞表面及胞外聚合物中带负电的成分发生静电作用并被生物膜结构吸附。经洗涤去除未结合染料后,残留于孔壁的结晶紫用冰乙酸溶解,其在波长595 nm处的吸光度值(OD595 nm值)与孔内生物膜的总量(细胞及胞外基质)呈正相关,因此可作为生物膜形成量的间接定量指标。将经一夜活化的单增李斯特菌重新接种于新鲜BHI培养基中,并将菌液的OD600 nm值调整至0.1。 然后将溶液中GL肠球菌素终浓度调节为0、1/32 MIC和1/16 MIC。 取200 μL菌液分配至无菌96孔板中,并在37 ℃恒温培养箱中培养24 h。 之后轻柔吸去上清液,并用pH 7.2、浓度为0.1 mol/L的磷酸盐缓冲液(PBS)清洗孔壁3次,以去除未黏附细胞。 洗涤完成后,在60 ℃条件下静置15 min。 之后每孔加入200 μL 10 g/L的结晶紫溶液染色30 min。 染色结束后,弃去染液并再次使用PBS清洗3次以去除多余染料,于60 ℃静置15 min。 接着,每孔加入200 μL 33 mL/L的冰乙酸以溶解染色的结晶紫,并在37 ℃孵育40 min,使生物膜充分溶解。以未添加GL肠球菌素的样品作为阳性对照组,以BHI培养基为空白对照组,在波长595 nm处测定吸光度值(OD595 nm值),实验设置3次平行。生物膜相对形成量计算公式如下:
1.3.3 生物膜内活菌数测定
生物膜内菌代谢活力的测定采用CCK-8试剂盒,将经活化的单增李斯特菌重新接种于新鲜BHI培养基中,并将菌液的OD600 nm值调整至0.1。 然后将溶液中GL肠球菌素终浓度调节为0、1/32 MIC和1/16 MIC。 取200 μL菌液分装至无菌96孔板中,于37 ℃恒温培养箱中分别培养6 h和24 h。培养结束后,小心移除上清液,用pH 7.2、0.1 mol/L的PBS轻柔清洗3次以去除未黏附细胞。 接着,在每个孔中加入100μLPBS及10μLCCK-8,充分混匀后在37℃孵育1h。随后使用酶标仪在波长450 nm处测定吸光度值(OD450nm值)。 实验设置3次平行、阳性对照和空白对照。
生物膜内活菌数的测定:将上述经过PBS洗涤的样品每孔加入200 μL PBS,将96孔板置于超声仪中超声处理5 min,使附着于底部的细胞从生物膜中释放。使用移液枪反复吹打以充分分散细菌,取100 μL菌液进行梯度稀释后均匀涂布于BHI琼脂平板上。在37 ℃恒温条件下培养约20 h后进行菌落计数[27]。
1.3.4 泳动分析
将单增李斯特菌接种于BHI液体培养基中,并在37 ℃条件下恒温培养过夜。随后,取含有0.3%琼脂的BHI培养基进行高压灭菌处理,待培养基冷却至约50 ℃时,分别加入GL肠球菌素,使其终浓度设定为0、1/32 MIC和1/16 MIC[28]。充分混匀后,将培养基倒入无菌平皿中,于室温下静置至完全凝固。在制备好的琼脂平板中央滴加1 μL单增李斯特菌菌悬液,确保液滴均匀分布。 之后,将平板置于37 ℃恒温培养约15 h,以便菌体在表面扩散形成可观察的菌落扩散圈。
1.3.5 实时荧光定量聚合酶链式反应
将经一夜培养的单增李斯特菌按1%的接种量至新鲜BHI培养基中,培养至OD600 nm值=0.4,分别加入GL肠球菌素,使其终浓度为0、1/32 MIC和1/16 MIC,在37 ℃恒温培养箱中培养4 h时,取5 mL菌液在4 ℃、5 000×g的条件下离心10 min,取沉淀在液氮条件下充分研磨,加入1 mL Trizol混匀,室温静置10 min后加入0.2 mL氯仿,振荡15 s后静置3 min,在4 ℃、12 000×g的条件下离心10 min。 取上层液体加入500 μL异丙醇充分混合,室温静置20 min,在4 ℃、12 000×g的条件下离心10 min。弃上清,用体积分数75%乙醇重悬沉淀,在4 ℃、12 000×g的条件下离心3 min,弃上清。 完全干燥后加入30 μL无菌无酶水,用超微量分光光度计测定浓度并使用HiScript R ⅢRT SuperMix for qPCR(+gDNA wiper)试剂盒进行逆转录获得互补脱氧核糖核酸(complementary deoxyribonucleic acid,cDNA)。
实时荧光定量聚合酶链式反应(RT-fqPCR)使用ChamQ SYBR qPCR Master Mix试剂盒,各基因的引物见表1。PCR扩增体系(20 μL):2×UltraSYBR混合物10 μL,正向引物0.4 μL,反向引物0.4 μL,cDNA 2 μL,无菌无酶水7.2 μL。PCR扩增程序为95 ℃预变性30 s,95 ℃、5 s,53 ℃、30 s,共40个循环,溶解曲线:95 ℃、5 s,60 ℃、1 min。
表1 本研究所用实时荧光定量聚合酶链式反应引物
Table 1 Primers of real time fluorescence quantative polymerase chain reaction in this study

基因引物序列(5'-3')motA motB flaA flgE fliG F:CAACGCTCGGTGTACTTGG R:CGCTAAGTTTGTCTGGGTTCG F:TTCTGTTTGCCTCCAGTTC R:CTCTTGTTCGTTTGCTTCTTTC F:CTGGTATGAGTCGCCTTAG R:CATTTGCGGTGTTTGGTTTG F:CAGCAGGTTCCCCGACTTC R:CGGCCTTGTAGTGCTGCAT F:AATCGCGACCGAAGTGGTT R:CTCGTGCAAGGCGTTGTTT
为了消除起始模板量和反转录效率差异的影响,选取16S rRNA作为内参基因,对目标基因的Ct值进行归一化处理。单增李斯特菌部分鞭毛相关相对表达量计算公式如下:

1.3.6 生物膜胞外多糖的测定
为测定GL肠球菌素对单增李斯特菌生物膜形成过程中胞外多糖生成量的影响,采用钌红染色法测定胞外多糖产量[29]。 将经一夜培养的单增李斯特菌重新接种至新鲜BHI培养基中,并调节菌液OD600nm值至0.1。随后,将GL肠球菌素分别加入菌悬液中,使其终浓度设定为0、1/32 MIC和1/16 MIC。 取4 mL菌液分装于无菌12孔板中,于37 ℃恒温培养箱中孵育24 h以促进生物膜形成。 培养结束后,轻轻去除上层浮游菌,并用pH 7.2、浓度为0.1 mol/L的PBS清洗两次去除非黏附细胞及残余培养基。
清洗完成后,在每孔中加入2 mL 0.1 g/L的钌红溶液,在37 ℃条件下染色孵育60 min。染色结束后,通过紫外可见分光光度计于波长450 nm处测定样吸光度值(OD450nm 值),以未添加GL肠球菌素作为阳性对照组,BHI培养基作为空白对照组,测定胞外多糖的生成量,其计算公式如下:
1.3.7 数据处理与统计分析
采用单因素方差分析(OneWayanalysisofvariance,One Way ANOVA)对实验结果进行显著性分析,P<0.05表明数据结果具有显著性差异。采用Graphpad Prism 8.0进行作图和分析。
2 结果与分析
2.1 亚抑菌浓度的选择
2.1.1 不同GL肠球菌素浓度下单增李斯特菌生长曲线
通过生长曲线分析确定GL肠球菌素的亚抑菌浓度,不同浓度下单增李斯特菌的生长曲线见图1。 由图1可知,当GL肠球菌素浓度为1/32 MIC和1/16 MIC时,GL肠球菌素对单增李斯特菌的生长几乎不产生明显影响,表明在该浓度范围内,其抑菌作用较弱但对菌体生理活性无显著抑制[30]。因此,本研究选取1/32 MIC和1/16 MIC两个浓度作为后续实验条件,用以探讨GL肠球菌素对单增李斯特菌生物膜形成的影响。
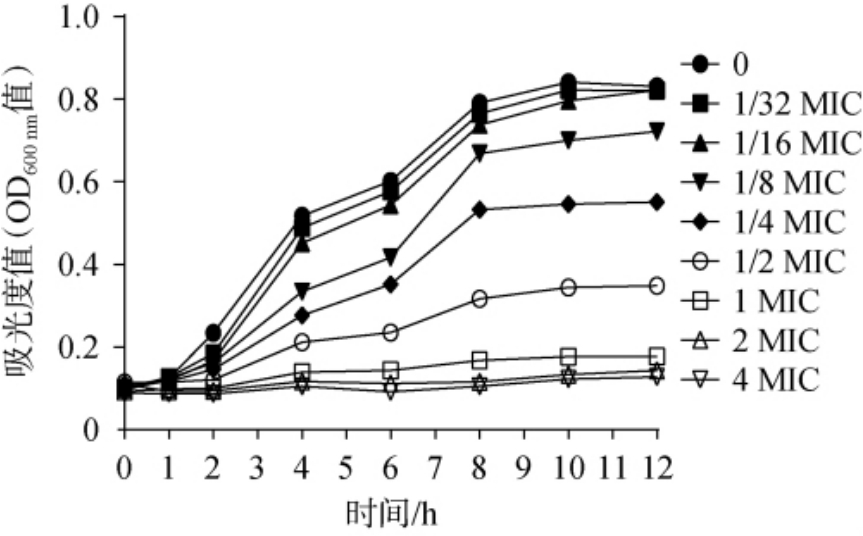
图1 不同GL肠球菌素浓度条件下单增李斯特菌的生长曲线
Fig. 1 Growth curves of Listeria monocytogenes under different concentration of enterocin GL conditions
2.1.2 GL肠球菌素对单增李斯特菌杀菌作用
不同GL肠球菌素浓度对单增李斯特菌的杀菌曲线见图2。
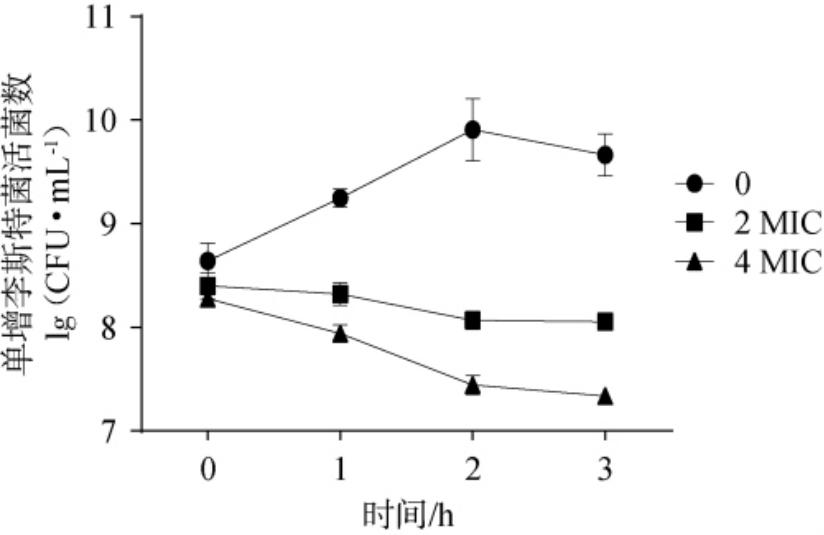
图2 不同GL肠球菌素浓度对单增李斯特菌的杀菌作用
Fig. 2 Bactericidal effect of different concentration of enterocin GL on Listeria monocytogenes
由图2可知,GL肠球菌素对单增李斯特菌浮游菌具有显著的杀灭作用,且其杀菌效果与浓度呈明显依赖关系。随着GL肠球菌素浓度的增加,菌体数量显著下降,说明该物质能够有效破坏单增李斯特菌的存活状态并抑制其生长繁殖。 通过生长曲线与杀菌曲线的综合分析,可以初步确认GL肠球菌素在低浓度下对菌体生长影响有限,而在较高浓度下表现出明显的杀菌活性,为后续研究其在生物膜形成中的抑制作用奠定了实验基础。
2.2 GL肠球菌素浓度对单增李斯特菌生物膜相对形成量的影响
进一步探究亚抑菌浓度下GL肠球菌素对单增李斯特菌生物膜形成的影响,使用结晶紫染色法对其生物膜相对形成量进行测定,结果见图3。由图3可知,经GL肠球菌素处理后,单增李斯特菌的生物膜形成显著受到抑制。与未处理组相比,当GL肠球菌素浓度分别为1/32 MIC和1/16 MIC时,生物膜相对形成量分别下降了50%和63.1%。这一结果表明,在较低浓度下,GL肠球菌素可明显干扰单增李斯特菌的黏附及聚集过程,从而减弱其生物膜的形成能力。
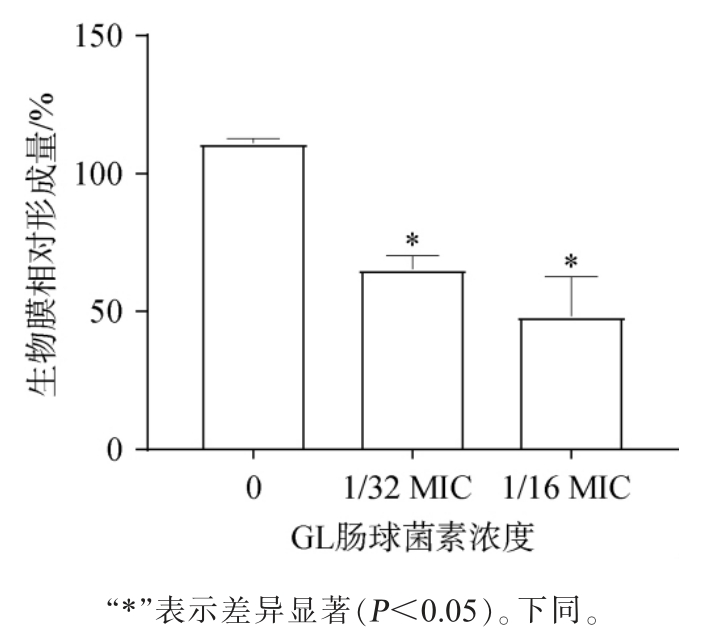
图3 不同GL肠球菌素浓度对单增李斯特菌生物被膜形成的影响
Fig. 3 Effects of different concentration of enterocin GL on the biofilm formation of Listeria monocytogenes
进一步分析发现,GL肠球菌素的抑制效果与其浓度呈一定的依赖关系,较高浓度的处理组表现出更强的抑制作用,为进一步探讨其作用机制及在食品防腐中的应用潜力提供了实验依据。
2.3 GL肠球菌素浓度对生物膜内单增李斯特菌生长及活菌数的影响
GL肠球菌素浓度对生物膜内单增李斯特菌生长及活菌数的影响结果见图4。由图4A可知,通过检测生物膜内菌群的代谢活力可以发现,不同GL肠球菌素浓度处理6 h和24 h后,GL肠球菌素显著降低了单增李斯特菌生物膜内细胞的代谢水平。 与未添加GL肠球菌素的样品相比,处理组吸光度值明显下降,活细胞数量减少,表明GL肠球菌素能够有效抑制生物膜内菌体的代谢活性,削弱其生理功能。这种代谢活力的降低说明GL肠球菌素不仅对浮游状态下的细胞具有抑制作用,还能影响附着在生物膜中的细胞,使其生理代谢受限,从而阻碍生物膜的进一步生长与稳态维持。
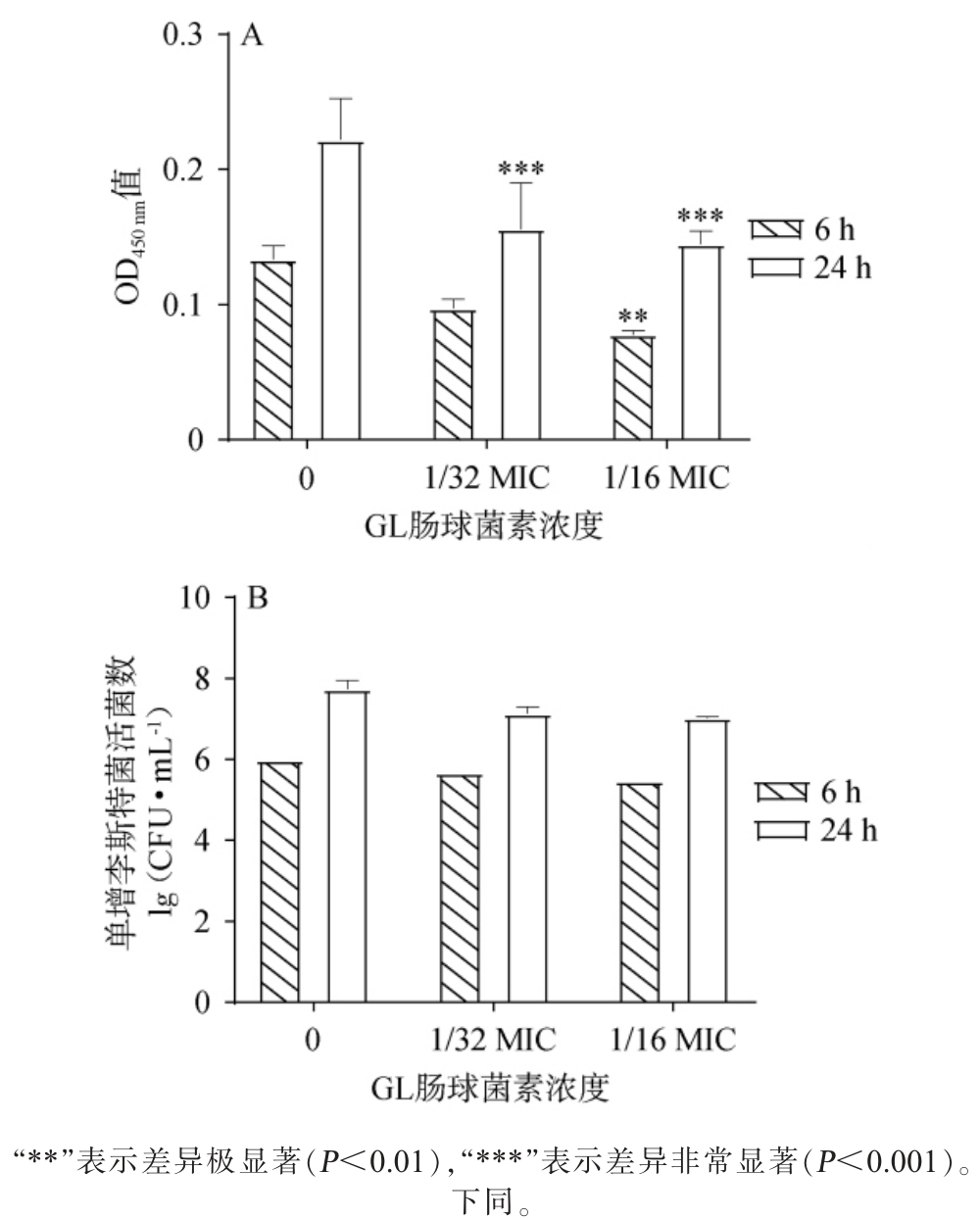
图4 不同GL肠球菌素浓度对生物被膜内单增李斯特菌生长(A)及活菌数(B)的影响
Fig. 4 Effect of different concentration of enterocin GL on the growth(A) and viable cell counts (B) of Listeria monocytogenes in biofilm
由图4B可知,GL肠球菌素处理后,生物膜内单增李斯特菌细胞数量显著下降。 与未添加GL肠球菌素的样品相比,6 h处理组的单增李斯特菌细胞数量在1/32 MIC浓度下减少约3×106CFU/mL,在1/16 MIC浓度下减少约5×106 CFU/mL,24 h处理组在1/32 MIC浓度下减少约6×106 CFU/mL,在1/16 MIC浓度下减少约8×106 CFU/mL,说明GL肠球菌素能够有效抑制单增李斯特菌在生物膜中的增殖。细胞数量的减少也间接反映出GL肠球菌素可能通过干扰细菌黏附及早期生物膜形成过程,降低细菌在表面的定植能力。综合分析表明,GL肠球菌素在亚抑菌浓度下即可通过抑制生物膜内菌的代谢活力与减少菌体数量,协同抑制单增李斯特菌的生物膜形成与生长。这一结果为其作为潜在天然抑菌剂在食品安全防控中的应用提供了有价值的实验依据。
2.4 GL肠球菌素浓度对生物膜内单增李斯特菌部分鞭毛相关基因的相对表达及泳动分析
生物膜的胞外聚合物主要由胞外多糖、蛋白质和DNA等成分构成,这些物质共同形成致密的胞外基质,在生物膜的形成、稳定及结构维持中起着关键作用。 胞外多糖尤其在细菌黏附、群体聚集及对外界胁迫的抵抗中发挥重要功能,是生物膜形成过程中不可或缺的组成部分。此外,细菌的运动性与生物膜形成密切相关,运动能力通常有助于细菌在表面扩散、寻找适合附着的部位,从而促进生物膜的初始形成阶段。不同浓度GL肠球菌素对生物膜内单增李斯特菌部分鞭毛相关基因的相对表达及泳动分析结果见图5。
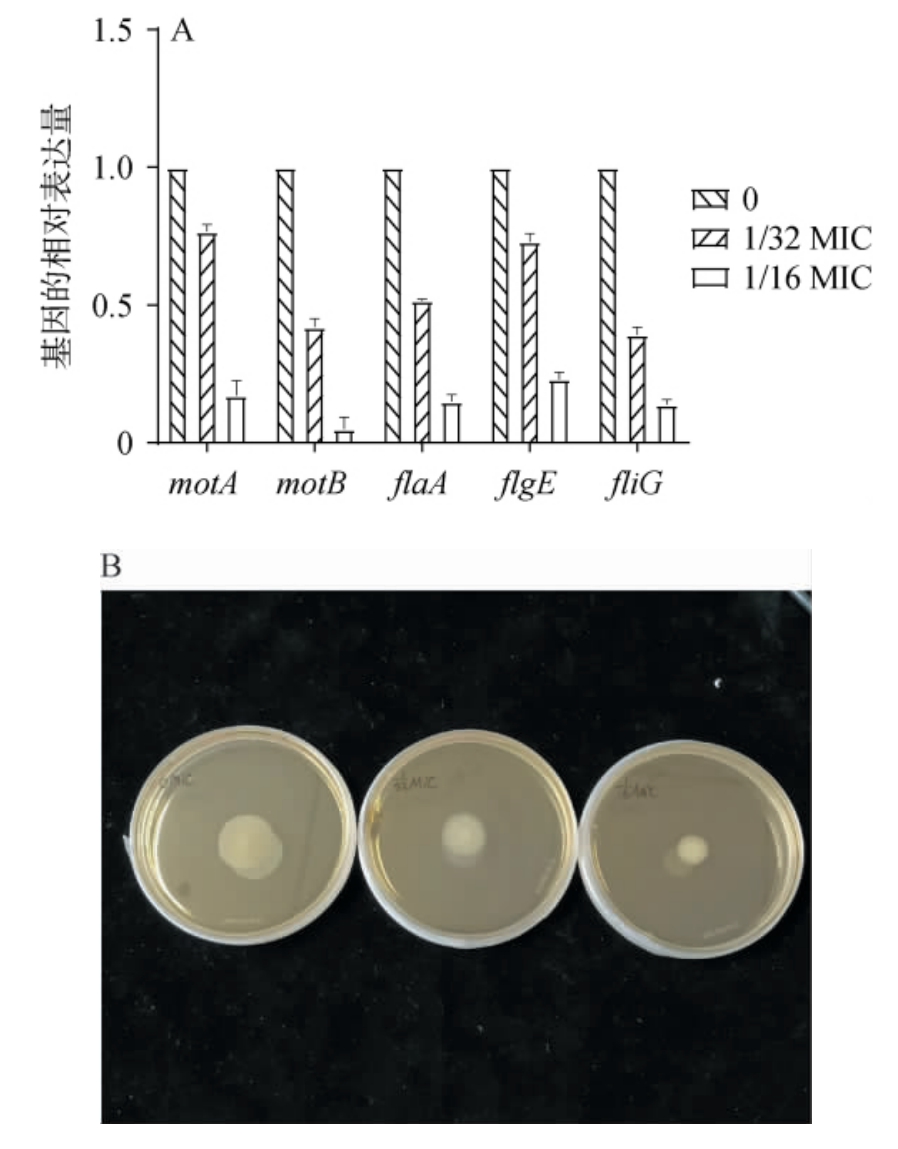
图5 不同GL肠球菌素浓度的生物被膜内单增李斯特菌部分鞭毛相关基因相对表达量(A)及泳动分析结果(B)
Fig. 5 Relative expression levels of some flagella-related genes in biofilm of Listeria monocytogenes under different concentrations of enterocin GL (A) and motility analysis results (B)
由图5A可知,不同浓度GL肠球菌素处理后,生物膜内单增李斯特菌部分鞭毛相关基因的相对表达量均发生明显变化。 与未添加GL肠球菌素的样品相比,在1/32 MIC和1/16 MIC浓度下,相关鞭毛基因相对表达量呈下调趋势,且随GL肠球菌素浓度升高,下调幅度进一步增强,表明GL肠球菌素在亚抑菌浓度条件下即可对鞭毛相关基因的转录产生抑制作用。由于鞭毛结构是细菌运动性的关键基础,上述结果提示GL肠球菌素可能通过影响鞭毛相关基因表达量进而干扰细菌运动功能。
由图5B可知,GL肠球菌素处理对单增李斯特菌的泳动能力具有显著影响。未添加GL肠球菌素样品中菌株在半固体培养基上形成由中心向外扩散的典型环状菌落,显示其在正常培养条件下具有较强的运动性和表面扩散能力。当培养体系中加入1/32 MIC浓度的GL肠球菌素后,菌落扩散圈直径明显减小,细胞迁移范围受到限制;当GL肠球菌素浓度进一步提高至1/16 MIC时,菌落圈继续缩小,扩散能力显著减弱。结果表明,GL肠球菌素可抑制单增李斯特菌的运动行为,且该抑制效应随浓度升高而增强,呈现出明显的剂量依赖性特征。
综上,GL肠球菌素可在亚抑菌浓度下干扰单增李斯特菌的鞭毛结构或相关基因表达量,从而削弱细菌的运动能力。运动性的下降可能导致菌体难以在固体表面有效扩散和附着,进而影响生物膜的早期形成与空间扩展过程。综上所述,GL肠球菌素对单增李斯特菌运动性的抑制具有明显的浓度依赖性,这一特性进一步揭示其在阻断生物膜形成过程中的潜在作用机制。
2.5 生物膜胞外多糖的测定
胞外聚合物是生物膜结构的核心组成部分,主要由胞外多糖、蛋白质和DNA构成。其中,胞外多糖在维持生物膜空间结构稳定性、促进细胞黏附及生物膜的形成与成熟过程中起着至关重要的作用。它不仅为细菌提供物理屏障以抵御外界胁迫,还能帮助细胞之间建立稳定的三维网络结构,从而维持生物膜整体的完整性与功能性。
生物膜胞外多糖:采用钌红染色法测定。 钌红是一种常用的阳离子染料,能够与胞外多糖形成稳定复合物,其结合程度可用于表征生物膜中多糖量和分布情况。 不同GL肠球菌素浓度对单增李斯特菌生物膜胞外多糖分泌的影响结果见图6。由图6可知,经GL肠球菌素处理后,染色反应的颜色明显减弱,表明单增李斯特菌胞外多糖的分泌量显著下降。 结果表明,在未达到抑菌水平的条件下,GL肠球菌素已能够对单增李斯特菌胞外多糖的分泌产生显著影响。与对照组相比,1/32 MIC处理后胞外多糖含量极显著下降(P<0.01);1/16 MIC处理后胞外多糖含量显著下降(P<0.05)。
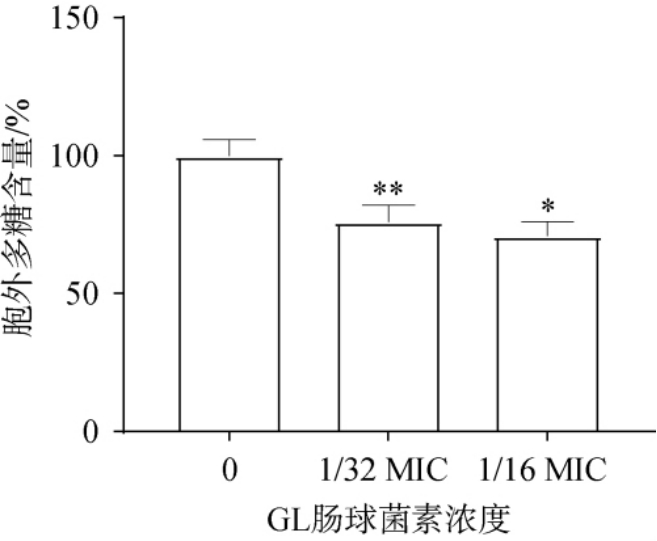
图6 不同GL肠球菌素浓度对单增李斯特菌生物被膜胞外多糖生成量的影响
Fig. 6 Effect of different concentration of enterocin GL on extracellular polysaccharide yield in biofilm of Listeria monocytogenes
胞外多糖的减少意味着生物膜的黏附力和结构稳定性均受到破坏,从而削弱细菌在表面的聚集和定植能力。综合分析可推测,GL肠球菌素可能通过影响细菌胞外多糖的合成与分泌过程,从而干扰生物膜的形成与维持。 该结果进一步证实了GL肠球菌素在抑制单增李斯特菌生物膜形成方面的显著作用,并为其作为天然抑菌剂在食品防腐与微生物控制中的潜在应用提供了重要实验依据。
3 结论
本研究通过结晶紫法定量分析发现,与对照组相比,经1/32 MIC和1/16 MIC浓度的GL肠球菌素处理后,单增李斯特菌生物膜形成量分别减少了36.5%和54.9%,表明GL肠球菌素对单增李斯特菌生物膜形成具有显著的抑制作用,且该作用呈现浓度依赖性。 不同浓度GL肠球菌素处理单增李斯特菌生物膜6 h和24 h后,生物膜内活菌数量显著下降,菌体运动性减弱,胞外多糖分泌量也明显减少。这些结果从多个角度共同表明,GL肠球菌素能够有效干扰单增李斯特菌的生物膜形成过程,并通过影响菌体生理活性和胞外基质分泌,从而削弱其黏附与聚集能力。 综上所述,GL肠球菌素在亚致死浓度下即可对单增李斯特菌生物膜形成产生显著抑制作用,其效果具有浓度依赖性。 本研究为进一步阐明GL肠球菌素的作用机制及其在食品防腐和致病菌控制中的潜在应用奠定了基础。
[1] 周旋.姜黄素抑制单增李斯特菌溶血素活性的分子机制研究[D] .长春:吉林大学,2016.
[2] 张文敏,董庆利,辛宝,等. 猪肉制品中单增李斯特菌污染现状及致病力控制分析[J] .食品与发酵工业,2023,49(17):299-307.
[3] JÓZEF A Z, JOANNA G, WIOLETA C, et al. Prevalence of Listeria monocytogenes and other Listeria species in fish, fish products and fish processing environment:A systematic review and meta-analysis[J] . Sci Total Environ,2023,907:167912.
[4] CONG Z,XIONG Y,LYU L,et al.The relationship between Listeria infections and host immune responses:Listeriolysin O as a potential target[J] .Biomed Pharmacother,2024,171:116129.
[5] SOLÈNE G,MARIE-CATHERINE L,OLIVIER D,et al.Rapid eradication of Listeria monocytogenes by moxifloxacin in a murine model of central nervous system listeriosis[J] .Antimicrob Agents Chemother,2008,52(9):3210-3215.
[6] XU Y,WANG Z,DENG J,et al.Ulk1 regulates T cell development and response to Listeria monocytogenes stimulation[J] .J Leukoc Biol,2024,117(1):183.
[7] HASSEN A,KEBA A,EBRAI S M,et al.Prevalence of Listeria monocytogenes and Listeria species and associated risk factors for contamination of milk and cottage cheese along the value chains in Ethiopia[J] .Int J Food Microbiol,2024,429:111021.
[8] 张心怡,陆兆新,郑丽平,等. 群体感应系统对单增李斯特菌生物被膜形成的影响[J] .食品科学,2022,43(18):105-112.
[9] JIANYAO L,XUECHAO H,LUJING R.Biofilm control strategies in food industry:Inhibition and utilization[J] . Trends Food Sci Technol,2022,123:103-113.
[10] SAHARAN S B,BENIWAL N,DUHAN S J.From formulation to function:A detailed review of microbial biofilms and their polymer-based extracellular substances[J] .Microbe,2024,100(5):194.
[11] BERNE C,ELLISON C K,DUCRET A,et al.Bacterial adhesion at the single-cell level[J] .Nat Rev Microbiol,2018,16(10):616-627.
[12] PRAMANA A,FIRMANDA A,ARNATA W I,et al.Reduction of biofilm and pathogenic microorganisms using curcumin-mediated photodynamic inactivation to prolong food shelf-life[J] .Int J Food Microbiol,2024,425:110866.
[13] ARTHUR M,SMITH A M,JOHNSON R,et al.Recent advances in factors influencing Listeria monocytogenes biofilms under biocides[J] .NPJ Biofilms and Microbiomes,2024,10(1):34.
[14] KASIMIN M E,HASSAN Z,AB KARIM M S,et al.Enterocin:promising biopreservative produced by Enterococcus[J] .Foods,2022,10(4):684.
[15] O'TOOLE G A. Microtiter-dish biofilm formation assay[J] .J Vis Exp,2011,47:2437.
[16] DE OLIVEIRA T F, SANTOS M A S, LOPES E S, et al. Anti-listerial activity of bacteriocin-like inhibitory substances from Enterococcus lactis[J] .Antibiotics,2024,13(3):889.
[17] WANG Z,LI Y,ZHAO J,et al.Bacteriocins attenuate Listeria monocytogenes infection and protect intestinal integrity[J] . Front Microbiol,2024,15:1367441.
[18] MU Y,SUN H,ZHOU X,et al. Antibacterial activity and action mode of bacteriocin C2-1 against Listeria monocytogenes[J] .J Food Compos Anal,2024,125:105762.
[19] XIA T, LI S, HUANG Y, et al. A novel two-component bacteriocin,Acidicin P,with antilisterial activity[J] . Microbiol Spectrum,2023,11(2):e05210-e05222.
[20] ROLON M L,CORDERO N G,Martínez A I,et al.Multi-species biofilms of environmental microbiota with Listeria monocytogenes show enhanced resistance to sanitizers[J] .Science,2024,27(5):109088.
[21] 李瑞胜. 乳酸菌素LLC518对单核增生李斯特氏菌作用机理的研究[D] .合肥:安徽农业大学,2015.
[22] SARAOUI T,FALL P A,LEROI F,et al.Inhibition mechanism of Listeria monocytogenes by a bioprotective bacteria Lactococcus piscium CNCM I-4031[J] .Food Microbiol,2016,53:70-78.
[23] WANG Y, QIN Y, ZHANG Y, et al. Antibacterial mechanism of plantaricin LPL-1,a novel class IIa bacteriocin against Listeria monocytogenes[J] .Food control,2019,97:87-93.
[24] 雷瑶. 高活性GL肠球菌素抑制单增李斯特菌生长活性及机理研究[D] .南京:南京财经大学,2024.
[25] SHI C,SUN Y,ZHENG Z,et al.Antimicrobial activity of syringic acid against Cronobacter sakazakii and its effect on cell membrane[J] .Food Chem,2016,197(PA):100-106.
[26] SALAZAR K J,FAY L M,FLEISCHMAN G,et al.Inactivation kinetics of Listeria monocytogenes and Salmonella enterica on specialty mushroom garnishes based on ramen soup broth temperature[J] .Front Microbiol,2024,15:1485398.
[27] FELIPE V, BRESER L M, BOHL P L, et al. Chitosan disrupts biofilm formation and promotes biofilm eradication in Staphylococcus species isolated from bovine mastitis[J] .Int J Biol Macromol,2018,12(6):60-67.
[28] 刘昀阁. 单增李斯特菌生物膜形成特性及天然抑菌物质对其抑制机理的研究[D] .泰安:山东农业大学,2021.
[29] 乔柱. 异源表达细菌素BMP32r杀菌和抑制生物膜作用机制研究[D] .杨凌:西北农林科技大学,2021.
[30] RODRÍGUEZ-MELCÓN C,LAMAS A,FRANCO C M,et al.Low-dose biocides can increase Listeria monocytogenes biofilm formation and resistance[J] .Biology,2025,14(4):495.