豆类,是植物蛋白质的重要来源,富含脂肪、膳食纤维、维生素和矿物质等[1]。发酵作为一种历史悠久且应用广泛的生物技术,在大豆加工中扮演着重要角色,可以改善大豆的营养、质地和风味。 发酵过程中微生物代谢活动将豆类中的大分子物质酶解并产生生物活性物质,如活性肽、不饱和脂肪酸、游离大豆异黄酮、B族维生素、γ-氨基丁酸(γ-aminobutyric acid,GABA)等,使发酵大豆制品在营养和健康方面更具优势,赋予其具有抗氧化、降压、抗肿瘤、降低血浆胆固醇、保护肝脏和抗衰老等功效[2-3]。研究表明,大豆是植物雌激素异黄酮的重要来源之一,通过发酵可以增加大豆中异黄酮、维生素和矿物质的生物利用度[4-6]。
传统发酵豆制品是大豆自然发酵从原料到发酵成品的转化,豆豉、大酱、腐乳、酱油是我国四大传统大豆发酵食品,已有数千年的历史[7]。种类繁多的发酵大豆食品形成了我国独特的豆制品文化,其凭借独特风味和营养价值备受青睐。地理条件的差异赋予发酵豆制品鲜明地域特色,在形成多样化风味体验的同时也成为了地域文化的象征。然而,发酵豆制品产业目前仍面临产品质量稳定性不足、生产有待提升和创新能力薄弱等挑战[7-8]。由于传统自然发酵方式依赖开放环境,易受发酵条件影响,使得微生物群落结构存在差异,导致产品色泽、风味不稳定,并影响整体品质与安全性[9-10]。 传统发酵豆制品独特风味与营养价值源于微生物群落的复杂代谢活动,产品的特性和质量取决于核心微生物群,因此,深入解析不同传统发酵豆制品中的微生物多样性,对于提升产品品质、保障食品安全具有重要意义。
近年来,高通量测序技术的发展为传统发酵食品微生物研究提供了新途径,相较于传统培养方法,该技术可全面揭示不可培养微生物信息,精准解析菌群结构[11-12]。 目前,对于传统发酵豆制品微生物资源挖掘的研究多只聚焦单一品类或局部产区,多类别、跨产区发酵豆制品微生物差异系统性比较的研究仍较缺乏。如马上超等[13]收集了恩施州不同产地的5种细菌型淡豆豉,运用高通量测序技术分析恩施地区豆豉发酵微生物菌群结构,共鉴定出17门、24纲、43目、78科、152属以及93种,各样品间优势菌属相同,相对丰度存在较大差异;马岩石等[14]对东北市售5 种常见豆酱进行微生物多样性分析,发现其微生物群落和风味与其地理位置以及加工方式存在一定关系。 CHEN C等[15]通过多组学技术阐明自然发酵腐乳中微生物群落、品质与风味形成之间的动态互作关系,结果显示毛霉(Mucor)、肠杆菌(Enterbacter)和四联球菌(Tetragenococcus)为腐乳核心功能微生物群,这些菌属与关键风味物质呈显著正相关。本研究以收集到不同产地的3大类12种传统发酵豆制品为研究对象,采用高通量测序技术对发酵豆制品16S rRNA基因和内部转录间隔区(internal transcribed spacer,ITS)基因序列进行测序,揭示不同种类以及同种类不同产地发酵豆制品微生物群落结构,并对细菌和真菌基因功能进行预测,旨在挖掘关键功能微生物资源,以期为优化发酵工艺,提高产品的稳定性以及精细调控微生物代谢途径,提升生产效率提供理论依据。
1 材料与方法
1.1 材料与试剂
1.1.1 原料
采集不同产地传统发酵豆制品样品的种类、编号及产地信息见表1。
表1 不同产地发酵豆制品样品的信息
Table 1 Information of fermented soybean product samples from different regions

样品种类样品名称产地样品编号豆酱黄豆酱黄豆酱黄豆酱黄豆酱江苏辽宁安徽浙江DJ1 DJ2 DJ3 DJ4
续表
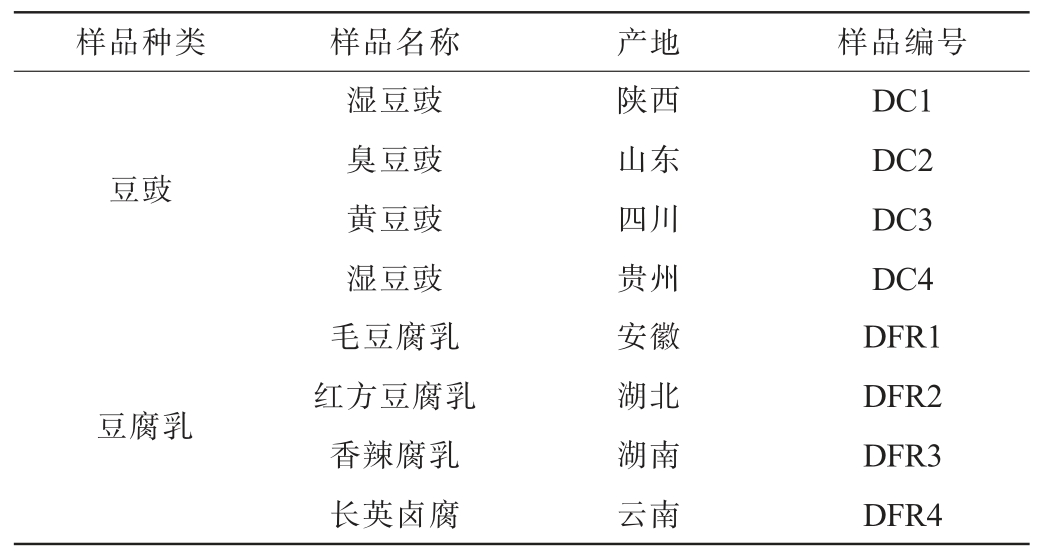
样品种类样品名称产地样品编号豆豉豆腐乳湿豆豉臭豆豉黄豆豉湿豆豉毛豆腐乳红方豆腐乳香辣腐乳长英卤腐陕西山东四川贵州安徽湖北湖南云南DC1 DC2 DC3 DC4 DFR1 DFR2 DFR3 DFR4
1.1.2 试剂
FastPureSoil 脱氧核糖核酸(deoxyribonucleicacid,DNA)抽提试剂盒、Clean-Up Kit DNA凝胶回收纯化试剂盒:上海美吉逾华生物医药科技有限公司;2×ProTaq HS PCR Master Mix ver2:湖南艾科瑞生物工程有限公司;琼脂糖(Agarose75510019):美国Thermo Scientific公司。
1.2 仪器与设备
Eppendorf 5430 R离心机:德国Eppendorf公司;ABI GeneAmpR 9700型聚合酶链式反应(polymerase chain reaction,PCR)仪:美国ABI公司;JY600C电泳仪:北京君意东方电泳设备有限公司;NanoDrop2000超微量分光光度计:美国ThermoScientific公司;Illumina Nextseq2000测序仪:美国Illumina公司。
1.3 方法
1.3.1 样品DNA提取
从12种不同发酵豆制品中无菌取样1 g样品,根据DNA抽提试剂盒说明书进行微生物群落总基因组DNA抽提,使用1%的琼脂糖凝胶电泳在电压5 V/cm、时间为20 min的条件下检测抽提的基因组DNA的完整性,使用NanoDrop 2000测定DNA 浓度和纯度,DNA 无明显降解、浓度合适、无杂质,方可进行后续实验。
1.3.2 PCR扩增和高通量测序
以提取的DNA为模板,细菌使用引物338F(5'-ACTCCTACGGGAGGCAGCAG-3')和806R(5'-GGACTACHVGGGTWTCTAAT-3')对16S rRNA基因V3-V4 可变区进行PCR 扩增,真菌使用引物ITS1F(5'-CTTGGTCATTTAGAGGAAGTAA-3')和ITS2R(5'-GCTGCGTTCTTCATCGATGC-3')对ITS基因进行PCR扩增。PCR扩增体系为:2×ProTaq 10 μL,上游引物(5 μmol/L)0.8 μL,下游引物(5 μmol/L)0.8 μL,模板DNA(10 ng/μL)2 μL,补双蒸水(ddH2O)至20 μL。 PCR扩增程序为95 ℃预变性3 min,细菌29个循环(95 ℃变性30 s,53 ℃退火30 s,72 ℃延伸45 s);真菌35 个循环(95 ℃变性30 s,55 ℃退火30 s,72 ℃延伸45 s),然后72 ℃稳定延伸10 min,最后10 ℃保存至反应结束。使用2%琼脂糖凝胶电泳检测PCR产物。 Illumina Nextseq2000高通量测序由上海美吉生物医药科技有限公司完成。
1.3.3 数据处理及分类学分析
使用Fastp 0.19.6和FLASH 1.2.11软件对双端原始测序序列进行质控与拼接。 基于默认参数,使用Qiime 2.0 流程中的DADA 2.0插件对质控拼接之后的优化序列进行降噪,获得扩增子序列变体(ampliconsequencevariants,ASVs)。基于Silva 16S rRNA基因数据库和Unite真菌ITS数据库,使用Qiime 2.0中的Naive bayes分类器对ASVs进行物种分类学分析,利用PICRUSt 2和FUNGuild 1.0软件进行16S和ITS功能预测分析。 采用美吉云平台提供的绘图工具进行绘图。
2 结果与分析
2.1 传统发酵豆制品高通量测序数据统计
采用高通量测序技术对传统发酵豆制品进行微生物多样性分析,通过对细菌16S rRNA基因测序,共获得378 037条有效序列,ASV数量范围为43~402;对真菌ITS区进行测序,共获得850 483条序列,ASV数量范围为1~128。绘制丰度等级曲线反映不同样品物种丰度和均匀度,曲线在横轴上的范围越大则物种的丰富度越高,曲线越平缓则物种分布越均匀。由图1a可知,细菌群落具有较高的物种丰富度,但其均匀度因样品种类和产地不同而有所差异,其中豆腐乳样品的细菌均匀度普遍高于豆酱和豆豉。 由图1b可知,真菌群落的物种丰富度总体低于细菌,细菌群落的曲线走势较真菌平缓,细菌群落分布更均匀。结果表明,发酵豆制品中细菌群落结构更复杂。
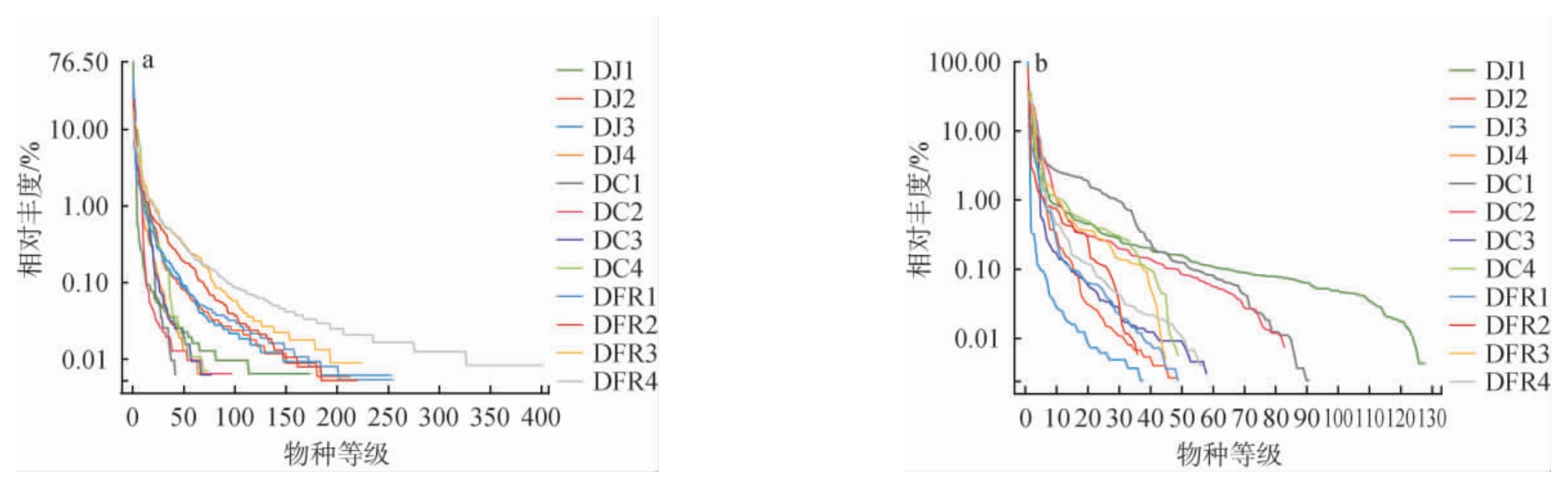
图1 不同传统发酵豆制品细菌(a)和真菌(b)丰度等级曲线
Fig. 1 Rank abundance curves of bacteria (a) and fungi (b) of different traditional fermented soybean products
2.2 传统发酵豆制品微生物群落多样性分析
2.2.1 Alpha多样性分析
对不同发酵豆制品样品中的细菌和真菌群落进行Alpha多样性分析,结果见表2。
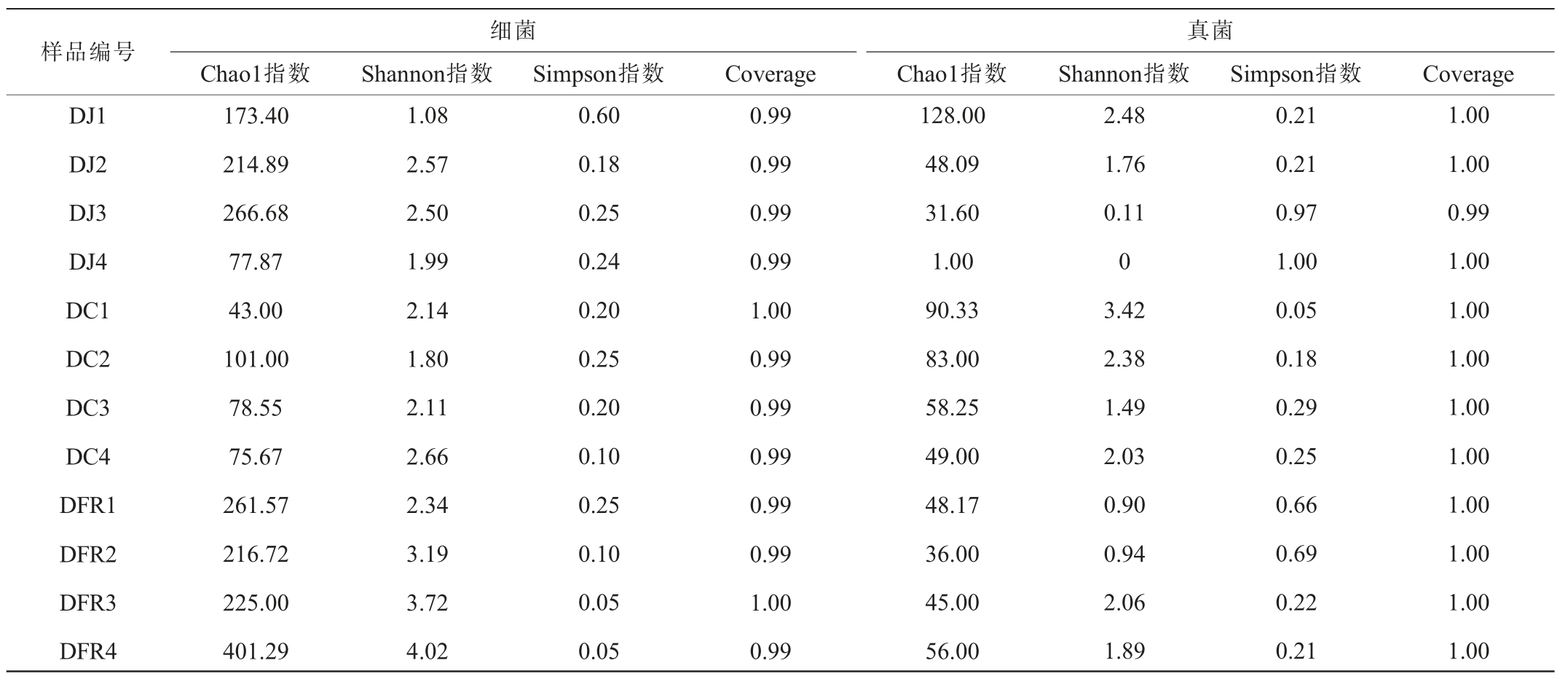
表2 不同传统发酵大豆制品细菌和真菌Alpha多样性分析
Table 2 Alpha diversity analysis of bacteria and fungi of different traditional fermented soybean products
样品编号DJ1 DJ2 DJ3 DJ4 DC1 DC2 DC3 DC4 DFR1 DFR2 DFR3 DFR4细菌Chao1指数Shannon指数Simpson指数173.40 214.89 266.68 77.87 43.00 101.00 78.55 75.67 261.57 216.72 225.00 401.29 1.08 2.57 2.50 1.99 2.14 1.80 2.11 2.66 2.34 3.19 3.72 4.02 0.60 0.18 0.25 0.24 0.20 0.25 0.20 0.10 0.25 0.10 0.05 0.05 Coverage 0.99 0.99 0.99 0.99 1.00 0.99 0.99 0.99 0.99 0.99 1.00 0.99真菌Chao1指数Shannon指数Simpson指数Coverage 128.00 48.09 31.60 1.00 90.33 83.00 58.25 49.00 48.17 36.00 45.00 56.00 2.48 1.76 0.11 0 3.42 2.38 1.49 2.03 0.90 0.94 2.06 1.89 0.21 0.21 0.97 1.00 0.05 0.18 0.29 0.25 0.66 0.69 0.22 0.21 1.00 1.00 0.99 1.00 1.00 1.00 1.00 1.00 1.00 1.00 1.00 1.00
由表2可知,所有样品的Coverage均>0.99,说明样品文库的覆盖率很大,测序结果代表了样本中微生物的真实情况。在细菌多样性方面,样品DFR4表现出最高的细菌物种丰富度和群落多样性(Chao1指数401.29,Shannon指数4.02,Simpson指数0.05),说明其具有复杂的细菌菌群结构。相反地,样品DC1细菌丰富度最低(Chao1指数43.00),样品DJ1的细菌菌群结构最简单(Shannon指数1.08,Simpson指数0.60)。由Chao1指数分析结果可知,3类传统发酵豆制品中豆腐乳的细菌物种丰富度最高,表明豆腐乳样品中的细菌物种数量最多;豆酱的丰富度次之,但各样品差异较大;豆豉的细菌丰富度整体最低。由Shannon和Simpson指数可知,3类发酵豆制品中豆腐乳拥有最高的细菌群落多样性,群落物种分布均匀;豆豉的细菌多样性处于中等水平,且样本间差异相对较小;豆酱的细菌多样性整体较低。
在真菌多样性方面,真菌群落的丰富度和多样性整体低于细菌群落。样品DJ1的真菌群落物种丰富度最高(Chao1指数128.00),样品DC1的真菌群落多样性最高(Shannon指数3.42、Simpson指数0.05)。由Chao1指数可知,豆酱样品真菌丰富度差异较大,从样品DJ4的极低值(1.00)到样品DJ1的最高值(128.00);豆腐乳的真菌丰富度整体最低;由Shannon和Simpson 指数可知,豆豉样品表现出最高的真菌群落多样性,其真菌物种丰富,且分布均匀;豆酱各样品的真菌多样性差异较大,其中DJ4的多样性极低(Shannon指数0,Simpson指数为1.00),表明其真菌群落由极少数物种主导,群落均匀度极低;豆腐乳样品的多样性表现出不同的差异,说明其真菌群落分布上有所不同,可能与发酵原料、工艺以及产地不同有关[16]。
2.2.2 主成分分析
主成分分析(principal component analysis,PCA),是对数据进行简化分析的技术,其运用方差分解,将复杂的微生物群落数据差异反映在二维坐标图上[17]。基于属水平分别对不同发酵豆制品细菌和真菌的微生物群落进行主成分分析,结果见图2。由图2a可知,豆酱样品(DJ2~DJ4)分布较为集中,说明其细菌群落组成有一定的相似性。 通常同一个地区的发酵豆制品在发酵时具有相似的温度和发酵条件[16],而PCA图中样品DJ1与其他3个地区的样品相距较远,表明地理环境对其细菌菌群结构有一定影响。 豆豉样品分布较为分散,尤其是样品DC2细菌群落与其他样品差异较大;豆腐乳样品呈现出一定的分散性,尤其样品DFR1与其他样品相距较远,表明其细菌群落具有独特性。此外,样品DJ1、DC3和DC1分布较为集中,表明不同种类发酵豆制品的细菌群落组成具有一定相似性。
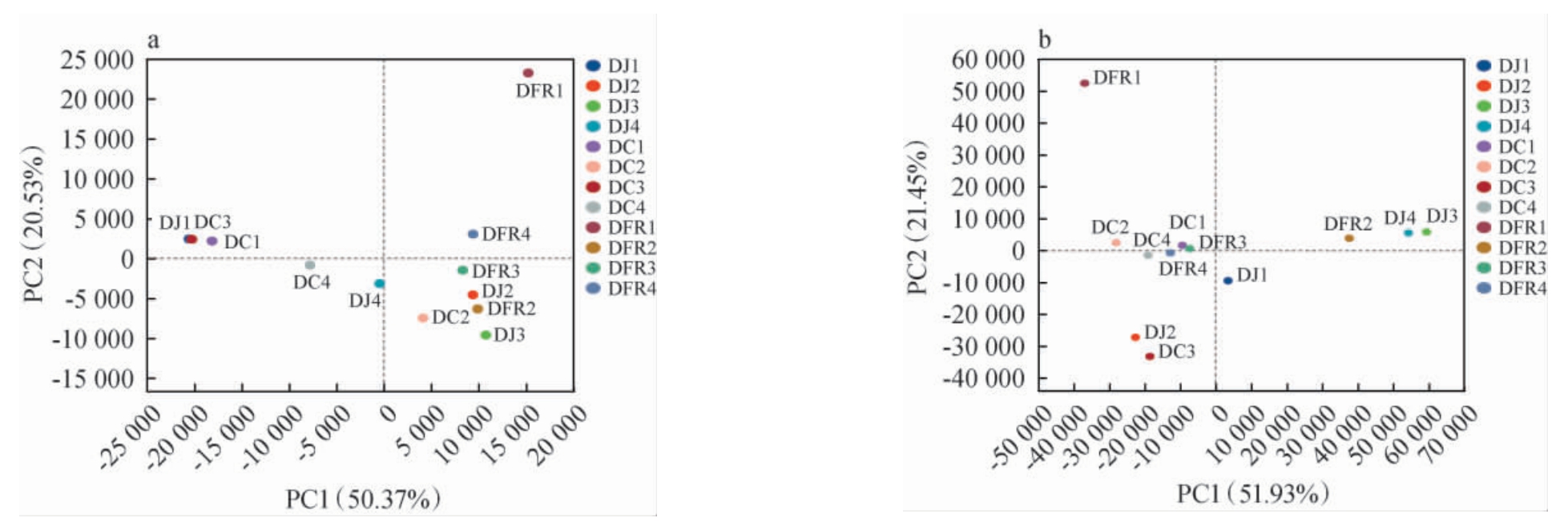
图2 基于属水平不同传统发酵豆制品细菌(a)和真菌(b)群落主成分分析结果
Fig. 2 Principal component analysis results of bacterial (a) and fungal (b) communities in different traditional fermented soybean products based on genus level
由图2b可知,不同类别的发酵豆制品在真菌群落结构上表现出明显分离。 豆酱样品分布范围较分散,表明其真菌群落可能存在一定的地域差异;样品DC1、DC2、DC4、DFR3和DFR4呈现聚集趋势,表明部分豆豉和豆腐乳的真菌群落具有相似性;此外,样品DFR1与其他样品分离明显,可能与毛豆腐乳特色发酵工艺有关。
主成分分析(PCA)结果表明,传统发酵豆制品微生物群落结构受产品种类和产地影响,通过PCA可以有效区分不同传统发酵豆制品。
2.3 传统发酵豆制品微生物群落组成分析
2.3.1 基于门水平的微生物群落结构分析
基于门水平,不同传统发酵豆制品中细菌和真菌群落结构的分布情况见图3。 由图3a可知,共检出4个优势细菌门(相对丰度>1%),分别为厚壁菌门(Firmicutes)、变形菌门(Proteobacteria)、拟杆菌门(Bacteroidota)和放线菌门(Actinobacteriota)。 厚壁菌门和变形菌门是主要优势细菌菌门,其中厚壁菌门在所有样品中均有较高相对丰度,尤其是在样品DJ4、DC2和DC4中,厚壁菌门相对丰度接近99%,表明其在豆制品发酵过程中起主导作用。厚壁菌门是一类革兰氏阳性菌,在含盐量高、缺水以及极端发酵环境中均能生长,广泛存在于发酵食品中[18-19]。变形菌门在不同种类样品中的分布差异显著,在样品DJ3和DC3中,变形菌门相对丰度为7.48%和7.47%,在部分腐乳样品中变形菌门相对丰度显著升高,如在样品DFR3和DFR4中变形菌门相对丰度分别为54.21%和21.78%,可能与变形菌门中的许多菌属(如假单胞菌)具有耐盐性以及分解蛋白质和脂肪能力有关,使其在腐乳中具有生长优势[20]。
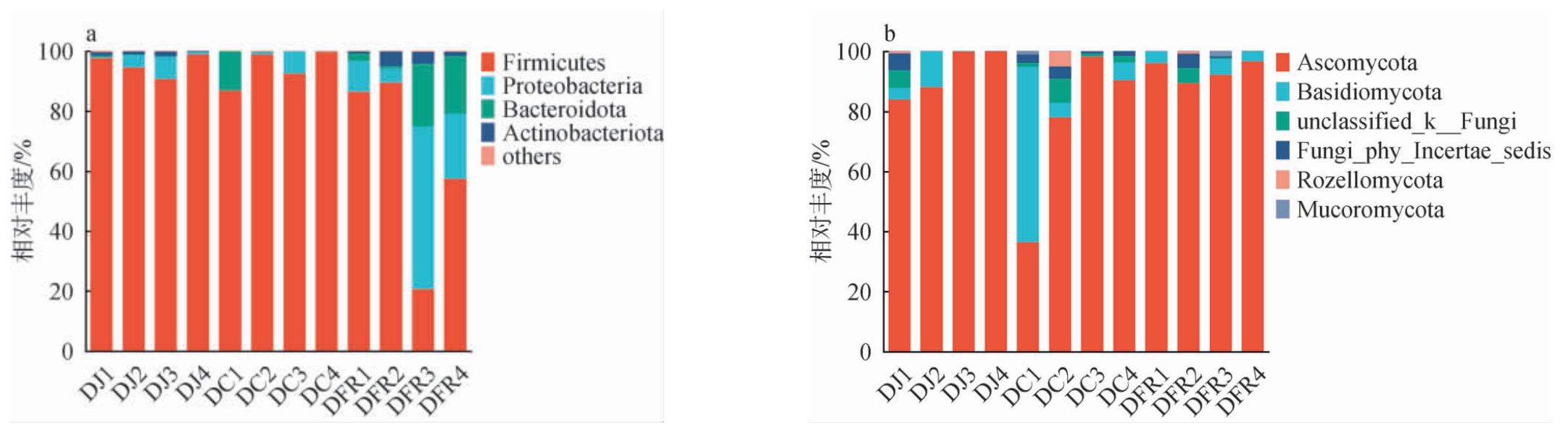
图3 基于门水平不同传统发酵豆制品中细菌(a)和真菌(b)群落结构分析结果
Fig. 3 Analysis results of bacterial (a) and fungal (b) community structure in different traditional fermented soybean products based on phylum level
由图3b可知,在真菌门水平上,共检出2个优势真菌门(相对丰度>1%),其中子囊菌门(Ascomycota)几乎是所有样品的优势真菌门,其次为担子菌门(Basidiomycota)。子囊菌门在多数样品中丰度极高,尤其在样品DJ4中达到100%,说明其在豆制品发酵中起核心作用。子囊菌门的高丰度符合传统发酵食品中真菌群落的普遍特征,其下属的酵母属、曲霉属等真菌在碳水化合物代谢和风味物质生成中具有重要作用[21-22]。 豆豉样品的真菌群落在门水平上呈现明显差异,样品DC3和DC4中子囊菌门相对丰度分别为98.23%和90.38%,显著高于样品DC1(36.42%)和DC2(78%),担子菌门在样品DC1中相对丰度最高,达到58.42%。
2.3.2 基于属水平的微生物群落结构分析
基于属水平,不同传统发酵豆制品中细菌和真菌群落结构的分布情况见图4。由图4a可知,检测到的优势细菌属(相对丰度>1%)包括芽孢杆菌属(Bacillus)、魏斯氏菌属(Weissella)、乳酸杆菌属(Lactobacillus)、葡萄球菌属(Staphylococcus)、四联球菌属(Tetragenococcus)、肠球菌属(Enterococcus)、假单胞菌属(Pseudomonas)等。不同传统发酵豆制品间的细菌菌群结构存在差异,豆酱样品中的主要优势菌属有芽孢杆菌属、魏斯氏菌属、葡萄球菌属、四联球菌属、伴生乳杆菌属(Companilactobacillus)等;豆豉样品中的主要优势菌属有芽孢杆菌属、魏斯氏菌属、肠球菌属、葡萄球菌属、鞘氨醇杆菌属(Sphingobacterium)等;豆腐乳样品中的主要优势菌属有乳酸杆菌属、假单胞菌属(Pseudomonas)、赖氨酸芽孢杆菌属(Lysinibacillus)、魏斯氏菌属、拉脱维亚乳酸杆菌(Latilactobacillus)、鞘氨醇杆菌属、Dysgonomonas等。其中,芽孢杆菌属是豆制品发酵的核心菌属,在豆豉和部分黄豆酱中相对丰度较高,样品DJ1中相对丰度最高(95.1%),其与蛋白酶和淀粉酶活性密切相关,有助于蛋白质、脂肪和碳水化合物的分解与风味形成[16,23]。豆腐乳样品细菌群落组成更多样,乳酸杆菌属在样品DFR1和DFR4中均有较高相对丰度,兰林等[19]对4种不同来源豆腐乳进行微生物多样性分析和相对丰度比对,发现乳酸杆菌属为纯种发酵与自然发酵豆腐乳优势菌属。各样品在属水平上的多样性及相对丰度存在较大差异,反映出不同种类以及不同地理来源的发酵豆制品之间的细菌菌群结构差异,这种差异可能与不同的原材料、发酵温度、气候与地理条件等因素有关。庞春霞等[24]研究发现,来自不同地区的同类产品菌群结构存在差异,归因于地域环境中微生物差异以及不同的加工工艺条件。
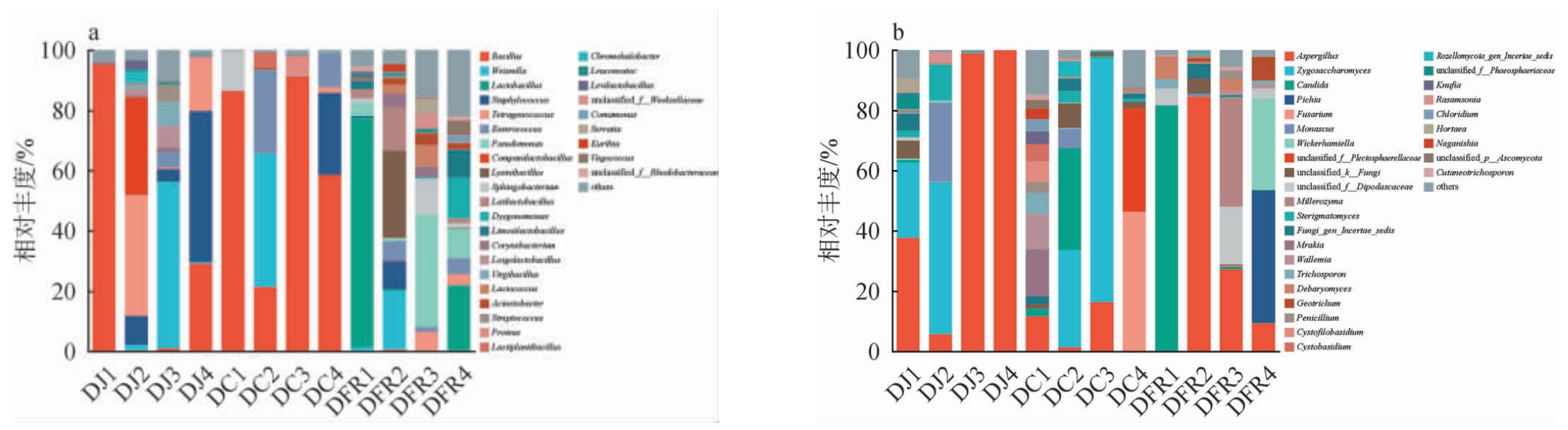
图4 基于属水平不同传统发酵豆制品中细菌(a)和真菌(b)群落结构分析结果
Fig. 4 Analysis results of bacterial (a) and fungal (b) community structure in different traditional fermented soybean products based on genus level
由图4b可知,在真菌属水平上检测到的优势真菌属(相对丰度>1%)包括曲霉属(Aspergillus)、接合酵母属(Zygosaccharomyces)、假丝酵母属(Candida)、毕赤酵母属(Pichia)等。豆酱样品中的优势真菌属为曲霉属、接合酵母属、红曲属(Monascus)、Sterigmatomyces等;豆豉样品中的优势真菌属为接合酵母属、假丝酵母属、曲霉属、镰刀菌属(Fusarium)、木拉克酵母属(Mrakia)、节担菌属(Wallemia)等;豆腐乳样品中的优势真菌属为曲霉属、假丝酵母属、毕赤酵母属、米勒氏酵母属(Millerozyma)、拟威客酵母属(Wickerhamiella)等。各样品真菌群落表现出明显的种类和地域差异,优势菌群的种类及相对丰度差异显著。 曲霉属是主要的优势真菌属,在样品DJ3、DJ4和DFR2中相对丰度为84.54%~100.00%。曲霉属能够产生蛋白酶、淀粉酶和脂肪酶等水解酶,在发酵过程中使淀粉糖化、蛋白质水解以及生成类黄酮,有助于氨基酸以及芳香类物质的生成[16,25-26]。接合酵母属和假丝酵母属在部分样品中具有较高丰度。酵母属在豆制品发酵前期起主导作用,参与代谢反应产生醇类和醛类等代谢物,促进风味物质的形成,如假丝酵母属中部分菌种和鲁氏接合酵母等可通过酒精发酵能力增加产品的醇香[10,25,27]。
2.4 细菌和真菌群落的功能预测
利用PICRUSt2软件基于16S rRNA基因数据对发酵豆制品细菌群落进行功能预测。将测序基因信息与京都基因和基因组百科全书(Kyoto encyclopedia ofgenesand genomes,KEGG)功能数据库进行比对,获得每个样本中对应的功能信息和丰度信息,在一级功能层(Level1)上注释得到6 类生物代谢通路,包括代谢(74.38%~77.63%)、环境信息处理(6.83%~8.61%)、遗传信息处理(5.82%~9.03%)、细胞过程(2.63%~5.07%)、人类疾病(2.59%~4.21%)和生物体系统(1.37%~1.93%),其中代谢通路在所有样本中均占据绝对主导地位,表明发酵豆制品中微生物主要参与各类代谢活动。 在二级功能层(Level2)上注释到46条功能子类,相对丰度排名前30的二级通路如图5a所示,全局和总览图谱(Global and overview maps)表现出最高相对丰度,其次是碳水化合物代谢(Carbohydrate metabolism)和氨基酸代谢(Amino acid metabolism),说明碳水化合物和氨基酸代谢是发酵过程中的核心生物过程,这与豆制品富含蛋白质和碳水化合物的基质特性一致。不同发酵豆制品细菌群落的基因功能预测类型基本相同,但功能预测表达量存在差异。从整体上看,豆豉类样品在多个代谢通路中的功能预测丰度高于其他两类,尤其是DC1和DC3在碳水化合物代谢、氨基酸代谢、膜运输(Membrane transport)、能量代谢(Energy metabolism)、辅因子与维生素代谢(Metabolism of cofactors and vitamins)及信号转导(Signal transduction)等多个通路中表现出较高丰度,表明其细菌群落具有更强的整体代谢活性和环境适应能力。
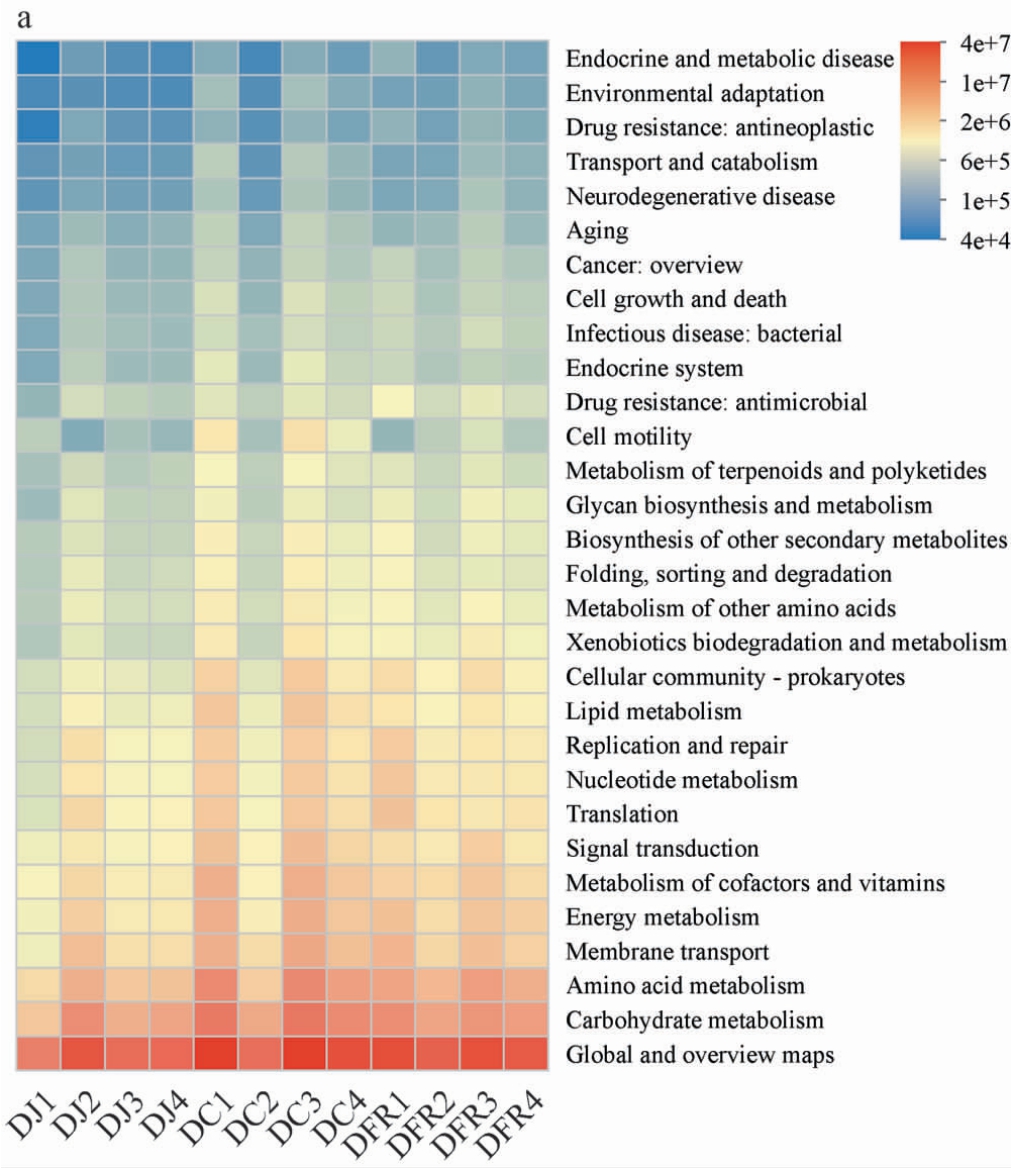
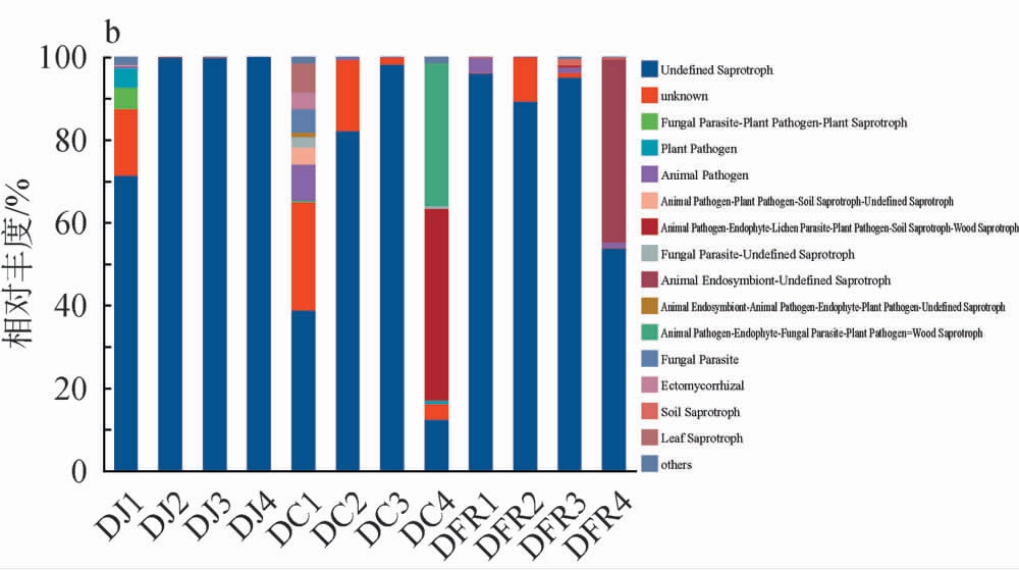
图5 不同传统发酵豆制品细菌(a)和真菌(b)群落功能预测
Fig. 5 Function prediction of bacterial (a) and fungal (b) community structure in different traditional fermented soybean products
FUNGuild 根据营养方式将真菌分为三大类:病理营养型(pathotroph)、共生营养型(symbiotroph)和腐生营养型(saprotroph)[28]。运用FUNGuild功能预测软件基于ITS基因序列对发酵豆制品真菌群落进行功能注释,共获得涵盖腐生型、病原型及共生型等多种营养方式的31个功能类群,结果见图5b。由图5b可知,未定义腐生真菌(UndefinedSaprotroph)为绝大多数样品的优势类群,其相对丰度在多数样品中超过50%,表明腐生营养模式是真菌在豆制品发酵过程中的主要功能类型。 豆酱样品中真菌功能群落较为单一,以Undefined Saprotroph为主,其说明其发酵过程以腐生降解为主;豆豉样品的真菌功能群落表现出较高的多样性,除Undefined Saprotroph外,在DC1和DC4中还检测到多种复合功能型真菌;豆腐乳样品真菌群落结构相对简单,Undefined Saprotroph仍占主导。
3 结论
为比较传统发酵豆制品微生物群落组成和基因功能差异,对不同产地的3大类12种传统发酵豆制品的微生物群落进行多样性分析及功能预测。发酵豆制品中细菌群落的丰富度和多样性整体高于真菌,细菌群落组成更复杂。同时,各样品微生物多样性受产品种类与产地共同调控,豆腐乳样品表现出更高的细菌多样性,而豆豉样品在真菌群落方面更具多样性,豆酱样品微生物多样性较低且受地域影响较大。 受产品种类、发酵工艺和不同地理环境微生物差异等多重因素影响,不同种类及产地的发酵豆制品在细菌和真菌群落结构及丰度上存在明显差异。 细菌群落中,厚壁菌门(Firmicutes)和变形菌门(Proteobacteria)为优势菌门,芽孢杆菌属(Bacillus)为多数样品的核心菌属,魏斯氏菌属(Weissella)、葡萄球菌属(Staphylococcus)、四联球菌属(Tetragenococcus)为部分样品优势菌属。与豆酱和豆豉样品相对比,豆腐乳表现出更丰富的细菌群落组成,其中乳杆菌属(Lactobacillus)具有较高相对丰度;真菌群落以子囊菌门(Ascomycota)为主导,曲霉属(Aspergillus)在多数样品中占据主导地位,接合酵母属(Zygosaccharomyces)、假丝酵母属(Candida)、毕赤酵母属(Pichia)在部分样品中具有较高相对丰度。 微生物在发酵过程中参与代谢反应,形成各具特色的豆制品风味。PICRUSt2和FUNGuild功能预测结果显示,细菌在一级功能层和二级功能层上分别注释得到6类生物代谢通路和46条功能子类,细菌群落功能以代谢活动为主,尤其是碳水化合物和氨基酸代谢;真菌获得涵盖腐生型、病原型及共生型等多种营养方式的31个功能类群,真菌群落以腐生营养模式为主,参与物质转化与风味形成,部分样品中检测到低丰度潜在病原菌,需关注其食品安全风险。本研究深入解析传统发酵豆制品的微生物多样性及其功能,有助于优化发酵工艺、提升产品品质与安全性,也为发酵豆制品中有益菌的筛选和有害菌的抑制以及研究微生物菌群与发酵食品风味相关性奠定理论基础。
[1] 叶听雨,樊铭聪,钱海峰,等. 豆制品加工过程中嘌呤去除方法的研究进展[J] .中国粮油学报,2025,40(6):216-224,234.
[2] LIU L B, CHEN X Q, HAO L L, et al. Traditional fermented soybean products:processing,flavor formation,nutritional and biological activities[J] .Crit Rev Food Sci Nutr,2022,62(7):1971-1989.
[3] JAYACHANDRAN M,XU B J.An insight into the health benefits of fermented soy products[J] .Food Chem,2019,271:362-371.
[4] CAO Z H,GREEN-JOHNSON J M,BUCKLEY N D,et al.Bioactivity of soy-based fermented foods:A review[J] . Biotechnol Adv, 2019, 37(1):223-238.
[5] DONKOR O N,SHAH N P.Production of beta-glucosidase and hydrolysis of isoflavone phytoestrogens by Lactobacillus acidophilus,Bifidobacterium lactis, and Lactobacillus casei in soymilk[J] . J Food Sci, 2008, 73(1):M15-20.
[6] CHAMPAGNE C P, TOMPKINS T A, BUCKLEY N D, et al. Effect of fermentation by pure and mixed cultures of Streptococcus thermophilus and Lactobacillus helveticus on isoflavone and B-vitamin content of a fermented soy beverage[J] .Food Microbiol,2010,27(7):968-972.
[7] 张鹏飞,乌日娜,武俊瑞. 传统发酵大豆制品挥发性成分和微生物多样性的研究进展[J] .中国酿造,2018,37(12):1-6.
[8] 胡会萍,刘丹赤,殷丽君,等. 豆豉后发酵中优势菌株筛选及其生产性能[J] .食品科学,2014,35(17):146-152.
[9] 杨智博,谭小琴,周才琼. 渝黔地区细菌发酵型豆豉食用安全性及风味特点比较分析[J] .食品与发酵工业,2023,49(5):124-133.
[10] 石黎琳,牟方婷,李安,等. 基于高通量测序技术分析腐乳自然发酵过程微生物多样性[J] .中国酿造,2021,40(2):144-149.
[11] 刘敏,林佳卫,焦昱玮,等. 基于高通量测序技术分析蒙古族传统奶酪微生物菌群多样性[J] .中国酿造,2024,43(3):116-120.
[12] LI X F,LI C,YE H,et al.Changes in the microbial communities in vacuum-packaged smoked bacon during storage[J] .Food Microbiol,2019,77:26-37.
[13] 马上超,程超,田成,等. 基于高通量测序技术分析恩施州淡豆豉的细菌多样性[J] .食品科学,2022,43(10):156-161.
[14] 马岩石,姜明,李慧,等. 基于高通量测序技术分析东北豆酱的微生物多样性[J] .食品工业科技,2020,41(12):100-105.
[15] CHEN C, LI J M, AHMED Z, et al. Dynamic interplay between core functional microbial succession and flavor metabolite formation in naturally fermented sufu:A multi-omics perspective[J] .Food Biosci,2025,71:107094.
[16] 付瑞敏,刘春雷,徐良,等. 基于高通量测序技术的不同产地腐乳微生物多样性分析[J] .食品工业科技,2023,44(2):134-142.
[17] NSHIMYIMANA J P,FREEDMAN A J E,SHANAHAN P,et al.Variation of bacterial communities with water quality in an urban tropical catchment[J] .Environ Sci Technol,2017,51(10):5591-5601.
[18] 石聪,李世瑞,李跑,等.基于高通量测序浏阳豆豉不同发酵阶段微生物多样性分析[J] .食品与发酵工业,2018,44(2):27-32,39.
[19] 兰林,段树华,汪晟羽,等. 基于高通量测序技术分析豆腐乳中微生物多样性[J] .中国酿造,2023,42(1):31-36.
[20] 陶康,吴凌伟,金晓芳,等. 基于高通量基因测序分析腐乳微生物多样性[J] .食品科学,2021,42(8):143-149.
[21] LIU N,PAN J H,MIAO S,et al.Microbial community in Chinese traditional fermented acid rice soup (rice-acid) and its correlations with key organic acids and volatile compounds[J] .Food Res Int,2020,137:109672.
[22] ZHOU X Y,GUO T,HADIATULLAH H, et al. Metabolic behavior of Aspergillus oryzae in salt-reduced soy sauce and its regulation for the brewing process[J] . Food Biosci,2024,59:104206.
[23] LI Z M,BAI Z H,WANG D L,et al.Cultivable bacterial diversity and amylase production in three typical Daqus of Chinese spirits[J] . Int J Food Sci Technol,2014,49(3):776-786.
[24] 庞春霞,李艺,虞任莹,等.基于Illumina Miseq技术比较不同地区传统发酵大豆制品细菌多样性[J] .食品工业科技,2022,43(8):133-140.
[25] 曾玲,金清.PCR-DGGE 技术分析韩式大酱与中式大酱中微生物多样性[J] .食品与发酵工业,2023,49(5):269-274.
[26] HE G Q, HUANG J, ZHOU R Q, et al. Effect of fortified Daqu on the microbial community and flavor in Chinese strong-flavor liquor brewing process[J] .Front Microbiol,2019,10:56.
[27] 崔玉琦,王雅炜,武瑞霞,等. 酵母菌在发酵乳制品中的应用研究[J] .食品科技,2014,39(10):53-56.
[28] 刘亚男,张龑,吴江超,等.新疆伊犁地区民族传统谷物发酵饮料的微生物多样性及功能预测[J] .食品与发酵工业,2025,51(7):150-158.