李子为蔷薇科李亚属木本植物浆果[1],含糖、蛋白质、矿物质及维生素[2],具有降低血压、止咳、美容养颜、促进消化、清肺等功效[3]。 李子中还含有大量多酚类和黄酮类化合物等功能性活性成分[4],具有抗2,2'-联氮-双-3-乙基苯并噻唑啉-6-磺酸(2,2'-azino-bis(3-ethylbenzothiazoline-6-sulfonic acid),ABTS)自由基活性和抑制血管紧张素转换酶的作用[5]。 我国李子种植面积较大,产量位列世界第一[6]。 其中,脆红李口感爽脆,营养丰富,酚类物质含量高,具有较强的抗氧化作用[7],布朗李富含糖、酸、维生素及钙、磷、铁等多种营养物质,具有清热利尿等功效[8]。近年来,随着种植规模不断扩大,采收期集中、采后不耐贮、丰产不丰收等诸多问题,制约了产业的健康持续发展,因此,对李子进行精深加工,提高其附加价值极为迫切。
果酒是由鲜果经过破碎压榨后发酵得到的低度酒[9]。李子果酒富含许多营养成分及微生物转化合成产生的各种风味物质[10],其酒精和糖含量低,兼具保健酒和饮料酒的双重作用[11]。李子果酒研究主要集中在挥发性成分分析、发酵工艺和澄清技术等方面[12-15]。近年来,随着代谢组学技术的发展,对果酒发酵过程中代谢物变化的研究逐渐深入。付勋等[16]分析了脆李果酒发酵过程中16种氨基酸的动态变化,发现除脯氨酸外,其余氨基酸在发酵前期(第2~3天)含量显著下降,之后趋于稳定,并通过主成分分析(principal component analysis,PCA)与聚类分析(cluster analysis,CA)揭示了不同发酵阶段氨基酸组成的差异性与相关性。而李子品种作为李子果酒发酵原料,与发酵过程紧密相关,其果酒差异代谢物以及代谢通路研究鲜见报道。
本研究以2个李子品种(脆红李、布朗李)为原料制备李子果酒,采用气相色谱-质谱联用(gas chromatography-mass spectrometry,GC-MS)技术对李子果酒发酵过程中的挥发性风味成分进行分析,结合变量重要性投影(variable importance in projection,VIP)值、t检验P值及差异倍数(fold change,FC)值筛选显著差异代谢物,并通过京都基因与基因组百科全书(Kyoto Encyclopedia of Genes and Genomes,KEGG)数据库富集其相关代谢通路。以期分析不同品种李子果酒代谢物差异,为李子果酒独特风味的形成机理解析及产品质量控制提供数据支撑。
1 材料与方法
1.1 材料与试剂
脆红李(CHL)、布朗李(BLL)、白砂糖:泸州市售;果酒酒曲:四川省今酿酿酒有限责任公司;甲醇、乙腈、甲酸(均为色谱纯):美国Thermo Fisher Scientific公司;正己烷、双(三甲基硅烷)三氟乙酰胺(含1%三甲基氯硅烷)(均为色谱纯):德国CNW Technologies GmbH公司;N,O-双(三甲基硅基)三氟乙酰胺(N,O-bis(trimethylsilyl)trifluoroacetamide,BSTFA):梯希爱(上海)化成工业发展有限公司;O-甲基羟胺盐酸盐(纯度为97%):上海麦克林生化科技股份有限公司;吡啶(色谱级):阿拉丁试剂(上海)有限公司。
1.2 仪器与设备
Agilent 9000GC/5977B MSD气相色谱-质谱联用仪、DB-5MS毛细管色谱柱(30 m×0.25 mm×0.25 μm):美国安捷伦公司;F-060SD超声波清洗机:深圳福洋科技集团有限公司;LNG-T98冷冻浓缩离心干燥器:太仓市华美生化仪器厂;Scientz-10N冷冻干燥机:宁波新芝生物科技股份有限公司;TGL-16MS高速冷冻离心机:上海卢湘仪仪器有限公司;THZ-82气浴恒温振荡器:上海力辰邦西仪器科技有限公司;DZF-6021真空干燥箱:上海慧泰有限公司;50 L发酵罐:靓美厨具有限公司。
1.3 方法
1.3.1 李子果酒加工工艺流程及操作要点
操作要点:
原料预处理:选择新鲜、饱满、无病虫害的李子,清洗后去核破碎、打浆,将20 kg李子果浆放入50 L的发酵罐。
调整糖度:向脆红李和布朗李中分别加入白砂糖,将糖度调整至24°Brix。
发酵:将原料质量0.6%的果酒酒曲(35 ℃温水活化10 min)添加至李子果浆中,于23 ℃发酵16 d,糖度不再变化时发酵结束。
过滤:发酵液经过4层纱布过滤后即得李子果酒成品。
1.3.2 代谢物分析
采用GC-MS衍生化方法测定李子果酒样品中的代谢物。
样品前处理:取500 μL样品离心(12 000 r/min、10 min),通过0.22 μm的有机相滤膜过滤,取50 μL滤液转移至衍生瓶中,利用离心浓缩干燥器挥干后加入80 μL质量浓度为15 mg/mL的甲氧胺盐酸盐吡啶溶液,在37 ℃条件下振荡反应60 min,完成肟化过程。加入50 μL BSTFA和20 μL正己烷,在70 ℃条件下反应60 min。 反应结束后,将样品在室温下静置30 min,随后进行GC-MS分析。质控样本(quality control,QC)则通过将各样品提取液等体积混合制备而成。
GC条件:采用DB-5MS毛细管色谱柱(30 m×0.25 mm×0.25 μm),载气为高纯氦气(He)(纯度≥99.999%),流速1.0 mL/min,进样口温度260 ℃,进样量1 μL,采用不分流模式,溶剂延迟时间5 min。升温程序设置为初始温度60 ℃维持0.5 min;以8 ℃/min的速率升温至125 ℃,再以相同速率升温至210 ℃;以15 ℃/min的速率升温至270 ℃;以20 ℃/min的速率升温至305 ℃,并保持5 min。
MS条件:采用电子电离(electron ionization,EI)源,离子源温度为230 ℃,四极杆温度为150 ℃。电离能量70 eV,扫描模式采用全扫描(SCAN),质量扫描范围为50~500 m/z。
定性定量分析:使用MS-DIALv4.24软件处理质谱数据,结合美国国家标准技术研究所(national institute of standards and technology,NIST)数据库进行代谢物分析,根据保留时间(retention time,RT)匹配度得分和化合物碎片匹配度得分进行定性分析。以匹配度得分≥90分(满分100分)为标准筛选有效代谢物。
1.3.3 数据处理
使用R语言(3.6.1版本)进行主成分分析(PCA)和正交偏最小二乘法-判别分析(orthogonal partial least squaresdiscriminant analysis,OPLS-DA)及层次聚类分析(hierar chical clustering analysis,HCA)。显著差异代谢物的筛选条件为:VIP值>1;t检验显著性P值<0.05;FC值>2或<0.5。利用KEGG数据库对显著差异代谢物进行通路富集分析[18]。
2 结果与分析
2.1 李子果酒发酵过程中代谢物分析
从两种李子果酒发酵样品中共鉴定出436种代谢物,筛选出144种有效代谢物。 李子果酒发酵过程中的代谢物分类及占比见图1。 由图1可知,一级分类中有机氧化合物(48种)(33.33%)、有机酸和衍生物(37种)(25.69%)、脂类和类脂分子(18种)(12.50%)占比较高;二级分类中有机氧化合物(48种)(33.33%)、羧酸及其衍生物(25种)(17.36%)和脂肪酰基(11种)(7.64%)占比较高;三级分类中碳水化合物(41种)(28.47%),氨基酸、多肽及类似物(20种)(13.89%)以及脂肪酸和缀合物(7种)(6.25%)占比较高。李子果酒中检出的大量脂肪酸、氨基酸、多肽以及糖类物质,为关键的呈香呈味成分[17],影响酸、甜、苦、咸、鲜、厚等6种基本滋味特性[18],对产品的品质具有重要影响。脂肪在发酵过程中可以转化为高级脂肪酸,为酒体增加独特香气,蛋白质分解为氨基酸后,经过氧化、还原、酯化,会分别形成醇类、酸类、酯类[19],增加酒体香气。研究表明,通过富集酒醅馏分中的多肽,能够有效调整白酒风味成分的构成。这些多肽物质与乙酸、己酸乙酯等关键风味成分之间可形成氢键,进而抑制其挥发行为,最终对白酒的整体风味特性产生显著影响[20]。
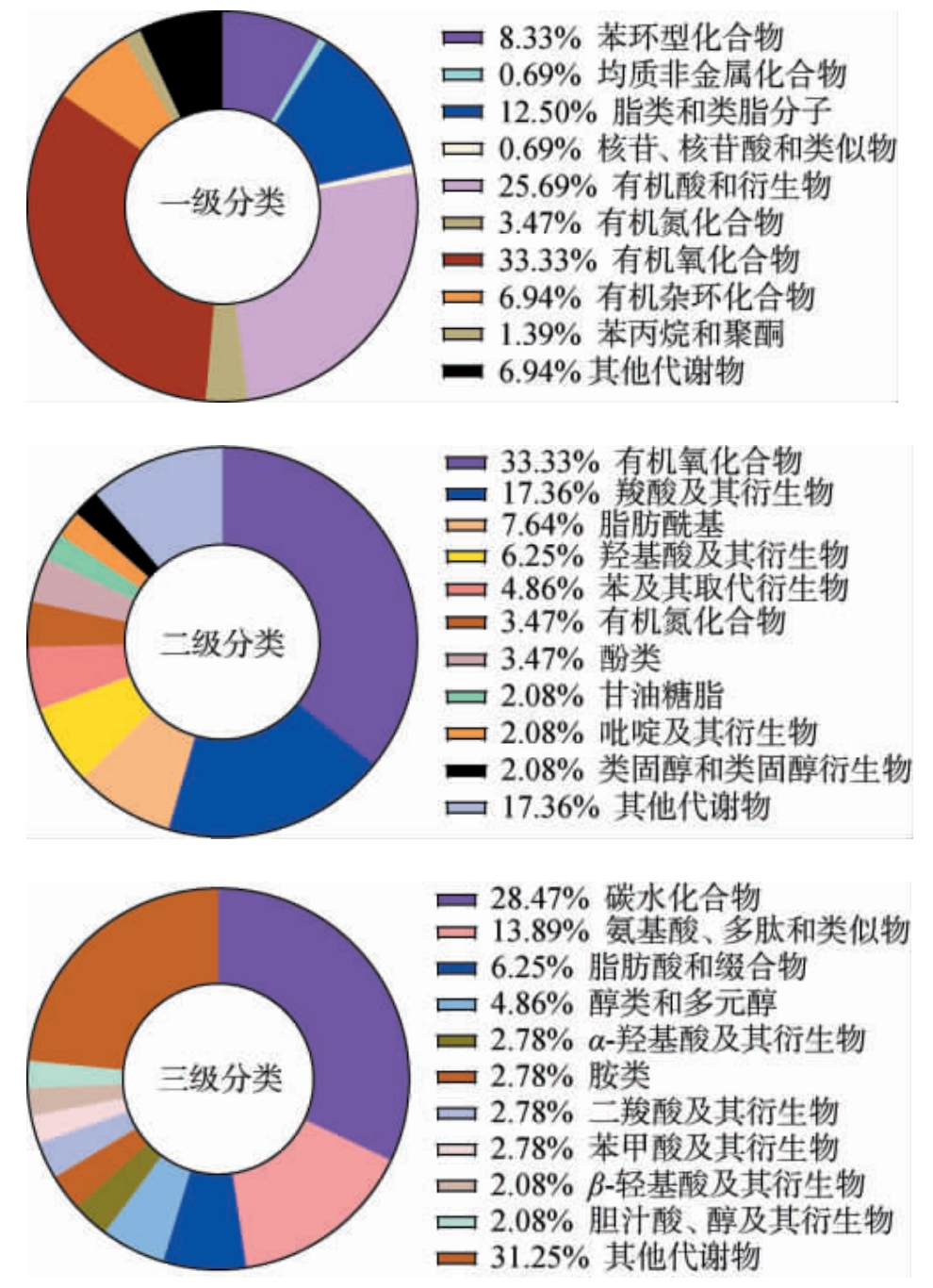
图1 李子果酒发酵过程中的代谢物分类及占比
Fig. 1 Classification and proportion of metabolites during the fermentation process of plum wine
2.2 李子果酒发酵过程中的代谢物分析
李子果酒发酵过程中代谢物的主成分分析散点图、正交偏最小二乘-判别分析得分图及200次置换检验结果见图2。由图2a可知,脆红李与布朗李果酒发酵过程中的代谢物,能明显区分开,说明两个品种李子果酒发酵过程中的代谢物质存在差异,同时QC样本集中在一起,说明仪器在整个检测过程中稳定性较好,采集的数据质量较好,可以用于后续分析。由图2b可知,脆红李和布朗李果酒发酵过程中的代谢物样本区分较明显,与PCA结果一致。由图2c可知,2个品种李子果酒样品发酵过程中代谢物的R2Y为0.991,Q2为0.965,Q2点的回归线与纵轴的相交点小于0,说明模型对数据不存在过拟合,模型验证有效。
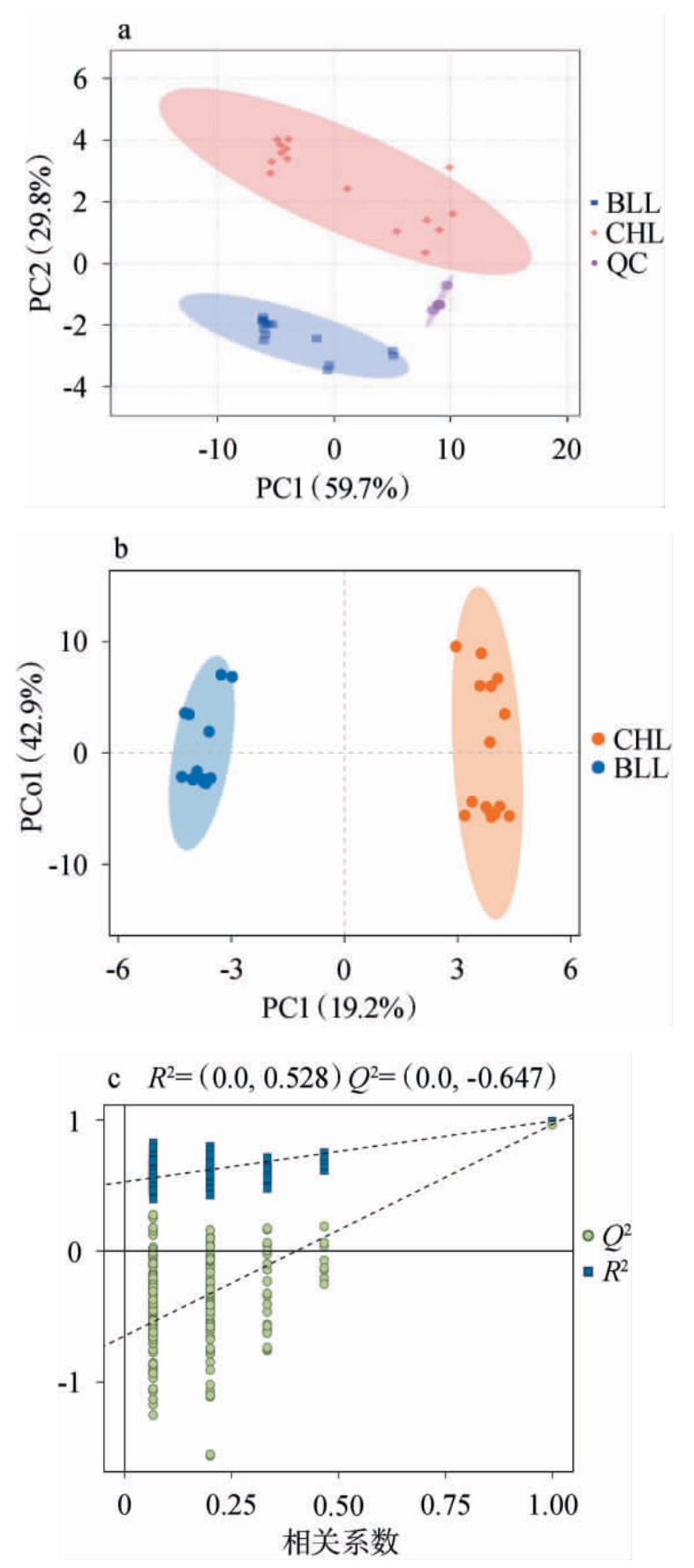
图2 李子果酒发酵过程中代谢物的主成分分析散点图(a)、正交偏最小二乘-判别分析得分图(b)及200次置换检验结果(c)
Fig. 2 Scatter plot of principal component analysis of metabolites (a),score plot of orthogonal partial least squares-discriminant analysis (b), and 200 permutation test results (c) during the fermentation process of plum wine
2.3 李子果酒发酵过程中的显著差异代谢物质筛选
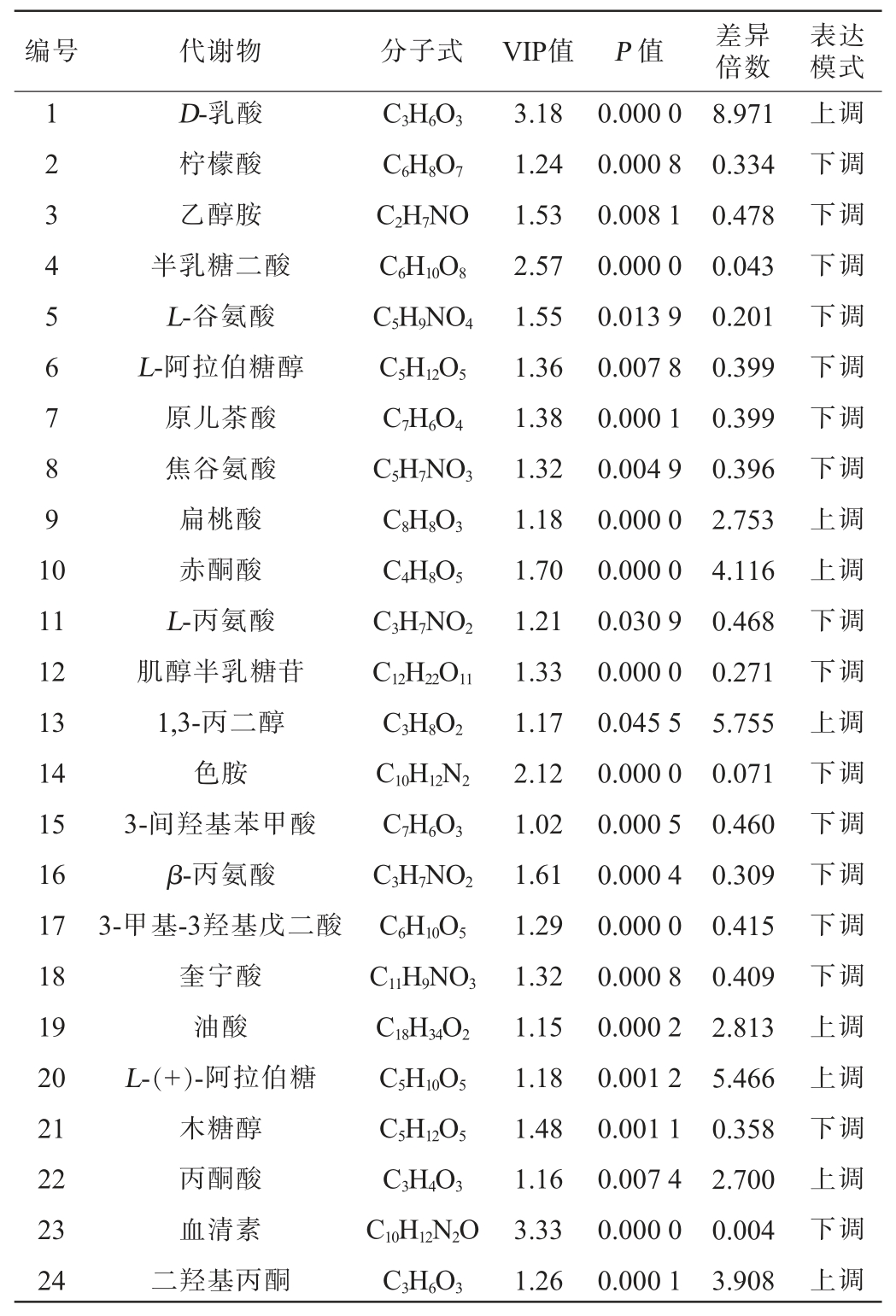
李子果酒发酵过程中显著差异代谢物火山图见图3,显著差异代谢物鉴定结果见表1。由图3及表1可知,两种李子果酒发酵的显著差异代谢物共35个(VIP值>1,t检验P值<0.05,FC>2或<0.5)。其中,L-(+)-阿拉伯糖、D-乳酸、脯氨酸等15个差异代谢物在脆红李果酒发酵过程中上调表达;柠檬酸、甘油磷酸酯、原儿茶酸等20个差异代谢物下调表达。
表1 李子果酒发酵过程中的显著差异代谢物鉴定结果
Table 1 Identification results of significantly differential metabolites during the fermentation process of plum wine
编号代谢物分子式 VIP值 P 值差异倍数表达模式1234567891 0 C3H6O3 C6H8O7 11 12 13 14 15 16 17 18 19 20 21 22 23 24 D-乳酸柠檬酸乙醇胺半乳糖二酸L-谷氨酸L-阿拉伯糖醇原儿茶酸焦谷氨酸扁桃酸赤酮酸L-丙氨酸肌醇半乳糖苷1,3-丙二醇色胺3-间羟基苯甲酸β-丙氨酸3-甲基-3羟基戊二酸奎宁酸油酸L-(+)-阿拉伯糖木糖醇丙酮酸血清素二羟基丙酮C2H7NO C6H10O8 C5H9NO4 C5H12O5 C7H6O4 C5H7NO3 C8H8O3 C4H8O5 C3H7NO2 C12H22O11 C3H8O2 C10H12N2 C7H6O3 C3H7NO2 C6H10O5 C11H9NO3 C18H34O2 C5H10O5 C5H12O5 C3H4O3 C10H12N2O C3H6O3 3.18 1.24 1.53 2.57 1.55 1.36 1.38 1.32 1.18 1.70 1.21 1.33 1.17 2.12 1.02 1.61 1.29 1.32 1.15 1.18 1.48 1.16 3.33 1.26 0.000 0 0.000 8 0.008 1 0.000 0 0.013 9 0.007 8 0.000 1 0.004 9 0.000 0 0.000 0 0.030 9 0.000 0 0.045 5 0.000 0 0.000 5 0.000 4 0.000 0 0.000 8 0.000 2 0.001 2 0.001 1 0.007 4 0.000 0 0.000 1 8.971 0.334 0.478 0.043 0.201 0.399 0.399 0.396 2.753 4.116 0.468 0.271 5.755 0.071 0.460 0.309 0.415 0.409 2.813 5.466 0.358 2.700 0.004 3.908上调下调下调下调下调下调下调下调上调上调下调下调上调下调下调下调下调下调上调上调下调上调下调上调
续表
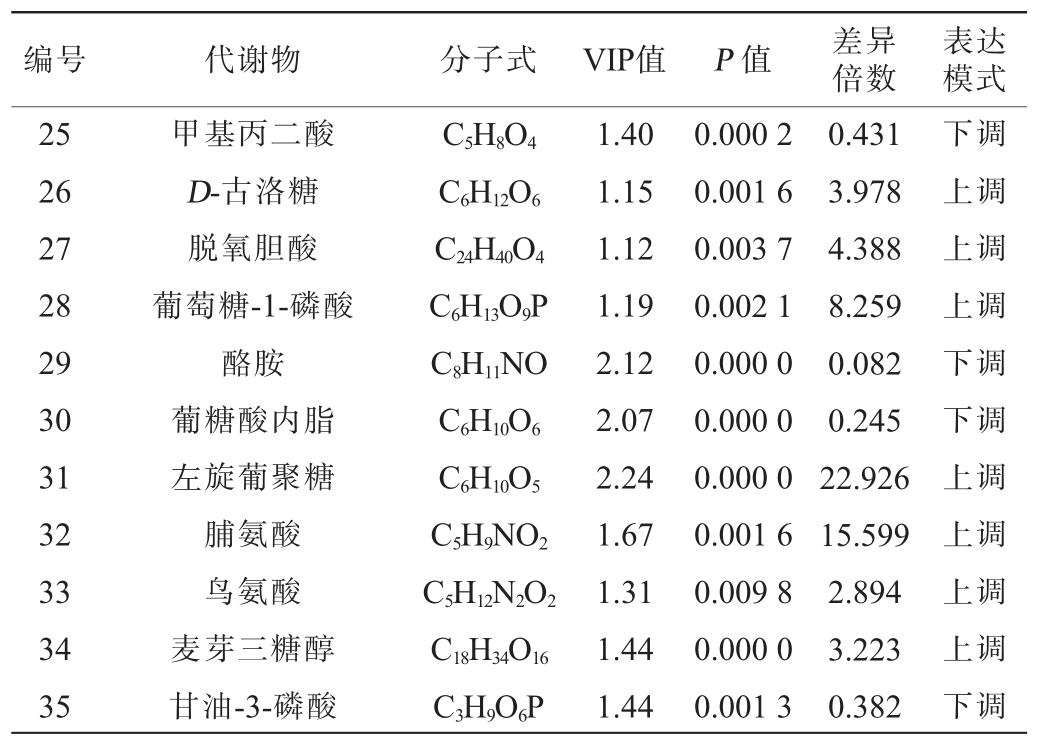
编号代谢物分子式 VIP值 P 值差异倍数表达模式25 26 27 28 29 30 31 32 33 34 35甲基丙二酸D-古洛糖脱氧胆酸葡萄糖-1-磷酸酪胺葡糖酸内脂左旋葡聚糖脯氨酸鸟氨酸麦芽三糖醇甘油-3-磷酸C5H8O4 C6H12O6 C24H40O4 C6H13O9P C8H11NO C6H10O6 C6H10O5 C5H9NO2 C5H12N2O2 C18H34O16 C3H9O6P 1.40 1.15 1.12 1.19 2.12 2.07 2.24 1.67 1.31 1.44 1.44 0.000 2 0.001 6 0.003 7 0.002 1 0.000 0 0.000 0 0.000 0 0.001 6 0.009 8 0.000 0 0.001 3 0.431 3.978 4.388 8.259 0.082 0.245 22.926 15.599 2.894 3.223 0.382下调上调上调上调下调下调上调上调上调上调下调
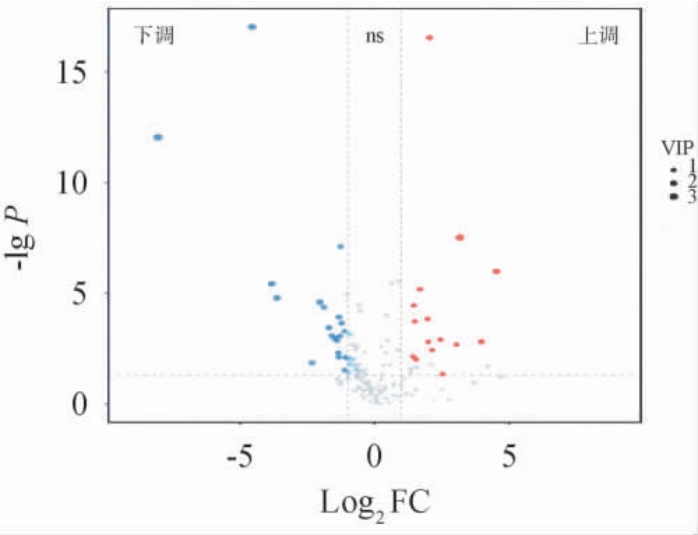
图3 李子果酒发酵过程中显著差异代谢物火山图
Fig. 3 Volcanic diagram of significantly differential metabolites during the fermentation process of plum wine
将脆红李和布朗李果酒发酵过程中的差异代谢物进行层次聚类分析(见图4)。由图4可知,脯氨酸、鸟氨酸等氨基酸及其衍生物在布朗李果酒发酵过程中相对含量高于脆红李子果酒,氨基酸是酒体中关键的呈味物质。研究表明,作为香气前体物质,氨基酸能够与还原糖发生美拉德反应,生成呋喃类衍生物、吡嗪类衍生物以及吡咯类衍生物等重要风味物质[21],这些物质对酒体的风味特征具有显著影响。半乳糖二酸、甲基丙二酸等有机酸在布朗李子果酒发酵过程中的相对含量高于脆红李,这些有机酸大部分是在酿酒发酵中产生的[22],可以调节酒体的香气结构,对李子果酒的风味起到积极作用[23],使酒体具有丰满度和酸爽感。而柠檬酸、丙酮酸等有机酸在脆红李发酵过程中相对含量高于布朗李,是风味物质转化过程中的重要中间产物[24]。此外,酪胺、乙醇胺、色胺等对人体有一定健康风险的代谢物质[25-27]在布朗李子果酒发酵过程中的相对含量也高于脆红李。
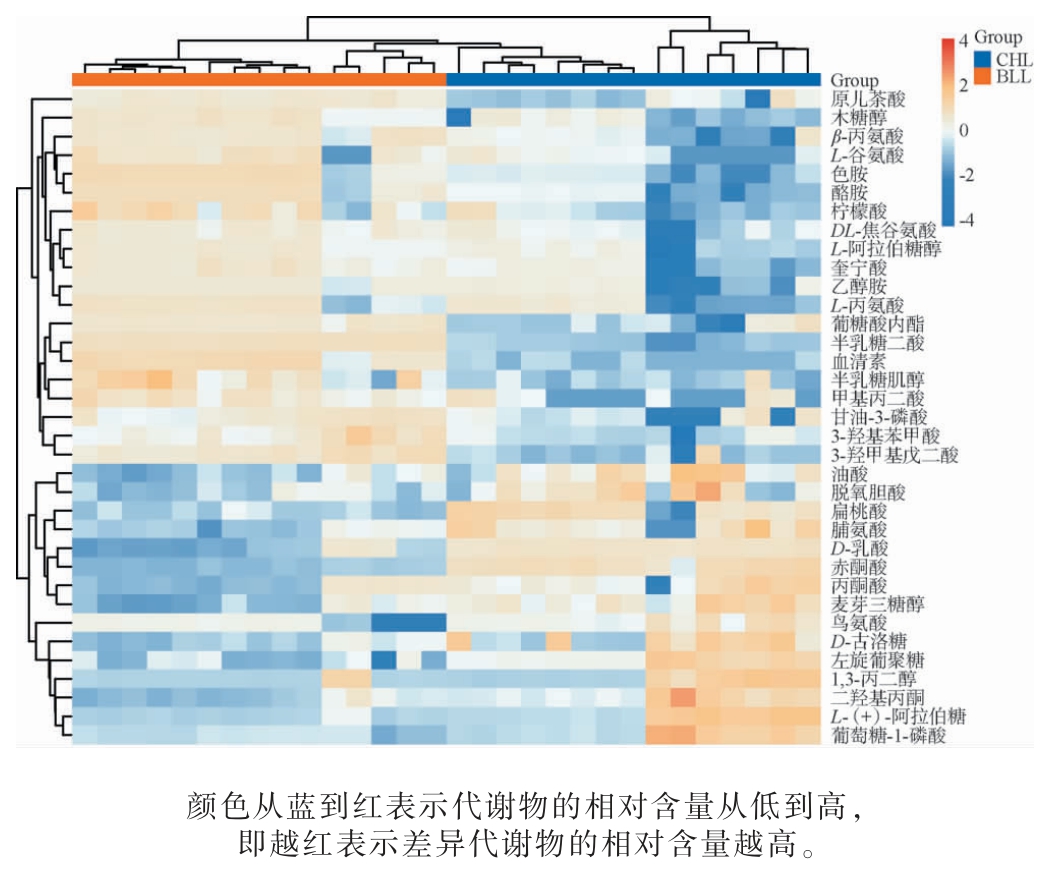
图4 李子果酒发酵过程中的差异代谢物的层次聚类分析热图
Fig. 4 Heat map of hierarchical clustering analysis of differential metabolites during the fermentation process of plum wine
选取上调及下调VIP值最大的10个差异代谢物进行火柴杆图分析,结果见图5。由图5可知,脆红李果酒发酵过程中左旋葡聚糖相对含量是布朗李的22.93倍,脯氨酸相对含量是布朗李的10.5倍,D-乳酸相对含量是布朗李的8.97倍;布朗李果酒发酵过程中半乳糖二酸相对含量是脆红李的23.26倍,L-谷氨酸相对含量是脆红李的4.98倍,葡糖酸内酯相对含量是脆红李的4.08倍。
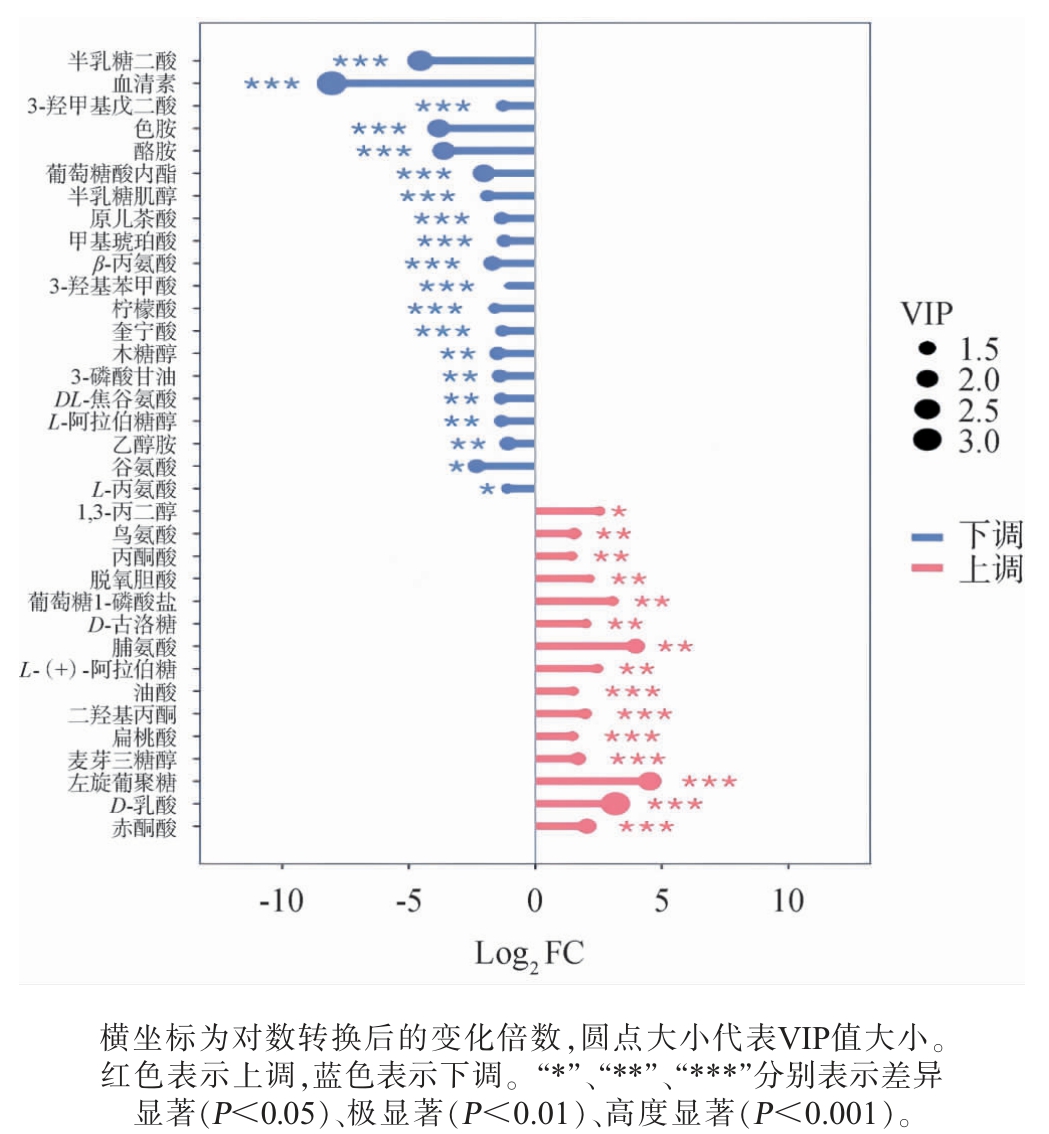
图5 李子果酒发酵过程中的显著差异代谢物的火柴杆图
Fig. 5 Matchstick plot of significantly differential metabolites during the fermentation process of plum wine
2.4 李子果酒发酵过程中的主要显著差异代谢物的定量分析
选取脆红李和布朗李果酒发酵过程中FC值>8的代谢物进行分析,结果见图6。 由图6可知,脆红李、布朗李果酒发酵过程中主要显著差异代谢物峰面积具有显著差异。D-乳酸在脆红李果酒发酵过程中的峰面积比较稳定,而在布朗李果酒发酵过程中的峰面积先上升后下降,第3天时达到最高值(86.96×104);葡萄糖-1-磷酸在脆红李果酒发酵过程中峰面积先上升后下降,在第3天时达到最高值(357.34×104),而在布朗李果酒发酵过程中峰面积先下降后上升,第3天时最低(8.56×104);左旋葡聚糖在脆红李果酒中的峰面积先上升后下降,之后趋于平稳,发酵结束时为291.14×104,而在布朗李果酒发酵过程中的峰面积整体呈先上升后平稳的趋势,发酵结束时为44.52×104;脯氨酸在脆红李和布朗李果酒发酵过程中的峰面积均呈先上升后下降再上升的趋势。D-乳酸、葡萄糖-1-磷酸、左旋葡聚糖和脯氨酸在脆红李果酒中的峰面积均显著高于布朗李果酒(P<0.05)。 其中,乳酸是酒体中的四大有机酸之一,具有一定的抑菌功能,有利于乙醇发酵的进行[28];可矫正和稳定酒体香气,减轻苦涩味和糙辣感,使酒质浓厚并带有回甜味[29]。 乳酸主要来源于发酵过程,原料经糖化产生的糖类被乳酸菌利用,在菌体内经糖酵解生成丙酮酸[30],再经乳酸脱氢酶作用后生成[31]。 脯氨酸是人体内合成蛋白质的18种氨基酸之一,为促进生长、新陈代谢、维持生命提供了物质基础[32]。 在果酒发酵过程中,脯氨酸参与一系列生化反应,并且可以为微生物生长代谢提供生存的氮源,影响着微生物的生长情况和代谢物的产生[33]。因此,李子品种对果酒发酵代谢物的含量具有一定影响。
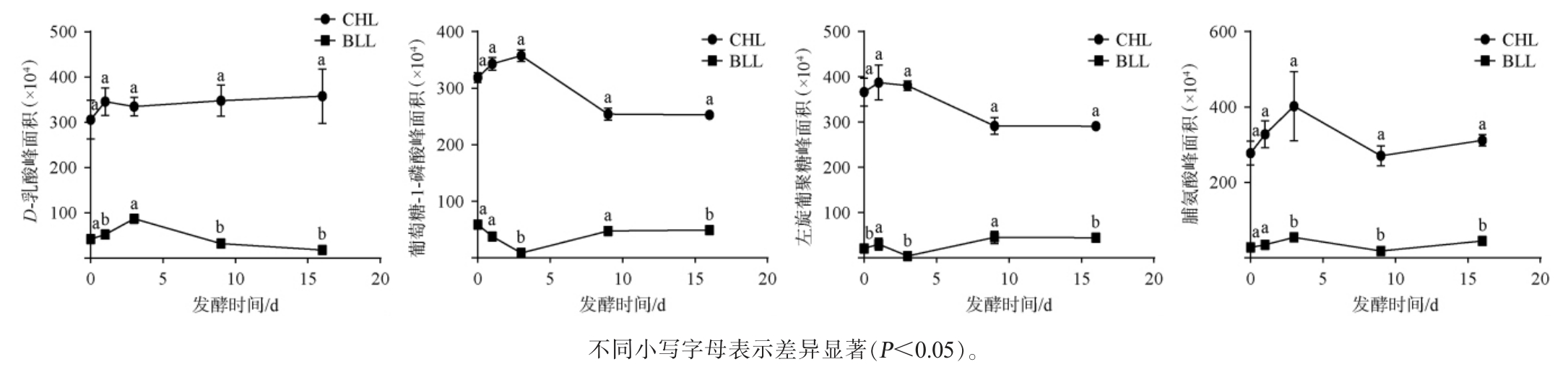
图6 李子果酒发酵过程中主要显著差异代谢物峰面积变化趋势
Fig. 6 Changing trend of the peak area of the mainly significantly differential metabolites during the fermentation process of plum wine
2.5 李子果酒发酵过程中显著差异代谢物的KEGG富集分析
KEGG数据功能架构主要划分为:新陈代谢、基因信息处理、环境信息处理、细胞过程、有机体系统、人类疾病以及药物开发[34]。 其中,新陈代谢与酒体发酵存在显著关联[35]。 利用KEGG数据库对李子果酒差异表达的代谢物进行注释,并进行代谢通路的富集分析,结果见图7。 由图7可知,脆红李和布朗李果酒发酵过程中的显著差异代谢物被注释到31条代谢通路中,显著差异代谢物在丁酸代谢、磷酸戊糖途径、戊糖和葡萄糖醛酸相互转化、天冬氨酸和谷氨酸代谢、ABC转运蛋白等20条代谢通路中显著富集(P<0.05)。研究表明,不饱和脂肪酸和脂肪酸的生物合成在短链及长链脂肪酸的合成与分解过程中发挥关键作用。丁酸通过代谢生成,既可作为丁酸乙酯的前体物质,也可进一步转化为己酸[36]。 此外,脂肪酸(如己酸、乙酸、丁酸、油酸、亚油酸等)及其酯化产物脂肪酸乙酯是白酒中重要的风味成分,对白酒的香气和口感具有显著影响[37]。甘氨酸、丝氨酸、脯氨酸、谷氨酸代谢等氨基酸代谢,苯丙氨酸、酪氨酸和色氨酸生物合成及甘油磷脂代谢等途径,也是酒体风味化合物的潜在生成途径[38]。因此,不同李子品种可影响李子果酒发酵过程中差异代谢物代谢通路,进而影响李子果酒的风味。
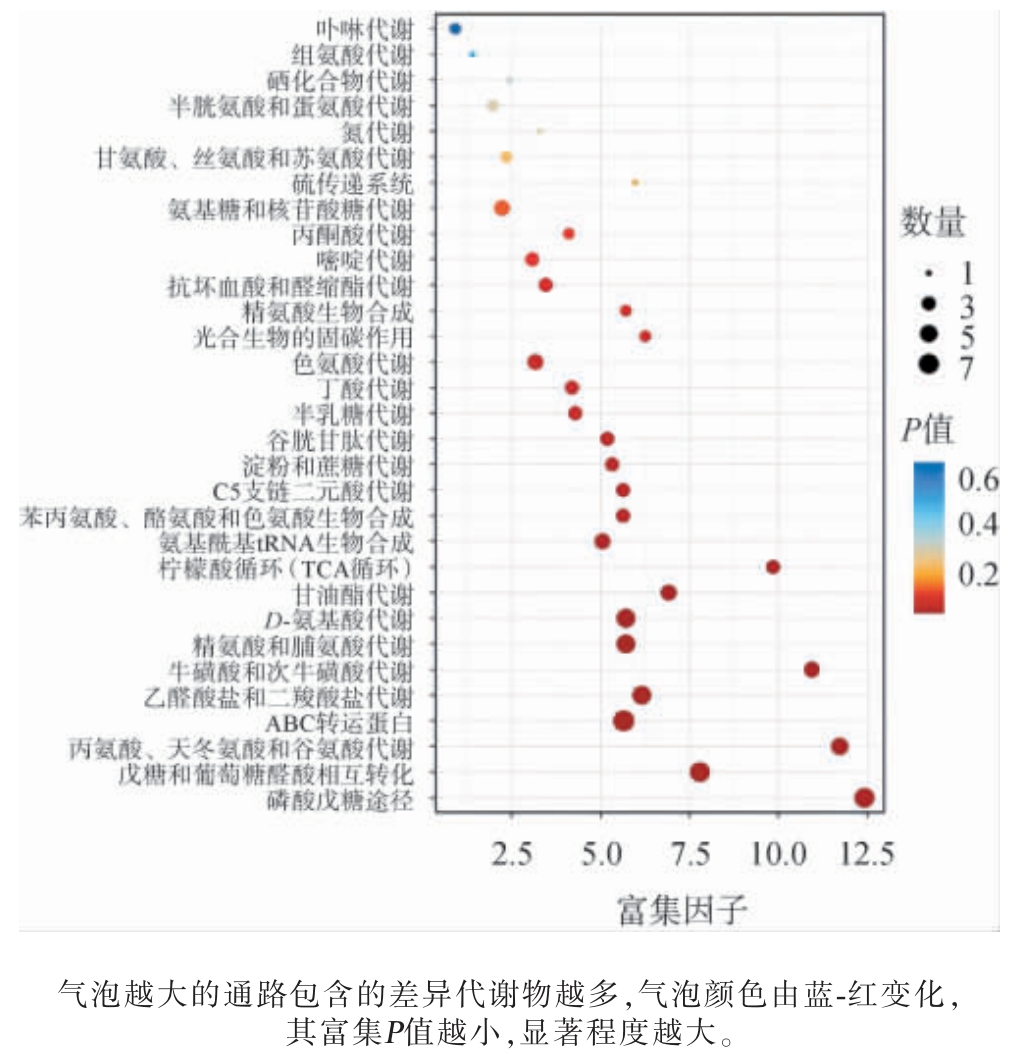
图7 李子果酒发酵过程中差异代谢物的京都基因与基因组百科全书富集通路
Fig. 7 Kyoto Encyclopedia of Genes and Genomes enrichment pathway of differential metabolites during the fermentation process of plum wine
3 结论
本研究采用GC-MS技术分析脆红李和布朗李果酒发酵过程中的代谢物差异,通过变量重要性投影(VIP)值、t检验P值及差异倍数(FC)值筛选出35种显著差异代谢物(VIP值>1,P<0.05,FC值>2或<0.5)。其中,L-(+)-阿拉伯糖等15种显著差异代谢物在脆红李果酒发酵过程中上调表达,而柠檬酸等20种显著差异代谢物下调表达。 脆红李果酒发酵过程中D-乳酸、葡萄糖-1-磷酸、左旋葡聚糖和脯氨酸峰面积较高。 KEGG富集分析结果表明,显著差异代谢物富集到丁酸代谢、D-氨基酸代谢、甘油酯代谢、谷氨酸代谢等影响酒体风味物质生成的代谢通路,影响果酒的风味特征。 本研究解析了不同品种李子果酒代谢物差异,可为优质李子果酒的原料选育与风味提升提供理论依据与实践指导。
[1] YU J,LI W,YOU B,et al.Phenolic profiles,bioaccessibility and antioxidant activity of plum(Prunus Salicina Lindl.)[J] .Food Res Int,2021,143(9):110300.
[2] 成策,陆俊,韩文琪,等. 李子果粒果汁饮料加工工艺研究[J] . 食品与机械,2015,31(6):215-218.
[3] 刘永衡,蔡倩,吴桂君.幸运李子果酒香气成分分析[J] .中国酿造,2015,34(10):138-141.
[4] NAN X, CHANG X X, QIN L W, et al. Insights into tissue-specific anthocyanin accumulation in Japanese plum (Prunus salicina L.) fruits:a comparative study of three cultivars[J] .Food Chem,2023,7:100178.
[5] GONZÁLEZ-GARCÍA E,MARINA M L,GARCÍA M C. Plum (Prunus Domestica L.) by-product as a new and cheap source of bioactive peptides:Extraction method and peptides characterization[J] .J Funct Foods,2014,11:428-437.
[6] 余德亿,黄鹏,方大琳,等. 李子贮藏保鲜技术及其应用前景[J] . 中国食物与营养,2011,17(9):51-55.
[7] 张曼,钟涛,魏雪,等. 不同非酿酒酵母与酿酒酵母混合发酵对脆红李酒品质的影响[J] .食品与发酵工业,2021,47(12):110-116.
[8] 胡云峰,庞权,阎瑞香,等. 布朗李果酒发酵工艺研究[J] . 包装工程,2019,40(9):43-47.
[9] 章雪玲,杨茜,杨敏,等. 固定化酵母酿造百香果玫瑰茄复合果酒发酵工艺优化[J] .中国酿造,2025,44(4):213-220.
[10] 梁艳玲,陈麒,伍彦华,等. 果酒的研究与开发现状[J] . 中国酿造,2020,39(12):5-9.
[11] 赵驰,朱永清,董玲,等. 李子果酒主发酵过程中理化指标及挥发性成分变化分析[J] .中国酿造,2019,38(9):65-68.
[12] LIU G M,SUN J,HE X M,et al.Fermentation process optimization and chemical constituent analysis on longan(Dimocarpus longan lour.)winescience direct[J] .Food Chem,2018,256:268-279.
[13] VENTER A,JOUBERT E,BEER D D.Nutraceutical value of yellow-and red-fleshed South African plums(Prunus salicina Lindl.):Evaluation of total antioxidant capacity and phenolic composition[J] .Molecules,2014,19(3):3084-3109.
[14] LIN Z X, LI B B, LIAO M W, et al. The physicochemical attributes,volatile compounds, and antioxidant activities of five plum cultivars in Sichuan[J] .Foods,2023,12(20):3801.
[15] 邢玉青,石飞,王君. 复合澄清剂对李子酒澄清效果的研究[J] . 中国酿造,2021,40(1):188-191.
[16] 付勋,聂青玉,王强,等. 脆李果酒发酵过程氨基酸差异分析[J] . 农产品加工,2024(15):19-22,26.
[17] 周艳,陈雅,廖茂雯,等.不同品种李子品质特性及其酿酒适宜性评价[J] .食品工业科技,2024,45(24):272-282.
[18] 覃芳丽,邹宇晓,王思远,等.发酵食品的滋味特性及其形成机制研究进展[J] .食品与发酵工业,2024,50(10):388-396.
[19] 史琳铭,杜艳红,聂建光,等.不同品种高粱理化品质与清茬大曲白酒风味品质的相关性研究[J] .食品工业科技,2025,46(2):231-238.
[20] 赵云浩,黄晓丹,王珺,等.酒醅与酱渣混蒸馏分中的多肽鉴定及风味成分分析[J] .食品与发酵工业,2024,50(11):55-61.
[21] 尹艳艳,杨军林,田栋伟,等. 超高效液相色谱-高分辨质谱法同时测定白酒中19种氨基酸[J] .分析测试学报,2023,42(3):330-336.
[22] 骆茂香,徐兴江,陈仁远,等. 不同工艺酱香型白酒中非挥发性有机酸及酚酸的差异分析[J] .酿酒科技,2024(7):17-24,42.
[23] 李时芬,张志伟,李茜,等. 易造成亚硝胺风险的乙醇胺等4类原料的安全使用[J] .香料香精化妆品,2024(4):69-74,192.
[24] 樊科权,周利,莫凯,等. 剑南春酒曲风味物质解析[J] . 酿酒,2025,52(5):85-89.
[25] LIU G M, WEI P, TANG Y, et al. Evaluation of bioactive compounds and bioactivities in plum (Prunus salicina Lindl.) wine[J] . Front Nutr,2021,8:766415.
[26] 戴卓凡,张玉华,马元辰,等. 氮掺杂生物质碳点荧光探针的构建及对发酵食品中酪胺的检测[J/OL] . 中国食品学报,1-10[2025-01-22] .http://kns.cnki.net/kcms/detail/11.4528.ts.20240808.1534.004.html.
[27] 刘慧,李蒙.超高效液相色谱-串联质谱测定巧克力中7种色胺类精神活性物质[J] .食品安全导刊,2024(14):84-88.
[28] 孙超,刘勇.白酒生产中乳酸菌的分布及主要代谢产物[J] .中国酿造,2012,31(5):1-4.
[29] 张方,张宿义,苏占元,等. 有机酸对浓香型白酒品质及其酿造过程影响的研究进展[J] .酿酒科技,2016(1):94-97,102.
[30] 杨帆.酱香型白酒中乳酸代谢机理及调控策略的研究[D] .无锡:江南大学,2020.
[31] 杨荣,华进,周亚宾. 白酒酿造中两种手性乳酸产生机理及控制措施的研究进展[J] .中国酿造,2024,43(5):18-24.
[32] 彭鹏,刘鹏,卢静静,等. 抗坏血酸与脯氨酸的相互作用研究[J] . 化学研究,2018,29(4):350-356.
[33] 张巧玲,吕锡斌,秦兴,等.酱香型白酒高温大曲游离氨基酸比较分析[J] .中国酿造,2019,38(4):53-57.
[34] KANEHISA M,GOTO S,HATTORI M,et al.From genomics to chemical genomics:New developments in KEGG[J] .Nucleic Acids Res,2006,34(Suppl 1):D354-D357.
[35] LIU M K, LIU C Y, TIAN X H, et al. Bioremediation of degraded pit mud by indigenous microbes for Baijiu production[J] .Food Microbiol,2022,108:104096.
[36] LIU M K, TANG Y M, GUO X J, et al. Structural and functional changes in prokaryotic communities in artificial pit mud during Chinese Baijiu production[J] .mSystems,2020,5(2):e00829-19.
[37] XU Y Q,ZHAO J R,LIU X,et al.Flavor mystery of Chinese traditional fermented Baijiu:The great contribution of ester compounds[J] . Food Chem,2022,369:130920.
[38] 耿晓杰,陈尔豹,马志莹,等. 基于非靶向代谢组学技术解析老白干白酒发酵过程中的代谢物特征[J] . 食品科学技术学报,2024,42(4):45-60.