在全球化的现代饮食模式下,高脂饮食(high-fat diet,HFD)已成为现代饮食结构中的显著特征[1]。长期高脂饮食导致机体能量摄入与消耗失衡,进而引发一系列代谢紊乱问题,包括肥胖、高血脂、糖尿病以及非酒精性脂肪性肝病(non-alcoholic fatty liver disease,NAFLD)等[2]。肝脏作为机体代谢的核心器官,在脂质代谢、糖代谢及解毒过程中发挥关键作用[3]。然而,高脂饮食通过促进肝脏脂质堆积、氧化应激及炎症反应,显著干扰肝脏代谢稳态,最终导致肝细胞损伤及机体代谢功能紊乱[4]。高脂饮食不仅直接作用于肝脏代谢,还通过诱导肠道菌群失调、破坏肠道屏障功能及引发全身性炎症,多途径紊乱机体代谢稳态[5]。此类代谢紊乱一旦形成,可能引发不可逆的代谢紊乱和组织损伤,对机体健康造成深远且持久的负面影响。因此,寻找创新有效的方式来预防高脂饮食所致的慢性代谢性疾病的发生发展是目前全球关注的重点问题。
近年来,发酵食品因其在调节代谢紊乱方面的潜力而备受关注[6]。贵州红酸汤是贵州地区特有的传统发酵食品,其发酵过程中产生的有机酸、多酚、多肽及微生物代谢产物,赋予其独特的风味和潜在的生物活性[7]。 多项研究表明,红酸汤具有抗氧化、抗炎、调节肠道菌群及改善代谢紊乱等作用[8-10]。YANG H等[11-12]研究表明,贵州红酸汤对高脂饮食诱导的肥胖大鼠具有显著的代谢调节作用,可有效改善高脂饮食引起的脂质代谢紊乱,降低大鼠体质量和脂肪积聚,并改善循环系统中的脂质水平;同时,红酸汤还能减轻肠道炎症,提高肠道激素肽YY(peptide YY,PYY)和胰高血糖素样肽-1(glucagon-like peptide-1,GLP-1)的含量,增强肠道紧密连接蛋白闭合蛋白(occludin)和闭锁小带蛋白-1(zonula occludens-1,ZO-1)的表达,进而改善肠道菌群紊乱,恢复肠道屏障功能,最终改善高脂饮食大鼠脂质代谢紊乱。然而,目前贵州红酸汤对高脂饮食诱导的肝脏脂质代谢紊乱的具体影响及其分子机制尚未被系统研究。
蛋白组学是一种高通量的蛋白质鉴定和定量技术,可了解特定生理或病理条件下蛋白质表达的全局变化,揭示疾病机理或生物过程的调控[13]。因此,本研究采用贵州传统发酵食品红酸汤干预高脂饮食大鼠,运用基于串联质谱标签(tandem mass tag,TMT)的蛋白组学技术结合生物信息学分析,系统探究红酸汤干预对高脂饮食大鼠肝脏蛋白质组表达图谱的影响,揭示红酸汤对高脂饮食诱导的肝脏脂质代谢紊乱的调控机制,为红酸汤的保健功能开发提供科学依据,并为开发基于传统发酵食品的功能性干预策略奠定理论基础。
1 材料与方法
1.1 材料与试剂
1.1.1 实验动物及喂养饲料
无特定病原体(specific pathogen free,SPF)级雄性SD大鼠(6周龄,体质量(160±20)g,共30只):由贵州医科大学实验动物中心提供,许可证号为SCXK(辽)2020-0001。饲养管理均符合《实验动物事务》,已获得贵州医科大学实验动物伦理审查委员会批准(伦理审批号:NO.2100228)。普通饲料(包含粗蛋白、粗脂肪、粗纤维、粗灰分、粗水分、微量元素和氨基酸等;高脂饲料由78.8%基础饲料、1%胆固醇、10%蛋黄粉、10%猪油及0.2%胆盐组成):贵州医科大学动物实验中心。贵州红酸汤:明洋食品有限公司。
1.1.2 主要试剂
二喹啉甲酸(bicinchoninic acid,BCA)蛋白浓度测定试剂盒、肿瘤坏死因子α(tumor necrosis factor-alpha,TNF-α)检测试剂盒、白介素6(interleukin-6,IL-6)检测试剂盒:北京索莱宝科技有限公司;蛋白酶抑制剂:德国Merck Millipore公司;尿素、碘乙酰胺、三氯乙酸(trichloroacetic acid,TCA)、四乙基溴化铵(tetraethylammonium bromide,TEAB)、DL-二硫苏糖醇(DL-dithiothreitol,DTT)(均为分析纯):美国Sigma-Aldrich公司;丙酮(分析纯):杭州汉诺化工有限公司;TMT标记试剂盒、乙腈(色谱纯):美国Thermo Fisher Scientific;胰蛋白酶(≥10 000 U/mg):美国Promega公司;甲酸(分析纯):德国Fluka公司。
1.2 仪器与设备
TDL-5000bR低速台式离心机:上海安亭科学仪器厂;SCIENTA-ⅡD超声波细胞破碎仪:宁波新芝生物科技股份有限公司;Lx-20全自动生化分析仪:美国Beckman Coulter公司;Multiskan GO酶标仪、UltiMate 3000高效液相色谱(high performance liquid chromatography,HPLC)仪、EASYnLC 1200超高效液相色谱(ultra performance liquid chromatography,UPLC)仪、Q ExactiveTM HF-X质谱(mass spectrometry,MS)仪:美国Thermo Fisher Scientific公司;300Extend C18色谱柱(4.6 mm×250 mm×5 μm):美国Agilent公司;Strata X C18固相萃取柱(500 mg/6 mL):美国Phenomenex公司。
1.3 方法
1.3.1 动物分组和干预
将30只SPF级雄性SD大鼠适应性喂养一周后,按体质量随机分为3组:普通饮食组(ND)、高脂饮食组(HFD)和酸汤干预组(HFDS),每组10只。ND组喂普通饲料,HFD组和HFDS组喂高脂饲料,大鼠自主进食,HFDS组同时灌胃红酸汤8 g/kg体质量,ND组和HFD组灌胃等体积蒸馏水。每天下午3点对大鼠进行干预,每周测体质量,持续12周后,大鼠禁食12 h,腹腔注射戊巴比妥钠(0.5 mL/100 g体质量)麻醉,心尖取血保存于非抗凝生化管,常温静置10~20 min后3 000 r/min离心15 min,取血清,分装后-80 ℃保存。同时取腹内脂肪和肝脏组织称质量并于-80 ℃冻存,每组随机选3份肝脏样品进行蛋白组学检测。
1.3.2 肥胖指数和肝脏指数测定
参照文献[11] 计算肥胖指数和肝脏指数,具体计算公式如下:

1.3.3 血脂生化指标和肝功能指标检测
取400 μL血清,采用全自动生化分析仪测定大鼠血清中甘油三酯(triglyceride,TG)、总胆固醇(total cholesterol,TC)、低密度脂蛋白胆固醇(low density lipoprotein cholesterol,LDL-C)、高密度脂蛋白胆固醇(high densitylipoprotein cholesterol,HDL-C)含量以及谷丙转氨酶(alanine aminotransferase,ALT)和谷草转氨酶(aspartate aminotransferase,AST)的活性。
1.3.4 肝脏炎性因子TNF-α和IL-6的测定
取适量肝脏组织,按照TNF-α和IL-6试剂盒说明书测定各组大鼠肝脏中TNF-α和IL-6的含量。
1.3.5 肝脏蛋白质组学分析
蛋白提取及胰蛋白酶酶解:取肝脏样品,置于液氮预冷的研钵中,加液氮研磨成粉末。按粉末体积加入4倍体积裂解缓冲液(8 mL尿素,1%蛋白酶抑制剂),水浴超声(250 W超声3s、暂停5s,循环10次)裂解后,4 ℃、12 000g离心10min,采用BCA蛋白浓度测定试剂盒测定蛋白浓度。等量蛋白样品加入适量标准蛋白,用裂解缓冲液调整体积一致,缓慢加入终浓度20%的TCA,涡旋混匀后于4 ℃沉淀2 h。4 500 g离心5 min,弃上清,用预冷丙酮洗涤沉淀2~3次,晾干。加入终浓度200 mmol/L的TEAB,水浴超声(60 W超声1 s、暂停5 s,循环3次)打散沉淀,按质量比1∶50加入胰蛋白酶,37 ℃酶解过夜。 56 ℃条件下,加入5 mmol/L DTT还原30 min,室温避光下加入11 mmol/L碘乙酰胺孵育15 min。 胰酶酶解肽段采用Strata X C18固相萃取柱除盐后,真空冷冻干燥。
TMT标记及HPLC分级:取冷冻干燥后的肽段,采用0.25 mL 0.5 mol/L TEAB溶解,按TMT试剂盒操作说明,采用乙腈溶解标记试剂后与肽段混合,室温孵育2 h。标记后的混合肽段采用Strata X C18固相萃取柱除盐后,真空冷冻干燥。采用高pH反相HPLC对干燥肽段进行分级,HPLC条件:300Extend C18色谱柱,流动相为乙腈-水(pH 9),梯度(8%~32%乙腈)洗脱,流速1.0 mL/min,分离得到60个组分后,按照非连续合并策略(将第1、10、19、28、37、46、55管合并为第1个馏分;第2、11、20、29、38、47、56管合并为第2个馏分,以此类推)合并为9个组分,真空冷冻干燥。
超高液相色谱-质谱联用分析:真空冷冻干燥后的肽段用液相色谱流动相A相溶解后进行UPLC-MS分析[14]。
生物信息学分析:从UniProt数据库(https://www.uniprot.org/)中下载Rattus_norvegicus_10116_PR_20210721.fasta文件,采用Maxquant(v1.6.15.0)软件对文件进行检索鉴定蛋白质,以t检验结合差异倍数(fold change,FC)筛选差异表达蛋白,并用景杰生物云工具进行基因本体论(gene ontology,GO)功能富集分析、亚细胞结构定位和京都基因与基因组百科全书(kyoto encyclopedia of genes and genomes,KEGG)通路富集分析。差异表达蛋白与STRING(v.11.0)数据库比对后,导入Cytoscape 3.9.1绘制蛋白互作网络图。
1.3.6 数据处理
采用SPSS statistics 22.0及GraphPad Prism 8.0对各组数据进行统计分析及绘图,定量数据以“平均值±标准差”的形式呈现。 使用景杰生物云工具进行主成分分析(principal component analysis,PCA)和相对标准差(relative standard deviation,RSD)2种可视化统计分析,评估样品重复性。
2 结果与分析
2.1 贵州红酸汤对高脂饮食大鼠体质量、肥胖指数和肝脏指数的影响
贵州红酸汤对高脂饮食大鼠体质量、肥胖指数和肝脏指数的影响见图1。 由图1可知,在第12周干预结束时,与ND组相比,HFD组大鼠的体质量、肥胖指数和肝脏指数显著升高(P<0.05)。与HFD组相比,大鼠的体质量、肥胖指数和肝脏指数显著降低(P<0.05),表明贵州红酸汤对高脂饮食诱导的大鼠体质量、肥胖指数和肝脏指数的增加具有显著的抑制效果。
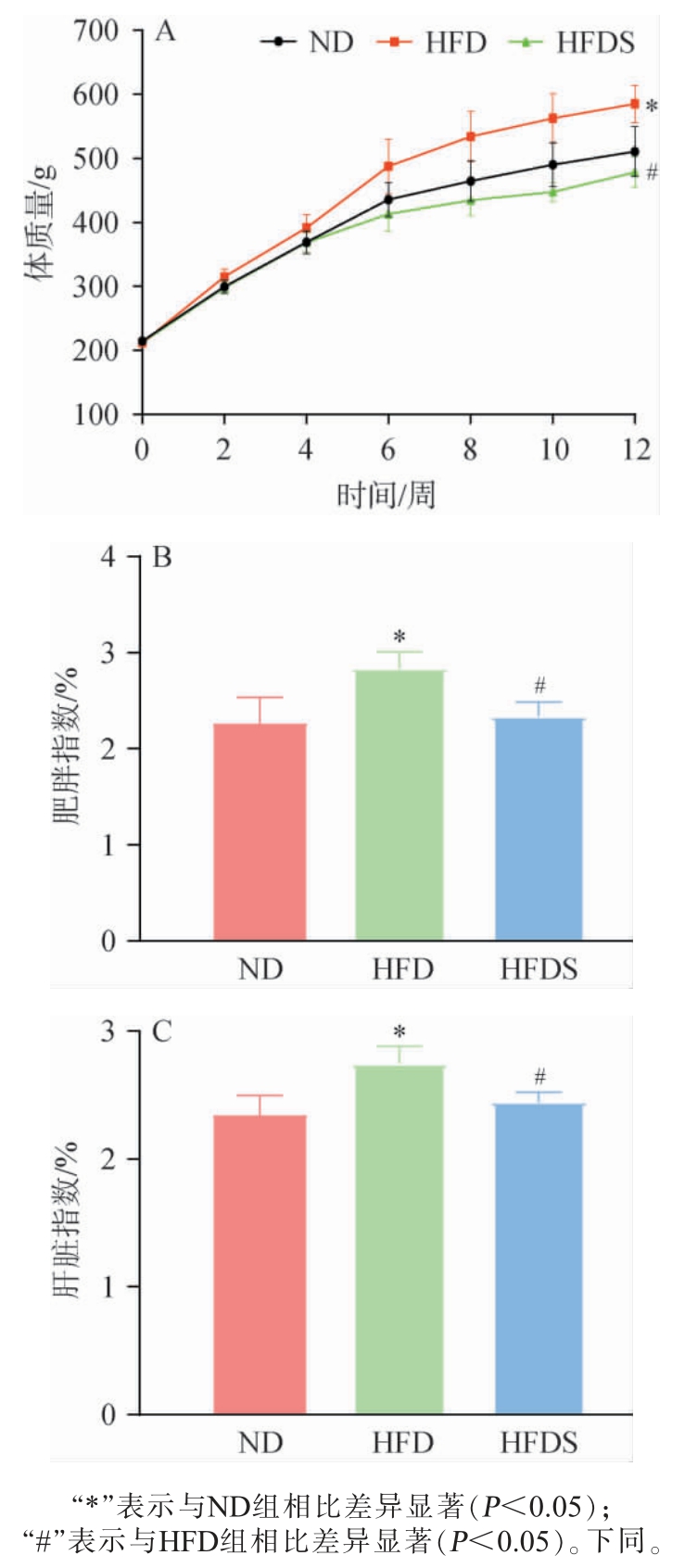
图1 贵州红酸汤对高脂饮食大鼠体质量(A)、肥胖指数(B)和肝脏指数(C)的影响
Fig. 1 Effect of Guizhou red sour soup on body mass (A), obesity index (B), and liver index (C) in rats with a high-fat diet
2.2 贵州红酸汤对高脂饮食大鼠血脂生化指标的影响
贵州红酸汤对高脂饮食大鼠血脂生化指标的影响见图2。由图2可知,与ND组相比,HFD组大鼠血清的TG、TC、LDL-C含量显著升高(P<0.05),HDL-C含量显著降低(P<0.05)。 与HFD组相比,HFDS组大鼠血清的TG、TC、LDL-C含量显著降低(P<0.05),HDL-C含量显著升高(P<0.05)。结果表明,贵州红酸汤对于肥胖相关血脂代谢异常具有显著的调节作用。
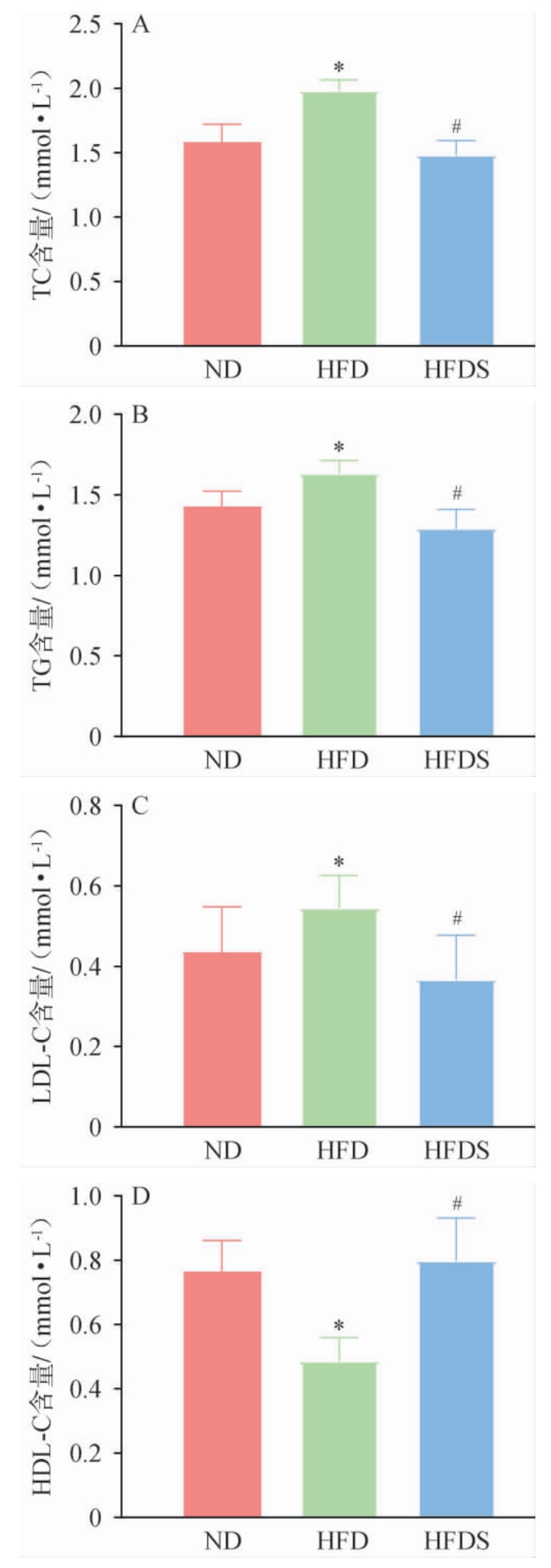
图2 贵州红酸汤对高脂饮食大鼠血脂生化指标的影响
Fig. 2 Effect of Guizhou red sour soup on lipid biochemical indicators in rats with a high-fat diet
2.3 贵州红酸汤对高脂饮食大鼠肝功能的影响
贵州红酸汤对高脂饮食大鼠肝功能的影响见图3。 由图3可知,与ND组相比,HFD组大鼠血清中ALT、AST的活性显著升高(P<0.05)。与HFD组相比,HFDS组大鼠血清中的ALT和AST活性均显著降低(P<0.05),说明贵州红酸汤干预能够有效改善高脂饮食诱导的大鼠肝功能损伤。
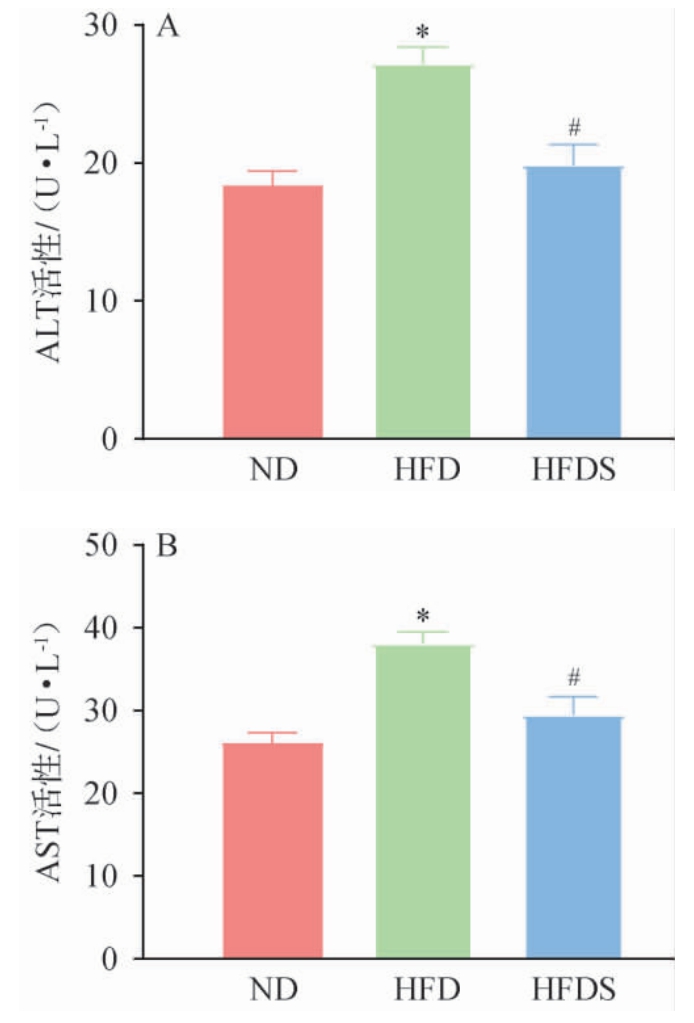
图3 贵州红酸汤对高脂饮食大鼠血清丙氨酸氨基转移酶(A)和天冬氨酸氨基转移酶(B)活性的影响
Fig. 3 Effect of Guizhou red sour soup on activities of alanine aminotransferase (A) and aspartate aminotransferase (B)in the serum of rats with a high-fat diet
2.4 贵州红酸汤对高脂饮食大鼠肝脏炎症因子的影响
贵州红酸汤对高脂饮食大鼠肝脏炎症因子的影响见图4。
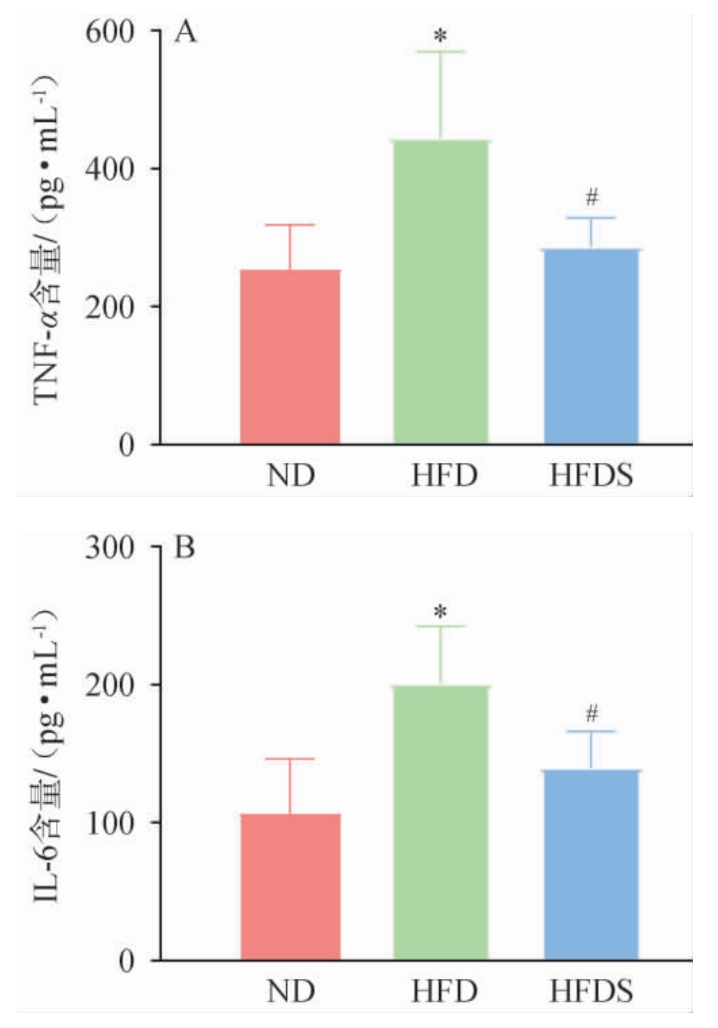
图4 贵州红酸汤对高脂饮食大鼠肝脏肿瘤坏死因子-α(A)和白细胞介素-6(B)含量的影响
Fig. 4 Effect of Guizhou red sour soup on contents of tumor necrosis factor-α(A)and interleukin-6(B)in the liver of rats with a highfat diet
由图4可知,与ND组相比,HFD组大鼠肝脏TNF-α和IL-6的含量显著升高(P<0.05)。与HFD组相比,HFDS组大鼠TNF-α和IL-6的含量显著降低(P<0.05),说明贵州红酸汤干预能够有效减轻高脂饮食大鼠肝脏炎症。LEE M R等[15]研究发现,高脂饮食喂养肥胖大鼠机体中TNF-α水平升高,经发酵食品干预后下调,改善了高脂饮食大鼠体内炎症环境,这与本研究结果一致。
2.5 贵州红酸汤对高脂饮食大鼠肝脏蛋白质组的影响
2.5.1 样品重复性检验
为能够全面而准确地评估样本定量结果的稳定性和可靠性,确保实验数据的准确性和可信度,采用PCA和RSD评估3次蛋白定量的重复性,结果见图5。 PCA图中样本间的聚集程度代表样本的差异性大小;RSD箱线图中RSD值越小,定量重复性越好,由图5可知,同组内样本紧密聚集,不同组样本明显分离,且整体RSD值较小,说明本次实验3组样本中各样本间的定量结果重复性较好。
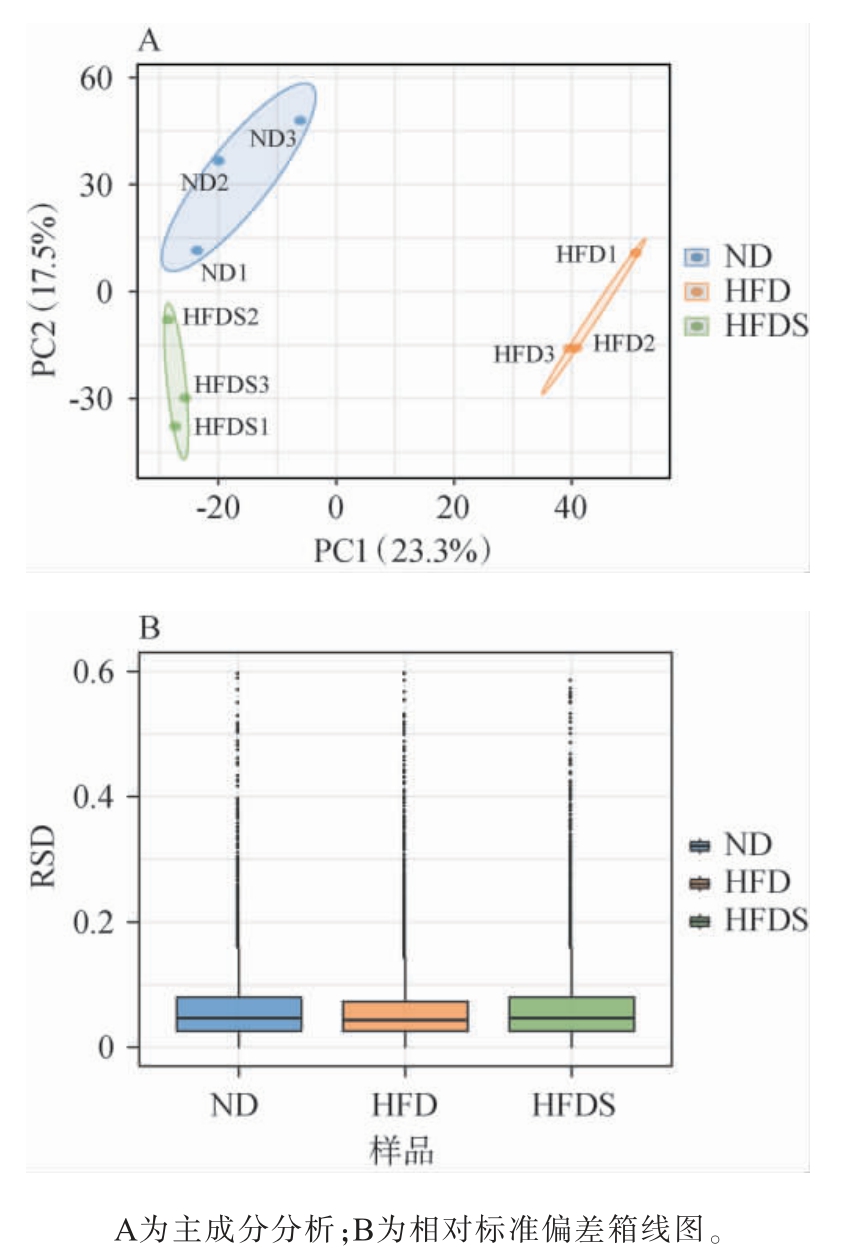
图5 蛋白组学样品重复性检验结果
Fig. 5 Repeatability test results of proteomics samples
2.5.2 差异表达蛋白的筛选与表达分析
以P<0.05和两组间蛋白定量值差异倍数(FC)>1.3或<1.3作为筛选条件,从HFDS组与HFD组、HFD组与ND组中筛选差异表达蛋白,结果见图6。由图6可知,在HFDS组与HFD组中共鉴定出126个差异表达蛋白,HFD组与ND组中共鉴定出121个差异表达蛋白,与ND组相比,55个差异蛋白在HFD组中表达显著上调,66个差异蛋白表达显著下调;与HFD组相比,76个差异蛋白在HFDS组中表达显著上调,50个差异蛋白表达显著下调。
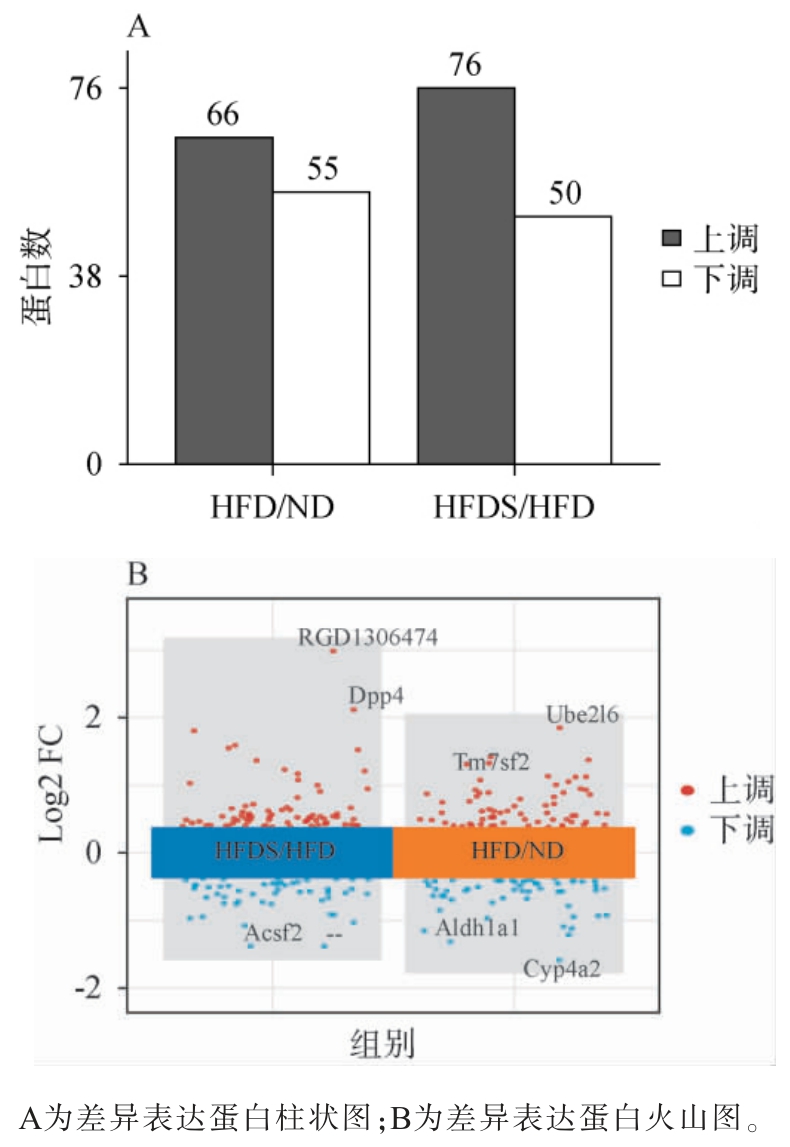
图6 各比较组间差异表达蛋白统计结果
Fig. 6 Statistical results of differentially expressed proteins among the comparison groups
2.5.3 差异表达蛋白GO、KEGG富集分析及亚细胞结构定位
对HFDS与HFD、HFD与ND两个比较组间的差异表达蛋白进行基因本体论(gene ontology,GO)富集分析和亚细胞结构定位,结果见图7。GO是当前国际通用的标准化蛋白质功能注释分类体系,其核心框架包含生物过程(biological process,BP)、分子功能(molecular function,MF)及细胞组分(cellular component,CC)三大维度。由图7A和图7B可知,两个比较组间的差异表达蛋白均富集于细胞过程、代谢过程、生物调节及对刺激的反应等生物过程,主要包含细胞及胞内等细胞组分,参与催化活性和结合等分子功能。由图7C和图7D可知,这些差异表达蛋白主要位于细胞质、细胞外、线粒体及内质网等细胞结构。
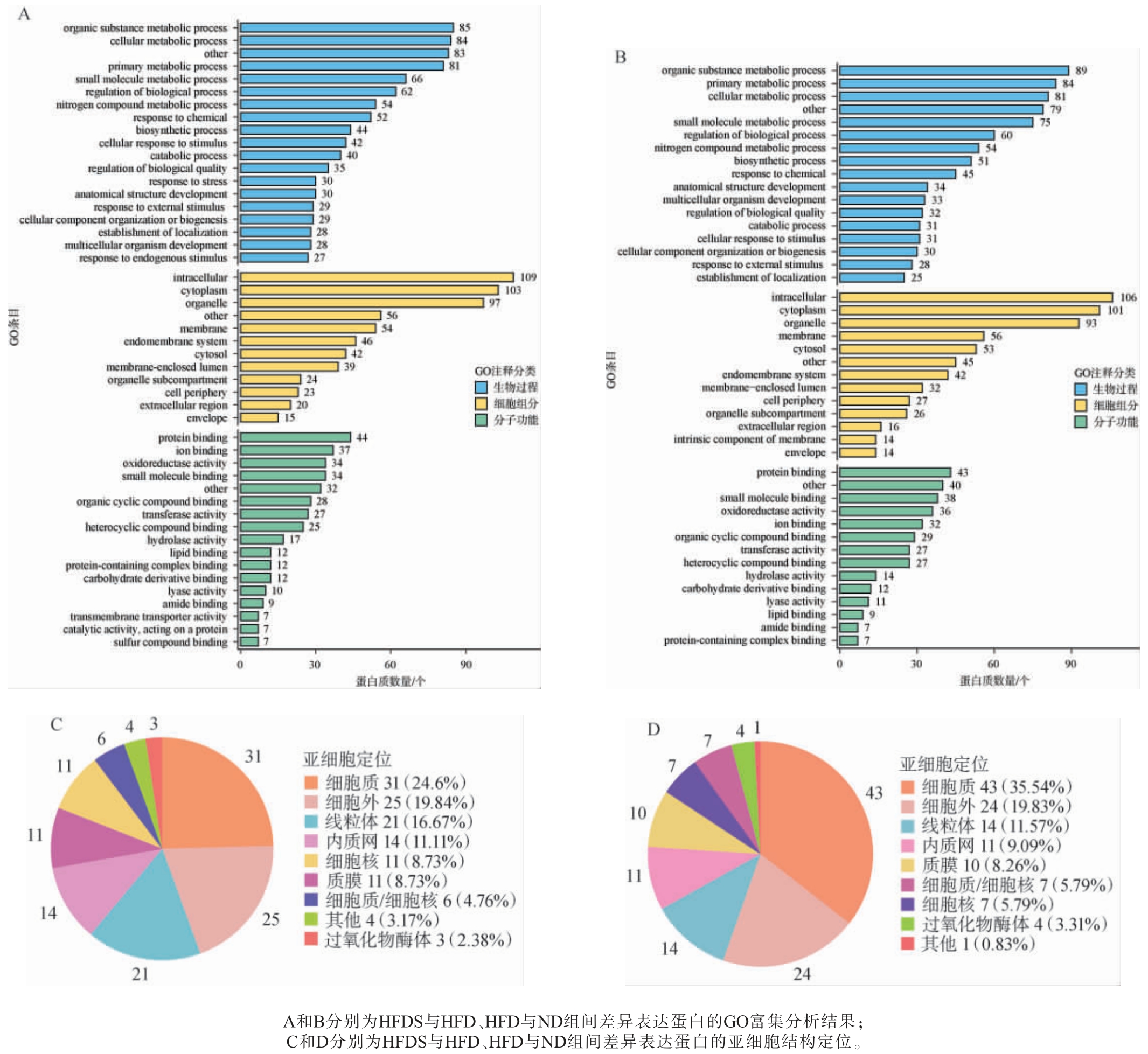
图7 各比较组间差异表达蛋白的基因本体论富集分析及亚细胞结构定位结果
Fig. 7 Results of gene ontology enrichment analysis and subcellular structure localization of differentially expressed proteins among the comparison groups
进一步针对两个比较组间的差异表达蛋白进行京都基因与基因组百科全书(Kyoto Encyclopedia of Genes and Genomes,KEGG)通路富集分析,并筛选显著富集的前20条通路(P<0.05),结果见图8。 由图8可知,HFDS组与HFD组间的差异表达蛋白主要富集于亚油酸代谢、脂肪酸伸长、视黄醇代谢、过氧化物酶体增殖物激活受体(peroxisome proliferator-activated receptor,PPAR)信号通路、脂肪酸降解、半胱氨酸和蛋氨酸代谢、不饱和脂肪酸的生物合成、花生四烯酸代谢和丙酮酸代谢等代谢相关通路;HFD组与ND组间的差异表达蛋白主要富集于类固醇的生物合成、酮体的合成和降解、脂肪酸伸长、视黄醇代谢、脂肪酸降解、不饱和脂肪酸的生物合成、PPAR信号通路、花生四烯酸代谢、丙酮酸代谢、亚油酸代谢和过氧化物酶体等代谢通路,表明贵州红酸汤对高脂饮食大鼠的调控作用是多途径、多效应的。高脂饮食引起机体游离脂肪酸过量,导致肝脏中线粒体功能障碍释放过多的活性氧,引起细胞中内质网及溶酶体等细胞器功能失调[16],与慢性炎症等因素共同作用引发肝脏代谢紊乱以及免疫功能受损等问题[17]。 KEGG富集的多个代谢通路均与线粒体健康密切相关。如PPAR可调节线粒体的生物发生、脂肪酸氧化等过程[18],同时,过氧化物酶体增殖物激活受体γ辅激活因子1α(peroxisome proliferator-activated receptor gamma coactivator 1 alpha,PGC-1α)等与PPAR信号通路相关的因子也参与线粒体的稳态调节[19]。半胱氨酸的代谢产物谷胱甘肽在维持线粒体的氧化还原平衡中起重要作用,参与抵御氧化应激,保护线粒体免受氧化损伤[20]。花生四烯酸在环加氧酶等作用下生成前列腺素等活性物质,可影响线粒体的呼吸功能、氧化磷酸化过程等,进而调节细胞的能量代谢[21]。 综上所述,贵州红酸汤可能通过线粒体等靶器官及脂质代谢、不饱和脂肪酸代谢、丙酮酸代谢和免疫调节等通路改善高脂饮食大鼠肝脏代谢紊乱。
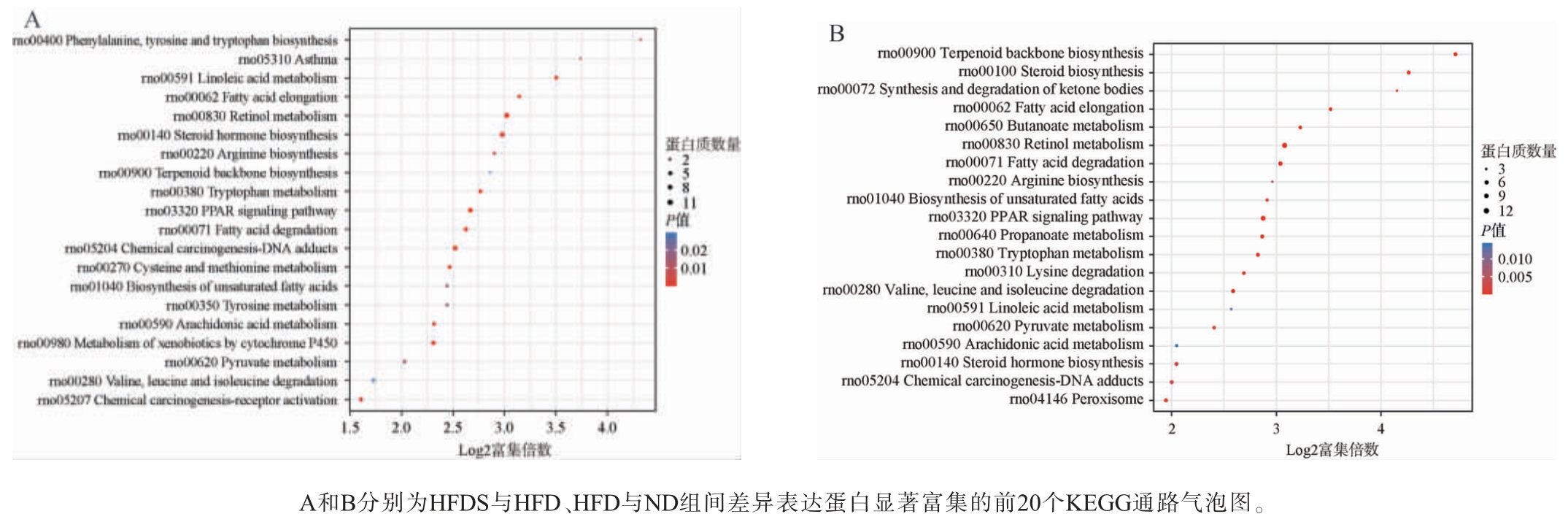
图8 各比较组间差异表达蛋白京都基因与基因组百科全书通路富集分析结果
Fig. 8 Enrichment analysis results of the Kyoto Encyclopedia of Genes and Genomes enrichment pathways for differentially expressed proteins among the comparison groups
2.5.4 关键蛋白相互作用网络
为探究红酸汤干预高脂饮食大鼠的潜在关键调控蛋白,通过比较HFDS与HFD、HFD与ND两个比较组间差异表达蛋白质组学数据,筛选两组共有差异表达蛋白,并利用Cytoscape 3.9.1对其进行网络拓扑分析,基于节点度(Degree)排序筛选核心靶标蛋白,结果见图9。
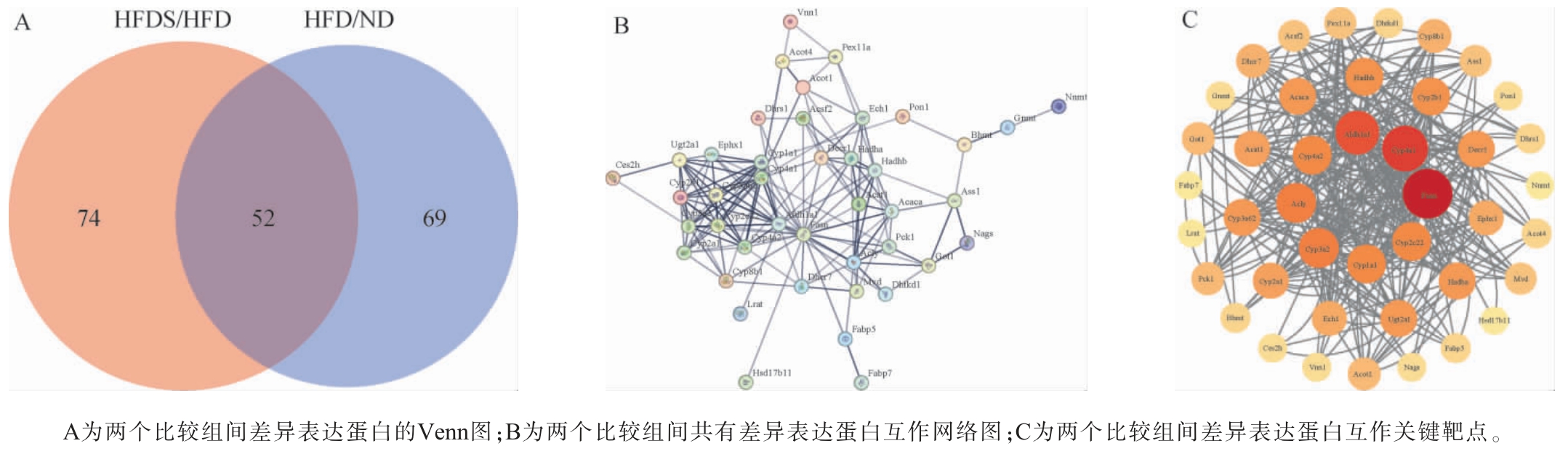
图9 各比较组间共有差异表达蛋白互作网络分析结果
Fig. 9 Analysis results of the common differentially expressed protein interaction networks among the comparison groups
由图9A可知,两比较组间共鉴定出52个共有差异表达蛋白,其中红酸汤干预后33个蛋白表达显著上调,19个蛋白表达显著下调。由图9B和图9C可知,上调蛋白包括脂肪酸合成酶(fattyacid synthase,Fasn)、三磷酸腺苷柠檬酸裂解酶(ATP-citrate lyase,Acly)、乙酰辅酶A羧化酶α(acetyl-CoA carboxylase alpha,Acaca)等,下调蛋白包括细胞色素P450 3A2(cytochrome P450 3A2,Cyp3a2)、细胞色素P450 3A62(cytochrome P450 3A62,Cyp3a62)、醛脱氢酶1A1(aldehyde dehydrogenas 1A1,Aldh1a1)、羟酰辅酶A脱氢酶β亚基(3-hydroxyacyl-CoA dehydrogenase beta subunit,Hadhb)等。Fasn是催化脂肪酸从头合成步骤的关键脂肪生成酶,与脂肪酸合成过程密切相关,是人类基因组中唯一能够催化烟酰胺腺嘌呤二核苷酸磷酸(nicotinamide adenine dinucleotide phosphate,NADPH)、乙酰辅酶A和丙二酰辅酶A从头合成长链脂肪酸的蛋白质[22]。Acly主要定位于细胞浆和线粒体中,在细胞内将柠檬酸裂解为乙酰辅酶A和草酰乙酸,为脂肪酸、胆固醇等的合成提供乙酰辅酶A,参与细胞的能量代谢和物质代谢[23]。Acaca通过调节丙二酰辅酶A的生成,控制脂肪酸合成的起始步骤,进而参与脂肪酸的从头合成过程,是脂肪酸合成的关键限速酶[24]。Cyp3a2和Cyp3a62主要在肝脏中表达,参与多种内源性和外源性物质的氧化代谢,包括类固醇激素、脂肪酸以及药物等,对维持体内物质代谢平衡和药物的代谢转化具有重要意义[25]。Aldh1a1在视黄醛代谢中起关键作用,通过将视黄醛氧化成视黄酸,参与维生素A类物质代谢,维持细胞内稳态[26]。Hadhb是线粒体三功能酶复合体的一个亚基,该复合体催化长链脂肪酸β-氧化的最后三个步骤,包括长链羟酰辅酶A的脱氢、L-β-羟脂酰辅酶A的构象改变以及第二次脱氢反应,从而将长链脂肪酸分解为乙酰辅酶A,参与脂肪酸的氧化代谢[27]。贵州红酸汤通过抑制高脂饮食大鼠肝脏中脂肪酸合成过程,促进脂肪酸代谢,进而减少了大鼠肝脏中脂肪堆积,改善大鼠肝脏脂质代谢,Fasn、Acly、Acaca、Cyp3a2、Cyp3a62、Aldh1a1、Hadhb等蛋白可能是贵州红酸汤改善肝脏脂质代谢紊乱的关键靶点。
3 结论
本研究采用贵州红酸汤对无特定病原体(SPF)级雄性SD大鼠持续干预12周后发现,贵州红酸汤可能作用于线粒体等靶器官,通过调控脂质代谢、不饱和脂肪酸代谢、丙酮酸代谢和免疫调节等通路,抑制高脂饮食大鼠体质量增长,降低血脂水平及脂肪堆积,减轻肝脏炎症和肝损伤,有效改善高脂饮食大鼠肝脏脂代谢紊乱,Fasn、Acly、Acaca、Cyp3a2、Cyp3a62、Aldh1a1、Hadhb 等蛋白可能为贵州红酸汤改善肝脏脂代谢紊乱的核心潜在靶点,本研究可为红酸汤的保健功能开发提供科学依据,亦为开发基于传统发酵食品的功能性干预策略奠定理论基础。
[1] CLEMENTE-SUÁREZ V J, BELTRÁN-VELASCO A I, REDONDOFLÓREZ L, et al. Global impacts of western diet and its effects on metabolism and health:A narrative review[J] .Nutrients,2023,15(12):2749.
[2] WANG Y,AI Z,XING X,et al.The ameliorative effect of probiotics on diet-induced lipid metabolism disorders:A review[J] .Crit Rev Food Sci Nutr,2024,64(11):3556-3572.
[3] CHEN X X, SUN C, LIU C, et al. lncRNA in hepatic glucose and lipid metabolism:A review[J] .Chin J Biomed Eng,2021,37(1):40-52.
[4] TSURU H, OSAKA M, HIRAOKA Y, et al. HFD-induced hepatic lipid accumulation and inflammation are decreased in factor D deficient mouse[J] .Sci Rep,2020,10(1):17593.
[5] LIANG H, JIANG F, CHENG R, et al. A high-fat diet and high-fat and high-cholesterol diet may affect glucose and lipid metabolism differentially through gut microbiota in mice[J] .Exp Anim,2021,70(1):73-83.
[6] JALILI M,NAZARI M,MAGKOS F.Fermented foods in the management of obesity:Mechanisms of action and future challenges[J] .Int J Mol Sci,2023,24(3):2665.
[7] 鲁杨,王楠兰,李贤,等. 凯里红酸汤主要营养和功能成分的分析研究[J] .食品研究与开发,2019,40(7):163-166.
[8] LI L,SUN H,TAN L,et al.Miao sour soup alleviates DSS-induced colitis in mice:Modulation of gut microbiota and intestinal barrier function[J] .Food Funct,2024,15(16):8370-8385.
[9] 周倩倩,袁钦,王楠兰,等. 贵州苗族红酸汤对单纯性肥胖大鼠血清及肠道炎性的影响[J] .中国酿造,2022,41(7):101-105.
[10] 杨红梅,王楠兰,周倩倩,等. 凯里红酸汤对肥胖大鼠脂质代谢及氧化应激的影响[J] .食品研究与开发,2021,42(11):41-46.
[11] YANG H,XIE J,WANG N,et al.Effects of Miao sour soup on hyperlipidemia in high-fat diet-induced obese rats via the AMPK signaling pathway[J] .Food Sci Nutr,2021,9(8):4266-4277.
[12] 曲子晗,王楠兰,杨红梅,等. 凯里红酸汤对大鼠肠道脂肪酸吸收和紧密连接蛋白的调控[J] .中国酿造,2021,40(5):129-133.
[13] CUI M,CHENG C,ZHANG L.High-throughput proteomics:A methodological mini-review[J] .Lab Invest,2022,102(11):1170-1181.
[14] YUAN Q, ZHOU Q, WANG N, et al. Integrative proteomics and metabolomics of Guizhou Miao sour soup affecting simple obese rats[J] .Front Nutr,2022,9:1019205.
[15] LEE M R,YANG H J,PARK K I,et al.Lycopus lucidus turcz.ex benth.attenuates free fatty acid-induced steatosis in HepG2 cells and non-alcoholic fatty liver disease in high-fat diet-induced obese mice[J] . Phytomedicine,2019,55:14-22.
[16] CHEN Y, YANG F, CHU Y, et al. Mitochondrial transplantation:Opportunities and challenges in the treatment of obesity,diabetes,and nonalcoholic fatty liver disease[J] .J Transl Med,2022,20(1):483.
[17] KHAN S, LUCK H, WINER S, et al. Emerging concepts in intestinal immune control of obesity-related metabolic disease[J] . Nat Commun,2021,12(1):2598.
[18] QIU Y Y,ZHANG J,ZENG F Y,et al.Roles of the peroxisome proliferator-activated receptors (PPARs) in the pathogenesis of nonalcoholic fatty liver disease(NAFLD)[J] .Pharmacol Res,2023,192:106786.
[19] 南淞华,彭超杰,崔应麟.PGC-1α对线粒体功能的调控作用及机制[J] .生理学报,2025,77(2):300-308.
[20] LIU Y Y,LIU S,TOMAR A,et al.Autoregulatory control of mitochondrial glutathione homeostasis[J] .Ann N Y Acad Sci,2023,382(6672):820-828.
[21] WEI C, WANG M, WANG X J. Evolutionary conservation analysis of human arachidonic acid metabolism pathway genes[J] .Life Med,2023,2(2):lnad004.
[22] WAKIL S J.Fatty acid synthase,a proficient multifunctional enzyme[J] .Biochem,1989,28(11):4523-4530.
[23] FENG X, ZHANG L, XU S, et al. ATP-citrate lyase (ACLY) in lipid metabolism and atherosclerosis:An updated review[J] .Prog Lipid Res,2020,77:101006.
[24] DONG J, LI M, PENG R, et al. ACACA reduces lipid accumulation through dual regulation of lipid metabolism and mitochondrial function via AMPK-PPARα-CPT1A axis[J] .J Transl Med,2024,22(1):196.
[25] KLYUSHOVA L S,PEREPECHAEVA M L,GRISHANOVA A Y.The role of CYP3A in health and disease[J] .Biomedicines,2022,10(11):2686.
[26] 胡忠昌,曹阳,秦立红,等.Aldh1a1基因研究进展[J] . 黑龙江畜牧兽医,2018(15):54-56.
[27] UCHIDA Y,IZAI K,ORII T,et al. Novel fatty acid beta-oxidation enzymes in rat liver mitochondria.II.purification and properties of enoylcoenzyme A(CoA) hydratase/3-hydroxyacyl-CoA dehydrogenase/3-ketoacyl-CoA thiolase trifunctional protein[J] .J Biol Chem,1992,267(2):1034-1041.