随着现代社会节奏的加快以及社交应酬频率的提升,饮酒已成为许多人日常生活中不可忽视的一环。然而,长期或过量饮酒所引发的肝脏损伤问题日益突出,尤其是急性酒精性肝损伤、脂肪肝乃至肝硬化等[1-2],已成为威胁公众健康的重要因素之一。如何有效减轻酒精对肝脏的毒性影响,开发具有解酒护肝功能的干预手段,已成为当前食品科学和医学领域关注的研究热点。
近年来,益生菌及其发酵产物因其在调节肠道菌群、增强免疫力及抗氧化等方面的潜在作用,引发了广泛关注。乳酸菌,作为常见的益生菌类型之一,不仅广泛用于发酵食品的生产,还被证实在改善酒精性肝损伤方面具有一定效果[3-8]。特别是在发酵过程中,乳酸菌可与多种植物原料协同作用,产生多种具有生物活性的代谢产物,如多酚、短链脂肪酸和抗氧化酶类,为开发功能性发酵食品提供了理论和实践基础。
红酸汤是贵州少数民族传统的发酵食品,富含多种有益菌[9]及植物成分,具有改善肝脏脂质代谢的作用[10]。 同时,已有研究表明其具备显著的抗氧化活性,能够有效减少自由基的产生,改善肝脏的抗氧化能力[11-12]。许九红[13]通过混菌强化发酵红酸汤,与自然发酵红酸汤相比,发现其能降低亚硝酸盐含量,提升总酸及氨基酸态氮含量,具有浓郁的发酵香味且酸辣鲜味适中,口感柔和,品质更优。为探索天然发酵乳酸菌在解酒护肝领域中的潜力,并为传统酸汤的功能性提升提供科学依据。本研究通过测定商业和筛选乳酸菌菌株的耐乙醇及降解乙醇的能力,优选乳酸菌菌株,并利用优选菌株对红酸汤半成品进行混菌强化发酵。进一步利用低(5 mL/kg)和高(15 mL/kg)剂量的混菌发酵红酸汤灌胃小鼠,通过测定小鼠醉酒时间、乙醇脱氢酶(alcohol dehydrogenase,ADH)活力、血清生化指标等相关指标,评价其解酒护肝功效,为开发安全、天然、具有保健功能的发酵饮品提供理论支持和实践路径,推动民族发酵食品的现代化和功能化发展。
1 材料与方法
1.1 材料与试剂
1.1.1 材料与菌株
雄性昆明小鼠(18~22 g,4周龄):珠海百试通生物科技有限公司;生产许可证号为SCXK(粤)2020-0051,实验动物伦理编号为2024B217。 植物乳植杆菌(Lactiplantibacillus plantarum):从陈酿柿子原醋液分离得到,保藏于本实验室;鼠李糖乳杆菌(Lactobacillus rhamnosus)、嗜酸乳杆菌(Lactobacillus acidophilus):安琪酵母股份有限公司;副干酪乳杆菌(Lactobacillus paracasei)H2、布氏乳杆菌(Lactobacillus brucei)H3、布氏乳杆菌(Lactobacillus brucei)H4:从传统发酵红酸汤样品分离获得,保藏于本实验室。传统发酵红酸汤半成品:由贵州省黔东南苗族侗族自治州雷山县农户提供;红星二锅头白酒(53%vol):北京红星股份有限公司。
1.1.2 试剂
利加隆水飞蓟素胶囊:德国马博士大药厂;谷丙转氨酶(alanine aminotransferase,ALT)测试盒、谷草转氨酶(aspartate aminotransferase,AST)测试盒、甘油三酯(triglyceride,TG)测试盒、超氧化物歧化酶(superoxide dismutase,SOD)测试盒、丙二醛(malondialdehyde,MDA)检测试剂盒、ADH检测试剂盒:南京建成生物科技有限公司;氯化钠(分析纯):广州历程实业有限公司;无水乙醇(分析纯):天津市大茂化学试剂厂。其他试剂均为国产分析纯或生化试剂。
1.1.3 培养基
MRS琼脂培养基、MRS肉汤培养基:广东环凯生物科技有限公司。
1.2 仪器与设备
HYL-X多功能恒温培养摇床:浙江太仓市强文实验有限公司;SW-CJ-2F双人单面超净工作台:贵州力辰科技有限公司;LS-50GH立式高压蒸汽灭菌锅:浙江江阴滨江医疗设备有限公司;HH-4恒温水浴锅:常州澳华仪器有限公司。
1.3 方法
1.3.1 乳酸菌的活化及培养
将保存于-80 ℃甘油中的乳酸菌菌株按3%(V/V)的接种量分别接种于MRS肉汤培养基中,37 ℃、180 r/min条件下活化传代培养2次。 菌液在4 ℃、10 000 r/min条件下离心10 min,采用0.85%的无菌生理盐水洗涤3次并调整菌液浓度至1×108 CFU/mL。
1.3.2 优良乳酸菌的筛选
乙醇耐受性分析:取活化后的菌液(1×108 CFU/mL)100 μL分别涂布于乙醇体积分数分别为0、5%、10%、15%的MRS固体培养基中,37℃条件下培养48h。参照GB4789.35—2023《食品微生物学检验乳酸菌检验》进行乳酸菌菌落计数,并计算存活率,分析各菌株的乙醇耐受能力,存活率计算公式如下:
式中:A1为MRS固体培养基上的乳酸菌活菌数,CFU;A2为活化后菌液中乳酸菌的活菌数,CFU。
降解乙醇能力测定:将活化后的菌液(1×108 CFU/mL)按照3%(V/V) 的接种量接种至100 mL MRS肉汤培养基中,37 ℃、180 r/min条件下振荡培养12 h,得到种子液。然后按照3%(V/V)的接种量接种到乙醇体积分数分别为10%、30%、40%的MRS肉汤培养基中,37 ℃、180 r/min培养48 h。采用重铬酸钾-硫酸法测定乙醇含量[14],并计算乙醇降解率,评估乳酸菌对乙醇的降解能力,乙醇降解率计算公式如下:
式中:A1为初始乙醇含量,%;A2为培养后乙醇含量,%。
1.3.3 红酸汤的乳酸菌混菌强化发酵
按照3%(V/V)的接种量将筛选菌株的活化菌液接种于半成品红酸汤中,各菌株活化菌液的比例为1∶1,在(28±1)℃条件下密封、避光、厌氧继续发酵15 d,获得混菌发酵红酸汤成品,阴凉避光处长期保存。
1.3.4 混菌发酵红酸汤解酒护肝功效研究
(1)灌胃混菌发酵红酸汤和阳性药物的制作
对混菌发酵红酸汤进行巴氏杀菌处理(67 ℃、20 min),冷却后在4 ℃、7 000 r/min条件下离心15 min,去沉淀,保留上清液,备用。
取水飞蓟素胶囊中的粉末用无菌水溶解,使其质量浓度为10 mg/mL,备用。
(2)实验动物与分组
将50只小鼠适应性喂养7 d,随机分为5组,每组10只。实验分组如下:空白对照组(A)、模型组(B)、阳性对照组(C)、低剂量组(D)和高剂量组(E)。 空白对照组和模型组小鼠每日灌胃5 mL/kg生理盐水(按体质量计算),阳性对照组小鼠灌胃5mL/kg水飞蓟素溶液(质量浓度为10mg/mL)[15],低剂量组和高剂量组分别灌胃5 mL/kg和15 mL/kg的混菌发酵红酸汤样品溶液。 所有给药组的小鼠在末次给药后30 min内,除空白对照组外,其余组均灌胃10 mL/kg红星二锅头白酒(53%vol),空白对照组灌胃等体积的生理盐水。灌胃操作持续14d,每天上午8∶00~9∶00进行,实验期间,每天对小鼠进行体质量测定,根据体质量变化调整每日给药剂量。
(3)醉酒潜伏期与醒酒时间测定
参考文献[16] 以翻正反射的消失作为判断小鼠醉酒与醒酒状态的标准。 实验开始时,小鼠被背部朝下平放在水平面上,观察其翻正反射的恢复情况。 若小鼠背部向下能够持续保持30 s以上,则认为翻正反射消失,表示小鼠处于醉酒状态;若小鼠背部向下保持时间<30 s,则认为翻正反射恢复,表明小鼠已醒酒。 醉酒潜伏期为小鼠从开始灌胃的酒例首次翻正反射消失后的30 s内无法翻身的时间,醒酒时间为从醉酒状态起,30 s内小鼠成功翻身的时间点。
(4)小鼠肝脏ADH活性及血清生化指标测定
肝脏组织的采集及ADH活性测定:最后一天灌胃90min后,立即剖腹取出肝脏,使用生理盐水冲洗肝脏,并用滤纸吸干表面液体,精确称质量,计算肝脏指数,其计算公式如下:
随后将肝脏组织放入2 mL冻存管中,迅速置于液氮中急冻,存放于-80 ℃冰箱中待测。按照试剂盒说明书测定肝脏中的ADH活性[17]。
血清样本的采集及生化指标测定:最后一天灌胃90 min后,通过眼眶静脉采血,样本静置1 h后,使用微量冷冻离心机在4 ℃、3 500 r/min条件下离心15 min,取上清,按照试剂盒说明书测定血清中ALT、AST含量。
(5)小鼠肝脏组织中抗氧化相关指标的测定
按照试剂盒说明书测定肝组织中TG含量、SOD活性和MDA含量。
(6)肝脏组织病理学观察
最后一天灌胃90 min后,立即剖取小鼠肝脏,并切取小鼠肝脏右叶,使用生理盐水冲洗后,置于4%的甲醛溶液中进行固定。 肝脏组织经过苏木精-伊红(hematoxylin-eosin,HE)染色后,采用显微镜(放大倍数200×)观察其病理组织学变化,并对肝脏组织的异常病变情况进行病理学分析。
1.3.5 数据处理与统计分析
每个实验均重复3次,数据以“平均值±标准差”表示。采用SPSS 27.0软件进行单因素方差分析,并使用Duncan检验比较各组间差异的显著性,P<0.05认为具有统计学显著性。使用Origin 2022软件绘制图表。
2 结果与分析
2.1 乳酸菌的乙醇耐受性和乙醇降解能力分析
各乳酸菌菌株的乙醇耐受性及乙醇降解能力分别见表1和表2。
表1 各乳酸菌菌株在不同乙醇体积分数下的存活率
Table 1 Survival rates of each lactic acid bacterial strain at different ethanol volume fractions%
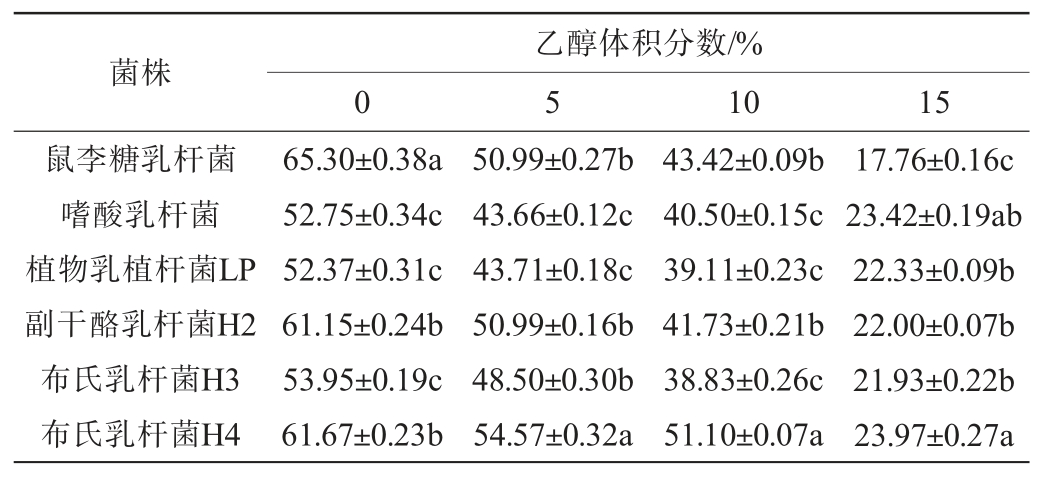
注:同列不同小写字母表示差异显著(P<0.05)。下同。
菌株乙醇体积分数/%0 5 1015鼠李糖乳杆菌嗜酸乳杆菌植物乳植杆菌LP副干酪乳杆菌H2布氏乳杆菌H3布氏乳杆菌H4 65.30±0.38a 52.75±0.34c 52.37±0.31c 61.15±0.24b 53.95±0.19c 61.67±0.23b 50.99±0.27b 43.66±0.12c 43.71±0.18c 50.99±0.16b 48.50±0.30b 54.57±0.32a 43.42±0.09b 40.50±0.15c 39.11±0.23c 41.73±0.21b 38.83±0.26c 51.10±0.07a 17.76±0.16c 23.42±0.19ab 22.33±0.09b 22.00±0.07b 21.93±0.22b 23.97±0.27a
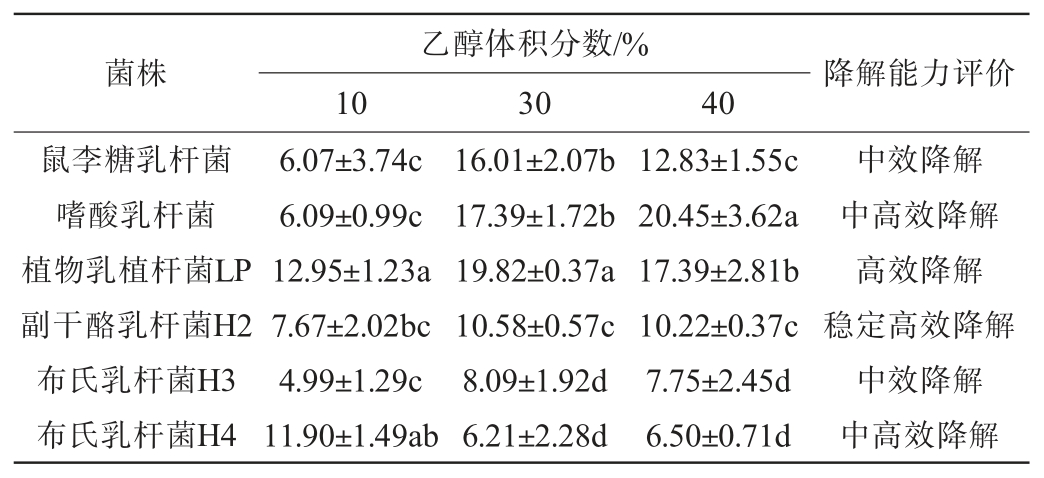
表2 各乳酸菌菌株在不同乙醇体积分数下对乙醇降解率
Table 2 Ethanol degradation rates of each lactic acid bacterial
strain at various ethanol volume fractions%
乙醇体积分数/%103040菌株降解能力评价鼠李糖乳杆菌嗜酸乳杆菌植物乳植杆菌LP副干酪乳杆菌H2布氏乳杆菌H3布氏乳杆菌H4 6.07±3.74c 6.09±0.99c 12.95±1.23a 7.67±2.02bc 4.99±1.29c 11.90±1.49ab 16.01±2.07b 17.39±1.72b 19.82±0.37a 10.58±0.57c 8.09±1.92d 6.21±2.28d 12.83±1.55c 20.45±3.62a 17.39±2.81b 10.22±0.37c 7.75±2.45d 6.50±0.71d中效降解中高效降解高效降解稳定高效降解中效降解中高效降解
由表1可知,乙醇体积分数对菌株存活率呈现明显的剂量效应。在低乙醇体积分数组(5%、10%)中,各菌株的存活率均>38%,当乙醇体积分数为10%时,布氏乳杆菌H4[(51.10±0.07)%] 、副干酪乳杆菌H2[(41.73±0.21)%] 和鼠李糖乳杆菌[(43.42±0.09)%] 的存活率显著高于其他菌株(P<0.05)。在高乙醇体积分数组(15%)中,除鼠李糖乳杆菌的存活率骤降至(17.76±0.16)%外,其余菌株的存活率均维持在20%以上,表现出较强的乙醇耐受性。结果表明,各菌株在高体积分数乙醇胁迫下仍能维持较高的存活率,具有较强的乙醇耐受性,可作为乙醇胁迫发酵体系或功能性益生菌开发的优选菌株。
由表2可知,在不同乙醇体积分数下,各菌株对乙醇均具有一定的降解能力,其中植物乳植杆菌LP和副干酪乳杆菌H2表现出高效的乙醇降解特性,植物乳植杆菌LP在体积分数为10%、30%、40%的乙醇中,乙醇降解率分别为(12.95±1.23)%、(19.82±0.37)%、(17.39±2.81)%,副干酪乳杆菌H2对乙醇的降解率分别为(7.67±2.02)%、(10.58±0.57)%、(10.22±0.37)%,表明两株菌均具备工业化乙醇降解的应用潜力。
在菌株挑选过程中,基于对混菌发酵红酸汤解酒护肝功效的研究,优先考虑解酒能力(即乙醇降解能力),其次是乙醇耐受能力。 因此,选择副干酪乳杆菌H2和植物乳植杆菌LP混合强化发酵红酸汤,研究其在解酒护肝方面的潜力与生物活性。
2.2 混菌强化发酵红酸汤的解酒护肝功效研究
2.2.1 混菌强化发酵红酸汤对酒精干预后小鼠的醉酒潜伏期和醒酒时间的影响
混菌强化发酵红酸汤对酒精干预后小鼠的醉酒潜伏期和醒酒时间的影响见图1。
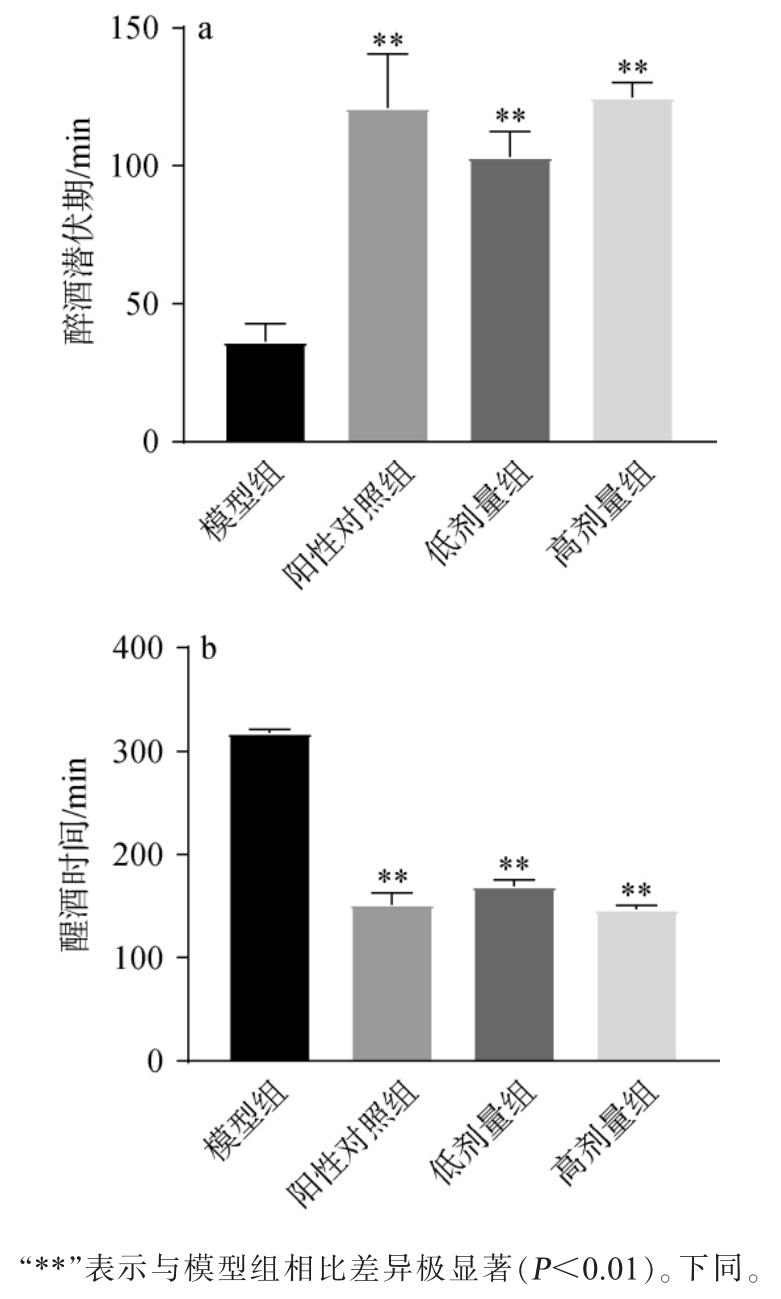
图1 不同剂量混菌强化发酵红酸汤对酒精干预后小鼠的醉酒潜伏期(a)和醒酒时间(b)的影响
Fig. 1 Effect of different doses of fermented red sour soup enhanced with mixed bacteria on the drunken incubation period (a) and sober time (b) of mice after alcohol intervention
由图1a可知,相较于模型组,阳性对照组、低剂量组和高剂量组小鼠的醉酒潜伏期均极显著升高(P<0.01),醉酒潜伏期由(36.21±6.53)min分别延长至(120.95±19.55)min、(103.16±9.30)min和(124.93±5.38)min。 由图1b可知,相较于模型组,阳性对照组、低剂量组和高剂量组小鼠的醒酒时间均极显著缩短(P<0.01),醒酒时间由(317.89±2.96)min分别缩短至(151.40±11.30)min、(169.10±6.23)min和(146.80±3.74)min。高剂量组与阳性对照组小鼠的醉酒和醒酒时间无显著差异(P>0.05)。结果表明,混菌强化发酵红酸汤能够延长小鼠的醉酒潜伏期,缩短醒酒时间,对小鼠摄入的酒精有较好的代谢作用,减弱了酒精的作用时长,加速了醒酒过程,减轻了酒精对机体的损伤。
2.2.2 混菌强化发酵红酸汤对小鼠肝脏指数的影响
肝脏指数是评价肝脏是否受到损伤的指标之一,因为在摄入酒精后,可能会对肝脏造成损伤,进而引起肝脏肿大[18-19]。混菌强化发酵红酸汤对小鼠肝脏指数的影响见图2。由图2可知,与空白对照组相比,模型组小鼠的肝脏指数极显著升高13.41%(P<0.01);与模型组相比,阳性对照组、低剂量组和高剂量组小鼠的肝脏指数均下降,且阳性对照组与低剂量组小鼠的肝脏指数极显著下降(P<0.01)。结果表明,各剂量的混菌强化发酵红酸汤可以在不同程度上缓解酒精干预后小鼠肝脏肿大的问题。
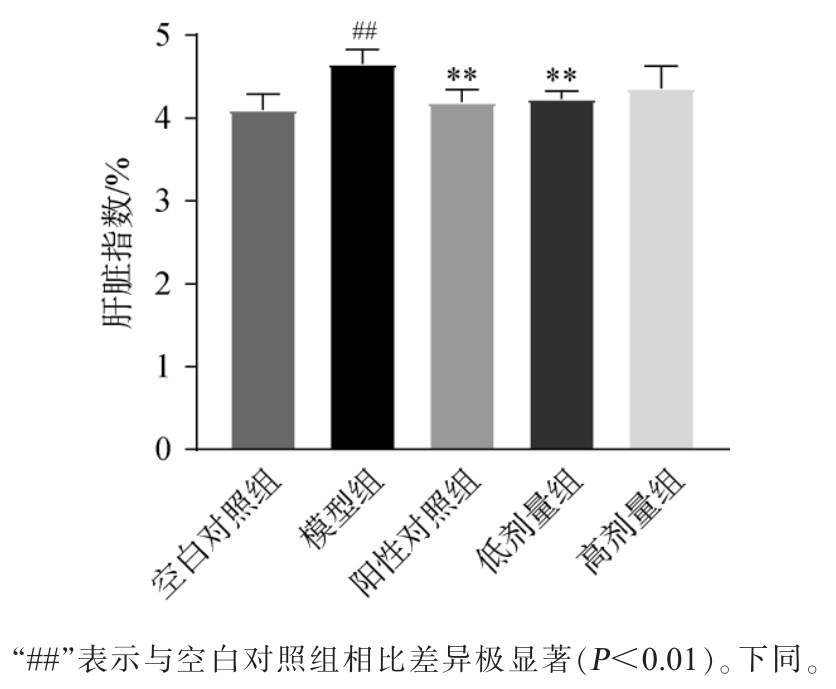
图2 混菌强化发酵红酸汤对小鼠肝脏指数的影响
Fig. 2 Effect of fermented red sour soup enhanced with mixed bacteria on liver indexes of mice
2.2.3 混菌强化发酵红酸汤对小鼠肝脏中ADH活性的影响
ADH是肝脏中主要的乙醇代谢酶,其活力变化直接反映了酒精代谢的效率[17,20]。因此,考察混菌强化发酵红酸汤对小鼠肝脏ADH活力的影响,结果见图3。由图3可知,与空白对照组相比,模型组小鼠肝脏中ADH活力极显著降低(P<0.01);与模型组相比,阳性对照组和高剂量组小鼠肝脏的ADH活力均极显著升高(P<0.01),低剂量组无显著变化(P>0.05)。 高剂量组小鼠肝脏的ADH活力由(3.13±1.41)U/mL提升至(6.30±0.75)U/mL,升高101.53%。表明高剂量混菌强化发酵红酸汤能够提升小鼠肝脏ADH的活力,加速乙醇的代谢过程,减少酒精在体内的积累,减轻酒精对肝脏及其他器官的负面影响。
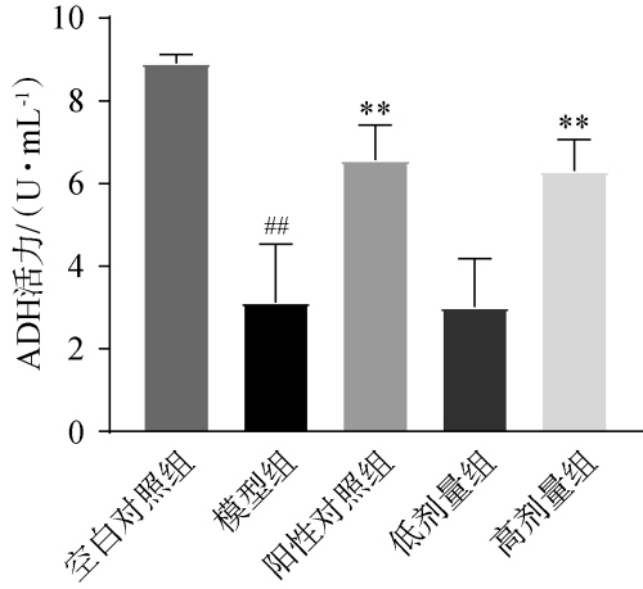
图3 混菌强化发酵红酸汤对小鼠肝脏乙醇脱氢酶活力的影响
Fig. 3 Effect of fermented red sour soup enhanced with mixed bacteria on the activities of alcohol dehydrogenase in mouse liver
2.2.4 混菌强化发酵红酸汤对小鼠血清中ALT及AST活力的影响
ALT和AST是主要分布于肝细胞中的转氨酶,当肝脏细胞受到损伤后,这两种酶会进入血液[21-22],因此,测定血清中ALT和AST活力水平来评估肝脏的健康状态[16]。 混菌强化发酵红酸汤对酒精干预后小鼠血清中ALT和AST活力的影响见图4。由图4可知,相对于空白对照组,模型组小鼠血清中的ALT和AST活力均极显著升高(P<0.01),ALT活力由(4.17±1.37)U/L增高至(11.37±2.61)U/L,AST活力由(13.93±1.68)U/L增高至(28.42±4.13)U/L。 与模型组相比,阳性对照组和两个剂量组小鼠血清中的ALT活力均降低,但并无显著性差异(P>0.05);阳性对照组和两个剂量组小鼠血清中的AST活力均降低,且高剂量组小鼠血清中的AST活力极显著降低(P<0.01),AST活力降低了56.88%。结果表明,混菌强化发酵红酸汤对酒精干预后小鼠肝脏有一定程度的保护作用,高剂量组的混菌强化发酵红酸汤对酒精干预小鼠血清中AST水平影响较大。
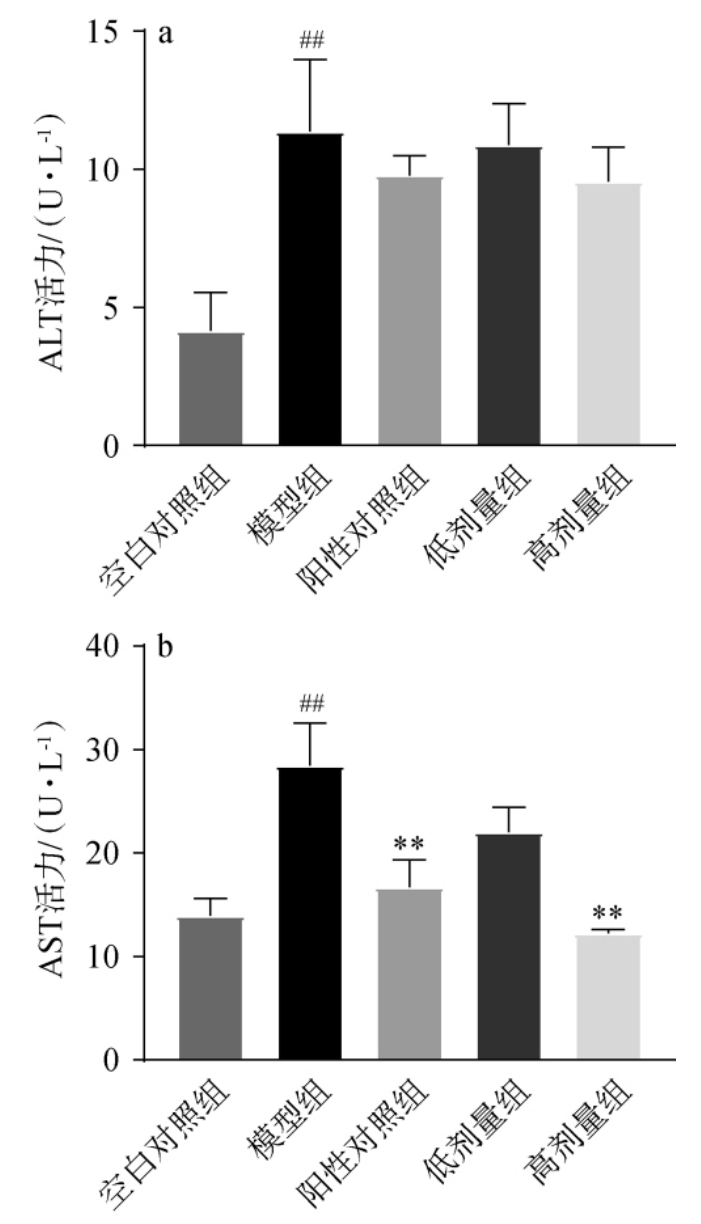
图4 混菌强化发酵红酸汤对小鼠血清中谷丙转氨酶(a)和谷草转氨酶(b)活力的影响
Fig. 4 Effect of fermented red sour soup enhanced with mixed bacteria on alanine aminotransferase (a) and aspartate aminotransferase (b) activities in mouse serum
2.2.5 混菌强化发酵红酸汤对小鼠肝脏中SOD、MDA及TG水平的影响
乙醇的摄入不仅会对乙醇代谢系统造成影响,还会打乱机体内氧化与抗氧化系统的平衡状态[23]。 研究表明,乙醇介导的氧化应激消耗了SOD等抗氧化物,使肝脏细胞内脂肪酸氧化受限,游离脂肪酸堆积,继而TG含量上升,并引发肝细胞膜脂质过氧化,MDA即由脂质过氧化产生[24-25]。MDA含量升高会干扰抗氧化预防,引起肝脏损伤。SOD作为抗氧化剂,起到清除体内多余自由基的作用,将其转化为氧和水排出体外,保护肝脏以免受到氧化应激的损伤[26]。混菌强化发酵红酸汤对酒精干预后小鼠肝脏的SOD、MDA和TG水平的影响见图5。
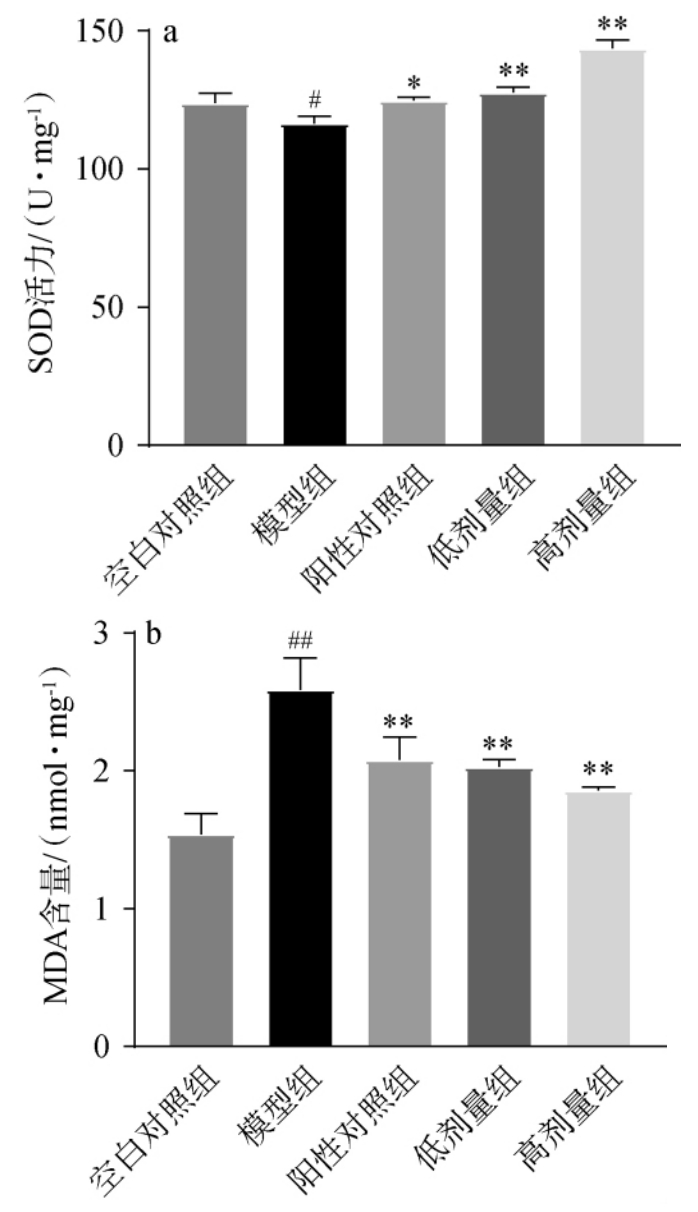
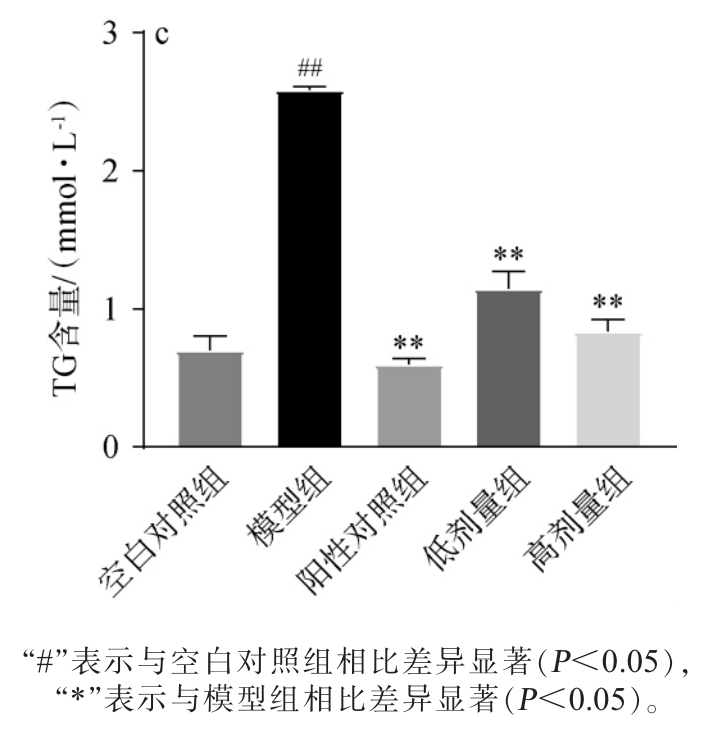
图5 混菌强化发酵红酸汤对小鼠肝脏超氧化物歧化酶(a)、丙二醛(b)和甘油三酯(c)含量的影响
Fig. 5 Effect of fermented red sour soup enhanced with mixed bacteria on superoxide dismutase (a), malondialdehyde(b) and triglyceride (c) contents in mouse liver
由图5可知,相较于空白对照组,模型组小鼠肝脏的SOD活力显著下降(P<0.05)、MDA和TG含量极显著升高(P<0.01),这一现象可能是由于小鼠肝脏已经受到损伤,肝脏抗氧化能力下降。 相较于模型组,阳性对照组小鼠肝脏SOD活力显著升高(P<0.05),低剂量组和高剂量组小鼠肝脏的SOD活力均极显著升高(P<0.01),分别提高7.01%、9.52%、23.17%;各组小鼠肝脏的MDA和TG含量均极显著下降(P<0.01),MDA和TG含量分别降低19.59%、21.58%、28.31%和76.78%、55.69%、67.60%。 结果表明,使用混菌强化发酵红酸汤后,酒精干预后小鼠肝脏中SOD、MDA和TG与模型组相比都有明显的改善效果,说明发酵红酸汤可通过增加机体内抗氧化能力,缓解肝脏氧化应激。
2.2.6 混菌强化发酵红酸汤对小鼠肝组织病理形态的影响
小鼠肝组织HE染色的显微结果见图6。由图6可知,空白对照组和阳性对照组小鼠肝脏切片显示正常的生理结构,肝脏外观平整,无病变;而模型组小鼠则出现了明显的肝细胞排列紊乱、细胞肿胀及空泡变性等病理变化。 低剂量组小鼠肝脏虽仍可见空泡变性,但其程度明显减轻,表明低剂量混菌发酵红酸汤对肝脏损伤有一定的缓解作用。高剂量组小鼠肝脏切片几乎恢复正常,仅见少量微小空泡,肝细胞结构接近正常,显示出极为显著的修复效果。结果表明,不同剂量的混菌强化发酵红酸汤能够有效减轻急性酒精性肝损伤,且高剂量具有更好的修复作用。
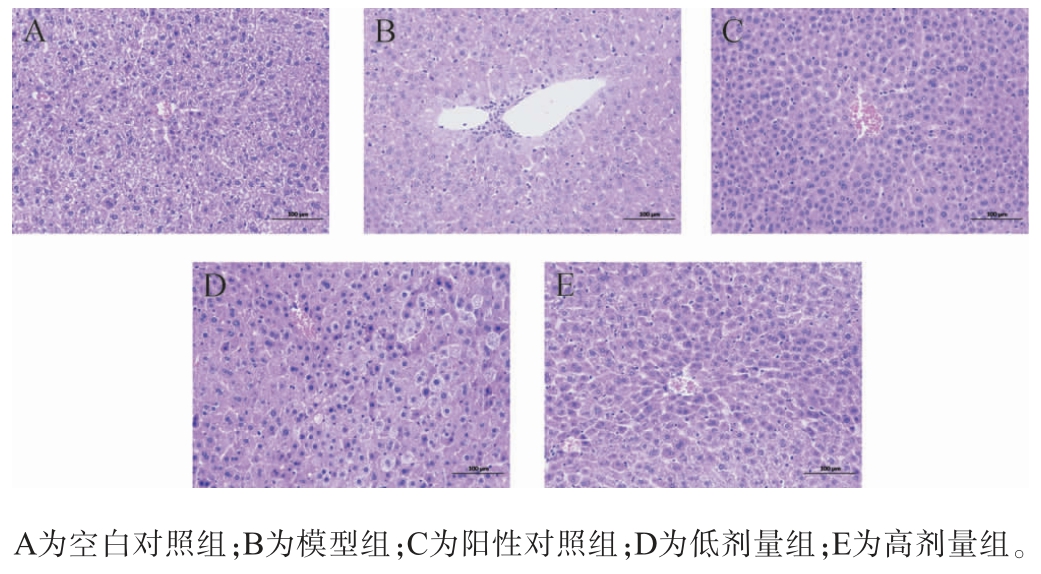
图6 小鼠肝组织苏木精-伊红染色的显微结果
Fig. 6 Microscopic results of hematoxylin-eosin staining of liver tissue in mice
3 结论
本研究筛选得到两株具有较好耐乙醇和降解乙醇能力的植物乳植杆菌(Lactiplantibacillus plantarum)LP和副干酪乳杆菌(Lactobacillus paracasei)H2。 将这两株菌按照1∶1的比例混合强化发酵红酸汤并灌胃小鼠后,发现混菌强化发酵红酸汤具有明显的解酒和护肝功能。 与模型组相比,各剂量组均极显著缩短小鼠醒酒时间(P<0.01);高剂量组小鼠肝脏的ADH活力极显著升高101.53%(P<0.01),血清的AST活力极显著降低56.88%(P<0.01);低剂量组小鼠肝脏指数极显著降低(P<0.01);低、高剂量组小鼠肝脏的SOD活力分别极显著升高9.52%、23.17%(P<0.01),MDA和TG含量分别极显著降低21.58%、28.31%和55.69%、67.60%(P<0.01);各剂量组小鼠酒精诱导的肝脏病变减轻,且高剂量组小鼠肝脏修复效果最好。 综上,该混菌强化发酵红酸汤不仅能加速酒精代谢,缩短酒精作用时长,还能减轻酒精引起的肝脏损伤、改善脂质代谢、增强肝脏抗氧化能力,进而发挥解酒护肝作用,为乳酸菌发酵食品提高抗氧化能力和防治酒精性肝损伤提供理论支持。
[1] KUPRYS P V,CANNON A R,SHIEH J,et al.Alcohol decreases intestinal ratio of Lactobacillus to Enterobacteriaceae and induces hepatic immune tolerance in a murine model of DSS-colitis[J] .Gut Microbes,2020,12(1):1-16.
[2] 厉有名,范建高. 酒精性肝病防治指南(2018年更新版)[J] . 实用肝脏病杂志,2018,21(2):23-29.
[3] 居金明.胡柚葛根发酵饮料加工工艺及其解酒功效研究[D] .南京:南京农业大学,2020.
[4] 李冬梅,李晴晖,李宝玉,等. 藤茶解酒功能发酵乳的制备及功效评价[J] .中国酿造,2025,44(2):128-135.
[5] 钱籽霖.乳酸菌发酵拐枣汁工艺优化及抗氧化活性评价[D] .重庆:西南大学,2019.
[6] 任佳妮. 解酒功能益生菌发酵苹果汁制备及其功能评价[D] . 杨凌:西北农林科技大学,2024.
[7] 王楠. 枳椇乳酸菌发酵饮料对小鼠酒精肝损伤的保护作用[D] . 杨凌:西北农林科技大学,2016.
[8] 谢子军.乳酸菌发酵夏茶解酒保肝功能研究及产品研发[D] .南昌:南昌大学,2023.
[9] 宫路路,李洁,明婷,等.产酸乳酸菌红酸汤发酵研究[J] .廊坊师范学院学报(自然科学版),2024,24(2):72-76.
[10] 胡诗瑶,袁钦,郑远翠,等. 贵州红酸汤对高脂饮食大鼠脂质代谢的影响[J] .中国酿造,2025,44(3):100-106.
[11] 周绍琴,李凤兰,吴映梅,等. 红酸汤的抗氧化活性研究[J] . 中国调味品,2021,46(7):17-21.
[12] 秦伟军,包爱明,陈兴兴,等. 贵州红酸汤产业关键技术升级与应用发展[J] .中国酿造,2024,43(1):261-266.
[13] 许九红.贵州红酸汤品质影响因素研究及风味品质变化分析[D] .贵阳:贵州大学,2024.
[14] 杨小柏.乙醇降解菌的筛选及特性研究[D] .重庆:重庆大学,2005.
[15] JUAN M H,BRUNO C F,JOSE V P.Preventing and mitigating alcohol toxicity:A review on protective substances[J] .Beverages,2018,4(2):39.
[16] 田颖蕾,夏婷,康超艳,等. 山西老陈醋对急性醉酒小鼠防醉及护肝作用研究[J] .中国酿造,2021,40(12):40-44.
[17] 卓鑫鑫,邓丽萍,何冰浩,等. 解酒机制及解酒产品研究进展[J] . 中国酿造,2024,43(2):22-28.
[18] 王月. 甘草次酸介导的芍药苷海藻酸锌纳米凝胶抗急性肝损伤研究[D] .天津:天津中医药大学,2022.
[19] 章秀莉,陈雅婧,郑志鸿,等.牡蛎蛋白肽对急性酒精性肝损伤的保护作用及活性肽筛选[J] .食品科学,2025,46(11):198-207.
[20] GIRIWONO P E, HASHIMOTO T, OHSAKI Y, et al. Extract of fermented barley attenuates chronic alcohol induced liver damage by increasing antioxidative activities[J] .Food Res Int,2010,43(1):118-124.
[21] PANELLI M F,PIERINE D T,DE SOUZA S L B,et al.Bark of Passiflora edulis treatment stimulates antioxidant capacity, and reduces dyslipidemia and body fat in db/db mice[J] . Antioxidants,2018,7(9):120.
[22] ZHANG Y, MA J, JING N, et al. Bifidobacterium animalis A12 and Lactobacillus salivarius M18-6 alleviate alcohol injury by keap1-Nrf2 pathway and thioredoxin system[J] .Foods,2023,12(3):439.
[23] 曹燕峰,常立炀,张修正,等. 海湾扇贝抗氧化肽对酒精性肝损伤的保护作用[J] .食品科学,2024,45(19):87-93.
[24] LIOCHEV S I. Reactive oxygen species and the free radical theory of aging[J] .Free Radic Biol Med,2013,60:1-4.
[25] JUNG H A,ABDUL,Q A,BYUN,J S,et al.Protective effects of flavonoids isolated from Korean milk thistle Cirsium japonicum var.maackii(Maxim.)Matsum on tert-butyl hydroperoxide-induced hepatotoxicity in HepG2 cells[J] .J Ethnopharmacol,2017,209:62-72.
[26] AHN C B, KIM J G, JE J Y. Purification and antioxidant properties of octapeptide from salmon byproduct protein hydrolysate by gastrointestinal digestion[J] .Food Chem,2014,147:78-83.