馥香型白酒是以高粱、大米、糯米、小麦为酿酒原料,高温大曲、麸曲、细菌曲、酿酒酵母(Saccharomyces cerevisiae)和生香酵母为糖化发酵剂,经润料、蒸粮、配醅、堆积、入池发酵和蒸酒等工序酿制而成[1]。在其工艺特点上,融合了酱香、浓香和芝麻香型白酒的生产工艺,因此,酒体既有酱香的醇厚感,又有窖香的绵甜感,以及芝麻香的细腻感,呈现舒适、幽雅、爽净特征,深受消费者喜爱。
微生物代谢是白酒风味物质产生的基础,采用微生物强化技术,将功能菌株作为一种生物强化剂应用于白酒发酵过程是白酒现代化工艺改进和品质提升的重要手段,具有很好的发展潜力[2]。其在浓香、酱香等多种香型白酒中均有应用且取得了一些成果,菌株选育、强化大曲、人工老窖技术等是白酒提质增香的重要方面[3]。倪冰倩等[4]从酱香型白酒酒醅中筛选获得了重要风味物质乙酸苯乙酯的高产菌株,具有提升乙酸苯乙酯等多种风味物质含量的性能。芽孢杆菌属(Bacillus)菌株在制曲、堆积工艺过程起到重要作用,凌杰等[5]通过构建共培养体系,明确了地衣芽孢杆菌(Bacillus licheniformis)与Saccharomyces cerevisiae之间的相互作用关系。罗莉等[6]系统分析了芽孢杆菌在中国白酒酿造中的应用机理,为该类功能菌株的应用起到了指导作用。吕磊等[7]通过培养基筛选和挥发性风味物质分析,研究发现芝麻香型白酒关键菌株地衣芽孢杆菌和枯草芽孢杆菌(Bacillus subtilis)对芝麻香型白酒风味具有重要贡献。刘宇等[8]通过优化包括多种芽孢杆菌在内的菌种组合强化酱香大曲,结果提高了酱香型白酒的酱香、空杯留香、细腻度和典型性等感官品质。胡峰[9]采用生香微生物复合强化大曲和窖泥,提高了己酸乙酯生成速率和优质品率。张志伟等[10]根据北方酱香型白酒的特点,强化了芽孢杆菌属、酯化酵母等3种菌株,证实了强化菌株在多菌种发酵体系中能够很好存活,并提高了多种酯类和吡嗪类物质含量。此外,工艺的差异赋予了酒体不同的风格,风味物质与酒体感官品评相结合已经被广泛应用于工艺优化效果的评价[11-16]。馥香型白酒兼具高温大曲、堆积、泥窖等多种香型工艺特点,然而,馥香型白酒作为创新香型,生物强化技术对其风味感官的影响尚且缺乏深入研究。
基于地衣芽孢杆菌在白酒风味贡献中的重要作用,结合馥香型白酒生产工艺,本研究采用高通量测序、气相色谱(gas chromatography,GC)和感官品评等技术,研究地衣芽孢杆菌强化技术对馥香型白酒发酵过程中微生物群落结构、挥发性风味物质及感官品质的影响,对提升馥香型白酒工艺优化和酒体品质具有重要意义。
1 材料与方法
1.1 材料与试剂
1.1.1 菌株
地衣芽孢杆菌(Bacillus licheniformis)HTY-1:筛选自馥香型白酒高温大曲,保藏于国家酒类品质与安全国际联合研究中心菌种资源库。
1.1.2 试剂
E.Z.N.A.Soil脱氧核糖核酸(deoxyribonucleic acid,DNA)Kit试剂盒:上海索莱宝生物科技有限公司;Phusion⑥High-Fidelity聚合酶链式反应(polymerase chain reaction,PCR)Master Mix:美国New England Biolabs公司;乙酸乙酯、乳酸乙酯、正丙醇、乙醛、乙缩醛等标准品(均为色谱纯):美国Sigma-Aldrich公司;其他试剂均为国产分析纯或生化试剂。
1.1.3 培养基
LB固体培养基:胰蛋白胨10.0 g/L,酵母提取物5.0 g/L,氯化钠10.0 g/L,琼脂15.0 g/L,121 ℃高压蒸汽灭菌20 min。LB液态培养基:LB固体培养基中不添加琼脂。
1.2 仪器与设备
BSA224S电子分析天平:德国Sartorius公司;Gen Pure UV/UF超纯水系统:美国ThermoFisherScientific公司;Clarns 600气相色谱仪[配火焰离子检测器(flame ionization detector,FID)] :美国Perkin Elmer公司。
1.3 方法
1.3.1 地衣芽孢杆菌强化
采用无菌操作技术,从甘油管中取枯草芽孢杆菌HTY-1菌液100 μL,涂布接种于LB固体培养基中,置于37 ℃恒温培养箱培养48 h,备用。挑取地衣芽孢杆菌单菌落接种至装液量为50 mL/250 mL LB液体培养基中,37 ℃、200 r/min条件下活化培养12 h。再以2%(V/V)的接种量接种至装液量为50 mL/250 mLLB液体培养基中,37 ℃、200 r/min条件下培养24 h得到种子液(活菌数为7×108 CFU/mL)。在25.0 L种子液中加入30~35 ℃的温水至总质量为100 kg后接种至馥香型白酒粮醅中,收拢聚堆(收堆温度25~30 ℃),堆积成四棱台,高度为80 cm,依次进行自然堆积发酵和入池发酵,即为强化组。 以加入与种子液等体积的无菌水为对照组。采用五点取样法,于距离堆积堆子上表面约30 cm处,分别在堆积发酵前和堆积发酵后取堆积酒醅样品,在出窖时取窖池中层酒醅为出窖酒醅样品,取样量约500 g,样品在-80 ℃保藏备用。强化组和对照组发酵完成的酒醅,经车间蒸馏工序,获得对应馥香型白酒基酒,取500 mL备用。
1.3.2 微生物宏基因组提取及高通量测序
采用E.Z.N.A.Soil DNA Kit试剂盒提取酒醅微生物宏基因组DNA[17],以其为模板对细菌16S rRNA V3-V4区及真菌ITS区基因序列进行PCR扩增。PCR扩增体系:15 μL Phusion⑥High-Fidelity PCR Master Mix、0.2 μmol/L引物和10 ng基因组DNA。PCR扩增程序:98 ℃预变性1 min;98 ℃变性10 s,50 ℃退火30 s,72 ℃延伸30 s,共循环30次;72 ℃下再延伸5 min。 细菌PCR所用引物为341F(5'-CCTAYGGGRBGCASCAG-3')和806R(5'-GGACTACNNGGGTATCTAAT-3');真菌PCR扩增所用引物为ITS3-2024F(5'-GCATCGATGAAGAACGCAGC-3')和ITS4-2409R(5'-TCCTCCGCTTATTGATATGC-3')。 PCR扩增产物委托天津诺和致源生物信息科技有限公司采用Illumina Miseq PE250高通量测序平台进行高通量测序。
下机数据经拼接、过滤、剔除嵌合体,舍弃低质量序列等得到clean tags,利用USEARCH(v11.0.667)对clean tags进行过滤和分析,按97%的相似性划分操作分类单元(operational taxonomic unit,OTU),提取OTU代表序列获得丰度表,细菌使用SILVA138数据库进行物种注释,真菌使用UNITE(v8.2)数据库进行物种注释。 测序数据利用Mothur(v1.42.1)进行均一化处理后,使用QIIME2软件计算Alpha多样性指数。
1.3.3 挥发性风味物质的测定及OAV分析
采用气相色谱法检测馥香型白酒基酒中的骨架挥发性风味物质[18],并计算气味活度值(odor activity value,OAV),OAV是酒体中某一风味物质质量浓度与其阈值的比值,一般OAV>1时,表明该化合物对风味有贡献,是关键风味化合物。OAV越大,表明该化合物对白酒风味贡献越大。
1.3.4 有机酸含量的测定
白酒中有机酸的含量采用离子色谱法(ion chromatography,IC)进行测定[19]。
1.3.5 感官品评方法
馥香型白酒成品酒一般从香气(酱香、复合酯香、醇香等)、口感(酸味、苦味、涩味等)和风格(爽净感、绵甜感、丰满感等)3个方面共30个维度评价其品质特征[1]。 针对本研究中的样品为新蒸馏出的馥香型白酒基酒,采用感官维度中代表馥香型白酒典型特征的8个维度进行感官评价,即酱香、花果香、窖香、芝麻香、回味、绵甜感、丰满感和馥合感。
由10名品酒技术人员(包含3名国家评委)组成评价小组,在白酒品评室内进行感官品评。将基酒依次倒入50 mL的标准品评杯中品尝,每次品尝微量,品尝完漱口进行下一基酒品尝,确立描述术语,并进行打分,打分范围为0~9分。品评规则:0—没有味道;1分—刚能察觉,难以辨识;2分—非常轻;3分—较轻;4~5分—中等;6~7分—较强;8~9分—主导。
1.3.6 数据处理与统计分析
采用OriginPro9.1及Excel2016绘图;采用CANOCOV4.56软件进行主成分分析(principal component analysis,PCA);采用IBMSPSS Statistics 24.0软件处理数据并进行差异显著性分析。
2 结果与分析
2.1 地衣芽孢杆菌强化对酒醅发酵过程中微生物群落多样性的影响
2.1.1 细菌菌群Alpha多样性及群落结构分析
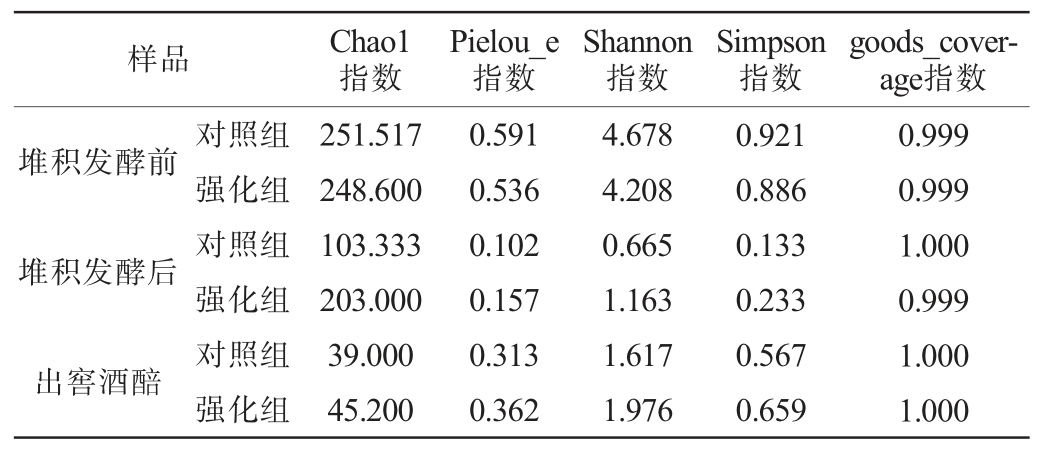
采用高通量测序技术对发酵过程中酒醅样品中的细菌菌群α多样性进行分析,结果见表1。由表1可知,所有样本的goods_coverage指数均在0.999以上,说明测序结果能较好地代表样本中细菌菌群的真实情况。堆积发酵前对照组和强化组酒醅细菌菌群的α多样性指数差异不明显,经堆积和入池发酵后,对照组和强化组酒醅细菌菌群的α多样性指数相差较大,且强化组的Chao1指数、Pielou_e指数、Shannon指数和Simpson指数均高于对照组,说明强化组的细菌群落结构的丰富度、均匀度和多样性更高,地衣芽孢杆菌强化明显提高了细菌菌群多样性。
表1 地衣芽孢杆菌强化对酒醅发酵过程中细菌菌群α多样性的影响
Table 1 Effect of Bacillus licheniformis enhancement on α-diversity of bacterial community in fermented grains during fermentation process
样品Chao1指数Pielou_e指数Shannon指数Simpson指数goods_coverage指数堆积发酵前堆积发酵后出窖酒醅对照组强化组对照组强化组对照组强化组251.517 248.600 103.333 203.000 39.000 45.200 0.591 0.536 0.102 0.157 0.313 0.362 4.678 4.208 0.665 1.163 1.617 1.976 0.921 0.886 0.133 0.233 0.567 0.659 0.999 0.999 1.000 0.999 1.000 1.000
进一步在属水平上对酒醅发酵过程中细菌群落结构进行分析,结果见图1。由图1可知,相对丰度较大的细菌属有乳酸杆菌属(Lactobacillus)、芽孢杆菌属(Bacillus)、寡养单胞菌属(Stenotrophomonas)、代尔夫特菌属(Delftia)、金黄杆菌属(Chryseobacterium)、葡萄球菌属(Staphylococcus)、魏斯氏菌属(Weissella)、链霉菌属(Streptomyces)和糖多孢菌属(Saccharopolyspora)。 其中,芽孢杆菌属、乳酸杆菌属、魏斯氏菌属和葡萄球菌属为优势菌群,在堆积发酵和入池发酵过程中发生明显演替。
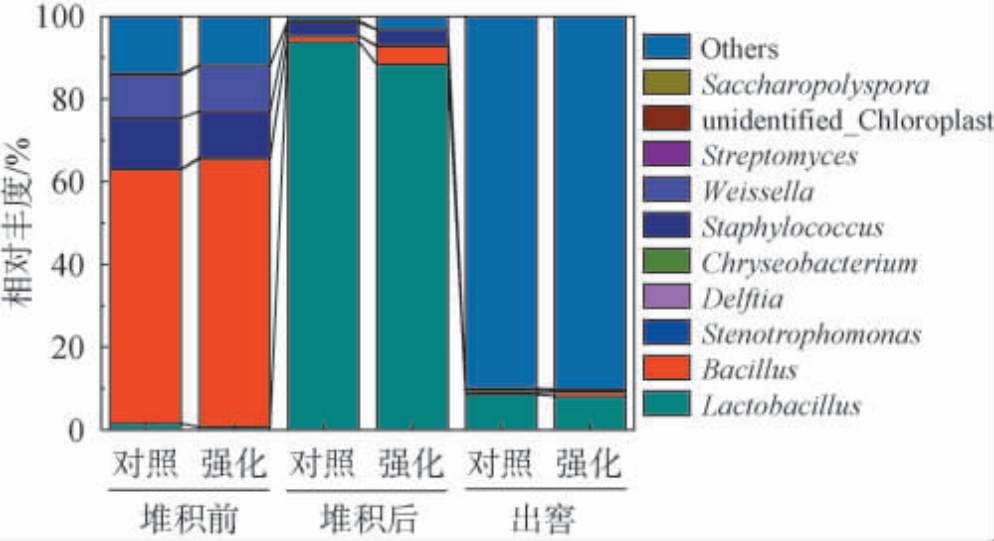
图1 基于属水平地衣芽孢杆菌强化对酒醅发酵过程中细菌群落结构的影响
Fig. 1 Effect of Bacillus licheniformis enhancement on bacterial community structure in fermented grains during fermentation process at the genus level
堆积发酵前,芽孢杆菌属相对丰度最高,是堆积前酒醅中的主导菌群,强化组芽孢杆菌属的相对丰度比对照组提高了3.56%。经过堆积发酵过程,在堆积发酵后酒醅中乳酸杆菌属相对丰度最高,演变成为新的主导菌群,此外,相对丰度较高的还有芽孢杆菌属和寡养单胞菌属,强化组芽孢杆菌属的相对丰度为4.35%,是对照组的3.07倍,即地衣芽孢杆菌的强化能够显著提高堆积发酵过程中芽孢杆菌的相对丰度,这与α多样性分析结果一致。堆积完成的酒醅开启入池发酵过程,出窖酒醅中相对丰度最高的仍然是乳酸杆菌属,芽孢杆菌属的相对丰度均降低至1%以下,对入池发酵过程的影响相对较小。
2.1.2 真菌菌群Alpha多样性及群落结构分析
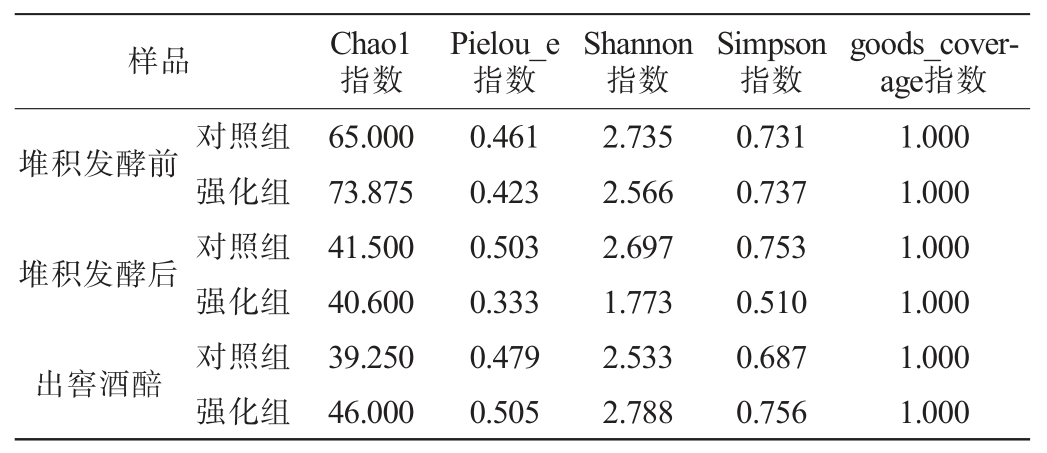
采用高通量测序技术对发酵过程中酒醅样品中的真菌菌群α多样性进行分析,结果见表2。 由表2可知,所有样本的goods_coverage指数均为1.000,说明测序结果能较好地代表样本中真菌菌群的真实情况。堆积发酵前,强化组Chao1指数明显高于对照组,而Pielou_e指数、Shannon指数和Simpson指数差异不明显,说明堆积发酵前强化组酒醅真菌菌群丰富度较高,而真菌菌群均匀度、多样性与对照组差异较小。堆积发酵后,强化组Chao1指数与对照组无明显差异,而Pielou_e指数、Shannon指数和Simpson指数明显低于对照组,说明堆积发酵后强化组酒醅真菌菌群均匀度、多样性与对照组降低,而丰富度无明显差异。 营养物质在酵母生长中起主要作用,真菌菌群多样性降低可能与芽孢杆菌对不同酵母的生长抑制效应有关[20]。出窖酒醅中Chao1指数等4个α多样性指数值均呈现强化组高于对照组,即出窖酒醅中强化组真菌菌群在丰富度、均匀度和多样性方面均高于对照组。
表2 地衣芽孢杆菌强化对酒醅发酵过程中真菌菌群α多样性的影响
Table 2 Effect of Bacillus licheniformis enhancement on α-diversity of fungal community in fermented grains during fermentation process
样品Chao1指数Pielou_e指数Shannon指数Simpson指数goods_coverage指数堆积发酵前堆积发酵后出窖酒醅对照组强化组对照组强化组对照组强化组65.000 73.875 41.500 40.600 39.250 46.000 0.461 0.423 0.503 0.333 0.479 0.505 2.735 2.566 2.697 1.773 2.533 2.788 0.731 0.737 0.753 0.510 0.687 0.756 1.000 1.000 1.000 1.000 1.000 1.000
进一步在属水平上对酒醅发酵过程中真菌群落结构进行分析,结果见图2。由图2可知,相对丰度较高的10个真菌属分别为伊萨酵母属(Issatchenkia)、曲霉属(Aspergillus)、克鲁维酵母属(Kluyveromyces)、哈萨克斯坦酵母属(Kazachstania)、根霉属(Rhizopus)、热子囊菌属(Thermoascus)、嗜热真菌属(Thermomyces)、覆膜孢酵母属(Saccharomycopsis)、念珠菌属(Diutina)和青霉菌属(Penicillium),是馥香型白酒堆积和窖池发酵过程中的主要真菌属。
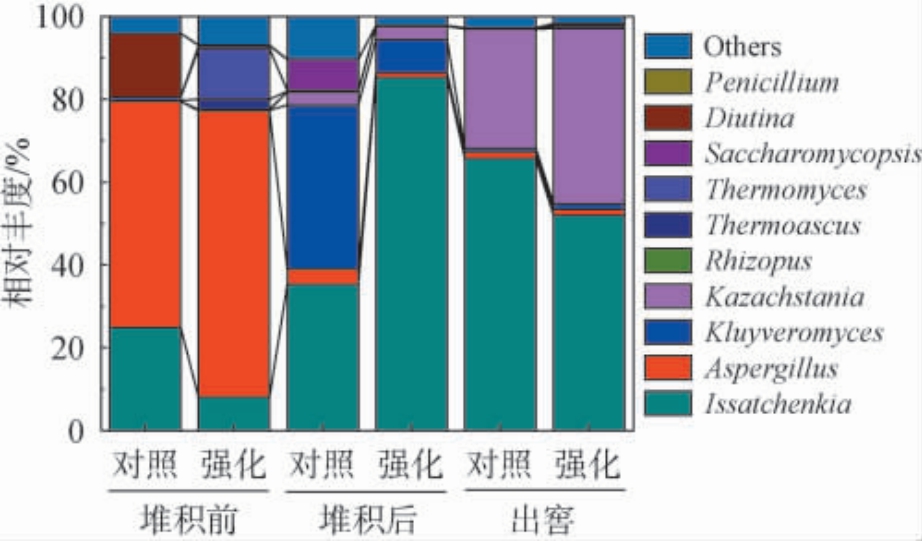
图2 基于属水平地衣芽孢杆菌强化对酒醅真菌群落结构的影响
Fig. 2 Effect of Bacillus licheniformis enhancement on fungal community structure in fermented grains during fermentation process at the genus level
堆积发酵前,对照组和强化组酒醅均以曲霉属为主导菌群,相对丰度较高的还有伊萨酵母属、念珠菌属和嗜热真菌属。 堆积发酵结束,对照组酒醅中相对丰度最高的两种真菌属分别为伊萨酵母属和克鲁维酵母属,两者的相对丰度分别为35.26%和39.62%,为对照组酒醅的主导菌群,相对丰度较高的还有覆膜孢酵母属。强化组酒醅中相对丰度最高的为伊萨酵母属(85.23%),是强化组酒醅的主导菌群,此外,相对丰度较高的还有克鲁维酵母属。强化组和对照组相比,真菌属相对丰度发生较大变化,这可能与地衣芽孢杆菌强化菌株对于不同真菌具有不同的生长促进和抑制有关[5,20-21]。 出窖酒醅中,对照组和强化组中伊萨酵母属的相对丰度分别为65.65%和52.00%,均为出窖酒醅中的主导真菌。 相对丰度较高的真菌属还包括哈萨克斯坦酵母属,在对照组和强化组酒醅中的相对丰度相差较大,分别为28.81%和42.35%,也是出窖酒醅中的优势菌群之一。
2.2 地衣芽孢杆菌强化对馥香型白酒基酒挥发性风味物质的影响
采用GC检测对照组和强化组馥香型白酒基酒中挥发性风味物质的含量,并基于OAV>1对关键挥发性风味物质进行分析,结果见表3。
表3 地衣芽孢杆菌强化对馥香型白酒基酒挥发性风味物质含量及香气活性值的影响
Table 3 Effect of Bacillus licheniformis enhancement on the contents and odor activity values of volatile flavor compounds in Fu-flavor Baijiu base liquor
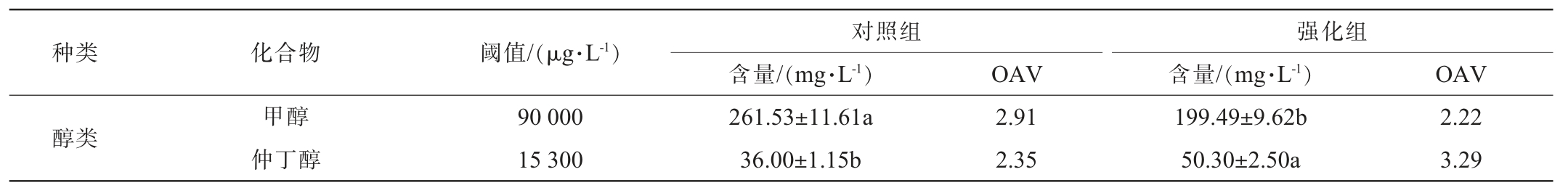
种类化合物阈值/(μg·L-1)醇类甲醇仲丁醇90 000 15 300对照组含量/(mg·L-1)261.53±11.61a 36.00±1.15b OAV强化组含量/(mg·L-1)OAV 2.91 2.35 199.49±9.62b 50.30±2.50a 2.22 3.29
续表
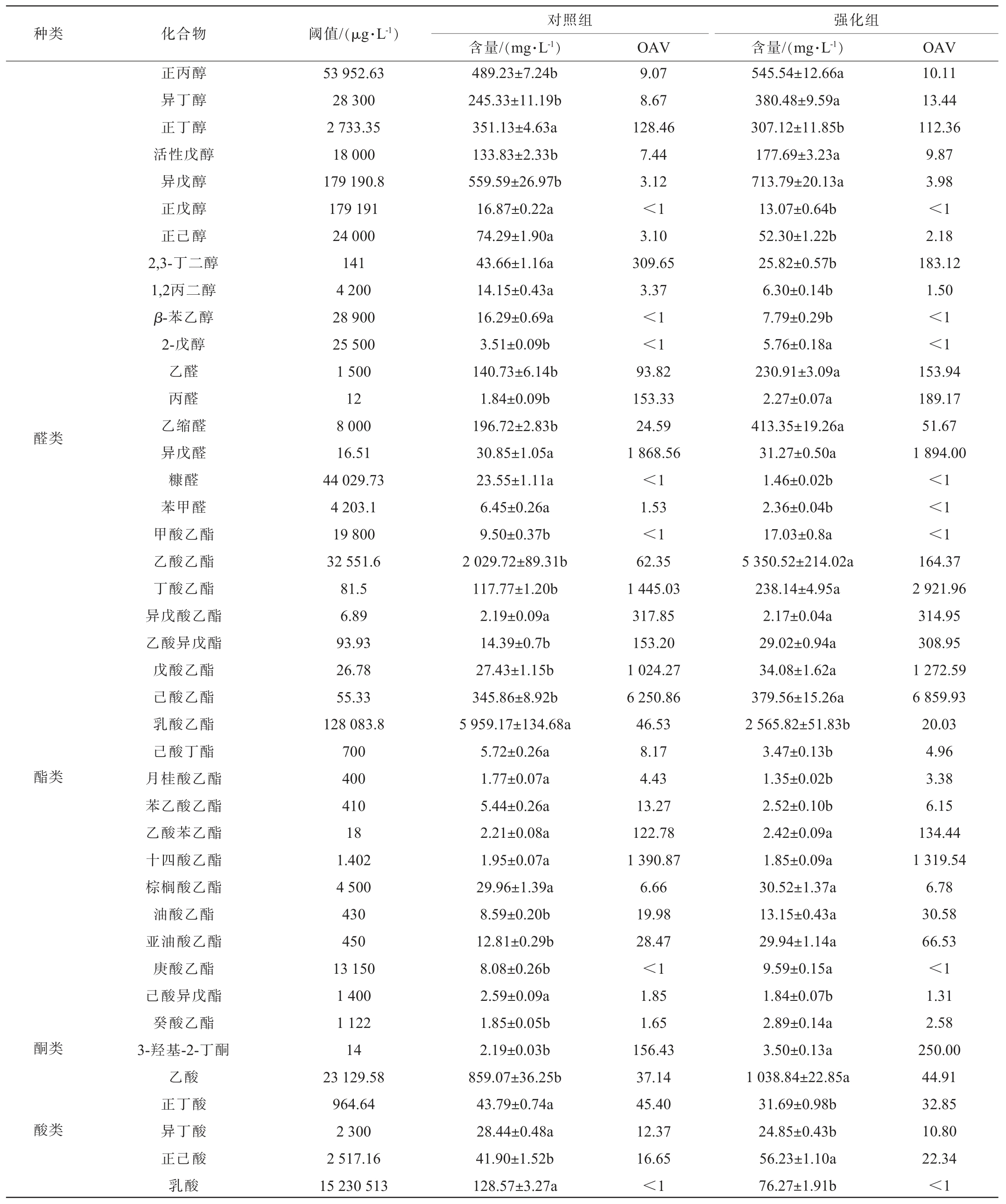
注:同行不同小写字母表示差异性显著(P<0.05)。
种类化合物阈值/(μg·L-1)醛类酯类酮类酸类正丙醇异丁醇正丁醇活性戊醇异戊醇正戊醇正己醇2,3-丁二醇1,2丙二醇β-苯乙醇2-戊醇乙醛丙醛乙缩醛异戊醛糠醛苯甲醛甲酸乙酯乙酸乙酯丁酸乙酯异戊酸乙酯乙酸异戊酯戊酸乙酯己酸乙酯乳酸乙酯己酸丁酯月桂酸乙酯苯乙酸乙酯乙酸苯乙酯十四酸乙酯棕榈酸乙酯油酸乙酯亚油酸乙酯庚酸乙酯己酸异戊酯癸酸乙酯3-羟基-2-丁酮乙酸正丁酸异丁酸正己酸乳酸53 952.63 28 300 2 733.35 18 000 179 190.8 179 191 24 000 141 4 200 28 900 25 500 1 500 12 8 000 16.51 44 029.73 4 203.1 19 800 32 551.6 81.5 6.89 93.93 26.78 55.33 128 083.8 700 400 410 18 1.402 4 500 430 450 13 150 1 400 1 122 14 23 129.58 964.64 2 300 2 517.16 15 230 513对照组含量/(mg·L-1)489.23±7.24b 245.33±11.19b 351.13±4.63a 133.83±2.33b 559.59±26.97b 16.87±0.22a 74.29±1.90a 43.66±1.16a 14.15±0.43a 16.29±0.69a 3.51±0.09b 140.73±6.14b 1.84±0.09b 196.72±2.83b 30.85±1.05a 23.55±1.11a 6.45±0.26a 9.50±0.37b 2 029.72±89.31b 117.77±1.20b 2.19±0.09a 14.39±0.7b 27.43±1.15b 345.86±8.92b 5 959.17±134.68a 5.72±0.26a 1.77±0.07a 5.44±0.26a 2.21±0.08a 1.95±0.07a 29.96±1.39a 8.59±0.20b 12.81±0.29b 8.08±0.26b 2.59±0.09a 1.85±0.05b 2.19±0.03b 859.07±36.25b 43.79±0.74a 28.44±0.48a 41.90±1.52b 128.57±3.27a OAV 9.07 8.67 128.46 7.44 3.12<1 3.10 309.65 3.37<1<1 93.82 153.33 24.59 1 868.56<1 1.53<1 62.35 1 445.03 317.85 153.20 1 024.27 6 250.86 46.53 8.17 4.43 13.27 122.78 1 390.87 6.66 19.98 28.47<1 1.85 1.65 156.43 37.14 45.40 12.37 16.65<1强化组含量/(mg·L-1)OAV 545.54±12.66a 380.48±9.59a 307.12±11.85b 177.69±3.23a 713.79±20.13a 13.07±0.64b 52.30±1.22b 25.82±0.57b 6.30±0.14b 7.79±0.29b 5.76±0.18a 230.91±3.09a 2.27±0.07a 413.35±19.26a 31.27±0.50a 1.46±0.02b 2.36±0.04b 17.03±0.8a 5 350.52±214.02a 238.14±4.95a 2.17±0.04a 29.02±0.94a 34.08±1.62a 379.56±15.26a 2 565.82±51.83b 3.47±0.13b 1.35±0.02b 2.52±0.10b 2.42±0.09a 1.85±0.09a 30.52±1.37a 13.15±0.43a 29.94±1.14a 9.59±0.15a 1.84±0.07b 2.89±0.14a 3.50±0.13a 1 038.84±22.85a 31.69±0.98b 24.85±0.43b 56.23±1.10a 76.27±1.91b 10.11 13.44 112.36 9.87 3.98<1 2.18 183.12 1.50<1<1 153.94 189.17 51.67 1 894.00<1<1<1 164.37 2 921.96 314.95 308.95 1 272.59 6 859.93 20.03 4.96 3.38 6.15 134.44 1 319.54 6.78 30.58 66.53<1 1.31 2.58 250.00 44.91 32.85 10.80 22.34<1
由表3可知,从馥香型白酒基酒中共检出44种主要挥发性风味物质,包括醇类13种、醛类6种、酸类5种、酯类19种和酮类1种。 强化组馥香型白酒基酒中的醇类、醛类、酸类和酮类物质含量均显著高于对照组(P<0.05),分别比对照组高10.69%、70.42%、11.89%和59.82%,酯类物质差异不显著(P>0.05)。 强化组馥香型白酒基酒中挥发性风味物质的总含量比对照组高6.38%,说明地衣芽孢杆菌强化提高了基酒中挥发性风味物质的总量,这可能与地衣芽孢杆菌促进整个发酵体系的糖及其衍生物代谢,进而提升挥发性风味物质产量有关[22]。
在醇类物质中,异戊醇含量最高,其次是正丙醇。 与对照组相比,强化组中含量显著提高的醇类物质有6种(P<0.05),分别是仲丁醇、正丙醇、异丁醇、活性戊醇、异戊醇和2-戊醇,其中含量提高较多的是异戊醇、异丁醇;含量显著降低的醇类物质有7种(P<0.05),分别是甲醇、正丁醇、正戊醇、正己醇、2,3-丁二醇、1,2丙二醇和β-苯乙醇,其中含量降低较大的是正丁醇和正己醇。在醛类物质中,乙醛和乙缩醛是含量较高的两种醛类物质。 与对照组相比,强化组含量显著提高的醛类物质有乙醛、丙醛和乙缩醛(P<0.05),其中含量提高较大的主要是乙醛和乙缩醛;含量显著降低的醛类物质是糠醛和苯甲醛(P<0.05)。在酸类物质中,乙酸是含量最高的有机酸,其次是乳酸。与对照组相比,强化组含量显著提高的有机酸分别是乙酸、正己酸(P<0.05),含量提高较多的是乙酸;含量显著降低的有机酸分别是正丁酸、异丁酸和乳酸(P<0.05),含量降低较多的是乳酸。在酯类物质中,含量较高的两种酯类物质是乙酸乙酯和乳酸乙酯,其次是己酸乙酯和丁酸乙酯,对照组和强化组中上述4种酯类含量之和占酯类物质总量的比例分别是98.43%和97.91%,是最主要的酯类物质。与对照组相比,强化组中酯类物质的含量变化较大,含量显著提高的酯类物质有甲酸乙酯、乙酸乙酯、丁酸乙酯、乙酸异戊酯、戊酸乙酯、己酸乙酯、油酸乙酯、亚油酸乙酯、庚酸乙酯、癸酸乙酯(P<0.05),其中含量升高较多的是乙酸乙酯、丁酸乙酯和己酸乙酯;含量显著降低的酯类物质有乳酸乙酯、己酸丁酯、月桂酸乙酯、苯乙酸乙酯和己酸异戊酯(P<0.05),其中含量降低较多的是乳酸乙酯。在酮类物质中,与对照组相比,强化组中3-羟基-2-丁酮含量由(2.19±0.03)mg/L提升到(3.50±0.13)mg/L,提升了59.82%。3-羟基-2-丁酮呈现奶油等香气,是地衣芽孢杆菌的主要风味物质[23],其含量的提升与地衣芽孢杆菌的生物强化有关。
在44种主要挥发性风味物质中,OAV>1的关键风味物质共37种,这些挥发性风味物质对酒体风味产生重要贡献。 具体的,OAV>1 000的有5种,分别是己酸乙酯、异戊醛、丁酸乙酯、十四酸乙酯和戊酸乙酯,对酒体风味贡献最大。 OAV在100~320之间的有7种,分别是异戊酸乙酯、2,3-丁二醇、3-羟基-2-丁酮、丙醛、乙酸异戊酯、正丁醇和乙酸苯乙酯,对酒体风味有重要贡献。 其余25种物质的OAV在1~100之间,对酒体风味贡献相对较小。 基于44种主要挥发性风味物质的OAV对两组基酒进行PCA,结果见图3。
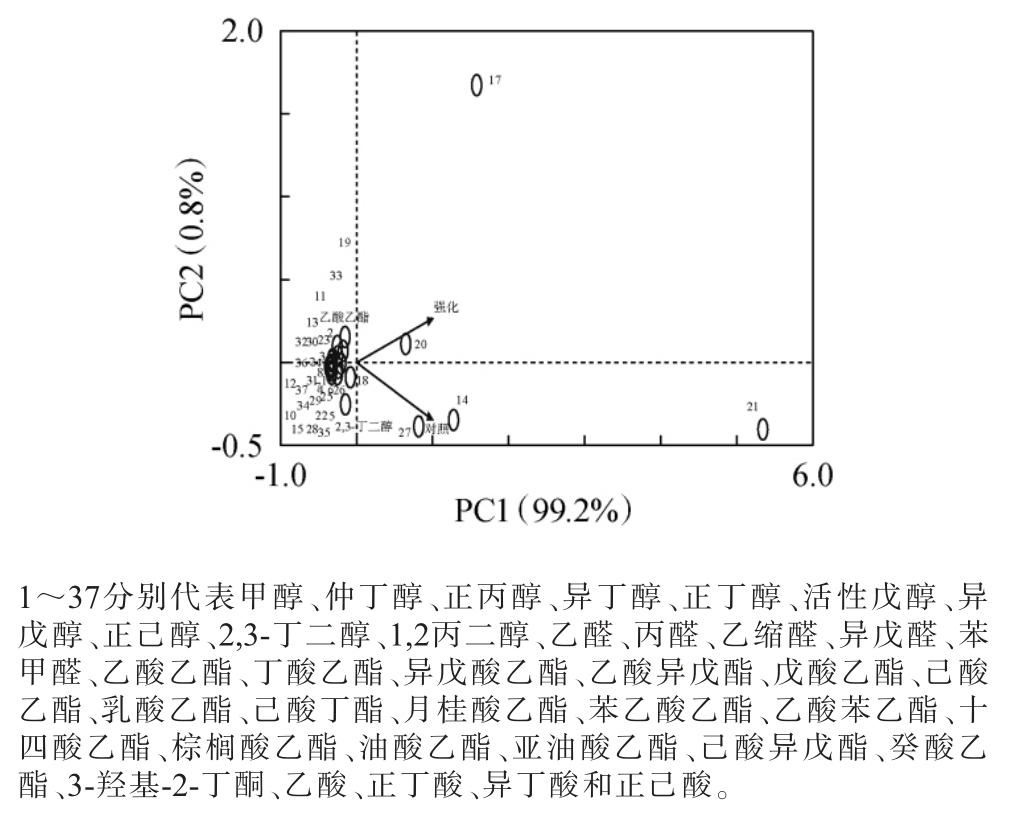
图3 基于挥发性风味物质香气活性值不同馥香型白酒基酒样品的主成分分析
Fig. 3 Principal component analysis of different Fu-flavor Baijiu base liquor samples based on odor activity values of volatile flavor compounds
由图3可知,第一主成分(PC1)和第二主成分(PC2)的方差贡献率分别为99.2%、0.8%,累计方差贡献率为100%,说明前两个主成分代表了挥发性风味物质的全部信息,能很好地表示风味物质的贡献情况。其中对基酒影响最大的挥发性风味物质是己酸乙酯,其次是异戊醛、丁酸乙酯、十四酸乙酯和戊酸乙酯,这5种挥发性风味物质的OAV均>1 000,对酒体风味具有主要贡献。 对基酒影响较大的挥发性风味物质还有异戊酸乙酯、3-羟基-2-丁酮、乙酸乙酯等,它们的OAV>100。 强化组和对照组相比,根据挥发性风味物质OAV变化大小,OAV提升最多的是丁酸乙酯,其次是己酸乙酯、戊酸乙酯、乙酸异戊酯和乙酸乙酯,提升较多的还有3-羟基-2-丁酮、乙醛、亚油酸乙酯、丙醛、乙缩醛、异戊醛、乙酸苯乙酯和油酸乙酯,这些挥发性风味物质是受生物强化影响的主要风味物质。
2.3 地衣芽孢杆菌强化对馥香型白酒基酒感官品质的影响
感官品评是评价酒体品质的最有效手段,采用感官品评方法对馥香型白酒的8个感官维度(酱香、花果香、窖香、芝麻香、回味、绵甜感、丰满感和馥合感)进行评价,结果见图4。
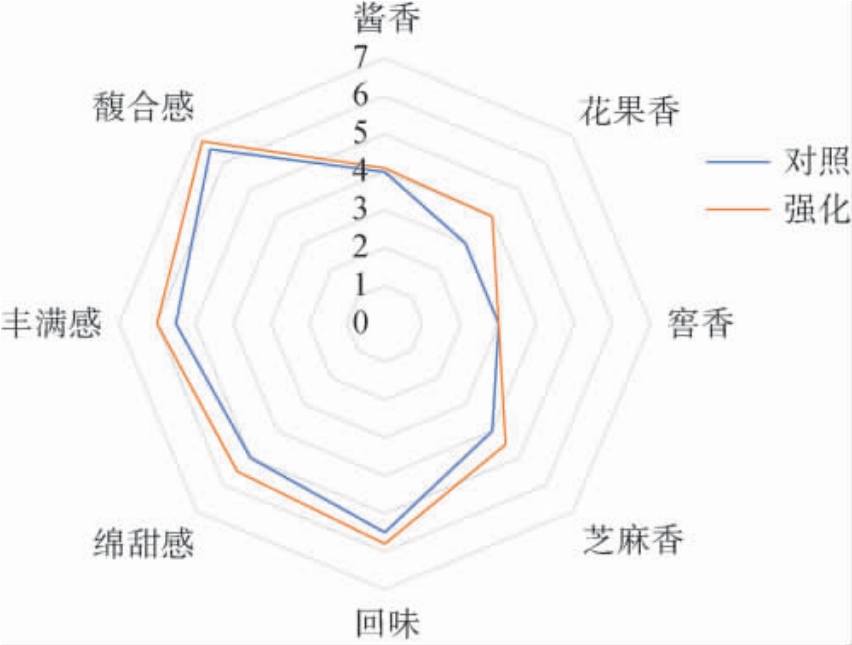
图4 地衣芽孢杆菌强化对馥香型白酒基酒感官品质的影响
Fig. 4 Effect of Bacillus licheniformis enhancement on the sensory quality of Fu-flavor Baijiu base liquor
由图4可知,所有感官维度中,较强的感官特征有馥合感、丰满感、绵甜感和回味。强化组与对照组比较分析显示,在香气方面,强化组馥香型白酒基酒在花果香和芝麻香感官特征上高于对照组,在酱香和窖香特征上无明显差异。酯类物质是馥香型白酒基酒中占比最大的挥发性风味成分,呈现令人愉悦的芳香气味。如乙酸乙酯呈现菠萝香气,己酸乙酯呈现水果香气[24],丁酸乙酯也呈现类似菠萝香气[25]。结合表3可知,强化组馥香型白酒基酒中乙酸乙酯、己酸乙酯和丁酸乙酯的含量分别比对照组提升了163.61%、9.74%和102.22%,乳酸乙酯的含量降低了56.94%,然而,乳酸乙酯的阈值远高于另3种酯类物质的阈值,因此,虽然两组酯类物质总含量变化不显著,但乙酸乙酯、己酸乙酯和丁酸乙酯贡献了强化组酒体更多的花果香,是强化组花果香较对照组突出的重要原因。 此外,芝麻香型白酒中有较高含量的丁酸乙酯,因此,丁酸乙酯的含量的提升可能是酒体芝麻香变得突出的重要原因之一[26]。 在口感方面,强化组馥香型白酒基酒的回味高于对照组,酸类物质含量的提升对酒体的回味有正向作用,是回味提高的重要原因。在风格方面,强化组馥香型白酒在绵甜感、丰满感和馥合感特征上高于对照组,醇类、醛类、酸类、酯类和酮类物质含量的提高,使酒体更丰满,馥合感是各风味物质共同呈现的结果,与风味物质的种类及含量占比有关,微生物强化之后也有一定的提升。
3 结论
地衣芽孢杆菌的强化应用提升了馥香型白酒酒醅中芽孢杆菌属的相对丰度以及细菌菌群的多样性和丰富度。本研究明确了馥香型白酒堆积和入池发酵过程中的主要优势菌群及其演替规律,芽孢杆菌属为堆积发酵前的主要优势细菌属,堆积发酵后和入池发酵过程的主要优势细菌属为乳酸杆菌属,即馥香型白酒发酵过程中主要优势细菌由芽孢杆菌属向乳酸杆菌属演替;堆积发酵前的主要优势真菌属为曲霉属,堆积发酵后为伊萨酵母属和克鲁维酵母属,出窖酒醅优势真菌属为伊萨酵母属和哈萨克斯坦酵母属。地衣芽孢杆菌强化使馥郁香型白酒基酒中的挥发性风味物质总量提升了6.38%,在香气感官上提升了花果香和芝麻香特征,口感和风格上提升了回味、绵甜感、丰满感和馥合感。进一步通过OAV和PCA发现,影响地衣芽孢杆菌强化后基酒感官品质提高的挥发性风味物质主要为己酸乙酯、丁酸乙酯、戊酸乙酯、异戊醛和十四酸乙酯。 本研究结果为通过地衣芽孢杆菌强化提升馥香型白酒的品质奠定了基础。
[1] 薛新新,孙守营,张娇娇,等. 馥郁香型白酒感官风格及特征风味构成的剖析[J] .中国酿造,2022,41(2):76-79.
[2] 任杰.生物强化在传统白酒酿造中的应用[J] .酿酒科技,2022(9):105-108.
[3] 杨磊,穆敏敏,文成兵,等.浓香型白酒提质增香技术研究进展[J] .酿酒,2022,49(1):17-21.
[4] 倪冰倩,夏韩硕,闵伟红,等.Pichia kudriavzevii生物强化对酱香型白酒酒醅微生物群落结构及挥发性风味组分的影响[J] .食品科学技术学报,2024,42(2):93-108,130.
[5] 凌杰,吴群,徐岩,等. 酱香型白酒发酵中地衣芽孢杆菌与酿酒酵母的相互作用[J] .微生物学通报,2013,40(11):2014-2021.
[6] 罗莉,李欣,常煦,等. 芽孢杆菌在中国白酒酿造中的应用机理研究进展[J] .酿酒科技,2019(1):99-104.
[7] 吕磊,王腾飞,汤丹丹,等. 芝麻香型白酒芽孢杆菌培养基的筛选及其产香分析[J] .酿酒科技,2014(9):29-32.
[8] 刘宇,管桂坤,万自然,等. 复合功能微生物在酱香型白酒生产中的应用研究[J] .酿酒科技,2019(12):98-104,118.
[9] 胡峰. 微生物技术在浓香型白酒生产中的应用研究[J] . 酿酒科技,2008(12):56-59.
[10] 张志伟,聂士昊,汪俊卿,等. 强化酒醅微生物对北方酱香型白酒风味影响的研究[J] .酿酒科技,2022(8):24-29.
[11] JIN G Y,ZHU Y,XU Y.Mystery behind Chinese liquor fermentation[J] .Trends Food Sci Tech,2017,63:18-28.
[12] LIU H L,SUN B G. Effect of fermentation processing on the flavor of Baijiu[J] .J Agr Food Chem,2018,66(22):5425-5432.
[13] 倪兴婷,孙细珍,宁珍珍,等. 感官结合化学分析技术解析单粮型和多粮型清香型白酒风味差异[J] .食品与发酵工业,2024,50(20):259-265.
[14] 张乃云,李学思. 浅议白酒中的风味物质与感官分析[J] . 酿酒,2024,51(2):29-33.
[15] 王玉荣,马佳佳,田龙新,等. 酱香型白酒第六轮次堆积发酵醅堆微生物类群与感官品质的相关性分析[J] . 现代食品科技,2024,40(9):107-117.
[16] 任金玫,陈君平,贾玮,等.凤香型白酒风味轮的初步建立及感官特征研究[J] .中国酿造,2023,42(10):80-85.
[17] 郭松波,谢三款,张娇娇,等.茅台地区酱香大回酒轮次发酵机理分析[J] .中国酿造,2022,41(7):38-44.
[18] 韩兴林,潘学森,刘民万,等. 云门酱香型白酒风味特征的分析研究[J] .酿酒科技,2014(10):6-8.
[19] 张娇娇,梁明锋,雷显仲,等. 贵州迎宾酒绵柔酱香型白酒酒体感官特征与特征风味的相关性分析[J] .中国酿造,2022,41(2):69-75.
[20] 李欣,黄实宽,常旭,等. 酵母与芽孢杆菌在小麦粉基质中共培养的生长规律[J] .酿酒科技,2018(8):116-123.
[21] 凌杰. 白酒酿造中地衣芽孢杆菌与酿酒酵母的相互作用及应用研究[D] .无锡:江南大学,2013.
[22] WANG J W,YAN C Y,MA C L,et al.Effects of two kinds of Bacillus on flavour formation of Baijiu solid-state fermentation with pure mixed bacteria[J] .Int J Food Sci Tech,2023,58(3):1250-1262.
[23] YUAN H L, XU Y, CHEN Y Z, et al. Metabolomics analysis reveals global acetoin stress response of Bacillus licheniformis[J] .Metabolomics,2019,15(3):25.
[24] GAO W J,FAN W L,XU Y.Characterization of the key odorants in light aroma type Chinese liquor by gas chromatography-olfactometry,quantitative measurements, aroma recombination, and omission studies[J] . J Agr Food Chem,2014,62(25):5796-5804.
[25] 丁力杰,唐云,赵亚雄,等. 白酒中的重要酯类物质及主要来源研究现状[J] .酿酒科技,2024(3):91-100,107.
[26] 吴翔,丁萍,张温清,等. 小窖宣酒芝麻香型白酒主要酯类化合物在蒸馏过程中的变化规律[J] .酿酒,2015,42(3):25-28.