生物胺是指一类含氮小分子碱性有机化合物,由有机生物体生成[1]。常见的生物胺主要有腐胺、色胺、组胺、尸胺、章鱼胺、酪胺、β-苯乙胺、精胺、亚精胺等,通常由氨基酸经脱羧过程或醛酮氨基化生成[2]。生物胺作为生物体必要的活性成分,适量条件下可有效调节遗传物质和蛋白质的生物合成过程,并在炎症反应、免疫反应、神经传导及肠道功能等生理过程中发挥积极作用,对生物体正常生理功能的维持具有关键作用[3]。但过量的生物胺则易对生物体造成负面影响,常见的症状包括动脉、血管的扩张、头疼、腹部抽搐、心慌、腹泻和呼吸紊乱等,极特殊情况下还会出现危及生命的严重后果[4]。现有研究表明,食品在发酵加工、贮藏过程中易产生大量生物胺,在微生物和蛋白酶的共同作用下,生物胺逐渐富集,该过程广泛存在于酒类[5]、肉制品[6]、水产品[7]和乳制品[8]等各类食品中,尤其是发酵酒类食品(果酒、黄酒、啤酒等)[9]。
我国食用发酵酒文化历史悠久,因其独特的风味和高营养价值深受国人的喜爱[10]。发酵酒主要以谷物、稻米等为原料,经过酵母、霉菌和细菌的共同发酵而成[11],其在发酵过程中,丰富的微生物环境会产生大量的蛋白酶和氨基酸脱羧酶[12],蛋白酶将发酵过程中的蛋白质分解为氨基酸,氨基酸通过氨基酸脱羧酶的作用脱羧反应生成大量生物胺[13-14]。生物胺是衡量发酵酒质量、安全性和卫生状况的重要指标[15]。目前,发酵酒中常见的生物胺检测技术包括超高效液相色谱(ultra performance liquid chromatography,UPLC)[16]、薄层色谱(thin-layer chromatography,TLC)[17]、气相色谱(gas chromatography,GC)[18]和离子色谱(ion chromatography,IC)[19]等,其中薄层色谱法仅为半定量检测方法,准确性较差,检测结果信度不足[20];气相色谱技术只能局限于挥发性生物胺的检测,而对于难挥发的生物胺则需在衍生化完成后进一步检测[21];离子色谱技术抗干扰能力较差,无法将所有生物胺一次检出[22];与其他检测方法不同,UPLC因其精密度和灵敏度高的优点被广泛使用[23]。由于大部分生物胺缺乏天然荧光或紫外发色基团,需通过衍生化放大检测结果,提高检测的灵敏度[24]。常见的衍生试剂包括苯甲酰氯、邻苯二甲醛和丹磺酰氯等[25]。 苯甲酰氯的优势在于其成本相对较低且易获取,但苯甲酰氯的缺陷也很明显,不仅衍生时间偏长,还存在与羟基反应,干扰化合物检测的问题[26];相对而言,邻苯二甲醛的抗干扰能力较强、灵敏度高,但由于其易出现衍生后不能净化、衍生物不稳定的现象,故难以满足本研究要求[27];与其他衍生剂相比,丹磺酰氯因其衍生操作简单、衍生物稳定性好且检测范围更广,被广泛应用于UPLC检测中[28],是生物胺检测中应用最多的衍生剂。使用丹磺酰氯作为衍生剂不仅能提高实验检测灵敏度,还可大大缩短分析时间及成本。
因此,本研究选择以丹磺酰氯作为衍生剂,通过优化柱前衍生条件,从而建立同时测定3种发酵酒(啤酒、葡萄酒、黄酒)中9种生物胺的超高效液相色谱检测方法,并应用于实际样品分析,以期为提高我国发酵酒的质量和安全性提供技术支撑,为制定发酵酒中生物胺限量标准提供参考。
1 材料与方法
1.1 材料与试剂
1.1.1 材料
啤酒、葡萄酒、黄酒样品:市售,每种样品各5份,共计15份样品。
1.1.2 试剂
1,7-二氨基庚烷(纯度98.5%)、3,3'-二氨基二丙胺(纯度99.8%)、亚精胺(纯度99.8%)、色胺(纯度99.2%)、腐胺(纯度99.7%)、β-苯乙胺盐酸盐(纯度99.9%)、章鱼胺盐酸盐(纯度98.5%)、尸胺(纯度99.7%)、精胺(纯度99.7%)、组胺(纯度99.9%)、酪胺(纯度98.0%):天津阿尔塔科技有限公司;丹磺酰氯(纯度99.9%):坛墨质检科技有限公司;浓盐酸(分析纯):杭州双林化工试剂厂;氢氧化钠(分析纯):国药集团化学试剂有限公司;甲醇、乙腈(均为色谱纯):美国Merck公司;碳酸氢钠(分析纯):上海虹光化工厂;碳酸钠(分析纯):宁波市化学试剂厂;浓氨水、乙酸(均为色谱纯):上海麦克林生化科技股份有限公司;氯化钠(分析纯):西陇化工股份有限公司;乙酸铵(色谱纯):美国ACS恩科化学。实验用水均为Milli-Q所制超纯水。
1.2 仪器与设备
ACQUITY UPLC ICLASS超高效液相色谱仪:美国Waters公司;JA5003型电子天平:上海舜宇恒平科学仪器有限公司;Sorvall-ST 16R高速冷冻离心机:美国赛默飞公司;MFV24恒温氮吹仪:得泰仪器科技有限公司;Fotector Plus固相萃取装置:美国Reeko公司;VM800多管旋涡混合器:群安实验仪器有限公司;MILLI-Q INTEGRAL-5超纯水系统:美国密理博公司;UC-23超声波清洗器、ZK5030恒温水浴锅:浙江浙科仪器设备有限公司。
1.3 方法
1.3.1 标准溶液的配制
生物胺标准混合使用液配制:准确吸取1 mL质量浓度均为1 000 μg/mL的9种生物胺(色胺、β-苯乙胺盐酸盐、腐胺、尸胺、组胺、章鱼胺盐酸盐、酪胺、亚精胺、精胺)的混合标准溶液于10 mL容量瓶中,采用50 mmol/L盐酸溶液定容,配制成质量浓度为100 μg/mL的生物胺混合标准使用液,4 ℃条件下冷藏避光保存。
内标混合工作液配制:分别准确吸取5 mL质量浓度均为1 000 μg/mL 1,7-二氨基庚烷、3,3'-二氨基二丙胺标准溶液于10 mL容量瓶中,采用50 mmol/L盐酸溶液定容,配制成质量浓度为500 μg/mL的内标混合工作液,4 ℃条件下冷藏储存。
生物胺标准系列溶液:分别准确吸取10 μL、50 μL、100μL、200μL生物胺混合标准使用液(100μg/mL)及50μL、100 μL生物胺混合标准溶液(1 000 μg/mL)于15 mL离心管中,加入50 μL生物胺内标工作液(500 μg/mL)、0.5 mL饱和碳酸氢钠溶液,补超纯水至1 mL,配制得到质量浓度分别为1.0 μg/mL、5.0 μg/mL、10.0 μg/mL、20.0 μg/mL、50.0 μg/mL、100.0 μg/mL的生物胺标准系列溶液(内标质量浓度为25.0 μg/mL)。
1.3.2 样品前处理
准确量取1 mL试样,置于15 mL离心管中,再加入50 μL 500 μg/mL生物胺内标工作液、3 mL 50 mmol/L盐酸溶液,通过涡旋混匀,并以10 000 r/min离心2 min,取上清液,备用。
1.3.3 生物胺的检测
衍生条件:(1)依次用4 mL甲醇、4 mL超纯水、4 mL 50 mmol/L HCl淋洗固相萃取柱,并保持湿润,以活化固相萃取柱。待活化完成后加入全部预处理样品或标准溶液,依次用4 mL超纯水、2 mL甲醇淋洗除杂,抽干。(2)固相萃取柱中准确加入4 mL 0.2%氢氧化钠-甲醇溶液洗脱于15 mL离心管,洗脱液中加入0.25 mL 1 mol/L盐酸溶液,混匀,45 ℃水浴中氮吹至0.25 mL左右,净化液待衍生。(3)净化液中加入0.5 mL饱和NaHCO3溶液,用超纯水补加至1 mL,然后加入1 mL的0.2 mol/L NaHCO3-Na2CO3缓冲溶液(pH10)和1 mL 15 mg/mL丹磺酰氯-乙腈衍生试剂,放置60 ℃恒温水浴中衍生15 min,衍生液取出后用水从外壁淋洗快速冷却至室温,处理完成后,再加入0.2 mL浓氨水,混匀,60 ℃恒温水浴中放置15 min,取出后用水从外壁淋洗快速冷却至室温,加入0.5 mL乙腈和1.0 g氯化钠,混匀涡旋2 min,5 000 r/min离心2 min,取上清液过0.22 μm有机相滤膜于进样瓶,待上机测定。
UPLC条件:XBridgeC18色谱柱(100mm×4.6mm,3.5μm),柱温35 ℃,流速0.5 mL/min;进样量10 μL;流动相A为含1%乙酸的0.01 mol/L乙酸铵溶液-乙腈(1∶9,V/V),流动相B为含1%乙酸的0.01 mol/L乙酸铵溶液-乙腈(9∶1,V/V),梯度洗脱,洗脱程序为0~22 min,60%~85%A;22~25 min,85%~100%A;25~32 min,100%~60%A。
定性定量方法:根据生物胺标准品的保留时间进行定性,采用内标方法定量。
1.3.4 衍生条件优化
在方法1.3.3生物胺检测条件基础上,分别考察衍生剂质量浓度(2mg/mL、5mg/mL、10mg/mL、15mg/mL、20 mg/mL)、衍生反应温度(30 ℃、45 ℃、60 ℃、75 ℃、90 ℃)、衍生反应时间(5 min、10 min、15 min、20 min、30 min)、衍生反应溶液pH(9.5、10.0、10.5、11.0、11.5)对目标物峰面积的影响,确定最佳衍生剂质量浓度、衍生反应温度、衍生反应时间、衍生反应pH。
1.3.5 方法学考察
线性回归方程、检出限及定量限:按照最优方法对9种生物胺的标准工作溶液进行测定,以9种生物胺衍生物与相对应内标的色谱峰面积之比(y)为纵坐标,9种生物胺与相对应内标的质量浓度比值(x)为横坐标,绘制标准曲线,并拟合得到标准曲线回归方程。以3倍信噪比(S/N=3)计算得到检出限(limit of detection,LOD),以10倍信噪比(S/N=10)计算得到定量限(limit of quantitation,LOQ)。
加标回收率试验及精密度试验:分别取低本底的啤酒、葡萄酒、黄酒样品,分别添加9种生物胺标准溶液,加标量分别为1.0 mg/L、5.0 mg/L、10.0 mg/L、50.0 mg/L,进行加标回收率与精密度试验,每个加标质量浓度水平平行测定6次,计算得到平均回收率和精密度试验结果的相对标准偏差(relative standard deviation,RSD)。
1.3.6 数据处理与统计分析
使用Excel 2021、Origin 2021软件及Empower进行数据处理、显著性分析以及可视化。
2 结果与分析
2.1 衍生条件的选择
2.1.1 衍生剂质量浓度的选择
衍生剂质量浓度是影响生物胺衍生反应的重要因素之一,衍生剂质量浓度不同会导致生物胺检出峰面积出现差异[29]。因此,考察不同衍生剂质量浓度对9种生物胺衍生物峰面积的影响,结果见图1。 由图1可知,随着衍生剂质量浓度的升高,9种生物胺衍生物的峰面积变化趋势存在一定差异,但基本上展现出峰面积先增大后减小的趋势。出现该结果的原因可能是,衍生剂质量浓度过低时,衍生反应不完全,表现出目标物检测结果偏低;衍生剂质量浓度过高时,过量的衍生剂可能与部分生物胺发生副反应,从而降低目标衍生物浓度。实验结果显示亚精胺和精胺的最佳衍生剂质量浓度为15 mg/mL,色胺的最佳衍生剂质量浓度为5 mg/mL,而绝大部分生物胺的最佳衍生剂质量浓度为10 mg/mL,综合考量各目标生物胺的整体衍生效果,选定丹磺酰氯的最佳质量浓度为10 mg/mL。
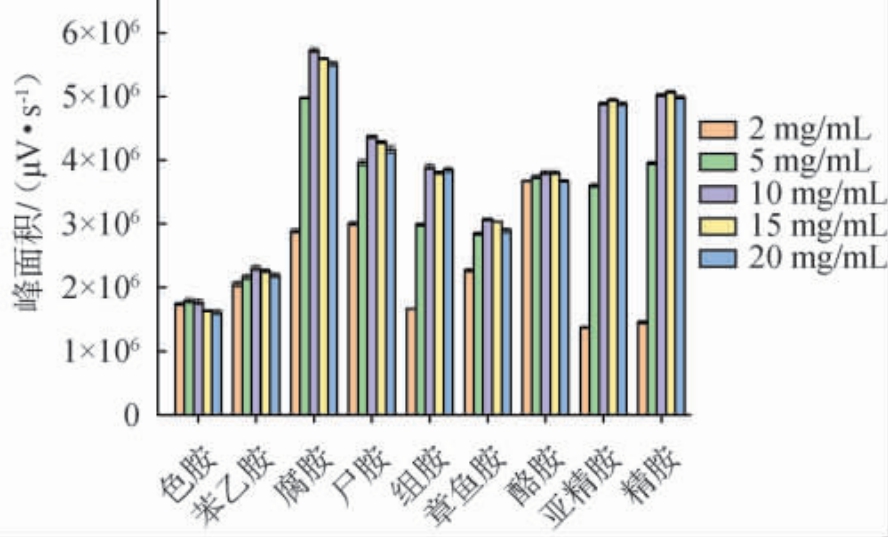
图1 衍生试剂质量浓度对9种生物胺衍生效果的影响
Fig. 1 Effect of derivatization reagent mass concentration on derivatization efficiency of 9 bioamines
2.1.2 衍生反应温度的选择
除衍生剂质量浓度外,衍生反应温度对生物胺的衍生效果影响也很明显,为了优化衍生反应温度,保证最佳衍生效果,考察不同衍生反应温度对9种生物胺衍生物峰面积的影响,结果见图2。由图2可知,随着衍生反应温度的上升,9种生物胺衍生物峰面积大致呈现先增大后减小趋势,并均在60 ℃时达到最大值,且明显高于其他衍生温度条件下的峰面积。 这表明适当的升温可以加快衍生反应的进行,得到目标物丹磺酰胺;但温度过高使得生物胺的衍生物丹磺酰胺稳定性变差,丹磺酰胺出现分解[30]。 综合考量各目标生物胺的整体衍生效果,确定最佳的衍生反应温度为60 ℃。
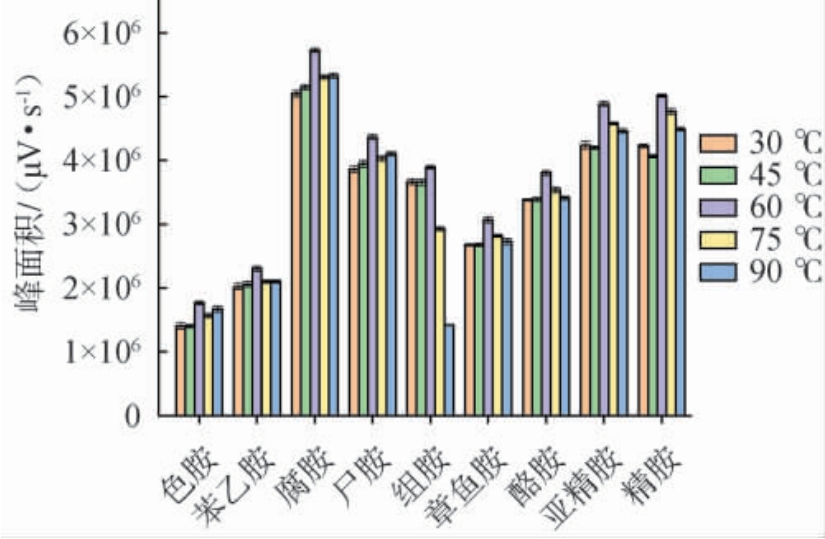
图2 衍生反应温度对9种生物胺衍生效果的影响
Fig. 2 Effect of derivatization temperature on derivatization efficiency of 9 bioamines
2.1.3 衍生反应时间的选择
生物胺衍生反应中,衍生时间也是一项重要影响因素,衍生时间过短易出现生物胺未完全反应的问题,随着衍生时间的增加,此时丹磺酰氯与生物胺反应饱和,继续延长时间无意义甚至出现负面效果[31]。 因此,考察本不同衍生时间对生物胺衍生物峰面积的影响,结果见图3。由图3可知,随着反应时间延长,9种生物胺衍生物峰面积大致呈现先增大后减小趋势,并均在15 min条件下出现最大值,因此,确定最佳衍生反应时间为15 min。
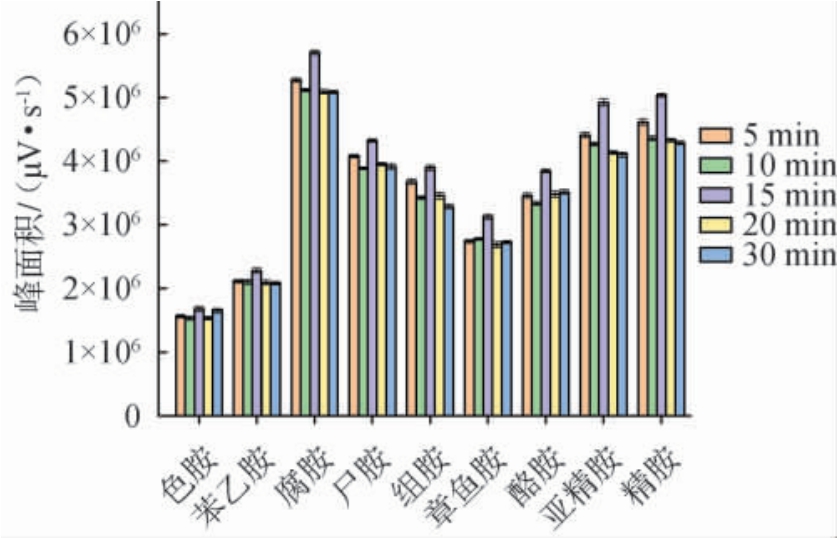
图3 衍生反应时间对9种生物胺衍生效果的影响
Fig. 3 Effect of derivatization time on derivatization efficiency of 9 bioamines
2.1.4 衍生反应溶液pH的选择
生物胺与丹磺酰氯的衍生反应发生在碱性条件下,为了探究衍生时溶液pH值对衍生结果的影响,考察了不同衍生反应溶液pH对生物胺衍生物峰面积的影响,结果见图4。由图4可知,整体上衍生反应溶液pH对各生物胺衍生物峰面积的影响较小,强碱性条件下各生物胺衍生物峰面积均出现了下降。这或许是由于生物胺与丹磺酰氯需要在碱性条件中进行反应,以保证丹磺酰氯与胺基的结合,但pH过高会导致丹磺酰氯出现了水解[32]。实验结果显示,色胺、腐胺、尸胺、亚精胺、精胺这5种生物胺衍生物在pH 10.5时峰面积最大,综合考量各目标生物胺的整体衍生效果,最终确定最佳衍生反应溶液的pH为10.5。
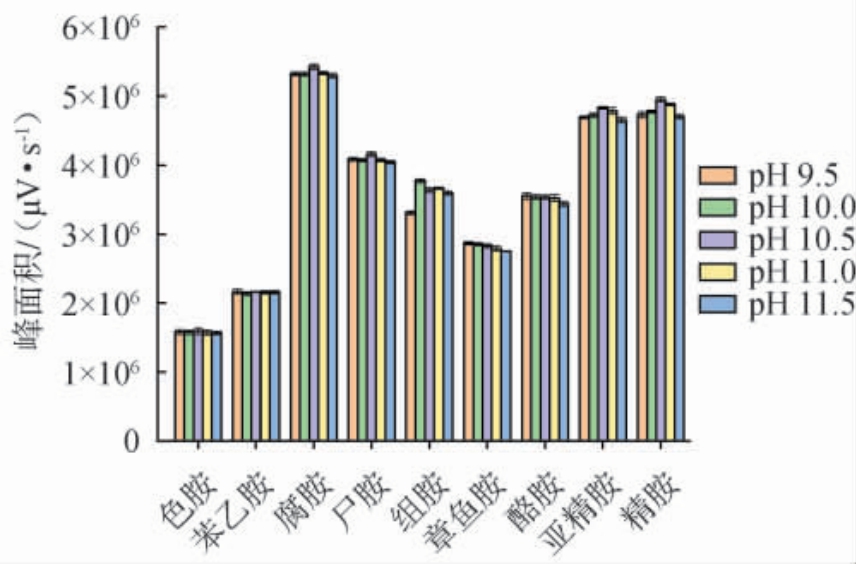
图4 衍生反应溶液pH值对9种生物胺衍生效果的影响
Fig. 4 Effect of derivatization solution pH on derivatization efficiency of 9 bioamines
2.2 9种生物胺的检测
基于1.3.3中的色谱条件和2.1的最佳衍生条件对9种生物胺混合标准溶液和加标发酵酒实际样品中9种生物胺进行UPLC分析,结果见图5。由图5可知,9种生物胺以及2种内标(1,7-二氨基庚烷和3,3'-二氨基二丙胺)均显示出良好的峰形,且在28 min内完成了检测,说明该方法衍生效果好、分析速度快,适用于发酵酒中9种生物胺的检测。
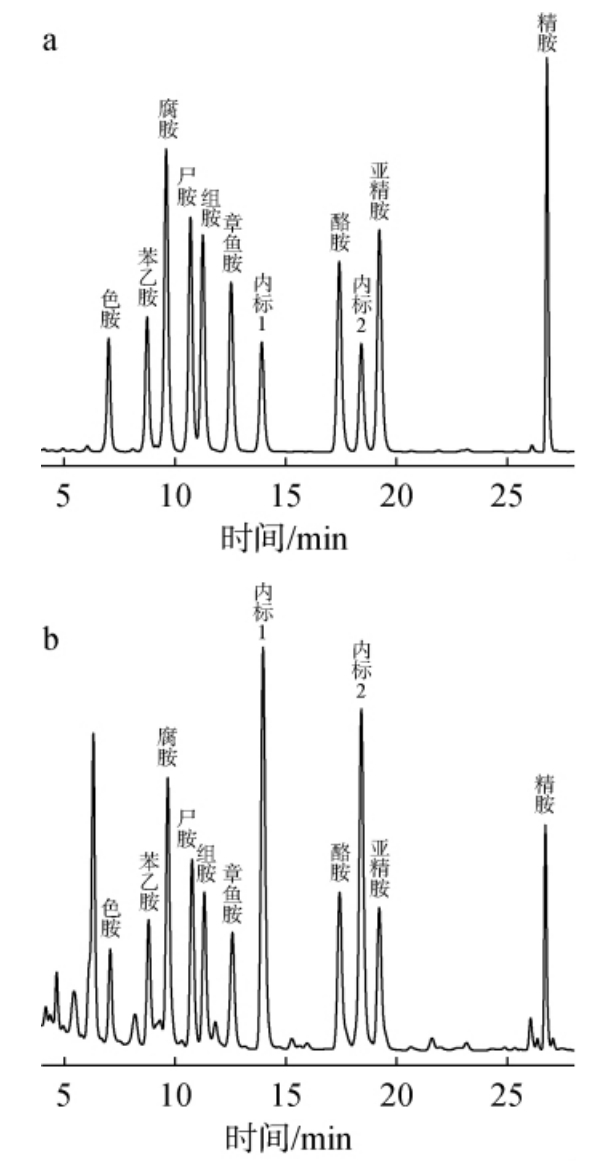
图5 混合标准溶液(a)和加标啤酒样品(b)中9种生物胺检测的超高效液相色谱图
Fig. 5 Ultra-high performance liquid chromatogram of 9 bioamines in mixed standard solution (a) and spiked beer samples (b)
2.3 方法学考察
2.3.1 线性范围、回归方程、检出限和定量限
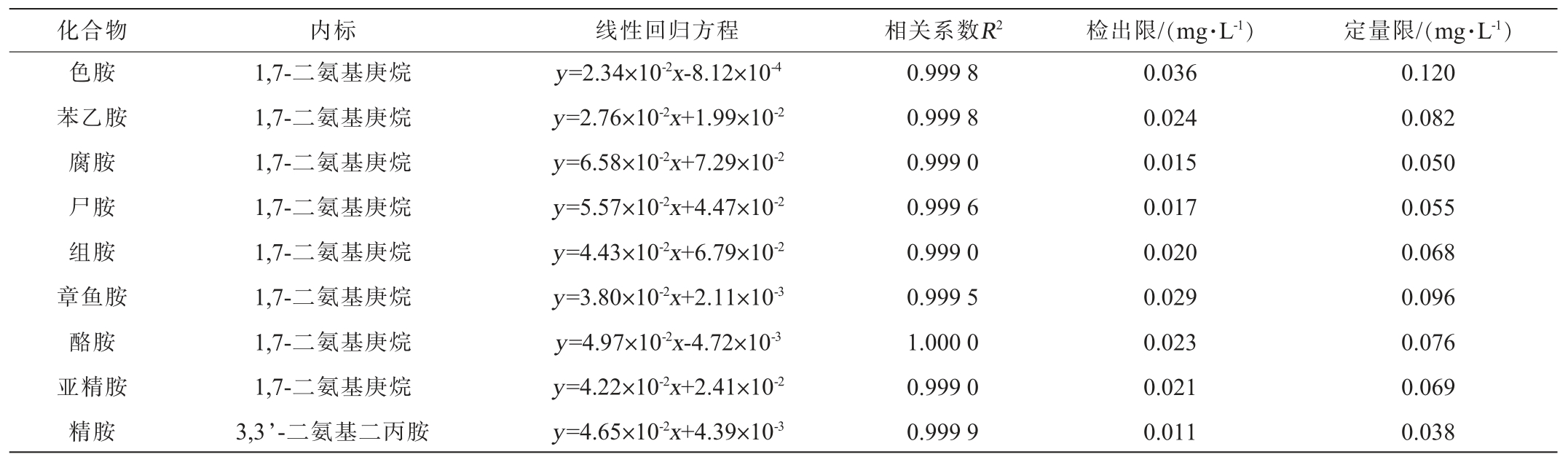
采用最优的方法对生物胺标准系列溶液进行检测,9种生物胺的线性回归方程、相关系数及检出限和定量限见表1。由表1可知,9种生物胺在质量浓度1.0~100.0 mg/L范围内标准曲线线性关系良好,相关系数R2均≥0.999 0,以3倍信噪比(S/N=3)计算得到该方法的检出限为0.011~0.036mg/L,以10倍信噪比(S/N=10)计算得到该方法的定量限为0.038~0.120 mg/L。结果表明,该方法检测9种生物胺灵敏度高,能满足样品测定的要求。
表1 9种生物胺的线性回归方程、相关系数、检出限和定量限
Table 1 Linear regression equations, correlation coefficients, limits of detection, and limits of quantification of 9 bioamines
化合物内标线性回归方程相关系数R2检出限/(mg·L-1)定量限/(mg·L-1)色胺苯乙胺腐胺尸胺组胺章鱼胺酪胺亚精胺精胺1,7-二氨基庚烷1,7-二氨基庚烷1,7-二氨基庚烷1,7-二氨基庚烷1,7-二氨基庚烷1,7-二氨基庚烷1,7-二氨基庚烷1,7-二氨基庚烷3,3’-二氨基二丙胺y=2.34×10-2x-8.12×10-4 y=2.76×10-2x+1.99×10-2 y=6.58×10-2x+7.29×10-2 y=5.57×10-2x+4.47×10-2 y=4.43×10-2x+6.79×10-2 y=3.80×10-2x+2.11×10-3 y=4.97×10-2x-4.72×10-3 y=4.22×10-2x+2.41×10-2 y=4.65×10-2x+4.39×10-3 0.999 8 0.999 8 0.999 0 0.999 6 0.999 0 0.999 5 1.000 0 0.999 0 0.999 9 0.036 0.024 0.015 0.017 0.020 0.029 0.023 0.021 0.011 0.120 0.082 0.050 0.055 0.068 0.096 0.076 0.069 0.038
2.3.2 加标回收率与精密度试验
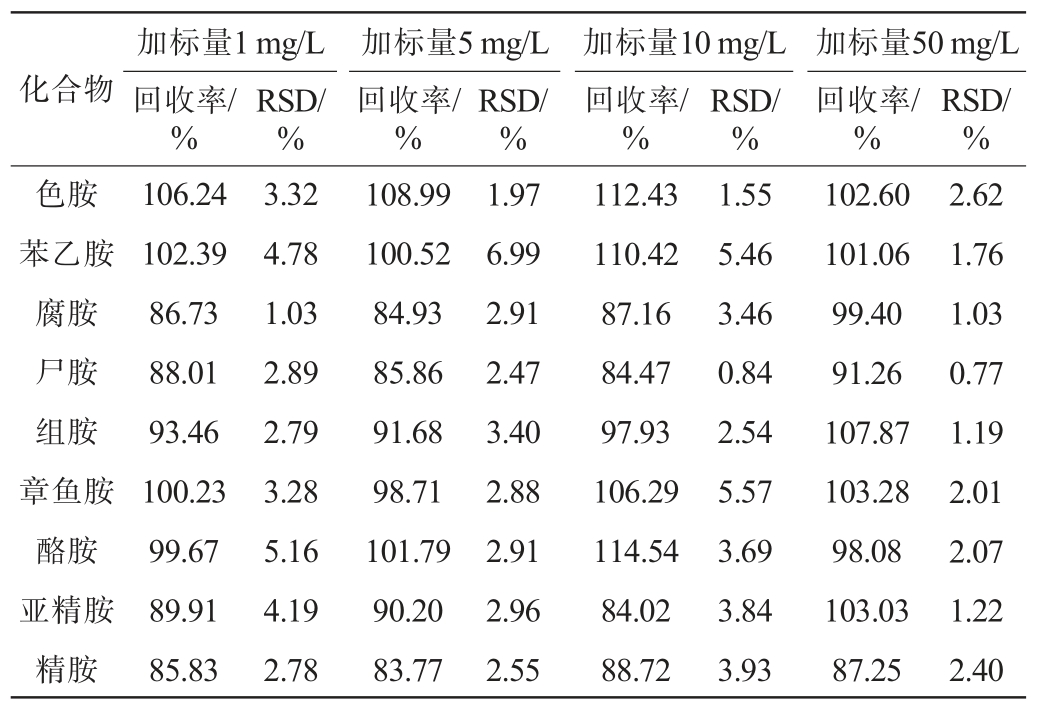
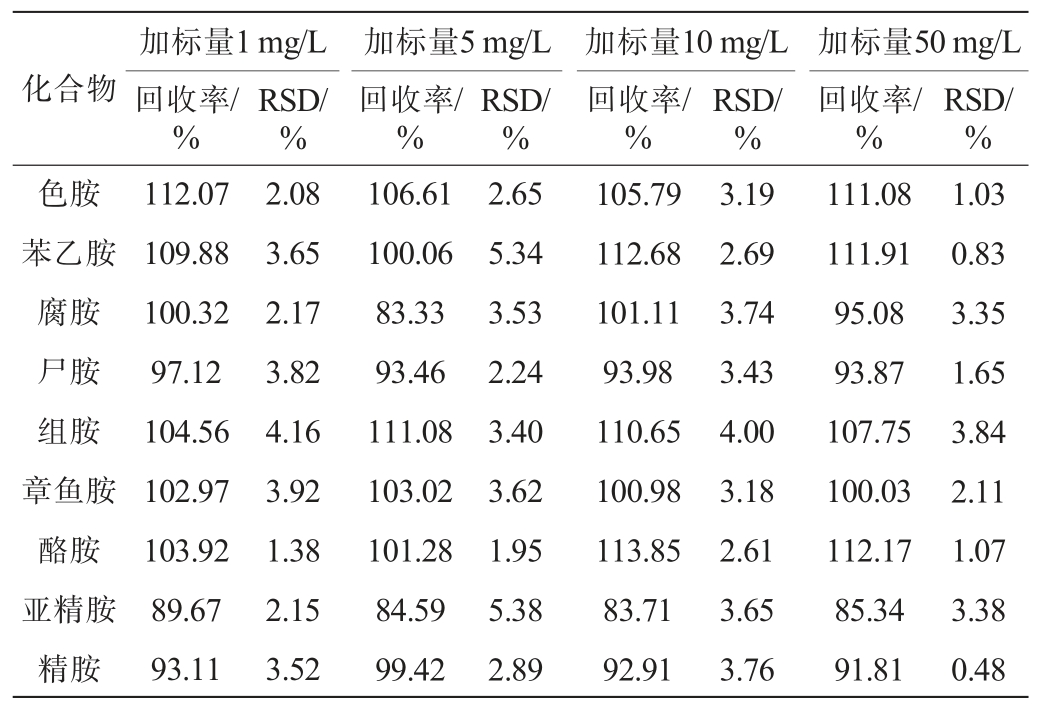
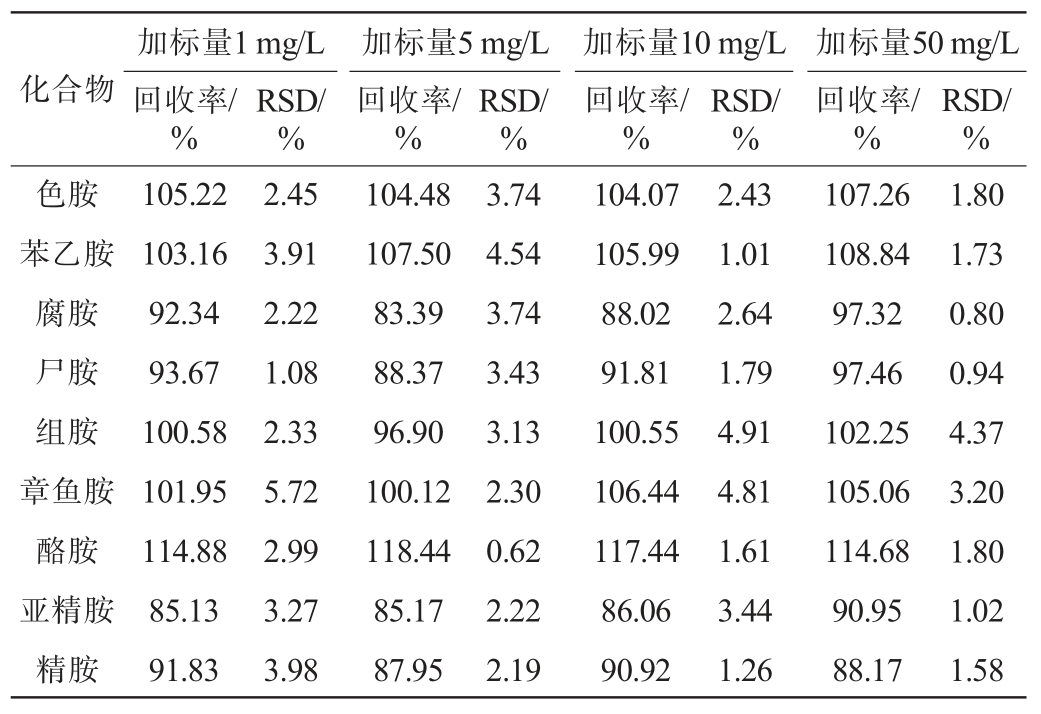
分别向3种发酵酒(黄酒、葡萄酒、啤酒)实际样品中添加1 mg/L、5 mg/L、10 mg/L、50 mg/L 4种不同质量浓度的9种生物胺混合标准溶液进行加标回收试验,每个加标水平重复测定6次,结果见表2~表4。 由表2可知,啤酒基质中9种生物胺的平均加标回收率为83.77%~114.54%,精密度试验结果的RSD为0.77%~6.99%;由表3可知,葡萄酒基质中9种生物胺的平均加标回收率为83.33%~113.85%,精密度试验结果的RSD为0.48%~5.38%;由表4可知,黄酒基质中9种生物胺的平均加标回收率为83.39%~118.44%,精密度试验结果的RSD为0.62%~5.72%。 结果表明,该方法准确可靠,可用于检测3种发酵酒(啤酒、葡萄酒、黄酒)中9种生物胺的种类和含量。
表2 啤酒样品中9种生物胺的加标回收试验结果
Table 2 Results of spike recovery tests of 9 bioamines in beer samples
化合物加标量1 mg/L回收率/%RSD/%色胺苯乙胺腐胺尸胺组胺章鱼胺酪胺亚精胺精胺106.24 102.39 86.73 88.01 93.46 100.23 99.67 89.91 85.83 3.32 4.78 1.03 2.89 2.79 3.28 5.16 4.19 2.78加标量5 mg/L回收率/%RSD/%108.99 100.52 84.93 85.86 91.68 98.71 101.79 90.20 83.77 1.97 6.99 2.91 2.47 3.40 2.88 2.91 2.96 2.55加标量10 mg/L回收率/%RSD/%112.43 110.42 87.16 84.47 97.93 106.29 114.54 84.02 88.72 1.55 5.46 3.46 0.84 2.54 5.57 3.69 3.84 3.93加标量50 mg/L回收率/%RSD/%102.60 101.06 99.40 91.26 107.87 103.28 98.08 103.03 87.25 2.62 1.76 1.03 0.77 1.19 2.01 2.07 1.22 2.40
表3 葡萄酒样品中9种生物胺的加标回收试验结果
Table 3 Results of spike recovery tests of 9 bioamines in wine samples
化合物加标量1 mg/L回收率/%RSD/%加标量5 mg/L回收率/%RSD/%加标量10 mg/L回收率/%RSD/%加标量50 mg/L回收率/%RSD/%色胺苯乙胺腐胺尸胺组胺章鱼胺酪胺亚精胺精胺112.07 109.88 100.32 97.12 104.56 102.97 103.92 89.67 93.11 2.08 3.65 2.17 3.82 4.16 3.92 1.38 2.15 3.52 106.61 100.06 83.33 93.46 111.08 103.02 101.28 84.59 99.42 2.65 5.34 3.53 2.24 3.40 3.62 1.95 5.38 2.89 105.79 112.68 101.11 93.98 110.65 100.98 113.85 83.71 92.91 3.19 2.69 3.74 3.43 4.00 3.18 2.61 3.65 3.76 111.08 111.91 95.08 93.87 107.75 100.03 112.17 85.34 91.81 1.03 0.83 3.35 1.65 3.84 2.11 1.07 3.38 0.48
表4 黄酒样品中9种生物胺的加标回收试验结果
Table 4 Results of spike recovery tests of 9 bioamines in Huangjiu samples
化合物加标量1 mg/L回收率/%RSD/%色胺苯乙胺腐胺尸胺组胺章鱼胺酪胺亚精胺精胺105.22 103.16 92.34 93.67 100.58 101.95 114.88 85.13 91.83 2.45 3.91 2.22 1.08 2.33 5.72 2.99 3.27 3.98加标量5 mg/L回收率/%RSD/%104.48 107.50 83.39 88.37 96.90 100.12 118.44 85.17 87.95 3.74 4.54 3.74 3.43 3.13 2.30 0.62 2.22 2.19加标量10 mg/L回收率/%RSD/%104.07 105.99 88.02 91.81 100.55 106.44 117.44 86.06 90.92 2.43 1.01 2.64 1.79 4.91 4.81 1.61 3.44 1.26加标量50 mg/L回收率/%RSD/%107.26 108.84 97.32 97.46 102.25 105.06 114.68 90.95 88.17 1.80 1.73 0.80 0.94 4.37 3.20 1.80 1.02 1.58
2.4 发酵酒样品中9种生物胺的检测
采用最优方法对3种发酵酒(啤酒、葡萄酒及黄酒,每种样品各5份)中的9种生物胺含量进行测定,结果见表5。由表5可知,所有发酵酒中均未检出章鱼胺,葡萄酒中色胺、苯乙胺的含量相对较高;黄酒中腐胺、尸胺、组胺和酪胺这4种生物胺含量相对较高;亚精胺、精胺在3种发酵酒中含量相当。 其中啤酒中生物胺总含量最低,黄酒中生物胺总含量最高,黄酒中生物胺的显著富集现象可能与陈酿过程中微生物脱羧酶活性增强及氨基酸底物长期累积有关[33]。
表5 不同发酵酒样品中9种生物胺含量的测定结果
Table 5 Determination results of 9 bioamines contents in different fermented alcoholic drink samples mg/L
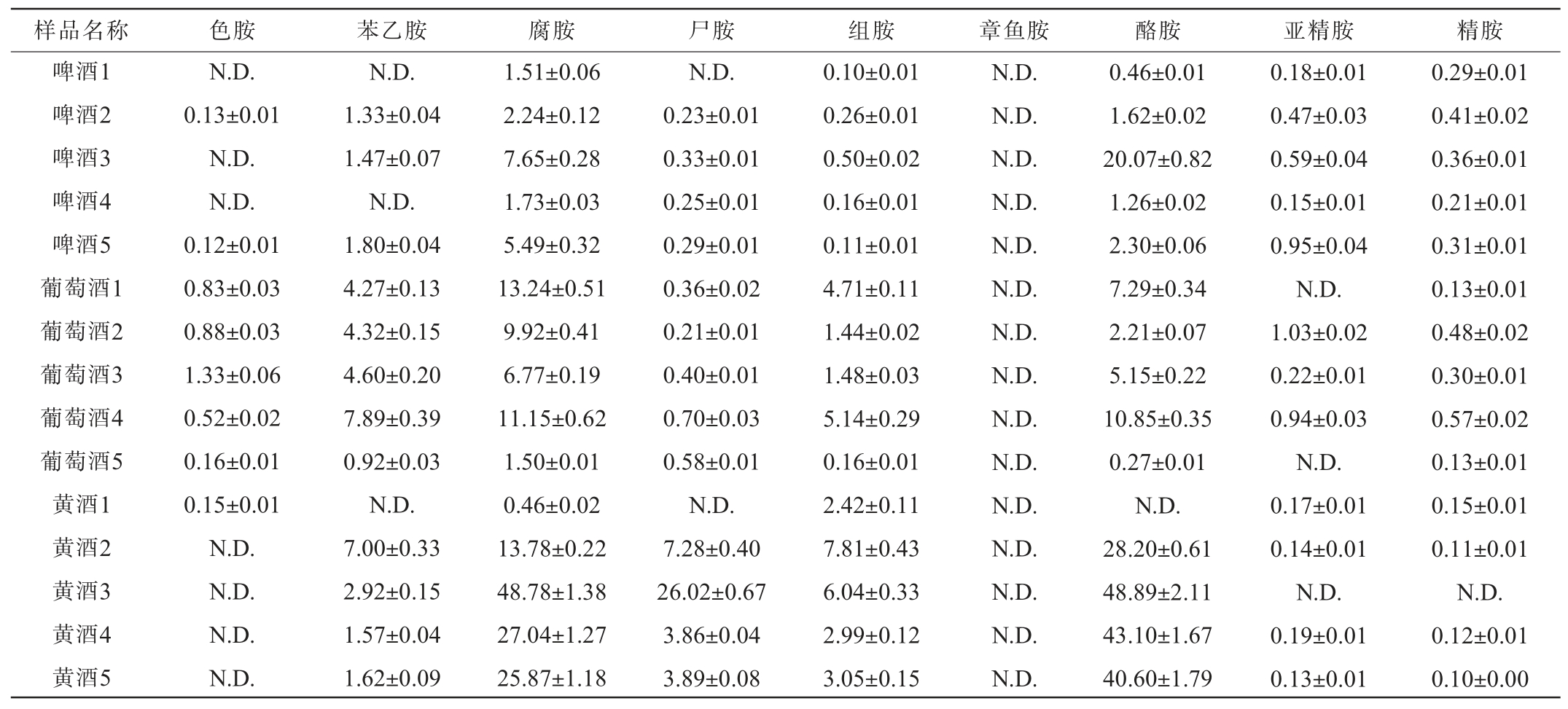
注:“N.D.”表示未检出。
样品名称色胺苯乙胺腐胺尸胺组胺章鱼胺酪胺亚精胺精胺啤酒1啤酒2啤酒3啤酒4啤酒5葡萄酒1葡萄酒2葡萄酒3葡萄酒4葡萄酒5黄酒1黄酒2黄酒3黄酒4黄酒5 N.D.0.13±0.01 N.D.N.D.0.12±0.01 0.83±0.03 0.88±0.03 1.33±0.06 0.52±0.02 0.16±0.01 0.15±0.01 N.D.N.D.N.D.N.D.N.D.1.33±0.04 1.47±0.07 N.D.1.80±0.04 4.27±0.13 4.32±0.15 4.60±0.20 7.89±0.39 0.92±0.03 N.D.7.00±0.33 2.92±0.15 1.57±0.04 1.62±0.09 1.51±0.06 2.24±0.12 7.65±0.28 1.73±0.03 5.49±0.32 13.24±0.51 9.92±0.41 6.77±0.19 11.15±0.62 1.50±0.01 0.46±0.02 13.78±0.22 48.78±1.38 27.04±1.27 25.87±1.18 N.D.0.23±0.01 0.33±0.01 0.25±0.01 0.29±0.01 0.36±0.02 0.21±0.01 0.40±0.01 0.70±0.03 0.58±0.01 N.D.7.28±0.40 26.02±0.67 3.86±0.04 3.89±0.08 0.10±0.01 0.26±0.01 0.50±0.02 0.16±0.01 0.11±0.01 4.71±0.11 1.44±0.02 1.48±0.03 5.14±0.29 0.16±0.01 2.42±0.11 7.81±0.43 6.04±0.33 2.99±0.12 3.05±0.15 N.D.N.D.N.D.N.D.N.D.N.D.N.D.N.D.N.D.N.D.N.D.N.D.N.D.N.D.N.D.0.46±0.01 1.62±0.02 20.07±0.82 1.26±0.02 2.30±0.06 7.29±0.34 2.21±0.07 5.15±0.22 10.85±0.35 0.27±0.01 N.D.28.20±0.61 48.89±2.11 43.10±1.67 40.60±1.79 0.18±0.01 0.47±0.03 0.59±0.04 0.15±0.01 0.95±0.04 N.D.1.03±0.02 0.22±0.01 0.94±0.03 N.D.0.17±0.01 0.14±0.01 N.D.0.19±0.01 0.13±0.01 0.29±0.01 0.41±0.02 0.36±0.01 0.21±0.01 0.31±0.01 0.13±0.01 0.48±0.02 0.30±0.01 0.57±0.02 0.13±0.01 0.15±0.01 0.11±0.01 N.D.0.12±0.01 0.10±0.00
3 结论
本研究通过优化柱前衍生条件建立了固相萃取-柱前衍生-UPLC同时测定3种发酵酒(啤酒、葡萄酒、黄酒)中9种生物胺的方法,最佳衍生条件为:以丹磺酰氯作为衍生试剂,衍生剂质量浓度10 mg/mL,衍生反应温度60 ℃,衍生反应时间15 min,衍生反应溶液pH 10.5。在此检测条件下,9种生物胺在质量浓度1.0~100.0 mg/L范围内线性关系良好,相关系数R2均≥0.999 0。该方法的检出限为0.011~0.036 mg/L,定量限为0.038~0.120 mg/L,平均加标回收率为83.33%~118.44%,精密度试验结果的相对标准偏差(RSD)为0.48%~6.99%,说明该方法操作简单、衍生效果好、准确度高,适用于不同种类发酵酒中9种生物胺的快速检测。采用该方法对啤酒、葡萄酒及黄酒中的9种生物胺含量进行检测,结果显示黄酒中生物胺总含量最高,葡萄酒次之,啤酒中生物胺总含量最低。 该方法为同时测定发酵酒中9种生物胺的研究提供了可靠的理论依据与数据支撑。
[1] 刘景,任婧,孙克杰. 食品中生物胺的安全性研究进展[J] . 食品科学,2013,34(5):322-326.
[2] PARK Y K, LEE J H, MAH J H. Occurrence and reduction of biogenic amines in traditional Asian fermented soybean foods:A review[J] .Food Chem,2019,278:1-9.
[3] 王光强,俞剑燊,胡健,等. 食品中生物胺的研究进展[J] . 食品科学,2016,37(1):269-278.
[4] MATHUR P R. Determination of biogenic amines in foods by capillary electrophoresis[J] .J Res Sci Eng,2024,6(11):76-82.
[5] HAYDEN K B L P. Brewing and the chemical composition of aminecontaining compounds in beer:A review[J] .Foods,2022,11(3):257.
[6] 段雨帆,钟媛媛,朱霄,等. 葡萄球菌对发酵肉制品中生物胺降解机制研究进展[J] .肉类研究,2022,36(1):49-55.
[7] 周朗君,陈钦,李秀英. 丹磺酰氯柱前衍生-反相高效液相色谱法同时测定水产品中9种生物胺[J] .食品安全质量检测学报,2025,16(5):24-31.
[8] FLASAROVA R,PACHLOVA V,BUNKOVA L, et al. Biogenic amine production by Lactococcus lactis subsp cremoris strains in the model system of Dutch-type cheese[J] .Food Chem,2016,194:68-75.
[9] 张凤杰,薛洁,王异静,等.黄酒中生物胺的形成及其影响因素[J] .食品与发酵工业,2013,39(2):62-68.
[10] 杨姗姗,张凤艳,蒋万枫,等. 发酵酒中生物胺的研究进展[J] . 中国酿造,2022,41(3):18-23.
[11] 赵斌,李娣娣,袁源,等. 发酵型功能酒的现代研究进展[J] . 酿酒,2025,52(2):43-49.
[12] 李信,饶文俊,胡帅,等. 米香型白酒小曲发酵酒醅微生物群落演绎与理化因子的相关性[J] .中国食品学报,2024,24(10):384-393.
[13] LI X,YAO J,LEI D,et al.The dynamic of biogenic amines and higher alcohols of Chinese rice wine during fermentation[J] .Food Sci Biotechnol,2024,34(6):1-10.
[14] 吴玉田,王颖怡,张权,等. 超高效液相色谱-串联质谱法测定冷冻水产品中生物胺[J] .分析科学学报,2023,39(6):737-742.
[15] IVANA R,BORIS S,PAVLINA J,et al.Detection of microbiota during the fermentation process of wine in relation to the biogenic amine content[J] .Foods,2022,11(19):3061.
[16] KRSTE TAŠEV, IVANOVA-PETROPULOS V, STEFOVA M. Ultraperformance liquid chromatography-triple quadruple mass spectrometry(UPLC-TQ/MS)for evaluation of biogenic amines in wine[J] .Food Anal Met,2017,10(10):1-11.
[17] 刘慕妆,任红,孙哲,等. 黄酒生物胺的研究进展[J] . 中国酿造,2022,41(3):30-37.
[18] 周江平,木玉仙,和春映,等.氯甲酸异丁酯衍生结合气相色谱-质谱法测定葡萄酒和黄酒中7种生物胺的含量[J] .理化检验-化学分册,2025,61(3):338-344.
[19] 何宇芬,邱佩丽,曾游,等. 基于不同检测器的水产品生物胺离子色谱法研究进展[J] .质量安全与检验检测,2024,34(3):30-37.
[20] 魏家保,唐双燕,谢嘉慧,等. 基于薄层色谱和指纹图谱的百合成分差异性研究[J] .中国现代中药,2024,26(9):1503-1510.
[21] 杨静,王琨,周元. 气相色谱-电子捕获检测器分析葡萄酒中的8种生物胺[J] .中国酿造,2023,42(2):228-234.
[22] 易雨欣,金米聪. 离子色谱-质谱联用技术在生命健康领域中的应用进展[J] .色谱,2024,42(10):923-934.
[23] JIA S,KANG Y P,PARK J H,et al.Determination of biogenic amines in Bokbunja(Rubus coreanus Miq.)wines using a novel ultra-performance liquid chromatography coupled with quadrupole-time of flight mass spectrometry[J] .Food Chem,2012,132(3):1185-1190.
[24] SON C Y,KEE A L,LIN M C,et al.Determination of biogenic amines in chicken, beef, and mutton by dansyl chloride microwave derivatization in Malaysia[J] .J Food Sci,2023,88(2):650-665.
[25] 吴迪,黄海琴,蔡成岗,等. 生物胺丹磺酰氯衍生条件优化研究[J] . 食品与发酵科技,2018,54(1):45-49.
[26] 张文豪,樊金星,张叶,等. 苯甲酰氯衍生-高效液相色谱法测定鱼露中的生物胺[J] .河南预防医学杂志,2022,33(7):488-491.
[27] 杨媖舒,金昊坤,舒耀皋.邻苯二甲醛/巯基乙醇柱前衍生—高效液相色谱法测定水中3种氟乙胺类化合物的含量[J] .理化检验-化学分册,2022,58(11):1338-1341.
[28] YU W L,LEWIS N S,GRAY H B,et al.Isotopically selective quantification by UPLC-MS of aqueous ammonia at submicromolar concentrations using dansyl chloride derivatization[J] . ACS Energy Lett, 2020,5(5):1532-1536.
[29] 郭雯,郑冬梅,李晓东,等.RP-HPLC柱后衍生法检测干酪中6种生物胺[J] .中国食品学报,2015,15(5):213-218.
[30] MEY E D, DRABIK-MARKIEWICZ G, MAERE H D, et al. Dabsyl derivatisation as an alternative for dansylation in the detection of biogenic amines in fermented meat products by reversed phase high performance liquid chromatography[J] .Food Chem,2012,130(4):1017-1023.
[31] 李冉冉,李洪军,贺稚非. 响应面法优化丹磺酰氯衍生生物胺的衍生条件[J] .食品与发酵工业,2019,45(17):136-143.
[32] 吴玉田,王颖怡,张权,等. 超高效液相色谱-串联质谱法测定冷冻水产品中生物胺[J] .分析科学学报,2023,39(6):737-742.
[33] 李书婷,尹礼国,吴正云,等.中国黄酒和白酒中生物胺的研究进展[J] .食品与发酵工业,2024,50(10):327-334.