普鲁兰多糖(pullulan)是一种由出芽短梗霉(Aureobasidium pullulans)发酵所产生的类似葡聚糖、黄原胶的胞外水溶性粘质多糖。是由α-1,4糖苷键连接的麦芽三糖重复单位经α-1,6糖苷键聚合而成的直链状多糖,聚合度100~5 000,分子质量大小为4.5×104~4.5×105 Da[1]。 普鲁兰多糖具有优异的成膜性、可塑性、生物兼容性、可降解性和水溶性[2],且无毒无害、无色无味[3],被广泛应用于食品包装、医药载体、化妆品及环境友好材料等领域[4]。近年来,随着可持续发展理念的深化和绿色材料需求的增长,普鲁兰多糖作为一种可再生的生物高分子,受到了学术界和工业界的广泛关注[5]。尽管普鲁兰多糖具有显著的应用潜力,但其工业化生产仍面临诸多挑战,其中发酵成本高和产量不稳定是制约其大规模推广的核心问题。普鲁兰多糖的生产效率高度依赖于菌株性能、培养基组成及发酵工艺的优化。目前的研究主要围绕高产菌株的选育(如诱变育种和基因工程改造)[6-7]、机理研究[8]、廉价碳源(如淀粉水解物、工业副产物)的替代[9],以及发酵参数(pH、温度、溶氧量)的动态调控[10]展开。 此外,培养基优化是降低生产成本的关键环节,通过响应面法[11]、人工神经网络(artificial neural network,ANN)[12] 等策略对碳氮源比例及微量元素进行精准调配,可显著提高多糖产率并减少原料浪费。
机器学习可以利用人工神经网络(ANN)和遗传算法(genetic algorithm,GA)处理复杂非线性关系,通过主动学习动态调整实验设计,具有高效准确、可实现多目标优化、支持工业化放大的优点[13-14]。现今,人工神经网络已被广泛应于各种发酵条件优化的建模和预测[15-16]。 在普鲁兰多糖发酵条件的优化过程中,采用GA-ANN进行发酵培养基的优化可以提高普鲁兰多糖的产量[17]。机器学习优化技术相比传统的优化策略(如响应面试验设计、正交试验设计等)具有更好的适用性,凸显了机器学习技术在复杂生物过程优化中的显著优势[18-19]。 正交实验偶联人工神经网络可以对显著因素进行精细优化,处理复杂非线性关系,提升优化效率和精度。
本研究以出芽短梗霉(Aureobasidium pullulans)为出发菌株,利用紫外诱变技术筛选高产普鲁兰多糖菌株,进一步通过正交试验偶联人工神经网络对高产普鲁兰多糖菌株的发酵条件进行优化。旨在为普鲁兰多糖工厂化生产提供数据参考。
1 材料与方法
1.1 材料与试剂
1.1.1 菌株
出芽短梗霉(Aureobsidium pullulans)[中国普通微生物菌株保藏管理中心(China General Microbiological Culture Collection Center,CGMCC)NO.7055] :天津慧智百川生物工程有限公司。
1.1.2 化学试剂
葡萄糖(分析纯):西王药业有限公司;酵母浸粉a~n(均为生化试剂):新疆托克新生物科技有限公司;硫酸铵、无水硫酸钠(均为分析纯):天津市大茂化学试剂厂;磷酸氢二钾(分析纯):北京奥博星生物技术有限公司;氯化钠(分析纯):天津市津东天正精细化学试剂厂;结晶硫酸镁(分析纯):博欧特(天津)化工贸易有限公司;硫酸亚铁:天津博迪化工股份有限公司;味精(谷氨酸钠):梅花集团。
1.1.3 培养基
马铃薯葡萄糖琼脂(potato dextrose agar,PDA)斜面培养基:土豆200.00 g/L,琼脂20.00 g/L,葡萄糖20.00 g/L,121 ℃高压灭菌20 min。
种子培养基:酵母浸粉a 2.00 g/L,(NH4)2SO4 0.50 g/L,K2HPO4 3.00 g/L,MgSO4·7H2O 0.80 g/L,NaCl 3.00 g/L,FeSO4·7H2O 0.06 g/L,葡萄糖75.0 g/L,初始pH值6.00。121 ℃高压灭菌20 min。
基础发酵培养基:葡萄糖125 g/L,酵母浸粉a 8.00 g/L,MgSO4·7H2O 1.50 g/L,K2HPO4 2.50 g/L,NaCl 5.00 g/L,初始pH值6.03。121 ℃高压灭菌20 min。
曲利苯蓝筛选培养基:土豆200.00 g/L,琼脂20.00 g/L,葡萄糖20.00 g/L,曲利苯蓝0.02 g/L。121 ℃高压灭菌20 min。
1.2 仪器与设备
紫外诱变箱:自制;UV-1200紫外分光光度计:上海元析仪器有限公司;SKY-2102摇床:上海苏坤实业有限公司;YJ-875S医用超净工作台:苏州净化设备厂;SPK-250恒温生化培养箱:北京永光明医疗器械厂;TDL-5-A高速离心机:上海安亭科学仪器厂;LC-20A高效液相色谱分析仪:日本株式会社岛津制作所。
1.3 方法
1.3.1 培养方法
斜面培养:取-80 ℃甘油管保藏菌种化冻后三区划线平板培养转接至PDA斜面,28 ℃恒温培养箱中培养3~4 d。
种子培养:取出低温保存的斜面,活化后挑取一环孢子转接至种子培养基,28 ℃、180 r/min摇床恒温振荡培养24 h,即得种子培养液。
发酵培养:按3%(V/V)接种量将种子培养液转接至装液量为100 mL/250 mL发酵培养基中,总培养周期96 h,采用两阶段控温发酵:先于32 ℃、180 r/min振荡培养24 h,后于28 ℃、180 r/min振荡培养72 h。
1.3.2 分析检测
(1)生物量
生物量:采用干燥法测定。取5.00 mL发酵液置于10 mL离心管中离心、重悬,弃上清,置于65 ℃恒温烘箱中烘干至恒质量并称量,生物量计算公式如下:
式中:m为生物量,g/L;m1为离心管干质量,g;m2为菌体与离心管总质量,g。
(2)普鲁兰多糖产量
普鲁兰多糖产量:采用醇沉法测定。取上清液20.0 mL按体积比1∶2加入无水乙醇,于4 ℃静置12 h后抽滤,将滤纸与沉淀置于65 ℃烘箱中烘干至恒质量并称量,普鲁兰多糖的产量计算公式如下:
式中:m为普鲁兰多糖产量,g/L;m1为干燥滤纸质量,g;m2为普鲁兰多糖与干燥滤纸总质量,g。
(3)普鲁兰多糖重均分子质量
普鲁兰多糖重均分子质量:采用高效液相色谱法[20-21]测定。
1.3.3 紫外诱变实验
(1)孢子悬液制备
采用差速离心法(5 000 r/min离心5 min)从对数生长期菌液中分离菌体,经2次无菌生理盐水离心洗涤并用无菌生理盐水重悬菌体,加入灭菌玻璃珠(直径5 mm,10~15粒),通过涡旋振荡(20 min)的方法使孢子充分分散,无菌条件下取样检测菌悬液吸光度值(OD620 nm值),调整至0.3~0.5范围,获得标准化孢子悬液。
(2)紫外诱变处理
向置有灭菌磁力转子的无菌培养皿中(直径90 mm)加入2.00 mL孢子悬液,使用紫外诱变箱进行处理。取1.00 mL不同照射时间处理液稀释到适合的浓度,取100 μL稀释液涂布于PDA培养基上,28 ℃避光培养72~96 h,进行活菌计数,以未经紫外处理的菌悬液为对照,计算不同照射时间条件下致死率,并绘制致死率曲线。致死率计算公式如下:
(3)平板初筛
将诱变后孢子悬浮液稀释,均匀涂布于曲利苯蓝筛选平板上,于生化箱中28 ℃恒温培养72~96 h。曲利苯蓝与多糖结合显蓝色的本质是醌基-氨基/羟基间的多重相互作用,受pH、多糖结构及环境离子强度调控,对诱变菌的胞外多糖生产差异能够明显分辨。 以菌落大小、颜色深浅等特征为筛选指标,挑取出芽短梗霉菌落直径大、表面湿润的变异株,将其进行编号保存。 将平板初筛获得的变异菌株进行摇瓶发酵培养,选取普鲁兰多糖产量提高率20%以上的突变菌株,进行下一步摇瓶复筛。
(4)摇瓶发酵复筛
对初筛得到的正突变变异菌株进行摇瓶发酵,测定普鲁兰多糖产量,并选出产量提升率高于35%的突变株进行遗传稳定性试验验证。
(5)遗传稳定性验证试验
将复筛获得变异菌株连续斜面传代十次,取一、三、五、七、十代进行发酵验证,测定突变株的普鲁兰多糖产量,验证其遗传稳定性。
1.3.4 发酵条件优化
(1)单因素试验
分别以发酵培养基中氮源种类、最佳氮源、葡萄糖、无机盐、味精添加量、初始pH值为影响因素,考察其对普鲁兰多糖产量、分子质量和生物量的影响。
(2)正交试验偶联人工神经网络
在单因素试验结果基础上,以普鲁兰多糖产量为评价指标,设计多因素正交试验,发酵条件优化正交试验因素与水平见表1。 通过使用正交设计助手进行正交试验的设计,在网站(www.spsspro.com)进行极差分析和方差分析。以正交试验结果为基础作为人工神经网络的学习样本建立模型,通过遗传算法寻找发酵条件模型最优解。
表1 发酵条件优化正交试验因素与水平
Table 1 Factors and levels of orthogonal experiments for fermentation condition optimization
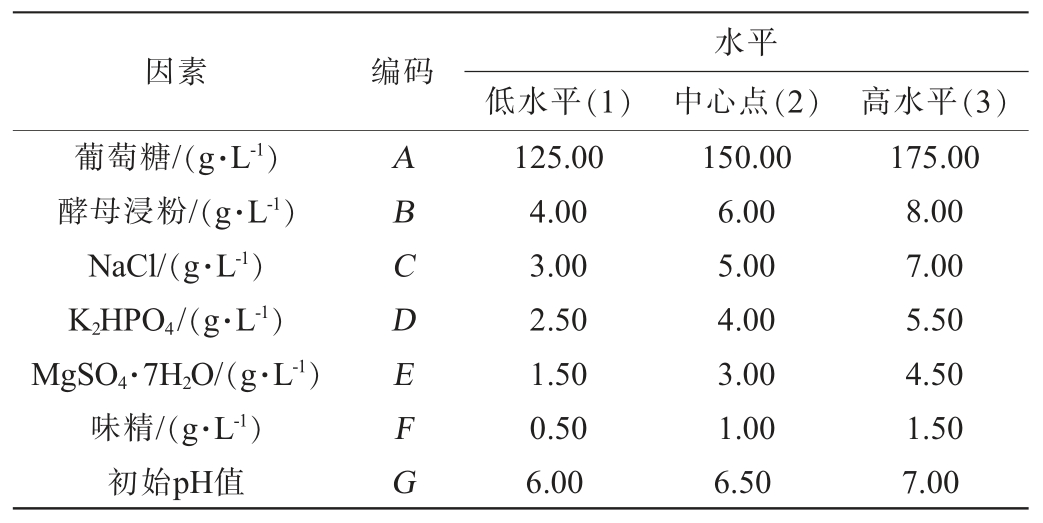
因素编码低水平(1)水平中心点(2) 高水平(3)葡萄糖/(g·L-1)酵母浸粉/(g·L-1)NaCl/(g·L-1)K2HPO4/(g·L-1)MgSO4·7H2O/(g·L-1)味精/(g·L-1)初始pH值ABCDEFG 125.00 4.00 3.00 2.50 1.50 0.50 6.00 150.00 6.00 5.00 4.00 3.00 1.00 6.50 175.00 8.00 7.00 5.50 4.50 1.50 7.00
2 结果与分析
2.1 紫外诱变
2.1.1 诱变时间的确定
对原始菌株CGMCC NO.7055进行紫外诱变处理,并绘制致死率曲线,结果见图1。
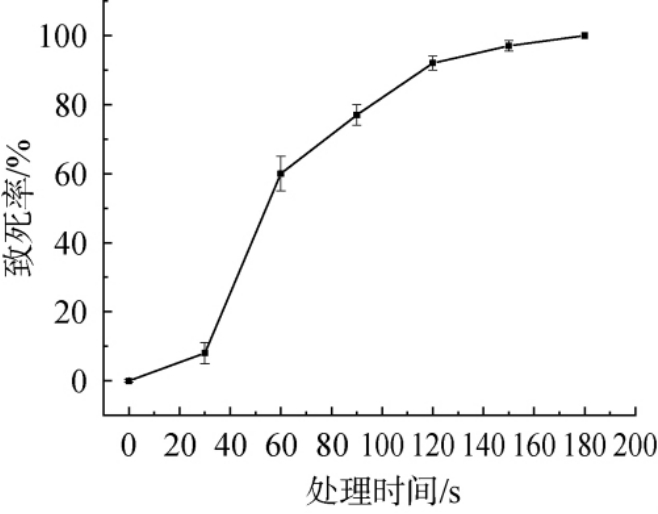
图1 菌株CGMCC NO.7055紫外诱变致死率曲线
Fig. 1 Ultraviolet mutagenesis lethality curve of strain CGMCC NO.7055
由图1可知,随紫外照射时间延长,致死率逐渐增加,诱变处理时间为120 s时,致死率达到92%,诱变处理时间为150 s时,致死率达到97%,研究表明[22],当致死率控制在80%~90%时,既能保证脱氧核糖核酸(deoxyribonucleicacid,DNA)发生足够多的损伤以产生有效突变,又能保留足够数量的存活菌株用于后续筛选,从而提高正突变概率,紫外诱变后若菌体未完全失活(如致死率过低),残留的活菌可能通过光复活作用修复DNA损伤,导致突变率虚高。 而90%左右的致死率可有效减少光复活干扰,确保筛选结果的准确性[23]。因此,选择最佳诱变处理时间为110 s。
2.1.2 突变菌株筛选
通过平板初筛和摇床复筛得到4株高产普鲁兰多糖突变菌株,分别命名为菌株UV008、UV013、UV033、UV064,其结果见表2。由表2可知,4株高产普鲁兰多糖突变菌株多糖产量[(65.00~67.60)g/L] 均高于原始菌株(40.00 g/L),重均分子质量[(1.06×105~1.26×105 Da)] 均低于原始菌株(1.46×105Da),普鲁兰多糖产量比原始菌株提高了62.50%~69.00%。
表2 突变菌株复筛结果
Table 2 Re-screening results of the mutant strains
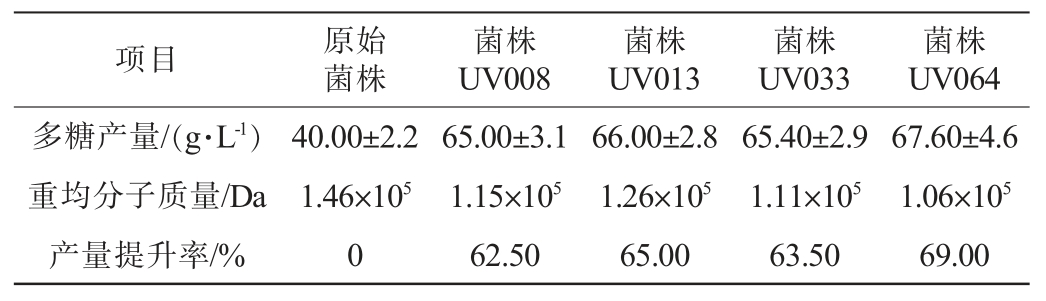
项目原始菌株菌株UV008菌株UV013菌株UV033菌株UV064多糖产量/(g·L-1)重均分子质量/Da产量提升率/%40.00±2.2 1.46×105 0 65.00±3.1 1.15×105 62.50 66.00±2.8 1.26×105 65.00 65.40±2.9 1.11×105 63.50 67.60±4.6 1.06×105 69.00
2.1.3 诱变菌种遗传稳定性试验及验证试验
以普鲁兰多糖产量、分子质量和生物量为评价指标,诱变菌株UV008、UV013、UV033、UV064进行五代以内遗传稳定性试验及诱变菌株UV013十代以内遗传稳定性验证试验结果见图2。
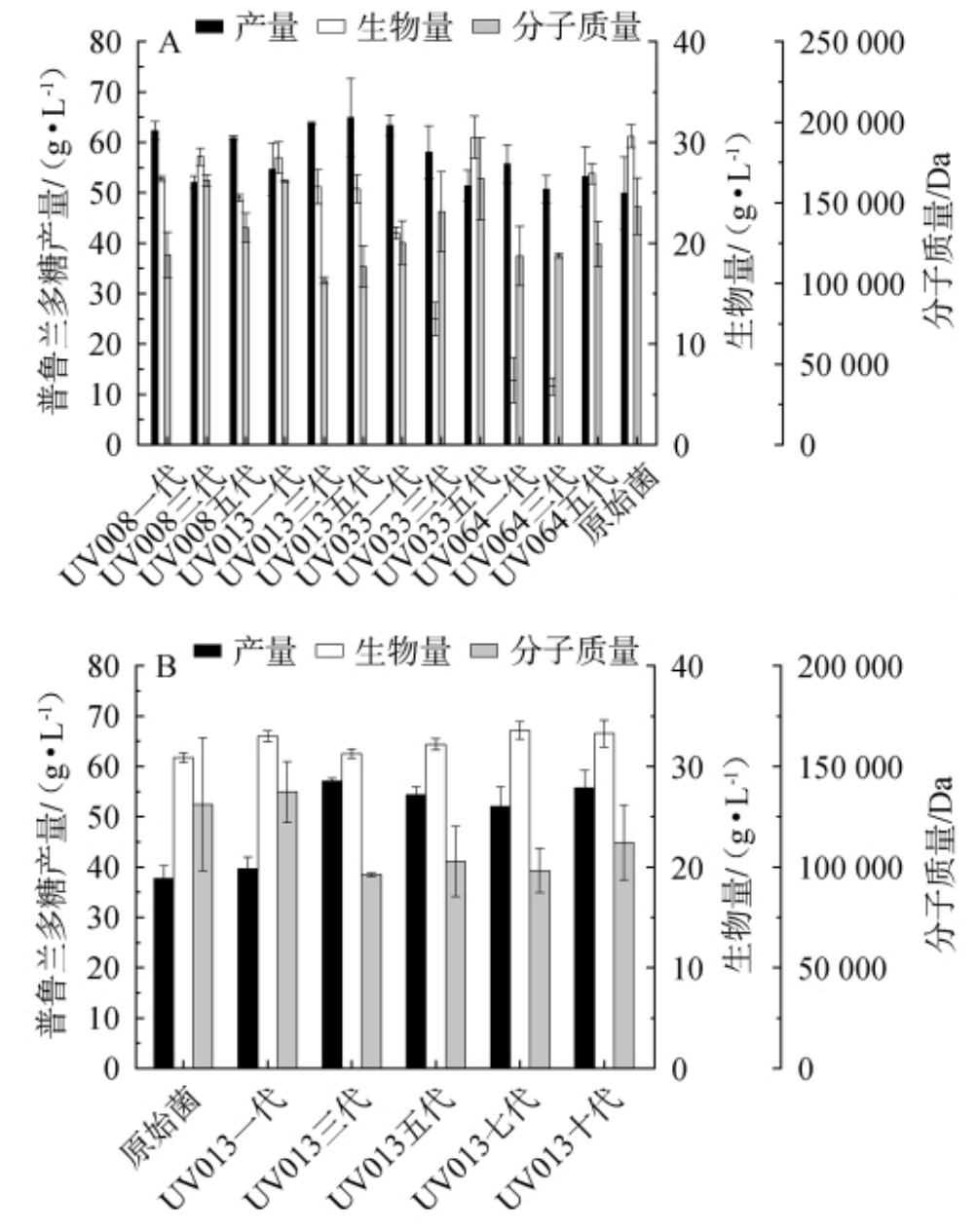
图2 诱变菌株遗传稳定性试验(A)及诱变菌株UV013验证试验(B)结果
Fig. 2 Results of genetic stability tests of the mutant strains (A) and verification tests of the mutant strain UV013 (B)
由图2A可知,初步对4株诱变菌株进行五代以内的稳定性验证,结果表明,只有诱变菌株UV013在五代传代稳定性验证中保持产量稳定,因此进一步对菌株UV013进行十代以内遗传稳定性验证试验。由图2B可知,诱变菌株UV013除第一代产量略高于原始菌株以外,其产量稳定且高于原始菌株,诱变菌株UV013的普鲁兰多糖产量平均达到55.70 g/L,较原始菌株普鲁兰多糖产量提升了39.30%,重均分子质量达到1.12×105 Da。将筛选得到一株稳定的高产普鲁兰多糖菌株UV013进行发酵条件优化。
2.2 发酵条件的优化
2.2.1 氮源对菌株UV013发酵产普鲁兰多糖的影响
氮源是微生物生长和代谢中的关键物质,由于目前市场上的各种有机氮源的成分及生产工艺存在差异。不同有机氮源对于出芽短梗霉生长以及发酵生产普鲁兰多糖的影响也十分显著。 添加量均为8 g/L不同种类氮源以及最佳氮源添加量对菌株UV013发酵产普鲁兰多糖的影响见图3。
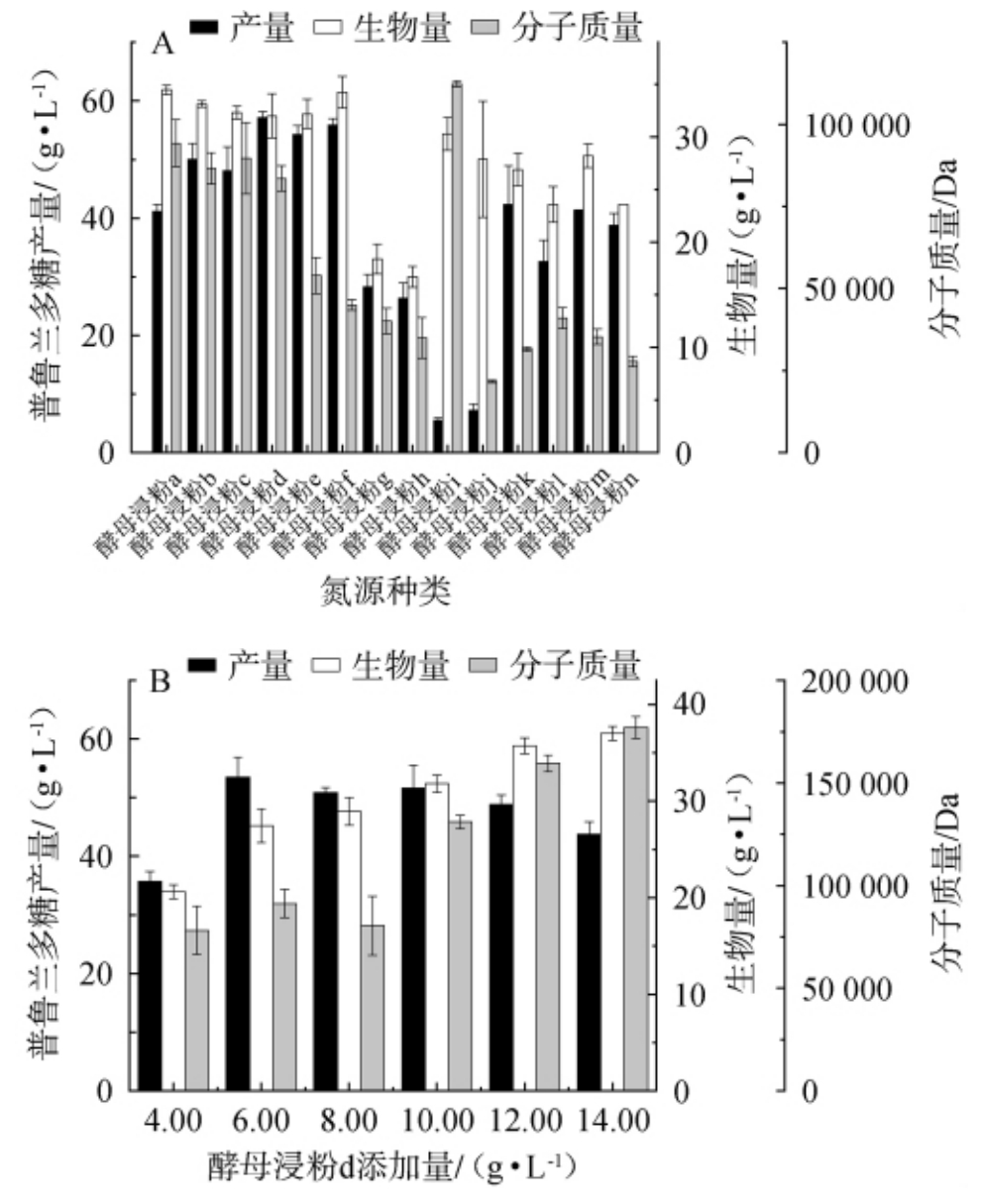
图3 不同氮源种类(A)和酵母浸粉d添加量(B)对菌株UV013发酵产普鲁兰多糖的影响
Fig. 3 Effect of different nitrogen source types (A) and yeast extract powder d addition (B) on pullulan yield fermented by strain UV013
由图3A可知,酵母浸粉a作为原始氮源,菌株UV013发酵普鲁兰多糖产量为41.30 g/L,生物量为34.70 g/L,重均分子质量9.42×104 Da;选择酵母浸粉d作为氮源时,普鲁兰多糖产量最高,为57.40 g/L,生物量32.00 g/L,重均分子质量为8.35×104 Da,与原始氮源(酵母浸粉a)相比,普鲁兰多糖产量显著提高了39.00%(P<0.05),重均分子质量显著下降约11.40%(P<0.05),生物量下降7.78%。因此,选用酵母浸粉d作为最佳氮源。
由图3B可知,随着酵母浸粉d添加量在4.00~14.00 g/L范围内的增加,普鲁兰多糖产量呈先上升后下降的趋势。当酵母浸粉d添加量为6.00 g/L时,普鲁兰多糖产量最高,为53.50 g/L,生物量为27.40 g/L,重均分子质量为9.13×104 Da。有机氮源会促进菌体生长和尿苷二磷酸葡萄糖-焦磷酸化酶等酶的活性,当氮源不足时会使菌体生长受限,而过量则转向菌体增殖,减少多糖积累[24]。 当酵母浸粉d添加量>6.00 g/L之后,多糖产量逐渐降低,这可能是由于过多的有机氮源供给促使碳源流向生物体自身用于菌体增殖[25-27]。因此,酵母浸粉d最适添加量为6.00 g/L。
2.2.2 葡萄糖添加量对菌株UV013发酵产普鲁兰多糖的影响
不同葡萄糖添加量对菌株UV013发酵产普鲁兰多糖的影响结果见图4。
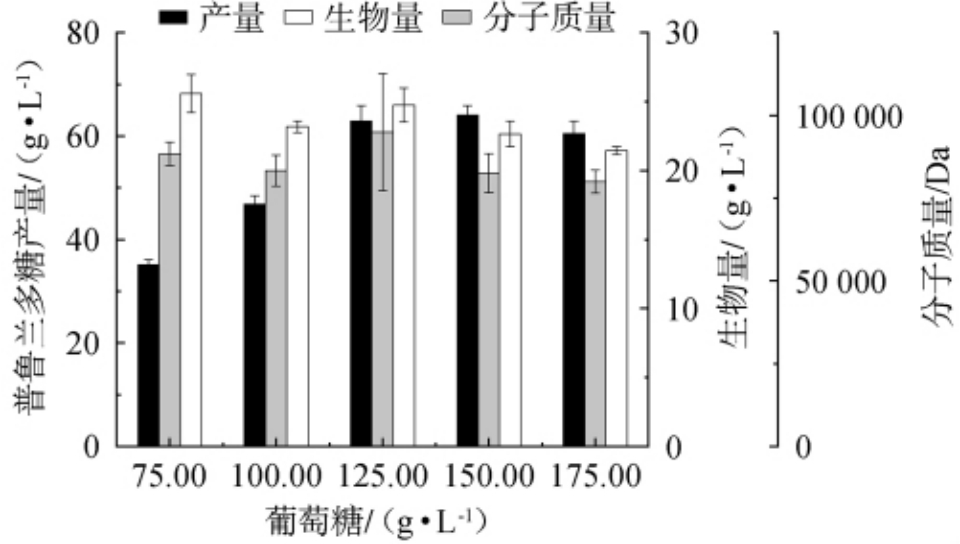
图4 葡萄糖添加量对菌株UV013发酵产普鲁兰多糖的影响
Fig. 4 Effect of glucose addition on pullulan yield fermented by strain UV013
由图4可知,随着葡萄糖添加量在75~175 g/L范围的增加,普鲁兰多糖产量呈先上升后下降的趋势。当葡萄糖添加量为150.00 g/L时,普鲁兰多糖产量最高,为64.10 g/L,重均分子质量为9.44×104 Da,生物量为19.80 g/L。相较于初始发酵条件而言,普鲁兰多糖产量提高约1.91%,重均分子质量下降约8.48%,生物量下降约13.16%。葡萄糖作为底物和能源供应,促进菌体生长和酶的活性。当葡萄糖添加量>150.00 g/L之后,C/N比过高,可能引发代谢副产物抑制多糖的合成;过高浓度也会导致渗透压应激,抑制菌体生长[28];此外引发葡萄糖阻遏效应,抑制多糖合成[29]。因此,碳源最适葡萄糖添加量为150.00 g/L。
2.2.3 不同无机盐及添加量对菌株UV013发酵产普鲁兰多糖的影响
不同无机盐对菌株UV013发酵产普鲁兰多糖的影响结果见图5。
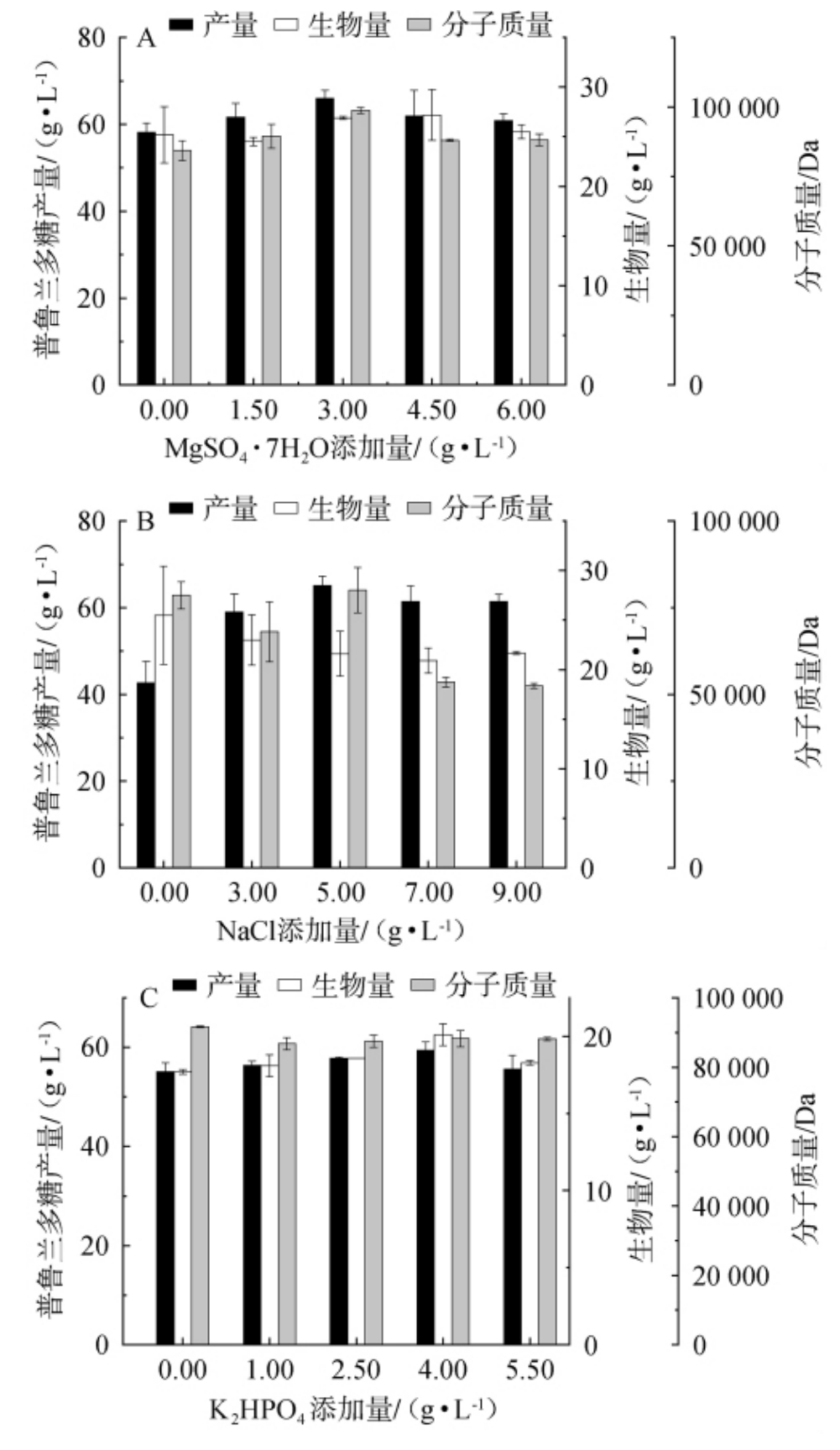
图5 不同无机盐添加量对菌株UV013发酵产普鲁兰多糖的影响
Fig. 5 Effect of different inorganic salts addition on pullulan yield fermented by strain UV013
由图5A可知,随着MgSO4·7H2O添加量的增加,普鲁兰多糖产量呈先上升后下降的趋势,当MgSO4·7H2O添加量为3.00 g/L时,普鲁兰多糖产量最高,为66.10 g/L,重均分子质量为9.87×104 Da,生物量为26.90 g/L。Mg2+是多种酶的辅因子,尤其是与糖代谢相关的激酶(如已糖激酶)和三磷酸腺苷(adenosine triphosphate,ATP)依赖的酶[30]。 普鲁兰多糖合成需要二磷酸尿甘葡糖(uridine diphosphate glucose,UDP)作为前体,其生成途径依赖Mg2+参与的磷酸化反应。 Mg2+通过增强糖酵解途径和磷酸戊糖途径,增加UDP-葡萄糖的供应,从而促进普鲁兰多糖前体的生成[31]。MgSO4可调节发酵液的渗透压,影响微生物的胞内环境。适度的渗透压可能刺激微生物分泌多糖作为保护机制,但过高浓度会抑制生长。因此,MgSO4·7H2O最适添加量为3.00 g/L。
由图5B可知,随着NaCl添加量的增加,普鲁兰多糖产量呈先上升后下降的趋势,当NaCl添加量为5.00 g/L时,普鲁兰多糖产量最高,为65.10 g/L,重均分子质量为8.00×104 Da,生物量为21.60 g/L。分析其可能的原因是NaCl对出芽短梗霉合成普鲁兰多糖的影响具有浓度依赖性,NaCl主要会影响渗透压和代谢途径。合适的NaCl添加量可以调节渗透压处于合适范围,可维持细胞膜稳定性,促进菌丝体网络形成,增强代谢物交换效率[32]。 NaCl浓度过高会导致细胞质水分外流,膜脂质过氧化,菌体存活率下降。高盐激活Hog1全局调控因子,优先分配能量至抗逆基因(如热激蛋白),抑制多糖合成通路。低盐环境抑制生物膜相关基因(如bmlA)表达,削弱多糖合成酶的辅因子(如Na+)激活作用[33]。 因此NaCl最适添加量为5.00 g/L。
由图5C可知,随着K2HPO4添加量的增加,普鲁兰多糖产量呈先上升后下降的趋势。 当K2HPO4添加量为4.00 g/L时,普鲁兰多糖产量最高,为59.40 g/L,重均分子质量为8.83×104 Da,生物量为20.10 g/L。发酵培养基中磷酸盐浓度偏低不利于菌体生长,偏高则抑制普鲁兰合成,因为偏高的浓度增加了培养基缓冲容量而阻止了向有利于合成的最佳范围转变[34-35]。因此,K2HPO4最适添加量为4.00 g/L。
2.2.4 味精添加量对菌株UV013发酵产普鲁兰多糖的影响
不同味精添加量对菌株UV013发酵产普鲁兰多糖的影响结果见图6。
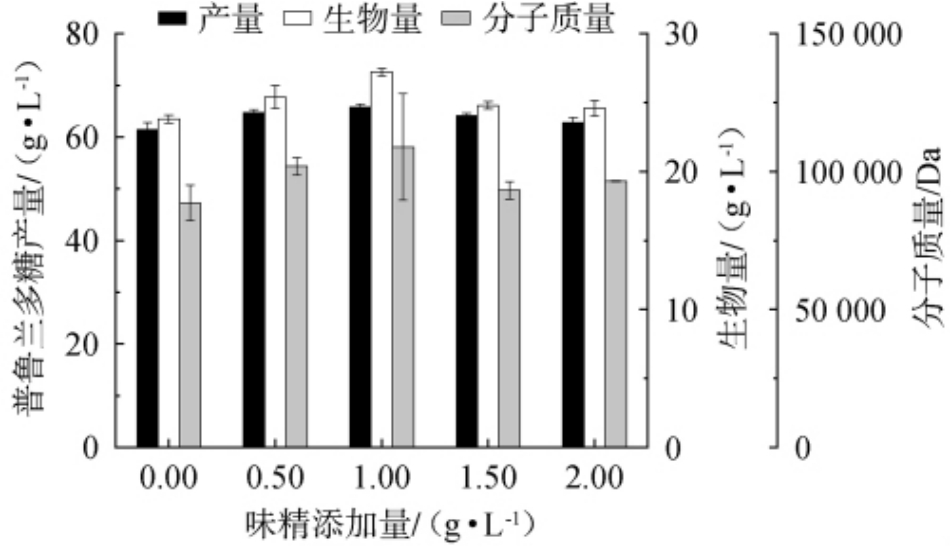
图6 味精添加量对菌株UV013发酵产普鲁兰多糖的影响
Fig. 6 Effect of monosodium glutamate addition on pullulan yield fermented by strain UV013
由图6可知,随着味精添加量的增加,普鲁兰多糖产量呈先上升后下降的趋势。 当味精添加量为1.00 g/L时,普鲁兰多糖产量最高,为66.00 g/L,重均分子质量为1.09×105Da,生物量为27.20 g/L。谷氨酸可以直接或间接转化为三羧酸循环的中间代谢物,加强了三羧酸循环,能够为菌体生长和合成普鲁兰多糖提供更多能量,L-谷氨酸经过多步反应可以生成ABC转运蛋白,这种蛋白有利于向细胞外分泌普鲁兰多糖,减少底物的抑制,促进普鲁兰多糖的合成[36]。高浓度的味精会提高发酵液的渗透压,对菌体细胞造成胁迫,抑制菌体的生长和代谢活性,导致产量下降。因此,味精最适添加量为1.00 g/L。
2.2.5 初始pH值对普鲁兰多糖发酵的影响
不同初始pH值对菌株UV013发酵产普鲁兰多糖的影响结果见图7。
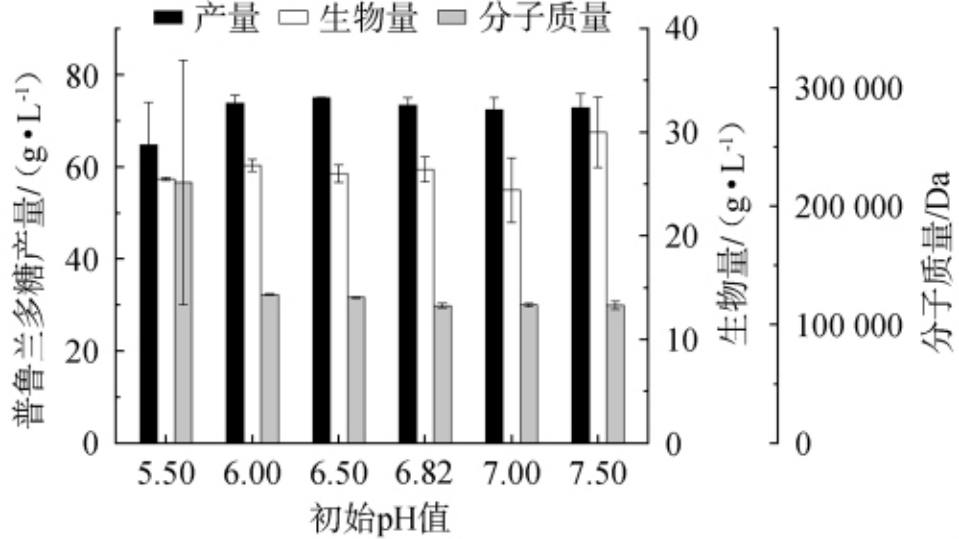
图7 初始pH值对菌株UV013发酵产普鲁兰多糖的影响
Fig. 7 Effect of initial pH values on pullulan yield fermented by strain UV013
由图7可知,当培养基初始pH值在5.50~7.50时,随着pH值的增大,普鲁兰多糖产量呈先上升后下降的趋势。普鲁兰多糖产量在pH为6.50时普鲁兰多糖产量最高,为75.00 g/L,分子质量达到1.23×105 Da,生物量为26.00 g/L。培养基的pH对菌株的形态,普鲁兰的分子质量大小及产量均有影响[37]。弱酸性条件有利于普鲁兰多糖的生物合成[38-39]。当初始pH值变化范围在6.00~7.50之间时,普鲁兰多糖产量并无显著性差异。因此,最适初始pH值为6.50。
2.3 正交试验偶联人工神经网络优化发酵条件
2.3.1 正交试验
正交试验设计与结果见表3,对正交试验结果进行多因素方差分析,结果见表4。 由表3可知,按照极差分析得出最佳发酵条件为:葡萄糖175.00 g/L、酵母浸粉d 8.00 g/L、NaCl 7.00 g/L、K2HPO4 5.50 g/L、MgSO4·7H2O 3.00 g/L、味精1.50 g/L、初始pH值6.50。 在此优化条件下进行3次平行验证试验,普鲁兰多糖产量平均值为77.10 g/L。
表3 发酵条件优化正交试验设计与结果
Table 3 Design and results of orthogonal experiments for fermentation conditions optimization
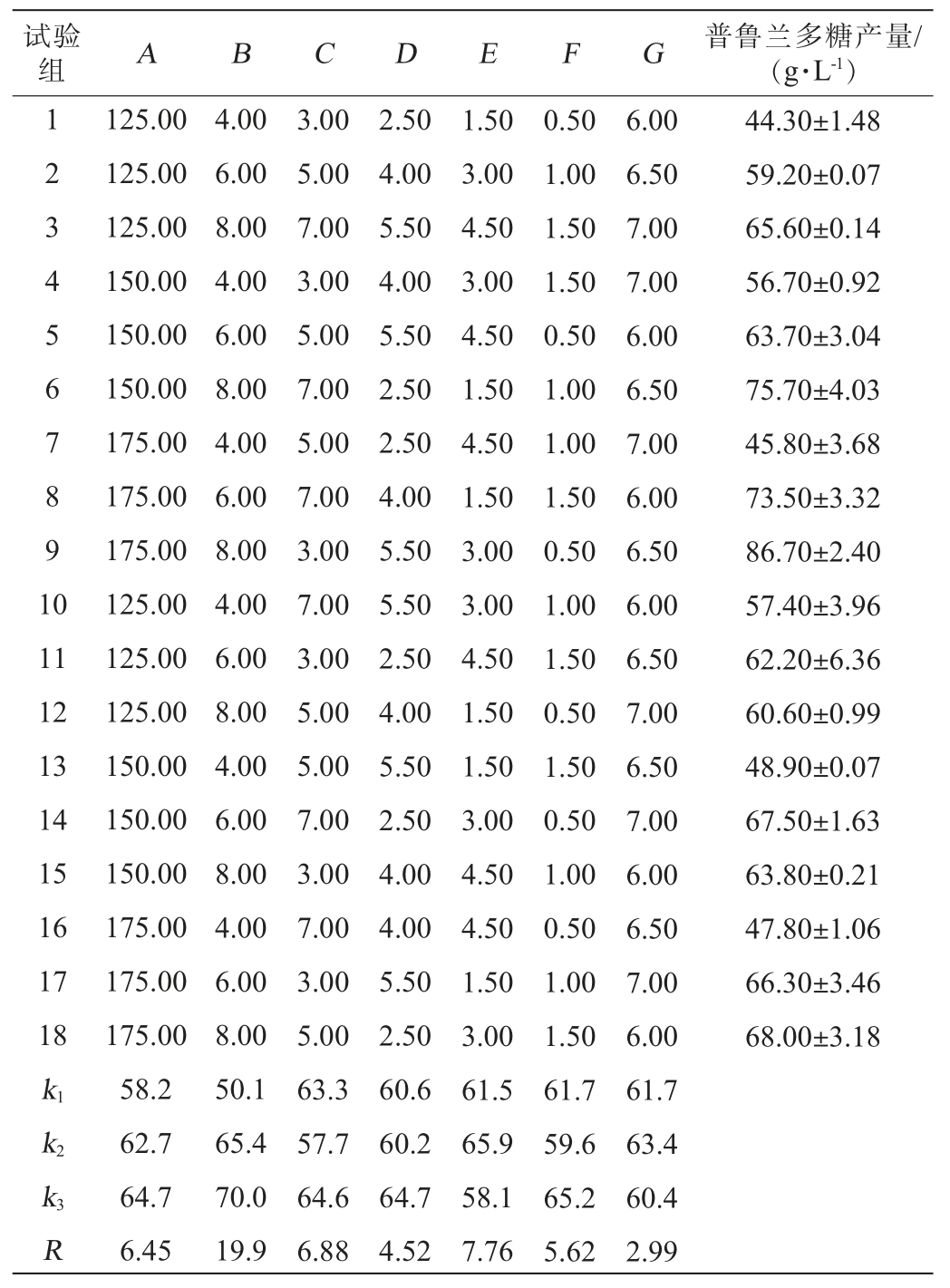
试验组ABCDEFG普鲁兰多糖产量/(g·L-1)1 2 3 4 5 6 7 8 9 1 0 11 12 13 14 15 16 17 18 k1 k2 44.30±1.48 59.20±0.07 65.60±0.14 56.70±0.92 63.70±3.04 75.70±4.03 45.80±3.68 73.50±3.32 86.70±2.40 57.40±3.96 62.20±6.36 60.60±0.99 48.90±0.07 67.50±1.63 63.80±0.21 47.80±1.06 66.30±3.46 68.00±3.18 k3 R 125.00 125.00 125.00 150.00 150.00 150.00 175.00 175.00 175.00 125.00 125.00 125.00 150.00 150.00 150.00 175.00 175.00 175.00 58.2 62.7 64.7 6.45 4.00 6.00 8.00 4.00 6.00 8.00 4.00 6.00 8.00 4.00 6.00 8.00 4.00 6.00 8.00 4.00 6.00 8.00 50.1 65.4 70.0 19.9 3.00 5.00 7.00 3.00 5.00 7.00 5.00 7.00 3.00 7.00 3.00 5.00 5.00 7.00 3.00 7.00 3.00 5.00 63.3 57.7 64.6 6.88 2.50 4.00 5.50 4.00 5.50 2.50 2.50 4.00 5.50 5.50 2.50 4.00 5.50 2.50 4.00 4.00 5.50 2.50 60.6 60.2 64.7 4.52 1.50 3.00 4.50 3.00 4.50 1.50 4.50 1.50 3.00 3.00 4.50 1.50 1.50 3.00 4.50 4.50 1.50 3.00 61.5 65.9 58.1 7.76 0.50 1.00 1.50 1.50 0.50 1.00 1.00 1.50 0.50 1.00 1.50 0.50 1.50 0.50 1.00 0.50 1.00 1.50 61.7 59.6 65.2 5.62 6.00 6.50 7.00 7.00 6.00 6.50 7.00 6.00 6.50 6.00 6.50 7.00 6.50 7.00 6.00 6.50 7.00 6.00 61.7 63.4 60.4 2.99
表4 正交试验结果方差分析
Table 4 Variance analysis of orthogonal experiments results
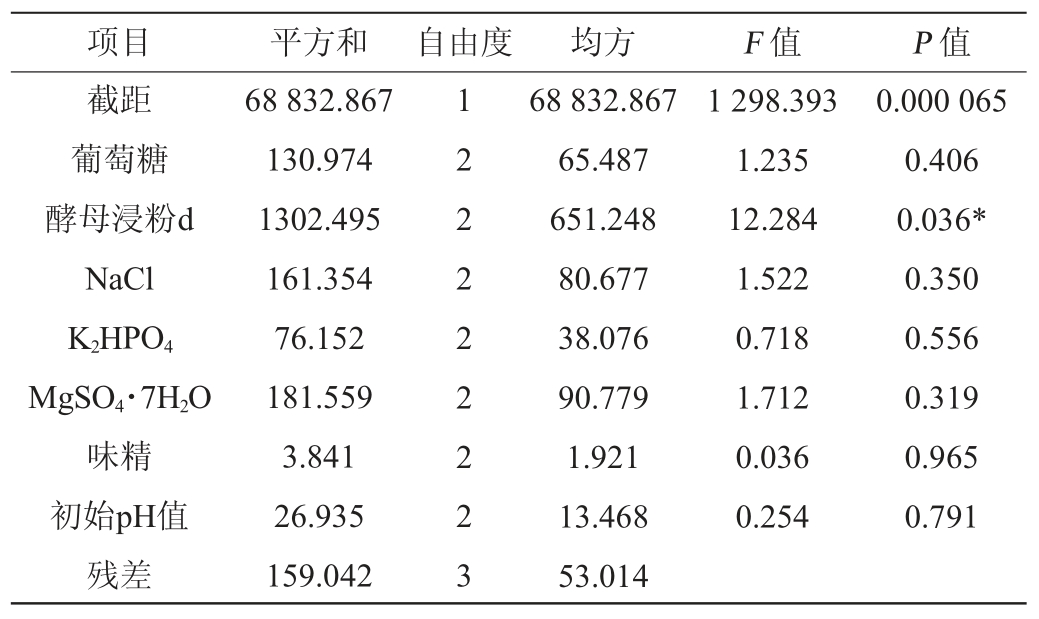
注:“*”表示对结果影响显著(P<0.05)。
项目平方和 自由度均方F 值P 值截距葡萄糖酵母浸粉d NaCl K2HPO4 MgSO4·7H2O味精初始pH值残差68 832.867 130.974 1302.495 161.354 76.152 181.559 3.841 26.935 159.042 1 2 2 2 2 2 2 2 3 68 832.867 65.487 651.248 80.677 38.076 90.779 1.921 13.468 53.014 1 298.393 1.235 12.284 1.522 0.718 1.712 0.036 0.254 0.000 065 0.406 0.036*0.350 0.556 0.319 0.965 0.791
由表4可知,酵母浸粉d对普鲁兰多糖的产量具有显著影响(P<0.05),其余各因素对普鲁兰多糖的产量影响不显著(P>0.05)。各因素对结果影响顺序为酵母浸粉d>MgSO4·7H2O>NaCl>葡萄糖>味精>K2HPO4>初始pH值。
2.3.2 人工神经网络建模寻优
以正交试验结果为基础,选择葡萄糖(A)、酵母浸粉d(B)、NaCl(C)、K2HPO4(D)、MgSO4·7H2O(E)、味精(F)和初始pH值(G)这7个因素为人工神经网络的输入层,普鲁兰多糖产量为输出层,使用反向传播算法进行训练,通过训练集与验证集对模型可靠性进行验证,使用标准遗传算法对ANN模型进行迭代进化,结果见图8。 由图8a可知,当隐含层的个数为8时,BP神经网络的误差最小,因此确定人工神经网络模型的结构为7-8-1。由图8b可知,当训练轮数在第40轮时,模型的均方误差满足设定目标。由图8c和8d可知,训练集和测试集的ANN 拟合曲线的相关系数R2分别为0.999 9和0.994 3,均>0.99,证明此模型可靠,可用于进行最佳发酵条件的预测。由图8e可知,设置最大迭代次数为200次,以使该模型可以寻找最优解。标准遗传算法最优解在遗传迭代到达第80代左右被找到,普鲁兰多糖产量预测值为109.00g/L。由图8f可知,经人工神经网络标准算法优化后得出最佳发酵条件为葡萄糖174.50 g/L,酵母浸粉d 7.96 g/L,MgSO4·7H2O 1.64 g/L,K2HPO4 5.08 g/L,NaCl 6.39 g/L,味精0.53 g/L,初始pH值为6.08。在此优化条件下进行3次平行验证试验,普鲁兰多糖产量为(87.50±2.40)g/L,重均分子质量为1.26±105 Da,生物量为30.75 g/L。 与优化前基础发酵培养基相比,普鲁兰多糖的产量显著提高了57.10%(P<0.05),重均分子质量显著提高了约30.8%(P<0.05),生物量提高了7.52%。
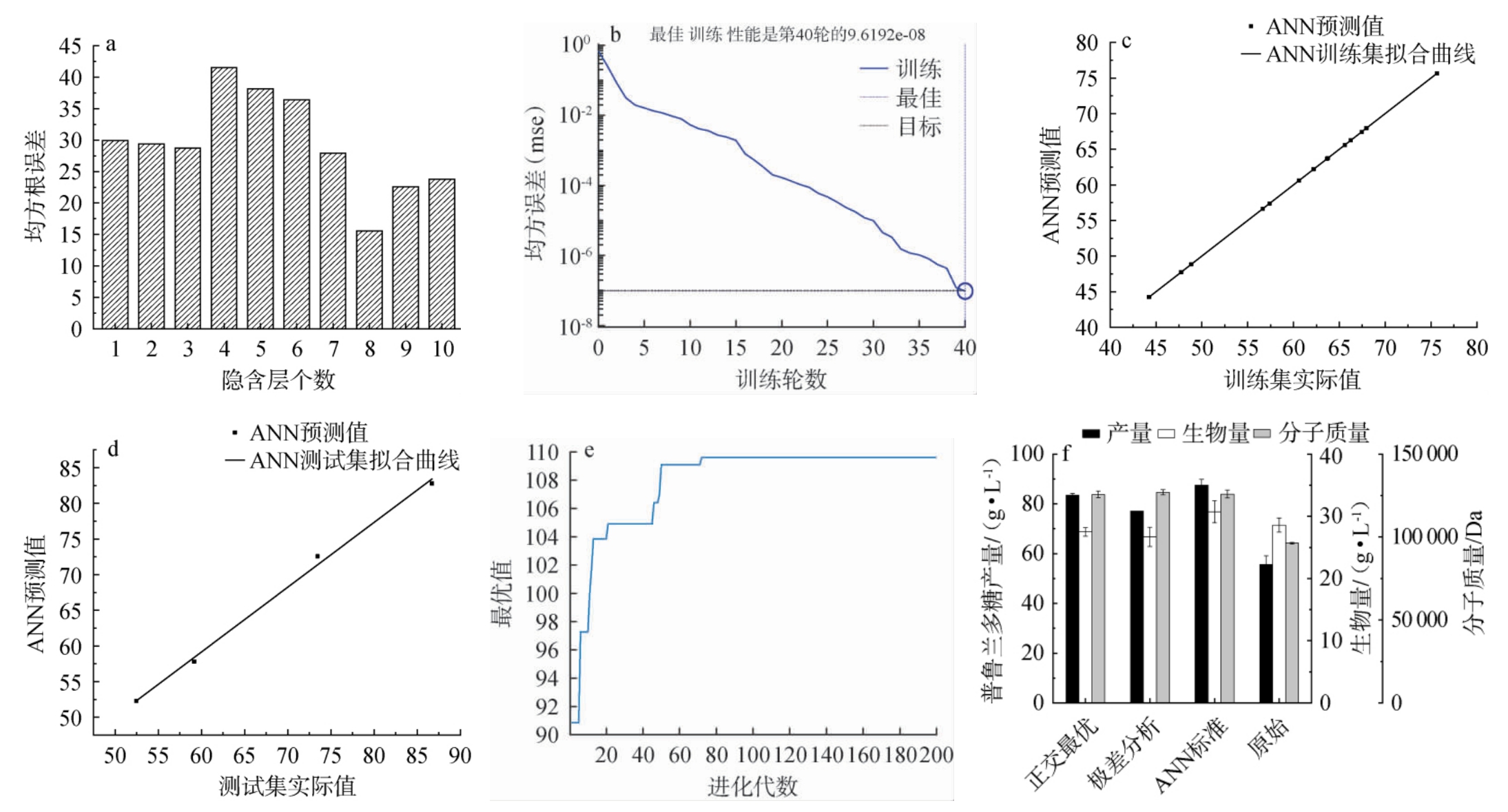
图8 基于正交试验结果的人工神经网络优化发酵条件
Fig. 8 Optimization of fermentation conditions by artificial neural network based on orthogonal experiment results
人工神经网络已被广泛应于各种发酵条件优化的建模和预测。 结果显示,普鲁兰产量预测值和真实值的相对误差为24.57%。表明模型可能存在一定程度的过拟合现象,而使用更多的数据进行模型训练,将可能继续增加模型的预测准确性。近年来,小样本机器学习已被广大的研究者们所关注[40],随着机器学习技术的不断更新迭代,将会使得在有限的数据条件下,获得鲁棒性更好的预测模型。
3 结论
本研究以出芽短梗霉(Aureobsidium pullulans)(保藏号CGMCCNO.7055)为出发菌株,通过紫外诱变后得到一株高产普鲁兰多糖的稳定菌株UV013,利用正交试验偶联人工神经网络分析,进行发酵条件优化,得到最优发酵条件为葡萄糖174.50 g/L,酵母浸粉d 7.96 g/L,MgSO4·7H2O 1.64 g/L,K2HPO4 5.08 g/L,NaCl 6.39 g/L,味精0.53 g/L,初始pH值为6.08。 在此优化条件下,普鲁兰多糖产量为(87.50±2.40)g/L,重均分子质量为1.26×105 Da,生物量为30.75 g/L。与优化前基础发酵培养基相比,普鲁兰多糖产量显著提高了57.10%(P<0.05),重均分子质量显著提高了约30.80%(P<0.05),生物量提高了7.52%。本研究成果对普鲁兰多糖的产业化生产和应用具有重要意义。
[1] LI Y, CHI Z, WANG G Y, et al. Taxonomy of Aureobasidium spp. and biosynthesis and regulation of their extracellular polymers[J] . Crit Rev Microbiol,2015,41(2):228-237.
[2] SHAO P,NIU B,CHEN H,et al.Fabrication and characterization of tea polyphenols loaded pullulan-CMC electrospun nanofiber for fruit preservation[J] .Int J Biol Macromol,2018,107:1908-1914.
[3] MARIABERCEA,BERNHARDA.Intrinsic viscosities of polymer blends:Sensitive probes of specific interactions between the counterions of polyelectrolytes and uncharged macromolecules[J] . Macromolecules, 2018,51(19):7483-7490.
[4] ZHANG S,WEI F,HAN X J.An edible film of sodium alginate/pullulan incorporated with capsaicin[J] .New J Chem,2018,42(21):17756-17761.
[5] GUERRERO J,OLIVEIRA H,CATROS S,et al.The use of total human bone marrow fraction in a direct three-dimensional expansion approach for bone tissue engineering applications:Focus on angiogenesis and osteogenesis[J] .Tissue Eng Part A,2015,21(5/6):861-874.
[6] CHEN S Y,ZHENG H C,GAO J Q,et al.High-level production of pullulan and its biosynthesis regulation in Aureobasidium pullulans BL06[J] .Front Bioeng Biotechnol,2023,11:1131875.
[7] BAI R X,CHEN J L,HAO Y Q,et al.ARTP mutagenesis of Aureobasidium pullulans RM1603 for high pullulan production and transcriptome analysis of mutants[J] .Arch Microbiol,2024,206(9):375.
[8] 李淼鑫,马正旺,赵晓雯,等. 基于代谢组学研究不同通风比对普鲁兰多糖发酵的影响[J] .食品与发酵工业,2025,51(12):259-268.
[9] CRUZ-SANTOS M M,ANTUNES F A F,ARRUDA G L,et al.Production and applications of pullulan from lignocellulosic biomass:Challenges and perspectives[J] .Bioresource Technol,2023,385:129460.
[10] XIA Z Q,WU S J,PAN S K.Effect of two-stage controlled pH and temperature on pullulan production by Auerobasidium pullulans[J] .Carbohydr Polym,2011,86(4):1814-1816.
[11] MUJDECI G N,BOZDEMIR M T,OZBAS Z Y.Experimental modeling and optimization of pullulan production by Aureobasidium pullulans AZ-6[J] .Polymer Bulletin,2024,81(10):9139-9180.
[12] CHEN S W,LI W M,ZHAO X W,et al.Application of explainable machine learning in the production of pullulan by Aureobasidium pullulans CGMCCNO.7055[J] .Int J Biol Macromol,2025,308(2):142374.
[13] SAHU N,MAHANTY B,HALDAR D.Response surface methodology and artificial neural network based media optimization for pullulan production in Aureobasidium pullulans[J] .Int J Biol Macromol,2024,284(P1):138045.
[14] CHEN S,ZHAO T,LI M,et al.Efficient production of pullulan by Aureobasidium pullulans using a multi-objective optimization strategy with orthogonal experimental design coupling artificial neural network and genetic algorithm[J] .Int J Biol Macromol,2024,280(P1):135588.
[15] VARDIAMBASIS I O,KAPETANAKIS T N, NIKOLOPOULOS C D,et al.Hydrochars as emerging biofuels:Recent advances and application of artificial neural networks for the prediction of heating values[J] .Energies,2020,13(17):4572.
[16] 王单单,白淑贤,陈雪平,等.基于正交试验设计结合BP神经网络优选银丹活血通瘀胶囊提取工艺[J] .中国现代中药,2025,27(2):318-327.
[17] 陈世伟,罗嘉伟,王舸楠,等.基于遗传算法进化的人工神经网络(GAANN)对葡萄糖发酵生产普鲁兰多糖的条件优化[J] . 食品与发酵工业,2023,49(8):60-66.
[18] PENG W,SADAGHIANI O K.Enhancement of quality and quantity of woody biomass produced in forests using machine learning algorithms[J] .Biomass Bioenergy,2023,175:106884.
[19] HE C Y,ZHANG Z,ZHANG Y D,et al.Efficient pullulan production by Aureobasidium pullulans using cost-effective substrates[J] . Int J Biol Macromol,2021,186:544-553.
[20] 张攀. 维生素B5对出芽短梗霉发酵产普鲁兰多糖分子量及产量影响的研究[D] .天津:天津科技大学,2021.
[21] SUGUMARAN K R,SINDHU R V,SUKANYA S,et al.Statistical studies on high molecular weight pullulan production in solid state fermentation using jack fruit seed[J] .Carbohydr Polym,2013,98(1):854-860.
[22] GUO J, LI J, CHEN Y, et al. Improving erythritol production of Aureobasidium pullulans from xylose by mutagenesis and medium optimization[J] .Appl Biochem Biotech,2016,180(4):717-727.
[23] ZHANG S,FENG Z,ZENG Q,et al.Enhancing pullulan production in Aureobasidium pullulans through UV mutagenesis breeding and highthroughput screening system[J] .Fermentation,2024,10(2):103.
[24] JIANG L F, WU S J, KIM J M. Effect of different nitrogen sources on activities of UDPG-pyrophosphorylase involved in pullulan synthesis and pullulan production by Aureobasidium pullulans[J] . Carbohydr Polym,2011,86(2):1085-1088.
[25] LIN Y,ZHANG Z,THIBAULT J.Aureobasidium pullulans batch cultivations based on a factorial design for improving the production and molecular weight of exopolysaccharides[J] .Process Biochem,2007,42(5):820-827.
[26] 安超,马赛箭,常帆,等. 酵母粉对出芽短梗霉发酵普鲁兰多糖相对分子质量的影响[J] .食品与生物技术学报,2018,37(1):76-81.
[27] SHENG L,ZHU G,TONG Q.Comparative proteomic analysis of Aureobasidium pullulans in the presence of high and low levels of nitrogen source[J] .J Agr Food Chem,2014,62(43):10529-10534.
[28] LI X W,ZHAO S Z,CHEN L L,et al.High-level production of pullulan from high concentration of glucose by mutagenesis and adaptive laboratory evolution of Aureobasidium pullulans[J] .Carbohydr Polym,2023,302:120426.
[29] DUAN X,CHI Z,WANG L,et al.Influence of different sugars on pullulan production and activities of α-phosphoglucose mutase,UDPG-pyrophosphorylase and glucosyltransferase involved in pullulan synthesis in Aureobasidium pullulans Y68[J] . Carbohydr Polym, 2008, 73(4):587-593.
[30] VAN DEN EYNDE K,BOON V,GASPAR R C,et al.Biofabrication of functional pullulan by Aureobasidium pullulans under the effect of varying mineral salts and sugar stress conditions[J] .Molecules,2023,28(6):2478.
[31] 张攀,张伊凡,成刚刚,等. 基于代谢组学分析MgSO4·7H2O和K2HPO4协同对普鲁兰多糖生物合成的影响[J] .食品科技,2021,46(4):1-8.
[32] GAO W,KIM Y J,CHUNG C H,et al.Optimization of mineral salts in medium for enhanced production of pullulan by Aureobasidium pullulans HP-2001 using an orthogonal array method[J] .Biotechnol Bioproc Eng,2010,15(5):837-845.
[33] YU X L,WANG Y,WEI G,et al.Media optimization for elevated molecular weight and mass production of pigment-free pullulan[J] .Carbohydr Polym,2012,89(3):928-934.
[34] WANG D H,NI T F,JU X M,et al.Sodium chloride improves pullulan production by Aureobasidium pullulans but reduces the molecular weight of pullulan[J] .Appl Microbiol Biotechnol,2018,102(20):8921-8930.
[35] 余小六.普鲁兰生物合成及其高产策略研究[D] .苏州:苏州大学,2013.
[36] 罗嘉伟.氮源对出芽短梗霉合成普鲁兰多糖的影响[D] .天津:天津科技大学,2024.
[37] LEE K Y,YOO Y J.Optimization of pH for high molecular weight pullulan[J] .Biotechnol Lett,1993,15(10):1021-1024.
[38] PAN S,YAO D,CHEN J,et al.Influence of controlled pH on the activity of UDPG-pyrophosphorylase in Aureobasidium pullulans[J] .Carbohydr Polym,2013,92(1):629-632.
[39] BADR-ELDIN S M, EL-TAYEB O M, EL-MASRY H G, et al. Polysaccharide production by Aureobasidium pullulans:factors affecting polysaccharide formation[J] .World J Microb Biot,1994,10(4):423-426.
[40] HOLLMANN N, MÜLLER S, PURUCKER L, et al. Accurate predictions on small data with a tabular foundation model[J] . Nature, 2025,637(8045):319-326.