酿酒葡萄和葡萄酒中一类关键呈色物质是花色苷类,是葡萄与葡萄酒丰富色泽的来源[1]。花色苷是花色素与糖以糖苷键结合而成的一类化合物,因其单体形式很不稳定,容易受到光照、水分、温度等环境因素的影响而发生分解,进而影响其含量和组分的改变[2];花色苷是类黄酮—以黄酮核为基础的一类物质中能呈现红色的一族化合物,是一种水溶性色素[3]。由于其独特的功能性,而被应用于清除体内自由基、增殖叶黄素、抗肿瘤、抗癌、抗炎[4]、抑制脂质过氧化和血小板凝集、预防糖尿病、减肥、保护视力等。花色苷的甲基化、糖基化和酰基化等修饰作用影响其稳定性[5-6]。而酰基化修饰花色苷因其稳定性使其赋予葡萄酒更浓郁的色泽[7]。 从葡萄转色期开始,花青素在葡萄的表皮中积累;它们主要以飞燕草素、矢车菊素、天竺葵素等的葡萄糖苷衍生物存在[8]。而在酿酒葡萄中的花色苷主要包括花青素、甲基花青素、花翠素、二甲花翠素以及甲基花翠素[9]。 它们的种类与含量共同塑造了葡萄及葡萄酒最终的色泽特征。
颜色不稳定是新疆葡萄酒普遍存在的问题,而花色苷的稳定性直接决定了酒体的色泽表现。花青素的稳定性受到多种因子的影响,这既与品种自身的遗传特性有关,也与外界环境(如光照、栽培管理等)有关[10]。已有研究表明,光是调控花青素生物合成的重要环境因素之一,而光照强度与葡萄果实着色程度密切相关[11-12]。 为解决新疆葡萄酒颜色不稳定的问题,目前普遍采用遮阴网、摘叶疏穗和铺反光膜等方法,旨在直接改善花色苷的积累与合成[13-14]。譬如在葡萄栽培中使用遮阴网不仅可以调节葡萄的成熟期,还能显著影响果实糖酸比和大小等基本指标[15-16]。 此外,遮阴处理也可以通过抑制果实不同成熟期的光合作用,进而影响花色苷的合成和代谢[17]。这些研究为提升新疆葡萄酒的颜色稳定性奠定了重要的理论基础,并提供了切实可行的技术路线。
新疆地区昼夜温差大,光照时间长、强度高,是影响葡萄果实花色苷合成的重要环境因子。目前,关于马瑟兰葡萄在不同采收期花色苷的积累规律,以及遮阴处理对其含量与组分的影响尚不明确。 本研究以马瑟兰葡萄为材料,在果实5%转色至完全成熟期间,采用不同遮光率的遮阴网进行遮阴处理,采用超高效液相色谱-串联质谱技术(ultra high performance liquid chromatography-tandem mass spectrometry,UPLC-MS/MS)测定花色苷组分与含量,并结合正交偏最小二乘-判别分析(orthogonal partial least squares discriminant analysis,OPLS-DA)解析不同遮阴处理葡萄和葡萄酒花色苷积累与组成差异,旨在改善马瑟兰葡萄和葡萄酒花色苷含量及种类,从而提升葡萄酒的色泽稳定性。
1 材料与方法
1.1 材料与试剂
马瑟兰(Marselan)酿酒葡萄,于2017年定植于新疆焉耆县七个星镇乡都酒庄种植基地(北纬42°2′23″,东经86°16′17″),长势良好、大小均匀的马瑟兰。树龄8年,南北行向,间距5.0 m×1.0 m。架势为单蔓篱架搭配“厂”字形,树势基本一致,采取滴灌方式浇灌。该地区属于中温带干旱大陆气候,四季明显,日照充足,昼夜温差15 ℃,土壤为砂质壤土。海拔约1 087 m。 该地无霜期长达180 d,非常适合酿酒葡萄的生长。采摘时综合考虑阴阳面和果穗的上、中、下部进行取样。
黑色单层遮阳网(规格为25 m×10 m,网1遮光率为20%,网2遮光率为50%):市售;甲酸(色谱纯):美国Sigma-Aldrich公司;甲醇(色谱纯):德国Merck公司;盐酸(分析纯):信阳市化学试剂厂;纯净水:杭州娃哈哈集团有限公司;去离子水:Milli-Q超纯水系统;花色苷标准品(纯度均>99%):法国Extrasynthese公司;果胶酶(500 U/mg):上海源叶生物科技有限公司;F33酵母:法国Laffort公司;偏重亚硫酸钾(分析纯):上海麦克林生化技术有限公司。
1.2 仪器与设备
OSA-WXNY106小型气象站:河北隆运电子科技有限公司;MM400型球磨仪:德国Retsch公司;QTRAP 6500+UPLC-MS/MS:美国SCIEX公司;PAL-1手持式糖度计:广州速为电子科技有限公司;pH-10便携式pH计:上海浦春计量仪器有限公司;5424R型离心机:德国Eppendorf公司;CAT-1自动电位滴定仪:德国ChenTron公司。
1.3 方法
1.3.1 遮阴处理
本试验所用的马瑟兰酿酒葡萄果实糖度均达到24~26°Brix。 设置3种处理:Q1为5%转色-完全成熟期间采用遮阳网1(20%遮光率)遮阴处理;Q2为5%转色-完全成熟期间采用遮阳网2(50%遮光率)遮阴处理;以正常生长未遮阴处理葡萄果实为对照(CK);在5%转色-完全成熟期间第7、14、21、28天取样。每个处理均设3个重复,实验在2025年7、8月进行。
1.3.2 气象数据收集
试验期间使用OSA-WXNY106小型气象站监测Q1、Q2二种遮阴处理与对照CK之间的气象数据,每30 min采集一次数据。
1.3.3 葡萄酒的酿造
葡萄采收后剔除叶片、霉烂及生青果,除梗破碎置于5 L酿酒玻璃罐(装填体积约为80%),果实破碎30%后加偏重亚硫酸钾50 mg/L、1 h后加入果胶酶40 mg/L、搅拌均匀后在10 ℃低温条件下浸渍24 h后,待回温到20~25 ℃时添加200 mg/L F33酵母进行发酵。每天早中晚压帽3次,同时测定温度和比重,当比重达到0.996时酒精发酵结束,皮渣分离后启动苹乳发酵,苹乳发酵结束后,将葡萄酒与酒泥分离,在恒温12~15 ℃的酒窖中陈酿6个月。在酒精发酵结束后取50 mL酒样置于-20 ℃冰箱内保存,剩余酒样置于8~12 ℃条件下瓶储。
1.3.4 葡萄和葡萄酒理化指标检测
百粒质量:使用分析天平测定;总可溶性固形物(total soluble solid,TTS)含量:采用手持糖度仪测定;总酸含量(以酒石酸计):采用自动电位滴定仪测定;pH值:使用便携式pH计测定;还原糖含量:根据GB 5009.7—2016《食品中还原糖的测定》中的直接滴定法测定;总酚含量:采用福林酚法[18]测定;总单宁含量:采用磷钼酸-磷钨酸比色法[19]测定;总花色苷含量:采用pH示差法[19]测定;挥发酸、酒精度的含量:采用Foss全自动葡萄酒分析仪;游离SO2、总SO2的含量:采用GB/T 15038—2006《葡萄酒、果酒通用分析方法》的方法。
1.3.5 葡萄皮和葡萄酒单体花色苷含量的测定
葡萄皮和葡萄酒单体花色苷含量的测定:采用UPLCMS/MS法[20-21],略有改动。
葡萄皮预处理:在液氮中快速剥离后研磨成粉,再经冷冻干燥机冻干备用。 在50 mL离心管中加入2 mL提取液(甲酸∶甲醇=2∶98,V/V)和0.100 g葡萄果皮干粉,20 ℃避光超声10 min,25 ℃避光振荡30 min,在4 ℃条件下以8 000 r/min转速离心10 min,收集上清液,重复4次提取,合并4次提取收集的上清液,使用旋转蒸发仪蒸发至干,然后甲醇定容至2 mL,用于UPLC-MS/MS分析。
葡萄酒预处理:吸取50 μL的葡萄酒样品,溶解于950μL提取液(体积分数为50%甲醇溶液,含0.1%盐酸)中;涡旋5 min,超声5 min,离心3 min(12 000 r/min,4 ℃),吸取上清,用微孔滤膜(0.22 μm)过滤样品,并保存于进样瓶中,用于UPLC-MS/MS分析。
UPLC条件:采用ACQUITY BEH C18色谱柱(100 mm×2.1 mm×1.7 μm)进行分离,保持柱温为40 ℃,用含有0.5%甲酸水作为流动相A,用含有0.5%甲酸的甲醇作为流动相B。 梯度洗脱过程如下:0~6 min,B相由5%升至50%;6~12 min,B相升至95%并保持2 min;14~16 min,B相降到5%并平衡2 min。流速为0.35 mL/min,进样量为2 μL。
MS条件:利用电喷雾离子源(electrospray ionization,ESI)正离子模式对样品进行质谱分析。设置离子源温度为550 ℃,离子化电压为5 500 V,气帘气(curtain gas,CUR)压力为35 psi。利用优化后的去簇电压(declustering potential,DP)与碰撞能量(collision energy,CE)扫描各待测离子对。
1.3.6 数据处理
数据整理与计算使用Excel 2021;数据进行显著性分析使用IBM SPSS Statistics 27.0;图形绘制采用Origin 2021软件;通过数据分析网站Metware Cloud(https://cloud.metware.cn.)进行正交偏最小二乘-判别分析(OPLS-DA)。
2 结果与分析
2.1 遮阴处理对果际微气候的影响
以正常生长未遮阴处理葡萄为对照(CK),遮阴处理对果际微气候的影响结果见图1。 由图1可知,各处理间的平均温湿度差异不明显。由图1A可知,随着采收期的推移,遮阴网1和遮阴网2均降低了温度,5%转色-完全成熟期第10天CK组温度达到最高值(31.4 ℃),而同一天Q1和Q2处理的平均温度分别为29.3 ℃和30.8 ℃;由图1B可知,5%转色-完全成熟期第14天时三个处理的相对湿度达到最大值,分别为79.9%、78.5%和77.6%,总体来说,整个时期各处理之间平均温度和相对湿度无明显差异。
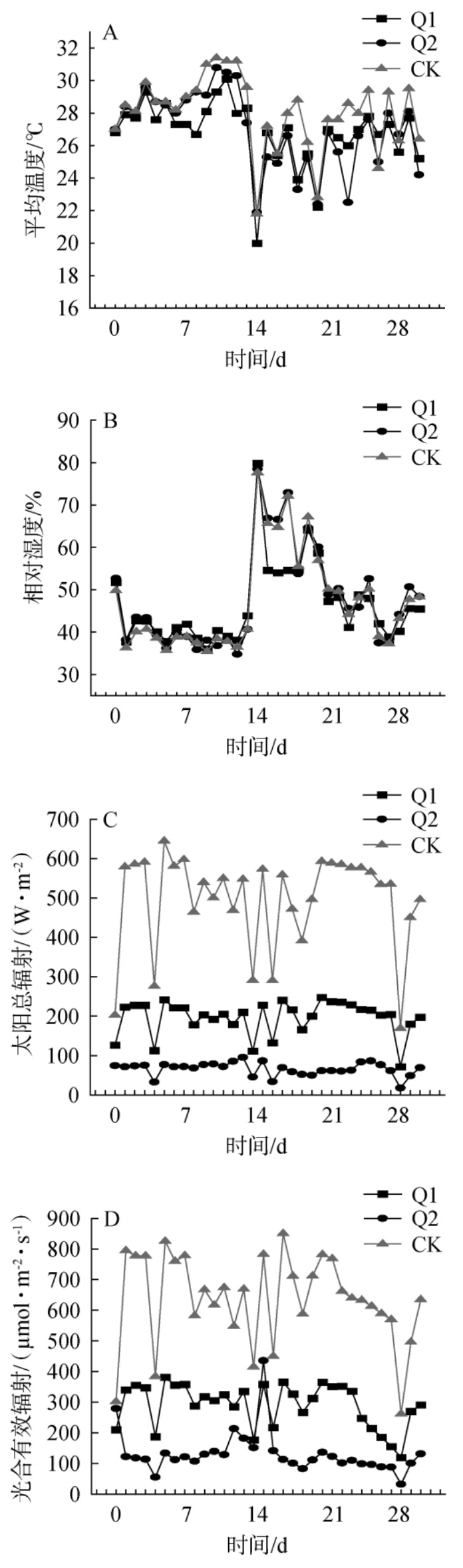
图1 遮阴处理对果际微气候的影响
Fig. 1 Effect of shading treatments on the microclimate of fruit
由图1C可知,CK组太阳总辐射在5%转色-完全成熟期第6天时达到峰值,为645.1 W/m2,较Q1和Q2处理组分别增加了1.67倍和7.38倍,说明遮阴处理能够显著影响太阳总辐射;由图1D可知,CK组光合有效辐射在5%转色-完全成熟期第18天时达到峰值,为851 μmol/(m2·s),分别比Q1和Q2处理组显著增加了1.33倍和6.54倍(P<0.05)。 与CK相比,Q1、Q2两种遮阴处理均使葡萄穗周围的光合有效辐射及总辐射显著下降(P<0.05)。结果表明,遮阴处理能有效地减弱光照强度,但对果际微环境的温湿度影响不大。 这与史红军等[22-23]研究结果一致。
2.2 遮阴处理对不同采收期马瑟兰葡萄和葡萄酒基理化指标的影响
以正常生长未遮阴处理葡萄为对照(CK),遮阴处理对不同采收期马瑟兰葡萄和葡萄酒基本理化指标的影响结果分别见表1和表2。由表1可知,遮阴处理对不同采收时期马瑟兰葡萄果实品质均有显著影响。百粒质量随时间推移逐渐增加。在采收期第7天时Q1处理的百粒质量为72.99 g,第28天时百粒质量升至85.56 g,增加了17.2%;Q2处理的葡萄采收期第7~28天,百粒质量从74.39 g增至90.15 g,增幅达21.1%,且在各时期均显著高于Q1与CK(P<0.05)。遮阴处理对不同采收期葡萄的pH值无显著的影响;而遮阴处理不同采收期葡萄TSS和还原糖含量显著上升(P<0.05),其中CK葡萄TSS和还原糖含量在采收期第28天时达到最高值,分别为25.7°Brix、243.85 mg/L,显著高于Q1与Q2处理组(P<0.05)。总酸随果实发育逐渐下降,Q2处理在5%转色-完全成熟期第7天总酸含量最高(16.28 g/L)。 而CK葡萄5%转色-完全成熟期第28天时总酸含量最低(7.92g/L),显著低于同一时期的Q1(8.90 g/L)与Q2(10.22 g/L)处理组(P<0.05)。糖酸比及总酚含量随采收期显著上升,而总单宁含量随着采收期下降。采收期第28天时,CK组糖酸比为30.79,显著高于Q1与Q2处理(P<0.05),Q1处理葡萄总酚含量(3.82 mg/g)达到峰值,显著高于其他处理组(P<0.05);CK组总单宁含量为0.62 mg/g,显著低于Q1(0.71 mg/g)和Q2(0.68 mg/g)处理组(P<0.05);遮阴处理下葡萄总花色苷含量随着采收时间呈先升后降的趋势,Q1和Q2处理葡萄在采收期第14天时总花色苷含量最高,分别为12.33 mg/g和10.24 mg/g,相较CK 组(8.54 mg/g)分别显著增加了44.24%和19.88%(P<0.05)。综上,遮阴处理可以有效降低马瑟兰葡萄的TSS和还原糖含量,提高总酸含量,对百粒质量、pH值无显著影响。这与GU W等[24-25]得出的结论一致。
表1 遮阴处理对不同采收期马瑟兰葡萄果实基础理化指标的影响
Table 1 Effect of shading treatments on basic physicochemical indexes of Marselan grape fruits at different harvest periods
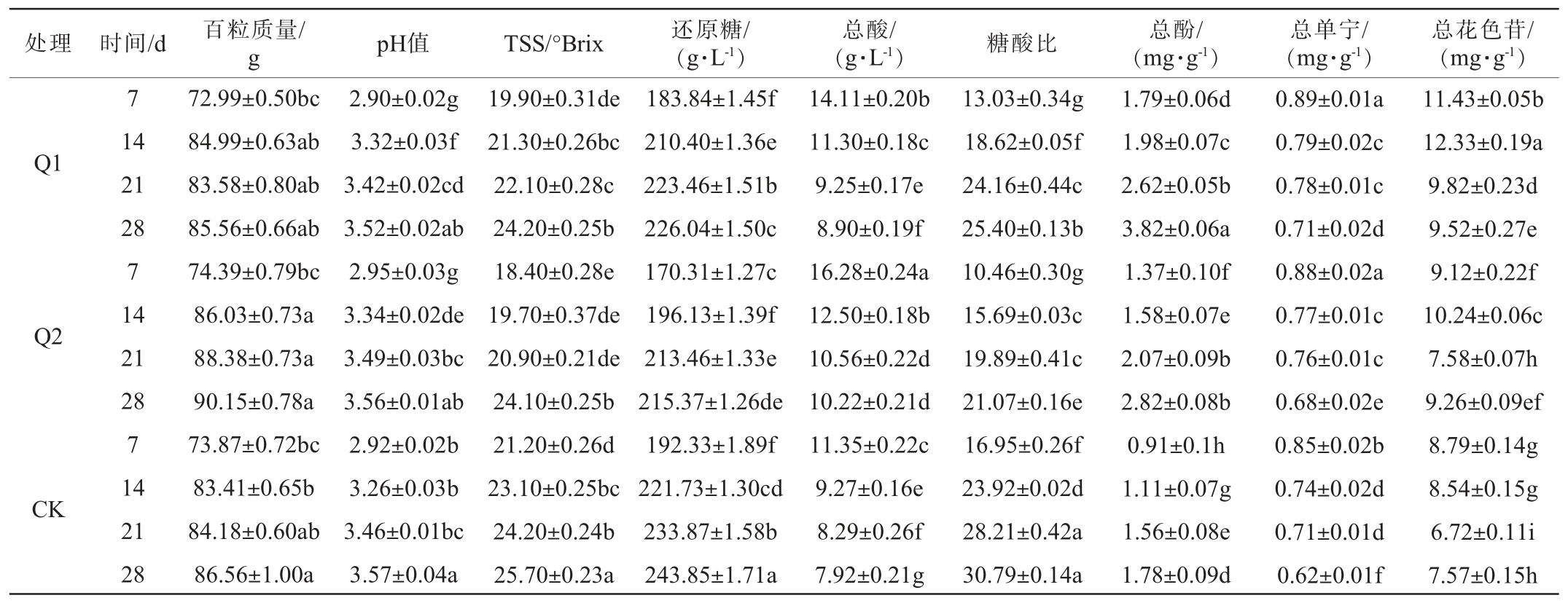
注:同列不同小写字母表示差异显著(P<0.05)。下同。
处理 时间/d 百粒质量/g pH值TSS/°Brix还原糖/(g·L-1)(g·L-1)糖酸比总酚/(mg·g-1)总酸/总单宁/(mg·g-1)总花色苷/(mg·g-1)7 Q1 Q2 CK 14 21 28 7 14 21 28 7 14 21 28 72.99±0.50bc 84.99±0.63ab 83.58±0.80ab 85.56±0.66ab 74.39±0.79bc 86.03±0.73a 88.38±0.73a 90.15±0.78a 73.87±0.72bc 83.41±0.65b 84.18±0.60ab 86.56±1.00a 2.90±0.02g 3.32±0.03f 3.42±0.02cd 3.52±0.02ab 2.95±0.03g 3.34±0.02de 3.49±0.03bc 3.56±0.01ab 2.92±0.02b 3.26±0.03b 3.46±0.01bc 3.57±0.04a 19.90±0.31de 21.30±0.26bc 22.10±0.28c 24.20±0.25b 18.40±0.28e 19.70±0.37de 20.90±0.21de 24.10±0.25b 21.20±0.26d 23.10±0.25bc 24.20±0.24b 25.70±0.23a 183.84±1.45f 210.40±1.36e 223.46±1.51b 226.04±1.50c 170.31±1.27c 196.13±1.39f 213.46±1.33e 215.37±1.26de 192.33±1.89f 221.73±1.30cd 233.87±1.58b 243.85±1.71a 14.11±0.20b 11.30±0.18c 9.25±0.17e 8.90±0.19f 16.28±0.24a 12.50±0.18b 10.56±0.22d 10.22±0.21d 11.35±0.22c 9.27±0.16e 8.29±0.26f 7.92±0.21g 13.03±0.34g 18.62±0.05f 24.16±0.44c 25.40±0.13b 10.46±0.30g 15.69±0.03c 19.89±0.41c 21.07±0.16e 16.95±0.26f 23.92±0.02d 28.21±0.42a 30.79±0.14a 1.79±0.06d 1.98±0.07c 2.62±0.05b 3.82±0.06a 1.37±0.10f 1.58±0.07e 2.07±0.09b 2.82±0.08b 0.91±0.1h 1.11±0.07g 1.56±0.08e 1.78±0.09d 0.89±0.01a 0.79±0.02c 0.78±0.01c 0.71±0.02d 0.88±0.02a 0.77±0.01c 0.76±0.01c 0.68±0.02e 0.85±0.02b 0.74±0.02d 0.71±0.01d 0.62±0.01f 11.43±0.05b 12.33±0.19a 9.82±0.23d 9.52±0.27e 9.12±0.22f 10.24±0.06c 7.58±0.07h 9.26±0.09ef 8.79±0.14g 8.54±0.15g 6.72±0.11i 7.57±0.15h
表2 遮阴处理对不同采收期马瑟兰葡萄酿造葡萄酒基本理化指标的影响
Table 2 Effect of shading treatments on basic physicochemical indexes of wine brewed by Marselan grape at different harvest periods
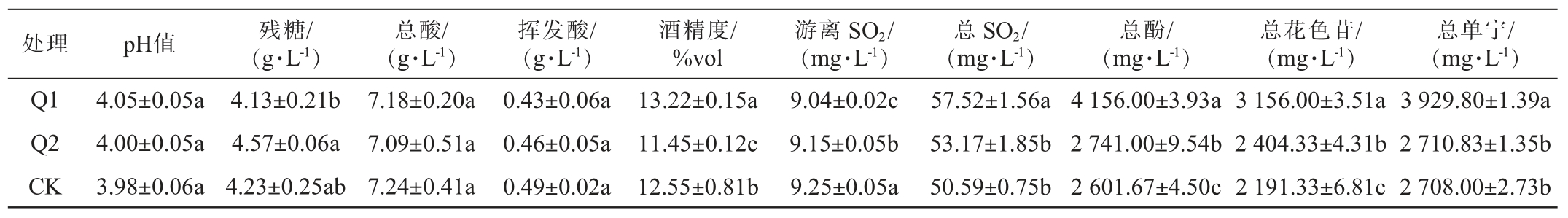
处理pH值残糖/(g·L-1)总酸/(g·L-1)挥发酸/(g·L-1)酒精度/%vol游离SO2/(mg·L-1)总SO2/(mg·L-1)总酚/(mg·L-1)总花色苷/(mg·L-1)总单宁/(mg·L-1)Q1 Q2 CK 4.05±0.05a 4.00±0.05a 3.98±0.06a 4.13±0.21b 4.57±0.06a 4.23±0.25ab 7.18±0.20a 7.09±0.51a 7.24±0.41a 0.43±0.06a 0.46±0.05a 0.49±0.02a 13.22±0.15a 11.45±0.12c 12.55±0.81b 9.04±0.02c 9.15±0.05b 9.25±0.05a 57.52±1.56a 53.17±1.85b 50.59±0.75b 4 156.00±3.93a 2 741.00±9.54b 2 601.67±4.50c 3 156.00±3.51a 2 404.33±4.31b 2 191.33±6.81c 3 929.80±1.39a 2 710.83±1.35b 2 708.00±2.73b
由表2可知,各处理葡萄酿造葡萄酒指标均符合国标GB/T 15037—2006《葡萄酒》中的要求。各处理葡萄酒之间的pH值、总酸和挥发酸含量差异不显著;残糖量Q2>CK>Q1,Q1处理葡萄酿造葡萄酒残糖量最低(4.13 g/L),参照GB/T 15037—2006《葡萄酒》中残糖含量在4.1~12.0 g/L,属于半干型葡萄酒。说明Q1处理葡萄发酵最为彻底,消耗了更多的糖分; 不同处理葡萄酿造葡萄酒的酒精度大小为Q1>CK>Q2,三者之间酒精度存在显著差异(P<0.05)。不同处理葡萄酿造葡萄酒游离SO2和总SO2含量有差异,其中Q1处理葡萄酿造葡萄酒游离SO2和总SO2含量最高,分别为9.25 mg/L和57.52 mg/L,推断其原因为pH直接决定了二氧化硫的比例,pH越低,二氧化硫更易以H2SO3形式存在,而Q1处理葡萄酿造葡萄酒pH最高,所以游离态的二氧化硫比例下降,总二氧化硫含量提升[26]。总酚、总单宁和总花色苷含量变化趋势一致,Q1葡萄酿造葡萄酒中总酚、总单宁和总花色苷含量最高,分别为4 156.00 mg/L、3 929.80 mg/L和3 156.00 mg/L。 从理化指标结果来看,Q1处理葡萄酿造葡萄酒品质最好。
2.3 遮阴处理对不同采收期马瑟兰葡萄果皮和葡萄酒中甲基化、未甲基化花色苷的影响
甲基化可以增加花色苷分子的疏水性,减少其在水溶液中的溶解度,从而降低其对光、热和pH值变化的敏感性[27]。 以正常生长未遮阴处理葡萄为对照(CK),遮阴处理对不同采收期马瑟兰葡萄果皮和葡萄酒中甲基化、未甲基化花色苷的影响结果见图2。
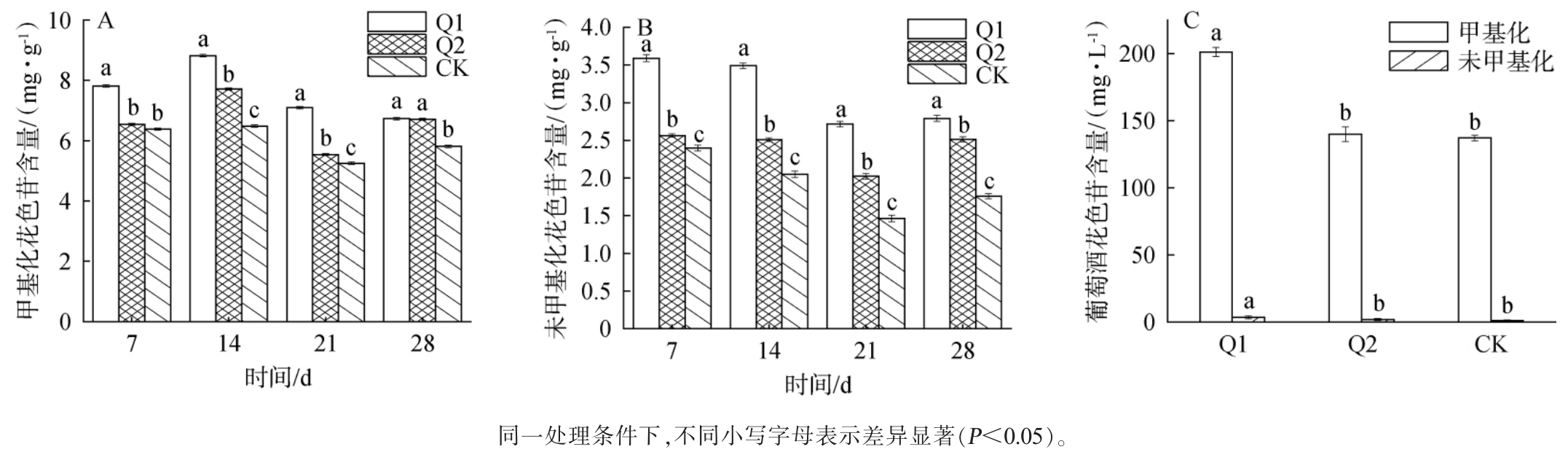
图2 遮阴处理对马瑟兰葡萄果皮(A,B)和葡萄酒(C)中甲基化、未甲基化花色苷含量的影响
Fig. 2 Effect of shading treatment on the contents of methylated and unmethylated anthocyanins in Marselan grape pericarp (A,B) and wine (C)
由图2A可知,甲基化花色苷含量在采收期总体上呈先升高后下降的趋势。 Q1和Q2处理葡萄果皮中甲基化花色苷含量均高于对照,Q1处理葡萄果皮中甲基化花色苷含量呈先上升后下降的趋势,Q2处理及CK葡萄果皮中甲基化花色苷含量呈先上升后下降再上升的趋势。在葡萄采收期第14天时,Q1和Q2处理葡萄果皮中甲基化花色苷含量最高,分别为8.818 mg/g、7.714 mg/g,相较CK组分别显著增加了36.19%、19.14%(P<0.05)。由图2B可知,随着采收时间的推移,未甲基化花色苷含量整体呈现下降的趋势,在葡萄采收期第7~14天时,Q1、Q2处理及CK葡萄果皮中未甲基化花色苷含量变化量分别为3.590~3.489 mg/g、2.565~2.508 mg/g、2.398~2.049 mg/g。 在葡萄采收期第28天时,Q1、Q2处理及CK葡萄果皮中未甲基化花色苷含量分别为2.792 mg/g、2.512 mg/g和1.759 mg/g,相比CK,Q1和Q2处理组含量分别增加58.73%和42.87%。 这与ZHANG Z等[28]研究结果相似。 由图2C可知,甲基化花色苷是马瑟兰葡萄酒中的主要花色苷,Q1处理葡萄酒中的甲基化花色苷的含量(201.212 mg/L)显著高于Q2处理(139.988 mg/L)和CK组(137.144 mg/L)(P<0.05),比CK提升了46.72%。不同处理马瑟兰葡萄酒中未甲基化花色苷含量很低,为0.999~3.498 mg/L。 综上,适当的遮阴处理会增加马瑟兰葡萄和葡萄酒中甲基化花色苷的含量,采用Q1处理的遮阴网可以使葡萄果皮和葡萄酒中累积更多甲基化花色苷。
2.4 遮阴处理对不同采收期马瑟兰葡萄果皮和葡萄酒中酰化、未酰化花色苷含量的影响
酰基化不仅可以影响花色苷的物理化学性质,如溶解性、稳定性等,还可能会增强或减弱花色苷的抗氧化能力,这对于食品工业和医药领域具有重要意义[29]。以正常生长未遮阴处理葡萄为对照(CK),遮阴处理对不同采收期马瑟兰葡萄果皮和葡萄酒中酰化、未酰化花色苷含量的影响见图3。
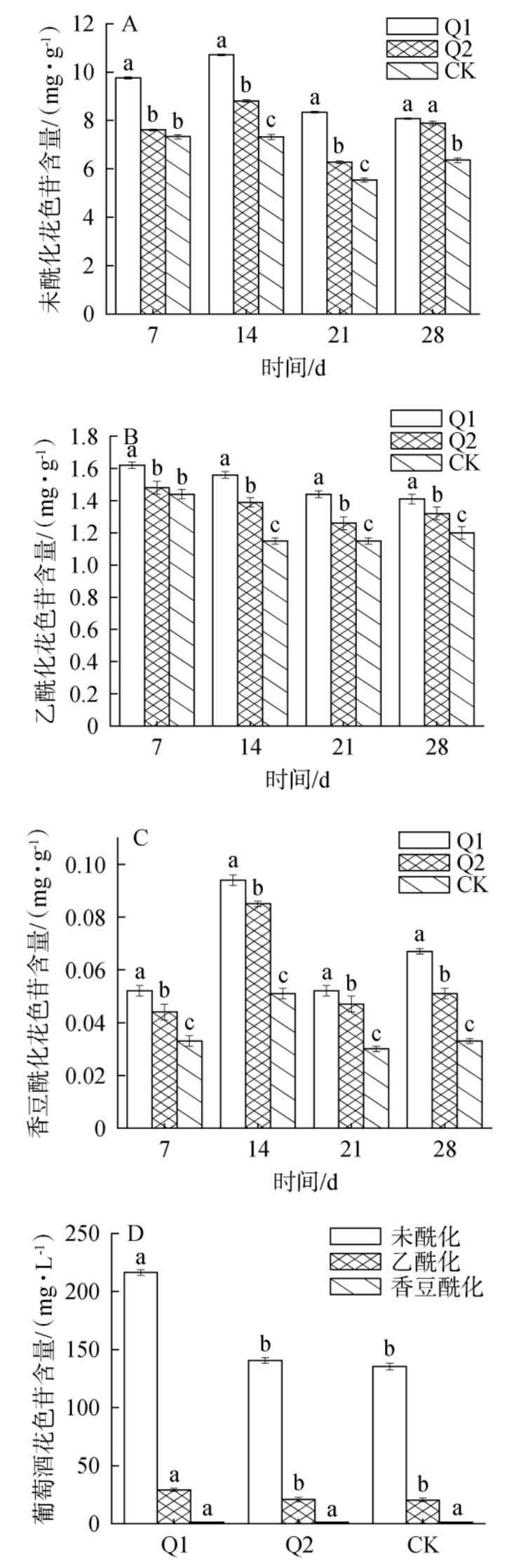
图3 遮阴处理对马瑟兰葡萄果皮(A,B,C)和葡萄酒(D)中酰化、未酰化花色苷含量的影响
Fig. 3 Effect of shading treatments on the contents of acylated and non-acylated anthocyanin in Marselan grape pericarp (A,B,C)and wine (D)
由图3A可知,Q1和Q2处理葡萄果皮中未酰化花色苷含量均高于对照,Q1处理葡萄果皮中未酰化花色苷含量呈先上升后下降的趋势,Q2处理及CK葡萄果皮中未酰化花色苷含量呈先上升后下降再上升的趋势。采收期第14天时,Q1和Q2处理葡萄果皮中未酰化花色苷含量最高,分别为10.711 mg/g、8.813 mg/g,均显著高于CK(7.315 mg/g)(P<0.05)。这与付东艳等[13]研究结果基本一致。由图3B可知,葡萄果皮中乙酰化花色苷含量因遮阴处理和采收期的不同而有差异。 采收期第7天时,Q1、Q2处理葡萄果皮中乙酰化花色苷含量最高,分别为1.618 mg/g、1.476 mg/g,显著高于CK乙酰化花色苷含量(1.439 mg/g)(P<0.05)。 由图3C可知,第14天时,Q1、Q2处理葡萄果皮中香豆酰化花色苷含量最高,分别为0.094 mg/g、0.085 mg/g,显著高于CK香豆酰化花色苷含量(0.051 mg/g)(P<0.05)。这与王舒伟[30]的研究结果一致。由图3D可知,葡萄酒中香豆酰化花色苷含量Q1、Q2和CK分别为1.383 mg/L、1.281 mg/L和1.353 mg/L,无显著差异。Q1处理葡萄酒的未酰化和乙酰化花色苷的含量分别为216.482 mg/L、29.219 mg/L,均显著高于CK(P<0.05)。综上,Q1处理能使葡萄果皮和葡萄酒中积累更多的酰基化花色苷,这对新疆焉耆地区的马瑟兰葡萄酒颜色的稳定性具有重大意义。
2.5 基于花色苷组分的正交偏最小二乘-判别分析
以正常生长未遮阴处理葡萄为对照(CK),基于单体花色苷组分的正交偏最小二乘-判别分析、置换检验结果及变量重要性投影(variable important in the projection,VIP)值见图4。 由图4A可知,整个采收期不同遮阴处理葡萄皮单体花色苷OPLS-DA,X轴和Y轴分别解释了样本间14.9%和32.8%的变异,是区分样本的主要维度。 不同遮阴处理和不同采收期之间完全分开,没有重叠,组内紧凑聚集于各自椭圆内,表明重复性良好,说明不同处理之间的单体花色苷存在显著差异,通过OPLS-DA可以有效区分不同遮阴处理和不同采收期的葡萄。由图4B可知,因变量解释指数R2Y=0.971、预测能力Q2=0.921,表明模型具有较好的解释能力和预测能力。经200次置换检验,Q2回归线与纵轴的相交点小于0,表明模型不存在过拟合,模型验证有效。 由图4C可知,整个采收期葡萄果皮中共筛选出19种差异花色苷组分(VIP>1),分别为锦葵色素-3-O阿拉伯糖苷、锦葵色素-3-O-(6''-O-乙酰)鼠李糖苷、锦葵色素-咖啡酰-对香豆酰-乙酰-木糖苷-木糖苷、矢车菊素-3-芥子酰-鼠李糖苷、锦葵色素-3-O-(6''-O-乙酰)半乳糖苷、矢车菊素-3-O-槐糖苷、锦葵色素-3-O-(6''-O-对香豆酰)木糖苷、锦葵色素-3-O-(6''-O-乙酰)葡萄糖苷、芍药花素-3-O-槐糖苷、飞燕草素-3-O-葡萄糖苷-5-O-半乳糖苷、飞燕草素-3,5-O-二葡萄糖苷、芍药花素-3-O-阿拉伯糖苷、矮牵牛素-3,5-O-二葡萄糖苷、飞燕草素-3-O-阿拉伯糖苷、矢车菊素-3-O-木糖苷、锦葵色素-3-O-半乳糖苷、锦葵色素-3,5-O-二葡萄糖苷、矢车菊素-3-O-阿拉伯糖苷-葡萄糖苷、锦葵色素-3-O-葡萄糖苷。
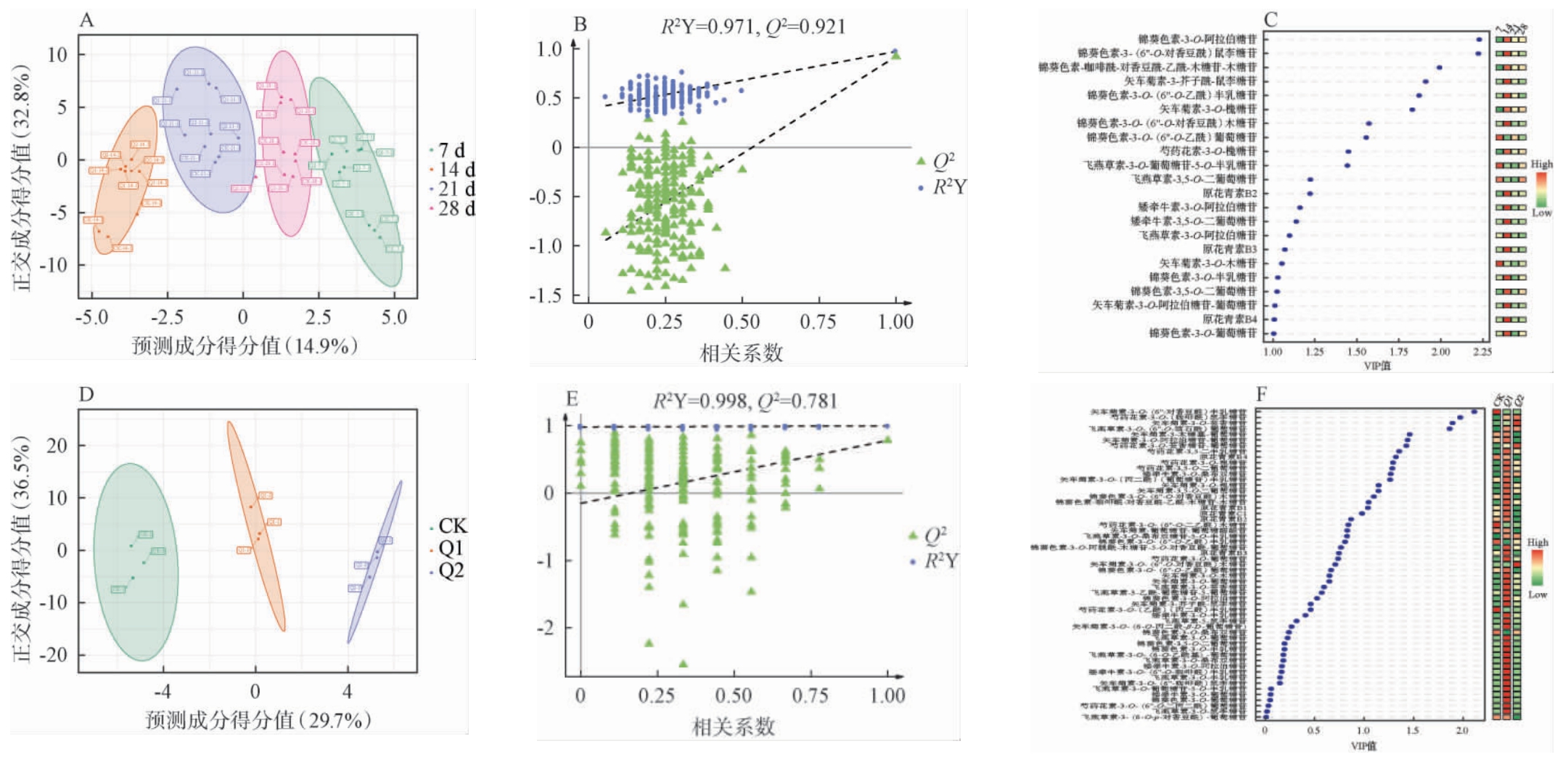
图4 遮阴处理马瑟兰葡萄果皮(A、B、C)和葡萄酒(C、D、F)花色苷组分正交偏最小二乘-判别分析、200次置换检验结果及变量重要性投影值
Fig. 4 Orthogonal partial least squares-discriminant analysis, 200 permutation test results and variable important in the projection values of anthocyanin components in Marselan grape pericarp (A, B, C) and wine (C, D, F) with different shading treatments
由图4D可知,CK与Q1、Q2遮阴处理组在OPLS-DA得分图中呈现明显分离,表明遮阴处理显著改变了葡萄酒中花色苷的组成与含量。 其中,Q2处理样本集中分布于X轴正半轴区域,进一步说明该遮阴条件对花色苷类代谢产物谱具有显著调控作用。通过OPLS-DA可以有效区分不同遮阴处理和不同采收期葡萄酿造的葡萄酒。由图4E可知,因变量解释指数R2Y=0.998、预测能力Q2=0.781,表明模型具有较好的解释能力和预测能力。经200次置换检验,Q2回归线与纵轴的相交点小于0,表明模型不存在过拟合,模型验证有效。由图4F可知,不同遮阴处理葡萄酿造葡萄酒中共筛选出16种差异花色苷组分(VIP>1),分别为矢车菊素-3-O-(6''-对香豆酰)半乳糖苷、芍药花素-3-O-(咖啡酰)鼠李糖苷、矢车菊素-3-O-芸香糖苷、飞燕草素-3-O-(6''-O-酒石酰)葡萄糖苷、矢车菊素-3-木糖基-葡萄糖苷、矢车菊素-3-O-阿拉伯糖苷-葡萄糖苷、芍药花素-3-O-芸香糖苷-葡萄糖苷、芍药花素-3,5-二半乳糖苷、芍药花素-3-O-槐糖苷、芍药花素-3,5-O-二葡萄糖苷、矮牵牛素-3-O-桑布双糖苷、矢车菊素-3-O-(丙二酰)(葡萄糖苷)半乳糖苷、矢车菊素-3-O-槐糖苷、矢车菊素-3,5-O-二葡萄糖苷、锦葵色素-3-O-(6''-O-对香豆酰)木糖苷、锦葵色素-咖啡酰-对香豆酰-乙酰-木糖苷-木糖苷。
2.6 遮阴处理对不同采收期马瑟兰葡萄果皮和葡萄酒中
主要花色苷含量的影响
遮阴处理对不同采收期马瑟兰葡萄果皮和葡萄酒中主要花色苷含量的影响结果分别见表3和表4。
表3 遮阴处理对不同采收期马瑟兰葡萄果皮中主要花色苷组分含量的影响
Table 3 Effect of shading treatment on the main anthocyanin components contents in Marselan grape pericarp at different harvest periods mg/g
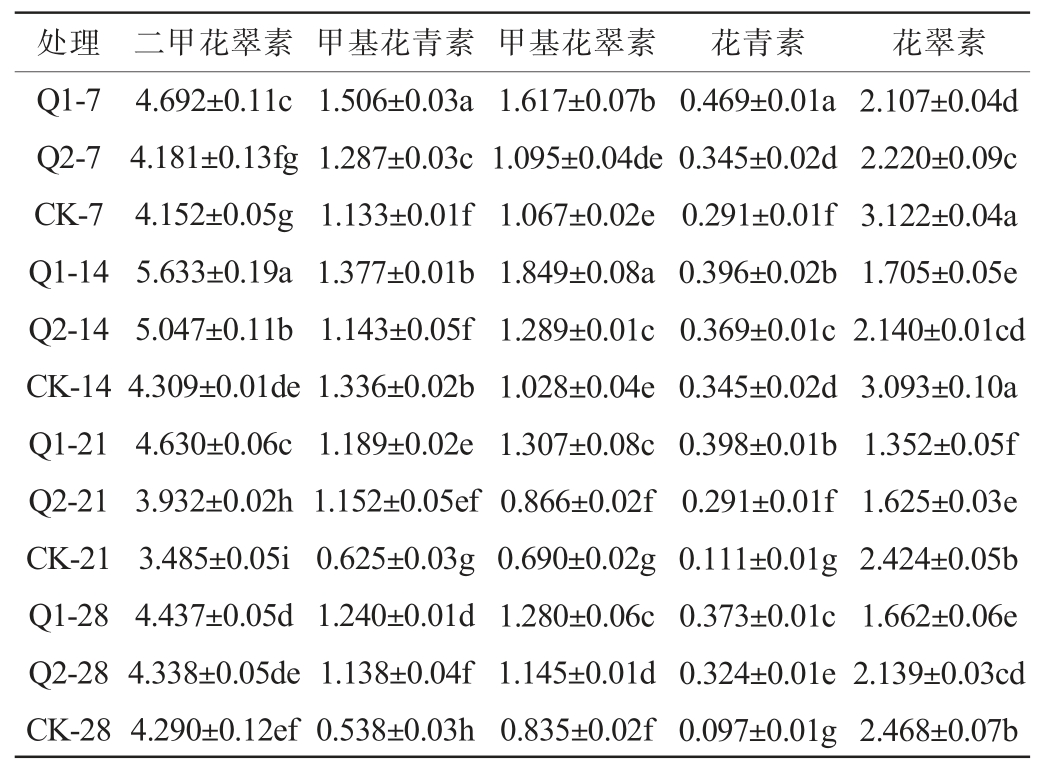
处理 二甲花翠素 甲基花青素 甲基花翠素花青素花翠素Q1-7 Q2-7 CK-7 Q1-14 Q2-14 CK-14 Q1-21 Q2-21 CK-21 Q1-28 Q2-28 CK-28 4.692±0.11c 4.181±0.13fg 4.152±0.05g 5.633±0.19a 5.047±0.11b 4.309±0.01de 4.630±0.06c 3.932±0.02h 3.485±0.05i 4.437±0.05d 4.338±0.05de 4.290±0.12ef 1.506±0.03a 1.287±0.03c 1.133±0.01f 1.377±0.01b 1.143±0.05f 1.336±0.02b 1.189±0.02e 1.152±0.05ef 0.625±0.03g 1.240±0.01d 1.138±0.04f 0.538±0.03h 1.617±0.07b 1.095±0.04de 1.067±0.02e 1.849±0.08a 1.289±0.01c 1.028±0.04e 1.307±0.08c 0.866±0.02f 0.690±0.02g 1.280±0.06c 1.145±0.01d 0.835±0.02f 0.469±0.01a 0.345±0.02d 0.291±0.01f 0.396±0.02b 0.369±0.01c 0.345±0.02d 0.398±0.01b 0.291±0.01f 0.111±0.01g 0.373±0.01c 0.324±0.01e 0.097±0.01g 2.107±0.04d 2.220±0.09c 3.122±0.04a 1.705±0.05e 2.140±0.01cd 3.093±0.10a 1.352±0.05f 1.625±0.03e 2.424±0.05b 1.662±0.06e 2.139±0.03cd 2.468±0.07b
表4 遮阴处理对马瑟兰葡萄酒中主要花色苷组分含量的影响
Table 4 Effect of shading treatment on the main anthocyanin components contents in Marselan wine mg/L

处理 二甲花翠素 甲基花青素 甲基花翠素花青素花翠素Q1 Q2 CK 2.953±1.03a 1.382±0.79ab 0.678±0.40b 17.779±3.44a 10.396±3.45b 6.393±2.73b 41.857±4.44a 20.291±4.18b 18.197±8.89b 48.420±3.83a 28.602±2.37b 27.665±8.12b 135.013±3.17a 100.991±5.02b 103.087±1.44b
由表3可知,Q1和Q2处理均增加了二甲花翠素、甲基花翠素和花青素含量,Q1处理在采收期第14天时葡萄果皮中二甲花翠素和甲基花翠素含量最高,分别为5.633 mg/g和1.849 mg/g,相比同一时期CK组增加了30.73%和79.86%;采收期第21天时CK葡萄果皮中二甲花翠素和甲基花翠素含量是最低的,分别为3.485 mg/g和0.690 mg/g;Q1处理在采收期第7天时甲基花青素和花青素含量最高,分别为1.506 mg/g、0.469 mg/g,相比同一时期的CK组增加了32.92%和61.17%,而在采收期第28天时,CK组的甲基花青素和花青素含量最低。结果表明,Q1和Q2处理降低了葡萄果皮花翠素含量,增加了葡萄果皮二甲花翠素和甲基花翠素含量。
由表4可知,Q1处理马瑟兰葡萄酒中5种主要花色苷组分含量均为最高,这表明Q1处理对提升这些主要花色苷组分含量具有显著的效果。花翠素的含量是葡萄酒花色苷组分中最高的,分别为Q1(135.013 mg/L)、Q2(100.991 mg/L),CK组(103.087mg/L)。Q1相较对照组含量增加了30.97%。二甲花翠素的含量最低,分别为Q1(2.953mg/L)、Q2(1.382 mg/L),CK组(0.678 mg/L)。Q1相较对照组含量增加了3.36倍。
结果表明,Q1处理能最有效提高葡萄果皮及葡萄酒中花色苷含量。
3 结论
该研究以新疆焉耆产区马瑟兰葡萄为试材,通过测定葡萄和葡萄酒基本理化指标,利用超高效液相色谱串联质谱分析(UPLC-MS/MS)测定葡萄及葡萄酒花色苷类物质含量和组分并对其进行OPLS-DA分析。 结果表明,遮阴处理可以有效降低马瑟兰葡萄的可溶性固形物和还原糖含量,提高总酸含量,对百粒质量、pH值无显著影响。Q1处理葡萄酒品质最佳,总酚、总单宁和总花色苷含量最高,分别为4 156.00 mg/L、3 929.80 mg/L和3 156.00 mg/L。Q1处理葡萄果酒的甲基化花色苷的含量(201.212 mg/L)显著高于Q2处理(139.988 mg/L)和CK组(137.144 mg/L)(P<0.05);Q1处理葡萄酒的未酰化和乙酰化花色苷的含量分别为216.482 mg/L、29.219 mg/L,均显著高于CK(P<0.05),并提高了葡萄果皮和葡萄酒中主要花色苷含量。通过正交偏最小二乘-判别分析(OPLS-DA)可以有效区分CK及Q1、Q2处理葡萄和葡萄酒,整个采收期葡萄及其酿造葡萄酒中分别共筛选出19种、16种差异花色苷组分(VIP>1)。 本研究结果为新疆焉耆葡萄酒产区优化栽培管理、提升葡萄酒色泽品质提供了重要的理论依据与实践指导。
[1] TIAN M B, LIU Y, LU H C, et al. Cluster spatial positions varied the phenolics profiles of 'Cabernet Sauvignon'grapes and wines under a fan training system with multiple trunks[J] .Food Chem,2022,387:132930.
[2] LU H C, TIAN M B, HAN X, et al. The key role of vineyard parcel in shaping flavonoid profiles and color characteristics of Cabernet Sauvignon wines combined with the influence of harvest ripeness,vintage and bottle aging[J] .Food Chem X,2023,19:100772.
[3] 夏玲,陈小兰,王自超,等. 吡喃花色苷结构、稳定性及功能活性研究进展[J/OL] .食品与发酵工业,1-13[2025-12-03] .https://doi.org/10.13995/j.cnki.11-1802/ts.043555.
[4] WU Y, HAN T, LYU L, et al. Research progress in understanding the biosynthesis and regulation of plant anthocyanins[J] .Sci Hortic,2023,321:112374.
[5] 夏玲,陈小兰,王自超,等. 酰基化花色苷的结构、稳定性及降血糖作用研究进展[J] .食品与发酵工业,2025,51(15):374-383.
[6] LI B,WANG L,BAI W, et al. Modification and Stabilization of Anthocyanins[M] .Singapore:Springer Nature Singapore,2022:115-140.
[7] 王政.刺葡萄花色苷酶促酰化反应条件的优化及光稳定性研究[D] .长沙:湖南农业大学,2021.
[8] 张欣珂,赵旭,刘沛通,等. 红葡萄酒的花色苷:来源、呈色与反应[J] .食品科学,2023,44(23):342-352.
[9] REN R,SHI J,ZENG M,et al.Inter-and intra-varietal genetic variations co-shape the polyphenol profiles of Vitis vinifera L.grapes and wines[J] .Food Chem X,2023,20:101030.
[10] SHI N,ZHAO Y F,LU H C,et al.Flavoromics analysis and sensory evaluation of wines produced from nine red grape cultivars in Manas region,Xinjiang,China:Implications for terroir adaptation[J] .Food Chem,2025,490:145096.
[11] 任婷婷,张廷秀,战良,等.不同光质补光对设施栽培‘阳光玫瑰’葡萄果实品质的影响[J] .园艺学报,2025,52(9):2464-2476.
[12] 宁琳,李文超,杨彭程,等.贺兰山东麓不同风土条件下霞多丽葡萄果实和葡萄酒酚类物质特征分析[J] .果树学报,2025,42(9):2043-2056.
[13] 付东艳,汪蕾,张龙生. 遮阳对马瑟兰葡萄花色苷组分及合成相关基因表达的影响[J] .果树学报,2025,42(1):30-47.
[14] REYNOLDS A G.Viticultural and vineyard management practices and their effects on grape and wine quality[J] .Manag Wine Qual,2010,490:365-444.
[15] 盘丰平,韦荣福,吴代东,等.基于广泛靶向代谢组学的半遮阴处理腺枝葡萄果实差异代谢物解析[J] .中外葡萄与葡萄酒,2024(4):6-13.
[16] 宫小敏,虞光辉,李秀杰,等. 不同光质对避雨栽培阳光玫瑰葡萄光合特性及果实品质的影响[J] .果树学报,2025,42(4):790-801.
[17] 张珍珍,李倩,董荣,等. 树体遮光对采收期‘赤霞珠’葡萄果实花色苷类物质积累的影响[J] .食品科学,2020,41(4):157-163.
[18] 徐洪宇,张京芳,成冰,等.26种酿酒葡萄中抗氧化物质含量测定及品种分类[J] .中国食品学报,2016,16(2):233-241.
[19] 张旭东,万卓吾,付东艳,等. 栽培措施对宁夏贺兰山东麓美乐果实着色的影响[J] .中国酿造,2025,44(8):230-235.
[20] 翟亚巍,蔡军社,户金鸽,等.不同成熟度酿酒葡萄对干红葡萄酒品质的影响[J] .食品研究与开发,2024,45(15):25-31,99.
[21] 李磊,谷威杰,苏旺春,等.遮阳网颜色和宽度对‘马瑟兰’葡萄果实和葡萄酒品质的影响[J] .西北植物学报,2024,44(9):1355-1364.
[22] 史红军,李京宝,宋文静,等.3种园林树木对光环境变化的适应性研究[J] .山东林业科技,2025,55(6):25-30.
[23] LU H C,TIAN M B,SHI N,et al.Volatilomics of Cabernet Sauvignon grapes and sensory perception of wines are affected by canopy side in vineyards with different row orientations[J] . Food Chem, 2024, 460:140508.
[24] GU W,CHEN L,LI H,et al.Enhancing wine grape quality in hot climate viticulture regions:The role of shading net coverage and light transmittance[J] .J Agr Food Res,2025,24:102468.
[25] 翟亚巍. 吐鲁番3个品种不同成熟度酿酒葡萄对葡萄酒品质的影响[D] .乌鲁木齐:新疆农业大学,2024.
[26] ASHMORE P L,VALDEZ F,HARBERTSON J F,et al.Rapid determination of free sulfur dioxide in wine and cider by capillary electrophoresis[J] .J Chromatogr A,2023,1695:463936.
[27] LU Z,WANG X,LIN X,et al.Plant anthocyanins:Classification,biosynthesis,regulation,bioactivity,and health benefits[J] .Plant Physiol Biochem,2024,217:109268.
[28] ZHANG Z,HU Y,ZHANG Y,et al.Effects of combined application of abscisic acid and methyl jasmonate on the regulation of anthocyanin and monoterpene biosynthesis in'Jumeigui'grape[J] .Hortic Plant J,2025.
[29] 王政. 刺葡萄花色苷酶促酰化反应条件的优化及光稳定性研究[D] .长沙:湖南农业大学,2021.
[30] 王舒伟.葡萄采收成熟度对葡萄酒色泽品质和陈酿稳定性的影响研究[D] .乌鲁木齐:新疆农业大学,2022.