面对现代技术的飞跃,白酒企业纷纷积极转变发展思路,以机械化、自动化和智能化替代传统手工酿造工艺,并以数字化、智能化作为强大引擎,加速推动白酒产业实现智能化升级[1]。现代技术多以自动化和精细的过程控制,在提高生产效率和保障产品一致性方面发挥了重要作用,而传统酿造技术重经验、手工,强调风味文化,在市场上因其独特性具有竞争力[2]。馥郁香型白酒作为中国十二大香型白酒之一,拥有“前浓、中清、后酱”独特的口感[3]。酒鬼酒作为馥郁香型白酒的典型代表,在传承传统生产技艺的基础上,其智能化酿造的转型也在紧跟时代科技进步的步伐,积极推进中[4]。
馥郁香型白酒酿造过程中,培菌糖化作为重要工艺环节之一,是以小曲为糖化发酵剂,将高粱、大米、玉米等多粮组合的熟料在开放环境中培养富集有益微生物生长繁殖的培菌过程,为淀粉转化为糖、糖转化为酒精提供必要的微生物和丰富的酶系,其工艺效果影响白酒的出酒率和基酒品质[5-6]。目前,馥郁香型白酒糖化料的制作在保留手工生产的基础上,推进机械形式的集中糖化生产。手工糖化为人工操作清蒸与润拌,糖化箱箱体设计直接与地面接触;机械集中糖化使用高压蒸锅、恒温糖化箱等设备,通过设定压力、温度、网带速度等参数实现工艺流程的控制[3,7]。杨再懿等[3]从入箱温度、原料厚度、糖化箱箱温层面对恒温糖化箱培菌糖化的工艺条件进行了探索,研究表明在入箱温度28 ℃、原料厚度26 cm、糖化箱箱温28 ℃的条件下获得的糖化物料在感官、基酒出酒率及优级品率方面均高于同期生产车间平均值,为后续优化馥郁香型白酒酿造机械化和自动化生产的工艺参数提供了基础数据支撑。而微生物作为白酒发酵动力源[8],糖化料中堆积培养的微生物是泥窖粮醅发酵的主要菌源之一[4],其微生物差异会影响酒醅初始菌群的形成并改变风味,故而群落结构解析对维持酒醅正常发酵尤为重要[9]。
因此,本研究基于微生物传统培养方法和高通量测序技术,以手工班组敞开糖化和机械班组集中糖化两种方式生产的馥郁香型白酒糖化料为研究对象,探究两种糖化物料间微生物数量和群落结构的差异,并对其感官、理化指标进行检测分析,初步揭示其理化与微生物间的相关性,以期助力馥郁香型白酒糖化料微生态的调控生产实践,并为优化培菌糖化不同方式生产管理提供微生物群落层面的理论参考。
1 材料与方法
1.1 材料与试剂
1.1.1 样品
糖化料样品:取自酒鬼酒工厂手工、机械糖化车间。
1.1.2 试剂
氨苄青霉素:上海麦克林生化科技股份有限公司;酚酞:天津市众联化学试剂有限公司;氢氧化钠:重庆川东化工集团有限公司;葡萄糖:成都金山化学试剂有限公司;盐酸:茂名市雄大化工有限公司;次甲基蓝:天津市科密欧化学试剂有限公司;五水硫酸铜、酒石酸钾钠、氯化钠:国药集团化学试剂有限公司;Hipure Soil脱氧核糖核酸(deoxyribonucleic acid,DNA)Kit:广州美基生物科技有限公司;QubitR dsDNA HS Assay Kit:南京诺唯赞生物科技股份有限公司;2×Hieff CanaceR AdvanceFast聚合酶链式反应(polymerase chain reaction,PCR)Master Mix:翌圣生物科技(上海)股份有限公司。以上试剂均为分析纯或生化试剂。
1.1.3 培养基
马铃薯葡萄糖琼脂(potato dextrose agar,PDA)培养基、酵母浸出粉胨葡萄糖(yeast peptone dextrose,YPD)培养基、MRS培养基、营养琼脂(nutrient agar,NA)培养基、LB培养基:杭州微生物试剂有限公司。
1.2 仪器与设备
BKQ-B75II立式压力蒸汽灭菌器:山东博科消毒设备有限公司;HCB-1300V洁净工作台:青岛海尔生物医疗股份有限公司;SYG-A2-4电热恒温水浴锅、WHL-125L电热恒温干燥箱、SPX-150L生化培养箱:天津市泰斯特仪器有限公司;MP2002电子天平:上海舜宇恒平科学仪器有限公司;拓尔为T-105温度计:深圳市拓尔为电子科技有限公司;5430R冷冻高速离心机:德国艾本德股份公司;Fluo-800荧光剂:杭州奥盛仪器有限公司;ETC811基因扩增仪:苏州东胜兴业科学仪器有限公司。
1.3 方法
1.3.1 糖化料样品的采集及温度的测定
随机抽取同一批次糖化结束后的手工班组和机械班组的糖化料,共抽取3批次,手工班组(Y)抽取的糖化料编号依次为Y1、Y2、Y3,机械班组(S)抽取的糖化料编号依次为S1、S2、S3,共计糖化料样品6个。每个样品采用五点取样法(即从糖化箱的四角距边50 cm及中心处五点)采集,每点采样时包含上、中、下层糖化料(剔除上层谷壳等异物),充分混匀,一分为三,一份用于高通量测序分析,一份用于可培养微生物计数,一份用于理化分析。采样的同时,将温度计插入糖化箱测定温度,糖化料采样点及温度测定点见图1。

图1 糖化料及温度采样点示意图
Fig. 1 Diagram of saccharification material and temperature sampling points
1.3.2 感官评价
每批次样品均由一个5人评审小组进行盲评。该小组由4名工艺师和1名质量检验员组成,共同对样品的色泽、香气及口味进行评判。
1.3.3 理化指标的测定
水分含量、酸度、还原糖含量、粗淀粉含量的测定:参照赵千慧等[10]的方法。
1.3.4 可培养微生物计数
细菌总数、乳酸菌、芽孢杆菌、酵母菌、霉菌活菌数的测定:参照赵千慧等[10-12]的计数方法。
1.3.5 微生物多样性测定
使用Magen Hipure Soil DNA Kit并参照说明书提取糖化料样品微生物的宏基因组DNA,利用QubitR dsDNA HS Assay Kit进行高灵敏度荧光定量。以提取的基因组DNA为模板,采用引物338F(5'-ACTCCTACGGGAGGCAGCAG-3')和806R(5'-GGACTACHVGGGTWTCTAAT-3')PCR 扩增细菌的16S rRNA V3-V4区基因序列[13];采用正向引物(5'-GTGAATCATCGARTC-3')和反向引物(5'-TCCTCCGCTTATTGAT-3')PCR扩增真菌的ITS1-ITS2区基因序列[14]。所有扩增产物经1.5%琼脂糖凝胶电泳检测、切胶纯化并定量后,委托上海华测艾普医学检验所有限公司在Illumina Nextseq 2000平台上进行双端测序(2×300 bp)。下机数据经质控、拼接与嵌合体去除后,按照97%相似性进行操作分类单元(operational taxonomic unit,OTU)聚类,细菌序列基于Silva 138数据库进行分类学注释,真菌序列则基于UNITE ITS数据库进行分类学注释。
1.3.6 数据处理
采用Qiime 1.9.1、R语言绘制稀释曲线和堆积柱状图等;采用Excel 2016、IBM SPSS Statistics 27.0统计数据并进行相关性分析,采用Origin 2024软件作图;采用Galaxy在线分析平台(http://huttenhower.sph.harvard.edu/galaxy/)进行线性判别分析效应值大小(linear discriminant analysis effect size,LEfSe)分析。
2 结果与分析
2.1 不同糖化料样品的理化指标及感官评价
不同糖化料样品的理化指标及感官评价结果见表1。糖化的最终产物还原糖是微生物发酵的关键底物,糖化料中主要的淀粉及其他营养成分为后续粮醅泥窖发酵代谢产乙醇和风味提供基础物质[4]。由表1可知,两种方式生产的糖化料在水分、酸度、还原糖及粗淀粉含量上均无显著差异(P>0.05),表明在整个糖化发酵周期中,微生物对原料中淀粉等物质的利用效率在两种生产方式下较为接近。温度是影响微生物生长及发酵的关键因素之一[15],两种糖化料在糖化终点时的温度差异极显著(P<0.01),说明两种糖化料的菌群组成及代谢类型可能存在差异。与Y组糖化料相比,S组糖化料甜味稍淡,醪糟味偏重一点,异味明显,分析原因可能为过热发酵导致不同风味的呈现。综上,机械化集中糖化生产的糖化料在糖化终点时温度异常偏高,产生原因可能跟机械班组糖化箱的安置密度、箱体材料、糖化车间空气流通性、微生物的分布及发酵过程微生物代谢产热等因素有关,具体影响机制还需深入监控和研究。这种温度差异不仅影响微生物的数量及菌群组成,还可能对糖化料自身风味和后续粮醅入窖发酵初期菌群的形成及后续代谢风味造成影响。
表1 不同糖化料样品的理化指标及感官评价
Table 1 Physicochemical indexes and sensory evaluation of different saccharification material samples
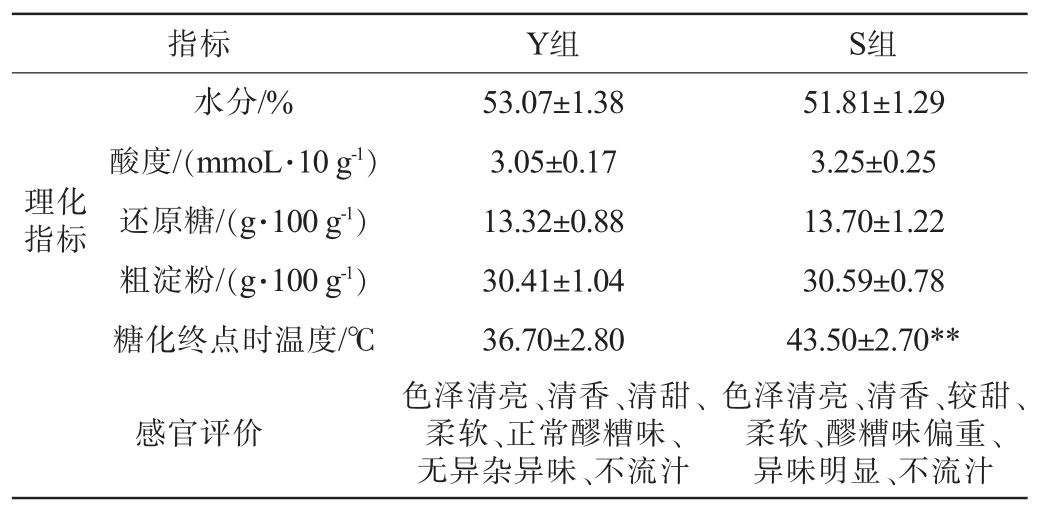
注:“**”表示差异极显著(P<0.01)。
指标Y组S组理化指标51.81±1.29 3.25±0.25 13.70±1.22 30.59±0.78 43.50±2.70**色泽清亮、清香、较甜、柔软、醪糟味偏重、异味明显、不流汁水分/%酸度/(mmoL·10 g-1)还原糖/(g·100 g-1)粗淀粉/(g·100 g-1)糖化终点时温度/℃感官评价53.07±1.38 3.05±0.17 13.32±0.88 30.41±1.04 36.70±2.80色泽清亮、清香、清甜、柔软、正常醪糟味、无异杂异味、不流汁
2.2 不同糖化料样品可培养微生物计数结果
霉菌、酵母菌、乳酸菌、芽孢杆菌等微生物是白酒发酵中不可或缺的关键角色[16],其数量跟酒糟发酵的走向有直接关系。 两种糖化料中可培养微生物计数结果见图2。 由图2可知,在两种糖化料中,细菌总数最高,酵母菌活菌数次之,霉菌活菌数最少。 基于原核微生物活菌计数,Y组糖化料的细菌总数(1.7×107 CFU/g)、乳酸菌活菌数(1.0×107 CFU/g)及芽孢杆菌活菌数(2.3×106 CFU/g)均高于S组(6.4×106 CFU/g、4.9×106 CFU/g、2.0×105 CFU/g),分别为S组的2.7倍、2.0倍、11.5倍。基于真核微生物活菌计数,Y、S组糖化料中的酵母菌活菌数相近,分别为2.7×106 CFU/g、2.4×106 CFU/g,但S组糖化料中的霉菌活菌数(2.8×105 CFU/g)高于Y组(3.6×104 CFU/g),为Y组的7.8倍。 结果表明,不同工艺生产的糖化料分别在芽孢杆菌和霉菌活菌数上存有较大差异。结合温度差异结果,说明S组糖化料中可能存在耐高温霉菌。
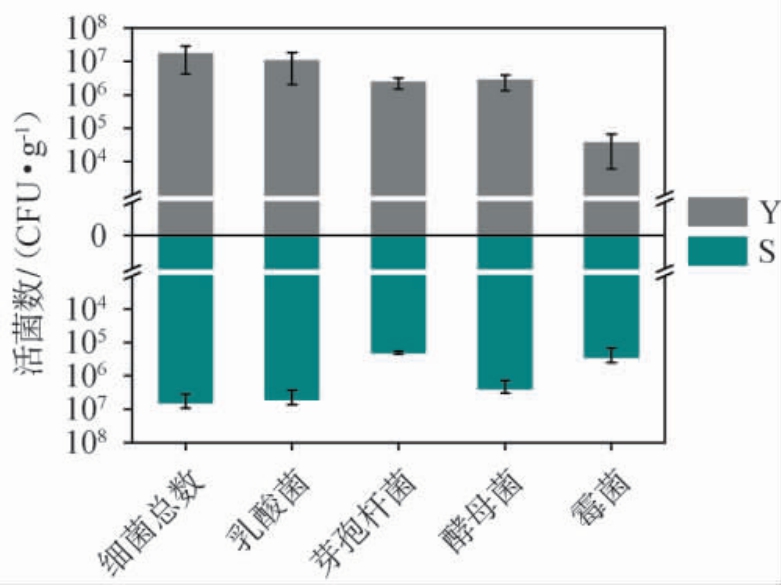
图2 不同糖化料样品可培养微生物计数结果
Fig. 2 Count results of culturable microorganisms in different saccharification material samples
2.3 不同糖化料样品微生物群落结构对比
2.3.1 α-多样性分析结果
不同糖化料样品基于OTU数构建的稀释曲线见图3。由图3可知,随着测序量的增加,两组糖化料样品细菌和真菌OTU稀释曲线均逐渐平缓,说明本次测序深度合适,测序数据较为合理,能反映糖化料样品中微生物菌群的真实情况。
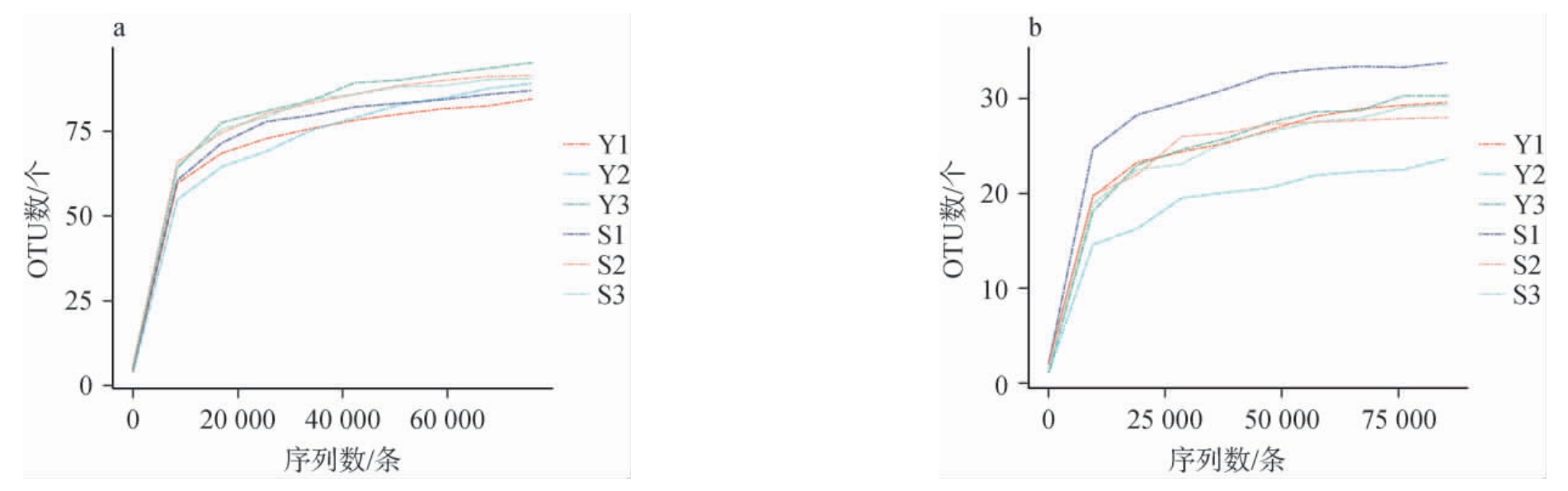
图3 不同糖化料样品细菌(a)及真菌(b)操作分类单元稀释曲线
Fig. 3 Rarefaction curves of operational taxonomic units of bacteria (a) and fungi (b) in different saccharification material samples
不同糖化料微生物菌群的Alpha多样性见图4。由图4可知,Y组糖化料样品中细菌和真菌菌群的ACE指数和Chao1指数高于S组,Shannon指数相反,但差异均不显著(P>0.05)。说明Y组糖化料中细菌和真菌菌群的物种丰富度高于S组,S组糖化料中细菌和真菌群落多样性稍高于Y组。 此外,整体上所有样品中细菌菌群的物种多样性和丰富度普遍高于真菌菌群。
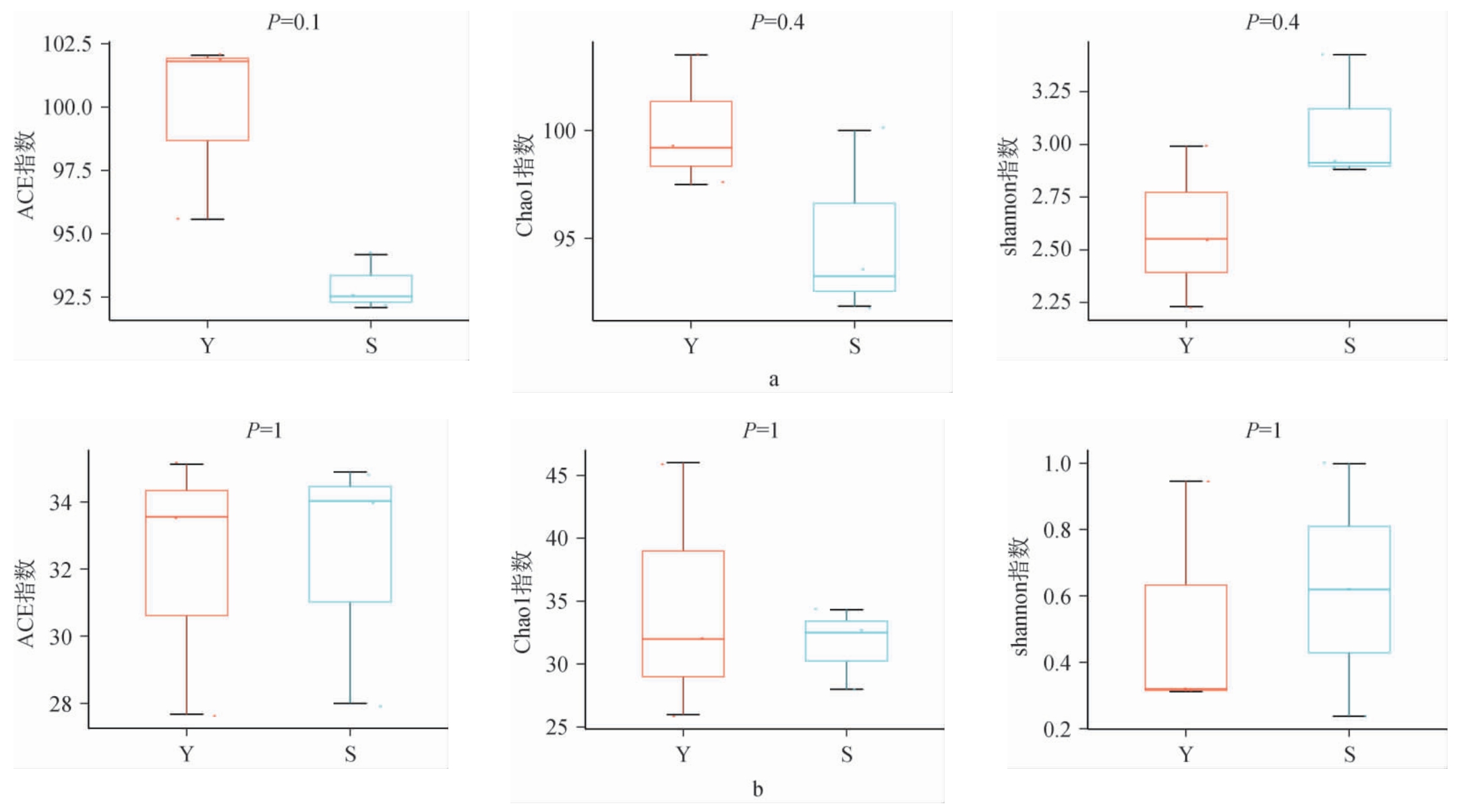
图4 两种糖化料样品细菌(a)及真菌(b)菌群Alpha多样性指数箱线图
Fig. 4 Boxplot of Alpha diversity indexes for bacterial (a) and fungal (b) communities in the two saccharification material samples
为了比较两组糖化料间特有的以及共有的OTU,绘制OTU韦恩图,结果见图5。由图5a可知,Y、S两组糖化料样品中检出的细菌OTU数分别为108个、104个,共有的OTU数为96个,共有的细菌OTU数分别占两组样品中OTU总数的88.89%、92.31%,特有的细菌OTU数分别为12个、8个。由图5b可知,Y、S两组糖化料中特有的真菌OTU数分别为4个、7个,共有的OTU数为29个,共有的真菌OTU数分别占两组样品中OTU总数的87.88%、80.56%。结果表明,两种糖化料样品中细菌及真菌的菌群结构既相似又独特。
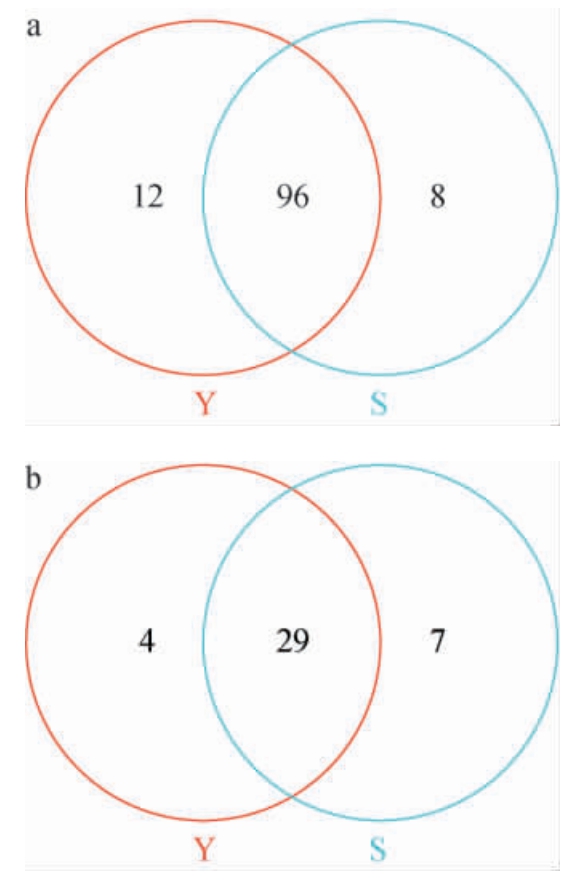
图5 两种糖化料样品细菌(a)及真菌(b)操作分类单元数Venn图
Fig. 5 Venn diagrams of bacteria (a) and fungi (b) operational taxonomic unit numbers of two saccharification material samples
2.3.2 β-多样性分析结果
在属水平上对两种糖化料的细菌及真菌物种组成进行分析,并将平均相对丰度>1%的菌属定义为优势菌属,结果见图6。
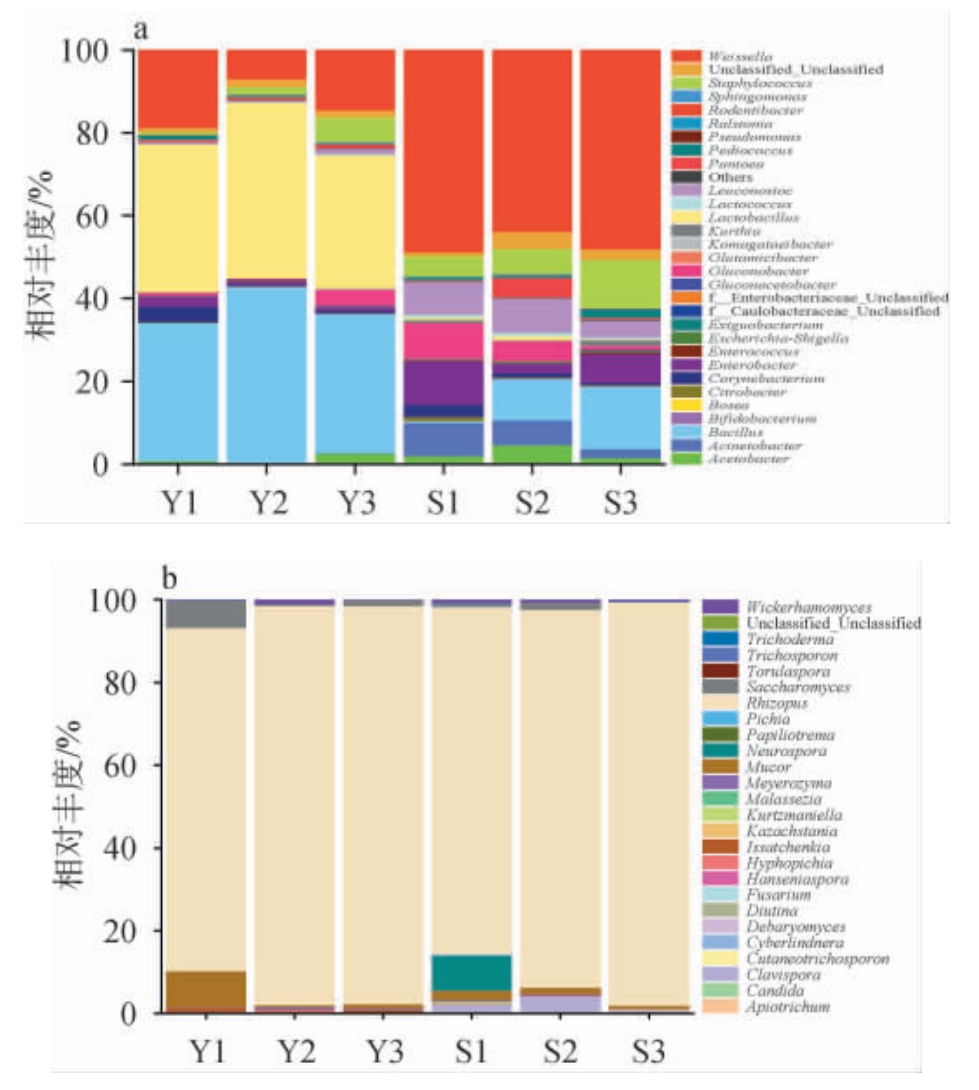
图6 基于属水平不同糖化料样品中细菌(a)及真菌(b)菌群结构
Fig. 6 Bacterial (a) and fungal (b) community structure in different saccharification material samples based on genus level
由图6a可知,在细菌属水平上,Y、S两组糖化料中的优势细菌属分别为9种、12种,共有的优势细菌属为8种,分别为芽孢杆菌属(Bacillus)(36.45%、8.50%)、魏斯氏菌属(Weissella)(13.52%、46.96%)、葡萄球菌属(Staphylococcus)(2.89%、7.63%)、葡糖杆菌属(Gluconobacter)(1.64%、4.72%)、棒状杆菌属(Corynebacterium)(1.57%、1.62%)、肠杆菌属(Enterobacter)(1.45%、6.56%)、醋酸杆菌属(Acetobacter)(1.19%、2.73%)及未分类细菌属(Unclassified_Unclassified)(1.40%、2.43%),这些共有的优势细菌属分别占两种糖化料中总优势细菌属的88.89%、66.67%,总平均相对丰度分别为60.11%、81.16%,表明它们尽管在菌落组成上有显著重叠,但相对丰度存在差异。乳杆菌属(Lactobacillus)在Y组糖化料中占比最高,其平均相对丰度为36.66%,而在S组中的平均相对丰度<1%。明串珠菌属(Leuconostoc)(6.78%)、不动杆菌属(Acinetobacter)(5.36%)、泛菌属(Pantoea)(1.76%)、片球菌属(Pediococcus)(1.05%)在S组糖化料中占有优势,但在Y组糖化料中的平均相对丰度<1%。 Lactobacillus、Weissella、Leuconostoc、Pediococcus均为乳酸菌,能发酵糖产生有机酸,调节发酵环境的pH值,参与香味物质的形成,若乳酸菌过量,易造成酸馊味[16]。Bacillus普遍存在于白酒酿造发酵的各个环节,能代谢产广谱抗菌活性的脂肽类物质,以及蛋白酶、淀粉酶、纤维素酶、酯化酶、果胶酶等酶类物质,对发酵和生香有重要影响[17-18]。这些微生物的丰度差异,可能会导致酒醅产生不同发酵机理。
由图6b可知,在真菌属水平上,Y、S组糖化料中的优势真菌属分别为3种、4种,其中共有优势真菌属为2种,分别为根霉属(Rhizopus)和毛霉属(Mucor)。Rhizopus在两组糖化料样品中的平均相对丰度分别为91.88%、90.96%,占据绝对优势,其糖化酶活力极强[19]。Mucor在两组糖化料样品中的平均相对丰度分别为3.40%、1.49%,其代谢产物如萜烯化合物等影响酒体风味[16]。 酵母属(Saccharomyces)作为Y组糖化料中的优势真菌属,平均相对丰度为2.71%,该菌属耐乙醇,在白酒发酵中主导己酸乙酯、辛酸乙酯等中链脂肪酸酯的合成,是白酒果香和甜香来源之一[20]。棒孢酵母属(Clavispora)为S组糖化料中的优势真菌属,平均相对丰度为2.39%,该菌属耐乳酸,可能与吡嗪类化合物的产生有关[21]。 脉孢霉属(Neurospora)只在S组样品中出现,为S组样品中的优势真菌属,平均相对丰度为2.90%,该菌属能降解纤维素和果胶,菌体富含蛋白[22-23],其来源还需进一步监控和分析。 值得注意的是,两组糖化料中霉菌的平均相对丰度所占比例较为接近,结合结果2.2中糖化料可培养霉菌计数结果,说明S组糖化料中霉菌的活性可能较Y组的高,且可培养霉菌极大可能跟新厂区机械集中糖化车间的环境微生物有关。
2.3.3 不同糖化料微生物群落物种差异分析
为探究不同方式生产的糖化料间微生物群落的差异,采用LEfSe分析具有显著性差异的细菌属和真菌属(筛选标准:LDA值>3,P<0.05),可进一步明确两组糖化料中独特的微生物类群,结果见图7。
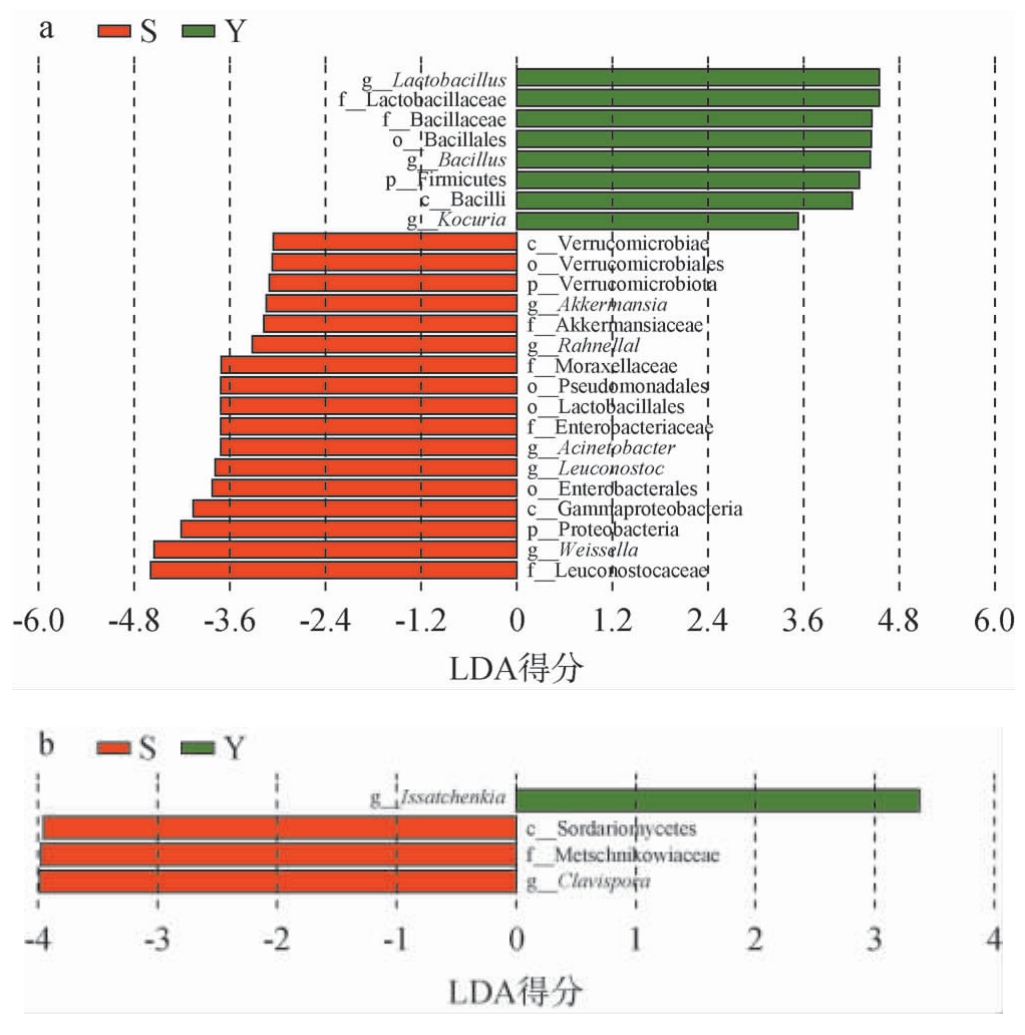
图7 不同糖化料样品细菌(a)及真菌(b)线性判别分析效应值大小分析结果
Fig. 7 Results of linear discriminant analysis effect size analysis of bacterial (a) and fungal (b) communities in different saccharification material samples
由图7a可知,从两组糖化料中共鉴定出8个差异细菌属,Y组糖化料中的差异细菌属为Lactobacillus、Bacillus、考克氏菌属(Kocuria),S组糖化料中的差异细菌属为Weissella、Leuconostoc、Acinetobacter、拉恩氏菌属(Rahnella)、阿克曼菌属(Akkermansia)。 其中Lactobacillus、Weissella、Bacillus的LDA值较高,说明这3个属在两种糖化料中差异最大。Bacillus具有产酶、生香等性能,能促使酵母代谢更多风味物质,在白酒酿造中应用极广[18]。Lactobacillus、Weissella虽同属乳酸菌[16],但在形态、代谢途径等方面存有区别,Lactobacillus多呈长杆状或球短杆状,发酵类型为同型乳酸发酵或异型乳酸发酵;Weissella呈短杆状或卵圆形,为专性异型乳酸发酵[24-25]。不同发酵类型的乳酸菌如何影响酒醅的微生物组成与代谢产物,其具体差异与影响机制仍有待深入研究。
由图7b可知,从两组糖化料中共鉴定出2个差异真菌属。其中Y组糖化料中的差异真菌属为伊萨酵母属(Issatchenkia),其产乙醇和高级醇的能力较强[21]。S组糖化料中的差异真菌属为Clavispora,其耐盐、耐酸、耐高温,与酿酒酵母协同发酵可增酯降醇[26]。
2.4 差异微生物与理化指标间的相关性分析
基于Spearman相关系数,进一步揭示两组糖化料中的差异微生物与理化之间的相关性,结果见图8。由图8可知,水分与Lactobacillus呈显著正相关(P<0.05),与Rahnella呈显著负相关(P<0.05),与Issatchenkia呈极显著正相关(P<0.01)。 温度与Rahnella呈显著正相关(P<0.05),与Issatchenkia呈显著负相关(P<0.05),其他理化指标与菌属间无显著相关性(P>0.05)。 水分、温度对微生物生长、繁殖及代谢具有调控作用[27]。在高水分条件下Lactobacillus不仅繁殖加快,还能通过与相关菌群的协调作用,促进酸类、醇类等挥发性风味物质的合成[28]。对于酵母而言,在一定范围内,其活菌数随水分添加量的增加而显著上升[29];Issatchenkia作为白酒酿造中具有较强产乙醇及高级醇能力的酵母[30],其生长与代谢活动高度依赖水分支持,且研究显示其能促进酒醅中Lactobacillus的增殖,共同影响风味形成[28,30],这解释了二者与水分呈正相关的现象。酵母在25~30 ℃生长最快,低温(10~20 ℃)则会显著延迟发酵启动[28]。彭俊等[31]的研究结果表明,东方伊萨酵母(Issatchenkia orientalis)在30~37 ℃生长旺盛,42 ℃时生长即受抑制,47 ℃时基本停止生长,说明其在高温环境下活性受限,这与本研究结果相一致。 相比之下,Rahnella隶属于肠杆菌科(Enterobacteriaceae)[32],其与水分呈负相关,与曾波等[33]的研究结果一致。该科细菌普遍偏好温暖环境[34],在酱香酒醅堆积过程中,其相对丰度随温度升高而增加[35],表明Rahnella可能更适应中高温条件,从而表现出与温度的正相关关系。此外,有研究表明,Rahnella与2-甲氧基-4-甲基苯酚(烟熏味)的产生呈显著正相关,且是馊味酒醅的主要优势菌属之一[36]。由此得出S组糖化料产生异味可能与Rahnella有关。
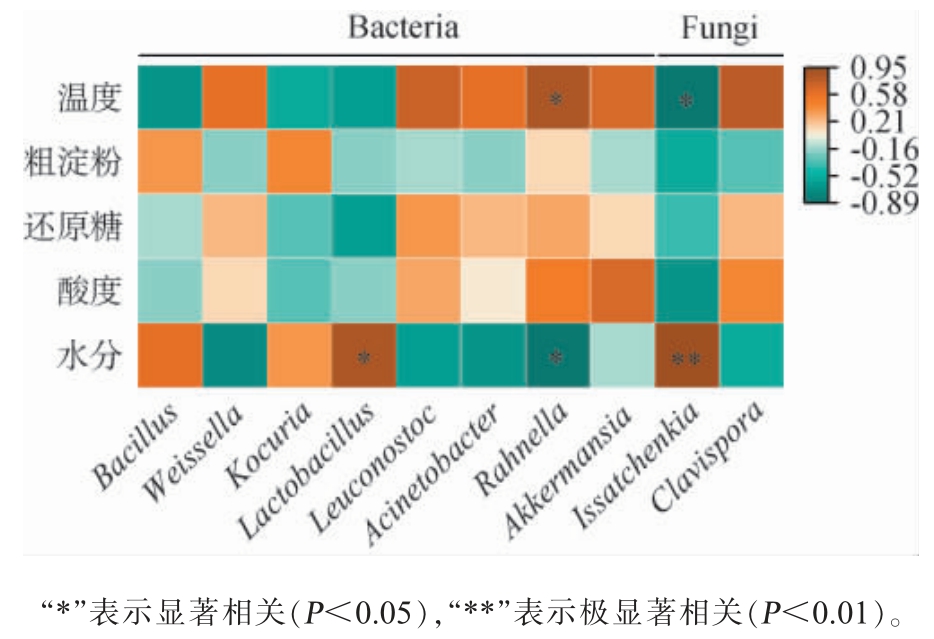
图8 不同糖化料样品间差异微生物属与理化指标间的相关性分析热图
Fig. 8 Heatmap of correlation analysis between differential microbial genus and physicochemical indexes of different saccharification material samples
3 结论
为明确传统手工和机械集中生产的糖化料在品质与微生物特征上的差异,本研究对两种糖化料的理化特性、感官品质、可培养微生物数量及菌群结构多样性进行了综合分析。结果表明,两组糖化料的水分、酸度、还原糖、粗淀粉含量无显著差异(P>0.05),但S组糖化料发酵终点温度极显著高于Y组(P<0.01),且呈现甜味稍淡、醪糟味偏重与异味较明显的过热发酵特征,其异味可能与Rahnella有关。两组糖化料间微生物菌群的Alpha多样性无显著差异(P>0.05),但菌群结构存在区别,基于LDA值>3、P<0.05共筛选出8个差异细菌属和2个差异真菌属。Lactobacillus、Weissella、Bacillus分别为两组糖化料中的主要优势细菌属,其相对丰度在两组间差异较大,贡献了最主要的组间差异。真菌属则以Rhizopus为两组糖化料中的绝对优势真菌属(相对丰度>90%),Issatchenkia和Clavispora为两组糖化料间的差异真菌属。水分和温度对其中乳杆菌属(Lactobacillus)、伊萨酵母属(Issatchenkia)、拉恩氏菌属(Rahnella)的影响显著或极显著(P<0.05或P<0.01)。 本研究揭示了传统手工和机械集中两种方式生产的糖化料在感官、理化指标、可培养微生物及微生物群落上的差异,为不同糖化料群落结构的研究提供相关基础,同时为机械集中培菌糖化工艺的优化升级和品质提升提供微生物层面的理论参考。
[1] 朱美乔.智能酿造助力白酒产业实现高效能[N] .中国食品报,2024-11-04(004).
[2] 杨城.酱香型白酒的传统与现代酿造技术比较研究[J] .中国食品工业,2024(20):96-98.
[3] 杨再懿,殷泽培,冯亮,等. 馥郁香型白酒恒温糖化箱培菌糖化的工艺条件研究[J/OL] . 酿酒科技,1-7[2025-12-25] .https://link.cnki.net/urlid/52.1051.TS.20250704.1601.004.
[4] 杨再懿,殷泽培,冯亮,等. 馥郁香型白酒机械化车间糖化入箱温度工艺优化[J] .现代食品,2024,30(23):98-102.
[5] 丁子元,叶力,郑晓卫,等.小曲培菌糖化研究进展[J] .中国酿造,2023,42(6):7-11.
[6] 王建成,孔茂竹,朱康,等. 不同糖化发酵剂在雅致香型白酒生产中的应用研究[J] .酿酒科技,2025(2):17-22.
[7] 李勇,殷泽培,杨再懿,等. 馥郁香型白酒高粱高压蒸锅蒸粮工艺的应用研[J/OL] . 酿酒科技,1-7[2025-12-25] . https://link.cnki.net/urlid/52.1051.ts.20251126.1115.002.
[8] 王佳佳,杨玉玲,李术钗,等. 基于高通量测序技术四种不同酒曲发酵酒醅真菌菌群研究[J] .中国酿造,2025,44(4):127-131.
[9] 洪彩云,赵燕妮,吴蔓,等. 长武地区凤香型白酒酿造微生物群落与风味物质相关性分析[J] .食品与发酵工业,2025,51(8):176-185.
[10] 赵千慧,周慧玲,秦洋. 冠突散囊菌协同发酵对高粱酒醅微生物及酒体风味的影响[J] .食品科技,2025,50(3):17-24.
[11] 崔东琦.基于微生物组合的强化曲制备及其应用初探[D] .贵阳:贵州大学,2022.
[12] 侯小歌.浓香白酒中温大曲品质解析及制曲小麦筛选模型的构建[D] .郑州:河南工业大学,2024.
[13] 蔡程山,白飞荣,许玲,等. 国井白酒窖池发酵过程中酒醅微生物多样性及理化特性[J] .中国酿造,2023,42(11):90-98.
[14] WHITE T J,BRUNS T D,LEE S B,et al.Amplification and direct sequecing of funfal ribosomal RNA genes for phylogenetics[M] .Cambridge:Academic Press Inc.,1990:315-322.
[15] CAO Y,ZHANG H X,DU H,et al.Microorganisms and metabolic characteristics of temperature-dependent fermentation during sauce-flavor Baijiu production[J] .Food Biosci,2025,63:105787.
[16] 时伟,郑红梅,黄婷,等.中国白酒酿造核心微生物相互作用研究进展[J] .食品与发酵工业,2025,51(20):427-436.
[17] LI Z,FERNANDEZ K X,VEDERAS J C,et al.Composition and activity of antifungal lipopeptides produced by Bacillus spp. in Daqu fermentation[J] . Food Microbiol,2023,111:104211.
[18] 蒋倩儿,梁会朋,李琳琳,等. 芽孢杆菌在白酒酿造过程中的应用研究进展[J] .食品工业科技,2025,46(8):391-401.
[19] 丁娟,许勤虎,王祥河,等.多微麸曲清香型白酒酿造用糖化菌种筛选研究[J] .天津科技,2023,50(7):19-22,26.
[20] 文悦,张宿义,宋攀,等. 浓香型白酒酒醅发酵过程中微生物群落阶段性演替规律及形成机理[J] .食品科学,2025,46(19):144-157.
[21] 李慧. 不同生产季汾香型白酒酿造微生物群落及其功能差异解析[D] .太原:山西大学,2024.
[22] DAI Y Q,LIU Y F,WANG Z,et al.Enhanced mycoprotein production of Neurospora intermedia from soy processing byproducts:Integration of ultrasonic stimulation with repeated-batch simultaneous saccharification and culture[J] .Bioresource Technol,2025:133124.
[23] PAUL S, WILLIAM C. The history of Neurospora crassa in fermented foods[J] .Discover Food,2025,5(1):232.
[24] 乌日罕.食品中乳酸菌种类及其应用前景探究[J] . 中国食品,2024(20):147-149.
[25] 魏梓晴. 酱曲源魏斯氏菌的筛选及其体外安全性与益生性研究[D] .佛山:佛山科学技术学院,2022.
[26] 彭立影.产酯酵母的筛选及其初步应用研究[D] .广州:仲恺农业工程学院,2021.
[27] 安凯园,杜艳红,聂建光,等. 酱香型白酒生产堆积酒醅中微生物、理化因子以及风味物质研究进展[J] .中国酿造,2025,44(6):20-25.
[28] 文悦,张宿义,宋攀,等. 浓香型白酒酒醅发酵过程中酵母菌群演替机理及代谢特征[J] .食品科学,2025,46(23):169-181.
[29] 余安玲,张小娜,李红. 酵母麸曲培养条件优化及其固态发酵应用研究[J] .食品与发酵工业,2024,50(11):47-54.
[30] 彭远凤,杨阳,赵东,等.东方伊萨酵母对浓香型白酒酒醅微生物群落结构及挥发性风味物质合成的影响[J] .食品科学,2024,45(16):97-104.
[31] 彭俊,杨团元,刘蒲临,等.白酒酿造酒醅与周边土壤中酵母菌多样性及东方伊萨酵母发酵特性比较[J] .中国酿造,2019,38(8):77-84.
[32] 梁婧,胡秀彩,吕爱军,等. 水生拉恩菌研究进展[J] . 水产科学,2020,39(6):972-978.
[33] 曾波,饶家权,邹永芳,等.浓香型白酒酒醅发酵过程中微生物群落结构演替及其与理化指标相关性[J] .食品科学,2024,45(7):111-118.
[34] 王思然. 冷暖季型牧草表面微生物菌群对青贮发酵品质及微生物群落结构的影响[D] .南京:南京农业大学,2020.
[35] 张飞,周生孝,高勤鑫,等. 黄淮地区酱香型白酒第五轮、第六轮次堆积不同温度节点细菌差异分析[J] .酿酒科技,2025(7):38-42,53.
[36] 龚佳欣. 基于感官风味的酱香型白酒挥发性异嗅味物质的表征及来源解析[D] .贵阳:贵州大学,2024.