光核桃(Prunus mira Koehne)俗称“西藏野桃”,又名“西藏桃”,为蔷薇科(Rosaceae)李属(Prunus)落叶乔木[1]。西藏特殊的气候环境造就了光核桃果实丰富的营养价值,其含有多糖、黄酮和多酚等多种功能性物质,是一种具有高营养价值和高经济利用价值的宝贵资源[2-4]。
随着高通量测序技术的快速发展,越来越多的植物果实微生物群落结构特征及组成已被相继研究,植物表皮和内生微生物组作为其第二基因组在植物适应性和病害防御中发挥着重要作用,果实微生物组对果实健康发育、营养品质、采后生理等方面的影响同样至关重要[5-6]。何萍等[7]研究发现,西藏林芝市不同品种葡萄果实表皮微生物群落结构组成及多样性差异明显,优势细菌属主要为伯克霍尔德氏菌属(Burkholderia)、慢生根瘤菌属(Bradyrhizobium)和寡养单胞菌属(Stenotrophomonas)等,优势真菌属主要为球腔菌属(Mycosphaerella)、曲霉属(Aspergillus)和枝孢属(Cladosporium);姜莉莉等[8]研究发现,红栗成熟期叶片和果实的链格孢菌属(Alternaria)相对丰度均较高,受板栗叶焦枯病侵染的风险较大;赵宇卓等[9]研究发现,果实品质与微生物息息相关,白枇杷根内微生物对果实品质有明显的调控作用,存在微生物-宿主互作关系;罗冬兰等[10]研究发现,贵州不同品种桃的微生物群落组成有明显差异,而红桃与黄桃的群落组成相似程度更高。
目前,有关西藏光核桃果实的研究主要集中在果实表型性状[11]、果仁活性物质提取[12]、果浆保鲜[13]、果粉特性[14]和果实品质[15]等方面,而关于其果实微生物的研究鲜见报道。因此,本研究以西藏林芝市巴宜区(真巴村、尼洋河畔、西藏农牧学院)、林芝市波密县桃花沟、米林市彩门村野生光核桃为实验材料,通过高通量测序技术分析光核桃果实微生物群落组成及结构特征,探究产地对光核桃果实微生物群落多样性的影响,以期为其野生资源的保护和利用奠定一定的理论基础。
1 材料与方法
1.1 材料与试剂
1.1.1 样品的采集
2024年8月采集林芝市5个产地光核桃果实,所有光核桃果实均为野生自然成熟,随机选取6棵生长一致的光核桃树,用无菌剪刀分别采集每棵光核桃树上的成熟果实,混合均匀后装入采样袋并编号,每组设置3个重复,置于-80 ℃冰箱保存备用。光核桃果实采样地的具体地理信息见表1。
表1 光核桃果实采样地的地理信息
Table 1 Geographical information for sampling site of Prunus mira fruit
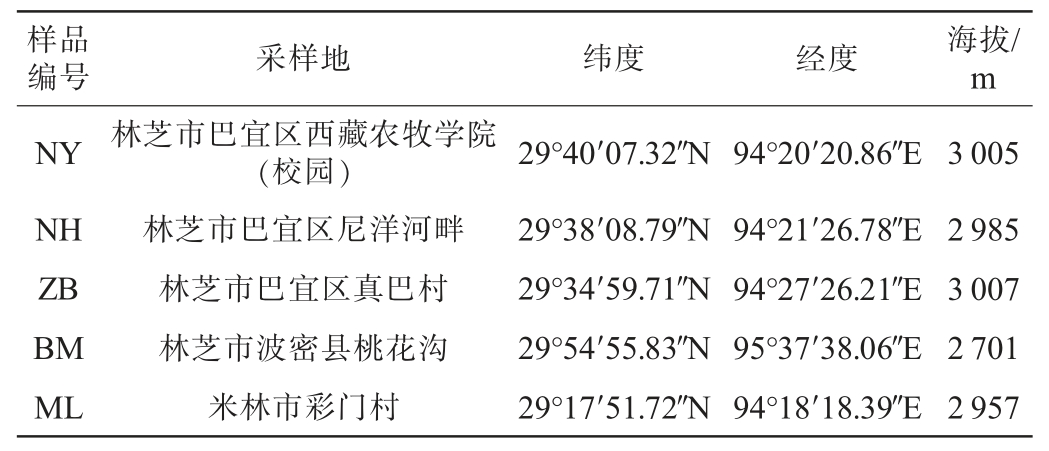
样品编号采样地纬度经度海拔/m NY NH ZB BM ML林芝市巴宜区西藏农牧学院(校园)林芝市巴宜区尼洋河畔林芝市巴宜区真巴村林芝市波密县桃花沟米林市彩门村29°40′07.32″N 29°38′08.79″N 29°34′59.71″N 29°54′55.83″N 29°17′51.72″N 94°20′20.86″E 94°21′26.78″E 94°27′26.21″E 95°37′38.06″E 94°18′18.39″E 3 005 2 985 3 007 2 701 2 957
1.1.2 主要试剂
Qubit2.0脱氧核糖核酸(deoxyribonucleic acid,DNA)检测试剂盒、琼脂糖:美国Invitrogen公司;DNeasy Plant Mini Kit提取试剂盒:美国Qiagen公司;AxyPrep DNA凝胶回收试剂盒:美国Axygen公司;脱氧核糖核苷三磷酸(deoxy-ribonucleoside triphosphate,dNTPs)(5 mmol/L)、Taq DNA聚合酶(5.0 U/μL)、普通DNA产物纯化试剂盒:天根生化科技(北京)有限公司。
1.2 仪器与设备
5418R高速冷冻离心机:德国Eppendorf公司;T100聚合酶链式反应(polymerase chain reaction,PCR)仪:美国Biorad公司;NanoDrop2000微量分光光度计:美国Thermo公司;DYY-15D电泳仪:北京六一生物科技有限公司;Tocan 240凝胶成像系统:上海领成生物科技有限公司。
1.3 方法
1.3.1 光核桃样品微生物宏基因组DNA提取及PCR扩增
采用DNeasyPlant Mini Kit提取试剂盒提取光核桃果实的微生物宏基因组DNA,利用1%琼脂糖凝胶电泳检测抽提的基因组DNA。以其为模板,采用通用引物338F(5'-ACTCCTACGGGAGGCAGCA-3')和806R(5'-GGACTACHVGGGTWTCTAAT-3')PCR扩增细菌菌群的16S rRNA基因序列,采用引物ITS1F(5'-CTTGGTCATTTAGAGGAAGTAA-3')和ITS2R(5'-GCTGCGTTCTTCATCGATGC-3')PCR 扩增真菌内源转录间隔区(internally transcribed spacer,ITS)基因序列[16]。PCR扩增体系(25μL):DNA模板1μL,TaqDNA聚合酶(5.0 U/μL)0.20 μL,10×PCR Buffer 2.0 μL,dNTPs(5 mmol/L)1 μL,正向和反向引物各1 μL,双蒸水(ddH2O)18.80 μL。PCR扩增程序:94 ℃预变性5 min;94 ℃变性30 s,55℃退火30s,72℃延伸45s,共35个循环;72℃再延伸10min。PCR扩增产物经琼脂糖凝胶电泳检测和纯化回收后委托上海美吉生物医药科技有限公司基于MiSeq PE300测序仪进行高通量测序。
1.3.2 数据处理与分析
使用QIIME2(v2022.2,https://qiime2.org)软件对原始序列进行过滤、拼接、质控、降噪和去嵌合体后获得扩增子序列变异体(amplicon sequence variant,ASV),进一步使用classify-consensus-vsearch(Vsearch)插件将ASVs在UNITE数据库(Release 8.0,https://unite.ut.ee/)和Greengenes数据库(Release 135,http://greengenes.secondgenome.com/)中进行比对,分别对真菌和细菌进行物种分类学注释。 利用QIIME2软件的qiime feature-table rarefy功能对ASVs的丰度表进行抽平(抽平深度设为最低样本序列量的95%)[17]。利用Qiime(2020.2.0)软件和R语言(version 3.3.1)进行Alpha多样性、Beta多样性、物种组成分析;利用R语言进行主成分分析(principal component analysis,PCA)和线性判别分析效应大小(linear discriminant analysis effect size,LEfSe)分析。 采用PICRUSt2和FUNGuild软件分别对细菌及真菌功能进行预测分析
2 结果与分析
2.1 不同产地光核桃果实微生物ASVs分析
不同产地光核桃果实中微生物ASVs组成分析结果见图1。由图1A可知,BM、ML、NY、NH和ZB 5个产地光核桃果实样品中的细菌ASVs数分别为14、158、134、26和46个,共有的细菌ASVs数为7个;由图1B可知,BM、ML、NY、NH和ZB 5个产地光核桃果实样品中的真菌ASVs数分别为249、180、196、191和278个,共有真菌ASVs数为30个,说明不同地区光核桃果实细菌及真菌群落结构组成差异较大。
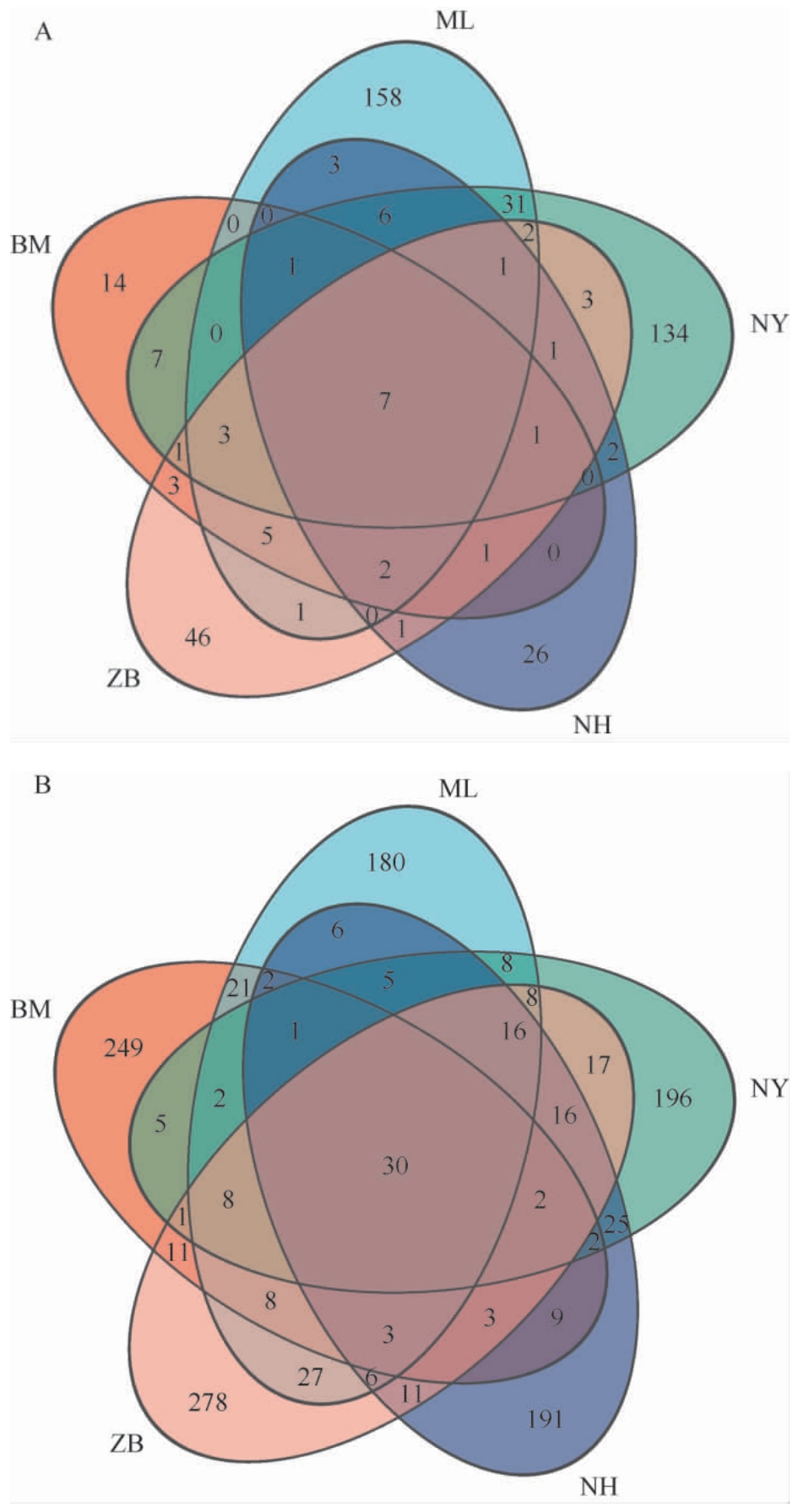
图1 不同产地光核桃果实中细菌(A)及真菌(B)扩增子序列变体组成分析韦恩图
Fig. 1 Venn diagram of composition of bacterial (A) and fungal (B)amplicon sequence variant in the Prunus mira fruits from different production areas
2.2 不同产地光核桃果实微生物群落Alpha多样性分析
Alpha多样性指数中的Coverage值表示各样品文库的覆盖率,其数值越高,说明样本中序列未被测出的概率越低,反映了测序结果是否代表样本的真实情况;Ace指数和Chao1指数反映微生物群落物种的丰富度,Shannon指数和Simpson指数反映微生物群落物种的多样性,Ace、Chao1和Shannon指数越大,Simpson指数越小,表明样品的微生物多样性和丰富度越高[17]。不同产地光核桃果实微生物群落Alpha多样性分析结果见表2。 由表2可知,5个产地光核桃果实样品微生物的Coverage值均>99%,说明测序结果能代表样本的真实情况,符合分析要求。5个产地光核桃果实真菌菌群的Ace、Chao1和Shannon指数均高于细菌菌群,且Simpson指数均低于细菌菌群,表明5个产地光核桃果实的真菌菌群多样性和丰富度均高于细菌菌群。ML产地光核桃果实样品细菌菌群的shannon指数最高,Simpson指数较低,NY产地光核桃果实样品细菌菌群的Ace指数和Chao1指数最高,表明ML产地光核桃果实样品的细菌菌群多样性最高,而NY产地光核桃果实样品细菌菌群丰富度最高。同理,ZB产地光核桃果实样品中真菌菌群丰富度最高,而ML产地光核桃果实样品中的真菌菌群多样性最高。 结果表明,不同产地光核桃果实样品微生物菌群多样性和丰富度存在差异。
表2 不同产地光核桃果实微生物群落多样性分析结果
Table 2 Analysis of microbial community diversity of Prunus mira fruits from different production areas
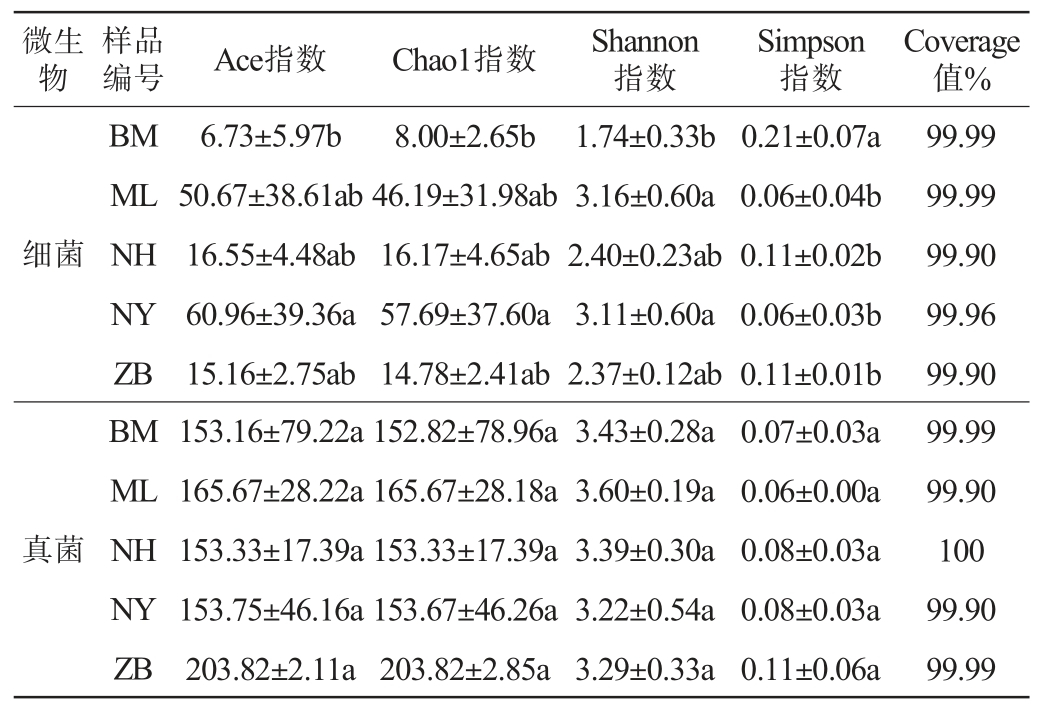
注:同列不同字母表示差异显著(P<0.05)。
微生物编号 Ace指数Chao1指数Shannon指数样品Simpson指数Coverage值%细菌真菌99.99 99.99 99.90 99.96 99.90 99.99 99.90 100 99.90 99.99 BM ML NH NY ZB BM ML NH NY ZB 6.73±5.97b 50.67±38.61ab 16.55±4.48ab 60.96±39.36a 15.16±2.75ab 153.16±79.22a 165.67±28.22a 153.33±17.39a 153.75±46.16a 203.82±2.11a 8.00±2.65b 46.19±31.98ab 16.17±4.65ab 57.69±37.60a 14.78±2.41ab 152.82±78.96a 165.67±28.18a 153.33±17.39a 153.67±46.26a 203.82±2.85a 1.74±0.33b 3.16±0.60a 2.40±0.23ab 3.11±0.60a 2.37±0.12ab 3.43±0.28a 3.60±0.19a 3.39±0.30a 3.22±0.54a 3.29±0.33a 0.21±0.07a 0.06±0.04b 0.11±0.02b 0.06±0.03b 0.11±0.01b 0.07±0.03a 0.06±0.00a 0.08±0.03a 0.08±0.03a 0.11±0.06a
2.3 不同产地光核桃果实中的微生物群落结构组成分析
2.3.1 基于门水平不同产地光核桃果实中的微生物群落结构组成分析
在门水平上,不同产地光核桃果实样品中微生物群落结构组成见图2。 由图2A可知,从5个产地光核桃果实样品中共注释到27个细菌门,包括5个优势细菌门(相对丰度≥1.00%),其中,假单胞菌门(Pseudomonadota)(6.54%~73.61%)为5个产地光核桃果实样品中共有的优势细菌门,拟杆菌门(Bacteroidate)(1.43%~14.72%)为ML、NY、NH和ZB 4个产地光核桃果实样品中共有的优势细菌门,热脱硫杆菌门(Thermodesulfobacteriota)(1.02%)和粘菌门(Myxococcota)(4.7%)为ML产地光核桃果实样品中共有的优势细菌门,放线菌门(Actinomycetota)(1.22%~1.84%)为NY和ZB产地光核桃果实样品中共有的优势细菌门。 有研究表明,毛白杨不同组织内生细菌群落中假单胞菌门和放线菌门为优势细菌门[18],本研究结果与其相近。
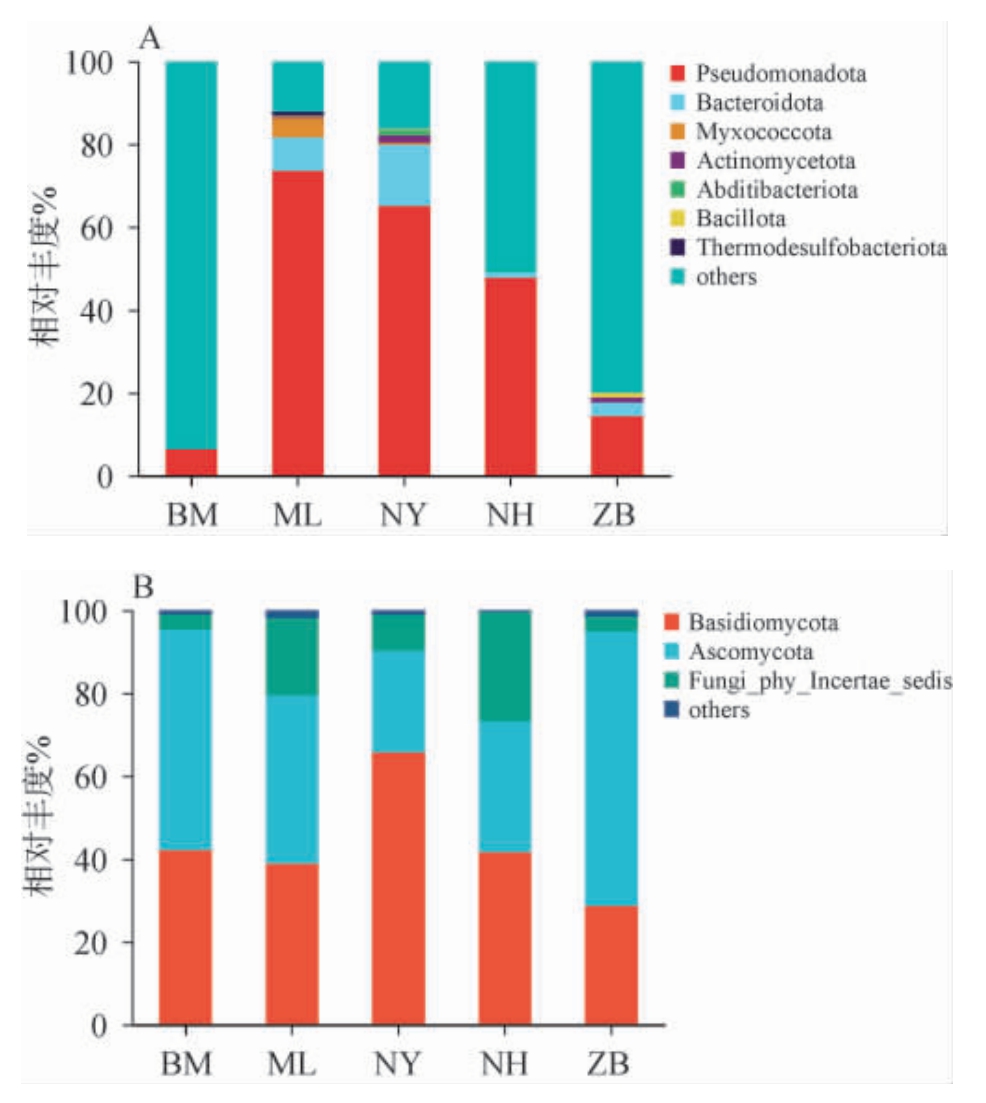
图2 基于门水平不同产地光核桃果实样品中细菌(A)及真菌(B)的群落结构组成
Fig. 2 Community structure composition of bacteria (A) and fungi (B)in Prunus mira fruit samples from different production areas based on phylum level
由2B可知,从5个产地光核桃果实样品中共注释到25个真菌门,包括3个优势真菌门,分别为担子菌门(Basidiomycota)(28.98%~67.89%)、子囊菌门(Ascomycota)(22.39%~66.86%)和Fungi_phy_Incertae_sedis(3.59%~26.36%)。 有研究发现,镇远红桃、镇远艳红桃和玉屏黄桃真菌群落组成中的优势真菌门均为子囊菌门、担子菌门[19],本研究结果与之相近。
2.3.2 基于属水平不同产地光核桃果实样品中的微生物群落结构组成分析
在属水平上,不同产地光核桃果实样品中共注释到85个细菌属、605个真菌属,平均相对丰度排名前20的微生物菌群结构见图3。 由图3A可知,从所有样品中共注释到18个优势细菌属(相对丰度>1%),BM产地光核桃果实样品中的优势细菌属为不动杆菌属(Acinetobacter)(3.48%)、埃希氏菌属(Escherichia)(1.43%)和草螺菌属(Herbaspirillum)(1.02%)。ZB产地光核桃果实样品中的优势细菌属为鞘氨醇单胞菌属(Sphingomonas)(3.68%)和薄层杆菌属(Hymenobacter)(3.27%)。NH产地光核桃果实样品中的优势细菌属为甲基杆菌属(Methylobacterium)(15.75%)、地衣球菌属(Lichenicoccus)(10.84)、地衣杆菌属(Lichenibacterium)(10.22%)、Sphingomonas(3.88%)、norank_f__Comamonadaceae(3.88%)和贪噬菌属(Variovorax)(2.45%)。NY产地光核桃果实样品中的优势细菌属为Methylobacterium(22.90%)、Sphingomonas(11.66%)、Lichenibacterium(9.2%)、螺状菌属(Spirosoma)(7.98%)、马赛菌属(Massilia)(6.54%)、Hymenobacter(5.72%)、Lichenicoccus(3.68%)、Acinetobacter(3.48%)、拜叶林克氏菌属(Beijerinckia)(2.66%)、喜热单胞菌属(Caldimonas)(1.43%)、Lichenihabitans(1.43%)、遥远杆状菌属(Abditibacterium)(1.27%)和黏液杆菌属(Mucilaginibacter)(1.02%)。ML产地光核桃果实样品中的优势细菌属为Sphingomonas (20.45%)、Methylobacterium(20.25%)、Lichenibacterium(13.09)、Hymenobacter(8.18%)、Lichenicoccus(5.31%)、蜂窝囊菌属(Melittangium)(4.70%)和Massilia(4.70%)。Acinetobacter在氮磷代谢中发挥着重要作用[20],Sphingomonas和Methylobacterium已被证实具有溶磷固氮、生物防治和促生作用[21-24]。
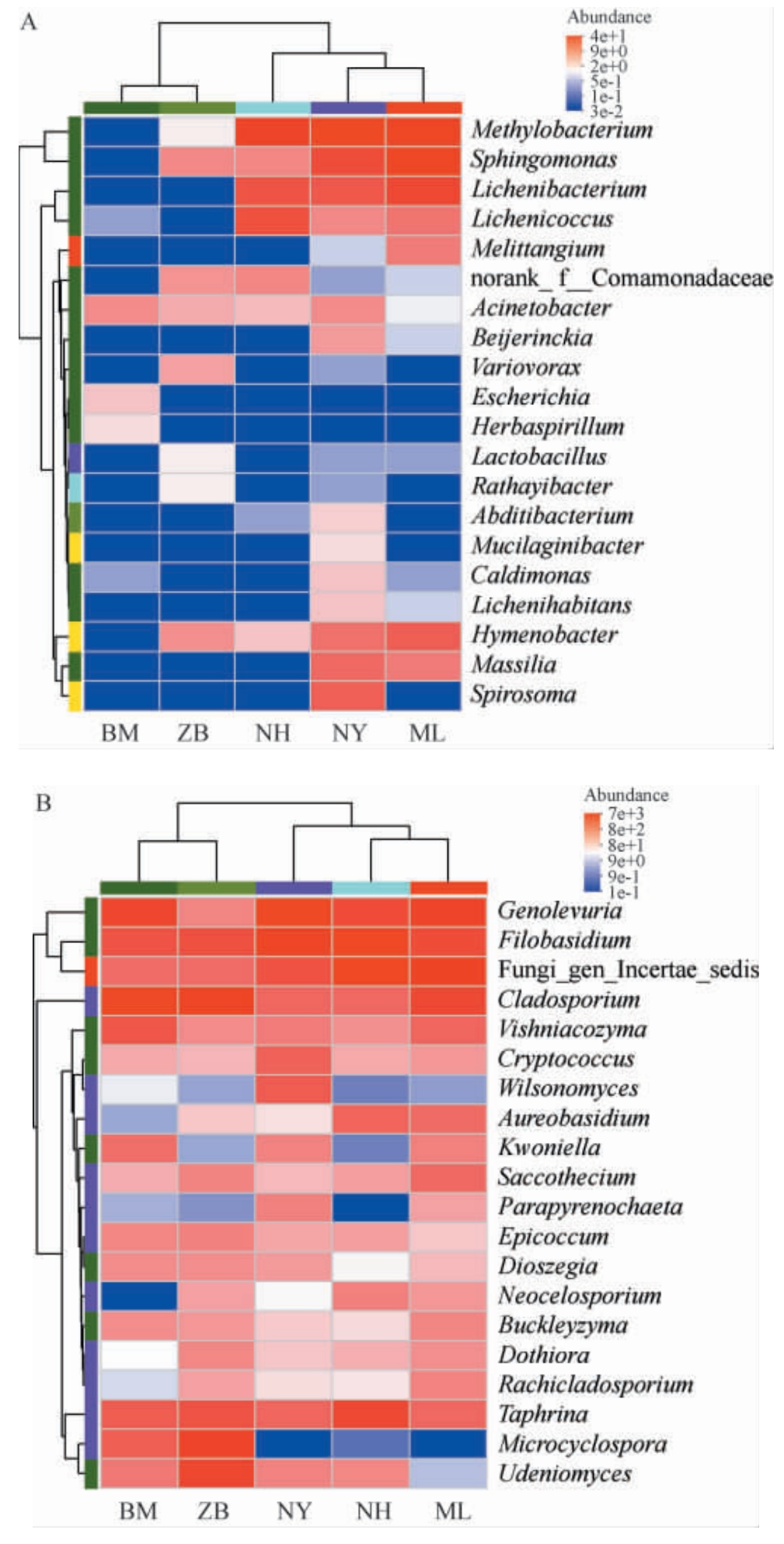
图3 基于属水平不同产地光核桃果实中平均相对丰度排名前20的细菌(A)和真菌(B)菌群聚类分析热图
Fig. 3 Cluster analysis heat map of the average relative abundance top 20 bacterial (A) and fungal (B) communities in Prunus mira samples from different production areas based on genus level
由图3B可知,从所有样品中共注释到22个优势细菌属(相对丰度>1%),BM产地光核桃果实样品中的优势真菌属为枝孢属(Cladosporium)(27.47%)、Genolevuria(13.57%)、线黑粉菌属(Filobasidium)(8.30%)、维希尼克氏酵母菌属(Vishniacozyma)(7.43%)、外囊菌属(Taphrina)(5.77%)、叠孢属(Microcyclospora)(5.63%)、Fungi_gen_Incertae_sedis(3.58%)、Kwoniella(3.46%)、乌登酵母属(Udeniomyces)(2.6%)、附球菌属(Epicoccum)(1.73%)、Dioszegia(1.43%)和巴克利酵母菌属(Buckleyzyma)(1.38%)。ZB产地光核桃果实样品中的优势真菌属为Cladosporium(19.75%)、Microcyclospora(15.16%)、Udeniomyces(12.52%)和Filobasidium(8.80%)、Taphrina(8.12%)、Fungi_gen_Incertae_sedis(3.67%)、Epicoccum(1.98%)、囊膜菌属(Saccothecium)(1.87%)、穴壳属(Dothiora)(1.68%)、Dioszegia(1.35%)、Vishniacozyma(1.48%)和Buckleyzyma(1.06%)。 NY产地光核桃果实样品中的优势真菌属为Genolevuria(29.47%)、Filobasidium(22.61%)、Fungi_gen_Incertae_sedis(8.53%)、Wilsonomyces(5.96%)、隐球菌属(Cryptococcus)(5.07%)、Taphrina(4.41%)、Cladosporium(4.26%)、Vishniacozyma(2.31%)、Parapyrenochaeta(2.01%)、Kwoniella(1.89%)、Udeniomyces(1.89%)。 NH产地光核桃果实样品中的优势真菌属为Fungi_gen_Incertae_sedis(26.36%)、Filobasidium(25.67%)、Taphrina(11.70%)和Genolevuria(10.51%)、短梗霉属(Aureobasidium)(4.74%)、Cladosporium(4.05%)、Neocelosporium(2.06%)。ML产地光核桃果实样品中的优势真菌属为Fungi_gen_Incertae_sedis(18.55%)、Genolevuria(16.43%)、Cladosporium(11.67%)、Filobasidium(10.32%)、Vishniacozyma(4.01%)、Taphrina(4.14%)、Saccothecium(4.07%)、Aureobasidium(3.81%)、Kwoniella(2.02%)和蒜孢属(Rachicladosporium)(1.88%)。5个产地光核桃果实样品中均检测出Vishniacozyma(1.30%~7.43%)。 枝孢属广泛分布于植物体内和土壤中,能合成多种类型的化合物,如萜类、生物碱和醌类等[7,25],线黑粉菌属参与有机质的转化过程,可为植物生长提供必要的营养[26-28]。
2.4 基于微生物属不同产地光核桃果实样品主成分分析
为了分析西藏林芝不同地区光核桃果实样品中微生物群落结构组成的差异,在细菌和真菌属水平上对其进行PCA,结果见图4。由图4A可知,在细菌群落组成中,PC1和PC2的方差贡献率分别为86.68%、4.80%,说明前两个主成分能代表91.48%的原始信息。BM和ZB距离较近,说明这两个产地的细菌群落结构较为相似。ML、NH、NY三个产地的样品点部分重叠,表明它们的细菌群落组成具有一定相似性,但组内变异较大。BM、ZB组与ML、NH、NY组分别位于不同象限,说明它们之间的细菌群落结构差异明显。 由图4B可知,在真菌群落组成中,PC1和PC2的方差贡献率分别为19.93%和36.60%,说明前两个主成分能代表56.53%的原始信息。ML、NY、NH三个产地的样品点重叠较多,表明它们的真菌群落结构较为相似。ZB与ML产地的样品点重叠较多,且与ML、NY、NH三个产地的样品点距离较远,表明他们之间的真菌群落结构组间差异较大,ZB产地的组内样品点分散,组内真菌群落结构存在一定差异,表明该产地真菌群落独特性强并且结构不太稳定或易受局部微环境影响明显。
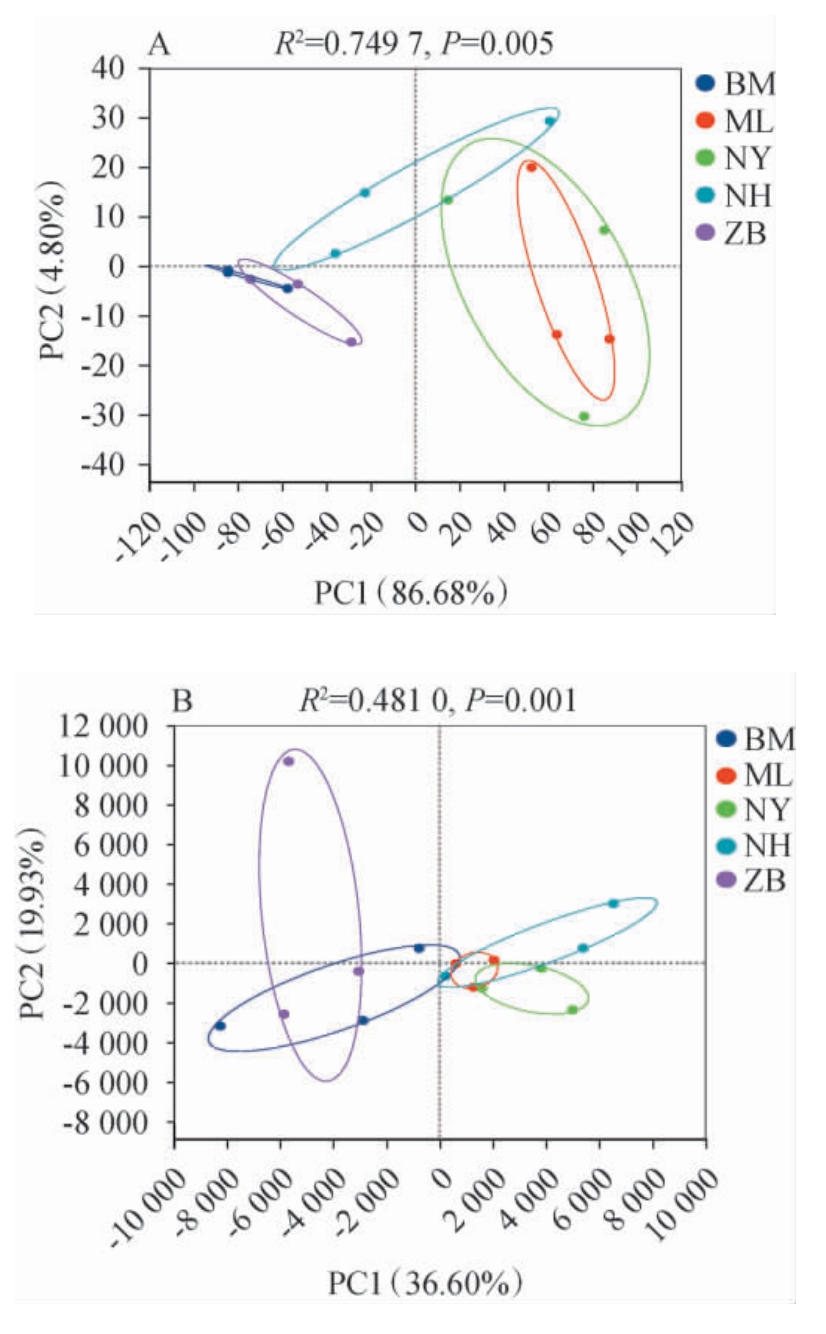
图4 基于属水平不同产地光核桃果实样品细菌(A)及真菌(B)群落主成分分析结果
Fig. 4 Principal component analysis results of bacterial (A) and fungal (B) communities in Prunus mira samples from different production areas based on genus level
2.5 不同产地光核桃果实样品中微生物的LEfSe分析
基于LEfSe分析方法对西藏林芝不同产地光核桃果实样品中的差异微生物菌群进行分析,结果见图5。由图5A可知,从不同产地光核桃果实样品中共检测到2个主要差异细菌属(LDA得分>4.5),NY产地光核桃果实样品中主要的差异细菌属为Spirosoma;NH产地光核桃果实样品中主要差异细菌属为Methylobacterium。
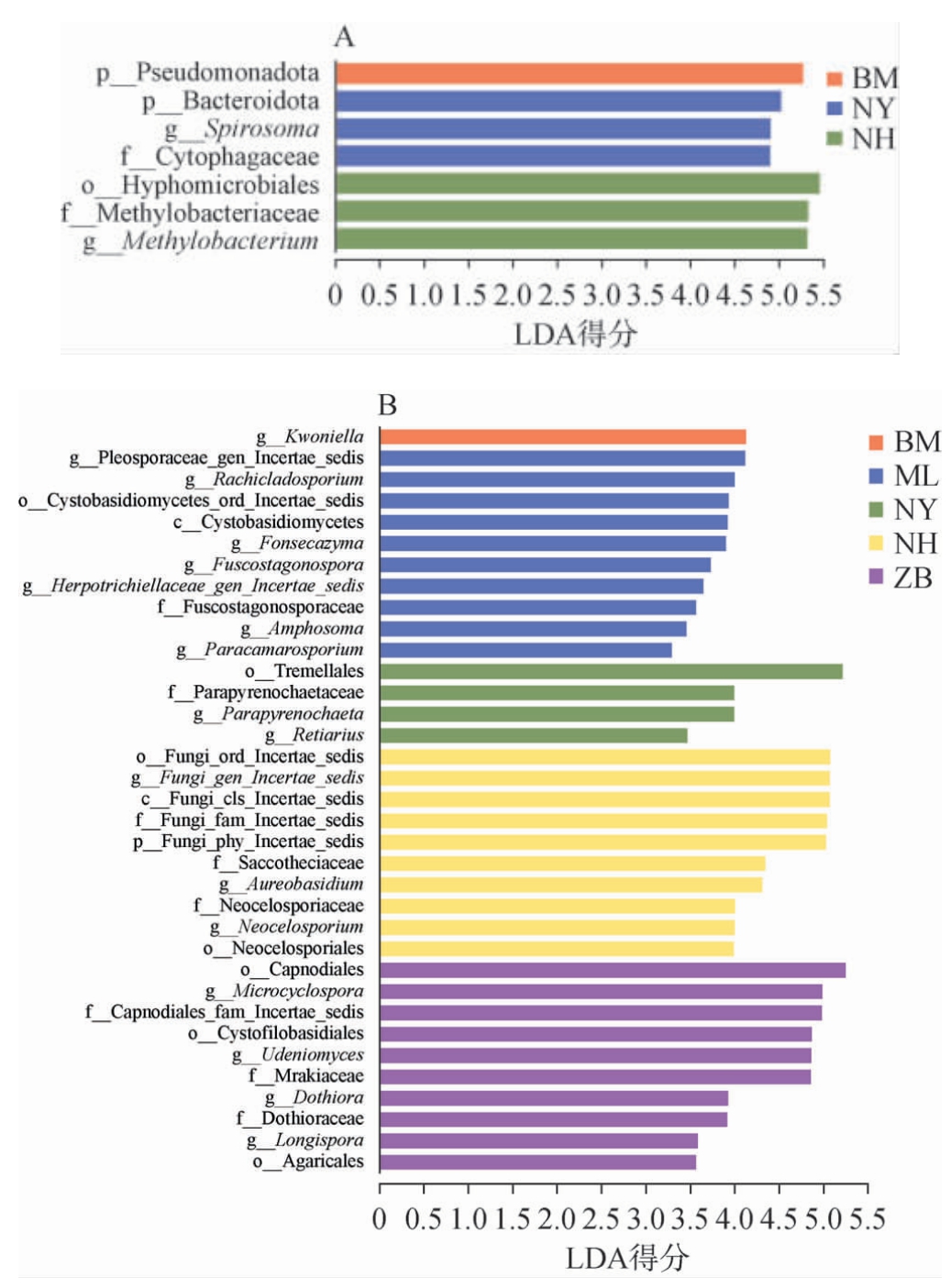
图5 不同产地光核桃果实样品中细菌(A)和真菌(B)群落线性判别分析效应大小分析结果
Fig. 5 Linear discriminant analysis effect size analysis results of bacterial (A) and fungal (B) communities in Prunus mira fruits samples from different production areas
由图5B可知,从不同产地光核桃果实样品中共检测到16个主要差异真菌属(LDA得分>3),BM产地光核桃果实样品中主要差异真菌属为Kwoniella;ML产地光核桃果实样品中主要差异真菌属为Pleospraceae_gen_Incertae_sedis、Rachicladosporium、Fonsecazyma、Fuscostagonospora、Herpotrichiellaceae_gen_Incertae_sedis、Amphosoma、Paracamarosporium;NY产地光核桃果实样品中主要差异真菌属为Parapyrenochaeta、Retiarius;NH产地光核桃果实样品中主要差异真菌属为Aureobasidium和Neocelosporium;ZB产地光核桃果实样品中主要差异真菌属为Microcyclospora、Udeniomyces、Dothiora和Longispora。
2.6 微生物群落的功能预测
为了进一步研究不同地区光核桃果实微生物群落的功能,采用PICRUSt2和FUNGuild软件分别对5种不同产地光核桃果实细菌及真菌菌群功能进行预测分析,结果见图6。由图6A可知,所有样品中的细菌菌群的一级功能均涉及6个生物代谢通路,均主要为代谢(metabolism)和遗传信息处理(genetic information processing)。
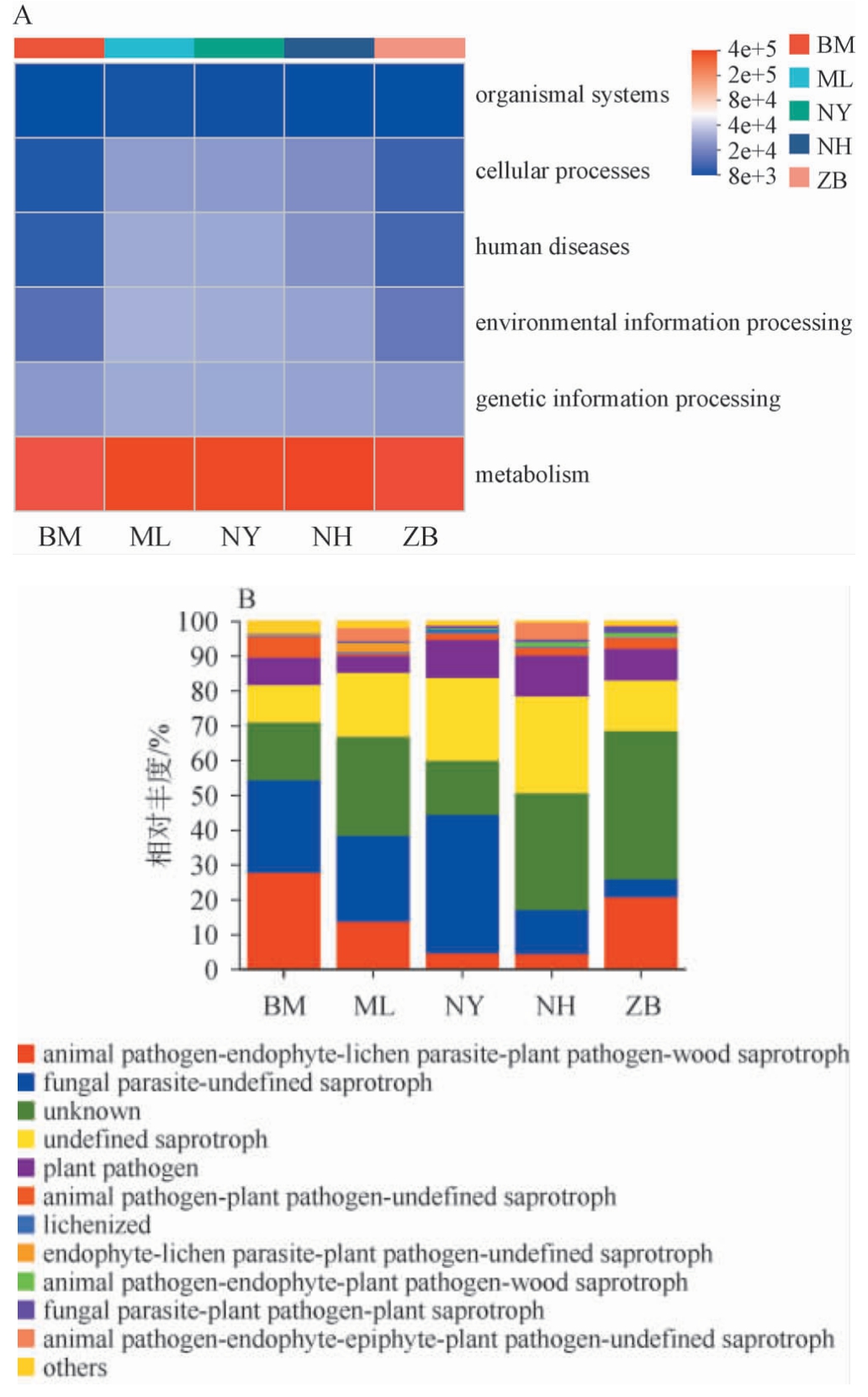
图6 不同产地光核桃果实样品中细菌(A)和真菌(B)功能预测分析结果
Fig. 6 Functional prediction analysis results of bacteria (A) and fungi (B) in Prunus mira fruits samples from different production areas
由图6B可知,BM产地光核桃果实样品中主要富集了动物病原菌-内生真菌-地衣寄生菌-植物病原菌-木质腐生真菌(animal pathogen-endophyte-lichen parasite-plant pathogenwood saprotroph);ML产地光核桃果实样品中主要富集了未定义真菌(unknown)和真菌寄生菌-未定义腐生菌(fungal parasite-undefined saprotroph);NY产地光核桃果实样品中主要富集了真菌寄生菌-未定义腐生菌(fungal parasite-undefined saprotroph);NH产地光核桃果实样品中主要富集了未定义真菌(unknown)和未定义腐生菌(undefined saprotroph);ZB产地光核桃果实样品中主要富集了未定义真菌(unknown)。
3 结论
通过高通量测序结合PCA发现,西藏林芝市不同产地光核桃果实微生物群落多样性及结构差异较为明显,米林市彩门村(ML)样品中细菌及真菌群落多样性最高,校园(NY)光核桃果实样品中细菌菌群丰富度最高,真巴村(ZB)光核桃果实样品中真菌菌群丰富度最高。从不同产地光核桃果实中共注释到18个优势细菌属(相对丰度>1%)和22个优势真菌属,优势细菌属主要为Acinetobacter和Sphingomonas等,优势真菌属主要为Cladosporium、Genole vuria和Filobasidium等。 通过LEfSe共筛选出2个主要差异细菌属和16个主要差异真菌属,不同产地光核桃果实微生物群落组成中指示性类群各不相同。通过微生物群落功能预测分析发现,细菌群落功能类型主要为代谢和遗传信息处理,真菌群落功能类型主要为真菌寄生菌-未定义腐生菌和未定义真菌。不同产地光核桃果实微生物群落结构组成及相对丰度差异较为明显,表明产地环境因素影响光核桃果实微生物群落的结构组成。
[1] 包福海. 光核桃遗传多样性及谱系地理学研究[D] . 呼和浩特:内蒙古农业大学,2024.
[2] 左力旭. 西藏光核桃功效成分及制粉技术研究[D] . 天津:天津科技大学,2019.
[3] 郭其强,罗大庆,王贞红,等. 光核桃幼苗光合特性和保护酶对干旱胁迫的响应[J] . 西北农林科技大学学报(自然科学版),2010,38(6):138-144.
[4] 郝海平,姜闯道,石雷,等. 根系温度对光核桃幼苗光合机构热稳定性的影响[J] .植物生态学报,2009,33(5):984-992.
[5] LUKŠA J,SERVIENE˙E.White mulberry(Morus alba L.)fruit-associated bacterial and fungal microbiota[J] .J Environ Eng Landscape Manage,2020,28(4):183-191.
[6] 闾星. 板栗果实内生菌群及果腐病拮抗细菌筛选[D] . 北京:中国林业科学研究院,2022.
[7] 何萍,王健强,高潭,等. 西藏林芝地区不同品种葡萄果实表皮微生物群落结构组成分析[J] .中国酿造,2022,41(12):144-149.
[8] 姜莉莉,武海斌,宫庆涛,等. 红栗和古栗微生物群落结构及果实养分含量的比较[J] .江西农业学报,2022,34(2):76-81.
[9] 赵宇卓,吴碧波,余朝旭,等. 白枇杷微生物组及其与果实品质的关系[J] .浙江大学学报,2024,50(6):907-919.
[10] 罗冬兰,瞿光凡.基于高通量测序技术研究不同品种桃果实的微生物多样性[J] .包装工程,2022,43(11):140.
[11] 魏丽萍,韩艳英,大布穷,等. 西藏光核桃果实表型性状变异分析与种质资源筛选[J] .北京林业大学学报,2020,42(7):48-57.
[12] 阚金涛,袁雷,钟政昌. 光核桃仁油和蛋白质同步提取工艺优化及油脂品质分析[J] .食品与机械,2020,36(1):210-236.
[13] 钟政昌,王腾飞,方江平. 均匀设计法优化西藏光核桃原果浆保鲜配方[J] .食品科技,2014,39(5):47-52.
[14] 吕健,左力旭,毕金峰,等. 蒸汽热烫预处理对光核桃粉粉体特性、功能因子溶出量及滋味的影响[J] .食品科学,2020,41(22):49-56.
[15] 李媛蓉,张姗姗,曾秀丽.不同贮藏条件对光核桃果实品质的影响[J] .西藏农业科技,2020,42(S1):73-76.
[16] 奉综涛,买地那·帕尔哈提,尹秀,等. 西藏不同地区枸杞果实表皮和叶际微生物多样性研究[J] .中国酿造,2025,44(2):150-157.
[17] 王兴红,边禄森,刘慧慧,等.血红色钉菇菌塘土壤微生物群落多样性[J] .菌物学报,2025,44(6):18-32.
[18] 杨敬敬,韩烁,王霞,等.三倍体毛白杨不同组织内生细菌多样性分析[J] .微生物学通报,2022,49(8):3021-3036.
[19] 罗冬兰,瞿光凡,马超,等.基于高通量测序技术研究不同品种桃果实的微生物多样性[J] .包装工程,2022,43(11):140-146.
[20] 韦新航,周铨,李亚妮,等.生物有机肥对温郁金根际微生物群落结构的影响[J] .浙江农业学报,2025,37(4):892-900.
[21] ASAF S,NUMAN M,KHAN A L,et al.Sphingomonas:From diversity and genomics to functional role in environmental remediation and plant growth[J] .Crit Rev Biotechnol,2020,40(2):138-152.
[22] ZHOU M,LIU Z,WANG J,et al.Sphingomonas relies on chemotaxis to degrade polycyclic aromatic hydrocarbons and maintain dominance in coking sites[J] .Microorganisms,2022,10(6):1109.
[23] ZHANG C, WANG M Y, KHAN N, et al. Potentials, utilization, and bioengineering of plant growth-promoting Methylobacterium for sustainable agriculture[J] .Sustainability,2021,13(7):3941.
[24] 马文清,郭强,黎正英,等.蔗鸭共生对甘蔗根际与非根际土壤微生物群落多样性的影响[J] .南方农业学报,2025,56(1):1-17.
[25] 董锦润,李靖,陈玉惠,等.枝孢属真菌次生代谢产物中化学成分及其生物活性的研究进展[J] .中草药,2021,52(19):6076-6087.
[26] 刘昊,麻仲花,刘威帆,等. 不同耕作方式配施有机肥对盐碱地玉米根际土壤微生物群落的影响[J] . 中国生态农业学报(中英文),2025,33(1):25-39.
[27] FANG Y,WANG Z,SHI Y,et al.Efficient biotransformation of sclareol to sclareolide by Filobasidium magnum JD1025[J] .Appl Biochem Biotech,2023,195(2):1184-1196.
[28] WEI X Y, ZHU H Y, SONG L, et al. Yeast diversity in the Qaidam Basin Desert in China with the description of five new yeast species[J] .J Fungi,2022,8(8):858.