清香型白酒因具有清香柔和、果香宜人和回味爽净的特点,受到了众多消费者的喜爱[1]。作为清香型白酒酿造过程中的糖化发酵剂,低温大曲与蒸煮、摊凉后的高粱混合后,在地缸中密封发酵28 d便可制得酒醅[2],而将酒醅进行蒸馏后便可得到清香型白酒。 由此可见,酒醅品质的好坏直接决定了清香型白酒品质的优劣。
低温大曲由富含碳水化合物的谷物经过自然固态发酵而来[3-5],通常以大麦和豌豆为主要原料。 由于发酵温度较低,低温大曲中大多数微生物都能在最高发酵温度下存活,因而其蕴含微生物类群的丰度和多样性均较高[6],且芽孢杆菌属(Bacillus)、覆膜孢酵母菌属(Saccharomycopsis)和毕赤酵母菌属(Pichia)为其主要群系[7-8]。根据曲块断面表观差异,低温大曲可分为后火曲、清茬曲和红心曲3类[9],其中后火曲的断面中心有浅褐色斑块,清茬曲断面呈青白色且无杂色,红心曲断面中心有红褐色斑点,斑点周围呈浅黄色。CAI W C等[7]的研究发现3种类型低温大曲中的微生物类群存在一定差异,后火曲中显著富集厚壁菌门(Firmicutes)中的细菌,清茬曲中显著富集放线菌门(Actinomycetia)中的细菌,而红心曲中显著富集变形菌门(Proteobacteria)的细菌。在实际生产中3种类型低温大曲通常混合使用,因而积极揭示不同类型低温大曲对酒醅微生物类群和品质的影响,对实际生产中酒曲的使用可能具有指导意义。
本研究分别采集了后火曲、清茬曲和红心曲各10块,按照“清蒸二次清”工艺进行了大茬酒醅的制备,然后采用MiSeq高通量测序技术对3种类型低温大曲发酵的大茬酒醅细菌类群结构进行解析,以期揭示不同类型低温大曲对酒醅细菌类群产生的影响,为清香型白酒酿造过程中酒曲的使用提供理论指导。
1 材料与方法
1.1 材料与试剂
DP302细菌基因组脱氧核糖核苷酸(deoxyribonucleic acid,DNA)提取试剂盒:天根生化科技(北京)有限公司;正/反向引物338F/806R:上海桑尼生物科技有限公司;AxyPre聚合酶链式反应(polymerase chain reaction,PCR)清洁试剂盒:爱思进生物技术(杭州)有限公司;Illumina MiSeq测序试剂盒:美国Illumina公司。
低温大曲:采集自湖北省襄阳市某清香型白酒生产企业;高粱和谷壳:市售。
1.2 仪器与设备
Vetiri PCR梯度基因扩增仪:美国AB公司;Fluor Chem FC3型化学发光凝胶成像系统:美国Protein Simple公司;MiSeq PE300高通量测序平台:美国Illumina公司;R930机架式服务器:美国DELL公司。
1.3 方法
1.3.1 清香型白酒大茬酒醅样品的制备
在湖北省襄阳市某清香型白酒生产企业酿酒车间跟随某一班组,参照以下的工艺流程进行大茬酒醅的制作。

操作要点:首先从制曲车间采集后火曲、清茬曲和红心曲各10块,每块酒曲分别粉碎后各取75 g备用;高粱经粉碎、润糁、入甑蒸煮、出甑和摊凉后,共取30份备用,每份1 650 g,此时高粱含水量约50%;将酒曲与摊凉后的高粱分别进行混合后,装入2.5 L陶坛中;将30个陶罐口用保鲜袋密封后放入地缸中发酵28 d,陶坛间隙用生产用酒醅填充,地缸口盖上塑料布后用水泥板压实;发酵完成后,将陶罐从地缸中取出运送回实验室,在实验室条件下将罐中的酒醅装入无菌自封袋中,置于-40 ℃贮存以便开展后续实验。
1.3.2 样品宏基因组DNA提取、PCR扩增与高通量测序
酒醅中的微生物基因组DNA严格参照DP302提取试剂盒说明书中提供的方法进行提取。使用添加了核苷酸标签的正向引物308F(5'-AGAGTTTGATCCTGGCTCAG-3')和反向引物806R(5'-GGTTACCTTGTTACGACTT-3')对细菌16S rRNA的V3~V4区域进行特性扩增。扩增体系和扩增程序参照文献[10] 并稍作修改。PCR扩增体系:2.5 μL Buffer缓冲液、2 μL脱氧核糖核苷三磷酸(deoxy-ribonucleoside triphosphate,dNTP)、正反引物各0.5 μL、0.5 μL DNA模板、0.5 μL rTaq DNA聚合酶,最后用无菌去离子水补至25 μL。PCR扩增程序:95 ℃预变性5 min;95 ℃变性30 s,55℃退火45s,72℃延伸90s,循环30次;72℃末端延伸10min,4 ℃保存。 使用2%琼脂糖凝胶电泳法检测扩增产物的完整性,然后对PCR产物进行纯化,最后将纯化的PCR产物送至上海美吉生物医药科技有限公司基于MiSeq PE300平台完成测序。
1.3.3 生物信息学分析
本研究基于QIIME(v 1.9.0)平台对下机序列进行生物信息学分析,分析流程参照郭壮等[11]的方法进行,使用两步UCLUST方法进行操作分类单元(operational taxonomic unit,OTU)的划分,使用核糖体数据库项目(ribosomal database project,RDP)(release 18)数据库完成细菌物种的注释[12],基于OTU表及系统发育树的构建,进行α多样性计算。基于主坐标分析(principal co-ordinates analysis,PCoA)和线性判别分析效应大小(linear discriminant analysis effect size,LEfSe)分析进行β多样性分析,采用PICRUSt(phylogenetic investigation of communities by reconstruction of unobserved states)软件对3种类型低温大曲发酵酒醅细菌类群的基因功能进行预测[13]。
1.3.4 数据处理
使用Kruskal-Wallis检验对3种类型低温大曲发酵酒醅细菌类群的α多样性指数和优势细菌属的差异进行显著性分析;使用Origin 2021软件绘制百分堆积柱状图对优势微生物类群相对含量实现可视化;采用R(v 4.3.2)软件绘制散点图和热图分别对三组酒醅的PCoA数据和基因功能预测数据进行可视化,亦采用该软件基于OTU表对三组酒醅进行LEfSe及其数据可视化;使用Spearman秩和检验计算各OTU之间的相关性,然后使用Gephi(v 0.9.2)实现数据可视化。
2 结果与分析
2.1 3种类型低温大曲发酵酒醅细菌类群的α多样性分析
本研究首先基于OTU水平计算了3种类型低温大曲发酵酒醅中细菌类群的Chao1指数和Shannon指数,以评估它们之间的物种丰富度和多样性,结果见图1。
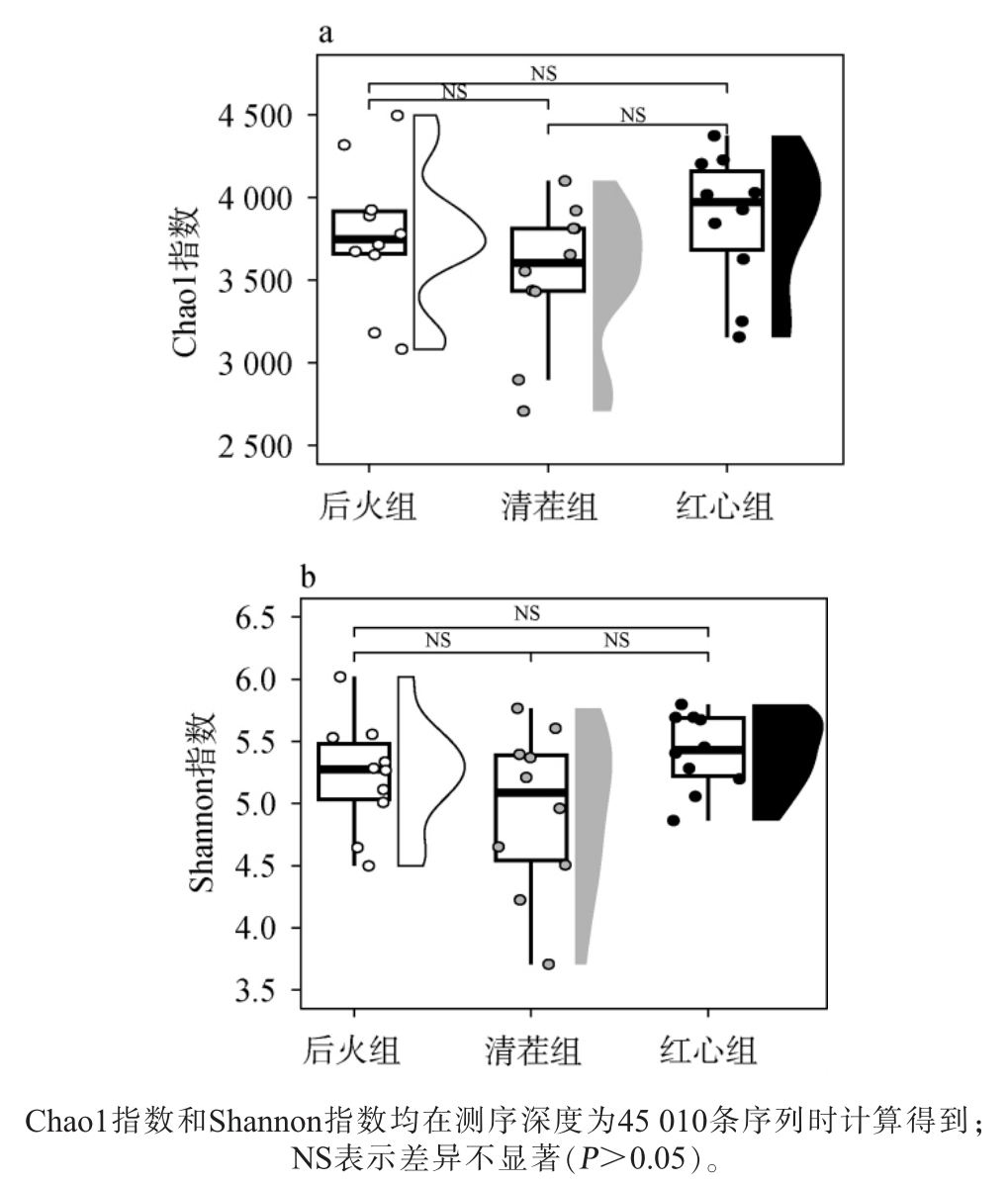
图1 3种类型低温大曲发酵酒醅细菌类群Chao1(a)和Shannon(b)指数比较分析
Fig. 1 Comparative analysis of Chao1 (a) and Shannon (b) indexes of the bacterial communities in fermented grains of 3 types low-temperature Daqu
由图1可知,后火曲、清茬曲和红心曲发酵酒醅细菌类群的平均Chao1指数分别为3 771、3 533和3 866,而Shannon指数分别为5.23、4.94和5.41,经Kruskal-Wallis和检验,3种类型低温大曲发酵酒醅细菌丰度和多样性差异均不显著(P>0.05)。
2.2 基于门和属水平3种类型低温大曲发酵酒醅细菌类群的比较分析
经过测序,本研究共获得1 776 238条16S rRNA基因序列,经过质控过滤掉35 656条低质量序列,余下1 740 582条有效序列,所有有效序列按照97%序列相似度划分到8961个OTU。平均每个样品中含有58 019条序列和1 051个OTU。经过数据库比对,所有有效序列被鉴定到18个门、37个纲、67个目、118个科和197个属,分别有0.03%和2.51%未鉴定到门和属水平。本研究将平均相对含量>1.0%的细菌门和细菌属定义为优势细菌门和细菌属,并采用Kruskal-Wallis检验对三组酒醅中相对含量存在显著差异的优势细菌属进行甄别(P<0.05),结果见图2。
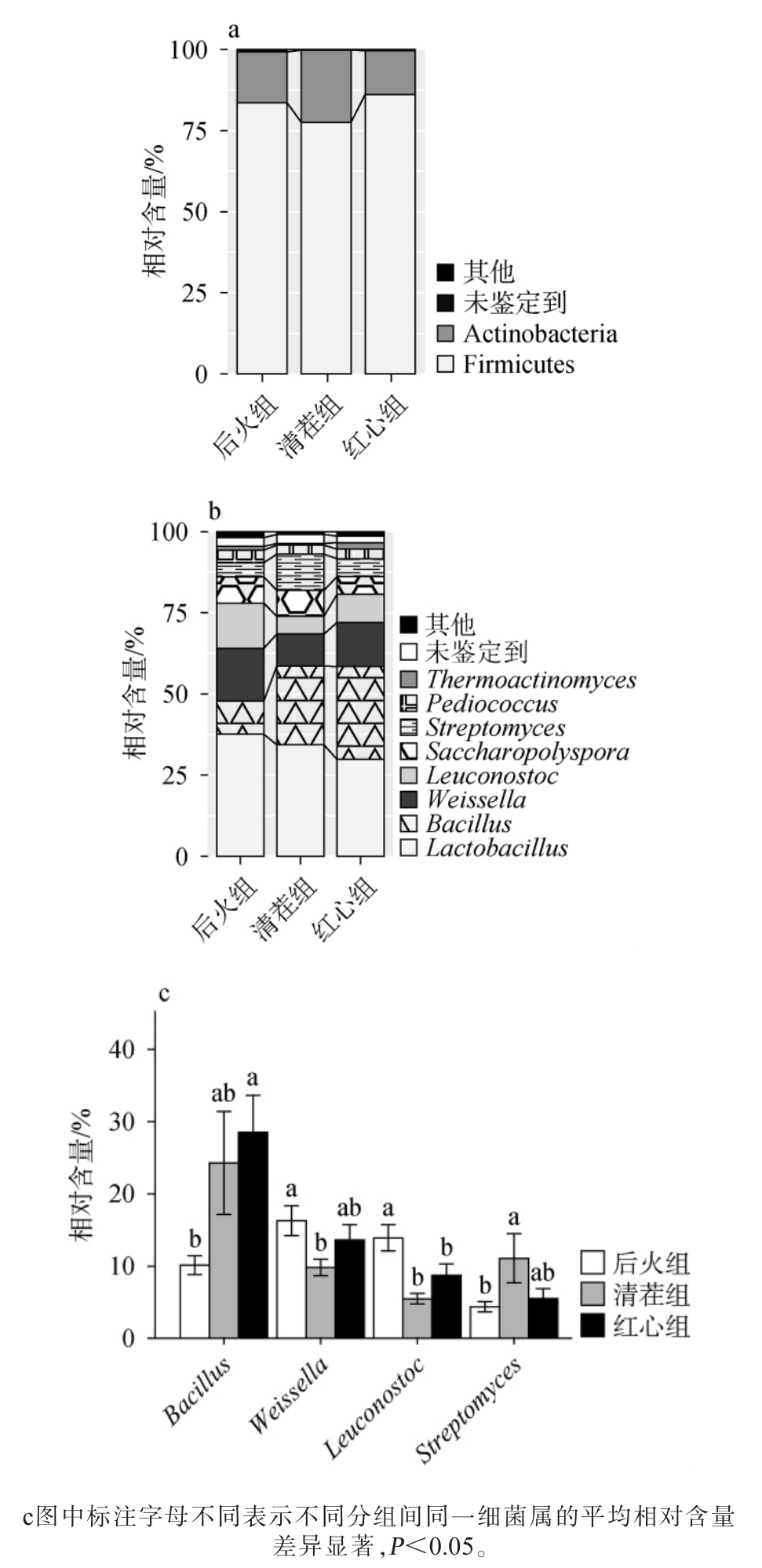
图2 3种类型低温大曲发酵酒醅中优势细菌门(a)、优势细菌属(b)和差异优势细菌属(c)分析
Fig. 2 Analysis of dominant bacterial phyla (a), dominant bacterial genera (b), and differential dominant bacterial genera (c) in the fermented grains of 3 types low-temperature Daqu
由图2(a)可知,3种类型低温大曲发酵酒醅中共含有2个优势细菌门,分别为厚壁菌门(Firmicutes)和放线菌门(Actinobacteria),平均相对含量分别为82.46%和17.14%。经Kruskal-Wallis检验发现,其在不同分组间差异均不显著(P>0.05)。
由图2(b)可知,3种类型低温大曲发酵酒醅中共含有8个优势细菌属,分别为乳酸杆菌属(Lactobacillus)、芽孢杆菌属(Bacillus)、魏斯氏菌属(Weissella)、明串珠菌属(Leuconostoc)、糖多孢菌属(Saccharopolyspora)、链球菌属(Streptomyces)、片球菌属(Pediococcus)和高温放线菌属(Thermoactinomyces),平均相对含量分别为33.93%、20.99%、13.24%、9.36%、7.16%、7.01%、3.19%和1.22%。值得注意的是,Lactobacillus、Weissella、Leuconostoc 和Pediococcus 都属于乳酸菌类群,累计相对含量达59.72%。 先前已有许多研究表明乳酸菌类群是清香型白酒酒醅中丰度较高的微生物类别之一[14-16]。 乳酸菌代谢产生的乳酸能够使酒体风味更加柔和,同时乳酸的积累对乙酸乙酯等风味物质的产生亦有一定的积极影响[17]。此外,芽孢杆菌通常在清香型白酒酒醅的细菌中也占有一定比例[18-19]。
由图2(c)可知,经Kruskal-Wallis检验发现,后火曲发酵酒醅中Weissella和Leuconostoc的相对含量显著高于清茬曲发酵酒醅(P<0.05),它们在后火曲发酵酒醅中的平均相对含量分别为16.30%和13.92%,而在清茬曲发酵酒醅中分别仅为9.81%和5.47%。 清茬曲发酵酒醅中Streptomyces的相对含量显著高于后火曲发酵酒醅(P<0.05),其在清茬曲发酵酒醅中的平均相对含量为11.40%,而在后火曲发酵酒醅中仅为4.38%。红心曲发酵酒醅中的Bacillus相对含量显著高于后火曲发酵酒醅(P<0.05),其在红心曲发酵酒醅中的平均相对含量为28.53%,在后火曲发酵酒醅中仅为10.15%。由此可见,后火曲发酵酒醅中乳酸菌含量相对偏高,而红心曲发酵酒醅中Bacillus相对偏高。
LI Z J等[20]研究发现,Bacillus的含量在酒醅发酵初期较高,随着发酵的进行,Lactobacillus的含量逐渐升高并占据主导地位,究其原因可能与大曲和酒醅的发酵环境差异有关。大曲发酵环境较为开放,氧含量高,更适宜以Bacillus为代表的好氧菌生长[21]。然而,酒醅在密封的地缸中发酵,随着发酵氧气逐渐被消耗殆尽,变为更适宜厌氧或兼性厌氧的乳酸菌类群生长[22]。因此,酒醅中的优势菌群以乳酸菌类群居多。
2.3 基于OTU水平3种类型低温大曲发酵酒醅核心细菌类群的分析
本研究从OTU水平上探究了3种类型低温大曲发酵酒醅中的核心细菌类群。 经统计,在所有样品中均存在的OTU有220个,本研究将这些OTU定义为核心OTU。 核心OTU的分类学地位及其相对含量统计见表1。
表1 3种类型低温大曲发酵酒醅细菌核心操作分类单元的分类学地位及其相对含量分析
Table 1 Analysis of the taxonomic status and relative content of the bacterial core operational taxonomic unit in the fermented grains of 3 types low-temperature Daqu
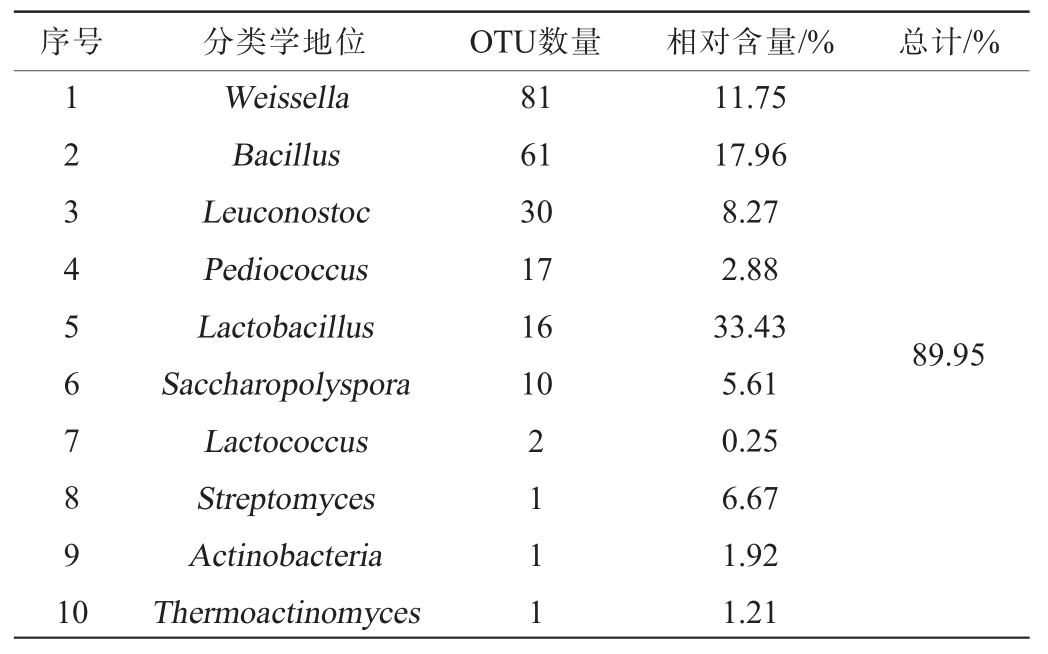
序号分类学地位OTU数量相对含量/%总计/%1234567891 0 Weissella Bacillus Leuconostoc Pediococcus Lactobacillus Saccharopolyspora Lactococcus Streptomyces Actinobacteria Thermoactinomyces 81 61 30 17 16 10 89.95 2111 11.75 17.96 8.27 2.88 33.43 5.61 0.25 6.67 1.92 1.21
由表1可知,220个核心OTU被鉴定到了9个细菌属和1个细菌门,总计相对含量达89.95%。 其中,有81个、61个、30个、17个、16个和10个核心OTU分别被鉴定为Weissella、Bacillus、Leuconostoc、Pediococcus、Lactobacillus 和Saccharopolyspora,平均相对含量为11.75%、17.96%、8.27%、2.88%、33.43%和5.61%,累计平均相对含量达79.90%。 由此可见,3种类型低温大曲发酵的酒醅中近90%的细菌菌群是相似的,且主要为乳酸菌和芽孢杆菌。
2.4 3种类型低温大曲发酵酒醅细菌类群的β多样性分析
本研究进一步通过PCoA和LEfSe对3种类型低温大曲发酵酒醅细菌的β多样性展开了分析。LEfSe分析中的线性判别分析(linear discriminant analysis,LDA)模型能够计算出各组之间差异的统计显著性和效果大小,结果用LDA得分表示,LDA得分越高,表示该特征在区分不同组别的作用越明显,结果见图3。
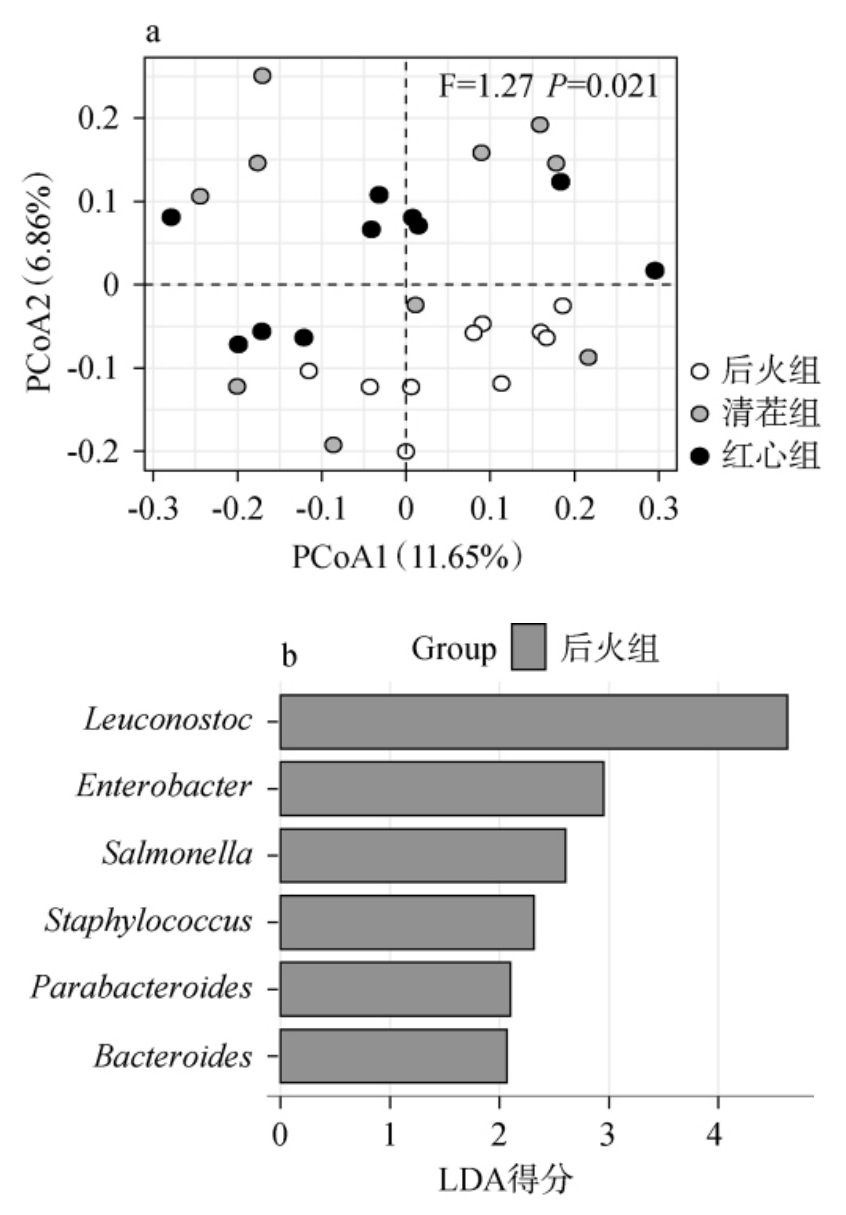
图3 基于主坐标分析(a)和线性判别分析效应大小(b)分析的3类低温大曲发酵酒醅细菌群落结构分析
Fig. 3 Bacterial community structure analysis of fermented grains of 3 types low-temperature Daqu based on principal coordinate analysis (a) and linear discriminant analysis effect size (b)analysis
由图3(a)可知,在二维空间结构中,后火曲和红心曲发酵酒醅的样本呈现明显的分离趋势,前者主要集中在一三象限对角线的下方,而后者主要集中在一三对角线的上方。清茬曲发酵酒醅样本则较为分散的排布在二维空间中,并与其他两组样品分布区域有一定的重叠。 由此可见,后火曲和红心曲发酵酒醅细菌群落结构存在明显差异,而两者与清茬曲发酵酒醅的差异均不明显。
由图3(b)可知,当LDA得分>2时,仅有后火曲发酵酒醅中存在生物标志物,分别为Leuconostoc、肠杆菌属(Enterobacter)、沙门氏菌属(Salmonella)、葡萄球菌属(Staphylococcus)、副拟杆菌属(Parabacteroides)和拟杆菌属(Bacteroides)。 Enterobacter、Salmonella、Parabacteroides和Bacteroides在样品中的含量很低(不足0.1%),它们大多在有关人或动物肠道微生物的研究中被报道[23-25],而在有关酒醅微生物的研究中鲜有报道,可能是环境或原料中有少量携带所导致的。值得注意的是,Leuconostoc的LDA得分>4,同时2.2部分的结果显示后火组酒醅中的Leuconostoc相对含量显著偏高(P<0.05)。因此,后火组酒醅中最重要的生物标志物是Leuconostoc,且该组中的低丰度菌群相较其他两组较为不同。
2.5 3种类型低温大曲发酵酒醅细菌的基因功能预测分析
本研究进一步使用PICRUSt软件对3类低温大曲发酵酒醅中细菌的基因功能进行了预测,经过与蛋白质直系同源簇数据库(clusters of orthologous groups of proteins,COG)比对,共预测到了4 792个COG,除去一般功能和未知功能外,共注释到21个功能大类,结果见图4。
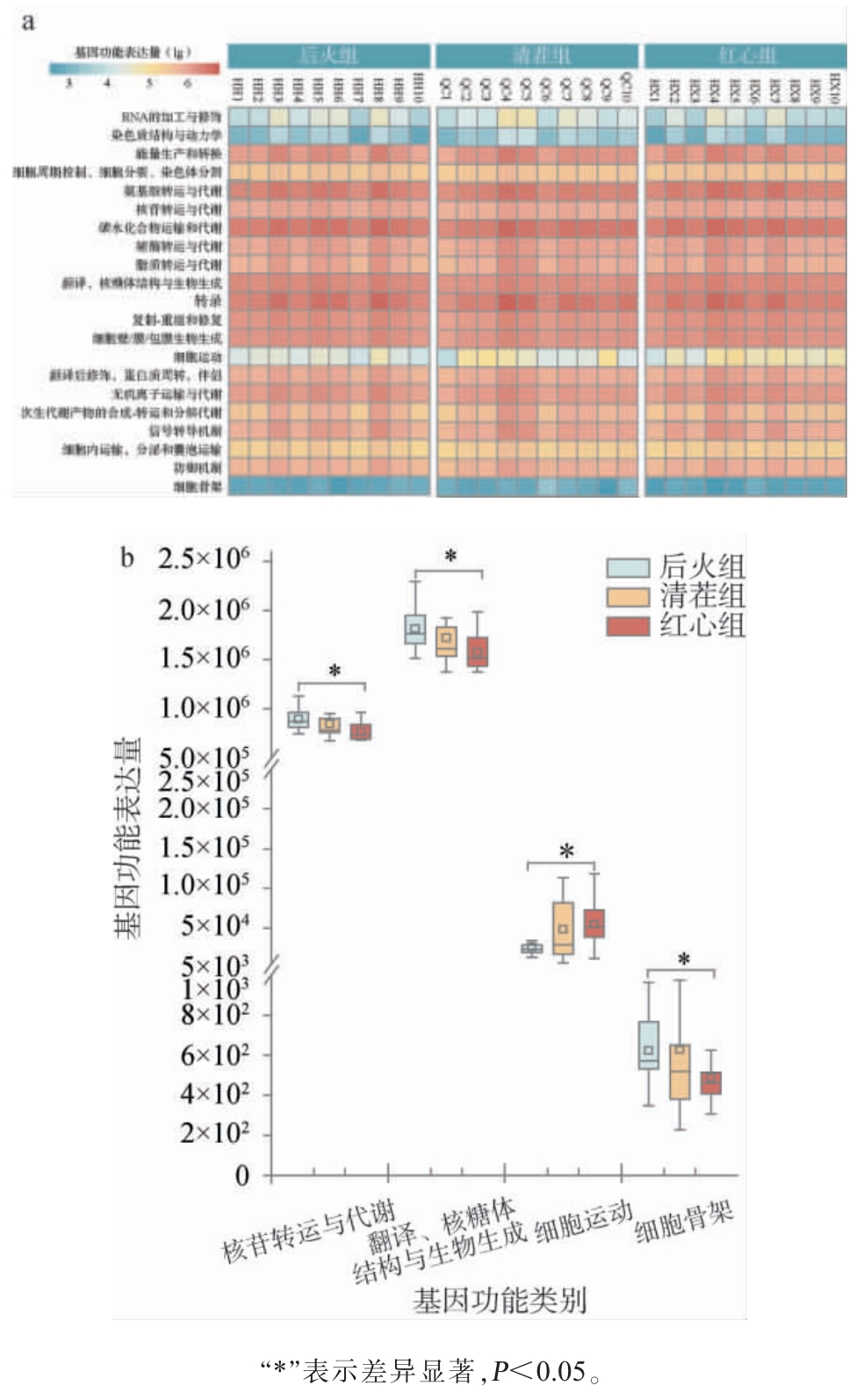
图4 3类低温大曲发酵酒醅细菌类群基因功能预测类别(a)及其差异类别(b)
Fig. 4 Predicted categories (a) and differential categories (b) of gene function of bacterial communities in fermented grains of 3 types low-temperature Daqu
由图4(a)可知,3类低温大曲发酵酒醅在氨基酸转运与代谢、碳水化合物转运与代谢和转录功能上具有较高表达,这间接表明在酒醅发酵过程中菌群进行了活跃的物质代谢活动。由图4(b)可知,经Kruskal-Wallis检验发现,后火曲发酵酒醅的细菌类群在核苷转运与代谢、翻译和核糖体结构与生成以及细胞骨架功能上的表达显著高于红心曲(P<0.05),而红心曲发酵酒醅菌群中的细胞运动功能上的表达显著高于后火曲(P<0.05)。
2.6 3种类型低温大曲发酵酒醅细菌类群的共现网络分析
本研究采用Spearman秩和检验计算了各OTU之间的相关性,并将相关性系数|r|>0.7并且显著相关(P<0.05)的关系定义为具有强相关关系,基于强相关关系构建了3种类型低温大曲发酵酒醅中细菌菌群的共现网络分析,结果见图5。
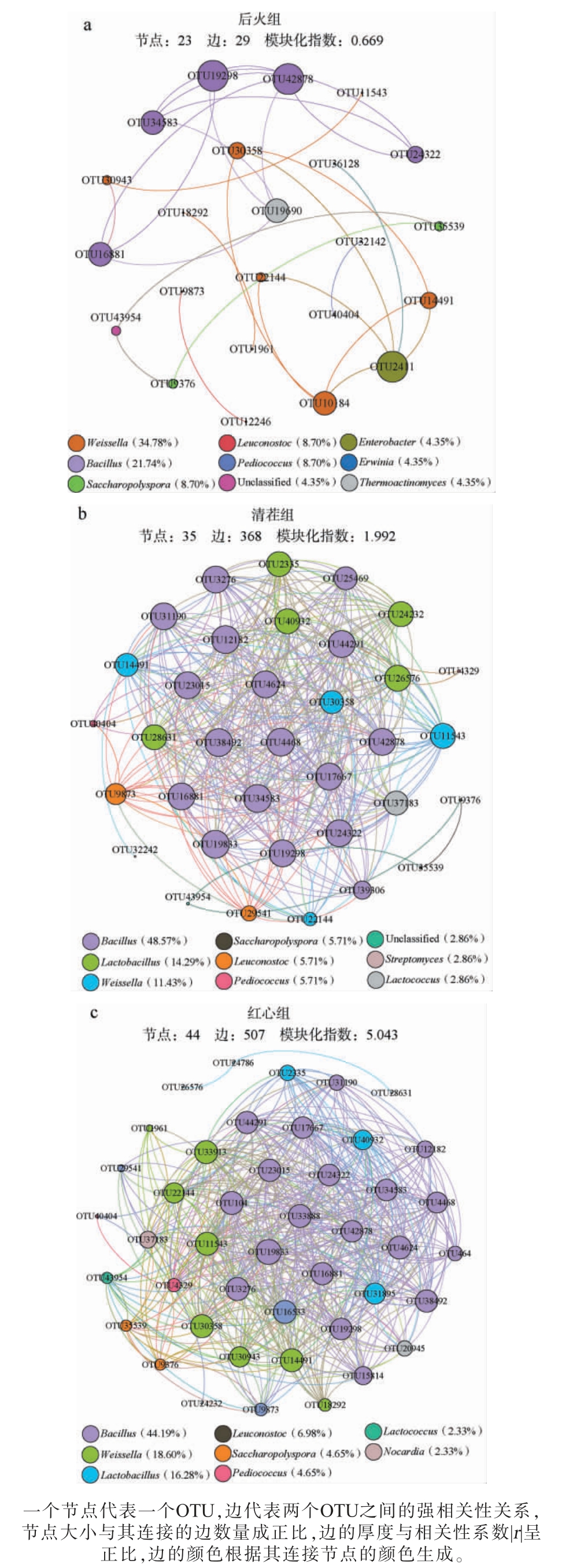
图5 3种类型低温酒曲发酵酒醅中细菌菌群共现网络分析
Fig. 5 Co-occurrence network analysis of bacterial communities in fermented grains of 3 types low-temperature Daqu
由图5可知,3类低温大曲发酵酒醅的细菌共现网络分析的模块化指数均>0.44,因此它们均具有模块化结构。后火曲发酵酒醅的细菌共现网络由23个OTU组成,它们主要隶属于Weissella、Bacillus、Saccharopolyspora、Leuconostoc和Pediococcus。 清茬曲发酵酒醅的细菌共现网络由35个OTU组成,它们主要隶属于Bacillus、Lactobacillus、Weissella、Saccharopolyspora、Leuconostoc和Pediococcus。 红心曲发酵酒醅的细菌共现网络由44个OTU组成,它们主要隶属于Bacillus、Weissella、Lactobacillus、Leuconostoc、Saccharopolyspora和Pediococcus。
由图5亦可知,后火曲、清茬曲和红心曲发酵酒醅的共现网络分析中分别含有29、368和507对强相关性关系。 由此可见,红心曲发酵酒醅细菌菌群间的相互作用最强,清茬曲次之,后火曲最弱。 导致这一结果的原因可能是后火曲发酵酒醅中乳酸菌含量偏高,它们代谢产生的有机酸积累会导致酒醅内环境pH值偏低,同时部分物种还可能产生细菌素,对其他物种产生抑制作用,从而削弱了菌群之间的相互作用[26-28]。 SELTEN G等[29]对涉及植物根系的9项合成微生物群落研究进行了荟萃分析,结果发现根系群落经常聚集成两种不同的功能状态,而这些状态的特征是Bacillus丰度的差异,这可能是受到群体感应和生物膜形成等微生物相互作用机制的驱动,同时也受到分泌物和免疫反应影响。在本研究中清茬组和红心组酒醅中Bacillus相对偏高,且共现网络分析中隶属于Bacillus的OTU占比最高,这或许是它们菌群间相互作用较强的原因之一。
3 结论
本研究使用后火曲、清茬曲和红心曲3类低温大曲在相同条件下制作了清香型白酒大茬酒醅,并采用MiSeq高通量测序技术对3类大曲发酵的大茬酒醅细菌类群进行了解析。结果表明,后火曲、清茬曲和红心曲发酵的大茬酒醅细菌丰富度和多样性等α多样性指标没有明显差异,且近90%的细菌菌群在3组酒醅中均存在,这些菌群主要包括Weissella、Leuconostoc、Pediococcus、Lactobacillus和Lactococcus等乳酸菌类群和Bacillus。尽管微生物类群存在高度相似性,但不同类型低温大曲发酵酒醅中的细菌在群落结构和基因功能方面仍存在明显差异,后火曲发酵酒醅中乳酸菌含量相对偏高,而红心曲发酵酒醅中Bacillus含量相对偏高,且红心曲发酵酒醅细菌菌群间的相互作用最强。
[1] KANG J,HU Y,JIA L,et al.Response of microbial community assembly and succession pattern to abiotic factors during the second round of lightflavor Baijiu fermentation[J] .Food Res Int,2022,162(12):111915.
[2] PANG X N,HUANG X N,CHEN J Y,et al.Exploring the diversity and role of microbiota during material pretreatment of light-flavor Baijiu[J] .Food Microbiol,2020,91(10):103514.
[3] DU H, WANG X S, ZHANG Y H, et al. Exploring the impacts of raw materials and environments on the microbiota in Chinese Daqu starter[J] .Int J Food Microbiol,2019,297(5):32-40.
[4] ZHENG X W, TABRIZI M R, NOUT M J R, et al. Daqu-a traditional Chinese liquor fermentation starter[J] .J I Brewing,2011,117(1):82-90.
[5] LI H D,LIU S Y,LIU Y B,et al.Functional microorganisms in Baijiu Daqu:Research progress and fortification strategy for application[J] .Front Microbiol,2023,14(1):1119675.
[6] HU Y N,HUANG X N,YANG B,et al.Contrasting the microbial community and metabolic profile of three types of light-flavor Daqu[J] .Food Biosci,2021,44(12):101395.
[7] CAI W C, WANG Y R, NI H, et al. Diversity of microbiota, microbial functions,and flavor in different types of low-temperature Daqu[J] .Food Res Int,2021,150(12):110734.
[8] XIANG F S,CAI W C,HOU Q C,et al.Comparative analysis of the microbial community structure in light-flavor Daqu in Taiyuan and Suizhou regions,China[J] .LWT-Food Sci Technol,2023,177(3):114599.
[9] HOU Q C,WANG Y R,CAI W C,et al.Metagenomic and physicochemical analyses reveal microbial community and functional differences between three types of low-temperature Daqu[J] .Food Res Int,2022,156(6):111167.
[10] 王生艳,孙亮霞,赵新民,等. 中高温大曲发酵过程中曲皮、曲心微生物群落的差异性和变化规律[J] .中国酿造,2024,43(11):92-98.
[11] 郭壮,葛东颖,尚雪娇,等.退化和正常窖泥微生物多样性的比较分析[J] .食品工业科技,2018,39(22):93-98.
[12] MAIDAK B L, COLE J R, LILBURN T G, et al. The RDP (ribosomal database project)continues[J] .Nucleic Acids Res,2000,28(1):173-174.
[13] AGRAWAL S, KINH C T, SCHWARTZ T, et al. Determining uncertainties in PICRUSt analysis-An easy approach for autotrophic nitrogen removal[J] .Biochem Eng J,2019,152(12):107328.
[14] LUO L J,SONG L,HAN Y,et al.Microbial communities and their correlation with flavor compound formation during the mechanized production of light-flavor Baijiu[J] .Food Res Int,2023,172(10):113139.
[15] TANG J,LIN B,SHAN Y,et al.Effects of sorghum varieties on microbial communities and volatile compounds in the fermentation of lightflavor Baijiu[J] .Front Microbiol,2024,15(7):1421928.
[16] 赵微,赵璇,崔美林,等. 清香型白酒酒醅中乳酸高产菌株的筛选及乳酸的分离纯化[J] .中国酿造,2022,41(6):63-68.
[17] 谢再斌,常煦,何国庆,等.清香型白酒酿造过程中功能微生物及应用研究[J] .中国酿造,2024,43(7):27-32.
[18] HUANG X N, FAN Y, LU T, et al. Composition and metabolic functions of the microbiome in fermented grain during light-flavor Baijiu fermentation[J] .Microorganisms,2020,8(9):1281.
[19] HUANG Q,LIU Y,HE Z J,et al.Environmental temperature variations drive the changes of microbial communities to affect Baijiu flavor quality:Case study of Qingxiangxing Baijiu[J] .Food Biosci,2024,59(6):104064.
[20] LI Z J,FAN Y,HUANG X N,et al.Microbial diversity and metabolites dynamic of light-flavor Baijiu with stacking process[J] . Fermentation,2022,8(2):67.
[21] LIANG F,ZHONG Z M,MA M Y,et al.Effect of storage on microbioa and enzyme proteomic profile of low-temperature Daqu[J] .Food Biosci,2024,59(6):104242.
[22] CAI W C,WANG Y R,LIU Z J,et al.Depth-depended quality comparison of light-flavor fermented grains from two fermentation rounds[J] .Food Res Int,2022,159(9):111587.
[23] SERINO M.Molecular paths linking metabolic diseases,gut microbiota dysbiosis and enterobacteria infections[J] .J Mol Biol,2018,430(5):581-590.
[24] GALÁN-RELAẼO Á,VALERO DÍAZ A,HUERTA LORENZO B,et al.Salmonella and salmonellosis:An update on public health implications and control strategies[J] .Animals,2023,13(23):3666.
[25] WEXLER A G,GOODMAN A L.An insider's perspective:Bacteroides as a window into the microbiome[J] .Nat Microbiol,2017,2(5):1-11.
[26] IBRAHIM S A,AYIVI R D,ZIMMERMAN T,et al.Lactic acid bacteria as antimicrobial agents:Food safety and microbial food spoilage prevention[J] .Foods,2021,10(12):3131.
[27] ROSS R P,MORGAN S,HILL C.Preservation and fermentation:past,present and future[J] .Int J Food Microbiol,2002,79(1-2):3-16.
[28] BISHT V,DAS B,NAVANI N K.Bacteriocins sourced from traditional fermented foods for ensuring food safety:the microbial guards[J] .J Sci Food and Agr,2024,2024(11):1-15.
[29] SELTEN G,DE JONGE R.Bacillus drives functional states in synthetic plant root bacterial communities[J] .Genome Biology,2025,26(1):270.