作为人类最早掌握的生物转化技术之一,酿酒技术见证了中国历史文明的进程[1]。 在中国特有的发酵食品体系中,白酒以其历史悠久的酿造传统,构建起独特的微生物发酵体系。特别是作为中国四大基础香型之一的酱香型白酒,其历史渊源可追溯至西汉武帝时期“枸酱酒”的酿造记载[2]。 酱香型白酒在开放式自然发酵环境中,以优质糯高粱为核心原料,通过细菌、霉菌、酵母菌等微生物群落的协同作用,历经传统固态发酵、蒸馏、窖藏、勾调等多重工序,最终形成“香气馥郁、醇厚绵长”的独特风格[3],其酿造工艺可浓缩为“四高两长,一大一多”。 酱香型白酒酿造工艺流程如下:
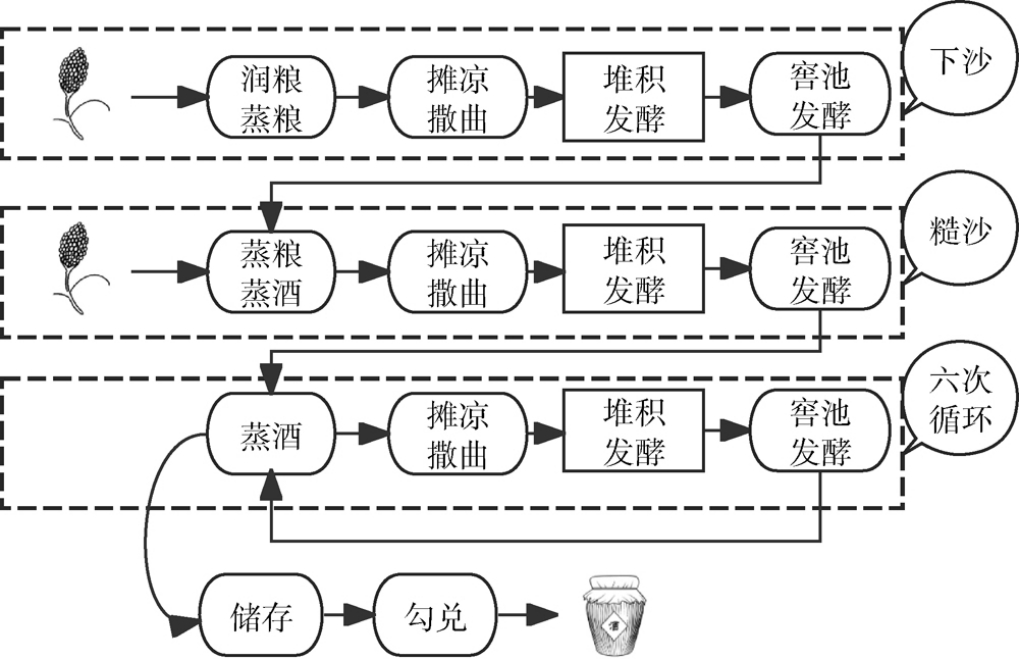
高温堆积发酵是酱香型白酒区别于其他香型白酒的核心技术。 由于在制曲过程中极端温度环境对产糖化酶、酯化酶等的常规菌群形成选择性抑制,导致曲药中酿酒功能微生物相对匮乏,酒醅在窖池发酵阶段的产酒、生香无法顺利完成[4-5]。而高温堆积发酵工艺将蒸煮糊化的酒醅与高温大曲混合堆积,通过开放式发酵对原料、工具以及生产环境中微生物的网罗和富集,实现微生物群落的动态重构,最终形成酱香型白酒独有的微生物菌群,对酱香型白酒风味物质及其前提物质的生成至关重要[6],因此该工艺也被誉为“二次制曲”。本文综述了酱香型白酒多轮次堆积发酵过程微生物群落的来源特征及其动态演变规律、核心功能微生物的种类及其在酿造过程中的关键作用,同时总结和展望了未来酱香型白酒高温堆积发酵过程微生物研究的多样性,以期为深入理解酱香型白酒堆积发酵微生物的作用机制及其对酱香型白酒特征风味的形成贡献提供理论参考。
1 微生物群落来源及其演替规律
1.1 微生物群落主要来源
酱香型白酒的酿造高度依赖高温堆积发酵这一核心环节。 在此过程中,通过创造特定的温度、湿度条件,能够高效富集并整合来自原辅料、生产器具表面、空气介质以及周边环境中的各类微生物资源。 研究表明,堆积发酵体系的细菌类群主要来源于大曲,并通过空气等介质定植于工具表面;而酵母菌群则通过场地内散落的谷物原料、曲粉颗粒及糖类物质实现快速增殖,经工人翻拌等操作被裹挟进入酒醅,并在堆积发酵状态下实现扩增[7]。酱香型白酒堆积发酵过程微生物群落来源见图1。
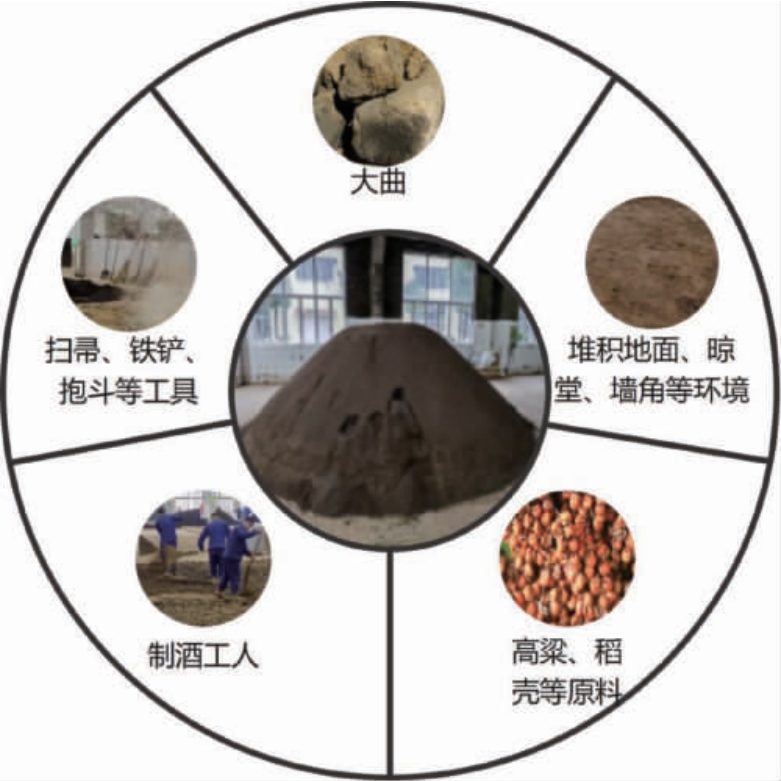
图1 酱香型白酒堆积发酵过程微生物群落来源
Fig. 1 Source of microbial community during accumulation fermentation process of sauce-flavor Baijiu
所谓“曲是酒之骨”,高温大曲在酱香型白酒酿造的菌种供应方面起着十分重要的作用。高温大曲的主要优势菌群微生物包括醋酸杆菌属(Acetobacter)、乳酸杆菌属(Lactobacillus)、芽孢杆菌属(Bacillus),并伴生极少的酵母菌、放线菌和霉菌等菌种[8]。另外,由于大曲制备过程为高温、高湿环境,在这种环境中,细菌种群数量在大曲制备过程中会出现增加的趋势;相反地,酵母菌等受温度影响会逐渐减少。大曲微生物特有的变化规律使其成为输送大量功能细菌到堆积酒醅内从而作用于后续发酵的强大驱动力。吴成等[9]研究结果表明,高温放线菌属、嗜热芽孢杆菌属、嗜热真菌属、曲霉菌属及丝衣霉属构成了高温大曲中的主导菌群。而且在糙沙轮次发酵开始时就能检测出上述特定种类的菌群,说明酱香型白酒堆积发酵体系的部分重要优势菌种直接来自于高温大曲。 除生产用曲外,生产环境作为堆积酒醅功能微生物的另一来源也不容忽视。 有研究表明,酱香型白酒堆积发酵过程的酵母类真菌主要来源于堆积发酵区的地面环境,如堆积场地、晾堂等地表[10]。 张红霞[11]运用贝叶斯概率模型SourceTracker软件溯源堆积酒醅微生物,研究发现大曲是堆积酒醅细菌类微生物的主要来源,占比高达95.6%,包括乳杆菌(1.75%)、海洋杆菌(14.60%)、芽孢杆菌(16.54%)、克罗彭斯特菌(21.07%)、枝芽孢杆菌(29.26%);对于堆积发酵体系的真菌来说,室内地面为真菌来源中心,其所提供的发酵体系真菌比例为49.6%,其中毕赤酵母为33.02%,酿酒酵母为4.77%。 ZHU A R等[12]用SourceTracker软件解析酱香型白酒一轮次堆积糟醅优势微生物的来源。研究表明,堆积过程糟醅中优势微生物主要来源于堆积地面、生产器具和窗台墙壁等物体表面,且糟醅中微生物来源随着堆积发酵时间不断变化。在堆积初期,地面微生物贡献率为32.44%~57.37%,生产器具贡献率为26.89%~50.74%微生物;堆积发酵6 d后微生物又主要来源于窗台墙壁等物体表面,其微生物贡献率为91.96%~94.91%。其他的环境类别包括制酒原料、水资源以及制酒工人等也是大量微生物载体,这些载体所携带的微生物也在通过空气传播、接触沾染等方式持续向发酵体系引入新的菌种资源。由此可见,酱香型白酒堆积发酵阶段的微生物区系主要由大曲接种与生产环境双重因素共同塑造,大曲和酿造环境的共同作用形成了酱香型白酒高温堆积发酵过程的丰富微生物菌系。
1.2 微生物群落变化规律
酱香型白酒堆积发酵过程的微生物群落主要由产各种酶与酱味物质的细菌[13]、提供糖化动力的丝状真菌[14]、产酒产香的酵母菌[15]和产次生代谢产物调控酿造微生态的放线菌[16]四大菌群组成。 在堆积发酵的初期,细菌群体数量最多、酵母菌群体数量高于霉菌数量、放线菌群体数量最少。随着堆积发酵进行,酒醅温度逐渐升高,当温度达到50 ℃左右,酒醅中真菌和细菌受温度抑制,数量开始减少。山其木格等[17]运用变性梯度凝胶电泳(denatured gradient gel electrophoresis,DGGE)技术对酱香型白酒堆积发酵糟醅中的微生物种群动态进行了系统性研究。结果表明,下沙轮次酒醅微生物组成比较简单,耐酸乳杆菌、乳酸片球菌及巴氏醋杆菌等为优势细菌,真菌仅检出白地霉与发酵毕赤酵母;进入糙沙期后,堆醅微生物多样性显著提升,新增面包乳杆菌、芽孢杆菌属、枝芽孢杆菌属等细菌类群,同时出现嗜酒假丝酵母、亚硝酸对粟酒裂殖酵母菌和酿酒酵母等真菌;至一轮次发酵时,新检测到Tsukamurella spumae、Acetobacter nitrogenifigens、Thermoactinomyces sanguinis等细菌属;二轮次堆醅细菌多样性达最高峰,新增苜蓿中华根瘤菌和直杆糖多孢菌,此时真菌群落趋于稳定,主要由假丝酵母、毕赤酵母、粟酒裂殖酵母菌及酿酒酵母构成;三轮次与四轮次堆醅细菌多样性保持平稳;而五轮次、六轮次堆醅的微生物多样性则呈现轻微下降趋势。
由此可知,酱香型白酒各轮次堆积过程微生物的组成不尽相同,同时这也反映了堆积发酵过程中微生物的多样性。不同轮次酱香型白酒堆积发酵过程中微生物群落变化规律见表1。由表1可知[18-28],基于前文所述堆积发酵微生物的来源,由于大部分细菌来源于高温大曲能够耐受堆积高温,而真菌属微生物主要来源于生产场地及酿造环境受温度抑制,导致细菌属微生物多样性大于真菌属微生物多样性。随着堆积发酵的进行,优势细菌魏斯氏菌属、乳酸杆菌属等相对丰度逐渐降低,于后续轮次转变为醋酸杆菌属;优势真菌由拟青霉属、威克汉姆酵母属等逐渐转变为假丝酵母属和嗜热真菌属,反映了酱香型白酒堆积发酵过程微生物群落结构及其动态变化。
表1 酱香型白酒堆积发酵过程微生物群落变化规律
Table 1 Changes in microbial community during accumulation fermentation process of sauce-flavor Baijiu
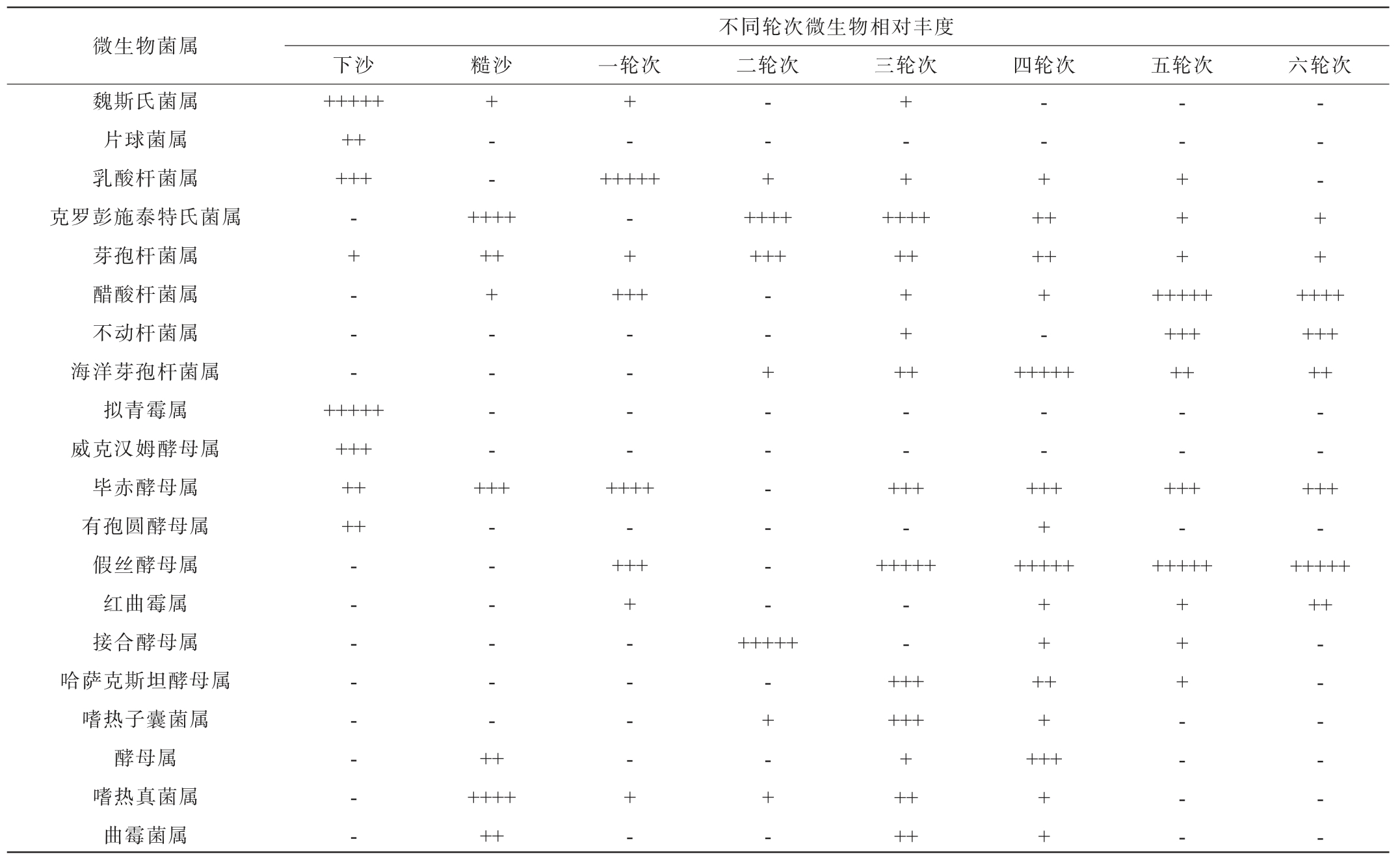
注:“-”表示相对丰度0~5%,“+”表示相对丰度5%~10%,“++”表示相对丰度10%~20%,“+++”表示相对丰度20%~30%,“++++”表示相对丰度30%~40%,“+++++”表示相对丰度40%~100%。
微生物菌属魏斯氏菌属片球菌属乳酸杆菌属克罗彭施泰特氏菌属芽孢杆菌属醋酸杆菌属不动杆菌属海洋芽孢杆菌属拟青霉属威克汉姆酵母属毕赤酵母属有孢圆酵母属假丝酵母属红曲霉属接合酵母属哈萨克斯坦酵母属嗜热子囊菌属酵母属嗜热真菌属曲霉菌属不同轮次微生物相对丰度下沙糙沙一轮次二轮次三轮次四轮次五轮次六轮次+++++++++++--+-+++++--++-+-+---++++++-++++++++++++++--+++++--+++---++----+----+++--+------++++-+++++++++++++++++++++++++++++++++++++--------+++--------------++++++-++++++-+++++++++++++++++-++++++----+-+++-++++++++++++--++++++++++++++-+-+-++++++++++++++++----------
虽然堆积过程微生物群落结构在组成上存在差异,但是各个轮次之间仍然具有共同的优势微生物类群。具体而言,海洋芽孢杆菌属、乳酸杆菌属、克罗彭斯特菌属和芽孢杆菌属等优势细菌属与毕赤酵母属、假丝酵母属、和嗜热真菌属等优势真菌属微生物在不同轮次堆积发酵过程都发挥着关键作用,持续推动着酱香型白酒堆积发酵的高效进行。
2 主要功能微生物及其作用
2.1 细菌
细菌为堆积发酵过程提供了α-淀粉酶、糖化酶、脂肪酶、蛋白酶等各种水解酶类,能够在高温条件下分解酿造原料中的淀粉、蛋白质等物质从而产生酯类、醛类、酚类等挥发性风味物质,因此细菌是酱香型白酒堆积发酵过程中香味物质的主要来源。酱香型白酒堆积发酵过程中酒醅常见细菌以芽孢杆菌属、醋酸杆菌属、乳酸杆菌属等为主。
芽孢杆菌具有独特的耐热机制,能够耐受堆积发酵过程的高温,因此芽孢杆菌在堆积发酵过程中数量最多,种类最为丰富,是堆积发酵过程的绝对优势菌。 有研究者发现,芽孢杆菌具有较为出色的产香能力,其是产四甲基吡嗪(tetramethylpyrazine,TTMP)的优势菌株,包括地衣芽孢杆菌(Bacilluslicheniformis)[1]、短小芽孢杆菌(Bacilluspumilus)、枯草芽孢杆菌(Bacillus subtilis)、甲基营养芽孢杆菌(Bacillus methylotrophicus)等,这些菌株在酱香型白酒酿造过程均可代谢并产生TTMP,其中枯草芽孢杆菌的产香效果最好,主要呈现出浓郁的甜酱香味[29-31]。WANG WY等[32]研究指出,高温发酵过程芽孢杆菌所产生的孢子内会大量蓄积2,6-吡啶二甲酸,在多轮次发酵后,该物质会逐步转化形成各类吡啶类化合物。此外,芽孢杆菌还具有启动白酒酿造系统内氨基酸生物合成的能力,能够有效推动芳香类风味物质的生成与积累[33]。WU Q等[34]将地衣芽孢杆菌接种在固态发酵培养基中,使得半胱氨酸的生物合成得以实现,四甲基吡嗪、3-羟基-2-丁酮及2,3-丁二醇等关键风味物质的含量显著提升。 醋酸菌在堆积发酵过程同样具有重要作用,其生长代谢会氧化原料中的葡萄糖和乙醇产生醋酸,与发酵过程中的乙醇等物质发生缩合反应生成酯类物质,为酱香型白酒风味物质的形成提供前体物质。但是醋酸菌含量过多也会使得糟醅酸度过高,抑制部分细菌和酵母菌的生长从而影响堆积发酵的进行,最终导致白酒产量降低甚至产生异味。片球菌属(Pediococcus)、魏斯氏菌属(Weissella)和乳酸杆菌属(Lactobacillus)是酱香型白酒堆积过程主要乳酸菌[35]。研究表明,乳酸菌在堆积发酵过程会产生大量乳酸、乙酸、乳酸乙酯等风味化合物及其前体,这些代谢物可以降低白酒的刺激感,增加白酒回甜风味,从而明显增强白酒的醇厚特性[36-38]。然而,乳酸菌过度繁殖会导致白酒乳酸乙酯含量过高,形成已乳倒挂的现象,酒体则会酸涩从而影响酒质。因此现阶段在生产上对乳酸菌的关注普遍体现在乳酸菌的数量控制上,在酱香型白酒的酿造过程中合理的监测和调控细菌菌群数量和结构对于白酒品质的保持尤为重要。
2.2 霉菌
霉菌可分泌多种关键酶系,包括果胶酶糖化酶、纤维素酶、液化酶、酯化酶、蛋白酶等[33]。 这些水解酶类共同作用,能够催化分解原料中的蛋白质、淀粉等高分子物质转变为易吸收的小分子组分,为共生微生物群落的生长繁殖创造营养条件[39-40]。 酱香型白酒堆积发酵酒醅中常见的霉菌包括根霉(Rhizopus)、曲霉(Aspergillus)、红曲霉(Monascus)等[41],这些优势真菌代谢产生的多种水解酶类在酒醅发酵过程中对原料的利用以及白酒风味物质的形成具有重要促进作用。
根霉是一类嗜热性真菌,在堆积发酵过程主要产糖化酶。 有研究表明,根霉在白酒酿造过程中参与挥发性风味物质的生成,其代谢活动可分泌酒精脱氢酶、酸性蛋白酶、乳酸、葡聚糖酶等多种活性物质,对酱香型白酒独特风味的形成具有重要作用[42-43]。 曲霉在堆积发酵酒醅中相对丰度较大,是堆积过程主导霉菌属。 曲霉在酱香型白酒堆积发酵过程主要产糖化酶、蛋白酶、果胶酶等,其在白酒发酵初期承担关键的淀粉糖化功能,将原料中大分子物质比如淀粉等分解为葡萄糖等小分子物质,供酒醅中酿酒酵母等真菌生长代谢[36]。张超[44]研究发现,红曲霉能分泌酯化酶、淀粉酶、糖化酶等各种水解酶类,可以显著改善白酒质量。陈卓等[45]探究了酱香型白酒三轮次酒醅风味物质与优势微生物间的关联性,结果表明酒醅中曲霉与多数酯类化合物存在极显著正相关关系(P<0.01)。尚柯[46]的研究进一步证实堆积酒醅中的曲霉具有关键作用,凭借其高效的糖化活性、液化能力及蛋白质分解能力,为优质白酒的生产提供了有力支撑。
2.3 酵母菌
酵母菌不仅仅决定着出酒率的高低,而且对于酒体的质量、风味以及后续的品质,都会产生很大的影响。因其是生产酒精和高级酯等风味物质的主体,同样起到不可替代的作用[47]。根据在生产工艺中所起的作用,又可以将这些酵母菌分为:产酒型、生香型及其他功能型3大类[48]。
一类是产酒酵母,其可通过糖酵解途径在无氧条件下将原料中的葡萄糖转换为乙醇,产生大量酒精,是酱香型白酒酿造的驱动力[49]。现阶段已发现的高产酒类酵母菌种主要涵盖东方伊萨酵母(Issatchenkia orientalis)、粟酒裂殖酵母(Schizosaccharomyces pombe)以及酿酒酵母(Saccharomyces cerevisiae)等典型菌株[48]。卢君等[50]将粟酒裂殖酵母LJ3和耐酸酿酒酵母NJ2接种在第四轮次糟醅中进行强化发酵,结果显示该实验并没有影响白酒的正常风味,且处理过的糟醅基酒产量显著提升13.47%~25.97%。 彭俊等[51]的研究证实,从酒醅中分离获得的东方伊萨酵母(Issatchenkia orientalis)展现出较强的环境适应性和发酵能力,在高粱糖化发酵培养基中可高产酒精(8.2%vol)及乙酸乙酯(385.5 mg/L),该菌株优异的代谢特性表明其具有极高的工业化应用价值。 另一类是生香酵母,这类酵母酒精产能较低,但具有合成多种挥发性风味化合物的能力,对酱香型白酒特征香气的形成起到关键的调控[52]。在白酒酿造过程中,具有生香功能的酵母类群主要包括假丝酵母、毕赤酵母、白地霉、汉逊酵母、酒香酵母[53]。YANG L Z等[54]研究表明,在酸性环境下接合酵母属(Zygosaccharomyces)亦能合成酯类物质。王晓丹等[55]通过系统筛选茅台镇某酒厂酒醅中的微生物资源,结合菌株鉴定与气相色谱质谱联用(gas chromatography-mass spectrometry,GC-MS)代谢产物分析技术,最终获得一株高产乙酸苯乙酯的库德里阿兹威氏毕赤酵母(Pichia kudriavzevii)以及一株高产乙酸乙酯的平常假丝酵母(Candida inconspicua)。 除生香和产酒,在堆积发酵体系中酵母菌还能够有效驱动发酵进程、分解底物提高原料利用率[48]。以扣囊复膜孢酵母(Saccharomycopsis fibuligera)为例,该菌株可高产纤维素酶、β-葡萄糖苷酶、蛋白酶等多种水解酶系,通过靶向作用于酒醅中的复杂底物,有效加速原料的降解转化过程,从而显著提升产酒率[56]。
2.4 放线菌
放线菌作为酱香型白酒堆积发酵过程的主要功能微生物之一,其作用主要体现在3个方面。一方面,放线菌在堆积发酵过程可以通过产酸、产酶等来调节酿酒微生态。李云英等[57]成功从酒醅中获取高温放线菌株,并证实其具备合成乳酸与柠檬酸的代谢功能。白成松等[58]在酒醅样本中分离得到一株性能优异的产色高温单孢菌(Thermomonospora chromogena),该菌株具有较强的蛋白酶、淀粉酶、纤维素酶活性。 另一方面,放线菌在酒醅发酵过程中不仅通过自身生长代谢参与物质转化,还能直接产生或降解多种风味成分。研究表明,这类微生物可分泌丁酸乙酯、己酸乙酯、乳酸乙酯等酯类芳香物质以及醇类化合物[59],作为萜类化合物的重要生物来源,能够有效丰富白酒的香气层次,对提升酒体风味品质具有显著促进作用[60]。 邹恬杏等[61]研究酱香型白酒酒醅中微生物与其风味物质之间的相关性,研究发现,高温放线菌(Thermoactinomyces)与2,6-二甲基吡嗪、乙酸苯乙酯、苯乙醇等关键香气成分存在显著正相关关系。除此之外,放线菌产生的次级代谢产物在酿造微生物生态系统中发挥着重要的生物调控功能,对其他产香微生物表现出促进或抑制效应,进而控制香气产物的代谢生成,改变白酒的风味组成[62]。 施思等[63]在芽孢杆菌和酵母菌发酵培养基中接种放线菌,结果显示外源加入的放线菌并不会影响芽孢杆菌和酵母菌的增殖,但会调控酵母菌的葡萄糖代谢,促进苯乙醇与己酸乙酯等风味物质的生成。尤小龙等[64]针对酱香型白酒酒醅中分离获得的两株放线菌展开深入研究,着重剖析其次生代谢产物的生物学活性特征。研究发现,这两株放线菌均具备合成非蛋白类且非肽类抗生素的能力,此类抗菌物质可特异性抑制产酱香芽孢杆菌的生长代谢活动,进而影响白酒中风味物质生成。DU H等[65]的研究揭示,产土臭素链霉菌产生的的庚烯大环内酯类抗生素会打破酿造体系的微生物稳态平衡,导致酵母菌在白酒风味塑造过程中的功能贡献度明显下降。
上述研究表明,酱香型白酒堆积发酵过程以产香细菌、产酶霉菌、产酒酵母菌以及产次生代谢物放线菌等四大菌群为主,构成了其丰富的酿造微生态。 堆积过程各菌群分别在原料的分解与利用、呈味物质的产生和贡献、酿造微生态的调控等方面发挥着重要作用,推动着整个过程堆积发酵的进行。此外,堆积发酵过程是是各菌种结合、共同作用、相互调控的混菌发酵,无论是细菌还是真菌在整个酿造阶段其生长和衰亡都会对堆积发酵过程产生影响,研究单一或几种功能菌对发酵过程的影响与实际生产脱节,并不具备说服力。因此,在挖掘酱香型白酒堆积发酵功能微生物的同时,加强对功能菌种之间互作机制的研究,对于改善白酒酒体风味具有重要意义。
2.5 微生物群落分析方法
酱香型白酒堆积发酵微生物的研究方法,分别是以生物、化学为依据的传统方法和以现代分子生物学技术为依据的新方法。 前者更为直接,可以从样品中获得真实的菌种标本,但是现有的研究发现,自然界中存在的微生物只有不到1%~10%是可以在现有培养条件下生长,并且得到纯培养的[66],因此引入了现代分子生物学技术。
目前对于酱香型白酒堆积发酵微生物的研究,应用比较广泛的主要技术手段有以下几种:醌指纹法(quinone profile,QP)、磷脂脂肪酸(phospholipid fatty acid,PLFA)图谱法、rDNA同源性分析方法、基因文库技术、限制性片段长度多态性(restriction fragment length polymorphism,RFLP)技术、DGGE技术、实时荧光定量聚合酶链式反应(real-time fluorescence quantitative polymerase chain reaction,RT-qPCR)技术、高通量测序技术、以及能全面解析微生物组的宏基因组学技术。 相较于微生物传统培养方式,分子生物学技术能够直接从样本中获取整个基因信息、快速且全面地解析整个微生物群落。 但是单靠分子生物学技术并不能分离纯化单个菌株,所以也无法在菌株层面进行更加详细的机理探讨。 因此,将传统可培养方法与现代生物技术有机结合起来,以分子生物技术的研究结果为导向,进行有针对性地分离纯化培养,在分离纯化培养的同时充分运用分子生物技术来确定目标菌株对于酱香型白酒酿造微生物的研究具有重要作用。
3 总结
酱香型白酒生产工艺中的的堆积发酵素有“二次制曲”之称,其在营造优良酿酒微生态环境的同时,提前为成品酒积累大量风味前体物质,并确保后续窖池发酵得以顺利开展,从而形成产品的特色风味和良好品质。因此,研究酱香白酒堆积发酵微生物群落特性及其作用对于白酒品质的改善和工艺机理的优化提升具有重要意义。
随着现代分子生物学技术的不断更新迭代,酱香型白酒堆积发酵微生物群落的多样性、演替规律以及微生物与风味物质相关性等被逐步解析。但是由于酱香型白酒堆积发酵周期长,受影响因素较多,目前对堆积发酵微生物的研究在研究方法、研究方向以及实际应用方面还有诸多不足。未来对酱香型白酒堆积发酵微生物群落的研究,可采用传统培养技术和现代分子生物技术相结合的方式进行,利用宏基因组学、宏转录组学、代谢组学、风味组学等多种组学技术,加强对酱香型白酒堆积发酵微生物的来源、相互作用关系以及其功能基因对风味物质的调控机制进行研究,同时开展堆积发酵功能微生物在酒曲强化、窖池养护和酒糟资源化利用等方面的应用研究,以实现酱香型白酒酿造工艺优化升级和酱酒行业的可持续发展。
[1] ZHANG H X,XU Y,DU H.Fungal community and sources of heap fermentation during Jiangxiangxing Baijiu production[J] . Food Ferment Indust,2024,50(20):42-49.
[2] 曾超.酱香白酒酿造过程中厌氧细菌的特性研究[D] .贵阳:贵州大学,2016.
[3] 赵侨,杨花,田茂玲,等. 酱香型白酒堆积发酵微生物与风味物质相关性研究进展[J] .中国酿造,2024,43(12):6-12.
[4] WANG C L, SHI D J, GONG G L. Microorganisms in Daqu:A starter culture of Chinese Maotai-flavor liquor[J] .World J Microbiol Biotechn,2008,24(10):2183-2190.
[5] WANG M Y,YANG J G,ZHAO Q S,et al.Research progress on flavor compounds and microorganisms of Maotai flavor Baijiu[J] .J Food Sci,2019,84(1):6-18.
[6] 张春林,杨亮,李喆,等. 酱香型白酒酒醅堆积微生物多样性及其与风味物质的关系[J] .食品科技,2022,47(4):111-118.
[7] 周恒刚.酱香型白酒生产工艺的堆积[J] .酿酒科技,1999(1):5-7.
[8] 王小平,黄永光,周文美. 酱香型白酒大曲细菌菌群结构及功能研究进展[J] .中国酿造,2020,39(2):19-25.
[9] 吴成,杨龙飞,胡峰,等. 酱香型白酒造沙轮次堆积发酵微生物及理化指标演替规律[J] .食品科技,2023,48(6):9-15.
[10] 胡小霞.茅台镇酱香型白酒酿造环境微生物群落结构研究[D] .贵阳:贵州大学,2020.
[11] 张红霞. 酱香型白酒酿造菌群形成规律及稳态调控机制研究[D] . 无锡:江南大学,2021.
[12] ZHU A R, WANG D Q, HU J F, et al. Microbial community structure and traceability in fermented grains for Jiang-flavor Baijiu during the first round of fermentation[J] .Food Sci,2025,46(4):117-125.
[13] WU Y F,DUAN Z G,NIU J L,et al.Spatial heterogeneity of microbiota and flavor across different rounds of sauce-flavor Baijiu in Northern China[J] .Food Chem X,2023,20:100970.
[14] LV X C,CAI Q Q,KE X X,et al.Characterization of fungal community and dynamics during the traditional brewing of Wuyi Hong Qu glutinous rice wine by means of multiple culture-independent methods[J] . Food Control,2015,54:231-239.
[15] ZHA M S, SUN B G, WU Y P, et al. Improving flavor metabolism of Saccharomyces cerevisiae by mixed culture with Wickerhamomyces anomalus for Chinese Baijiu making[J] .J Biosci Bioeng,2018,126(2):189-195.
[16] 李豆南,黄魏,王晓丹,等. 酱香型大曲中高温放线菌的筛选及风味成分分析[J] .食品科学,2018,39(6):171-176.
[17] 山其木格,梁慧珍,张长霞,等. 糟醅堆积过程中微生物种群的变化规律[J] .食品与生物技术学报,2016,35(3):330-335.
[18] YANG L,XIAN C,LI P,et al.The spatio-temporal diversity and succession of microbial community and its environment driving factors during stacking fermentation of Maotai-flavor Baijiu[J] . Food Res Int, 2023,169:112892.
[19] 龙亚飞,朱孜,郭淳钦,等. 酱香型白酒下沙、造沙堆积发酵过程中产四甲基吡嗪功能微生物的变化[J] .中国酿造,2024,43(10):65-73.
[20] 吕锡斌,吴耀领,郝飞,等. 高通量测序技术分析酱香型白酒下造沙轮次的微生物多样性[J] .酿酒科技,2019(3):52-58,64.
[21] 万旗钰,程玉鑫,黄永光,等. 酱酒1、2轮次窖池不同醅层微生态结构与酸性化合物组成解析及其相关性预测[J] . 食品科学,2024,45(4):88-95.
[22] XIE D,WU C,ZHAO W Y,et al.Microbial diversity and flavor of Maotaiflavor Baijiu during the first-round stacking fermentation[J] . Food Res Develop,2025,46(1):194-201.
[23] 张春林,杨亮,李喆,等. 酱香型白酒二轮次堆积酒醅微生物群落与理化指标相关性研究[J] .中国酿造,2021,40(11):31-36.
[24] 王欢.基于微生物组学的酱香型白酒酿造微生物及酒体风味研究[D] .贵阳:贵州大学,2020.
[25] 邹恬杏. 洞酿酱香酒前三轮次堆积发酵过程中微生物群落演替及其代谢特征解析[D] .贵阳:贵州大学,2024.
[26] 吴成,程平言,谢丹,等. 酱香型白酒4轮次堆积发酵理化因子、风味物质与微生物群落相关性分析[J] .食品科学,2023,44(2):240-247.
[27] 孙利林,李立郎,胡萍,等. 酱香型白酒第四轮次酒酿造过程中细菌多样性分析[J] .中国酿造,2020,39(5):35-39.
[28] 王玉荣,马佳佳,田龙新,等. 酱香型白酒第六轮次堆积发酵醅堆微生物类群与感官品质的相关性分析[J] . 现代食品科技,2024,40(9):107-117.
[29] 王晖,蒲叶,李霁阳,等. 白酒窖泥中乳酸菌分离鉴定及其发酵产挥发性风味物质比较[J] .食品科学技术学报,2020,38(1):26-35.
[30] 施小明,徐岩,崔凤元,等. 枯草芽孢杆菌在白酒生产中的应用[J] . 酿酒科技,2012(2):49-53.
[31] 王和玉,杨帆,姚翠屏,等. 枯草芽孢杆菌利用不同基质所产代谢物的分析对比[J] .酿酒科技,2009(12):93-95.
[32] WANG W Y,LIU R L,SHEN Y,et al.The potential correlation between bacterial sporulation and the characteristic flavor of Chinese Maotai liquor[J] .Front Microbiol,2018,9:01435.
[33] 刘正,培军,卢延想,等. 酱香型白酒酿造过程中微生物多样性及代谢过程研究进展[J] .中国酿造,2022,41(6):6-11.
[34] WU Q, XU Y. Transcriptome profiling of heat-resistant strain Bacillus licheniformis CGMCC3962 producing Maotai flavor[J] .J Agr Food Chem,2012,60(8):2033-2038.
[35] 肖辰. 泸型酒中温大曲微生物群落的演替及其对酒醅发酵的贡献[D] .无锡:江南大学,2018.
[36] 何小容,张庆,唐家环,等. 浓香型白酒大曲发酵过程中主要微生物群系及其作用研究进展[J] .中国酿造,2024,43(8):1-6.
[37] ZHOU Q F,MA K,SONG Y,et al.Exploring the diversity of the fungal community in Chinese traditional Baijiu Daqu starters made at low-,medium-and high-temperatures[J] .LWT-Food Sci Technol,2022,162:113408.
[38] LIU W H,CHAI L J,WANG H M,et al.Bacteria and filamentous fungi running a relay race in Daqu fermentation enable macromolecular degradation and flavor substance formation[J] .Int J Food Microbiol,2023,390:110118.
[39] 王世伟,王卿惠,芦利军,等. 白酒酿造微生物多样性、酶系与风味物质形成的研究进展[J] .农业生物技术学报,2017,25(12):2038-2051.
[40] 郭敏,黄永光,邱树毅,等. 高通量测序在酱香白酒微生态多样性研究中的应用[J] .中国酿造,2017,36(5):146-151.
[41] SHI S,LI Z,WU Z Y,et al.Analysis of the fungi community in multipleand single-grains Zaopei from a Luzhou-flavor liquor distillery in western China[J] .World J Microbiol Biotechn,2011,27:1869-1874.
[42] ZHENG X W,TABRIZI R M, NOUT R J M, et al. Daqu-A traditional Chinese liquor fermentation starter[J] .J I Brewing,2011,117(1):82-90.
[43] ZHU M,ZHENG J,XIE J,et al.Effects of environmental factors on the microbial community changes during medium-high temperature Daqu manufacturing[J] .Food Res Int,2022,153:110955.
[44] 张超.试论红曲霉在传统白酒中的生产与应用[J] .酿酒,2021,48(2):127-129.
[45] 陈卓,苏伟,母应春,等. 洞酿酱香型白酒第三轮次酒醅发酵过程中微生物与挥发性风味物质相关性分析[J] .中国酿造,2024,43(5):32-40.
[46] 尚柯.酱香型白酒高温堆积工艺机理的初步研究[D] .乌鲁木齐:新疆农业大学,2016.
[47] WANG D Q,CHEN L Q,YANG F,et al.Yeasts and their importance to the flavour of traditional Chinese liquor:A review[J] .J I Brewing,2019,125(2):214-221.
[48] 李景辉.酱香型白酒生香酵母菌的筛选与应用[D] .天津:天津科技大学,2021.
[49] 戎梓溢,白茹,闫学娇,等. 酱香型白酒酿造微生态中酵母菌的研究进展[J] .食品研究与开发,2022,43(13):180-188.
[50] 卢君,山其木格,唐平,等. 耐酸酵母菌株的筛选及其在酱香白酒酿造过程中的应用研究[J] .酿酒科技,2019(10):106-111.
[51] 彭俊,杨团元,刘蒲临,等.白酒酿造酒醅与周边土壤中酵母菌多样性及东方伊萨酵母发酵特性比较[J] .中国酿造,2019,38(8):77-84.
[52] 黄魏,程平言,张健,等.酱香型白酒风味形成的影响因素及主体风味成分研究进展[J] .酿酒科技,2020(4):85-93.
[53] 曹苗文,相里加雄,徐炳璋,等.功能型曲在清香型白酒生产中的应用[J] .食品与发酵工业,2020,46(5):134-139.
[54] YANG L Z,LI X L,LU Y H,et al.Ester synthesis mechanism and activity by Bacillus licheniformis, Candida etchellsii, and Zygosaccharomyces rouxii isolated from Chinese horse bean chili paste[J] .J Sci Food Agr,2021,101(13):5645-5651.
[55] 王晓丹,庞博,陈孟强,等. 酱香白酒酒醅中产香酵母分离与鉴定[J] .食品安全质量检测学报,2014,5(6):1799-1808.
[56] CHANG S,MA Y Y,YANG J G.Research progress of Saccharomycopsis fibuligera in liquor-making industry[J] .Food Res Develop,2018,39(1):205-209,220.
[57] 李云英,李能树.大曲酒微生物区系的初步研究[J] .生物学杂志,1996(3):19-21,15.
[58] 白成松,陈莉,卢红梅,等.茅台地区酱香型酒糟中高温放线菌的分离鉴定[J] .食品工业科技,2017,38(8):199-202.
[59] 陈继良.浓香型白酒在酿造中的功能菌研究进展[J] .酿酒,2020,47(2):15-18.
[60] FENG M X,HUO Q J,GAN L Y,et al.Effects of four strains of Actinomycetes on the content of terpenoids in Baijiu[J] . Foods, 2023, 12(7):1494.
[61] 邹恬杏,苏伟,母应春,等. 洞酿酱香酒第四轮次酒醅发酵过程中微生物群落与挥发性代谢物分析[J] .中国酿造,2023,42(6):64-71.
[62] 陈瑗,王守琴,贺巧玲,等. 白酒酿造中放线菌的分布与功能概述[J] .食品与发酵科技,2024,60(4):85-91.
[63] 施思,张霞,杨康卓,等. 放线菌对酿酒微生物调控的初步解析[J] . 酿酒科技,2021(2):17-20,26.
[64] 尤小龙,黄蕴莉,黄永光,等. 放线菌对发酵过程产酱香功能菌的生物学特性研究[J] .酿酒科技,2015(8):1-5,10.
[65] DU H,LU H, XU Y. Influence of geosmin-producing Streptomyces on the growth and volatile metabolites of yeasts during Chinese liquor fermentation[J] . J Agr Food Chem,2015,63(1):290-296.
[66] 潘虎,卢向阳,董俊德,等. 未培养微生物研究策略概述[J] . 生物学杂志,2012,29(1):79-83.