白酒作为中国传统的固态发酵蒸馏酒,不仅承载着深厚的文化与历史内蕴,其复杂的微量成分构成也日益成为健康与风味研究的热点。 白酒中已鉴定出的微量组分>3 000种[1],包括有机酸、酯类、醇类、醛类、吡嗪、萜烯及短肽等,尽管其含量甚微,却在白酒的风味呈现与潜在健康效应中扮演着关键角色[2-4]。 近年来研究表明,白酒中部分微量成分如阿魏酸、α-蒎烯、4-甲基愈创木酚以及某些短肽等,可能通过调控细胞自噬通路,对酒精性肝损伤等起到缓解作用[5-9]。细胞自噬是细胞内降解异常蛋白和受损细胞器的重要过程,对维持细胞稳态、应对氧化应激及调控多种疾病进程具有核心意义[10-13]。因此,探索白酒微量成分对细胞自噬的调控作用,对于解析其健康效应机制具有重要意义。
目前,国内外对白酒微量成分与细胞自噬关系的研究尚处于起步阶段,相关功能成分的筛选与效应评价主要依赖于蛋白免疫印记(Western blottin,WB)等传统技术。WB通过检测LC3和P62的变化趋势对细胞自噬进行分析,其中LC3是自噬体形成的标志物(其II型含量与自噬体数量正相关),而P62是自噬降解的货物受体(其含量与自噬降解活性负相关),两者结合可动态示踪自噬流的完整过程[14-15]。然而,此类方法存在通量低、耗时长、结果半定量且稳定性较差等局限,难以实现对大量样本的高效、精准分析。因此,亟需建立一种快速、可靠、高通量的检测模型,以系统评估白酒复杂体系中各组分对细胞自噬的影响。基于双荧光蛋白[绿色荧光蛋白(green fluorescent protein,GFP)与红色荧光蛋白(red fluorescent protein,RFP)] 标记的自噬通量探针可在细胞内被内源性自噬相关蛋白4(autophagy-related protein 4,ATG4)蛋白酶切割为绿色荧光蛋白-微管相关蛋白1轻链3(green fluorescent protein-microtubule-associated protein1A/1B-lightchain 3,GFP-LC3)与红色荧光蛋白-微管相关蛋白1轻链3甘氨酸缺失突变体(red fluorescent proteinmicrotubule-associated protein 1A/1B-light chain 3 glycine deletion mutant,RFP-LC3ΔG),前者与磷脂酰乙醇胺(phosphatidyl ethanolamine,PE)结合后被自噬体降解,后者由于不能被脂化,稳定存在于胞质作为内参,通过流式细胞术实时检测活细胞中GFP/RFP荧光比值,即可实现对自噬通量的精准定量分析[16]。该探针已被运用在斑马鱼和小鼠等细胞和生物体中来评估调节自噬的化合物[16]。相较于传统的WB方法,该技术具备高通量、高精度、高重现性及活细胞动态监测等显著优势。
本研究以人正常肝细胞LO2为载体,构建并筛选稳定高效表达细胞自噬通量探针GFP-LC3-RFP-LC3ΔG的细胞株,并结合流式细胞术与WB技术,系统评估白酒中2种代表性微量成分——月桂酸和4-甲基愈创木酚对细胞自噬的影响,以期验证自噬通量探针模型在评估自噬调控活性中的可行性与优越性,明确2种微量成分对LO2细胞自噬的作用效果,为白酒健康因子高通量筛选提供新技术平台,并为深入解析其分子机制奠定基础。本研究不仅有助于深化对白酒微量成分生理功能的理解,也为传统发酵食品中功能成分的快速发现与评价提供了创新方法支撑。
1 材料与方法
1.1 材料与试剂
1.1.1 材料
人正常肝细胞LO2、人胚肾细胞293T:国家实验细胞资源共享服务平台;大肠杆菌(Escherichia coli)DH5α感受态细胞:北京全式金生物技术有限公司;聚偏二氟乙烯(polyvinylidene fluoride,PVDF)膜:美国Merck Millipore公司;质粒pMRX-IP-GFP-LC3-RFP-LC3ΔG、pCDH-RFP-GFPhLC3B-EF1-Puro、pMD2G、pSPAX2:中国质粒载体菌种细胞基因保藏中心。
1.1.2 试剂
Lysis Buffer细胞裂解液:北京康为世纪生物科技有限公司;脱脂牛奶、5×蛋白质上样缓冲液:北京索莱宝科技有限公司;蛋白质Marker:美国BIO-RAD公司;一抗(anti-LC3 antibody、anti-P62 antibody):日本MBL公司;甘油醛-3-磷酸脱氢酶(glyceraldehyde-3-phosphate dehydrogenase,GAPDH)、二抗(anti-rabbit):美国CST公司;增强化学发光底物(enhanced chemiluminescence substrate,ECL)曝光液:美国Merck millipore公司;厄尔氏平衡盐溶液(Earle's balanced salt solution,EBSS):美国Thermo Fisher Scientific;Vigofect转染试剂:威格拉斯生物技术(北京)有限公司;巴佛洛霉素A1(bafilomycin A1,BafA1):美国MedChemExpress;月桂酸、4-甲基愈创木酚:上海麦克林生化科技有限公司;胎牛血清(fetal bovine serum,FBS)、胰蛋白酶、青霉素、链霉素溶液:美国Hyclone公司;氨苄青霉素钠:翌圣生物科技上海股份有限公司;聚凝胺(10 mg/mL)、嘌呤霉素(10 mg/mL):碧云天生物技术有限公司;本研究所用试剂均为分析纯。
1.1.3 培养基
RPMI-1640培养基:美国Gibco公司。
完全培养基:在445 mLRPMI-1640培养基中添加50 mL FBS、5 mL 100 U/mL青霉素和100 μg/mL链霉素的混合液。
杜尔贝科改良伊格尔培养基(Dulbecco's modified Eagle medium,DMEM):美国Thermo Fisher Scientific。
LB液体培养基[17]:胰蛋白胨10 g/L,酵母浸粉5 g/L,NaCl 10 g/L,去离子水定容至1 000 mL,121 ℃高压蒸汽灭菌20 min;LB固体培养基:在LB液体培养基中添加20 g/L琼脂。
1.2 仪器与设备
YXQ-50G立式灭菌锅:上海博迅生物仪器股份有限公司;MX-S可调式混匀仪、DLAB DM0506临床低速离心机:大龙兴创实验仪器(北京)股份公司;LEGEND Micro 21R微量台式离心机:美国赛默飞公司;NovoCyte 2000R流式细胞仪:安捷伦科技有限公司;Chenmi Scope 6200 Touch化学发光成像系统:上海勤翔科学仪器有限公司;CKX-53倒置相差显微镜:日本奥里巴斯有限公司;T20型双槽梯度聚合酶链式反应(polymerase chain reaction,PCR)仪:杭州朗基科学仪器有限公司;BPN-160CW二氧化碳培养箱:上海灯晟仪器制造有限公司。
1.3 方法
1.3.1 LO2细胞培养
采用10 mL完全培养基重悬LO2细胞,于37 ℃、5%CO2条件下培养,当细胞生长到约60%~80%的融合度时,加入1 mL 0.25%胰蛋白酶进行消化,3 min后加入1 mL完全培养基进行中和,采用移液枪将培养皿中的细胞吹打下来,进行传代培养。
1.3.2 慢病毒介导的自噬通量探针转染及稳定细胞株筛选流程
(1)质粒构建
以pMRX-IP-GFP-LC3-RFP-LC3ΔG质粒为模板,通过PCR扩增获得GFP-LC3-RFP-LC3ΔG基因片段,经NheI/BamHI双酶切后,连接到pCDH-RFP-GFP-hLC3B-EF1-Puro质粒上,得到含有自噬通量探针编码序列的pCDH-GFP-LC3-RFPLC3ΔG-Puro质粒。
(2)质粒转化
向100 μL的E.coli DH5a感受态细胞中加入1 μL质粒pCDH-GFP-LC3-RFP-LC3ΔG-Puro(质量浓度不超过50μg/μL),冰上静置30min,42℃热激处理90s,迅速置于冰上冷却5min,加入1 mL LB液体培养基,于37 ℃、200 r/min条件下培养1 h,培养结束后3 000 r/min离心2 min,弃部分上清,保留100 μL上清重悬菌液,并涂布于含有100 μg/mL氨苄抗生素的LB固体培养基平板上,于37 ℃条件下培养12~16 h。 从平板上挑选单一菌落,接种至5 mL LB液体培养基中,于37 ℃、200 r/min条件下培养12~16 h[18-19]。
(3)慢病毒转染
293T细胞转染前24 h进行铺板培养,即向6孔板中接种0.5 mL 293T细胞悬液,每孔补加1.5 mL DMEM培养基,细胞孔板置于37 ℃、5%CO2培养箱中培养,使细胞覆盖率达到70%~90%。 转染前2~3 h,更换新鲜的培养基。 按照pMD2G:pSPAX2:目的质粒(pCDH-GFP-LC3-RFP-LC3ΔGPuro)=4∶6∶10的比例将3质粒进行混合,取20 μg混合质粒,加入到400 μL 0.9%生理盐水中混匀,得到混合物1(Mix 1)。取8 μL Vigofect转染试剂加入到另外400 μL 0.9%生理盐水中,混匀后静置5 min,得到混合物2(Mix 2)。将Mix 1与Mix 2混合,静置15 min,然后逐滴加入到293T细胞培养板中,并轻轻摇晃使其混匀。置于37 ℃、5%CO2培养箱中培养,培养4~6 h后更换新鲜培养基。 在培养24 h后继续更换新鲜培养基,在培养48~72 h之间收取含有慢病毒的上清培养液至15 mL离心管中,在-80 ℃的条件下储存[20-21]。
LO2细胞转染前24 h按照6×104个/孔的数量接种在6孔板中。转染前对6孔板LO2细胞更换培养液,并加入1.5 mL RPMI-1640培养基、2 μL聚凝胺和1 mL慢病毒上清,将培养板置于37 ℃、5%CO2培养箱中培养36 h后,加入2 μL嘌呤霉素,继续培养24~48 h。观察细胞的状态,成功转染的细胞会贴壁生长,而未转染成功的细胞会漂浮在培养基上。此时,可以进行细胞传代和单细胞筛选以获取稳定表达的细胞株。
(4)单细胞筛选
通过流式细胞仪分选出高效表达红绿双荧光的单克隆细胞株,并从96孔板中挑选出仅含有一个克隆的细胞株。将单个细胞逐一传代至24孔板中,以便富集细胞数量,利用流式细胞仪检测GFP及RFP信号强度,挑选一株稳定高效表达红绿荧光的单克隆细胞株将其命名为LO2-GFP-RFP,将此细胞传代冻存。整个慢病毒介导的自噬通量探针转染及稳定细胞株筛选流程如下:

实验前将LO2-GFP-RFP细胞接种于含有10 mL RPMI-1640培养基的培养皿中,置于37 ℃、5%CO2培养箱中培养至细胞覆盖率达到70%~80%。 将培养皿中细胞回收到无菌的15 mL离心管中并按照6×104个/孔分装到6孔板中。在此基础上,实验分为4组:阴性对照组、营养组、饥饿处理组和饥饿处理加自噬抑制剂组。阴性对照组中接种6×104个/孔LO2细胞;营养组使用完全培养基培养;饥饿处理组将培养基替换为EBSS,使细胞处于饥饿状态,持续处理2 h;饥饿处理加自噬抑制剂组则在进行EBSS饥饿处理的同时,加入自噬抑制剂BafA1至终浓度为2.5 nmol/L,共同处理2 h。处理结束后,收集细胞并使用流式细胞仪检测GFP和RFP信号。
1.3.3 白酒微量成分对细胞自噬通量的影响
以接种1.2×105个/孔LO2细胞作为阴性对照组,在6孔板中接种1.2×105个/孔LO2-GFP-RFP细胞,每孔加入1.5 mL完全培养基,孔板置于37 ℃、5%CO2培养箱中培养24 h后,分别加入不同浓度的活性物质,包括4-甲基愈创木酚和月桂酸。根据细胞的存活情况设置月桂酸添加浓度范围为0~1 mol/L,4-甲基愈创木酚的添加浓度范围为0~4 mmol/L。置于37 ℃、5%CO2培养箱中共同培养24 h后,采用磷酸盐缓冲液(phosphate buffer saline,PBS)收集样本并采用流式细胞仪检测GFP和RFP信号。
1.3.4 蛋白印迹分析
将方法1.3.4中不同浓度活性物质与LO2-GFP-RFP细胞共同培养24 h后的样本,以及阴性对照组样本进行细胞收集,加入含蛋白酶抑制剂的裂解液裂解细胞,离心并收集上清液,以GAPDH的灰度值为内参,进行免疫印迹(western blot,WB)实验[22]。
1.3.5 统计分析
所有实验均独立重复3次,实验数据采用Origin 2021及SPSS 26.0等软件进行统计分析,结果以“平均值±标准差”表示,组间差异采用双尾独立样本t检验进行统计学分析,P<0.05表示具有统计学意义。WB图像使用ImageJ软件进行灰度值定量,结果以目标蛋白与内参蛋白(GAPDH)灰度比值表示。流式细胞术数据使用FlowJo 10进行分析。
2 结果与分析
2.1 稳定高效表达自噬通量荧光探针的LO2细胞株的构建与筛选
为建立基于自噬活性变化的高通量评价体系,首先构建了携带自噬通量探针编码序列的质粒pCDH-GFP-LC3-RFP-LC3ΔG-Puro,并通过慢病毒包装系统转染LO2细胞。经嘌呤霉素筛选后,利用流式细胞仪进行单细胞分选,成功分离出高效表达红绿双荧光的细胞群体,结果见图1。由图1A可知,P1门框选的细胞。由图1B可知,通过对96孔板中36株单克隆细胞株进一步筛选与鉴定,同时表达红绿荧光的细胞占比为28.45%,对该部分细胞进一步筛选鉴定最终获得一株荧光信号稳定且强度高的单克隆细胞株,命名为LO2-GFP-RFP细胞,为后续研究提供了可靠的细胞模型。
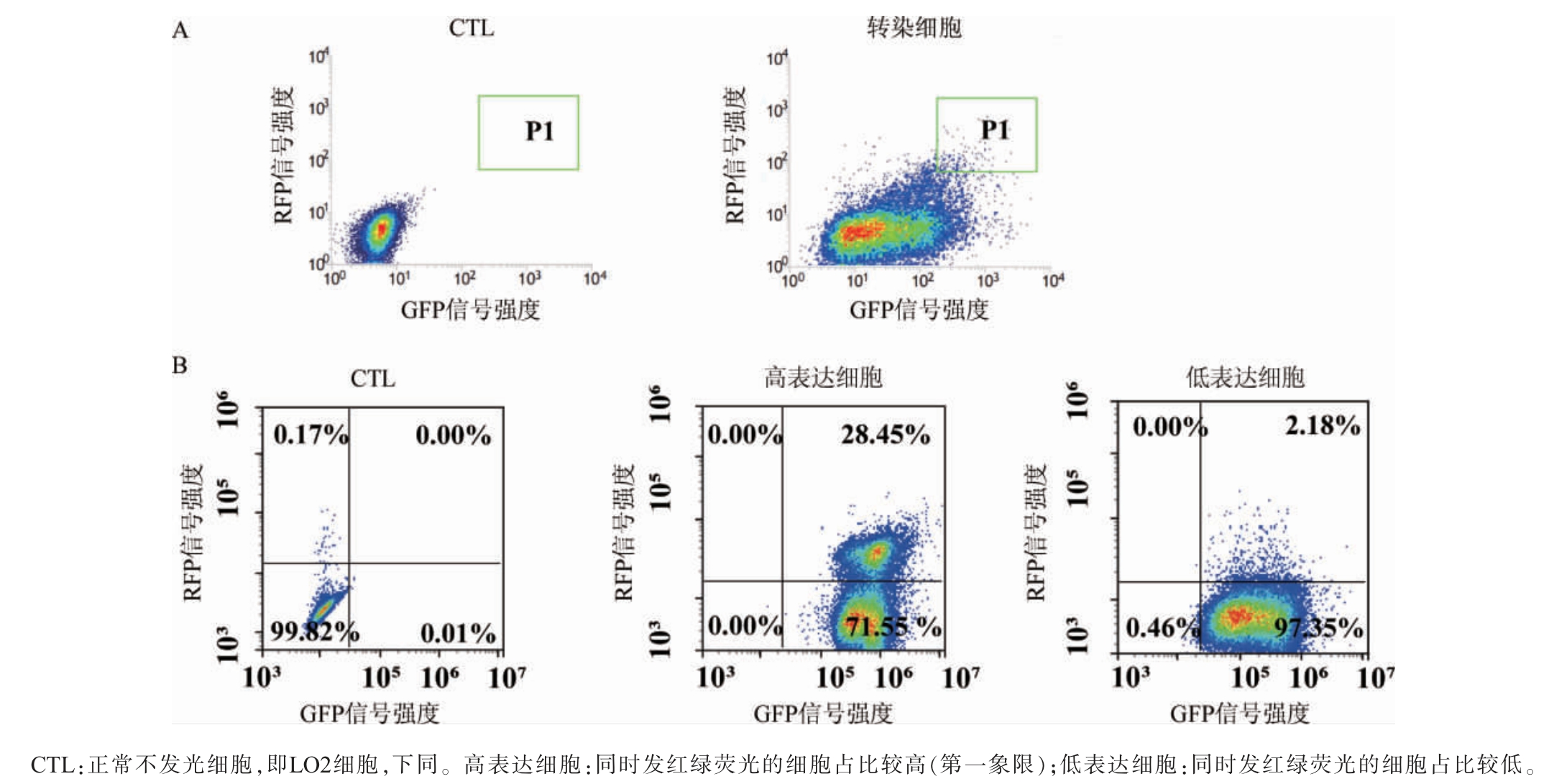
图1 稳定高效表达自噬通量探针LO2细胞的筛选
Fig. 1 Screening of LO2 cells with stable and highly efficient expression of autophagic flux probe
2.2 自噬通量荧光探针系统的可靠性验证
为评估所构建LO2-GFP-RFP细胞在检测自噬通量中的灵敏性与有效性,对其进行饥饿处理以及自噬抑制剂处理,结果见图2和表1。
表1 饥饿处理以及自噬抑制剂对细胞自噬通量的影响
Table 1 Effects of starvation treatment and autophagy inhibitors on autophagic flux
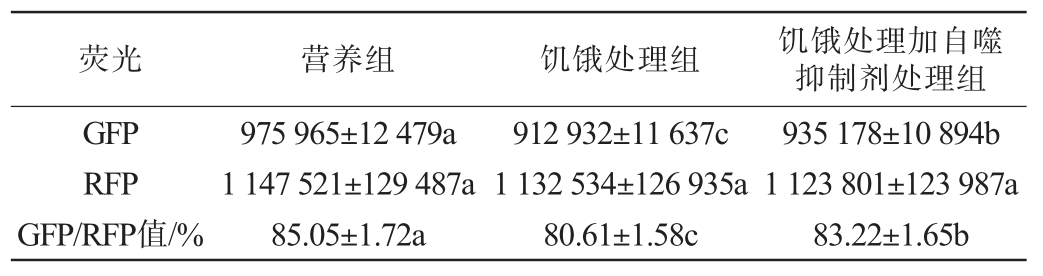
注:同行不同小写字母表示差异显著(P<0.05)。
荧光营养组饥饿处理组饥饿处理加自噬抑制剂处理组GFP RFP GFP/RFP值/%975 965±12 479a 1 147 521±129 487a 85.05±1.72a 912 932±11 637c 1 132 534±126 935a 80.61±1.58c 935 178±10 894b 1 123 801±123 987a 83.22±1.65b
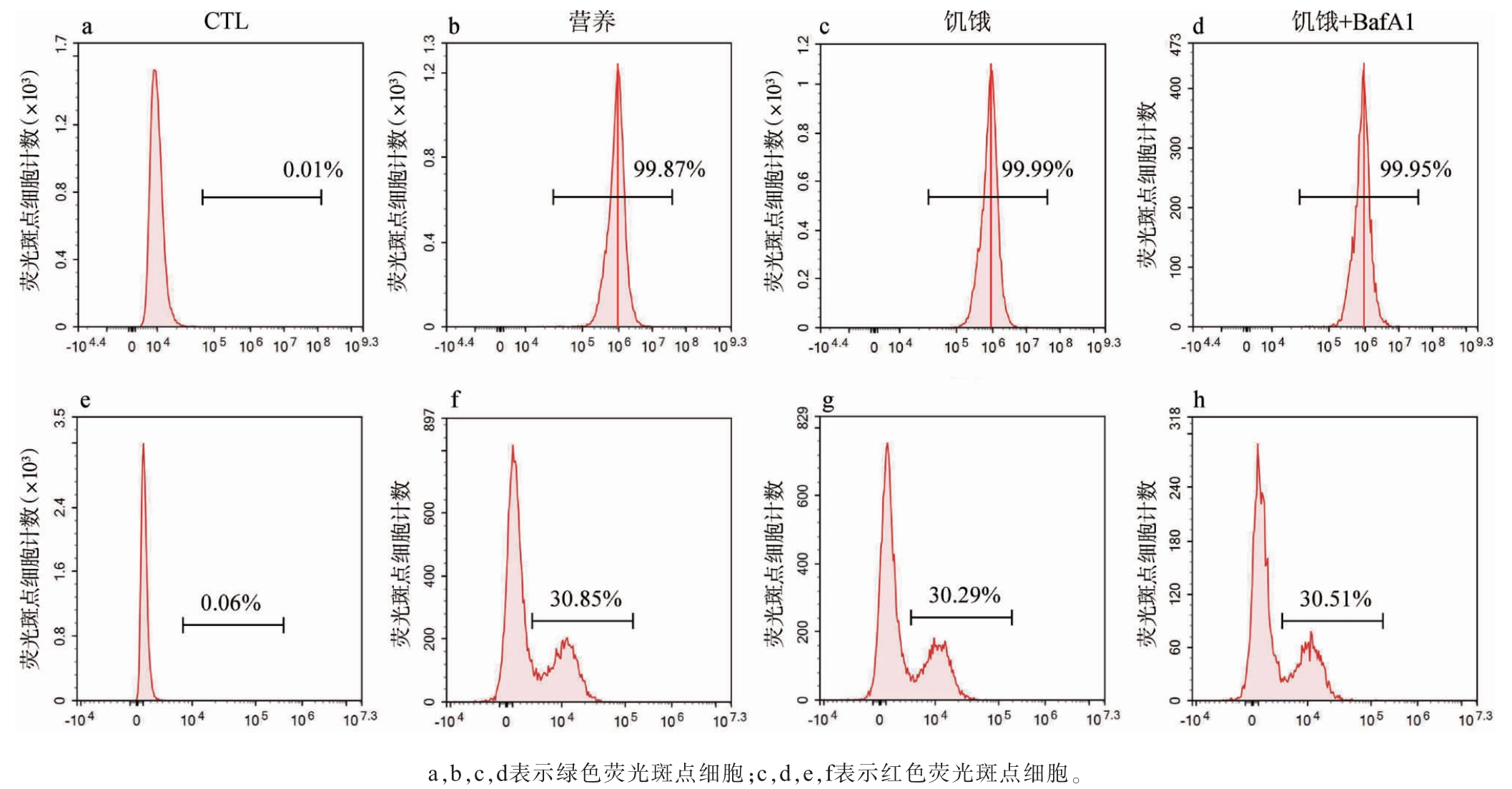
图2 饥饿处理以及自噬抑制剂对细胞自噬通量影响的流式直方图
Fig. 2 Flow cytometry histogram of effects of starvation treatment and autophagy inhibitors on cellular autophagic flux
由图2和表1可知,与营养组相比,饥饿处理显著降低了GFP/RFP值(从85.05%下降到80.61%)(P<0.05),表明自噬活性增强导致GFP-LC3降解增加;而在加入自噬抑制剂BafA1后,GFP/RFP比值显著回升(从80.61%上升到83.22%)(P<0.05),证实自噬在溶酶体降解阶段被有效阻断。综上,GFP-LC3-RFP-LC3ΔG探针系统能够灵敏、准确地反映细胞自噬通量的变化,适用于后续活性成分的筛选与评价。
2.3 白酒微量成分对LO2细胞自噬通量的调控作用
2.3.1 不同浓度月桂酸对细胞自噬通量的影响
月桂酸是一种在椰子产品中发现的饱和脂肪酸[23],也存在于白酒中,具有抗菌、抗炎、调节脂质和抗氧化的特性[24-26]。月桂酸作为一种中链饱和脂肪酸,其代谢过程与细胞能量稳态密切相关[27]。在一定浓度下,月桂酸可能通过激活腺苷酸活化蛋白激酶(adenosine monophosphate-activated protein kinase,AMPK)信号通路来诱导自噬[13,28]。通过流式细胞仪检测月桂酸处理组的GFP和RFP荧光强度,并通过WB检测LO2-GFP-RFP细胞中P62和LC3蛋白的表达水平,结果见图3。
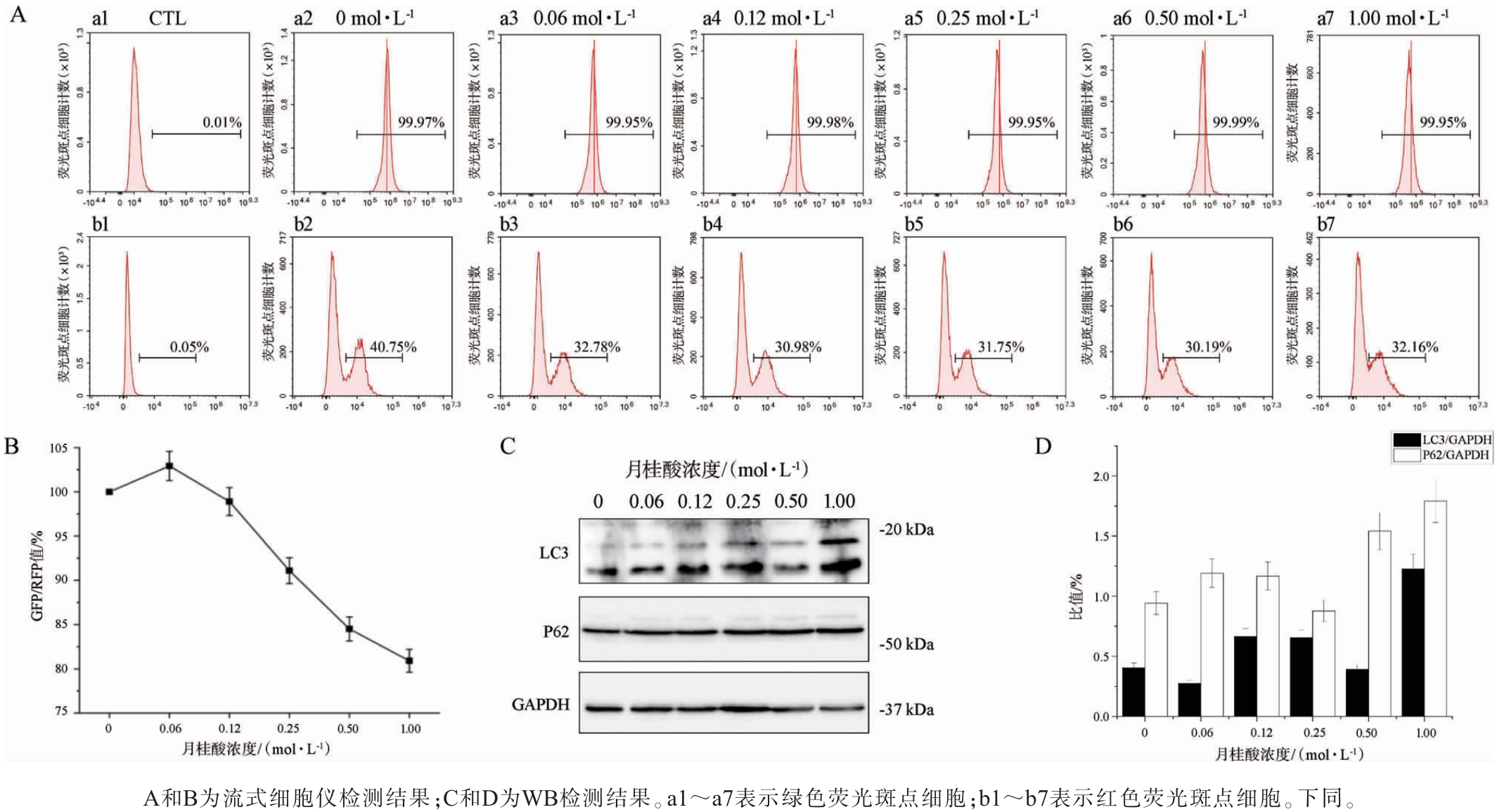
图3 不同浓度月桂酸对LO2细胞自噬通量的影响
Fig. 3 Effect of different concentrations of lauric acid on LO2 cellular autophagic flux
由图3A和3B可知,在月桂酸浓度为0.06 mol/L时LO2-GFP-RFP细胞表征为抑制自噬,随着月桂酸浓度在0.12~1.00 mol/L范围内的增加,GFP荧光强度呈现下降趋势,而RFP荧光强度基本维持稳定,导致GFP/RFP值降低,说明月桂酸在0.12~1.00mol/L浓度范围内促进了自噬流的进程。由图3C和3D可知,在月桂酸浓度为0.06 mol/L时LO2-GFP-RFP细胞表征为抑制自噬,这与流式细胞仪检测结果一致。当月桂酸浓度为0.12 mol/L、0.25 mol/L、1.00 mol/L时,LC3蛋白表达水平升高,可以判定在这3个浓度条件下月桂酸促进LO2-GFP-RFP细胞发生了自噬,与流式细胞仪检测结果一致。综合分析WB检验结果发现在月桂酸添加量为0.06mol/L、0.12 mol/L、0.50 mol/L、1.00 mol/L时,P62蛋白表达水平同步升高,分析原因可能是由于P62编码基因选择性自噬接头蛋白1(sequestosome 1,SQSTM1)的表达受AMPK与核因子-E2相关因子2(nuclear factor erythroid 2-related factor 2,Nrf2)通路双重调控所致。 AMPK可通过激活转录因子EB(transcription factor EB,TFEB)/转录因子E3(transcription factor E3,TFE3),直接促进SQSTM1转录;同时,AMPK磷酸化P62的S24/S226位点,增强其与kelch样环氧氯丙烷相关蛋白1(kelch-like ECH-associated protein 1,Keap1)结合,释放Nrf2并进一步上调SQSTM1表达,形成“AMPK激活→P62合成增加→P62堆积”的正反馈循环,即使降解正常,P62合成速率也可能超过降解速率[29]。月桂酸激活AMPK后,自噬体生成是快速反应(30~60 min),而溶酶体降解需2~4 h完成。因此,若检测时间点处于自噬体大量生成但降解尚未启动或完成的窗口期,会呈现LC3与P62同步升高的现象。
2.3.2 不同浓度4-甲基愈创木酚对细胞自噬通量的影响
4-甲基愈创木酚不仅存在于植物中,也存在于中国白酒中。研究发现,这种化合物通过激活Keap1-Nrf2抗氧化信号通路,具有显著的抗氧化特性[30],这一过程可提高转录因子Nrf2蛋白的水平,从而上调抗氧化相关基因的表达[9]。同时,作为自噬核心的蛋白P62也通过与Keap1竞争性结合并促进其自噬降解而发挥着关键作用,这一过程导致Nrf2蛋白释放并转运至细胞核,从而发挥其抗氧化作用[31]。通过P62蛋白和Nrf2蛋白之间的协同作用,4-甲基愈创木酚可有效保护细胞免受氧化应激引起的损伤[9]。通过流式细胞仪检测4-甲基愈创木酚处理组的GFP和RFP荧光强度,并通过WB检测LO2细胞中P62和LC3蛋白的表达水平,结果见图4。
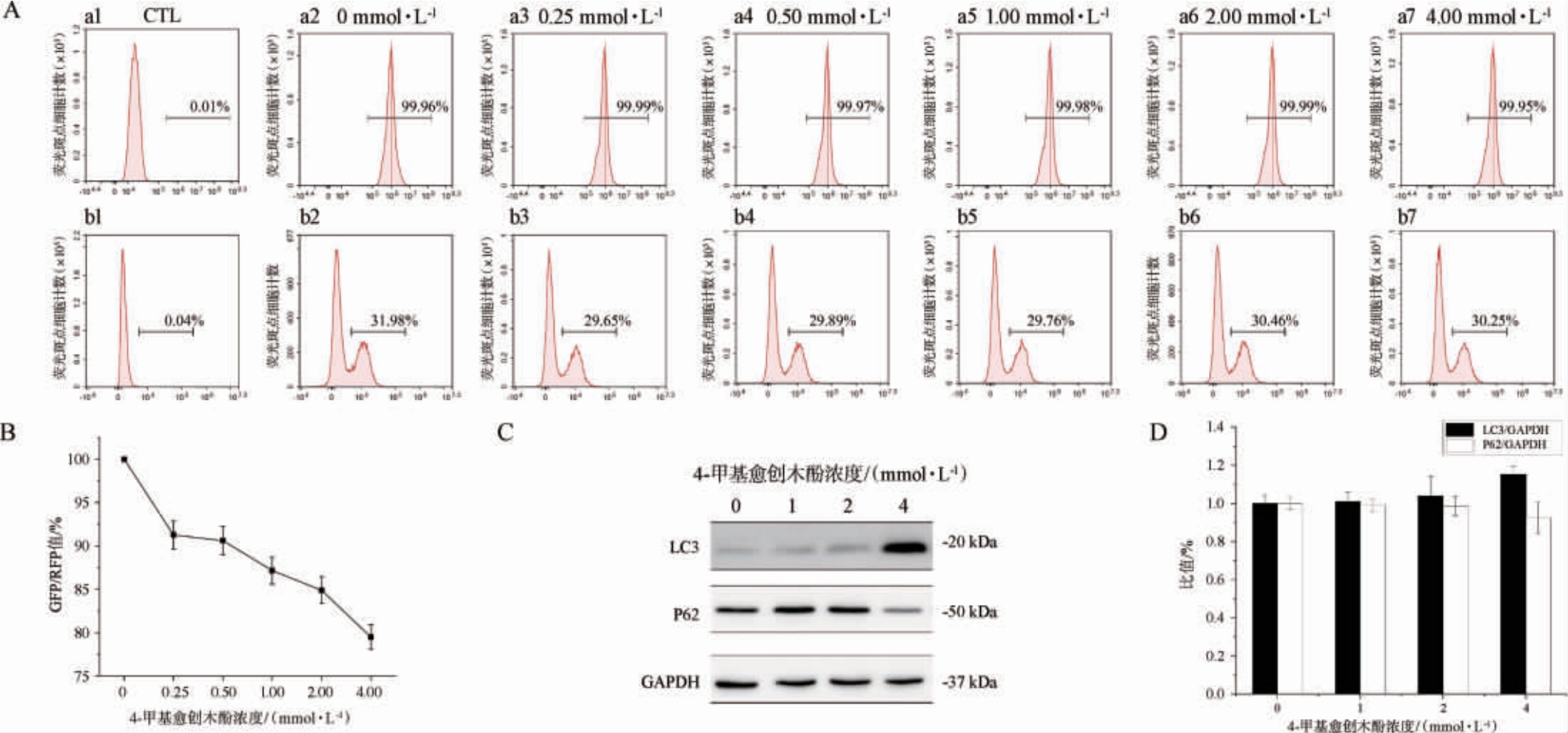
图4 不同浓度的4-甲基愈创木酚对LO2细胞自噬通量的影响
Fig. 4 Effects of different concentrations of 4-methylguaiacol on LO2 cellular autophagic flux
由图5A和B可知,随着4-甲基愈创木酚在0~4 mmol/L浓度范围内的增加,GFP荧光强度逐渐降低,而RFP荧光强度保持稳定,GFP/RFP值逐渐降低,表明4-甲基愈创木酚在0~4 mmol/L的浓度范围内随着浓度的升高自噬活性增强,表现出浓度依赖性。由图5C和D可知,4-甲基愈创木酚浓度的增加导致P62蛋白表达水平逐渐下降,LC3蛋白表达水平随之上升,表明4-甲基愈创木酚具有诱导自噬的能力,随着其浓度的增加,细胞的自噬活性会逐渐增强。
综上,流式细胞术测得的荧光信号变化值反映的细胞自噬结果与WB检测结果相吻合,表明构建的细胞自噬通量探针结合流式细胞仪可以用来检测月桂酸、4-甲基愈创木酚对人正常肝细胞LO2自噬的影响,且流式细胞术检测的双荧光蛋白信号变化结果更明显,结果更易判定。
3 结论
本研究以人正常肝细胞LO2为载体,采用慢病毒转导与流式细胞术分选的方法成功构建并筛选出稳定高效表达自噬通量探针GFP-LC3-RFP-LC3ΔG的细胞株LO2-GFP-RFP,对其进行饥饿处理可使GFP/RFP值从85.05%降至80.61%,而通过饥饿处理同时加入自噬抑制剂BafA1后可使GFP/RFP值回升至83.22%,说明该自噬通量探针的流式检测技术能灵敏响应细胞自噬调节。通过自噬通量探针结合流式检测技术与WB相互印证了月桂酸和4-甲基愈创木酚在一定浓度范围内对细胞自噬的调控作用,且基于自噬通量探针结合流式检测技术相较于WB具有更高通量与效率,适用于白酒微量成分自噬调节活性的快速筛选,为解析白酒健康效应提供了有效方法平台。
[1] SUN J Y,ZHU Y M,WANG P Y,et al.Research progress in the flavor chemistry and health effects of Baijiu[J] .Agric Prod Process Stor,2025,1(1):1-21.
[2] HONG J X, ZHAO D R, SUN B G. Research progress on the profile of trace components in Baijiu[J] .Food Rev Int,2023,39(3):1666-1693.
[3] SUN X F,OU Z H,CHEN R C,et al.Activation of the p62-Keap1-NRF2 pathway protects against ferroptosis in hepatocellular carcinoma cells[J] .Hepatology,2016,63(1):173-184.
[4] WU J H,HUO J Y,HUANG M Q,et al.Structural characterization of a tetrapeptide from sesame flavor-type Baijiu and its preventive effects against AAPH-induced oxidative stress in HepG2 cells[J] .J Agr Food Chem,2017,65(48):10495-10504.
[5] NI D R,CHEN C,YANG Y B,et al.Changes in polyphenols and antioxidant activity in fermentation substrate during Maotai-flavored liquor processing[J] .Foods,2024,13(12):1928.
[6] 李善文,王德良,黄和强,等.基于细胞自噬研究青稞酒及其特有功能成分对肝细胞作用机理的研究与应用[Z] . 海东:青海互助天佑德青稞酒股份有限公司,2023-06-14.
[7] 张瞭飞.4-甲基愈创木酚对细胞自噬活性的影响及其对小鼠酒精性肝损伤的保护作用[D] .乌鲁木齐:新疆农业大学,2021.
[8] CAO W Y,LI J H,YANG K P,et al.An overview of autophagy:Mechanism,regulation and research progress[J] .Bull Cancer,2021,108(3):231575188.
[9] LI A J,CHEN S B,YANG Z,et al.4-Methylguaiacol alleviated alcoholic liver injury by increasing antioxidant capacity and enhancing autophagy through the Nrf2-Keap1 pathway[J] .Food Biosci,2023,51:304-322.
[10] 王宠,张萍,朱卫国,等. 细胞自噬与肿瘤发生的关系[J] . 中国生物化学与分子生物学报,2010(11):17-26.
[11] YA D S,GUO B,JIANG Y L,et al.Interleukin 13 alleviates traumatic brain injury by promoting pericyte autophagy[J] .Free Radic Biol Med,2025,241:384-410.
[12] KLIONSKY D J,ABDELMOHSEN K,ABE A,et al.Guidelines for the use and interpretation of assays for monitoring autophagy(3rd edition)[J] .Autophagy,2016,12(1):1-222.
[13] FILALI-MOUNCEF Y, HUNTER C, ROCCIO F, et al. The ménage à trois of autophagy,lipid droplets and liver disease[J] .Autophagy,2022,18(1):50-72.
[14] 李晨红,宋长丰,林志康,等. 蛇葡萄素对结肠癌细胞增殖抑制、自噬诱导及自噬对增殖的影响研究[J] .四川师范大学学报(自然科学版),2021,44(3):390-397.
[15] BOYLE K B,RANDOW F. The role of 'eat-me' signals and autophagy cargo receptors in innate immunity[J] .Curr Opin Microbiol,2013,16(3):339-348.
[16] KAIZUKA T,MORISHITA H,HAMA Y,et al.An autophagic flux probe that releases an internal control[J] .Molecular Cell,2016,64(4):835-849.
[17] 姜晨,吴昕曈,陈慧玲,等.重组蔗糖异构酶在枯草芽孢杆菌中的表达及发酵优化[J] .生物学杂志,2024,41(6):39-46.
[18] 李贺侠.PI3K/AKT信号通路在FABP疫苗特异性免疫治疗中的作用机理研究[D] .淮南:安徽理工大学,2017.
[19] HADI F,MARYAM A,HADI A, et al. Induction of proteome changes involved in the cloning of mcr-1 and mcr-2 genes in Escherichia coli DH5-α strain to evaluate colistin resistance[J] .J Glob Antimicrob Resist,2023,36:151-159.
[20] KIM J H,LEE E J,HAN K H.An antagonist antibody that inhibits cancer cell growth in vitro through RACK1[J] .Pharmaceuticals,2024,17(10):1303.
[21] 王霞,叶曼红,黄智璇,等.沉默STAT3对姜黄素抑制食管癌细胞增殖、迁移的影响[J] .医学理论与实践,2024,37(24):4141-4144,4170.
[22] 邱香.p62蛋白稳态对细胞自噬的影响[D] .贵阳:贵州大学,2025.
[23] RAMYA V,SHYAM K P,KOWSALYA E,et al.Dual roles of coconut oil and its major component lauric acid on redox nexus:Focus on cytoprotection and cancer cell death[J] .Front Neurosci,2022,16:833630.
[24] KHAN H U, AAMIR K, JUSUF P R, et al. Lauric acid ameliorates lipopolysaccharide (LPS)-induced liver inflammation by mediating the TLR4/MyD88 pathway in Sprague Dawley(SD)rats[J] .Life Sci,2020,265:118750.
[25] GAO L,JIN L H,ZHANG S N,et al.Fabrication of novel polysaccharides and glycerol monolaurate based camellia oil composite oleogel:Application in wound healing promotion[J] .Int J Biol Macromol,2024,281(P1):136239.
[26] BOSE D, OLORUNLANA A, ABDEL-LATIF R, et al. Virgin coconut oil and its lauric acid, between anticancer activity and modulation of chemotherapy toxicity:A review[J] .J Xenobiotics,2025,15(4):126.
[27] AMEENA M,ARUMUGHAM M,RAMALINGAM K,et al.Biomedical applications of lauric acid:A narrative review[J] . Cureus,2024,16(6):e62770.
[28] KIM D H. Contrasting views on the role of AMPK in autophagy[J] .Bioessays,2024,46(3):e202300211.
[29] CHOI E J,OH H T,LEE S H,et al.Metabolic stress induces a doublepositive feedback loop between AMPK and SQSTM1/p62 conferring dual activation of AMPK and NFE2L2/NRF2 to synergize antioxidant defense[J] .Autophagy,2024,20(11):2490-2510.
[30] ZHAO D R,SHI D M,SUN J Y,et al.Quantification and cytoprotection by vanillin,4-methylguaiacol and 4-ethylguaiacol against AAPH-induced abnormal oxidative stress in HepG2 cells[J] . RSC Adv, 2018, 8(62):35474-35484.
[31] KHAN H, TUNDIS R, ULLAH H, et al. Flavonoids targeting NRF2 in neurodegenerative disorders[J] .Food Chem Toxicol,2020,146:111817.