发酵肉制品是以畜禽肉为原料,添加食盐、香辛料等调味品,在自然或人工条件下经特定微生物和酶的作用,加工制成的一类产品[1]。发酵肉制品产品质量与微生物菌群结构紧密相关,而生产环境、加工操作以及包装环节等都可能造成微生物菌群的改变,因此,许多研究人员采用接种外源微生物来改善发酵肉制品品质[2]。目前,寻求菌种发酵剂应用于肉制品发酵一直是备受关注的研究方向。
发酵肉制品中涉及的微生物主要包括酵母菌、葡萄球菌、乳酸菌等,不同的菌株将发挥不同的作用。酵母菌具有广泛的脂肪酶与蛋白酶活性,对肉中的脂肪和蛋白质的分解发挥促进作用;乳酸菌能快速降低肉制品的pH,抑制腐败菌、病原菌的生长,保证后续的发酵可以正常进行;葡萄球菌具有广泛的过氧化氢酶和硝酸还原酶活性,能很好的促进肉制品发色[3]。王福清等[4]从发酵牦牛肉中分离出格氏乳球菌(Lactococcus garvieae)和清酒乳杆菌(Lactobacillus sakei),并将L.sakei与酵母菌复配发酵发现其可对肉制品品质产生积极影响;吴昕颖等[5]从宣威火腿中筛选出乳酸菌并对其进行生产性能评价,将菌株应用于发酵肉后发现L.sakei KULG13在一定程度上改善了肉制品的品质且提升了肉类风味化合物的浓度;落桑央吉等[6]从西藏牦牛肉中分离出的诞沫假丝酵母(Candida zeylanoides)M1-3M和扣囊复膜孢酵母(Saccharomycopsis fibuligera)C-2产蛋白酶能力较强,酶活分别为76.20和67.86 U/mL,马克斯克鲁维酵母(Kluyveromyces marxianus)B2产脂肪酶能力较强,酶活达到58.91 U/mL,3株菌之间无拮抗作用,有望作为发酵肉制品加工的混菌发酵剂;韩永霞等[7]从发酵羊腿中筛选出了具有良好产酸、耐食盐、耐亚硝酸盐的植物乳植杆菌(Lactiplantibacillus plantarum)和肉葡萄球菌(Staphylococcus carnosus),将这两株菌复配接种猪肉香肠后,显著提高了猪肉香肠中的营养物质,降低了组胺、酪胺等有害胺类的含量;周佳乐等[8]对肉源乳酸菌的生长特性和发酵特性进行研究,发现L.plantarum、戊糖片球菌(Pediococcus pentosaceus)、乳酸片球菌(Pediococcus acidilactici)可耐受65 ℃高温、6%的NaCl、100 mg/kg的NaNO2,对葡萄糖和蛋白质均有降解能力,可作为菌种发酵剂应用于发酵肉制品的开发;HU M Z等[9]从腊肉中筛选出木糖葡萄球菌(Staphylococcus xylosus)P2,并将其应用到牛肉发酵后,牛肉的颜色、气味、质地及风味都得到了提升。 生长培养基的组成(氮和碳源的类型)、温度、矿物质成分和通气水平会显著影响风味物质的生物合成,因此,目前的研究多选择肉类模型和肉制品来研究微生物对风味贡献的影响,模拟肉汤培养基是很好的研究体系,可以较好反映菌株在肉制品中的生长情况以及对发酵肉制品风味的影响[10]。
本研究以从发酵肉制品(腊肉和香肠)中分离鉴定得到的9株菌株(3株酵母菌、3株乳酸菌、3株葡萄球菌)为研究对象,采用模拟肉汤培养基,对其生物学性能及产香特性进行测试分析,优选出适合肉制品发酵的菌株,为发酵肉制品的研究与应用提供参考。
1 材料与方法
1.1 材料与试剂
1.1.1 材料与菌株
汉逊德巴利酵母(Debaryomyces hansenii)LY090、汉逊德巴利酵母(Debaryomyces hansenii)Y52、季也蒙毕赤酵母(Pichia guilliermondii)LY190、植物乳植杆菌(Lactiplantibacillus plantarum)R3、植物乳植杆菌(Lactiplantibacillus plantarum)L19、清酒广布乳杆菌(Lactobacillus sakei)Q1、腐生葡萄球菌(Staphylococcus saprophyticus)S25、肉葡萄球菌(Staphylococcus carnosus)R1、木糖葡萄球菌(Staphy lococcus xylosus)M1:分离自四川腊肉和香肠,由四川农业大学食品学院畜产与发酵食品加工及安全实验室分离并保藏;猪里脊肉:雅安浙联优选超市。
1.1.2 试剂
氯化钠、氢氧化钠、溴甲酚紫、葡萄糖、MgSO4·7H2O、MnSO4·4H2O、FeSO4·7H2O、CaCO3、吐温80、磷酸吡哆醛、三丁酸甘油酯、硫酸(均为分析纯)、酵母浸粉(生化试剂):成都市科隆化学品有限公司;脱脂牛乳:恒天然商贸(上海)有限公司;亚硝酸盐(分析纯):四川金山制药有限公司;胰蛋白胨(生化试剂):青岛高科技工业园海博生物技术有限公司;色氨酸、组氨酸、酪氨酸、赖氨酸、鸟氨酸、精氨酸(纯度均为98.5%):上海康达氨基酸厂。其他试剂均为国产分析纯。
1.1.3 培养基
MSA肉汤培养基、MRS肉汤培养基、MRS培养基和酵母浸出粉胨葡萄糖(yeast extract peptone dextrose,YEPD)培养基:青岛高科技工业园海博生物技术有限公司;哥伦比亚血琼脂平板:南京全隆生物技术有限公司。
模拟肉汤培养基[3]:猪瘦肉1 000 g切成肉糜状,加1 000 mL蒸馏水,加热沸腾后继续煮制20 min,纱布过滤,蒸馏水补足到1 000 mL,加入5.0 g葡萄糖,121 ℃高压蒸汽灭菌20 min。
氨基酸肉汤培养基[11]:胰蛋白胨5 g/L、酵母浸粉5 g/L、氨基酸(色氨酸、组氨酸、酪氨酸、赖氨酸、鸟氨酸、精氨酸)5 g/L,氯化钠5 g/L、溴甲酚紫0.06 g/L、葡萄糖1 g/L、MgSO4·7H2O 0.2 g/L、MnSO4·4H2O 0.05 g/L、FeSO4·7H2O 0.04 g/L、CaCO3 0.1 g/L、吐温80 0.5 mL/L、磷酸吡哆醛0.05 g/L,pH调至5.3左右,121 ℃高压蒸汽灭菌15 min。
1.2 仪器与设备
HVE-50高压蒸汽灭菌锅:日本HIRAYAMA公司;DHP-9162型电热恒温培养箱、ZWY-2102C恒温振荡培养箱:上海恒科技有限公司;Thermo Scientific 1300生物安全柜:美国Thermo公司;PHSJ-3F pH计:上海雷磁仪器厂;UV-1800PC紫外分光光度计:上海美谱达仪器有限公司;6890N-5975C气相色谱-质谱(gas chromatography-mass spectrometry,GCMS)联用仪:美国Agilent Technologies公司。
1.3 方法
1.3.1 菌种活化
将酵母菌菌株LY090、LY190和Y52以3%(V/V)的接种量接种于YEPD液体培养基中,30 ℃条件下培养48 h,连续活化2次。将乳酸菌菌株Q1、L19和R3以3%(V/V)的接种量接种于MRS肉汤培养基中,37 ℃条件下培养24 h,连续活化2次。将葡萄球菌菌株R1、S25、M1以3%(V/V)的接种量接种于MSA培养基中,37 ℃条件下培养24 h,连续活化2次。
1.3.2 基本生物学性能测试
产粘试验[12]:将活化后的菌液按1%(V/V)的接种量接种于模拟肉汤培养基中,30 ℃条件下培养48 h,挑取菌落观察、记录。
产气试验[13]:将活化后的菌液按1%(V/V)的接种量接种于模拟肉汤培养基中,在30 ℃条件下静置培养48 h后,观察杜氏小管中有无气泡产生,记录菌株的产气情况。
产生物胺试验[11]:将活化后的菌液按1%(V/V)的接种量分别接种于含不同单一氨基酸的氨基酸肉汤培养基中,在30 ℃条件下培养48 h,观察培养基颜色变化。 若培养基呈紫色或酪氨酸沉淀消失,表示待测菌株为产胺阳性菌,若培养基呈黄色,表示待测菌株为产胺阴性菌。
溶血特性测定[14]:将活化后的菌液分别涂布于含绵羊血的哥伦比亚血琼脂平板上,细菌于37 ℃培养20~24 h,酵母于30 ℃培养48 h,观察菌落周围溶血环,判断其溶血性类型。 若菌落周围无透明圈形成,即无变化,说明为γ-溶血,可认为菌株不具有溶血性;若菌落周围呈现草绿色环,则为α-溶血;若菌落周围出现界限分明、完全透明的溶血环,则为β-溶血。
温度适应性测定[15]:将活化后的菌液按1%(V/V)的接种量接种于模拟肉汤培养基,分别于4 ℃、10 ℃、15 ℃、25 ℃、30 ℃、37 ℃条件下培养5 d,测定OD600nm值。
产蛋白酶及脂肪酶性能测定:参考陈瑶等[16]的方法进行测定。
生长曲线及产酸能力测定[17]:将活化的菌液按1%(V/V)的接种量分别接种于模拟肉汤培养基中,在30 ℃条件下培养48 h,平均2 h取1次样,测定其pH值及OD600 nm值,绘制生长曲线及产酸曲线。
1.3.3 耐受特性分析
将活化后的菌液按1%(V/V)的接种量分别接种于不同食盐含量(0、2%、4%、6%和8%)[18]、NaNO2含量(0、50 mg/kg、100 mg/kg、150 mg/kg、200 mg/kg和250 mg/kg)[19]及pH(3.0、3.5、4.0、4.5、5.0、5.5和6.0)[20]的模拟肉汤培养基中,30 ℃条件下培养48 h,采用紫外分光光度计在波长600 nm处测定OD600nm值,考察菌株的耐盐、耐亚硝酸盐及耐酸性能。
1.3.4 产香能力评价
将活化的菌液按1%(V/V)的接种量接种于模拟肉汤培养基中,于25 ℃、120 r/min条件下培养5 d,以未接菌的模拟肉汤培养基为空白对照(CK),采用顶空固相微萃取(headspace solid phase microextraction,HS-SPME)-GC-MS检测挥发性风味物质含量并计算气味活度值(odor activity value,OAV)[3,21]。气味活性值(OAV)指挥发性风味物质的含量与其嗅觉阈值的比值,用于衡量该成分对整体香气的贡献程度。OAV>1的化合物对整体香气的贡献程度较大,为关键挥发性风味物质;0.1≤OAV<1的化合物对整体香气具有修饰作用,为重要挥发性风味物质。
1.3.5 数据处理与统计分析
使用Excel 2019、IBM SPSS Statistics 22.0软件处理数据,结果以“平均值±标准偏差”表示,采用Origin 2021软件绘图。
2 结果与分析
2.1 基本生物学性能分析
2.1.1 产粘、产气、产胺及溶血特性分析
通过对9株菌株的产粘、产气、产胺及溶血特性分析,发现9株菌株均无产粘,杜氏小管中皆无气泡产生,且都没有溶血现象。菌株R1在添加酪氨酸和组氨酸的培养基中发酵后,培养基呈紫色,说明菌株R1为产生物胺阳性菌,然而其他菌株在添加氨基酸的培养基中发酵后,培养基呈黄色,说明不产生物胺。
2.1.2 温度适应性分析
在制作发酵肉制品的过程中,需经历多道温度变化,因此需要发酵菌株在每个生产环节的温度下皆具有一定的生长能力。因此,考察9株菌株的温度适应性,结果见图1。
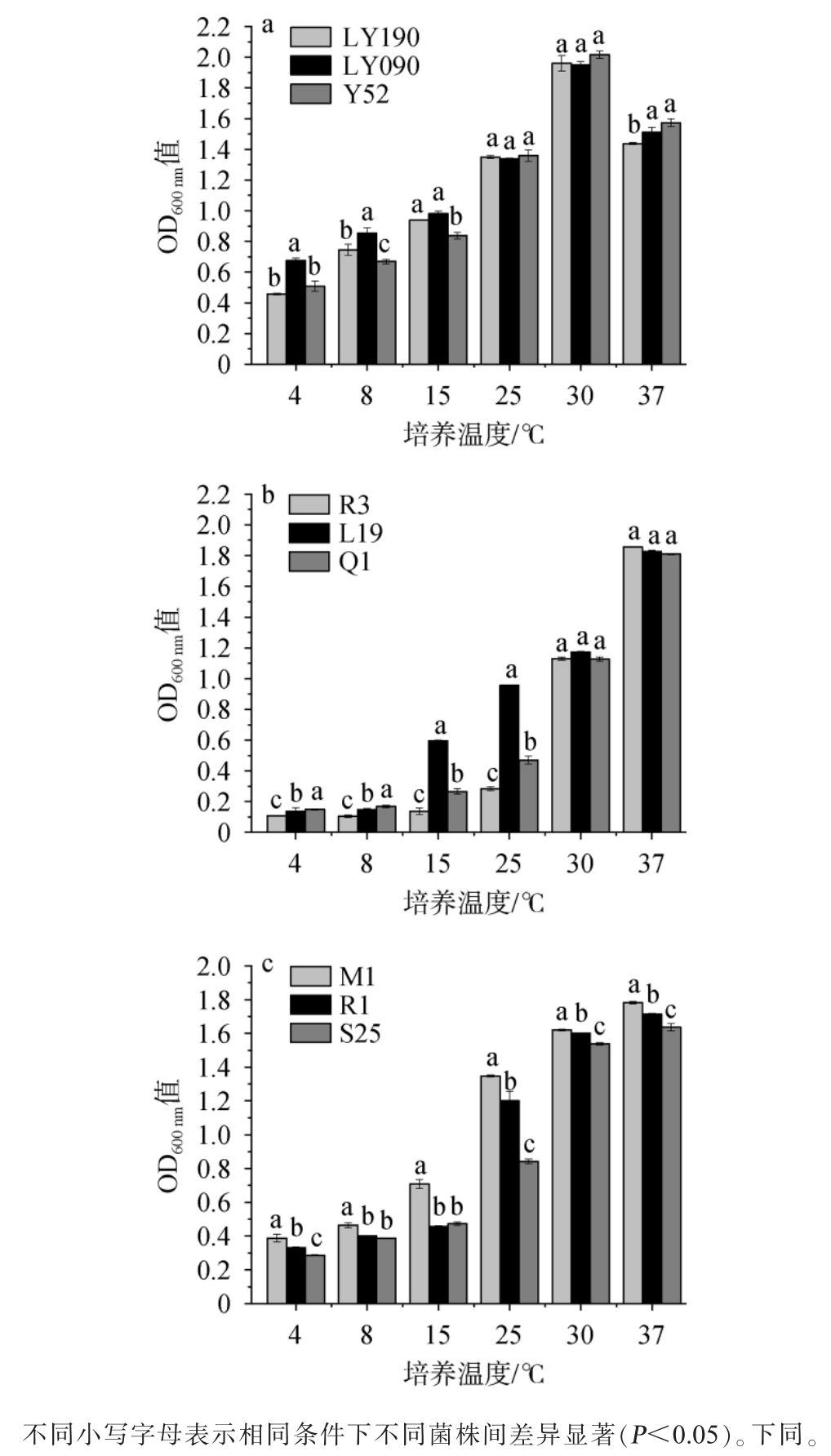
图1 9株菌株的温度适应性检测结果
Fig. 1 Determination results of temperature adaptability of 9 strains
由图1a可知,随着培养温度的升高,3株酵母菌株的OD600 nm值均呈先升高后降低的趋势。在4 ℃及8 ℃条件下,菌株LY090的OD600 nm值分别为0.68、0.86,皆显著高于菌株LY190和Y52(P<0.05)。当培养温度为30 ℃时,3株酵母菌株的OD600nm值均达到最大值,说明3株酵母菌株的最适生长温度均为30 ℃。当培养温度为37 ℃时,各菌株的OD600 nm值明显降低,但在各个温度条件下,菌株LY090的生长情况整体表现出较大优势。由图1b可知,随着培养温度的升高,3株乳酸菌菌株的OD600nm值均呈升高趋势。3株乳酸菌菌株在低温条件下即4 ℃、8 ℃时的生长情况较差,菌株R3和Q1在15 ℃和25 ℃条件下其生长状况仍然未见明显好转,而菌株L19从15 ℃开始生长能力变强,在15 ℃时的OD600 nm值为0.60,25 ℃时的OD600 nm值为0.960,皆显著优于菌株R3和Q1(P<0.05)。 当培养温度为30 ℃和37 ℃时,3株乳酸菌的生长情况无显著性差异(P>0.05)。 由图1c可知,随着培养温度的升高,3株葡萄球菌菌株的OD600 nm值均呈升高的趋势。菌株M1在各个温度下的生长能力始终显著优于菌株R1和S25(P<0.05)。
2.1.3 产蛋白酶及脂肪酶特性分析
9株菌株产蛋白酶及脂肪酶能力见表1。
表1 9株菌株产蛋白酶及脂肪酶能力测定结果
Table 1 Determination results of protease and lipase production abilities of 9 strains
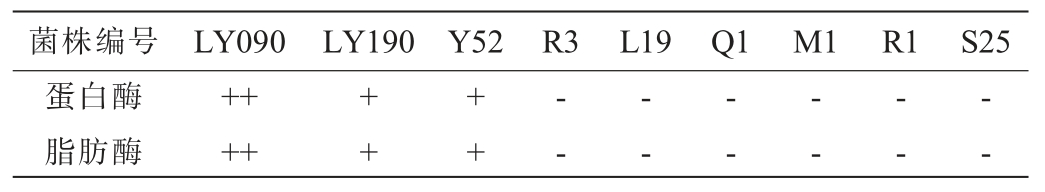
注:“++”表示产酶能力强,“+”表示产酶能力较强,“-”表示无产酶能力。
菌株编号 LY090 LY190 Y52 R3 L19 Q1 M1 R1 S25蛋白酶脂肪酶++++++++------------
由表1可知,3株酵母菌株在培养基上均产生了透明圈,说明3株酵母菌株皆具有产蛋白酶和脂肪酶的能力,其中以菌株LY090产生的透明圈最大,说明其分解蛋白质和脂肪的能力最强,然而,乳酸菌菌株Q1、L19、R3及葡萄球菌菌株R1、M1、S25在培养基上均未产生透明圈,说明这6株菌株均无产蛋白酶和脂肪酶的能力。
2.1.4 生长曲线及产酸能力分析
发酵肉制品的菌株要求具有一定的生长能力且能快速产酸[22]。因此,考察9株菌株的生长及产酸能力,结果见图2。
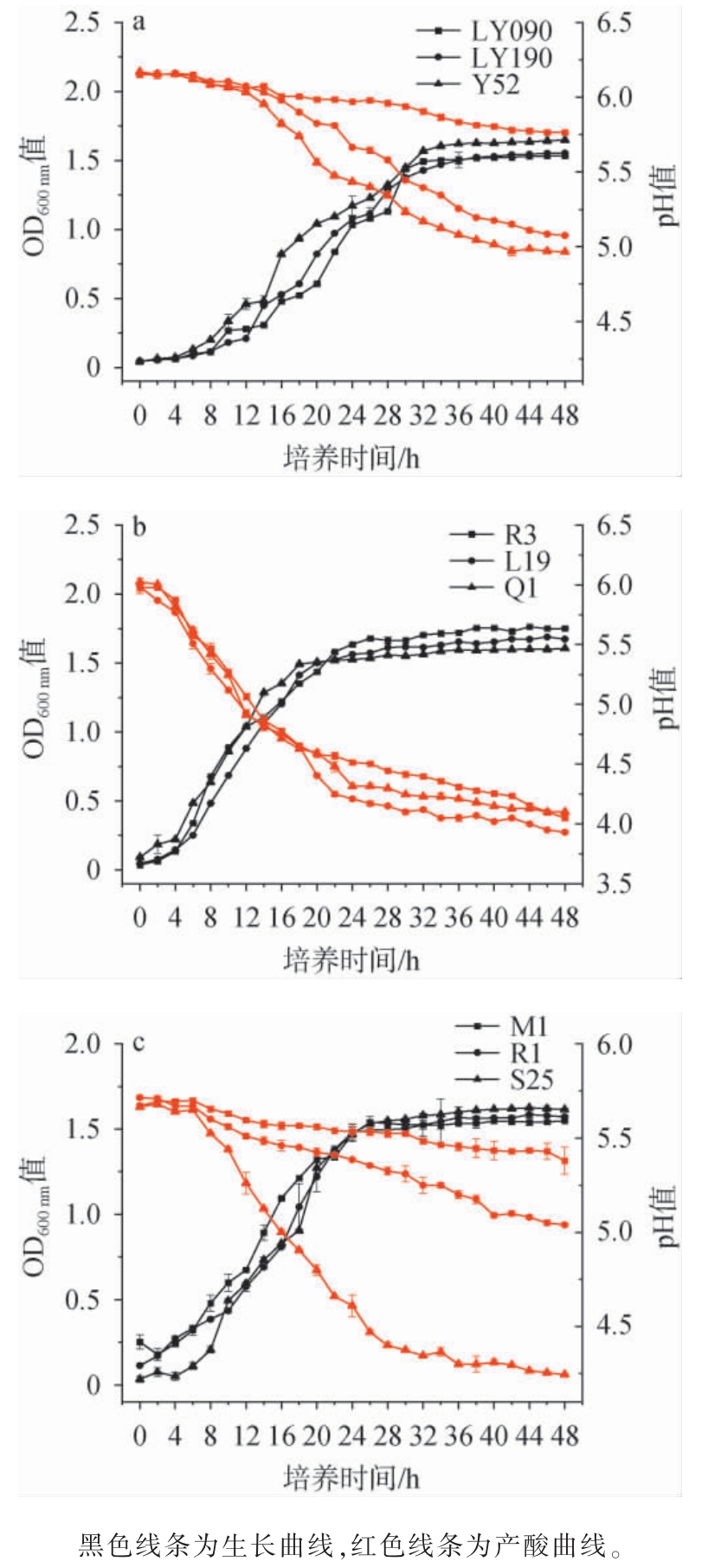
图2 9株菌株的生长曲线及产酸曲线
Fig. 2 Growth curves and acid production curves of 9 strains
由图2a可知,在3株酵母菌中,菌株LY090和LY190的生长曲线相似,延滞期均为0~8 h,对数生长期均为8~32 h,均在培养32 h后进入平稳期;然而,菌株Y52的延滞期为0~4 h,对数生长期持续时间更长,为4~36 h,培养36 h后进入平稳期。在培养过程中,菌株Y52的生长情况整体优于菌株LY190和LY090,其在培养48 h时,OD600 nm值为1.649。随着培养时间的延长,3株酵母菌株发酵液的pH均呈先下降后趋于平稳的趋势,且菌株Y52发酵液的pH最低,其次为菌株LY190,结果表明,菌株Y52的生长及产酸能力最强,而菌株LY090的产酸能力最弱。
由图2b可知,3株乳酸菌菌株的延滞期均为0~2 h,菌株Q1的对数生长期为2~18 h,菌株R3和L19的对数生长期稍长,均为2~22 h,菌株Q1在对数生长期生长情况最好,但在发酵48 h时,其OD600 nm值最低,为1.61,此时生长情况最好的为菌株R3,OD600nm值为1.75。随着培养时间的延长,3株乳酸菌菌株的产酸量逐渐增加,pH值逐渐降低,培养前8 h内,菌株Q1一直保持较快的产酸速度,在培养8 h时,pH为5.30,在培养12 h时,菌株L19和Q1发酵液的pH首先降低到5.0以下,分别为4.93和4.91,且产酸速度最快的为菌株L19,其在培养48 h时pH为3.93。结果表明,菌株L19的产酸能力最强。
由图2c可知,3株葡萄球菌菌株生长曲线相似,延滞期均为0~2 h,对数生长期均为2~24 h,在培养48 h时,菌株S25的OD600 nm值最高,为1.62,其次为菌株R1(OD600 nm值为1.57),菌株M1的OD600 nm值最小,为1.55。随着培养时间的延长,3株葡萄球菌菌株发酵液的pH均呈先下降后趋于平稳的趋势,且菌株S251发酵液的pH最低,其次为菌株R1,发酵48 h后,pH分别为4.25、4.99。 结果表明,菌株S25的生长及产酸能力最强,菌株M1的产酸能力最弱。
2.2 耐受性分析
2.2.1 耐盐特性分析
在发酵肉制品的制作过程中,食盐不仅是一种关键的调味品,还对发酵肉制品的品质和感官特性产生显著影响。随着肉制品发酵过程的推进,其水分逐渐减少,而食盐含量则相应增加[23]。因此,考察9株菌株的耐盐特性,结果见图3。
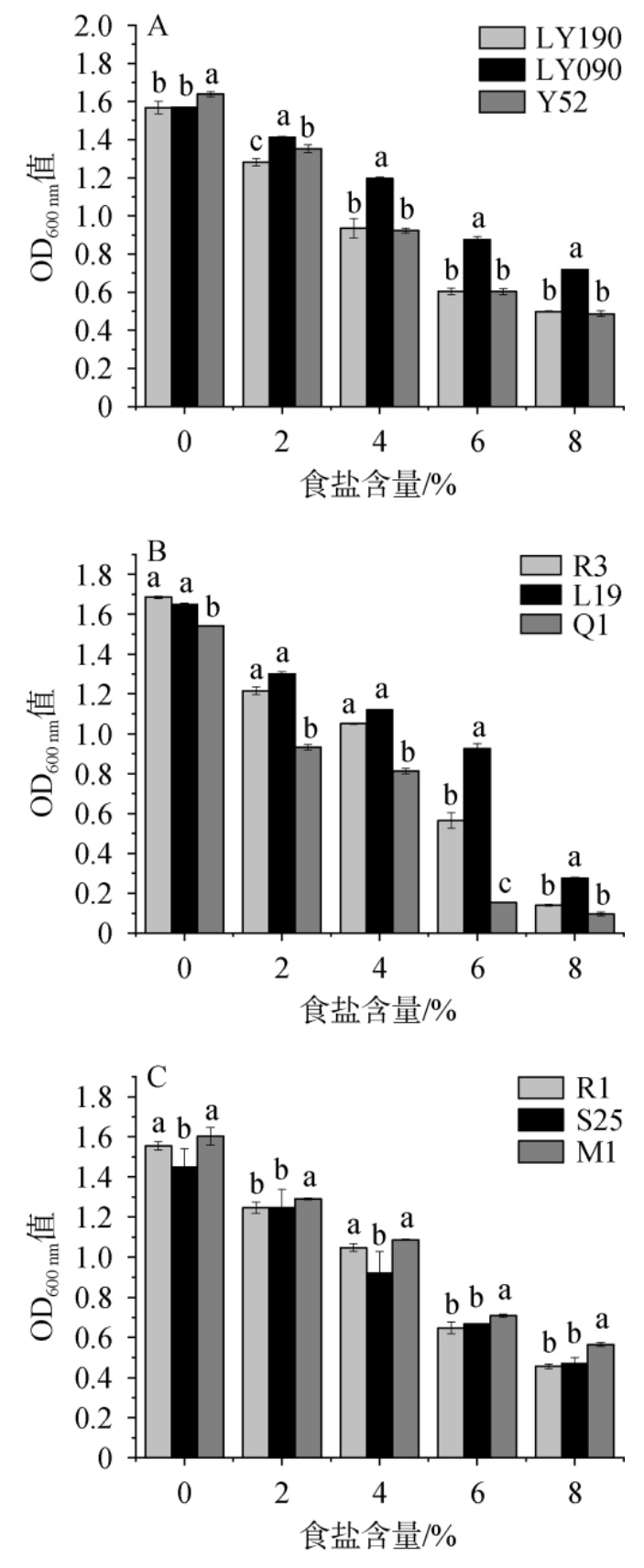
图3 9株菌株的耐盐特性分析结果
Fig. 3 Salt tolerance analysis results of 9 strains
由图3可知,随着食盐含量的升高,9株菌株的生长逐渐受到抑制,但均可在食盐含量为8%条件下生长。加入食盐后,酵母中菌株LY090的生长情况显著优于菌株LY190和Y52(P<0.05);乳酸菌中菌株L19的生长情况最好,其次为菌株R3;葡萄球菌中菌株M1的生长情况显著优于菌株R1和S25(P<0.05)。 结果表明,菌株LY090、L19及M1的耐盐特性较好。
2.2.2 耐亚硝酸盐特性分析
亚硝酸盐在肉制品加工中发挥着多重作用,包括改善色泽、提升风味以及延缓脂肪氧化,且具有抑制有害微生物生长的功能[24],因而被广泛用于发酵肉制品的生产。因此,考察9株菌株的耐亚硝酸盐特性,结果见图4。
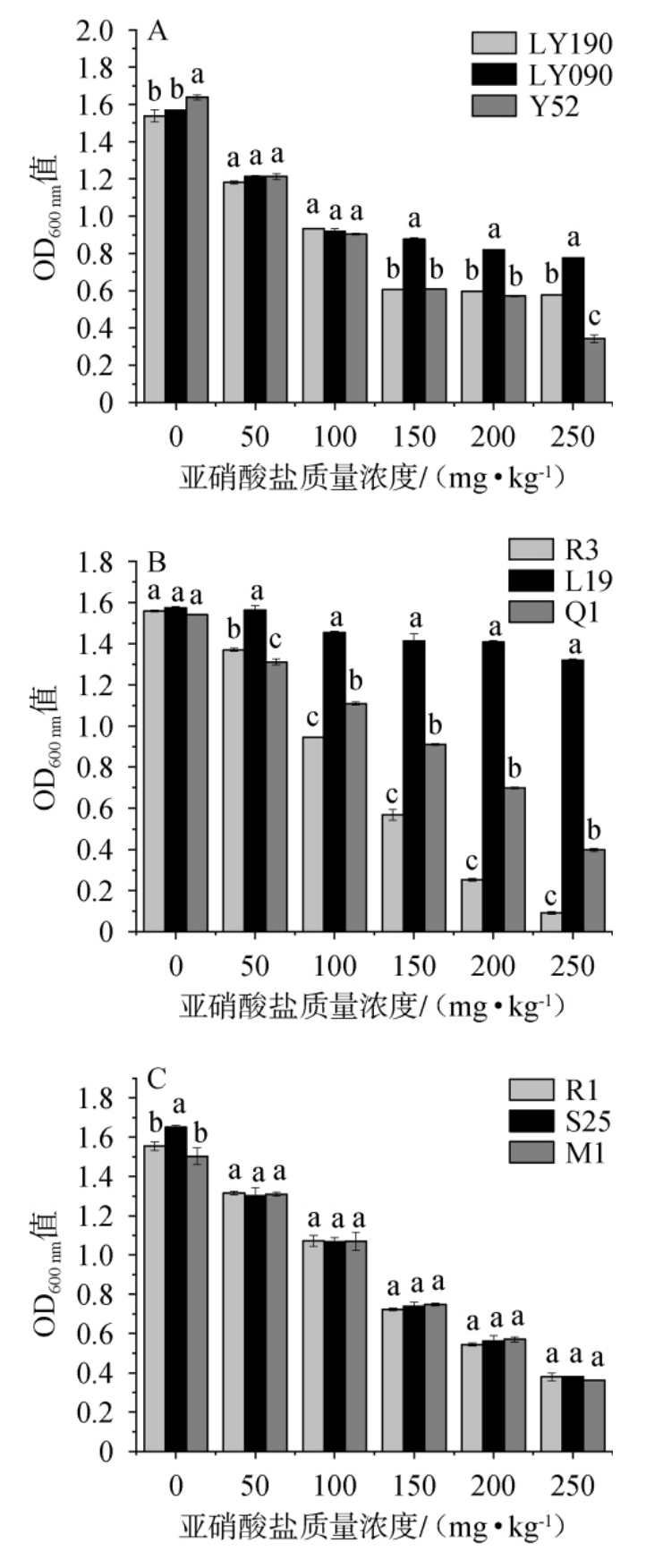
图4 9株菌株耐亚硝酸盐特性分析结果
Fig. 4 Nitrite tolerance analysis results of 9 strains
由图4可知,随着亚硝酸盐含量的升高,9株菌株的生长均逐渐受到抑制,但均可在亚硝酸盐含量为250 mg/kg条件下生长。在酵母菌株中,当亚硝酸盐含量>100 mg/kg之后,菌株LY090的生长情况显著优于菌株LY190和Y52(P<0.05)。在乳酸菌菌株中,菌株L19在添加亚硝酸盐的模拟肉汤中生长情况显著优于菌株R3和Q1(P<0.05)。3株葡萄球菌对亚硝酸盐的耐受能力并无显著差异(P>0.05),但菌株M1的耐受性相对较好。结果表明,菌株LY090、L19及M1的耐亚硝酸盐特性较好。
2.2.3 耐酸特性分析
乳酸菌具有较强的产酸能力,向肉制品中添加乳酸菌进行发酵后,肉中的pH会下降,因此,需要接种的菌株具备一定耐酸能力。考察9株菌株的耐酸特性,结果见图5。
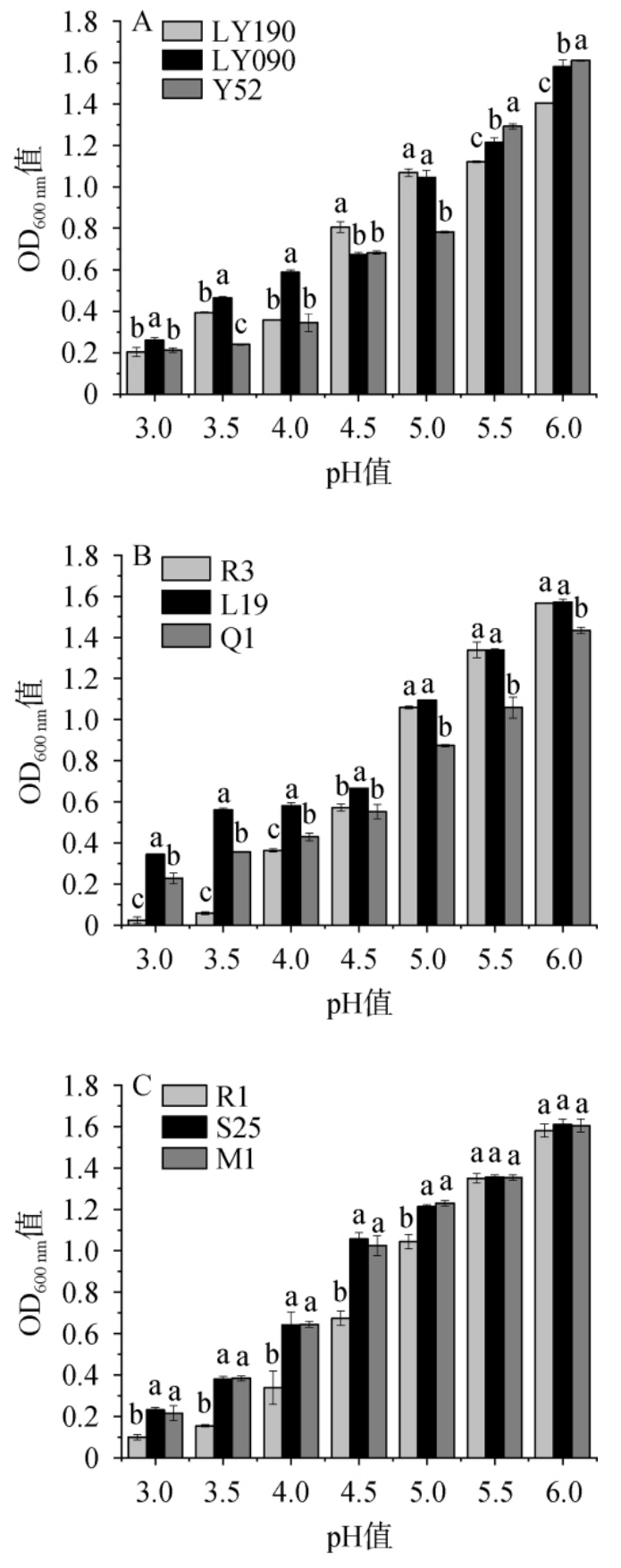
图5 9株菌株的耐酸特性分析结果
Fig. 5 Acid tolerance analysis results of 9 strains
由图5可知,随着pH的减小,9株菌株的生长均逐渐受到抑制。由图5A可知,当pH值为5.5和6.0时,菌株Y52的生长情况显著优于菌株LY090(P<0.05),而菌株LY090的生长情况又显著优于菌株LY190(P<0.05)。 然而,当pH<5.0时,菌株Y52的生长优势逐渐减弱。当pH为4.5和5.0时,菌株LY190的生长情况优于菌株LY090和Y52。 随着pH值进一步降低,菌株LY090的生长情况则显著优于菌株LY190和Y52(P<0.05)。由图5B可知,当pH为6.0、5.5和5.0时,菌株R3和L19的OD600 nm值显著高于菌株Q1(P<0.05),但当pH≤4.5时,菌株L19的生长状况显著优于菌株R3和Q1(P<0.05)。由图5C可知,3株葡萄球菌在pH为5.5和6.0的环境下,生长能力无显著性差异(P>0.05),但当pH值<5.5时,菌株S25和M1的生长情况显著优于菌株R1(P<0.05),且菌株M1的生长情况相对较好。结果表明,菌株LY090、L19及M1的耐酸特性较好。
2.3 产香特性分析
2.3.1 挥发性风味成分分析
采用GC-MS检测不同菌株发酵液中的挥发性风味成分,结果见表2。
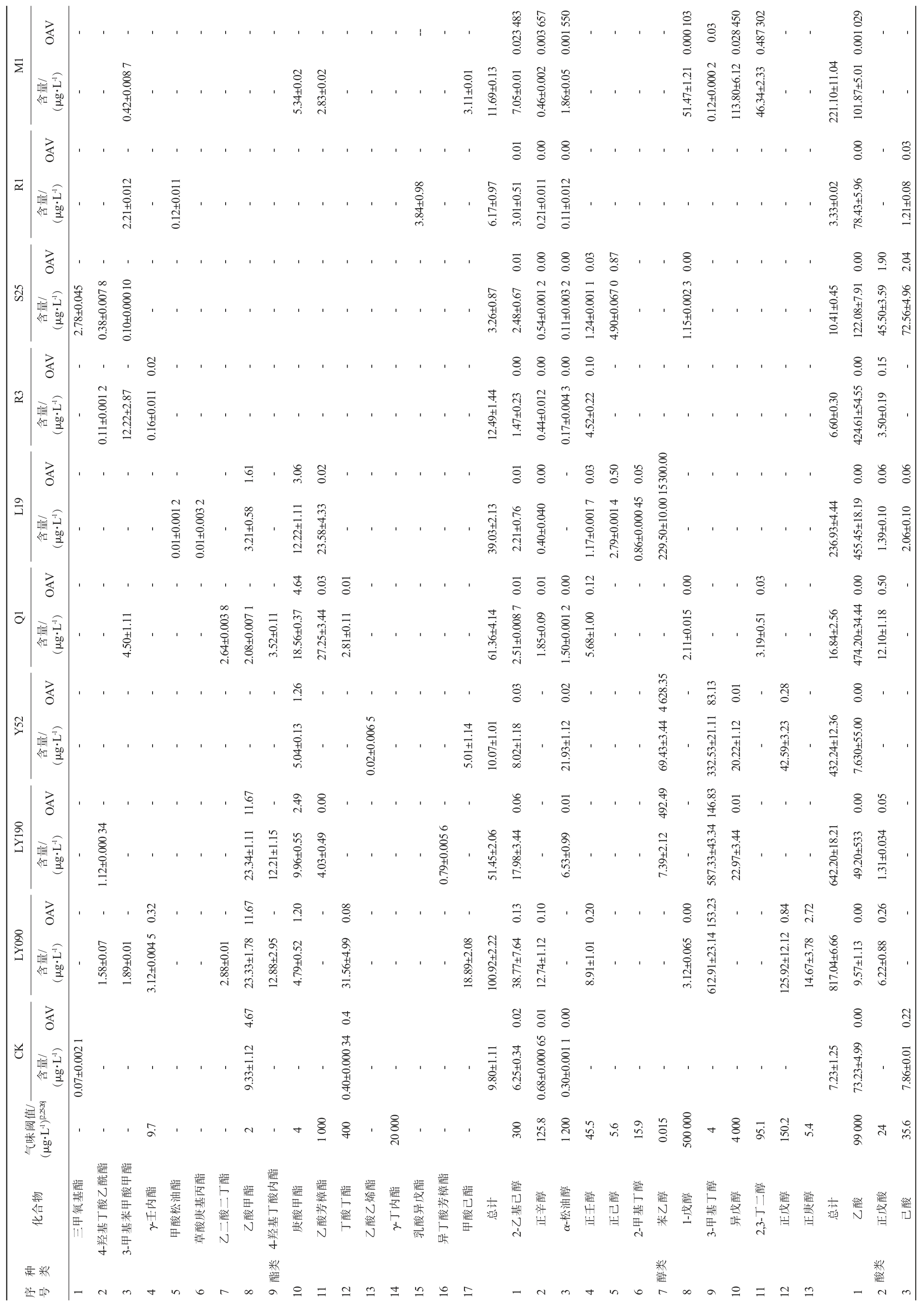
表2 9株菌株发酵液中挥发性风味物质含量GC-MS分析结果及气味活度值
Table 2 Resuts of volatile flavor compounds contents in fermentation broth of 9 strains analyzed by GC-MS and odor activity values
?
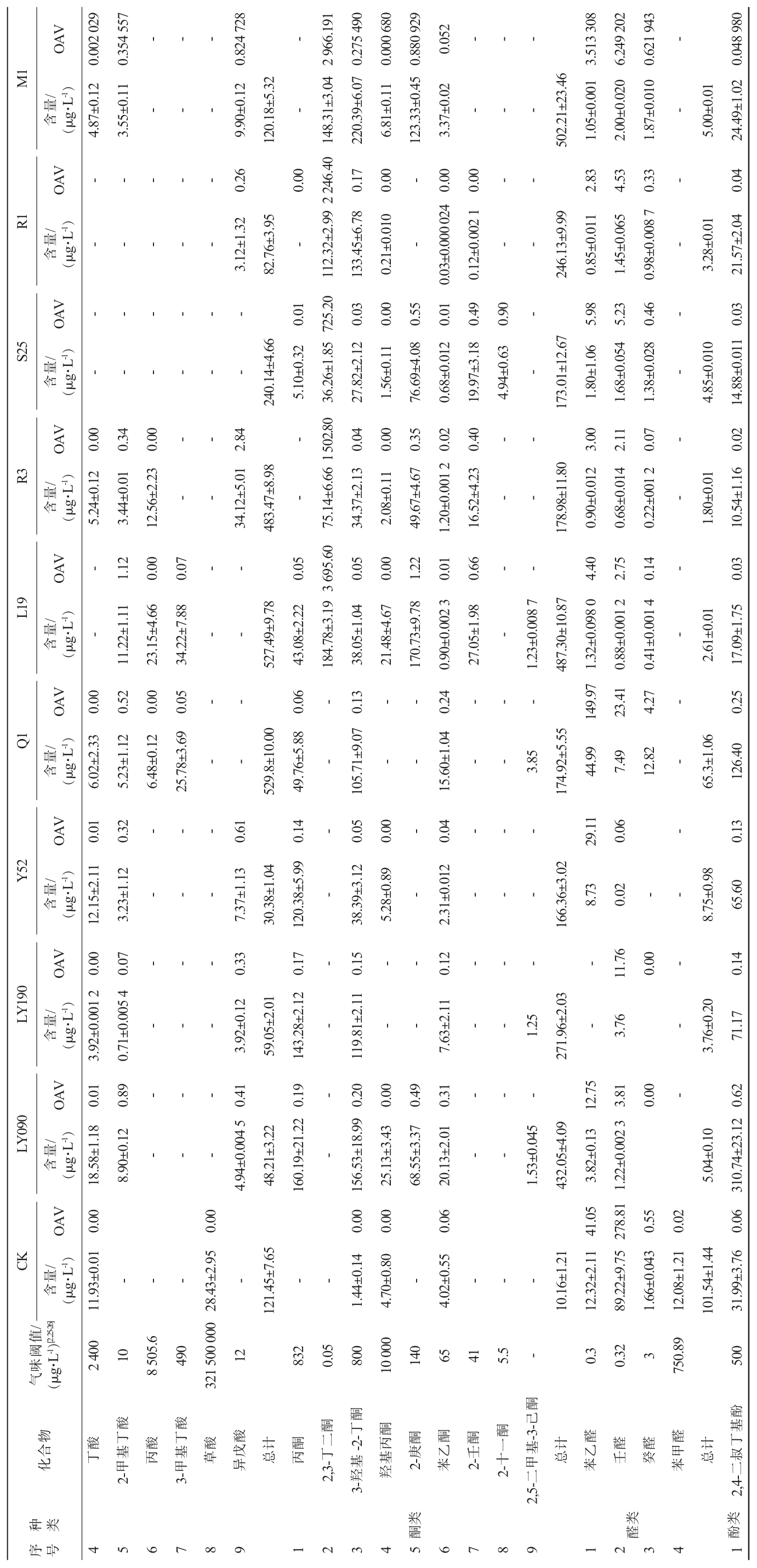
续表
?
由表2可知,CK组共检测出18种挥发性风味化合物,总含量为295.90 μg/L。菌株LY090、LY190、Y52发酵液中分别共检测出30种、22种、20种挥发性风味化合物,总含量分别为1 714.01 μg/L、1 099.60 μg/L、775.88 μg/L。菌株L19、Q1和R3发酵液中分别共检测出29种、27种、23种挥发性风味化合物,总含量分别为1 310.44 μg/L、974.62 μg/L、693.87 μg/L。菌株M1、R1和S25发酵液中分别共检测出25种、18种、24种化合物,总含量分别为884.59 μg/L、363.24 μg/L、446.54 μg/L。
3株酵母菌株在产香能力上存在明显差异。 发酵液中酯类物质含量较少,这可能与模拟肉汤中前体物质的不足有关[27]。 酵母菌能够高效合成3-甲基丁醇,该物质可能通过支链醛还原或氨基酸分解代谢(如Strecker降解和微生物代谢)实现。3-甲基丁醇具有类似脂肪的香气,是多种重要风味物质的前体,如其可被氧化为3-甲基丁酸,并进一步酯化为3-甲基丁酸乙酯等。与CK组相比,3株酵母菌发酵液中3-甲基丁醇的含量从0显著增加至332.53~612.91 μg/L(P<0.05),其中菌株LY090发酵液中含量最高。此外,3株酵母菌株还促进了2-乙基己醇的生成。在酮类物质方面,3株酵母菌均明显提高了其含量,尤其是菌株LY090,主要体现在3-羟基-2-丁酮、羟基丙酮和2-庚酮等物质。 CK组中检测到较高含量的苯甲醛和壬醛等物质,但在3株酵母菌发酵液中这些物质的含量明显降低甚至消失。 PURRIÑOS L等[28]在干发酵香肠的研究中也发现,添加酵母菌后醛类物质的生成减少,推测这可能是由于酵母菌抑制了脂肪酸败过程,从而降低了氧化反应的程度。综上,菌株LY090在产香评价中的表现最为突出,菌株LY090发酵液中共有6种关键香气物质(OAV≥1),包括3-甲基丁醇、乙酸甲酯、庚酸甲酯、正庚醇、苯乙醛和壬醛。此外,检测到13种重要挥发性风味物质(0.1≤OAV<1),这些化合物虽然香气贡献度较低,但通过协同作用对整体风味特征产生影响。
将3株乳酸菌分别接种到模拟肉汤中进行发酵后,肉汤中的挥发性风味物质含量明显增加。 然而,可能由于前体物质的缺乏,酯类物质的含量并未明显提高。 在醇类物质方面,接种菌株Q1和L19后,肉汤中醇类物质的总含量有所增加,但单个醇类物质的含量并不高,主要是醇类物质的种类有所增多。菌株L19发酵液中检测到较高含量的苯乙醇,对改善肉汤风味具有重要作用。在酸类物质方面,接种乳酸菌后,肉汤中酸类物质的含量和种类均有所增加。乳酸菌发酵液中检测到了CK组中未检出的正戊酸、2-甲基丁酸、丙酸和3-甲基丁酸。此外,接种乳酸菌后,乙酸含量明显增加,其从对照组中的73.23 μg/L增加到菌株Q1、L19和R3发酵液中的474.20 μg/L、455.45 μg/L、424.61 μg/L。在酮类物质中,菌株L19发酵液中的酮类物质总含量最高,主要体现在2,3-丁二酮(184.78 μg/L)、3-羟基-2-丁酮(38.05 μg/L)、2-庚酮(170.73 μg/L)和2-壬酮(27.05 μg/L)。菌株Q1和R3也对酮类物质的含量有所贡献,但其种类和含量均明显少于菌株L19。 3株乳酸菌对醛类物质的生成仍无明显促进作用。在3株乳酸菌中,菌株L19发酵液中挥发性风味物质最丰富,从中共检测到8种关键挥发性香气物质(OAV≥1),包括乙酸甲酯、庚酸甲酯、苯乙醇、2-甲基丁酸、2,3-丁二酮、2-庚酮、苯乙醛和壬醛。此外,还鉴定出3种重要挥发性香气物质(0.1≤OAV<1)。 这些化合物通过协同作用,共同形成了层次丰富的肉汤风味特征体系。
在M1中检测到少量酯类物质,如3-甲基苯甲酸甲酯、庚酸甲酯和乙酸芳樟酯。 然而,在醇类物质方面,M1组的表现尤为突出,明显提高了1-戊醇(51.47 μg/L)、异戊醇(113.80 μg/L)和2,3-丁二醇(46.34 μg/L)的含量。 模拟肉汤经菌株S25发酵后,醇类物质的种类从3种增加到6种,但由于含量较低,对肉汤风味的贡献有限。在酸类物质中,菌株S25展现出较强的产酸能力,肉汤中检测到的酸类物质总量最高,达到240.14 μg/L,其中包括乙酸(122.08 μg/L)、正戊酸(45.50 μg/L)和己酸(72.56 μg/L)。相比之下,菌株R1和M1对酸类物质的含量和种类影响较小。3株葡萄球菌均明显增加了酮类物质的含量,其中菌株S25发酵液中的酮类物质种类最多,而菌株M1发酵液中的酮类物质含量最高。在菌株M1发酵液中还检测到大量2,3-丁二酮、3-羟基-2-丁酮和2-庚酮,这与文瑜等[2]的研究结果一致,表明木糖葡萄球菌能够显著提升酮类物质的含量。 通过OAV分析表明,木糖葡萄球菌M1在促进肉汤风味物质形成方面明显优于菌株S25和R1。该菌株发酵液中鉴定出3种关键香气物质(OAV≥1),包括2,3-丁二酮、苯乙醛和壬醛。 此外,还检测到6种重要风味物质(0.1≤OAV<1)。 这些风味化合物共同构成了M1发酵肉汤的典型风味特征。
3 结论
通过在模拟肉汤培养基中对肉制品源9株菌株(3株葡萄球菌、3株乳酸菌和3株酵母菌)的生物学特性及产香能力进行评估发现,汉逊德巴利酵母(Debaryomyces hansenii)LY090、植物乳植杆菌(Lactiplantibacillus plantarum)L19和木糖葡萄球菌(Staphylococcus xylosus)M1均不产气、不产粘、不产生物胺、无溶血性、温度适应性良好,在高盐(8%)、高亚硝酸盐(250 mg/kg)、低酸(pH 3.0)环境下的耐受能力最强。 菌株LY090的产蛋白酶和脂肪酶能力最强,菌株L19的产酸速度最快、产酸量最高,菌株M1产香能力最强。 本研究结果为菌株复配及其在发酵肉制品中应用提供了参考依据。
[1] 宁家文,赵银峰,王蜀,等. 发酵肉制品中亚硝酸盐调控措施研究进展[J] .农产品加工,2023(13):68-71.
[2] 文瑜,张驰,杨思艺,等.木糖葡萄球菌对川式腊肉产品特性的影响[J] .食品研究与开发,2023,44(13):62-69.
[3] 王松,唐林,郭柯宇,等. 四川腊肉中酵母菌多样性及其特性研究[J] .中国食品学报,2023,23(4):334-344.
[4] 王福清,张春颖,姚雪晴,等. 发酵牦牛肉中的菌株分离鉴定及其应用研究[J] .中国调味品,2024,49(11):79-83.
[5] 吴昕颖,臧立萍,徐鸿挺,等. 植物乳杆菌KULG13对发酵肉块产生宣威火腿风味的影响[J] .食品与发酵工业,2025,51(12):199-206.
[6] 落桑央吉,王菲,黄晶晶,等. 西藏传统风干牦牛肉中功能潜力真菌的分离鉴定及生长特性分析[J] .食品工业科技,2025,46(8):192-201.
[7] 韩永霞,崔丽娟,高丽霞,等. 优良发酵菌株筛选鉴定及对发酵猪肉香肠营养品质与安全性的影响[J] .食品科技,2024,49(8):21-29.
[8] 周佳乐,李苗云,赵莉君,等. 三种肉源乳酸菌生长特性及其发酵特性的研究[J] .食品与发酵工业,2025,51(11):163-170.
[9] HU M Z,YU J S,YU J P,et al.Isolation and screening of Staphylococcus xylosus P2 from Chinese bacon:A novel starter culture in fermented meat products[J] .Int J Food Eng,2019,15:1-2.
[10] VERMA D K, AL-SAHLANY S T G, NIAMAH A K, et al. Recent trends in microbial flavor compounds:A review on chemistry,synthesis mechanism and their application in food[J] .Saudi J Biol Sci,2022,29:1565-1576.
[11] 黄岩,鲜双,李倩,等. 豇豆泡菜中产生物胺菌株的筛选鉴定及其产胺特性研究[J] .食品与发酵工业,2023,49(23):119-126.
[12] 牛雪峰. 发酵火腿中产香葡萄球菌的筛选及在发酵香肠中的应用[D] .哈尔滨:哈尔滨商业大学,2020.
[13] 陈骏飞,唐蓉,王晖,等. 低酸泡菜发酵乳酸菌与酵母菌筛选及其共发酵研究[J] .中国酿造,2024,43(2):134-139.
[14] 李秋月,杨雪娇,谭春艳,等. 罗非鱼源肠道益生菌的分离鉴定及其体外益生特性分析[J] .食品与生物技术学报,2023,42(12):1-9.
[15] 张楠. 川味香肠中组胺降解菌的筛选鉴定及其对组氨酸脱羧酶基因表达的影响[D] .雅安:四川农业大学,2018.
[16] 陈瑶,刘艳,许艳丰,等. 发酵肉用耐高温产香葡萄球菌优质菌株的筛选[J] .肉类工业,2019(9):21-27.
[17] 高绍金,李志江,赵家圆,等.鲁氏酵母菌对发酵香肠品质的影响研究[J] .中国调味品,2019,44(4):64-68,79.
[18] 徐鑫,王茜茜,王晓蕊,等. 传统农家大酱中耐盐性乳酸菌的分离与鉴定[J] .食品与发酵工业,2014,40(11):33-40.
[19] 张秋会,孟高歌,王晗等. 自然发酵腊肉中细菌的分离鉴定及其发酵特性[J] .中国食品学报,2023,23(7):161-168.
[20] 刘春燕. 传统四川泡萝卜发酵过程中酵母菌分离鉴定及其对泡菜风味的影响[D] .雅安:四川农业大学,2015.
[21] 郝飞龙,范莹,延莎,等. 山西清香型宗酒原酒与成品酒香气成分及其感官分析[J] .食品科技,2018,43(3):255-261.
[22] GUO X,HUANG F,ZHANG H,et al.Classification of traditional Chinese pork bacon based on physicochemical properties and chemometric techniques[J] .Meat Sci,2016,117:182-186.
[23] 刘雨萱. 传统四川腊肉中生物胺减除菌株的筛选及初步应用[D] . 雅安:四川农业大学,2022.
[24] 罗皓,付伟阳,曹敏,等. 高效降解亚硝酸盐乳酸菌的筛选及其在腊肉中的应用[J] .中国调味品,2024,49(6):91-96.
[25] 吴双慧,杨梓垚,牛茵,等. 复配发酵剂对发酵香肠的品质及挥发性风味的影响[J] .食品工业科技,2024,45(5):126-133.
[26] 范晓文,常荣,赵珠莲,等. 酸肉发酵中挥发性风味物质的变化及对品质的影响[J] .食品与发酵工业,2019,45(22):68-75.
[27] LIU Y,WAN Z,YOHANNES K W,et al.Functional characteristics of Lactobacillus and yeast single starter cultures in the ripening process of dry fermented sausage[J] .Front Microbiol,2021,11:121-123.
[28] PURRIÑOS L,CARBALLO J,LORENZO J M.The influence of Debaryomyces hansenii, Candida deformans and Candida zeylanoides on the aroma formation of dry-cured"lacon"[J] .Meat Sci,2013,93(2):344-350.