内蒙古位于我国北部地区,当地气候条件适宜,拥有充分的光照,大部分地区有效积温高,光热资源丰富,而充足的光热有利于葡萄的生长,进一步提高果实品质。内蒙古地区土壤经黄河水灌溉,土壤环境良好,利于葡萄根系发育,土壤pH值呈中碱性,这样的环境种植的葡萄具有甜度高、病虫害少、着色好等优势。用内蒙古地区的葡萄酿出的葡萄酒,具有口感适宜,风味良好的特点[1-2]。
酿酒酵母(Saccharomyces cerevisiae)是葡萄酒制作中的关键微生物之一,其种类和特性直接影响着葡萄酒的品质和风味[3]。 通常,酿酒酵母是从葡萄皮中分离出来的,我国大部分葡萄酒生产厂家采用商用酿酒酵母进行发酵[4]。但大量商业酵母的使用,无法充分的体现出不同地域葡萄品种的风格特色,造成国内生产的葡萄醋口味风格较为单一,导致我国大部分葡萄酒出现了“同质化”现象,不能很好的体现葡萄酒的复杂性、典型性和产地性[5]。国外很早就涉及有关改善葡萄酒品质、筛选优良酵母菌方面的研究,如KÁNTOR A等[6]在新型发酵酒“Federweisser”中分离和鉴定出酿酒酵母,为葡萄酒发酵用酿酒酵母的分离鉴定扩大了筛选范围。国内对于葡萄酒发酵相关酵母的研究也逐渐趋向于为提高品种特色和地域特征的方向发展,如闫兴敏等[7]初步筛选得到13株具有良好香气特征的本土酿酒酵母,对改善葡萄酒同质化有积极作用。
本研究主要通过传统培养分离法、WL鉴别培养基、形态学观察、生理生化试验等从内蒙古不同地区不同品种葡萄的表皮、发酵醪液以及葡萄园土壤中分离筛选具有性状优良、产酒精能力高的酿酒酵母菌株,并通过分子生物学技术对其进行菌种鉴定,这对于提升内蒙地区葡萄酒的品质和产业发展具有重要意义,同时这些酵母也可以作为重要的酿酒资源,为酿酒行业提供新的选择。
1 材料与方法
1.1 材料与试剂
1.1.1 材料与菌株
葡萄、葡萄园土壤:于2023年9月采集自内蒙古自治区巴彦淖尔市、鄂尔多斯市、乌兰察布市、阿拉善盟市、乌海市、包头市、呼和浩特市,其中包括葡萄样品35个、葡萄自然发酵5 d醪液样品(挑选颗粒饱满无病虫害的葡萄,粉碎于250 mL锥形瓶中,盖上纱布进行自然发酵5 d得到发酵醪液[8])13个、果园土壤样品7个,共计55个样品,4 ℃保藏。
酿酒酵母(Saccharomyces cerevisiae)ENARTIS488:意大利英纳帝斯公司。
1.1.2 试剂
酵母膏(生化试剂):北京奥博星生物技术有限责任公司;蛋白胨(生化试剂):大连美伦生物技术有限公司;酵母浸粉(生化试剂):大连博格林生物科技有限公司;葡萄糖(生化试剂)、无水乙醇(分析纯)、冰乙酸(分析纯):天津鑫铂特化工有限公司;氯霉素(分析纯):青岛高科技工业园海博生物技术有限公司;琼脂(生化试剂):天津市北联精细化学药品开发有限公司;脱氧核糖核酸(deoxyribonucleic acid,DNA)提取试剂盒:奥科生物科技有限公司。
1.1.3 培养基
酵母浸出粉胨葡萄糖(yeastextractpeptonedextrose,YPD)培养基[8]:酵母膏10 g/L、蛋白胨10 g/L、葡萄糖20 g/L,121 ℃高压蒸汽灭菌15 min。YPD固体培养基:在YPD培养基中添加20 g/L琼脂,115 ℃高压蒸汽灭菌30 min。
孟加拉红培养基[9]:蛋白胨5 g/L、葡萄糖10 g/L、磷酸二氢钾1 g/L、硫酸镁0.5 g/L、琼脂15 g/L、孟加拉红0.033 g/L、氯霉素0.1 g/L,121 ℃高压蒸汽灭菌15 min。
氯化三苯四氮唑(2,3,5-triphenyltetrazolium chloride,TTC)上层培养基[9]:葡萄糖5 g/L、TTC 0.5 g/L、琼脂15 g/L。TTC下层培养基[9]:葡萄糖10 g/L、磷酸二氢钾1.0 g/L、酵母浸粉1.5 g/L、硫酸镁0.4 g/L、琼脂20 g/L、蛋白胨2 g/L。均在121 ℃高压蒸汽灭菌15 min。
WL营养琼脂培养基[10]:酵母浸粉5 g/L、酸水解酪蛋白5 g/L、葡萄糖50 g/L、磷酸二氢钾0.55 g/L、氯化钾0.425 g/L、氯化钙0.125 g/L、硫酸镁0.125 g/L、氯化铁0.002 5 g/L、溴甲酚绿0.022 g/L、琼脂17 g/L,121 ℃高压蒸汽灭菌15 min。
1.2 仪器与设备
SW-CJ-2FD超净工作台:北京东联哈尔仪器制造有限公司;KG-SX-700立式压力蒸汽灭菌锅:上海莱睿科学仪器有限公司;HWS-250B恒温生化培养箱:天津市泰斯特仪器有限公司;XJ220A-SCS电子分析天平:上海天美天平仪器有限公司;ZHTY-50WV水浴摇床:上海知楚仪器有限公司;CX23光学显微镜:奥林巴斯(中国)有限公司;TU1901722型分光光度计:北京普析仪器厂;H/T16MM高速离心机:湖南赫西仪器装备有限公司;T100聚合酶链式反应(polymerase chain reaction,PCR)仪:德国BIOMETRA公司。
1.3 方法
1.3.1 酵母菌的分离纯化
在无菌条件下称取10 g葡萄样品于含有90 mL无菌生理盐水的三角瓶中;在无菌条件下称取1 g土样于含有9 mL无菌生理盐水的试管中;在无菌条件下吸取1 mL自然发酵醪液于含有9 mL无菌生理水的试管中,均充分振荡混匀,采用无菌生理盐水按十倍系列梯度稀释至10-7,取0.1 mL稀释度为10-4~10-7的稀释液涂布于孟加拉红培养基上,28 ℃条件下培养1~3 d,观察菌落颜色、形态及大小。 挑取具有酵母菌典型特征的单菌落,划线于含有100 mg/L氯霉素的YPD固体培养基上。 挑取单菌落划线于WL营养琼脂培养基上,28 ℃条件下培养5~8 d,观察菌落的形态及颜色[11-14]。
1.3.2 菌种的保藏与活化
将分离纯化后的菌株划线接种于YPD固体培养基上,28 ℃条件下培养36 h,于4 ℃条件下进行短暂保藏。将活化后的菌株接种于含有50%YPD培养基的甘油中,于-80 ℃条件下长期保存。在应用保藏的菌种之前,将保存的菌株接种于100 mL YPD培养基中,于28℃、150 r/min条件下活化培养24h。利用血球计数板法调整酵母菌的浓度>1×107CFU/mL,制成酵母菌悬液,备用[15]。
1.3.3 形态学观察
将活化后的酵母菌划线接种在YPD固体培养基上,在28 ℃条件下培养48 h,观察菌落的形状大小、菌落颜色、表面情况(粗糙或光滑、有无光泽)、隆起程度、边缘情况等[16]。挑取单菌落进行美蓝染液染色,采用显微镜观察单细胞形态结构及其大小[17]。
1.3.4 耐受性试验
将菌悬液以2%(V/V)的接种量分别接种于不同酒精度(5%vol、7%vol、9%vol、11%vol、13%vol)、不同葡萄糖含量(10%、20%、30%、40%、50%)及不同pH(2.0、2.5、3.0、3.5、4.0)的YPD培养基中,28 ℃条件下培养24 h,采用紫外分光光度计在波长600 nm处测定其OD600nm值,考察菌株对酒精度、葡萄糖和酸的耐受性[18-20]。
1.3.5 产酒精能力试验
将筛选得到的酵母菌株划线接种于TTC下层培养基上,28 ℃条件下培养至菌落成型,倒入TTC上层培养基,28 ℃条件下遮光培养2~3 h,观察培养皿上菌落的显色情况。 菌株的产酒精能力越强,菌落的红色显示越深[21]。通过对不同培养皿上菌落红色的深浅进行比较,从而直观判断菌株的产酒精能力,筛选出酒精产出率高的菌株。
1.3.6 优良酵母菌株生长曲线的绘制
将筛选得到的酵母菌的菌悬液以2%(V/V)的接种量接种于YPD培养基中,在28 ℃、200 r/min条件下培养60 h,取样并测定其OD600 nm值,以培养时间为横坐标,OD600 nm值为纵坐标,绘制生长曲线[22]。
1.3.7 优良酵母菌株的鉴定
生理生化试验:参照《酵母菌的特征与鉴定手册》[23]进行糖发酵试验以及碳氮源同化试验。
分子生物学鉴定:采用液氮研磨的方法综合DNA提取试剂盒提取筛选酵母菌株的基因组DNA,以其为模板,采用引物NL1F(5-GCATATCAATAAGCGGAGGAAAAG-3)、NL4R(5-GGTCCGTGTTTCAAGACGG-3)PCR扩增26SrDNA基因序列。PCR扩增体系:基因组DNA(20 ng/μL)1.0 μL、10×Buffer 5.0 μL、Ex Tag酶0.25 μL、脱氧核糖核苷三磷酸(deoxy-ribonucleoside triphosphate,dNTP)(10 mmol/L)2.0 μL、上下游引物(10 μmol/L)各1.0 μL、Math Processing Error 37.95 μL、双蒸水(ddH2O)50 μL。PCR扩增条件:98 ℃预变性1 min;98 ℃变性10 s,55 ℃退火30 s,72 ℃延伸90 s;72 ℃再延伸5 min。PCR扩增产物经1.5%琼脂糖凝胶电泳检验合格后委托北京颇凡森诺生物科技有限公司进行测序。将测序结果提交至美国国家生物技术信息中心(national center for biotechnology information,NCBI)的GenBank数据库中,利用基本局部比对搜索工具(basic local alignment search tool,BLAST)进行序列比对,确定菌株的种属[24]。
1.3.8 数据处理
每个试验重复3次,采用Excel 2019处理数据,结果用“平均值±标准差”表示。
2 结果与分析
2.1 酵母菌的分离纯化及初筛结果
从内蒙古不同地区葡萄、发酵醪液及果园土壤样品中共分离纯化出104株菌株,经WL营养琼脂培养基初筛得到42株酵母菌株(表1),其菌落及部分菌株的细胞形态分别见表2和图1。由表2可知,菌落颜色为乳白色或白色,菌落形态呈圆形凸出、规则或不规则,表面光滑、湿润。由图1可知,经过美兰染液染色后[25],分离酵母菌株的细胞形态呈现圆形或椭圆形。 参考《The Yeasts:A Taxonomic Study》[26]初步鉴定42株菌株为酵母菌株。
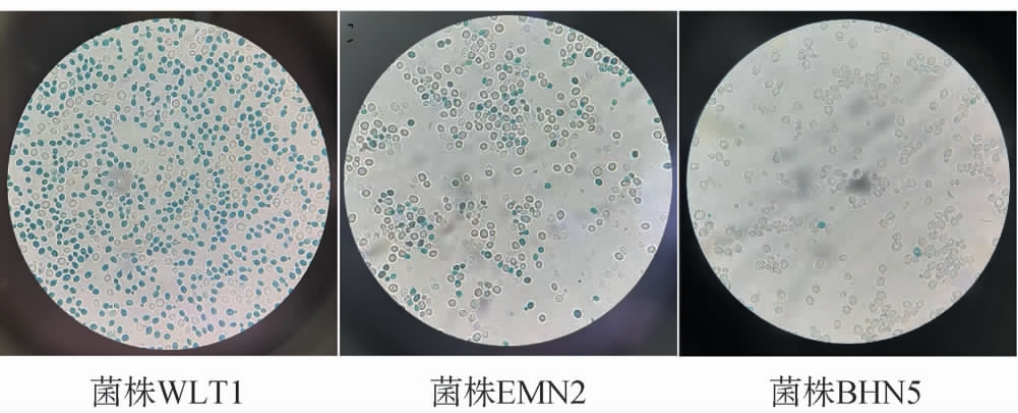
图1 部分初筛酵母菌株的细胞形态
Fig. 1 Cell morphology of some primary screening yeast strains
表1 初筛酵母菌株的来源及编号
Table 1 Source and number of primary screening yeast strains
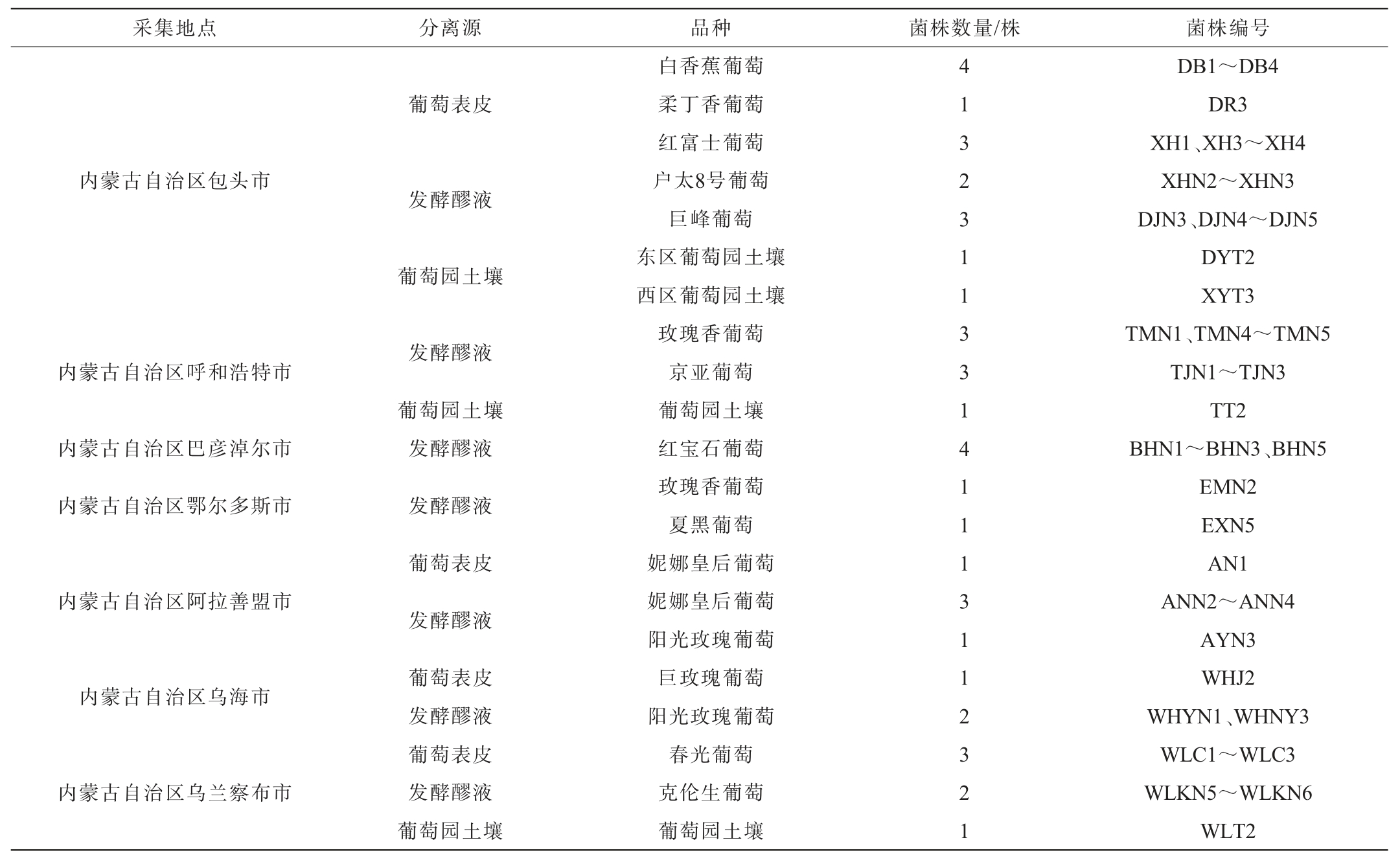
采集地点分离源品种菌株数量/株菌株编号内蒙古自治区包头市内蒙古自治区呼和浩特市内蒙古自治区巴彦淖尔市内蒙古自治区鄂尔多斯市内蒙古自治区阿拉善盟市内蒙古自治区乌海市内蒙古自治区乌兰察布市葡萄表皮发酵醪液葡萄园土壤发酵醪液葡萄园土壤发酵醪液发酵醪液葡萄表皮发酵醪液葡萄表皮发酵醪液葡萄表皮发酵醪液葡萄园土壤白香蕉葡萄柔丁香葡萄红富士葡萄户太8号葡萄巨峰葡萄东区葡萄园土壤西区葡萄园土壤玫瑰香葡萄京亚葡萄葡萄园土壤红宝石葡萄玫瑰香葡萄夏黑葡萄妮娜皇后葡萄妮娜皇后葡萄阳光玫瑰葡萄巨玫瑰葡萄阳光玫瑰葡萄春光葡萄克伦生葡萄葡萄园土壤413231133141113112 321 DB1~DB4 DR3 XH1、XH3~XH4 XHN2~XHN3 DJN3、DJN4~DJN5 DYT2 XYT3 TMN1、TMN4~TMN5 TJN1~TJN3 TT2 BHN1~BHN3、BHN5 EMN2 EXN5 AN1 ANN2~ANN4 AYN3 WHJ2 WHYN1、WHNY3 WLC1~WLC3 WLKN5~WLKN6 WLT2
表2 初筛酵母菌株的菌落形态特征
Table 2 Colony morphology characteristics of primary screening yeast strains

注:“+++”代表菌落大,“++”代表菌落较大,“+”代表菌落较小。
菌株编号形状 边缘状况颜色 表面隆起形状菌落大小BHN3、WLT1 TMN4、WLKN5、TJN2、TT2、EMN2、XHN2、XH4、WLC1、WHJM2、ANN3、WLC2 XHN3、DYT2 WHYN1 TJN3、DJN3、DB3、DB4 XH1 XH3 AN1 TMN5、EXN5、WHYN3 TMN1 BHN2、WLKN6 ANN2 XYT3 DJN4、BHN5、AYN3 DJN5、TJN1 DB1 DB2 DR3 ANN4 WLC3 BHN1圆形规则乳白光滑高凸+++圆形规则乳白光滑高凸++圆形圆形圆形圆形圆形圆形圆形圆形圆形圆形圆形圆形圆形圆形圆形圆形圆形圆形圆形规则规则规则不规则规则不规则规则不规则规则不规则不规则规则不规则规则规则规则规则规则不规则白色乳白乳白乳白乳白白色乳白乳白乳白乳白乳白乳白乳白乳白白色白色乳白白色乳白光滑光滑光滑光滑光滑光滑光滑光滑光滑光滑光滑光滑光滑光滑光滑光滑光滑光滑光滑高凸低凸低凸高凸高凸低凸高凸高凸低凸低凸高凸高凸高凸低凸低凸高凸低凸高凸低凸+++++++++++++++++++++++++++++++++++
2.2 初筛酵母菌株的耐受性评价
2.2.1 酸耐受性分析
42株初筛酵母菌株对酸的耐受性见表3。 由表3可知,4株酵母菌株(BHN2、EXN5、WHJ2、AYN3)仅能耐受pH 4.0,而其他38株酵母菌株均可耐受pH 2.5。 本研究所筛大多数菌株能耐受较低的pH,与曹施静等[27]的研究结果大致相同,适合用于葡萄酒等果酒偏酸性的发酵环境中生长。
表3 42株酵母菌株对酸的耐受性试验结果
Table 3 Results of acid tolerance test of 42 yeast strains
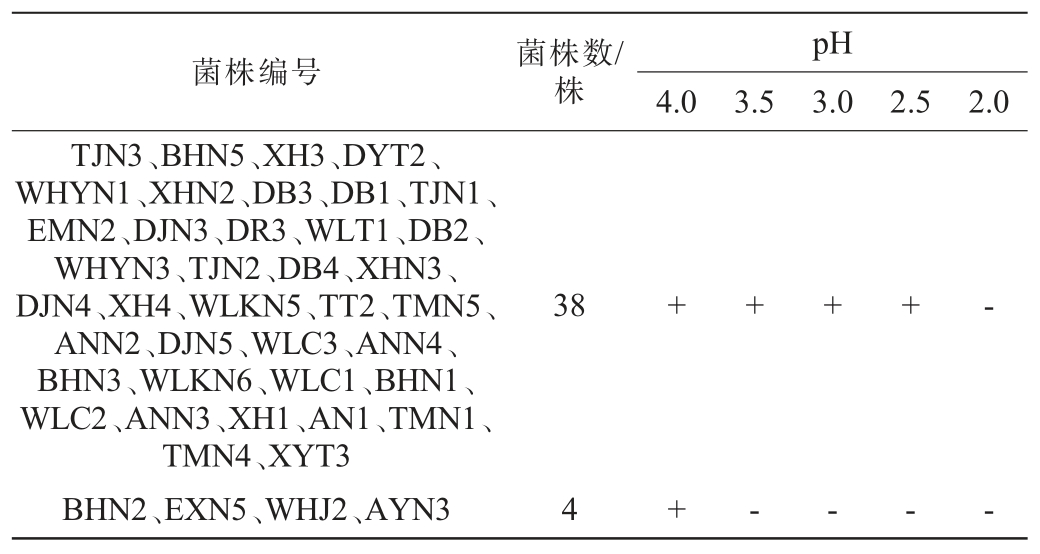
注:“+”表示菌株能生长;“-”表示菌株不能存活。 下同。
菌株编号菌株数/株pH 4.0 3.5 3.0 2.5 2.0 TJN3、BHN5、XH3、DYT2、WHYN1、XHN2、DB3、DB1、TJN1、EMN2、DJN3、DR3、WLT1、DB2、WHYN3、TJN2、DB4、XHN3、DJN4、XH4、WLKN5、TT2、TMN5、ANN2、DJN5、WLC3、ANN4、BHN3、WLKN6、WLC1、BHN1、WLC2、ANN3、XH1、AN1、TMN1、TMN4、XYT3 BHN2、EXN5、WHJ2、AYN3 38++++-4+----
2.2.2 酒精耐受性分析
42株初筛酵母菌株对酒精的耐受性结果见表4。由表4可知,有4株酵母菌株(BHN2、EXN5、WHJ2、AYN3)只能耐受酒精度5%vol,而其他38株酵母菌株均能耐受酒精度13%vol,与吕银德等[28]研究中酵母菌最高可耐受体积分数14%的乙醇的试验结果大致相同,说明本研究所筛选多数酵母菌能够在较高浓度的酒精环境下生存,表现出了良好的酒精耐受能力。
表4 42株酵母菌株对酒精度的耐受性试验结果
Table 4 Results of alcohol content tolerance test of 42 yeast strains
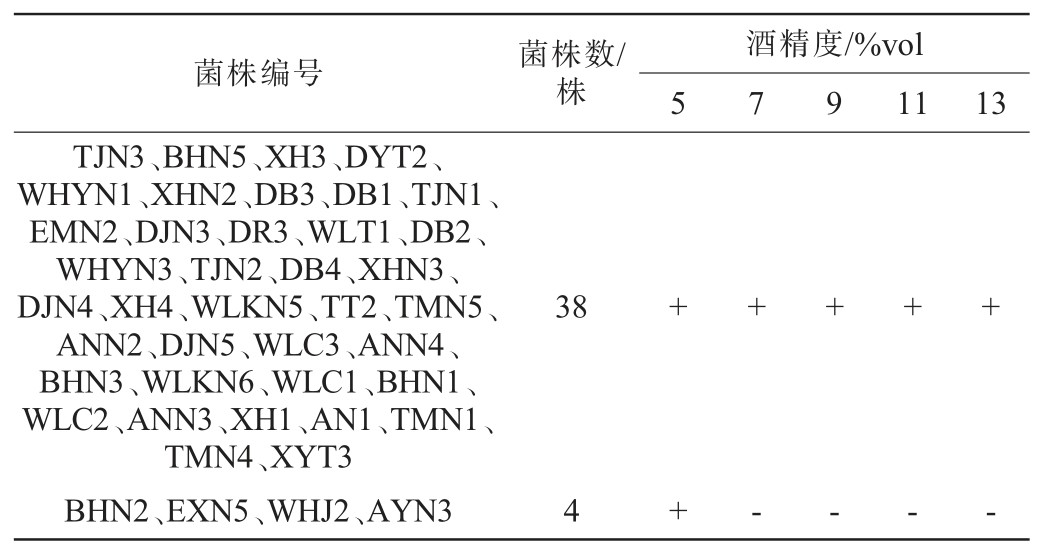
菌株编号菌株数/株酒精度/%vol 57911 13 TJN3、BHN5、XH3、DYT2、WHYN1、XHN2、DB3、DB1、TJN1、EMN2、DJN3、DR3、WLT1、DB2、WHYN3、TJN2、DB4、XHN3、DJN4、XH4、WLKN5、TT2、TMN5、ANN2、DJN5、WLC3、ANN4、BHN3、WLKN6、WLC1、BHN1、WLC2、ANN3、XH1、AN1、TMN1、TMN4、XYT3 BHN2、EXN5、WHJ2、AYN3 38+++++4+----
2.2.3 葡萄糖耐受性分析
42株初筛酵母菌株对葡萄糖的耐受性见表5。由表5可知,34株酵母菌株能耐受40%的葡萄糖,耐受性与周迪等[29]的实验结果大致相同,说明这34株酵母菌株具有良好的高糖耐受性,能够在酒精发酵初期高浓度糖溶液环境下生存,而其他8株酵母菌株只能耐受20%的葡萄糖。
表5 42株酵母菌株对葡萄糖的耐受性试验结果
Table 5 Results of glucose tolerance test of 42 yeast strains
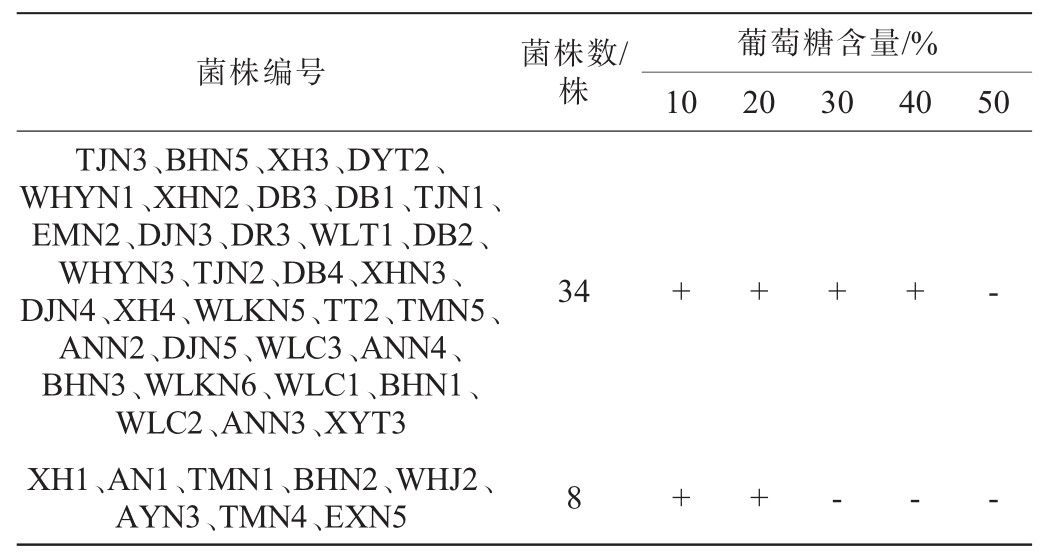
菌株编号菌株数/株葡萄糖含量/%10 20 30 40 50 TJN3、BHN5、XH3、DYT2、WHYN1、XHN2、DB3、DB1、TJN1、EMN2、DJN3、DR3、WLT1、DB2、WHYN3、TJN2、DB4、XHN3、DJN4、XH4、WLKN5、TT2、TMN5、ANN2、DJN5、WLC3、ANN4、BHN3、WLKN6、WLC1、BHN1、WLC2、ANN3、XYT3 XH1、AN1、TMN1、BHN2、WHJ2、AYN3、TMN4、EXN5 34++++-8++---
综上,34株酵母菌(TJN3、BHN5、XH3、DYT2、WHYN1、XHN2、DB3、DB1、TJN1、EMN2、DJN3、DR3、WLT1、DB2、WHYN3、TJN2、DB4、XHN3、DJN4、XH4、WLKN5、TT2、TMN5、ANN2、DJN5、WLC3、ANN4、BHN3、WLKN6、WLC1、BHN1、WLC2、ANN3、XYT3)的耐酒精、耐葡萄糖及耐酸能力较强,均可耐受酒精度13%vol,葡萄糖含量40%,pH 2.5,进一步对这34株酵母菌的产酒精能力进行分析。
2.3 筛选酵母菌株的产酒精能力评估
34株酵母菌株的产酒精能力见表6。 由表6可知,对照菌株ENARTIS488及16株酵母菌株(TJN3、BHN5、XH3、DYT2、WHYN1、XHN2、DB3、DB1、TJN1、EMN2、DJN3、DR3、WLT1、DB2、WHYN3、TJN2)的菌落在TTC培养基上呈深红色,说明这16株酵母菌株的产酒能力最强,且与商业酿酒酵母的产酒能力相当,确定这16株菌株为优良酵母菌株。
表6 33株酵母菌株的产酒精能力分析结果
Table 6 Results of alcohol-production capacity analysis of 33 yeast strains
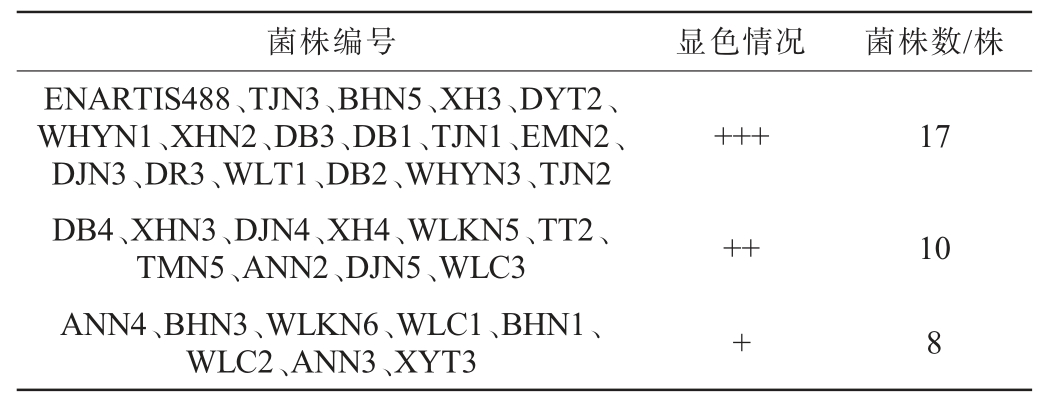
注:“+”表示菌落显示浅红色;“++”表示菌落显示红色;“+++”表示菌落显示深红色。
菌株编号显色情况菌株数/株ENARTIS488、TJN3、BHN5、XH3、DYT2、WHYN1、XHN2、DB3、DB1、TJN1、EMN2、DJN3、DR3、WLT1、DB2、WHYN3、TJN2 DB4、XHN3、DJN4、XH4、WLKN5、TT2、TMN5、ANN2、DJN5、WLC3 ANN4、BHN3、WLKN6、WLC1、BHN1、WLC2、ANN3、XYT3+++17++10+8
2.4 优良酵母菌株的生长曲线
16株优良酵母菌株的生长曲线见图2。由图2可知,16株优良酵母菌株的生长趋势相近,迟缓期均为0~10 h,对数生长期均为10~30 h,在第30小时后均达到稳定期,说明可以在酵母菌培养时间为10~30 h间进行接种。
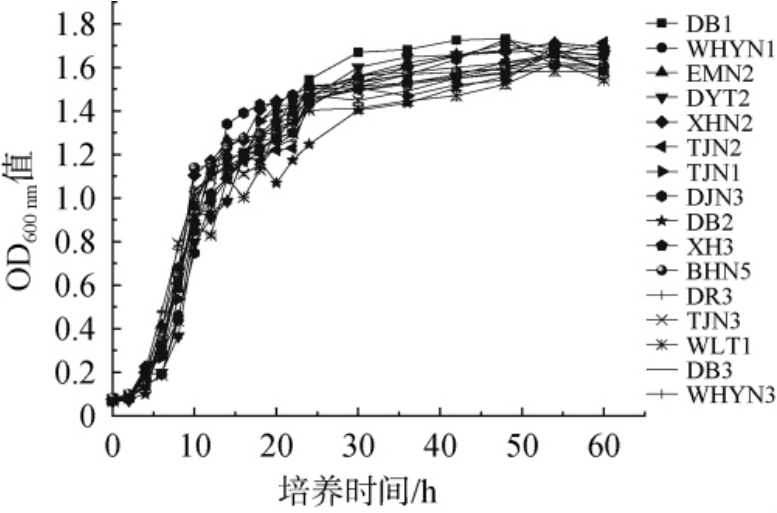
图2 16株优良酵母菌株的生长曲线
Fig. 2 Growth curves of 16 superior yeast strains
2.5 优良酵母菌株的鉴定
2.5.1 生理生化试验
16株优良酵母菌株的生理生化试验结果见表7~表9。由表7可知,16株优良酵母菌株在含有葡萄糖、蔗糖、果糖的杜氏小管中均有气体产生,说明均可以利用葡萄糖、蔗糖、果糖发酵产气,此外,菌株DB1在含有乳糖的杜氏小管中也产生了气体,说明菌株DB1不仅可以利用葡萄糖、蔗糖、果糖发酵产气,还可以利用乳糖发酵产气。
表7 16株优良酵母菌株的糖发酵试验结果
Table 7 Results of sugar fermentation tests of 16 superior yeast strains
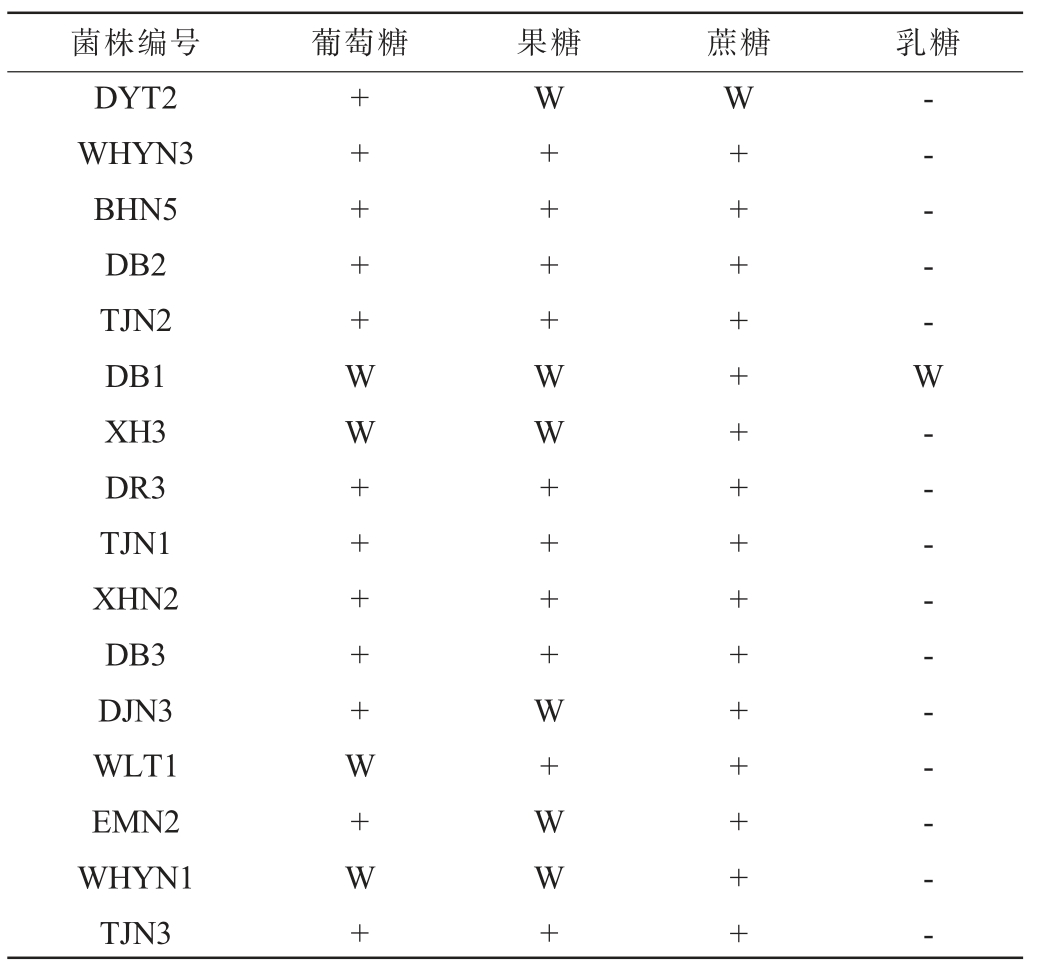
注:“+”代表结果呈阳性;“-”代表结果呈阴性;“W”代表结果呈弱阳性反应。下同。
菌株编号葡萄糖果糖蔗糖乳糖DYT2 WHYN3 BHN5 DB2 TJN2 DB1 XH3 DR3 TJN1 XHN2 DB3 DJN3 WLT1 EMN2 WHYN1 TJN3+++++WW+++++W+W+W++++WW++++W+WW+W+++++++++++++++-----W----------
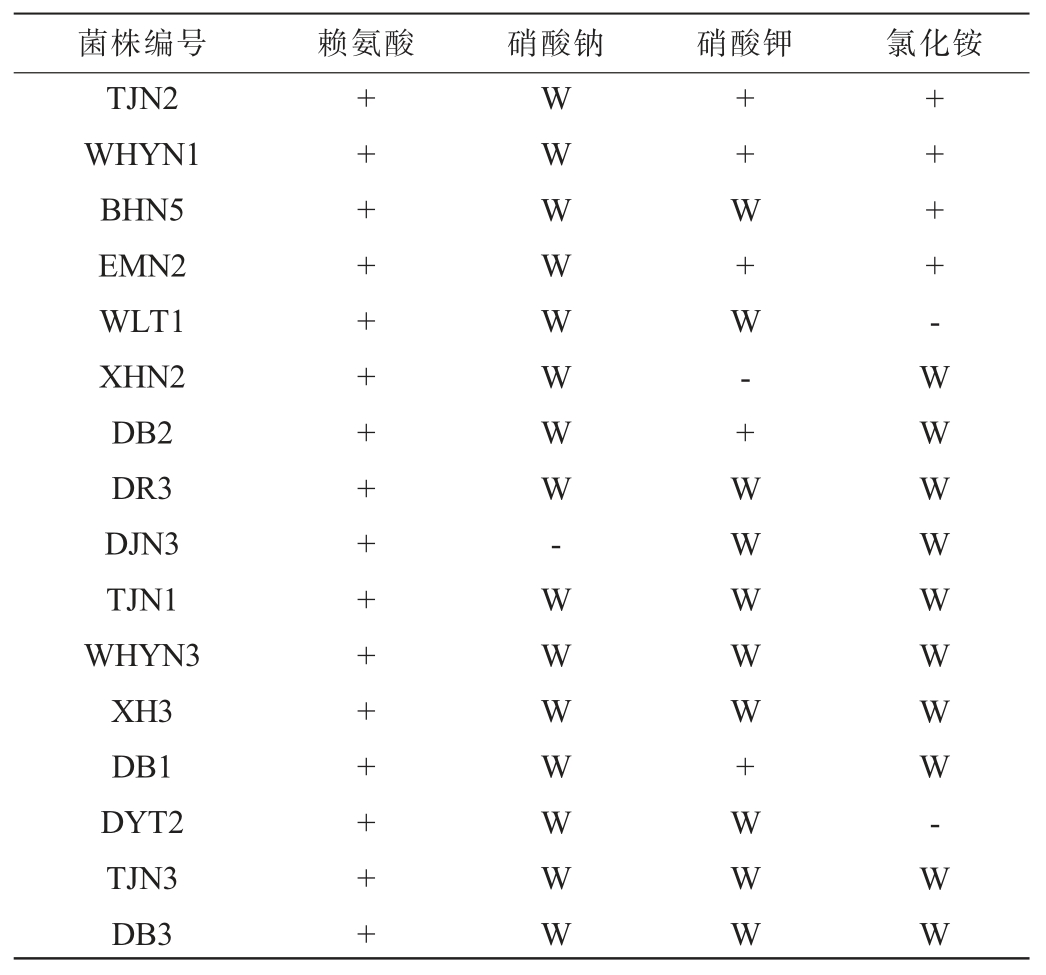
由表8可知,16种优良酵母菌株均可利用赖氨酸作为氮源生长。除菌株DJN3不能利用硝酸钾为氮源生长外,其余15株菌株均能以赖氨酸为氮源进行微弱生长。 除菌株XHN2不可利用硝酸钾作为氮源生长外,其余15株菌株均可利用硝酸钾作为氮源生长。 除菌株WLT1、DYT2不可利用氯化铵作为氮源生长外,其余14株菌株均可利用氯化铵作为氮源生长。
表8 16株优良酵母菌株的氮源同化试验结果
Table 8 Nitrogen source assimilation tests results of 16 superior yeast strains
菌株编号赖氨酸硝酸钠硝酸钾氯化铵TJN2 WHYN1 BHN5 EMN2 WLT1 XHN2 DB2 DR3 DJN3 TJN1 WHYN3 XH3 DB1 DYT2 TJN3 DB3++++++++++++++++WWWWWWWW-WWWWWWW++W+W-+WWWWW+WWW++++-WWWWWWWW-WW
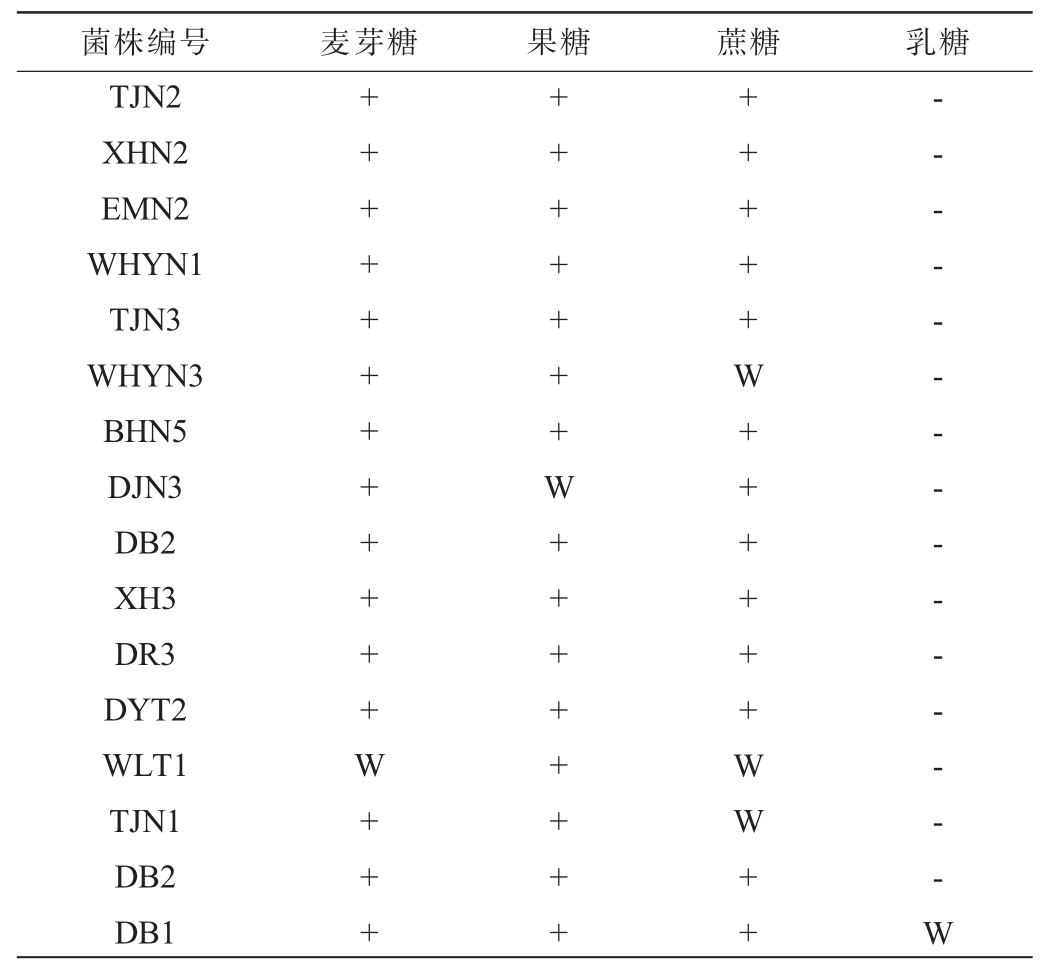
由表9可知,以麦芽糖为碳源时,菌株WLT1能微弱生长,其余菌株均能正常生长。以果糖为碳源时,菌株DJN3能微弱生长,其余15株菌株均能正常生长。以蔗糖为碳源时,菌株WHYN3、WLT1、TJN1能微弱生长,其余15株菌株均能正常生长。以乳糖为碳源时,菌株DB1能微弱生长,其余15株菌株均不能生长。
表9 16株优良酵母菌株的碳源同化试验结果
Table 9 Carbon source assimilation tests results of 16 superior yeast strains
菌株编号麦芽糖果糖蔗糖乳糖TJN2 XHN2 EMN2 WHYN1 TJN3 WHYN3 BHN5 DJN3 DB2 XH3 DR3 DYT2 WLT1 TJN1 DB2 DB1++++++++++++W++++++++++W+++++++++++++W++++++WW++---------------W
结合菌株的形态学特征及生理生化试验结果,参照《酵母菌的特征与鉴定手册》[23],初步鉴定这16株优良酵母菌株为均酵母菌属(Saccharomyces sp.)。
2.5.2 分子生物学鉴定
将16株优良菌株的26S rDNA基因序列上传到NCBI的GenBank数据库中进行BLAST对比,结果见表10。
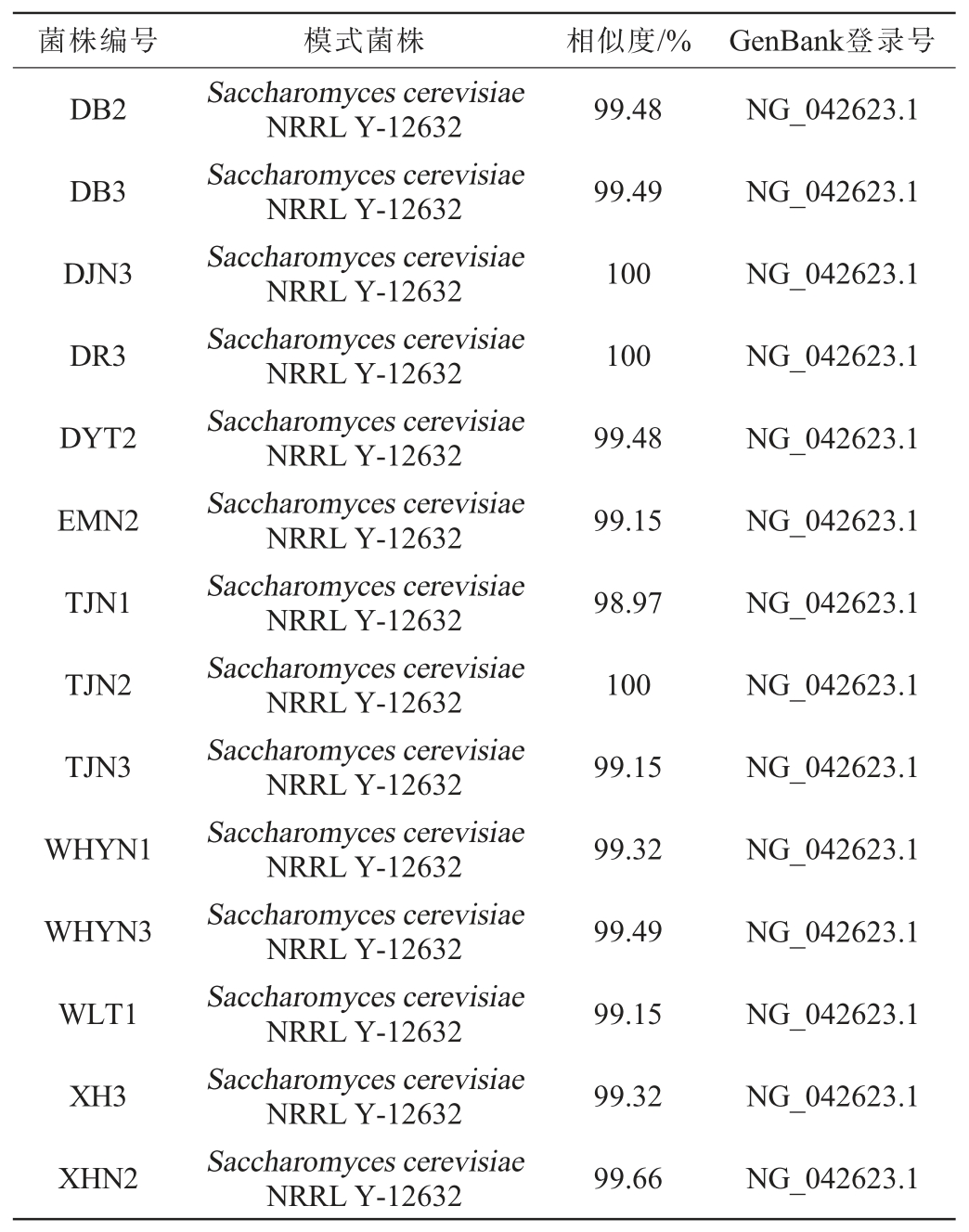
表10 16株优良酵母菌26S rDNA基因序列在GenBank数据库上的比对结果
Table 10 Comparison results of 26S rDNA gene sequences of 16 superior yeast strains in the GenBank database

菌株编号模式菌株相似度/% GenBank登录号BHN5 DB1 Saccharomyces cerevisiae NRRL Y-12632 Saccharomyces cerevisiae NRRL Y-12632 98.29 99.32 NG_042623.1 NG_042623.1
续表
菌株编号模式菌株相似度/% GenBank登录号DB2 DB3 DJN3 DR3 DYT2 EMN2 TJN1 TJN2 TJN3 WHYN1 WHYN3 WLT1 XH3 XHN2 Saccharomyces cerevisiae NRRL Y-12632 Saccharomyces cerevisiae NRRL Y-12632 Saccharomyces cerevisiae NRRL Y-12632 Saccharomyces cerevisiae NRRL Y-12632 Saccharomyces cerevisiae NRRL Y-12632 Saccharomyces cerevisiae NRRL Y-12632 Saccharomyces cerevisiae NRRL Y-12632 Saccharomyces cerevisiae NRRL Y-12632 Saccharomyces cerevisiae NRRL Y-12632 Saccharomyces cerevisiae NRRL Y-12632 Saccharomyces cerevisiae NRRL Y-12632 Saccharomyces cerevisiae NRRL Y-12632 Saccharomyces cerevisiae NRRL Y-12632 Saccharomyces cerevisiae NRRL Y-12632 99.48 99.49 100 100 99.48 99.15 98.97 100 99.15 99.32 99.49 99.15 99.32 99.66 NG_042623.1 NG_042623.1 NG_042623.1 NG_042623.1 NG_042623.1 NG_042623.1 NG_042623.1 NG_042623.1 NG_042623.1 NG_042623.1 NG_042623.1 NG_042623.1 NG_042623.1 NG_042623.1
由表10可知,16株优良酵母菌株均与模式菌株酿酒酵母(Saccharomyces cerevisiae)NRRL Y-12632(GenBank登录号NG_042623.1)的相似度最高,达到98%以上。因此,结合菌株的形态学特征及生理生化试验结果,最终鉴定16株优良酵母菌株均属于酿酒酵母(Saccharomyces cerevisiae)。
3 结论
本研究选用从内蒙古自治区7个不同地区的不同品种的葡萄及果园土壤作为分离源,采用传统培养分离法从孟加拉红培养基上分离纯化得到104株疑似酵母菌株,然后通过WL营养琼脂培养基结合形态学观察初筛得到42株酵母菌株,最后通过耐受性分析及产酒精能力复筛得到16株优良酵母菌株,编号分别为TJN1~TJN3、WHYN1、WHYN3、BHN5、EMN2、WLT1、XHN2、DB1~DB3、DR3、DJN3、XH3、DYT2。这16株优良酵母菌株均可耐受酒精度13%vol、pH 2.5、葡萄糖含量40%的环境,且产酒精能力较强。 经生理生化试验及分子生物学技术鉴定16株优良酵母菌株均为酿酒酵母(Saccharomyces cerevisiae)。 本研究结果为进一步推动内蒙古地区葡萄酒产业的发展,有望用于提升内蒙古地区葡萄酒的整体水平提供了优良菌株资源。
[1] 郭呼忠,刘俊,金亚辉,等. 内蒙古有机葡萄产业发展前景与对策[J] .北方果树,2022(3):45-49.
[2] 张云霞,刘俊,王锋,等. 内蒙古葡萄产业发展现状分析[J] . 现代农业,2022(5):21-25.
[3] PETROVIC′ S,ROŽIC′ L,JOVIC′ V,et al.Optimization of a nanoparticle ball milling process parameters using the response surface method[J] .Adv Powder Technol,2018,29(9):2129-2139.
[4] 魏玉洁. 新疆地产葡萄酒优良酿酒微生物的选育[D] . 乌鲁木齐:新疆农业大学,2016.
[5] PATRIGNANI F,LUCCI L,VALLICELLI M,et al.Role of surface-inoculated Debaryomyces hansenii and Yarrowia lipolytica strains in dried fermented sausage manufacture.Part1:Evaluation of their effects on microbial evolution,lipolytic and proteolytic patterns[J] .Meat Sci,2007,75(4):676-686.
[6] KÁNTOR A, PETROVÁ J, HUTKOVÁ J, et al. Yeast diversity in new still fermenting wine federweisser[J] .Slovak J Food Sci,2016,10(1):120-125.
[7] 闫兴敏,姜娇,高辉,等. 优良本土酿酒酵母的酿酒特性及产香能力初析[J] .食品与发酵工业,2022,48(4):62-68.
[8] DOMIZIO P, ROMANI C, LENCIONI L, et al. Outlining a future for non-Saccharomyces yeasts:Selection of putative spoilage wine strains to be used in association with Saccharomyces cerevisiae for grape juice fermentation[J] .Int J Food Microbiol,2011,147(3):170-180.
[9] 乔喜玲.干红葡萄酒酿酒酵母的优选及其酿酒特性研究[D] .呼和浩特:内蒙古农业大学,2020.
[10] 杨帆,卢灏泽,贾福晨,等. 葡萄酒中优良酵母菌的筛选研究[J] . 轻工科技,2021,37(5):30-31,36.
[11] SWANGKEAW J,VICHITPHAN S,BUTZKE E C,et al.Characterization of β-glucosidases from Hanseniaspora sp.and Pichia anomala with potentially aroma-enhancing capabilities in juice and wine[J] . World J Microbiol Biotechn,2011,27(2):423-430.
[12] 金洪伟,梁恒宇,郭坤,等.酿酒酵母F15和CC17共接种发酵对赤霞珠葡萄酒品质及感官特性的影响[J] . 食品工业科技,2021,42(8):109-116.
[13] 杨辉,王婷婷,赵敏,等. 非酿酒酵母发酵海红果酒的特性研究[J] . 陕西科技大学学报,2021,39(1):52-57.
[14] BUSSE-VALVERDE N,GÓMEZ-PLAZA E,LÓPEZ-ROCA J M,et al.Effect of different enological practices on skin and seed proanthocyanidins in three varietal wines[J] .J Agr Food Chem,2010,58(21):11333-11339.
[15] ESCRIBANO-BAILON T, ALVAREZ-GARCIA M, RIVAS-GONZALO J C,et al.Color and stability of pigments derived from the acetaldehyde-mediated condensation between malvidin 3-O-glucoside and (+)-catechin[J] .J Agr Food Chem,2001,49(3):1213-1217.
[16] 宋佳佳. 苏皖地区酿酒酵母的筛选鉴定及其发酵特性研究[D] . 呼和浩特:内蒙古农业大学,2022.
[17] 田辉,谢引荣,王琰,等. 三种传统发酵食品中酵母菌的分离鉴定与特性分析[J] .中国酿造,2022,41(3):87-92.
[18] 马延琴,徐晓裕,李甜,等. 酿酒葡萄表皮产酶非酿酒酵母的筛选及其产酶特性研究[J] .中国酿造,2021,40(12):149-154.
[19] 徐建坤,张旺,肖婧,等. 红提葡萄中酵母菌多样性的研究[J] . 中国酿造,2019,38(3):40-45.
[20] 蔡燕丽,刘欢,王翀,等. 新疆酿酒葡萄园可培养酵母菌多样性分析[J] .江苏农业科学,2019,47(2):282-287.
[21] 冯炘,何凯翔,解玉红.葡萄中酵母菌的筛选及菌株鉴定[J] .价值工程,2020,39(13):270-273.
[22] 郑雪珂,陈晖,陈浩燃,等.筒鲜鱼中优势酵母菌的筛选鉴定及其生长特性分析[J] .中国酿造,2024,43(9):79-84.
[23] 巴尼特,胡瑞卿. 酵母菌的特征与鉴定手册[M] . 青岛:青岛海洋大学出版社,1991:20-24.
[24] 陈亚蓝,陈顺心,邢淑婕,等.信阳商城筒鲜鱼中乳酸菌的分离及鉴定[J] .中国酿造,2025,44(4):159-164.
[25] LOPES R M, LARA A C, MOURA E M, et al. Characterisation of the diversity and physiology of cellobiose-fermenting yeasts isolated from rotting wood in Brazilian ecosystems[J] .Fungal Biol,2018,122(7):668-676.
[26] KREGER-VAN RIJ N J W.The Yeasts:A Taxonomic Study[M] .Amsterdam:Elsevier Science Publishers,2011:38-41.
[27] 曹施静,楠极,胡海霞.小米醋大曲及酒醪中优良酵母菌的筛选、鉴定及应用[J] .中国酿造,2025,44(2):121-127.
[28] 吕银德,赵俊芳,秦令祥. 鲜食葡萄降酸酵母菌的筛选、鉴定及酿造特性研究[J] .中国酿造,2023,42(9):120-124.
[29] 周迪,卢玲,王岚. 贺兰山东麓产区非酿酒酵母筛选及发酵特性研究[J] .食品与发酵工业,2025,51(1):72-80.