浓香型白酒作为中国白酒的典型代表,其“窖香浓郁、绵甜甘冽”典型风格的形成与窖泥微生态系统密切相关[1-2]。泸州作为中国浓香型白酒的核心产区,拥有悠久的酿酒历史和独特的地域酿酒生态,其“千年老窖万年糟”的传统工艺深刻体现了窖池微生态系统在白酒酿造中的核心地位[3-4]。 微生物栖息的窖泥理化环境(如含水量、pH值)通过调控菌群代谢路径,直接决定酒体品质与风味特征,而不同酒厂在窖池选址、工艺参数控制、老窖维护策略上的差异,可能导致窖泥微生态系统呈现显著分化[5]。
目前,针对窖泥理化和微生态的研究已取得阶段性进展。已有研究表明,窖泥各种理化指标(如含水量、pH值)与窖泥质量存在显著相关性[6-7]。 马龙等[8]的研究发现,四川不同地区浓香型白酒厂的古菌菌群结构存在较大差异;徐相辉等[9]探究了新老窖泥垂直维度的原核生物群落结构演替及其与理化因子的关联,发现部分微生物与有机酸含量呈正相关,为窖泥养护和窖池微生物群落的成熟和稳定提供了参考;晋湘宜等[10]研究发现,共营养乙酸菌属(Syntrophaceticus)、互营单胞菌属(Syntrophomonas)、嗜蛋白菌属(Proteiniphilum)、热粪杆菌属(Caldicoprobacter)、沉积物杆菌属(Sedimentibacter)等逐渐成为窖泥中的优势菌属。然而,现有研究多聚焦单一酒厂或特定工艺类型,关于泸州地区不同酿造工艺(单粮与多粮)对窖泥理化性质与微生物群落影响的系统性研究仍不充分。
本研究以四川泸州地区两个不同酒厂J_L(单粮)、J_LD(多粮)的窖泥为研究对象,通过理化指标测定与高通量测序技术,揭示单粮与多粮窖泥在理化性质、微生物多样性及功能菌属分布上的差异,旨在为解析浓香型白酒风味形成机制、优化窖泥养护技术提供科学依据。
1 材料与方法
1.1 材料与试剂
1.1.1 材料
窖泥样品取自于四川泸州地区两个不同酿造方式的浓香型白酒酒厂(J_L、J_LD)。两个酒厂分别取10~20年窖龄窖池(各两口作平行)。 参照DING X F等[11-12]的取样方法对窖池上层(S)、中层(Z)和底部(D)的窖泥进行取样(图1)。J_L酒厂窖池窖泥对应编号为J_LS10、J_LZ10、J_LD10;J_LD酒厂窖池窖泥对应编号为J_LDS10、J_LDZ10、J_LDD10。将样品装入无菌密封袋中密封,低温运输,置于-20 ℃进行储存,备用。
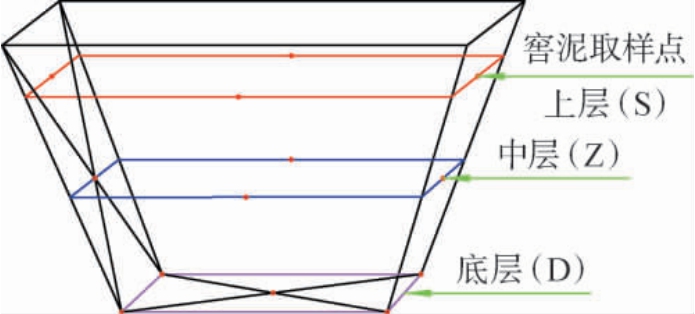
图1 窖泥的取样位置
Fig. 1 Sampling locations of pit mud
1.1.2 试剂
钼酸铵、氯化亚锡、氟化铵、碘化钾、碘化汞(均为分析纯):西陇科学股份有限公司;重铬酸钾(分析纯):广东光华科技股份有限公司;盐酸(分析纯):成都市科隆化学品有限公司;磷酸二氢钾、氢氧化钠(均为分析纯):天津市大陆化学试剂厂;氯化钠、酒石酸钠钾、氯化铵(均为分析纯):福晨(天津)化学试剂有限公司;土壤基因组脱氧核糖核酸(deoxyribonucleic acid,DNA)提取试剂盒:北京索莱宝科技有限公司。
1.2 仪器与设备
AR224CN电子分析天平:美国奥豪斯公司;GZX-9146MBE恒温鼓风干燥箱:上海博迅实业有限公司医疗设备厂;UV-5100B紫外-可见分光光度计:上海元析仪器有限公司;Illumina MiSeq高通量测序平台:美国Illumina公司;NanoDrop 2000 DNA浓度测定仪:美国Thermo Scientific公司;MG-1650台式高速离心机:美瑞克仪器(上海)有限公司;CFX96聚合酶链式反应(polymerase chain reaction,PCR)仪、Gel Doc XR+凝胶成像仪:美国BIO RAD公司;DYY-6D电泳仪:北京六一生物科技有限公司。
1.3 方法
1.3.1 窖泥理化指标
含水量测定:采用烘干法[13];pH值的测定:参照pH计[14];铵态氮含量的测定:采用奈氏试剂比色法[15];有效磷含量的测定:采用钼酸铵比色法[16];腐殖质的测定:根据DB34/T 2265—2014《窖泥中腐殖质的测定重铬酸钾氧化法》。
1.3.2 窖泥微生物高通量测序
采用土壤基因组DNA提取试剂盒提取窖泥样本的微生物宏基因组DNA,通过1%琼脂糖凝胶电泳检测宏基因组DNA质量,使用NanoDrop仪测定其浓度与纯度。以提取的宏基因组DNA为模板,采用通用引物515F_(5'-GTGYCAGCMGCCGCGGTAA-3')和806R_(5'-GGACTACNVGGGTWTCTAAT-3')PCR扩增细菌菌群的16S rDNA基因的V4可变区;采用通用引物ITS1F_(5'-CTTGGTCATTTAGAGGAAGTAA-3')和ITS2R_(5'-GCTGCGTTCTTCATCGATGC-3')PCR扩增真菌菌群的ITS1区。PCR扩增程序:95 ℃预变性3 min;95 ℃变性30 s,55 ℃退火30 s,72 ℃延伸30 s,共35个循环;72 ℃再延伸10 min,4 ℃保存,PCR扩增体系参照向港兴等[17]的方法。 PCR扩增产物委托上海美吉生物医药科技有限公司进行Illumina MiSeq高通量测序。
1.3.3 数据处理
利用Excel2019对窖泥样品理化指标数据进行整合及处理,应用单因素方差分析对窖泥理化数据及微生物α多样性指数进行显著性分析;微生物数据分析基于上海美吉生信云平台(https://cloud.majorbio.com/)进行。
2 结果与分析
2.1 窖泥理化指标分析
不同酒厂窖泥样品的理化指标见表1。由表1可知,不同酒厂窖泥样品间各理化指标存在一定的差异。 J_L酒厂窖泥水分含量为38.90%~42.37%,J_LD酒厂窖泥水分含量为32.19%~43.43%。两个酒厂随着窖池深度增加窖泥水分含量也逐渐增大,即窖底泥水分含量高于窖壁泥,分析原因可能是窖底泥长期接触黄水所致[9]。 此外,J_LD酒厂窖泥在不同位置的水分含量波动稍大于J_L酒厂窖泥,这可能是多粮发酵酿造原料更复杂及微生物代谢更复杂导致的[18]。所有窖泥样品的pH值均<6,偏酸性;J_L酒厂窖泥的pH值为3.77~4.87,J_LD酒厂窖泥的pH值为5.15~5.55,整体上,J_LD酒厂窖泥pH值较高,可能与多粮发酵中多种粮食的缓冲作用有关[19]。
表1 泸州地区不同酒厂窖泥的理化性质
Table 1 Physiochemical properties of pit mud from different distilleries in Luzhou area
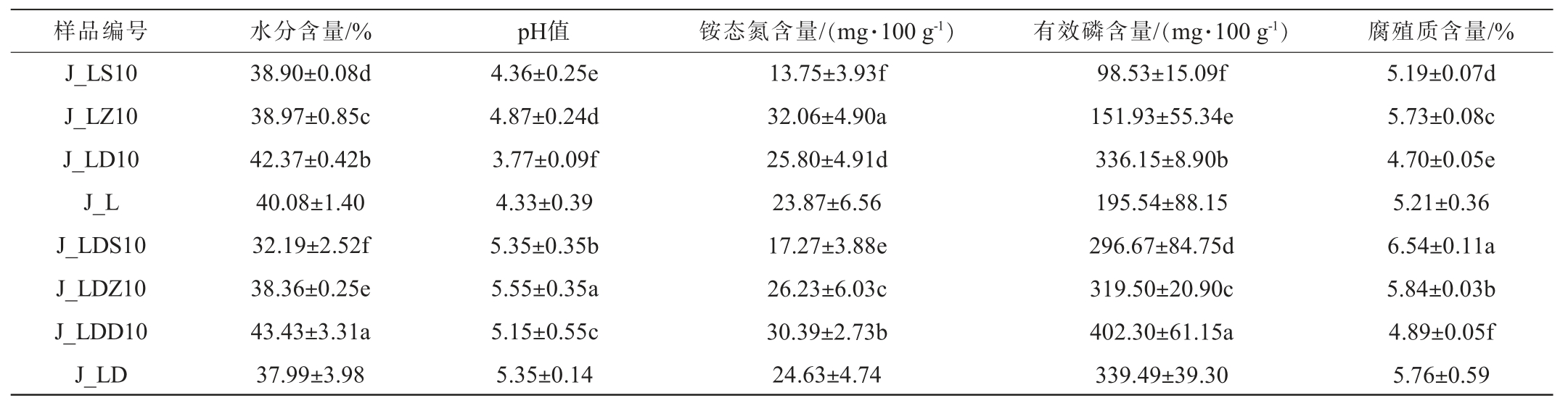
注:同列不同字母表示差异显著(P<0.05)。下同。
样品编号水分含量/%pH值铵态氮含量/(mg·100 g-1)有效磷含量/(mg·100 g-1)腐殖质含量/%J_LS10 J_LZ10 J_LD10 J_L J_LDS10 J_LDZ10 J_LDD10 J_LD 38.90±0.08d 38.97±0.85c 42.37±0.42b 40.08±1.40 32.19±2.52f 38.36±0.25e 43.43±3.31a 37.99±3.98 4.36±0.25e 4.87±0.24d 3.77±0.09f 4.33±0.39 5.35±0.35b 5.55±0.35a 5.15±0.55c 5.35±0.14 13.75±3.93f 32.06±4.90a 25.80±4.91d 23.87±6.56 17.27±3.88e 26.23±6.03c 30.39±2.73b 24.63±4.74 98.53±15.09f 151.93±55.34e 336.15±8.90b 195.54±88.15 296.67±84.75d 319.50±20.90c 402.30±61.15a 339.49±39.30 5.19±0.07d 5.73±0.08c 4.70±0.05e 5.21±0.36 6.54±0.11a 5.84±0.03b 4.89±0.05f 5.76±0.59
J_L和J_LD两个酒厂窖泥的铵态氮含量分别为13.75~32.06 mg/100 g、17.27~30.39 mg/100 g,均呈现出下层高于上层的特点,这与张明珠等[20]的研究结果一致,整体上,J_LD酒厂窖泥的铵态氮含量较高,分析原因可能是多粮原料蛋白质总量更高,从而为微生物提供了更充足的氮源底物[21]。 J_L和J_LD两个酒厂窖泥的有效磷含量分别为98.53~336.15 mg/100 g、296.67~402.30 mg/100 g,均随着窖池深度增加含量升高,分析原因可能是上层窖泥易受空气氧化等影响,抑制微生物代谢,影响有效磷生成[22]。 此外,J_LD酒厂相同位置窖泥的有效磷含量显著高于J_L(P<0.05)。J_L和J_LD两个酒厂窖泥的腐殖质含量分别为4.70%~5.19%、4.89%~6.54%,J_LD酒厂相同位置窖泥的腐殖质水平显著高于J_L酒厂窖泥(P<0.05),分析原因可能是多粮发酵产生的复杂有机质为腐殖质合成提供了丰富前体。整体上,J_LD与J_L的腐殖质含量随着窖池深度的增加而降低,分析原因可能是表层更容易接触到空气和微生物,微生物代谢活动更旺盛,有机物质分解较多,有利于腐殖质形成[23]。
综上,J_LD酒厂窖泥的pH值、铵态氮含量、有效磷含量及腐殖质含量均高于J_L酒厂窖泥,说明泸州地区不同酒厂窖泥样品的各项理化指标存在差异,这些差异可能与位置、酒厂工艺等因素相关,反映了窖泥理化性质的多样性和复杂性。
2.2 窖泥微生物群落多样性分析
2.2.1 高通量测序结果
基于Illumina MiSeq高通量测序方法对窖泥中的微生物群落进行分析,质控优化后得到有效细菌序列337 851条,有效真菌序列309 236条。 基于各窖泥样品在不同测序深度下的Shannon指数绘制稀释曲线,结果见图2。由图2可知,随着测序深度的增加,稀释曲线逐渐趋近于水平状态,表明当前的测序量已满足分析要求。
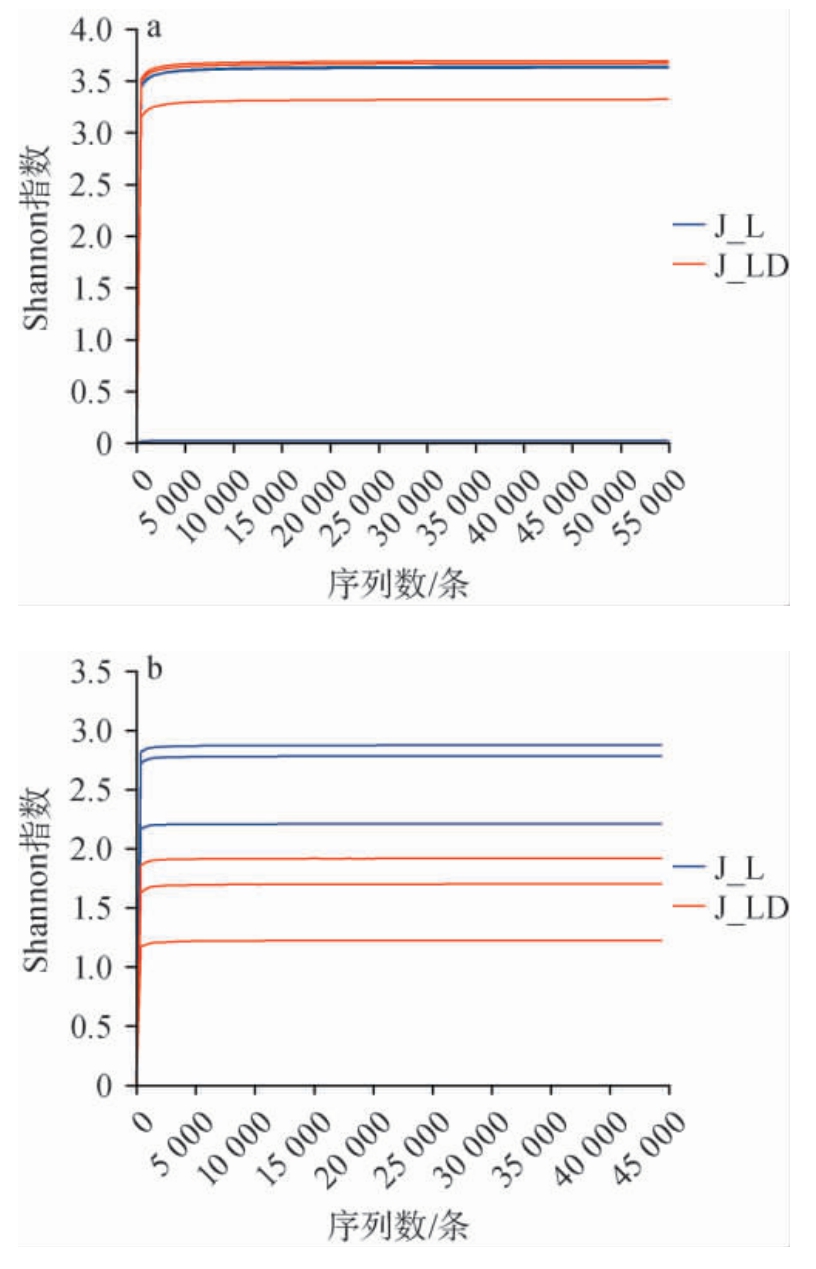
图2 基于Shannon指数泸州地区不同酒厂窖泥中细菌(a)和真菌(b)菌群的稀释曲线
Fig. 2 Dilution curves of bacterial (a) and fungal (b) communities in the pit mud from different distilleries in Luzhou area based on the Shannon index
2.2.2 α多样性分析
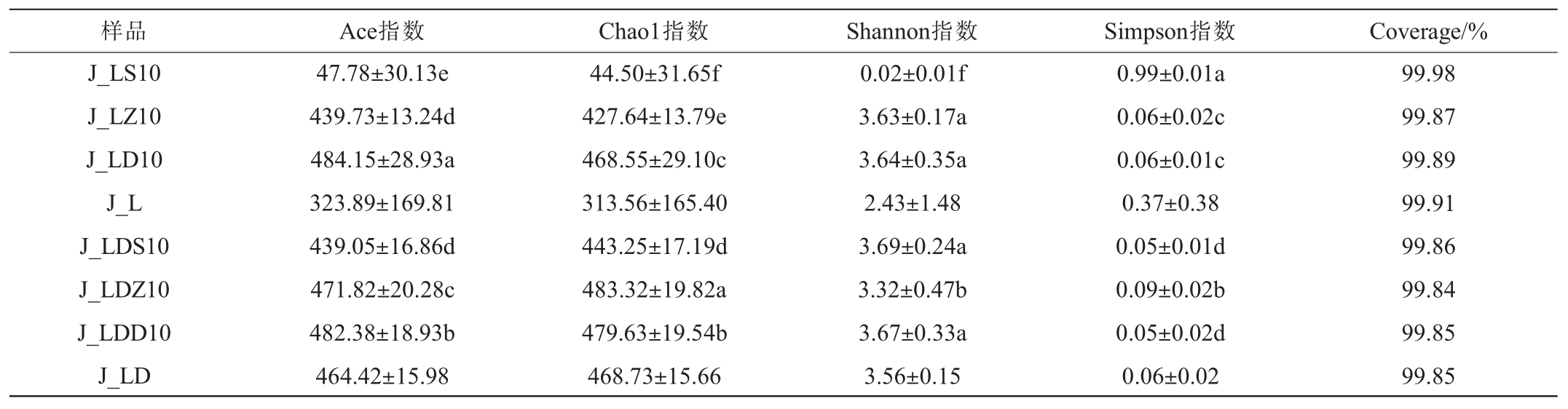
不同窖泥样品中微生物群落的α多样性分析结果见表2和表3。由表2及表3可知,Coverage均>99.9%,说明本次测序结果可以代表样本中微生物的真实情况。Chao1和Ace指数用来估计物种总数即物种丰富度,Simpson和Shannon指数用来衡量群落多样性[8]。整体上,两个酒厂窖泥中细菌菌群的Ace指数、Chao1指数、Simpson指数高于真菌菌群,而Shannon指数低于真菌菌群,说明细菌菌群的物种丰富度高于真菌菌群,而多样性低于真菌菌群,这符合细菌群落的网络复杂性远高于真菌群落的观点[24]。
表2 泸州地区不同酒厂窖泥中细菌菌群的α多样性分析结果
Table 2 Analysis results of α-diversity of bacterial communities in pit mud from different distilleries in Luzhou area
样品Ace指数Chao1指数Shannon指数Simpson指数Coverage/%J_LS10 J_LZ10 J_LD10 J_L J_LDS10 J_LDZ10 J_LDD10 J_LD 47.78±30.13e 439.73±13.24d 484.15±28.93a 323.89±169.81 439.05±16.86d 471.82±20.28c 482.38±18.93b 464.42±15.98 44.50±31.65f 427.64±13.79e 468.55±29.10c 313.56±165.40 443.25±17.19d 483.32±19.82a 479.63±19.54b 468.73±15.66 0.02±0.01f 3.63±0.17a 3.64±0.35a 2.43±1.48 3.69±0.24a 3.32±0.47b 3.67±0.33a 3.56±0.15 0.99±0.01a 0.06±0.02c 0.06±0.01c 0.37±0.38 0.05±0.01d 0.09±0.02b 0.05±0.02d 0.06±0.02 99.98 99.87 99.89 99.91 99.86 99.84 99.85 99.85
表3 泸州地区不同酒厂窖泥中真菌菌群的α多样性分析结果
Table 3 Analysis results of α-diversity of fungal communities in pit mud from different distilleries in Luzhou area
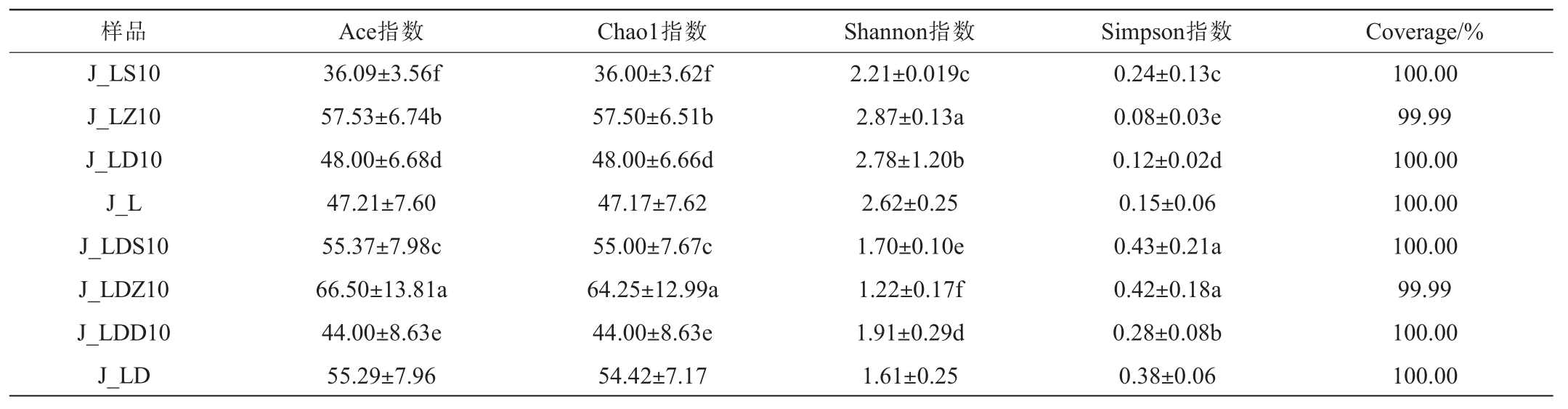
样品Ace指数Chao1指数Shannon指数Simpson指数Coverage/%J_LS10 J_LZ10 J_LD10 J_L J_LDS10 J_LDZ10 J_LDD10 J_LD 36.09±3.56f 57.53±6.74b 48.00±6.68d 47.21±7.60 55.37±7.98c 66.50±13.81a 44.00±8.63e 55.29±7.96 36.00±3.62f 57.50±6.51b 48.00±6.66d 47.17±7.62 55.00±7.67c 64.25±12.99a 44.00±8.63e 54.42±7.17 2.21±0.019c 2.87±0.13a 2.78±1.20b 2.62±0.25 1.70±0.10e 1.22±0.17f 1.91±0.29d 1.61±0.25 0.24±0.13c 0.08±0.03e 0.12±0.02d 0.15±0.06 0.43±0.21a 0.42±0.18a 0.28±0.08b 0.38±0.06 100.00 99.99 100.00 100.00 100.00 99.99 100.00 100.00
由表2可知,两个酒厂窖泥样品细菌菌群的丰富度均随着窖池深度的增加逐渐增大,与张朝正等[25]的研究结果相符合。此外,J_LS10样品的Ace指数(47.78)和Chao1指数(44.50)显著低于其他样品(P<0.05),说明该样品细菌物种丰富度极低,可能因处于上层、环境不适宜等,导致微生物种类少[26]。 整体上,J_LD酒厂窖泥细菌菌群的丰富度和多样性高于J_L酒厂,分析原因可能是多粮发酵通过更丰富的营养、多样化代谢及合理的微生物竞争环境提升了微生物的丰富度与多样性[27],这对白酒风味物质的形成具有积极意义。
由表3可知,真菌物种的丰富度与细菌菌群相似,即两个酒厂中下层窖泥样品真菌菌群的丰富度高于上层。两个酒厂中窖泥真菌菌群多样性普遍随着窖池深度的增加而增大,分析原因可能是底层厌氧环境、复杂底物及异质生境提供多样生态位,缓解上层细菌竞争,黄水携带真核微生物下沉,推动功能真菌共存与丰度上升[28-29]。 整体上,J_LD酒厂窖泥的真菌物种丰富度略高于J_L酒厂,而真菌物种的多样性恰恰相反,分析其原因可能为真菌因营养专一性、竞争压力小、环境稳定等优势,得以保持较高的多样性[30];而多粮发酵中,复杂的营养结构、激烈的微生物竞争(尤其是细菌的优势增殖)及环境波动,可能抑制真菌生长,使其多样性低于单粮,这一现象也反映了不同微生物类群对单一与复合营养环境的适应性差异。
2.2.3 微生物群落组成分析
为直观展示不同酒厂窖泥微生物群落中操作分类单元(operational taxonomic unit,OTU)的共有与特有情况,绘制不同酒厂窖泥样品微生物菌群OTU韦恩图,结果见图3。由图3a可知,两个酒厂细菌OTU总数为791个,其中共有433个,J_L酒厂窖泥独有174个,J_LD酒厂窖泥独有184个;由图3b可知,两个酒厂真菌OTU总数为164个,其中共有43个,J_L酒厂窖泥独有63个,J_LD酒厂窖泥独有58个。由此可知,不同酒厂窖泥之间微生物群落结构存在差异。
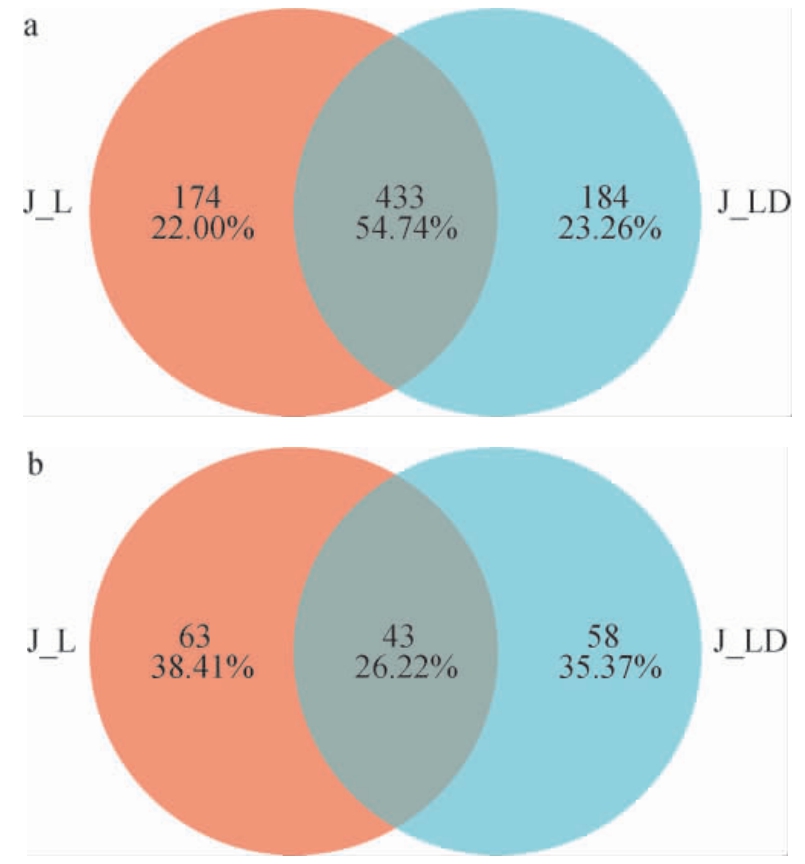
图3 泸州地区不同酒厂窖泥细菌(a)和真菌(b)操作分类单元Venn图
Fig. 3 Venn diagram of the operational taxonomic units of bacteria(a) and fungi (b) in the pit mud from different distilleries in Luzhou area
基于门水平分析泸州地区不同酒厂窖泥样品中的微生物群落组成,结果见图4。
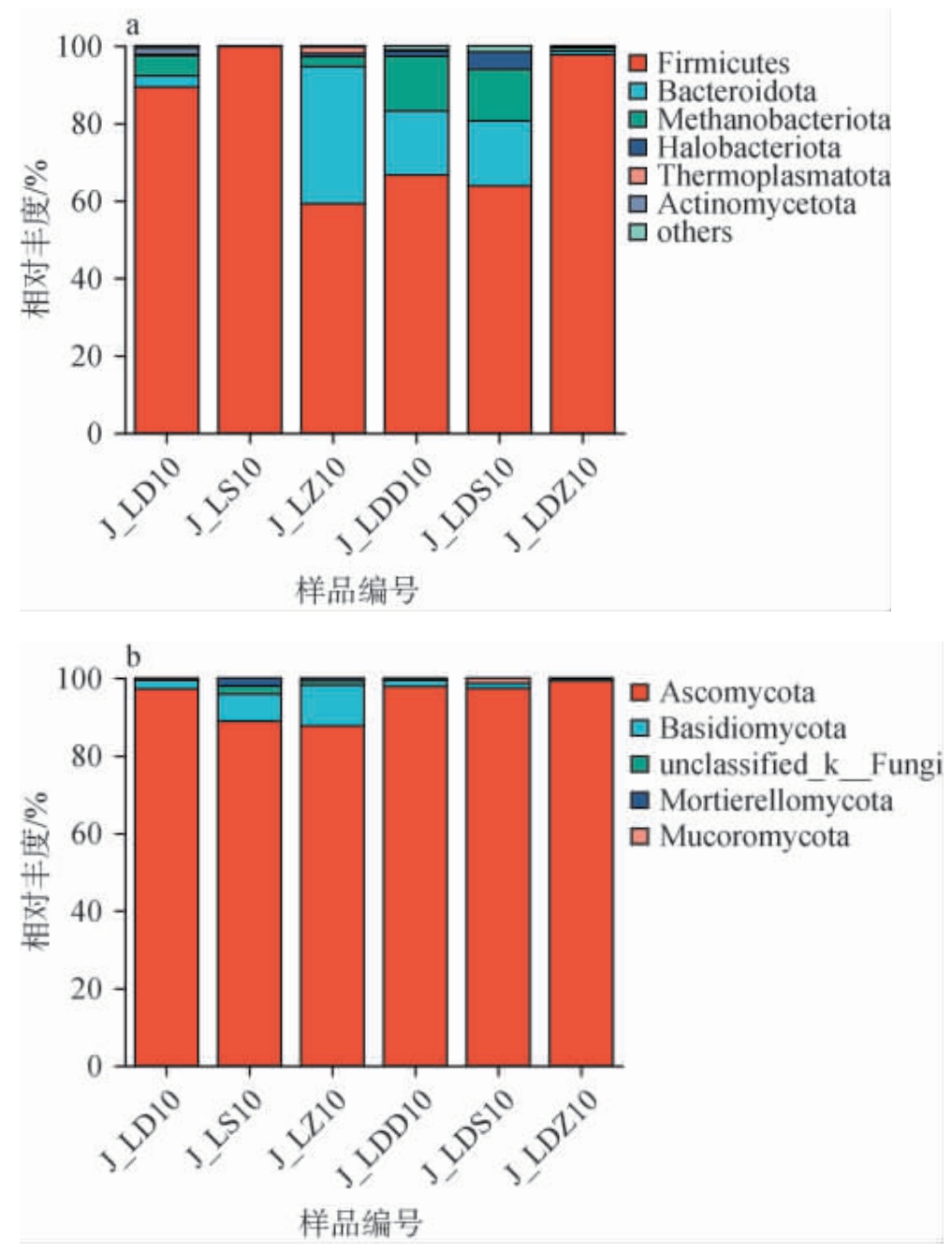
图4 基于门水平泸州地区不同酒厂窖泥样品中细菌(a)和真菌(b)菌群结构
Fig. 4 Bacterial (a) and fungal (b) community structure in pit mud samples from different distilleries in Luzhou area based on phylum level
由图4a可知,从两酒厂窖泥样品中共注释到21个细菌门。J-L酒厂窖泥样品中共注释到14个细菌门,包括3个优势细菌门(平均相对丰度≥1%),分别为厚壁菌门(Firmicutes)(82.85%)、拟杆菌门(Bacteroidota)(12.79%)、甲烷杆菌门(Methanobacteriota)(2.61%)。J-LD酒厂窖泥样品中共注释到18个细菌门,包括4个优势细菌门,分别为Firmicutes(76.06%)、Bacteroidota(11.43%)、Methanobacteriota(9.45%)、盐杆菌门(Halobacteriota)(1.98%)。两个酒厂窖泥中共有的优势细菌门有3个,其中Firmicutes在不同酒厂不同位置都占主导地位,Firmicutes通过产香产酸、维持微生态及促进窖泥老熟等对浓香型白酒品质起关键作用[31]。
由图4b可知,从两酒厂窖泥样品中共注释到5个真菌门。 J-L及J-LD酒厂窖泥样品中分别共检测到5个、4个真菌门,优势真菌门均为子囊菌门(Ascomycota)、担子菌门(Basidiomycota),其中Ascomycota在不同酒厂不同位置均占主导地位,Ascomycota在窖泥中是风味物质的生产者、生态系统的构建者和微生物互作的参与者[32],其作用不仅依赖自身代谢特性,还与窖泥环境(原料、温度、pH等)[33]及其他微生物密切相关,在多粮酿造中,Ascomycota的多样性和代谢复杂性较高,是形成白酒独特风味和品质的关键微生物类群之一。
基于属水平分析泸州地区不同酒厂窖泥样品中的微生物群落组成,结果见图5。由图5a可知,从两酒厂窖泥样品中共注释到254个细菌属。J-L酒厂窖泥样品中共注释到204个细菌属,包括17个优势细菌属,主要为unclassified_f__Lactobacillaceae(35.80%)、产己酸杆菌属(Caproiciproducens)(11.02%)、梭菌属(Clostridium)(7.13%)、拟杆菌属(Bacteroides)(6.46%)、Caldicoprobacter(2.69%)、甲烷杆菌属(Methanobacterium)(2.60%)。J-LD酒厂窖泥样品中共注释到216个细菌属,包括17个优势细菌属,主要为Clostridium(23.25%)、Caproiciproducens(12.50%)、Methanobacterium(9.45%)、油泥单胞菌属(Petrimonas)(6.29%)。两个酒厂共有的优势细菌属有10个,主要为Clostridium、Caproiciproducens、Methanobacterium、Sedimentibacter、Caldicoprobacter、Syntrophomonas。其中Caproiciproducens、Clostridium都可参与生成风味物质,前者通过代谢维持菌群稳定,后者通过微生物互作维持窖泥微生态平衡[34-35]。
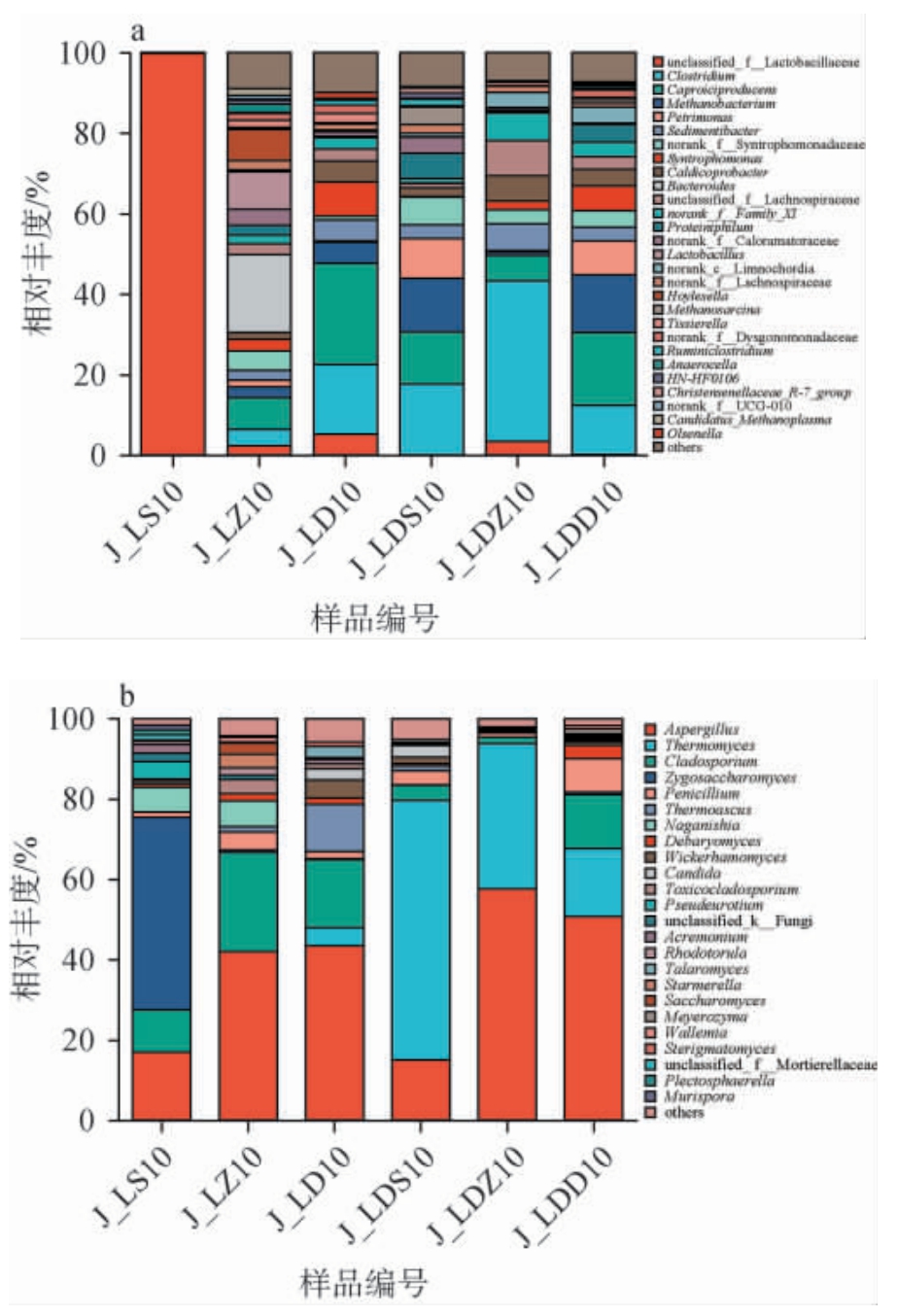
图5 基于属水平泸州地区不同酒厂窖泥样品中细菌(a)和真菌(b)菌群结构
Fig. 5 Bacterial (a) and fungal (b) community structure in pit mud samples from different distilleries in Luzhou area based on the genus level
由图5b可知,从两酒厂窖泥样品中共注释到80个真菌属。J_L酒厂窖泥样品中共注释到52个真菌属,包括16个优势真菌属,主要为曲霉菌属(Aspergillus)(34.10%)、枝孢霉属(Cladosporium)(17.44%)、接合酵母属(Zygosaccharomyces)(16.23%)、嗜热子囊菌属(Thermoascus)(4.35%)、长西氏酵母属(Naganishia)(4.21%)、青霉属(Penicillium)(2.54%)、嗜热真菌属(Thermomyces)(1.48%)。J-LD酒厂窖泥样品中共检测出57个真菌属,包括5个优势真菌属,分别为Aspergillus(41.07%)、Thermomyces(39.28%)、Cladosporium(6.24%)、Penicillium(4.29%)、德巴利酵母菌属(Debaryomyces)(1.48%)。J_L酒厂的优势真菌属组成完全涵盖了J-LD酒厂的全部优势真菌属类别。在两个酒厂窖泥样品中Aspergillus的平均丰度均较高,其存在不仅是窖泥微生态初期构建的关键环节,也为整个发酵体系提供了基础营养和风味前体[36]。
2.2.4 泸州地区不同酒厂窖泥样品差异微生物分析
为精准识别并量化影响窖泥微生态差异的关键微生物类群,采用线性判别分析效应大小(linear discriminant analysis effect size,LEfSe)方法分析泸州地区不同酒厂窖泥样品中微生物的主要差异类群,结果见图6。 由图6a可知,从两个酒厂窖泥样品中共检测出15个差异细菌(线性判别分析(linear discriminant analysis,LDA)>2),在纲、目、科水平上分别检出3种、4种、4种差异微生物。在属水平上,J-L酒厂窖泥样品中的差异细菌菌群为氨嗜菌属(Ammoniphilus)和norank_f__Atopobiaceae,其中,Ammoniphilus实际参与了窖泥铵态氮的消耗与转化,维持窖泥中的氮素平衡[37]。J-LD酒厂窖泥样品中的差异细菌菌群为扁平丝菌属(Planifilum)和norank_f__c__Limnochordia。由图6b可知,从两个酒厂窖泥样品中共检测出17个差异真菌(LDA>4),在纲、目、科水平上分别检出4、3、3种差异微生物。在门、属水平上,J-L酒厂窖泥样品中的差异真菌菌群为酵母属(Saccharomyces)、红酵母属(Rhodotorula)、毒枝孢属(Toxicocladosporium)、Basidiomycota。 J-LD酒厂窖泥样品中的差异真菌菌群为Ascomycota、Thermomyces、复膜孢酵母属(Saccharomycopsis)。 酵母菌在发酵过程有助于维持窖泥中微生物群落的稳定,可进一步提高酒制品品质[38]。
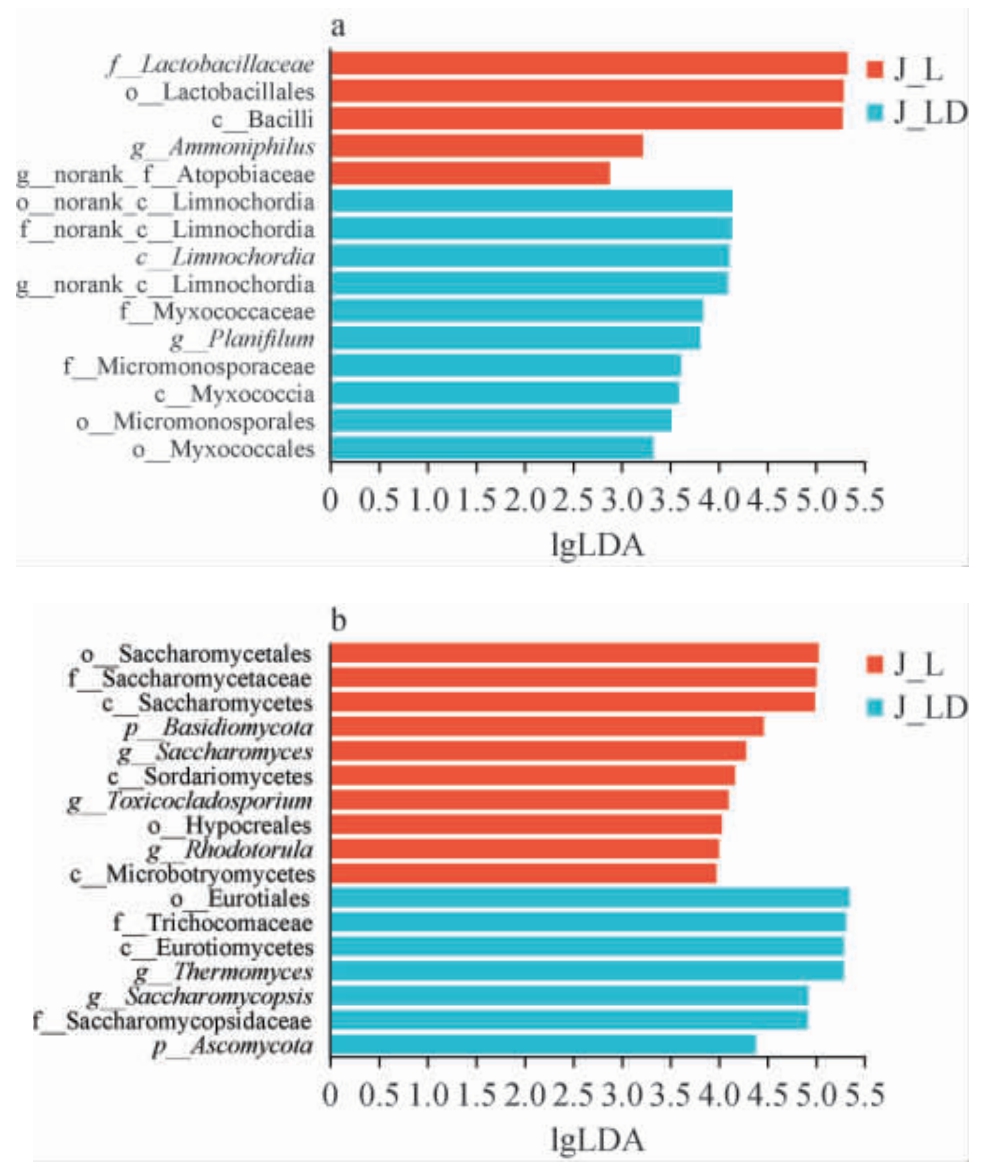
图6 泸州地区不同酒厂窖泥样品中细菌(a)及真菌(b)菌群的线性判别分析效应大小分析结果
Fig. 6 Linear discriminant analysis effect size analysis results of bacterial (a) and fungal (b) communities in pit mud samples from different distilleries in Luzhou area
3 结论
本研究以泸州地区两个不同酒厂的窖泥为研究对象,通过测定窖泥的理化指标,并结合高通量测序等方法,揭示了两个酒厂的窖泥在物质基础与微生物群落上的核心差异。结果表明,不同酒厂窖泥样品理化指标存在一定差异,J_LD酒厂窖泥样品的水分含量波动较大,pH值、铵态氮含量、有效磷含量及腐殖质含量较高。J_LD酒厂窖泥样品的细菌菌群丰富度和多样性及真菌菌群丰富度明显高于J_L酒厂,而真菌菌群的多样性相反。两个酒厂窖泥样品中共注释到254个细菌属和80个真菌属,其中J_L酒厂有17个优势细菌属(平均相对丰度≥1%)和16个优势真菌属,J_LD酒厂有17个优势细菌属和5个优势真菌属。 不同酒厂窖泥样品中的微生物菌群结构存在差异,从两酒厂窖泥样品共筛选到15个差异细菌(LDA>2)和17个差异真菌菌群(LDA>4),J_L酒厂窖泥样品中的差异微生物属为Ammoniphilus、Saccharomyces等,J_LD酒厂窖泥样品中的差异微生物属为Planifilum、Thermomyces等。 综上,泸州地区单粮与多粮酿造工艺通过改变窖泥的营养供给与微环境条件,塑造了截然不同的理化特征与微生物群落结构。本研究成果可为优化窖泥养护技术、提升酿造工艺水平提供科学参考,未来可进一步探究微生物间互作机制及环境因子对发酵的调控作用,为白酒产业高质量发展提供理论支撑。
[1] XU S S,ZHANG M Z,XU B Y,et al.Microbial communities and flavor formation in the fermentation of Chinese strong-flavor Baijiu produced from old and new Zaopei[J] .Food Res Int,2022,156:111162.
[2] 胡世伟,王超凡,王景春,等. 浓香型白酒窖泥微生物群落及其风味成分研究进展[J] .中国酿造,2023,42(12):9-12.
[3] 周晓静,周文,杨官荣,等. 浓香型白酒窖泥功能微生物对风味物质形成的影响研究[J] .酿酒,2022,49(5):29-33.
[4] SUN H,CHAI L J,FANG G Y,et al.Metabolite-based mutualistic interaction between two novel Clostridial species from pit mud enhances butyrate and caproate production[J] .Appl Environ Microbiol,2022,88(13):e00484-22.
[5] 吴树坤,穆敏敏,杨磊.浓香型白酒窖泥微生物群落及其养护技术研究进展[J] .中国酿造,2024,43(11):8-12.
[6] 赵荣寿,卓毓崇,邓林,等.不同腐殖质含量窖泥在浓香白酒的应用研究[J] .食品与发酵科技,2021,57(1):79-82.
[7] 谢军,朱莉莉,邓波,等. 浓香型白酒窖泥水分含量与水分活度的对比研究[J] .中国酿造,2018,37(1):79-81.
[8] 马龙,燕伟,王淑玉,等. 不同地区来源浓香型白酒窖泥古菌群落结构分析[J] .中国酿造,2025,44(2):185-190.
[9] 徐相辉,常强,孙伟,等. 文王浓香型白酒不同深度新老窖泥理化性质与微生物演替分析[J] .食品工业科技,2022,43(21):129-136.
[10] 晋湘宜,王华,赵述淼. 新窖泥微生物群落、理化因子演替规律及其相关性研究[J] .酿酒科技,2025(2):69-73.
[11] DING X F,WU C D,HUANG J,et al.Inter phase microbial community characteristics in the fermentation cellar of Chinese Luzhou flavor liquor determined by PLFA and DGGE profiles[J] .Food Res Int,2015,72:16-24.
[12] 任海伟,孙一帆,王希,等. 不同窖龄及位置浓香型白酒窖泥中细菌群落结构的差异性分析[J] .食品与发酵工业,2023,49(9):103-111.
[13] LIU M K, TANG Y M, GUO X J, et al. Deep sequencing reveals high bacterial diversity and phylogenetic novelty in pit mud from Luzhou Laojiao cellars for Chinese strong-flavor Baijiu[J] .Food Res Int,2017,102(9):68-76.
[14] TAN G,ZHOU R,ZHANG W,et al.Detection of viable and total bacterial community in the pit mud of Chinese strong-flavor liquor using propidium monoazide combined with quantitative PCR and 16S rRNA gene sequencing[J] .Front Microbiol,2020,11:896-904.
[15] 沈怡方.白酒生产技术全书[M] .北京:中国轻工业出版社,1998:641-645.
[16] 朱莉莉,罗惠波,黄治国,等. 浓香型白酒窖泥质量评价理化指标的筛选[J] .中国酿造,2018,37(12):33-39.
[17] 向港兴,陈莹琪,沈毅,等. 不同等级浓香型大曲微生物群落结构与理化性质的比较分析[J] .食品科学,2022,43(18):184-191.
[18] 毛凤娇,黄均,周荣清,等. 人工窖泥微生物群落对浓香型白酒发酵过程风味代谢物形成的影响[J] .食品科学,2024,45(4):125-134.
[19] 常勇勇,林一心,尉军强,等.浓香型白酒糟醅质构及微生物菌群研究进展[J] .中国酿造,2024,43(10):6-12.
[20] 张明珠,吴学凤,穆冬冬,等.基于高通量测序的窖泥原核微生物群落结构及其理化因子相关性分析[J] .食品科学,2021,42(18):111-118.
[21] 李璇,戚居胜,韩四海,等. 浓香型白酒杜康酒醅发酵过程中理化指标变化规律[J] .食品与发酵工业,2019,45(11):52-57.
[22] 刘治国,方超,张晓元,等. 浓香型白酒窖泥理化因子、微生物群落、感官质量以及相关性研究进展[J] .食品科学,2023,44(21):351-358.
[23] TAO Y,LI J B,RUI J P,et al.Prokaryotic communities in pit mud from different-aged cellars used for the production of Chinese strong-flavored liquor[J] .Appl Environ Microbiol,2014,80(7):2254-2260.
[24] ZHAO L N, WU Y, ZHAO Y, et al. Deciphering the intra-and interkingdom networks of microbiota in the pit mud of Chinese strong-flavor liquor[J] .LWT-Food Sci Technol,2022,165:113703.
[25] 张朝正,张天爽,董思文,等.窖泥中挥发性物质和微生物群落的空间分布规律及其关系[J] .食品工业科技,2022,43(5):147-157.
[26] 胡晓龙,付丹阳,王永亮,等. 浓香型白酒窖池空间位置及窖龄对窖泥原核微生物群落的影响[J] .中国酿造,2023,42(3):65-71.
[27] 徐岩,浓香型白酒单粮与多粮固态发酵酒醅微生物结构和代谢特征解析[D] .无锡:江南大学,2019.
[28] 王依文,田瑶瑶,张克粉,等.不同季节及层级浓香型白酒窖泥微生物群落多样性与风味物质的比较及相关性分析[J] . 食品科学,2025,46(4):100-109.
[29] DENG B,SHEN C H,SHAN X H,et al.PCR-DGGE analysis on microbial communities in pit mud of cellars used for different periods of time[J] .J I Brewing,2012,118(1):120-126.
[30] 王浩,吴爱姣,刘保兴,等.菌根真菌多样性与植物多样性的相互作用研究进展[J] .微生物学通报,2020,47(11):3918-3932.
[31] LIANG H P,LI W F,LUO Q C,et al.Analysis of the bacterial community in aged and aging pit mud of Chinese Luzhou-flavour liquor by combined PCR-DGGE and quantitative PCR assay[J] .J Sci Food Agr,2015,95(13):2729-2735.
[32] 梁欢,许长峰,唐伟斌,等. 泥坑浓香型白酒窖泥中微生物群落结构与多样性分析[J] .现代农业科技,2021(3):203-206,220.
[33] PU S,YAN S.Fungal diversity profiles in pit mud samples from Chinese strong-flavour liquor pit[J] .Foods,2022,11(22):3544.
[34] CHAI L J,QIAN W,ZHONG X Z,et al.Mining the factors driving the evolution of the pit mud microbiome under the impact of long-term production of strong-flavor Baijiu[J] .Appl Environ Microbiol,2021,87(17):e00885-21.
[35] FANG G Y,CHAI L J,ZHONG X Z,et al.Comparative genomics unveils the habitat adaptation and metabolic profiles of Clostridium in an artificial ecosystem for liquor production[J] .Msystems,2022,7(3):e00297-22.
[36] 高占争,吴云,张文学.浓香型白酒窖泥微生物群落研究进展[J] .中国酿造,2020,39(6):1-7.
[37] 赵亮亮,盛伟喜,时晓,等.浓香型白酒酿造生境中微生物群落多样性及群落间相互作用[J] .中国酿造,2023,42(11):15-21.
[38] 杜礼泉,饶家权,唐聪,等.窖泥功能菌在浓香型大曲酒生产中的应用[J] .酿酒,2010,37(6):43-44.