我国泡菜历史悠久,最早可以追溯到商周时期[1]。泡菜是以新鲜蔬菜为原料,添加一定量的食盐水以及调味品,经发酵后得到的传统蔬菜制品。在发酵过程中,微生物将原料中的碳水化合物、脂肪和蛋白质等大分子物质降解为更容易吸收的小分子物质,在提高营养利用率的同时也为蔬菜提供了独特的风味[2]。
在对食品安全高标准、严要求的今天,稳定的产品品质与风味优良的泡菜产品是满足当前市场需求的趋势所在。目前不少研究人员在泡菜、酸菜等直投式发酵剂上做了一定的研究,如周佳等[3-4]采用接种植物乳植杆菌(Lactiplantibacillus plantarum)与鼠李糖乳杆菌(Lactobacillus rhamnosus)的方式发酵包菜,所得泡菜的发酵时间短,口感佳,亚硝酸盐含量远低于泡菜产品的国家标准,具有大批量生产的潜质。 史婷等[5]分别采用发酵乳杆菌(Lactobacillus fermentum)、嗜酸乳杆菌(Lactobacillus acidophilus)、植物乳植杆菌发酵剁辣椒,发现经发酵乳杆菌发酵产生的剁椒泡菜酯类、烯类、酮类物质种类和含量都较高;而植物乳植杆菌与嗜酸乳杆菌发酵后,庚酸乙酯、癸酸乙酯、棕榈酸甲酯、正癸酸、丙酸、枯醛、己醛含量高于其他组,这些香气成分可以赋予剁辣椒独特的风味。李苹苹等[6]采用肠膜明串珠菌(Leuconostoc mesenteroides)、戊糖乳杆菌(Lactobacillus pentosus)和植物乳植杆菌发酵萝卜,发现肠膜明串珠菌发酵初期产酸快;戊糖乳杆菌和植物乳植杆菌发酵中后期产酸快且产酸量大,与自然发酵相比,能显著提升泡菜的发酵速度,亚硝酸盐含量更低。由此可见,乳酸菌作为泡菜发酵的主要微生物,在泡菜的发酵过程中起到至关重要的作用,筛选并应用纯种乳酸菌发酵是泡菜工业化的必经之路。
本研究从恩施本地萝卜泡菜与泡菜水中筛选产酸能力强、抗氧化活性高、耐H2O2、耐胆盐、耐酸能力强的乳酸菌,对其进行形态学观察及分子生物学鉴定,并将其应用到萝卜泡菜制备中。测定所得泡菜的亚硝酸盐、总酸、总糖含量、咀嚼性、弹性、硬度、感官评分等指标,并对其进行挥发性风味成分分析,得到适合于单菌发酵萝卜泡菜的优良乳酸菌,为萝卜泡菜安全、稳定的工业化生产提供一定的理论依据。
1 材料与方法
1.1 材料与试剂
1.1.1 材料
萝卜泡菜、泡菜母水、新鲜白萝卜:湖北恩施市某菜市场。
1.1.2 试剂
葡萄糖、碳酸钙、氯化钠、铁氰化钾(均为分析纯):国药集团药业股份有限公司;1,10-菲啰啉(分析纯):湖北标越生物科技发展有限公司;2-甲基-3-庚酮(色谱纯):上海源叶生物科技有限公司;亚硝酸盐速测试纸:北京智云达科技股份有限公司;1,1-二苯基-2-三硝基苯肼(1,1-diphenyl-2-picrylhydrazyl,DPPH)、硫酸亚铁、过氧化氢、三氯乙酸、三氯化铁、牛胆盐(均为分析纯):合肥博美生物科技有限公司;L-半胱氨酸、细菌脱氧核糖核酸(deoxyribonucleic acid,DNA)提取试剂盒:北京索莱宝科技有限公司。0.01 mol/L(pH值=7.4)磷酸盐缓冲溶液(phosphate buffer saline,PBS):山东吉田生物科技有限公司。
1.1.3 培养基
MRS琼脂培养基、MRS液体培养基:北京索莱宝科技有限公司。
1.2 仪器与设备
HP6890/5973气相色谱-质谱联用(gas chromatographymass spectrometry,GC-MS)仪、固相微萃取(solid-phase micro-extraction,SPME)萃取头(50/30 μm DVB/CAR/PDMS)、HP-5MS UI毛细管色谱柱(30 m×0.25 mm×0.25 μm):美国Agilent公司;UV9100紫外可见光分光光度计:北京莱伯泰科有限公司;BX53光学显微镜:日本奥林巴斯株式会社;PHSJ-3F pH计:上海仪电科学仪器股份有限公司;SW-CJ-2D超净工作台:苏州净化设备有限公司;DHG9070A电热鼓风干燥箱、DHP-9162电热恒温培养箱:上海一恒科学仪器有限公司;Gradient S聚合酶链式反应(polymerase chain reaction,PCR)扩增仪:德国Eppendorf公司。
1.3 方法
1.3.1 乳酸菌的分离
取1 mL泡菜汁,用无菌生理盐水进行梯度稀释。取1 mL稀释度为10-4、10-5、10-6的样品均匀涂布于添加有碳酸钙的MRS琼脂培养基上,37 ℃恒温培养48 h,培养完成后测量溶钙圈大小。 挑取有较大溶钙圈的单菌落进行平板划线,37 ℃培养48 h。多次传代纯化后的菌种用MRS琼脂斜面培养基保存。
1.3.2 高产酸乳酸菌的筛选
将分离得到的菌株接种于MRS液体培养基中,37 ℃培养36 h,取0.1 mL涂布于加有碳酸钙的MRS琼脂培养基上,37 ℃培养48 h,计算溶钙圈大小与菌落大小的比例。选取溶钙圈与菌落直径比例>2的菌落参照阿丽亚·阿达力等[7]的方法计算总酸含量,选取产酸能力较高的菌株进行革兰氏染色与过氧化氢酶实验,最终选取革兰氏阳性与过氧化氢酶阴性的菌种进行后续实验[8]。
1.3.3 种子液与菌悬液的制备
种子液的制备:在超净工作台中用接种环勾取一环培养基上的单菌落于MRS液体培养基中,37 ℃恒温培养48 h后观察菌体数量,达到1×109 CFU/mL后备用。
无细胞上清液与细胞破碎提取物的制备:取种子液4mL在5 000 r/min离心10 min,上层即为上清液。用pH为7的磷酸盐缓冲液(phosphate buffer solution,PBS)冲洗菌体,离心,重复3次后将菌体重悬于PBS中,即为菌悬液。使用显微镜直接计数法确定乳酸菌的初始菌落数达到1×109 CFU/mL。将此菌悬液超声冰浴破碎(超声功率为300 W,超声2 s,停止2.4 s,超声10 min),随后在4 ℃,8 000 r/min离心10 min得到细胞破碎提取物。
1.3.4 抗氧化能力的测定
(1)还原力的测定:参考HU X Y等[9]的方法。吸取0.5 mL无细胞上清液(或细胞破碎提取物)至试管中,加入0.5 mL PBS(pH值为6.6)和0.5 mL 1%的铁氰化钾溶液,混匀后50 ℃水浴20 min。再加入0.5 mL 10%的三氯乙酸溶液,5 000 r/min离心5 min,吸取1 mL上清液,加入1 mL蒸馏水和1 mL 0.1%的三氯化铁溶液,混匀静置10 min,在波长700 nm处测定吸光度值(OD700 nm值),无细胞上清液以MRS液体培养基(细胞破碎物以PBS)为对照组(下同)。 乳酸菌的还原能力用L-半胱氨酸盐酸盐当量来表示。
配制浓度分别为0、50 μmol/L、100 μmol/L、150 μmol/L、200 μmol/L、250 μmol/L、300 μmol/L的L-半胱氨酸盐标准溶液,按照还原能力的检测步骤进行测定。 标准曲线回归方程为:y=0.000 4x+0.035 4,相关系数R2=0.993 4。
(2)羟自由基清除能力测定:参考KANG C H等[10]的方法,取1 mL 1,10-菲啰啉(0.75 mmol/L)、2 mL磷酸盐缓冲液(pH值为7.4)和1 mL FeSO4溶液(0.75 mmol/L),混合后加入1 mL H2O2溶液(0.12%)和1 mL乳酸菌菌悬液(或无细胞提取液),置于37 ℃水浴90 min后,在波长536 nm处测定吸光度值(OD536nm值),记为Ai。
式中:Aj为以1 mL蒸馏水代替样品液的对照组吸光度值;A0为用1 mL的对照组代替样品并且体系中不包含H2O2的空白组吸光度值。
(3)DPPH自由基清除能力测定:参照檀茜倩等[11]的方法。取1 mL乳酸菌菌悬液(或无细胞提取物),加入1 mL DPPH乙醇溶液(0.2 mmol/L),摇匀后在室温下静置30 min,随后4 000 r/min离心10 min,取上清液在波长517 nm处测定吸光度值(OD517 nm值),记为Ai,以1 mL对照组和1 mL乙醇代替样品进行调零。
式中:A0为以1 mL乙醇代替样品液的对照组吸光度值;Aj为以1 mL乙醇代替DPPH乙醇液的对照组吸光度值。
1.3.5 耐受性分析
(1)H2O2耐受能力:参照赵山山等[12]的方法,将乳酸菌种子液按2%的接种量分别接种至H2O2浓度为0、0.4 mmol/L、0.7 mmol/L和1.0 mmol/L的MRS液体培养基中,37 ℃恒温培养36 h,测定培养后发酵液在波长610 nm下的吸光度值(OD610nm值)。
(2)胆盐耐受性:参照陈偲等[13]的方法,将乳酸菌种子液按2%的接种量分别接种至牛胆盐含量为0、0.3%、0.5%的MRS液体培养基中。37 ℃恒温培养36 h,测定培养后发酵液在波长610 nm下的吸光度值。
(3)pH耐受性:将乳酸菌种子液以2%(1.0×109CFU/mL)的接种量分别接种至pH为2.5、3.5、4.5、5.5、6.5的MRS液体培养基中37 ℃恒温培养36 h,测定培养后发酵液在波长610 nm下的吸光度值。
1.3.6 筛选乳酸菌的分子生物学鉴定
使用细菌基因组DNA提取试剂盒提取菌株DNA,以此DNA为模板,27F(5'-AGAGTTTGATCCTGGCTCAG-3')和1492R(5'-GGTTACCTTGTTACGACTT-3')作为引物进行PCR扩增,PCR扩增条件为:95 ℃变性10 min;95 ℃预变性30 s,58 ℃退火30 s,72 ℃延伸90 s,35次循环;72 ℃再延伸5 min。扩增产物纯化后委托生工生物工程(上海)股份有限公司进行测序,测序结果提交美国国家生物技术信息中心(national center for biotechnology information,NCBI)GenBank数据库采用基本局部比对搜索工具(basic local alignment search tool,BLAST)进行对比分析,并使用MEGA 7.0软件中的邻接法(neighbor-joining,NJ)构建系统发育树。
1.3.7 筛选菌株发酵制备萝卜泡菜
参照刘振恒等[14]的方法并稍作修改。在沸水中将泡菜罐煮5 min,烘箱烘干。添加质量分数3.0%的盐于纯净水中煮沸,冷却至室温后加入3%的52%vol白酒与2.0%的筛选菌株悬浮液备用。挑选组织鲜嫩、皮薄、粗纤维少,没有烂心、黑心,形状呈长条状的白萝卜,改刀为10 mm×10 mm×50 mm左右的长条形,放入泡菜罐中,泡菜水应没过萝卜,罐口周围用无菌水灌满,在20 ℃条件下发酵30 d。以不添加乳酸菌悬浮液的自然发酵组作为对照。
1.3.8 萝卜泡菜的理化指标、质构特性及感官评价
亚硝酸盐含量的测定:参考GB5009.33—2016《食品安全国家标准食品中亚硝酸盐与硝酸盐的测定》;总酸含量的测定:参考GB 12456—2021《食品安全国家标准 食品中总酸的测定》;总糖含量的测定:参考GB5009.8—2016《食品安全国家标准 食品中果糖、葡萄糖、蔗糖、麦芽糖、乳糖的测定》。
对萝卜泡菜的咀嚼性、脆性和硬度进行测定,其中测试模式为穿刺模式,探头为P/2柱形探头(直径2 mm),测试前速率为1 mm/s,测试中速率为5 mm/s,测试后速率为5 mm/s,压缩比为50%,最小感知力5 g,每个萝卜条取3个测试点[15]。
参照孟繁博等[16]的方法对所制备的萝卜泡菜进行感官评价。 邀请10名经过培训的食品专业同学和5名老师参照感官评分标准(见表1)对各泡菜的色泽、气味、滋味、脆度进行评分,结果取平均值。
表1 萝卜泡菜感官评分标准
Table 1 Sensory evaluation standards of radish pickle
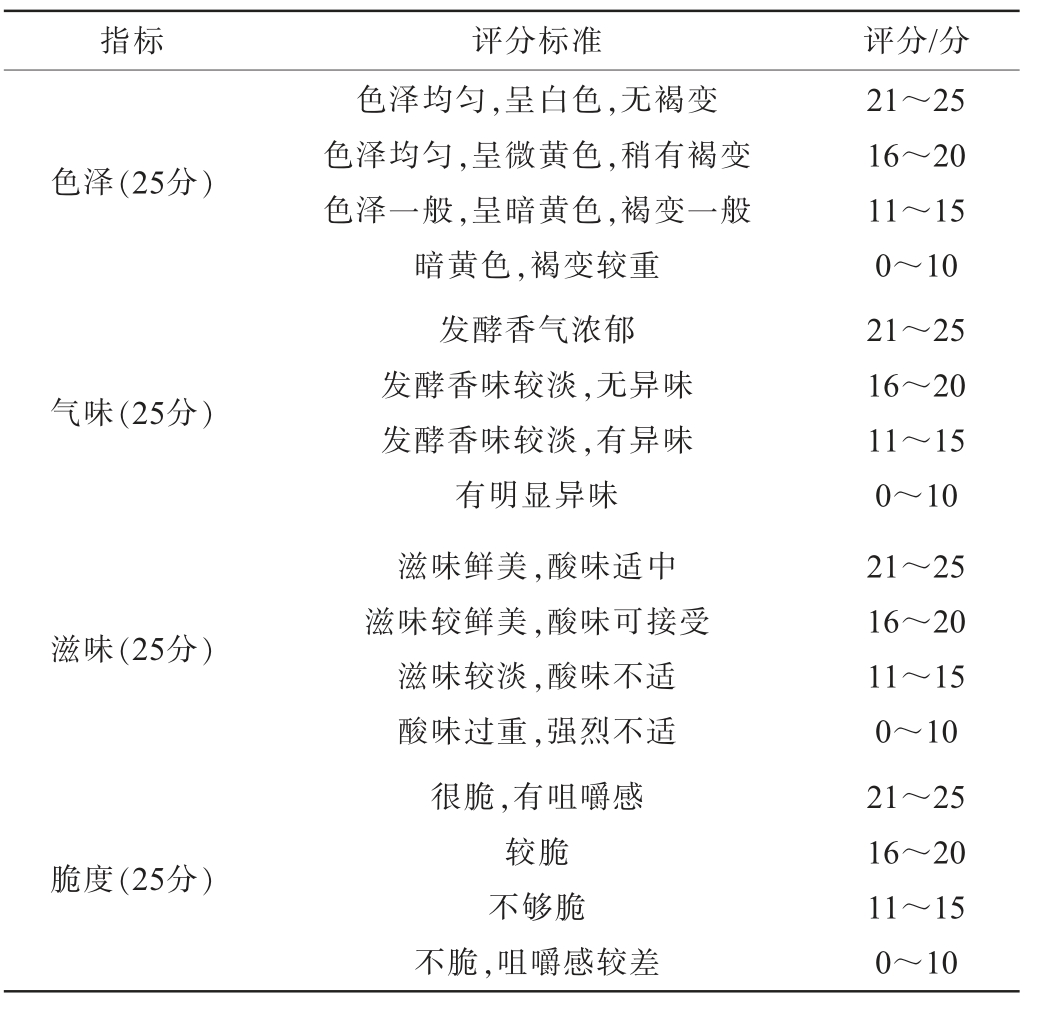
指标 评分标准 评分/分色泽(25分)气味(25分)滋味(25分)脆度(25分)色泽均匀,呈白色,无褐变色泽均匀,呈微黄色,稍有褐变色泽一般,呈暗黄色,褐变一般暗黄色,褐变较重发酵香气浓郁发酵香味较淡,无异味发酵香味较淡,有异味有明显异味滋味鲜美,酸味适中滋味较鲜美,酸味可接受滋味较淡,酸味不适酸味过重,强烈不适很脆,有咀嚼感较脆不够脆不脆,咀嚼感较差21~25 16~20 11~15 0~10 21~25 16~20 11~15 0~10 21~25 16~20 11~15 0~10 21~25 16~20 11~15 0~10
1.3.9 萝卜泡菜中挥发性风味成分检测
固相微萃取条件[17]:称取0.5 g泡菜与5 mL蒸馏水于20 mL萃取瓶中,加入3 g氯化钠和10 μL 2-甲基-3-庚酮(0.1 mg/mL)作为内标物。在50 ℃平衡15 min后将提前老化好的萃取探针插入样品瓶萃取20 min。萃取完成后将探针插入GC进样口,250 ℃解吸5 min。
气相色谱条件:HP-5MSUI毛细管色谱柱(30m×0.25mm×0.25 μm),载气为高纯氦气(He),流速为1.0 mL/min,不分流模式进样,进样口温度为250 ℃。 升温程序:起始温度50 ℃,保持3 min,以5 ℃/min升至150 ℃,保持3 min,再以10 ℃/min的速率升至230 ℃,保持3 min。
质谱条件:电离方式为电子电离(electron ionization,EI)源,电子能量70 eV,离子源温度230 ℃,接口温度280 ℃,全扫描模式,扫描范围25~450 m/z。
定性定量方法:由GC-MS得到的谱图与美国国家标准与技术研究院(national institute of standards and technology,NIST)2001标准谱库进行检索比对定性;采用内标法对挥发性风味成分进行半定量分析。
1.3.10 数据处理
所有实验均进行3次平行,使用SPSS 25进行数据分析处理,使用Duncan法进行显著性分析(P<0.05时认为差异显著),结果采用“平均值±标准差”表示。
2 结果与分析
2.1 萝卜泡菜与泡菜水中乳酸菌的分离与纯化
从市售的泡菜与泡菜水中分离得到40株与43株具有溶钙圈的菌株,分别编号为MP1~MP40与MS1~MS43,少部分菌落颜色为黄色,大部分菌落呈乳白色,表面凸起、光滑、湿润、边缘整齐,其中有17株溶钙圈与菌落直径比>2。将这17株菌株接种到MRS液体培养基中,37 ℃培养48 h后检测产酸量并进行革兰氏染色与过氧化氢酶实验,结果见表2。由表2可知,所选17株菌株均有较强的产酸能力,总酸含量在3.05~7.85 g/L之间,超过7 g/L的有6株,分别为MP26、MP34、MS6、MS15、MS27和MS32,其中MP26总酸含量最高,赵山山等[12]筛选得到的乳酸菌产酸量均在4 g/L以下,与本次筛选得到的菌株相比,均低于除菌株MS8外的乳酸菌,这可能是培养底物与培养条件存在差异。在溶钙圈>2的菌株中共发现革兰氏阳性菌13株,过氧化氢酶实验结果阴性菌株16株。选取同时满足革兰氏阳性与过氧化氢酶实验结果阴性的13株菌进行后续实验。
表2 初筛菌株的菌落形态、总酸含量、革兰氏染色及过氧化氢酶实验结果
Table 2 Colony morphology, total acid content, Gram staining and catalase test results of the initially screened strains
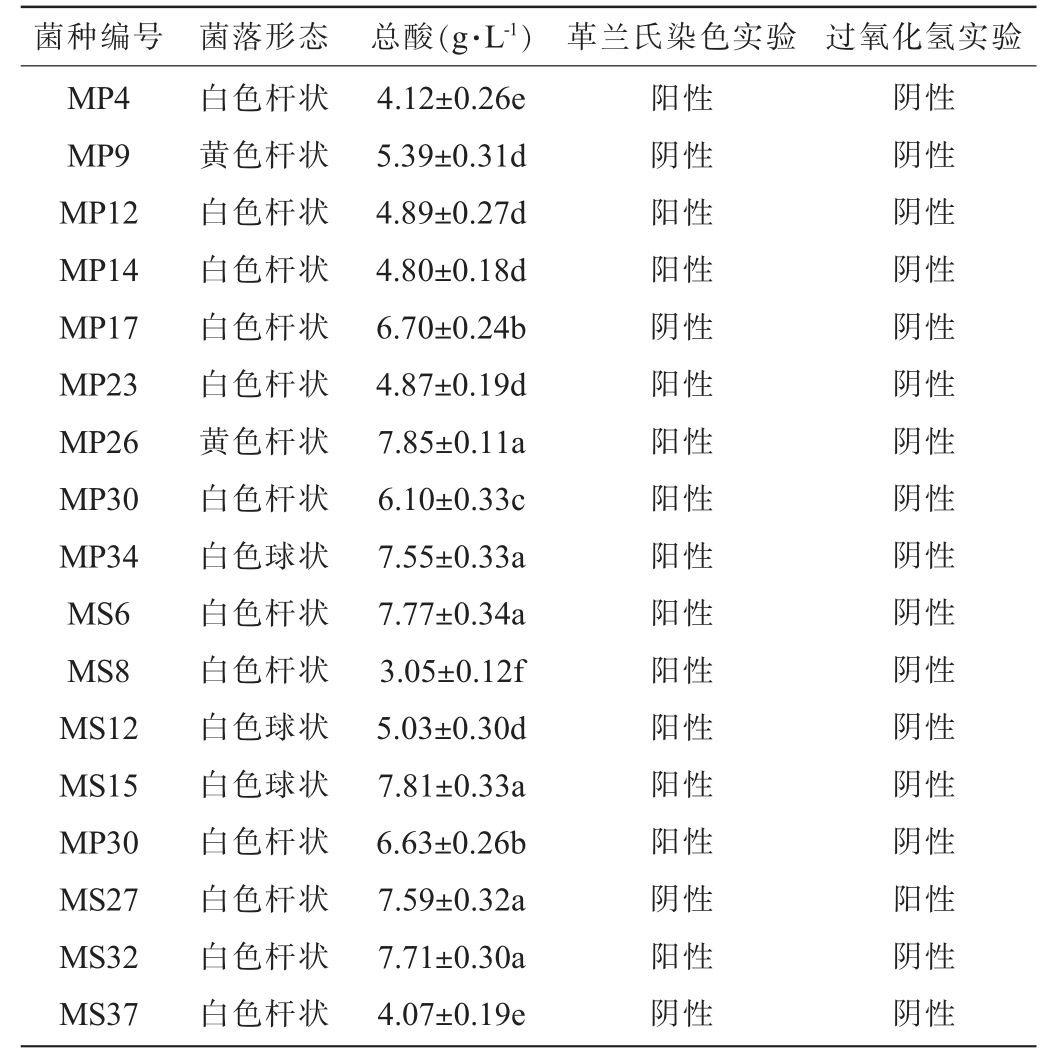
注:同一列不同字母表示不同菌株总酸含量差异显著(P<0.05)。下同。
菌种编号 菌落形态 总酸(g·L-1) 革兰氏染色实验 过氧化氢实验MP4 MP9 MP12 MP14 MP17 MP23 MP26 MP30 MP34 MS6 MS8 MS12 MS15 MP30 MS27 MS32 MS37白色杆状黄色杆状白色杆状白色杆状白色杆状白色杆状黄色杆状白色杆状白色球状白色杆状白色杆状白色球状白色球状白色杆状白色杆状白色杆状白色杆状4.12±0.26e 5.39±0.31d 4.89±0.27d 4.80±0.18d 6.70±0.24b 4.87±0.19d 7.85±0.11a 6.10±0.33c 7.55±0.33a 7.77±0.34a 3.05±0.12f 5.03±0.30d 7.81±0.33a 6.63±0.26b 7.59±0.32a 7.71±0.30a 4.07±0.19e阳性阴性阳性阳性阴性阳性阳性阳性阳性阳性阳性阳性阳性阳性阴性阳性阴性阴性阴性阴性阴性阴性阴性阴性阴性阴性阴性阴性阴性阴性阴性阳性阴性阴性
2.2 初筛菌株抗氧化活性分析
乳酸菌常用于泡菜、酸奶等产品的发酵,一是可以为产品增加风味,二是可以显著提升产品的抗氧化活性,增加产品的营养价值,因此,乳酸菌是否具有较强的抗氧化能力,是证明其功能性的重要指标[18]。 对比分析了筛选得到的13株菌株胞内物质与胞外物质的抗氧化活性,结果见表3。由表3可知,不同菌株的抗氧化活性存在较大差异,但同一株菌还原力、羟自由基清除能力均表现为无细胞上清液高于细胞破碎液,除菌株MP23外,其他12株菌无细胞上清液的DPPH自由基清除能力也高于细胞破碎物,说明筛选菌株产生的具有抗氧化活性的物质主要是胞外物质,在泡菜发酵过程中主要体现在泡菜水与泡菜中。
表3 初筛菌株无细胞上清液与细胞破碎物的抗氧化活性
Table 3 Antioxidant activity of cell-free supernatant and cell fragments of the initially screened strains
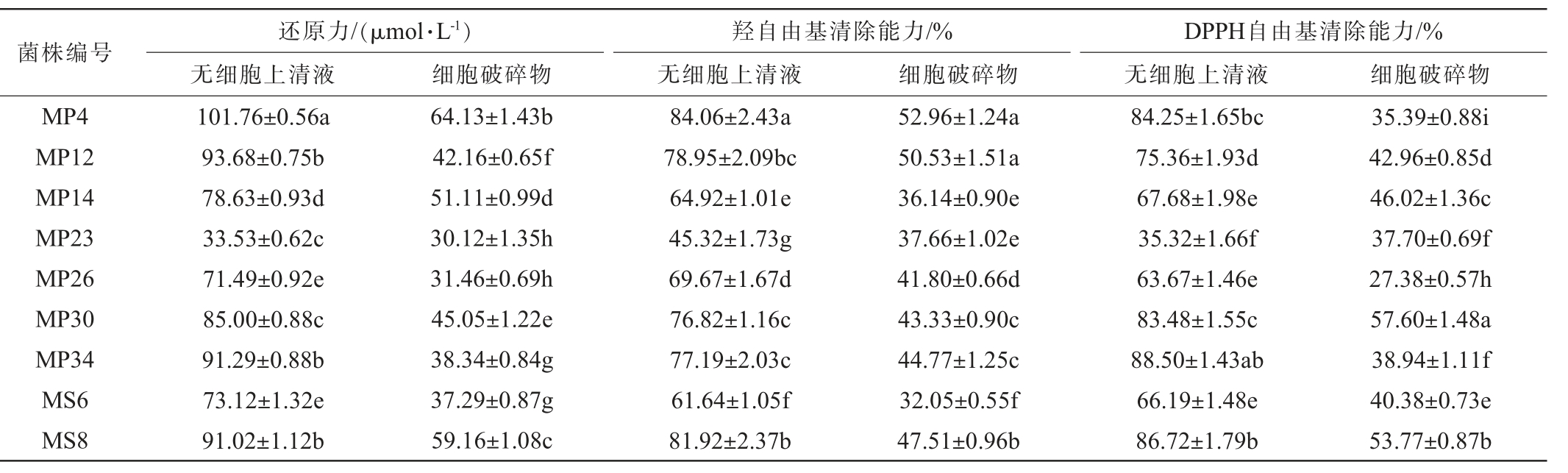
菌株编号 还原力/(μmol·L-1)无细胞上清液细胞破碎物 细胞破碎物羟自由基清除能力/%无细胞上清液DPPH自由基清除能力/%无细胞上清液 细胞破碎物MP4 MP12 MP14 MP23 MP26 MP30 MP34 MS6 MS8 101.76±0.56a 93.68±0.75b 78.63±0.93d 33.53±0.62c 71.49±0.92e 85.00±0.88c 91.29±0.88b 73.12±1.32e 91.02±1.12b 64.13±1.43b 42.16±0.65f 51.11±0.99d 30.12±1.35h 31.46±0.69h 45.05±1.22e 38.34±0.84g 37.29±0.87g 59.16±1.08c 84.06±2.43a 78.95±2.09bc 64.92±1.01e 45.32±1.73g 69.67±1.67d 76.82±1.16c 77.19±2.03c 61.64±1.05f 81.92±2.37b 52.96±1.24a 50.53±1.51a 36.14±0.90e 37.66±1.02e 41.80±0.66d 43.33±0.90c 44.77±1.25c 32.05±0.55f 47.51±0.96b 84.25±1.65bc 75.36±1.93d 67.68±1.98e 35.32±1.66f 63.67±1.46e 83.48±1.55c 88.50±1.43ab 66.19±1.48e 86.72±1.79b 35.39±0.88i 42.96±0.85d 46.02±1.36c 37.70±0.69f 27.38±0.57h 57.60±1.48a 38.94±1.11f 40.38±0.73e 53.77±0.87b
续表
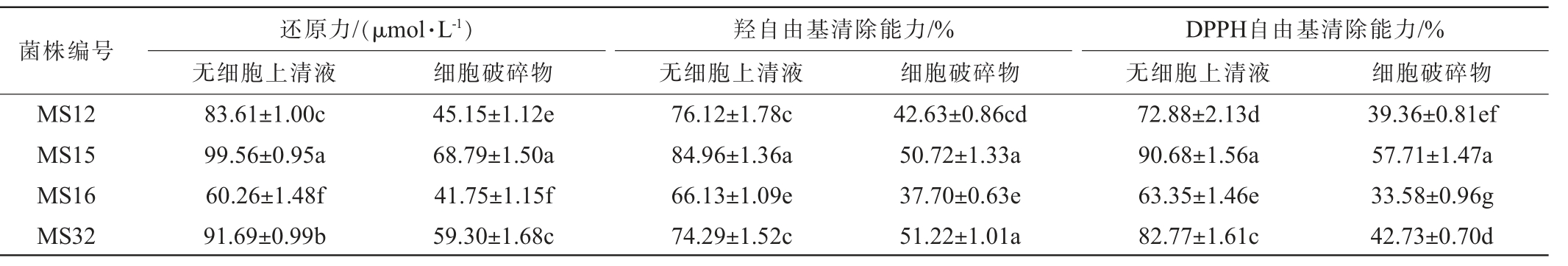
菌株编号 还原力/(μmol·L-1)无细胞上清液细胞破碎物 细胞破碎物羟自由基清除能力/%无细胞上清液DPPH自由基清除能力/%无细胞上清液 细胞破碎物MS12 MS15 MS16 MS32 83.61±1.00c 99.56±0.95a 60.26±1.48f 91.69±0.99b 45.15±1.12e 68.79±1.50a 41.75±1.15f 59.30±1.68c 76.12±1.78c 84.96±1.36a 66.13±1.09e 74.29±1.52c 42.63±0.86cd 50.72±1.33a 37.70±0.63e 51.22±1.01a 72.88±2.13d 90.68±1.56a 63.35±1.46e 82.77±1.61c 39.36±0.81ef 57.71±1.47a 33.58±0.96g 42.73±0.70d
13株菌的无细胞上清液还原力在33.53~101.76 μmol/L之间,总还原力最高为菌株MP4,其次为菌株MS15;羟自由基清除能力在45.32%~84.96%之间,超过70%的有8株,其中清除能力较强的有菌株MP4、MS8与MS15;DPPH自由基清除能力在35.32%~90.68%之间,最高的为菌株MS15。13株菌的细胞破碎物的还原力在30.12~68.79 μmol/L之间,总还原力最高为菌株MS15,其次为菌株MP4;羟自由基清除能力在36.14%~52.96%之间,最高的为菌株MP4;DPPH自由基清除能力在27.38%~57.71%之间,最高的为MS15。 综上,13株菌中具有较强抗氧化活性的为菌株MP4、MP12、MP30、MS8、MS15。
2.3 初筛菌株耐受性分析
2.3.1 H2O2耐受性
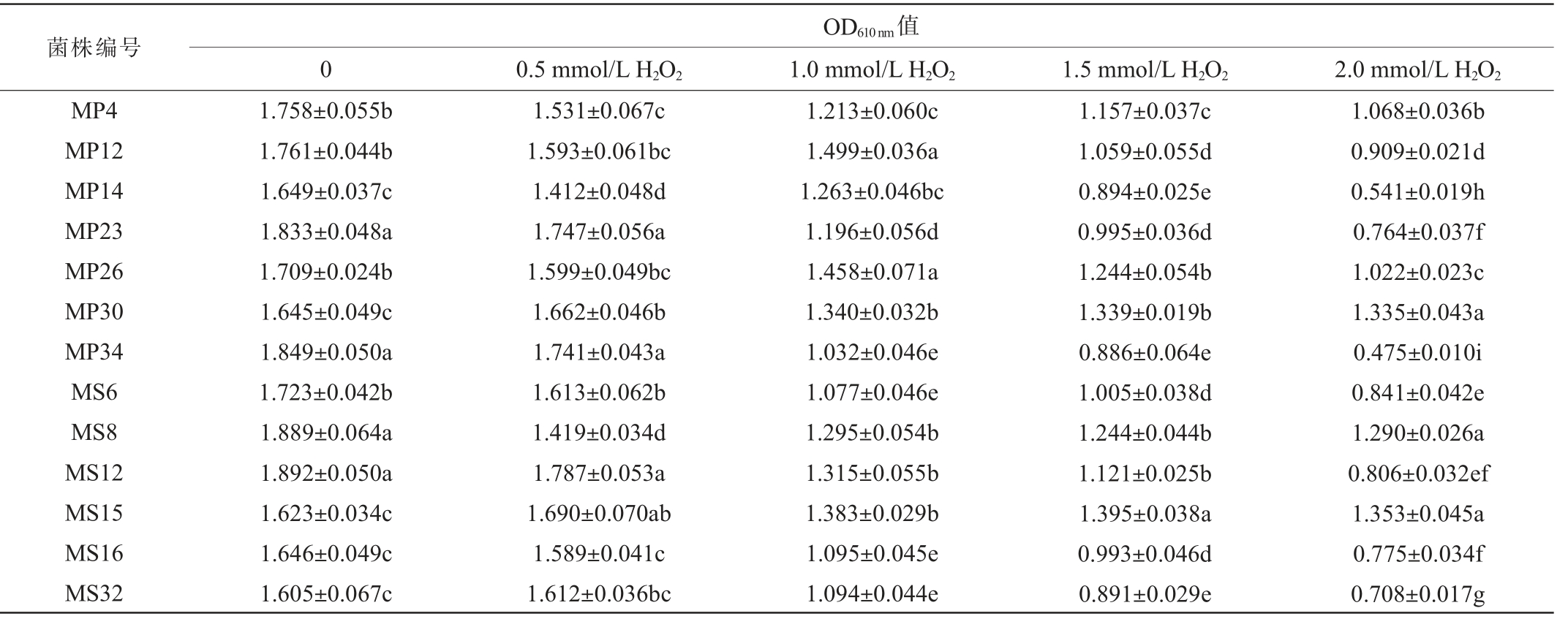
极性活性氧分子中,过氧化氢的稳定性最强[19]。乳酸菌通过人体,需具备一定的过氧化氢耐受能力,才能免被破坏。 因此,耐受过氧化氢能力为衡量乳酸菌抗氧化能力的指标之一[20]。 由表4可知,在H2O2浓度为0时,初筛菌株的生长情况良好,菌液的OD610nm值均>1.600。当H2O2浓度为0.5~1.5mmol/L时,随着浓度的增加,所有菌株的生长均受到不同程度的抑制。当H2O2浓度为2.0mmol/L时,菌株MP14、MP23、MP34、MS16和MS32的生长受到严重影响,生长基本停滞,而菌株MP4、MP26、MP30、MS8和MS15受过氧化氢影响较小,OD610 nm值均>1,表明其对高浓度过氧化氢具有较强的耐受能力。
表4 初筛菌株H2O2耐受性分析结果
Table 4 Analysis results of H2O2 tolerance of the initially screened strains
菌株编号MP4 MP12 MP14 MP23 MP26 MP30 MP34 MS6 MS8 MS12 MS15 MS16 MS32 OD610 nm值0 0.5 mmol/L H2O2 1.0 mmol/L H2O2 1.5 mmol/L H2O2 2.0 mmol/L H2O2 1.758±0.055b 1.761±0.044b 1.649±0.037c 1.833±0.048a 1.709±0.024b 1.645±0.049c 1.849±0.050a 1.723±0.042b 1.889±0.064a 1.892±0.050a 1.623±0.034c 1.646±0.049c 1.605±0.067c 1.531±0.067c 1.593±0.061bc 1.412±0.048d 1.747±0.056a 1.599±0.049bc 1.662±0.046b 1.741±0.043a 1.613±0.062b 1.419±0.034d 1.787±0.053a 1.690±0.070ab 1.589±0.041c 1.612±0.036bc 1.213±0.060c 1.499±0.036a 1.263±0.046bc 1.196±0.056d 1.458±0.071a 1.340±0.032b 1.032±0.046e 1.077±0.046e 1.295±0.054b 1.315±0.055b 1.383±0.029b 1.095±0.045e 1.094±0.044e 1.157±0.037c 1.059±0.055d 0.894±0.025e 0.995±0.036d 1.244±0.054b 1.339±0.019b 0.886±0.064e 1.005±0.038d 1.244±0.044b 1.121±0.025b 1.395±0.038a 0.993±0.046d 0.891±0.029e 1.068±0.036b 0.909±0.021d 0.541±0.019h 0.764±0.037f 1.022±0.023c 1.335±0.043a 0.475±0.010i 0.841±0.042e 1.290±0.026a 0.806±0.032ef 1.353±0.045a 0.775±0.034f 0.708±0.017g
2.3.2 胆盐耐受性
乳酸菌对胆盐的耐受力越高,说明其在肠道中的存活能力越强,越能展现乳酸菌在肠道中的益生特性[21]。由表5可知,胆盐含量为0时,微生物的生长情况良好,菌液的OD610nm值均>1.600。当胆盐含量为0.2%~0.6%时,随着其含量的增加,所有菌株的生长均受到不同程度的抑制。当胆盐含量为0.8%时,菌株MP12、MP14、MP23、MS6和MS32的生长受到严重抑制,菌株生长基本停滞,而菌株MP4、MS12、MS15和MS16的生长受胆盐影响较小,OD610 nm值均>1,表现出较好的胆盐耐受性。
表5 初筛菌株胆盐耐受性分析结果
Table 5 Analysis results of bile salt tolerance of the initially screened strains

菌株编号OD610 nm值0 0.2%胆盐 0.4%胆盐 0.6%胆盐 0.8%胆盐MP4 1.602±0.072c 1.571±0.032ab 1.481±0.055a 1.256±0.020a 1.115±0.017a
续表

菌株编号MP12 MP14 MP23 MP26 MP30 MP34 MS6 MS8 MS12 MS15 MS16 MS32 OD610 nm值0 0.2%胆盐 0.4%胆盐 0.6%胆盐 0.8%胆盐1.894±0.083a 1.896±0.040a 1.659±0.034c 1.621±0.060c 1.771±0.046b 1.681±0.053bc 1.740±0.076b 1.812±0.066ab 1.838±0.076ab 1.753±0.077b 1.783±0.042b 1.861±0.071a 1.611±0.047a 1.471±0.051bc 1.511±0.050b 1.325±0.044d 1.352±0.053d 1.644±0.066a 1.457±0.042c 1.434±0.031c 1.528±0.051b 1.627±0.049a 1.438±0.066c 1.616±0.034a 0.901±0.030f 0.944±0.030f 1.272±0.053c 1.184±0.052d 1.429±0.055ab 1.160±0.039d 1.317±0.051c 1.393±0.052b 1.203±0.056cd 1.444±0.030a 1.023±0.032e 1.419±0.063ab 0.629±0.026h 0.465±0.017k 0.549±0.020j 0.840±0.035f 0.834±0.032f 0.925±0.034e 0.581±0.021i 0.724±0.032g 1.280±0.040a 1.192±0.056b 1.281±0.041a 0.647±0.014h 0.447±0.022fg 0.405±0.027g 0.471±0.021f 0.811±0.027c 0.825±0.037c 0.875±0.018b 0.467±0.024f 0.705±0.026d 1.114±0.017a 1.105±0.040a 1.143±0.033a 0.557±0.018e
2.3.3 pH耐受性
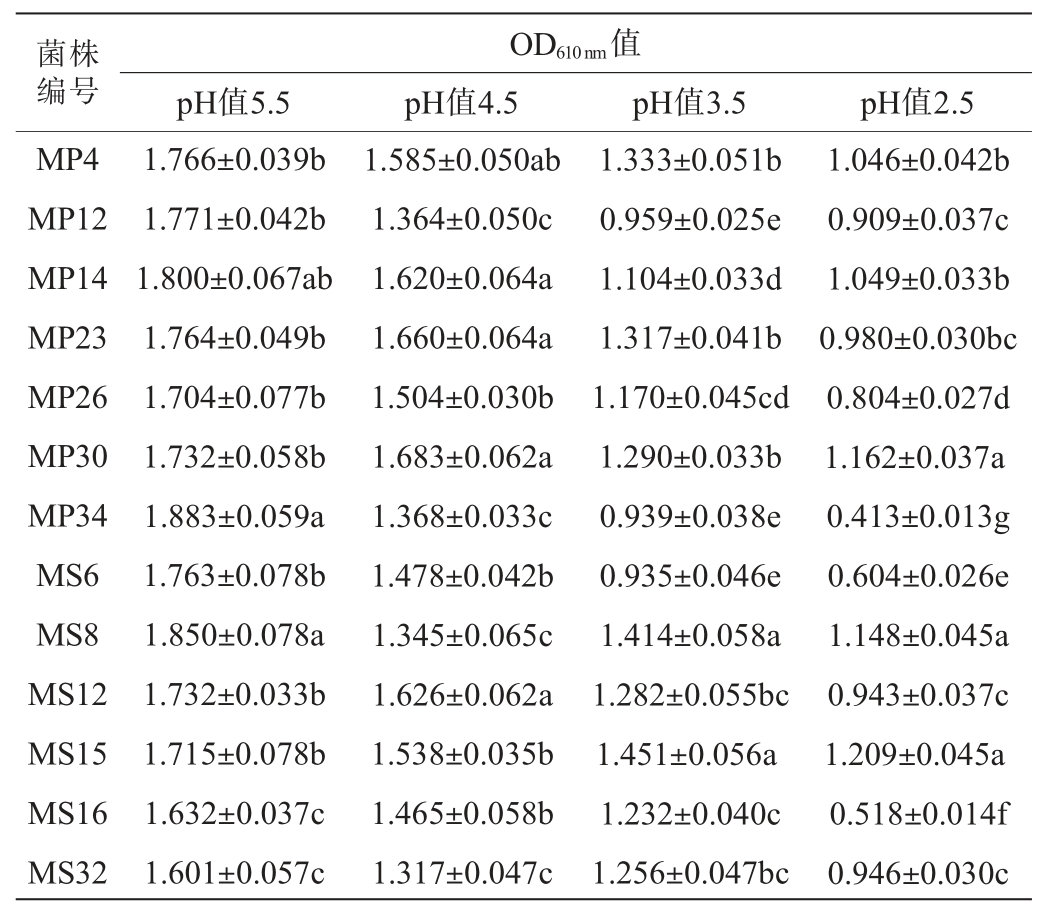
恩施泡菜的发酵为酸性环境,并且随着发酵时间的增加,环境中的酸度也随之增加,因此对微生物的耐酸性要求较高。由表6可知,当pH为5.5时,所有菌株生长良好,菌液的OD610nm值均>1.600。 当pH值为4.5和3.5时,随着pH的降低,所有菌株的生长均受到较大影响。当pH值为2.5时,菌株MP34、MS6、MP30生长受到严重抑制,而菌株MP4、MP14、MP30、MS8、MS15的生长受pH影响较小,OD610 nm值均>1,表现出较好的pH耐受性。
表6 初筛菌株pH耐受性分析结果
Table 6 Analysis results of pH tolerance of the initially screened strains
菌株编号MP4 MP12 MP14 MP23 MP26 MP30 MP34 MS6 MS8 MS12 MS15 MS16 MS32 OD610 nm值pH值5.5 pH值4.5 pH值3.5 pH值2.5 1.766±0.039b 1.771±0.042b 1.800±0.067ab 1.764±0.049b 1.704±0.077b 1.732±0.058b 1.883±0.059a 1.763±0.078b 1.850±0.078a 1.732±0.033b 1.715±0.078b 1.632±0.037c 1.601±0.057c 1.585±0.050ab 1.364±0.050c 1.620±0.064a 1.660±0.064a 1.504±0.030b 1.683±0.062a 1.368±0.033c 1.478±0.042b 1.345±0.065c 1.626±0.062a 1.538±0.035b 1.465±0.058b 1.317±0.047c 1.333±0.051b 0.959±0.025e 1.104±0.033d 1.317±0.041b 1.170±0.045cd 1.290±0.033b 0.939±0.038e 0.935±0.046e 1.414±0.058a 1.282±0.055bc 1.451±0.056a 1.232±0.040c 1.256±0.047bc 1.046±0.042b 0.909±0.037c 1.049±0.033b 0.980±0.030bc 0.804±0.027d 1.162±0.037a 0.413±0.013g 0.604±0.026e 1.148±0.045a 0.943±0.037c 1.209±0.045a 0.518±0.014f 0.946±0.030c
由于泡菜发酵环境独特,需要菌株具备生长迅速、产酸能力强的优点,同时作为益生菌,还应注重抗氧化活性高、耐酸、耐过氧化氢与耐胆盐的能力。 综上,菌株MP4、MP30、MS12和MS15为优良菌株。
2.4 四株筛选乳酸菌的分子生物学鉴定
基于16S rRNA基因序列构建了4株优良乳酸菌菌株的系统发育树,结果见图1。由图1可知,菌株MP4与副干酪乳杆菌(Lacticaseibacillus paracasei)(OR142127.1)和(Lacticaseibacillus paracasei)(OR029106.1)聚类在一起,同源性为100%,被鉴定为副干酪乳杆菌(Lacticaseibacillus paracasei);菌株MP30与植物乳植杆菌(Lactiplantibacillusplantarum)(OK287090.1)聚类在一起,同源性为100%,被鉴定为植物乳植杆菌(Lactiplantibacillus plantarum);菌株MS12与乳酸片球菌(Pediococcus acidilactici)(PP528156.1)聚类在一起,同源性为100%,菌株MS15与Pediococcus acidilactici(OR482644.1)和Pediococcus acidilactici(PP101259.1)聚类在一起,同源性为100%,被鉴定为乳酸片球菌(Pediococcus acidilactici)。
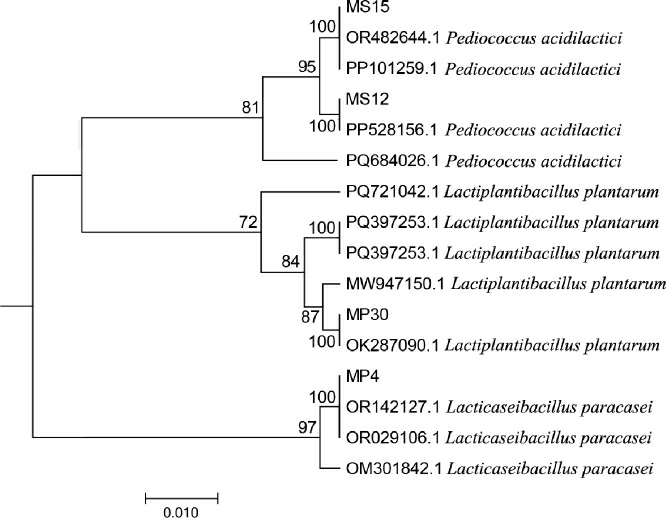
图1 基于16S rRNA基因序列4株筛选菌株的系统发育树
Fig.1 Phylogenetic tree of four screened strains based on 16S rRNA gene sequence
2.5 筛选菌株发酵萝卜泡菜的理化指标、质构特性及感官评分
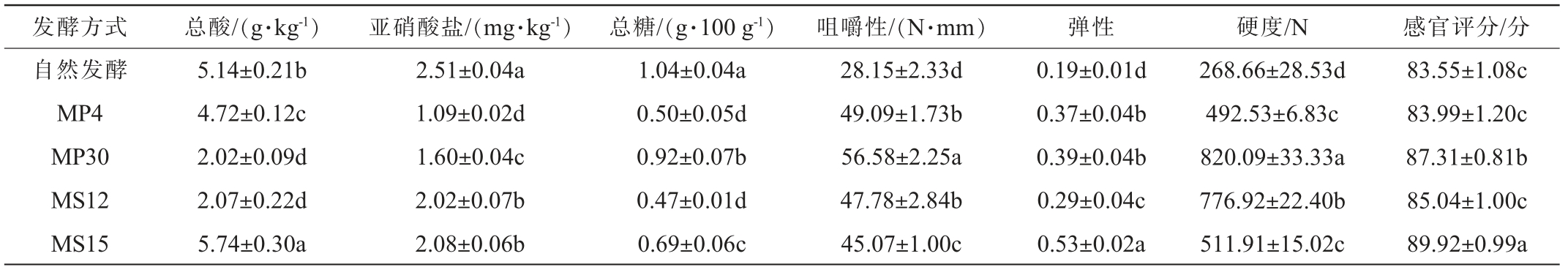
泡菜的酸度、清爽口感是其深受消费者喜爱的原因之一,果胶、纤维素、半纤维素、碳水化合物和少量的蛋白质是萝卜的主要成分,其中果胶的分解是导致泡菜脆度下降的主要因素,常用硬度、弹性和咀嚼性3个指标来评价泡菜的质构[22]。利用4株筛选的优良乳酸菌发酵制备泡菜,所得萝卜泡菜的理化指标、质构特性及感官评分见表7。 由表7可知,接种纯种乳酸菌发酵的泡菜亚硝酸盐、总糖含量显著低于自然发酵(P<0.05),分别为1.09~2.08 mg/kg、0.47~0.92 g/100 g;菌株MS15发酵的泡菜总酸含量显著高于自然发酵,其余3组均显著低于自然发酵(P<0.05);质构方面,接种乳酸菌制得的泡菜咀嚼性、弹性、硬度均显著高于自然发酵(P<0.05),一定程度上提升了泡菜的口感。 其中菌株MP30发酵的泡菜咀嚼性、硬度最高,分别为56.58 N·mm、820.09 N,MS15发酵的泡菜弹性最高,为0.53。感官评价中,接种4株优良乳酸菌发酵得到的泡菜感官评分均高于自然发酵方式,菌株MS15发酵的泡菜感官评分最高,为89.92分。产生上述现象原因可能是不同乳酸菌在生长繁殖过程中生产的酶种类与含量存在差异,导致接种不同乳酸菌发酵泡菜萝卜中果胶和果胶纤维素的分解速度存在较大差异,从而影响泡菜的各项指标[23]。 综上,菌株MS15发酵的泡菜总酸、弹性、感官评分等均优于其余四组,表现出较好的单菌发酵潜质。
表7 筛选菌株发酵萝卜泡菜的理化指标、质构特性及感官评分
Table 7 Physiochemical indicators, texture characteristics and sensory scores of radish pickle fermented by screened strains
发酵方式 总酸/(g·kg-1) 亚硝酸盐/(mg·kg-1) 总糖/(g·100 g-1) 咀嚼性/(N·mm) 弹性 硬度/N 感官评分/分自然发酵MP4 MP30 MS12 MS15 5.14±0.21b 4.72±0.12c 2.02±0.09d 2.07±0.22d 5.74±0.30a 2.51±0.04a 1.09±0.02d 1.60±0.04c 2.02±0.07b 2.08±0.06b 1.04±0.04a 0.50±0.05d 0.92±0.07b 0.47±0.01d 0.69±0.06c 28.15±2.33d 49.09±1.73b 56.58±2.25a 47.78±2.84b 45.07±1.00c 0.19±0.01d 0.37±0.04b 0.39±0.04b 0.29±0.04c 0.53±0.02a 268.66±28.53d 492.53±6.83c 820.09±33.33a 776.92±22.40b 511.91±15.02c 83.55±1.08c 83.99±1.20c 87.31±0.81b 85.04±1.00c 89.92±0.99a
2.6 筛选菌株发酵萝卜泡菜挥发性风味成分分析
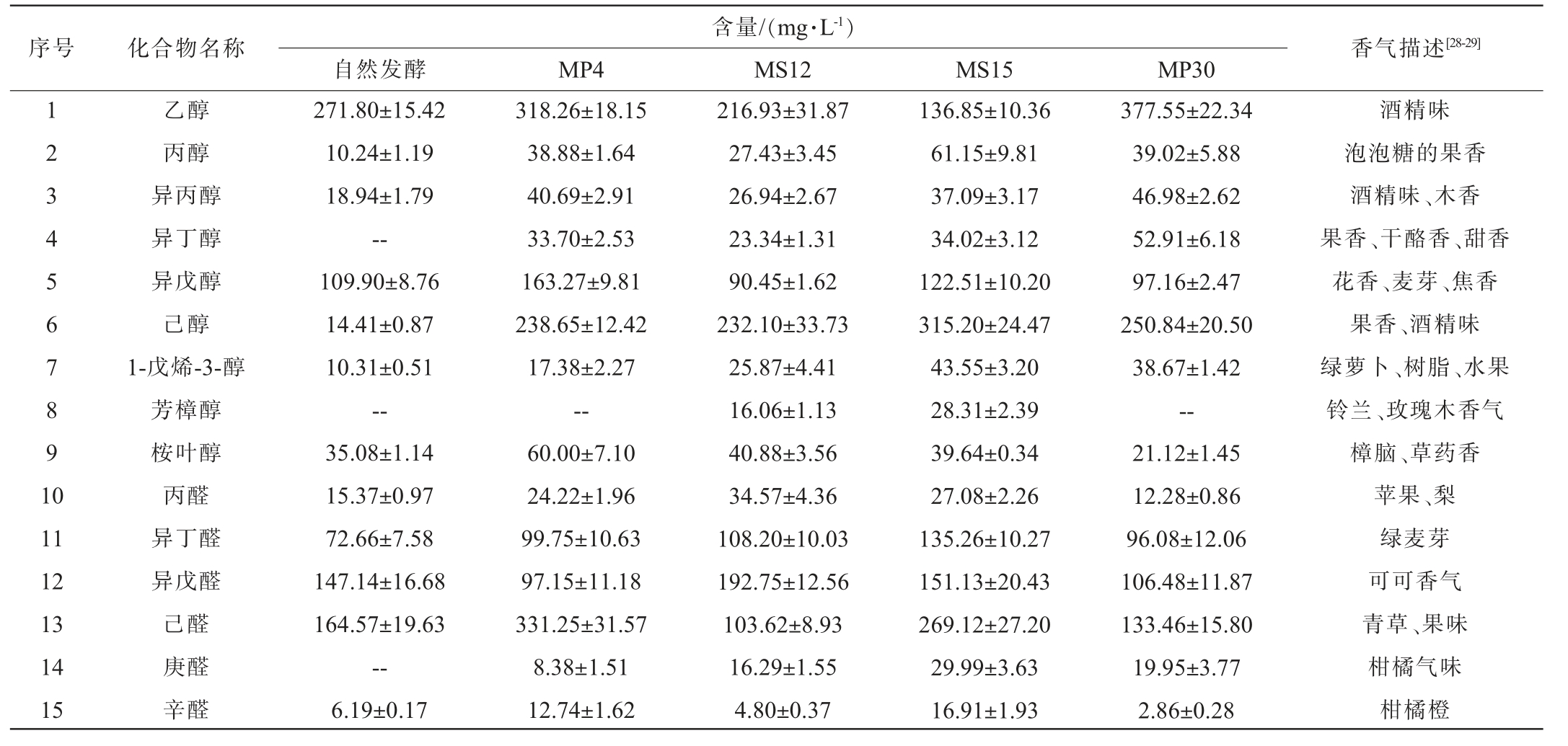
自然发酵与接种筛选乳酸菌发酵所得泡菜的挥发性风味成分种类、含量及香气描述见表8。 由表8可知,4组实验组与对照组样品中共检测到挥发性风味成分37种,包括9种醇类、6种醛类、12种酯类、2种烯类、3种酮类、4种酸类与1种胺类物质。自然发酵与菌株MP4、MP30、MS12、MS15发酵得到的萝卜泡菜中分别检出30、34、33、35与35种挥发性风味成分,含量分别为1 843.99 mg/L、2 725.28 mg/L、2 524.85 mg/L、2 447.34 mg/L与2 833.81 mg/L,由此可见,利用本研究所筛乳酸菌纯种发酵的萝卜泡菜中挥发性风味成分种类与数量均高于自然发酵。
表8 筛选菌株发酵萝卜泡菜的挥发性风味成分含量检测结果及香气描述
Table 8 Detection results of volatile flavor components contents and aroma description of fermented radish pickle by screened strains
序号 化合物名称 香气描述[28-29]含量/(mg·L-1)自然发酵 MP4 MS12 MS15 MP30 1 2 3 4 5 6 7 8 9 1 0 11 12 13 14 15乙醇丙醇异丙醇异丁醇异戊醇己醇1-戊烯-3-醇芳樟醇桉叶醇丙醛异丁醛异戊醛己醛庚醛辛醛271.80±15.42 10.24±1.19 18.94±1.79--109.90±8.76 14.41±0.87 10.31±0.51--35.08±1.14 15.37±0.97 72.66±7.58 147.14±16.68 164.57±19.63--6.19±0.17 318.26±18.15 38.88±1.64 40.69±2.91 33.70±2.53 163.27±9.81 238.65±12.42 17.38±2.27--60.00±7.10 24.22±1.96 99.75±10.63 97.15±11.18 331.25±31.57 8.38±1.51 12.74±1.62 216.93±31.87 27.43±3.45 26.94±2.67 23.34±1.31 90.45±1.62 232.10±33.73 25.87±4.41 16.06±1.13 40.88±3.56 34.57±4.36 108.20±10.03 192.75±12.56 103.62±8.93 16.29±1.55 4.80±0.37 136.85±10.36 61.15±9.81 37.09±3.17 34.02±3.12 122.51±10.20 315.20±24.47 43.55±3.20 28.31±2.39 39.64±0.34 27.08±2.26 135.26±10.27 151.13±20.43 269.12±27.20 29.99±3.63 16.91±1.93 377.55±22.34 39.02±5.88 46.98±2.62 52.91±6.18 97.16±2.47 250.84±20.50 38.67±1.42--21.12±1.45 12.28±0.86 96.08±12.06 106.48±11.87 133.46±15.80 19.95±3.77 2.86±0.28酒精味泡泡糖的果香酒精味、木香果香、干酪香、甜香花香、麦芽、焦香果香、酒精味绿萝卜、树脂、水果铃兰、玫瑰木香气樟脑、草药香苹果、梨绿麦芽可可香气青草、果味柑橘气味柑橘橙
续表
序号 化合物名称 香气描述[28-29]含量/(mg·L-1)自然发酵 MP4 MS12 MS15 MP30 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37甲酸乙酯乙酸乙酯丙酸乙酯丁酸乙酯异丁酸乙酯乙酸异丁酯乙酸戊酯乙酸异戊酯乙酸己酯己酸乙酯辛酸乙酯乙酸苯乙酯萜品油烯反-2-己烯丙酮2-戊酮2-辛酮丁胺乙酸丁酸辛酸棕榈酸20.92±1.48 360.90±21.38 5.30±0.59--1.94±0.07 10.50±1.52--21.86±1.81 16.04±0.92 31.10±1.70 20.24±0.91 158.71±12.56——41.87±2.01 4.59±0.44 10.60±0.87 34.00±3.82 193.09±11.22 11.70±1.59 5.21±0.61 18.81±1.49 42.40±3.82 471.56±73.63 14.65±1.85 20.40±1.38--7.89±0.70 16.64±1.98 19.42±0.61--13.14±1.62 34.23±3.79 217.27±24.58 2.69±0.30 12.62±1.27 32.27±2.94 6.25±0.66 29.81±2.79 21.65±1.94 230.42±14.00 13.96±1.45 2.15±0.13 31.54±3.48 35.92±0.80 436.74±5.84 7.73±0.68 24.26±1.71 1.03±0.04 3.85±0.15 46.31±4.09 10.36±0.42 15.54±1.32 36.21±3.94 15.69±1.47 236.21±35.52 8.08±0.60 21.80±2.17 16.44±1.41 10.97±1.07 13.55±1.54 54.57±2.97 276.41±21.49——15.44±0.40 73.61±6.41 411.35±86.10 16.20±1.64 14.52±2.21 14.31±2.39 9.18±1.76 14.11±1.28 21.93±2.07 30.27±1.57 47.36±3.77 31.94±2.99 253.66±6.78 27.59±2.15--29.02±4.86 4.68±0.28 52.47±5.25 35.17±2.19 285.55±25.19 10.10±0.31 2.98±0.22--43.61±3.11 389.86±34.52--4.99±0.29--2.89±0.24 9.49±0.94 11.39±1.50 23.24±0.73 26.30±1.93 31.93±1.72 205.02±13.28 6.44±0.69--50.64±1.27 7.87±0.61 17.28±2.08 19.88±1.48 341.85±28.57 4.16±0.30 10.32±1.69 22.33±1.54果味、葡萄酒味葡萄味、甜味甜味、酒味苹果味、甜味朗姆酒甜果味,香蕉味香蕉味、甜味甜果味,香蕉味苹果味、梨味香蕉味、菠萝味蜡味、果味玫瑰花、蜂蜜香气柠檬、酸橙味香蕉、果香、奶酪苹果味、梨味水果、辛辣木质香、奶酪、酵母氨样鱼腥味具有刺激性气味黄油、奶油香味菠萝、蜂蜜香味特殊的蜡香味
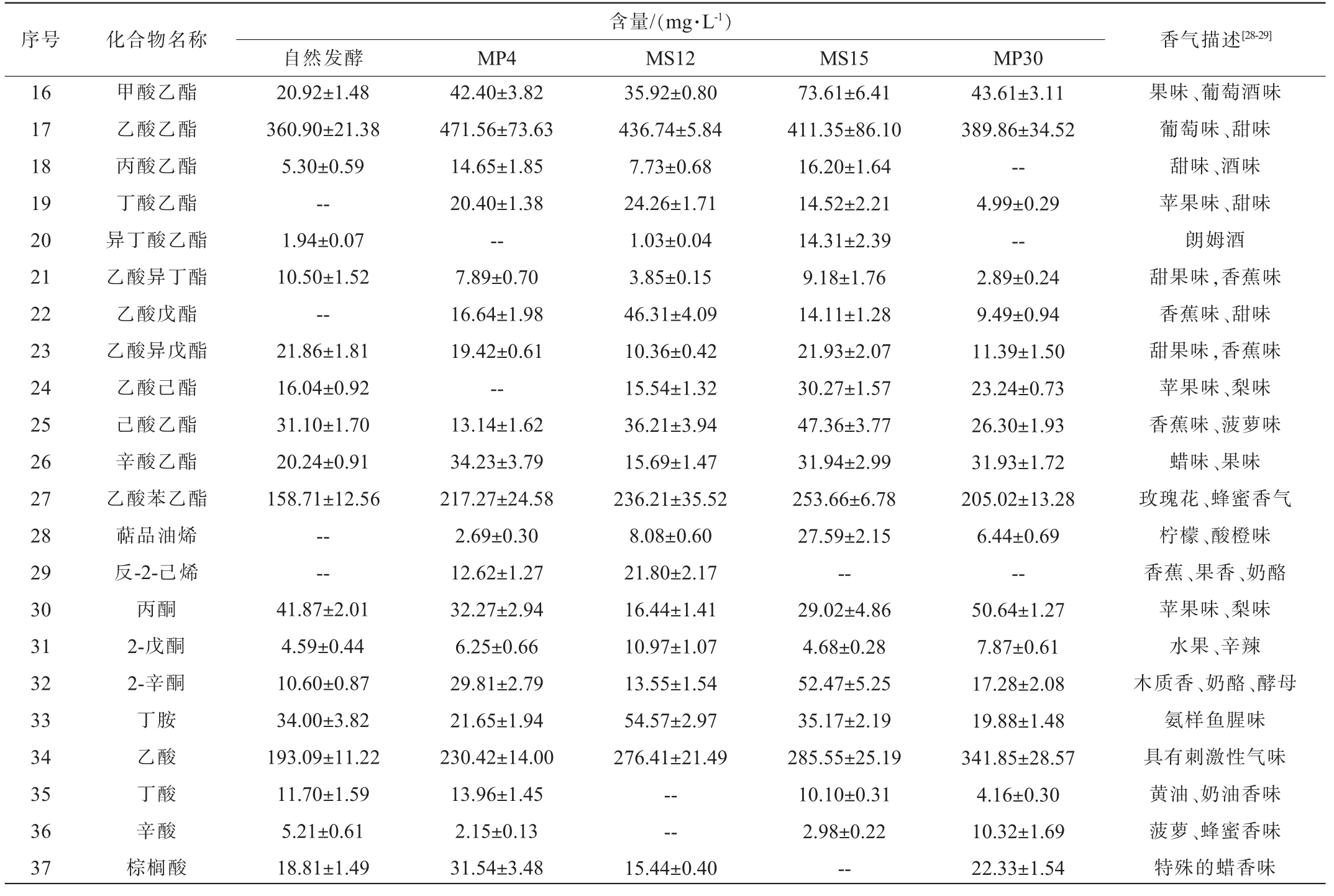
酯类物质具有果香味和香甜味,在自然发酵、菌株MP4、MP30、MS12与MS15发酵的萝卜泡菜中分别检出10种、10种、10种、12种和12种酯类物质,含量分别为647.51 mg/L、857.6 mg/L、748.72 mg/L、869.85 mg/L和938.44 mg/L,相对占比较高,对风味有较大影响。其中乙酸乙酯与乙酸苯乙酯含量相对较高,分别为360.90~471.56 mg/L、158.71~253.66 mg/L,可能是由于发酵前添加了一定量的高度白酒。三芥子酸甘油酯是一种特有的萝卜风味物质,具有辛辣味,也是萝卜香味的主要来源[24],但在本次实验中均未检出。
醇类物质是发酵蔬菜中重要的香气物质,可以赋予发酵蔬菜独特的风味。在自然发酵、菌株MP4、MP30、MS12与MS15发酵的萝卜泡菜中分别检测出7种、8种、8种、9种和9种醇类物质,含量分别为470.68mg/L、910.83mg/L、924.25mg/L、700 mg/L和818.32 mg/L,其中含量较高的有乙醇、异戊醇和己醇。 与自然发酵相比,菌株MS12与MS15发酵泡菜中乙醇含量相对较低,菌株MP4与MP30发酵泡菜中乙醇含量相对较高,而异戊醇刚好相反。4组乳酸菌发酵的泡菜中己醇含量与自然发酵相比均有明显提升,含量在232.10~315.20 mg/L之间,这可能是由于乳酸菌异型发酵产生的醇类物质导致,赋予了泡菜独特的果香风味[25]。
醛类物质通常具有辛辣味和刺激味,在5组样品中共检出6种醛类物质,以异丁醛、异戊醛与己醛为主,其中在自然发酵中未检出庚醛。酮类化合物以丙酮、2-戊酮和2-辛酮为主,可以赋予泡菜一定的果香[26]。酸类物质以乙酸为主,含量在193.09~341.85 mg/L之间,可以增加发酵萝卜的酸味,还可以减少醛类物质带来的刺激味。醛类、酮类和酸类物质的相对含量较少,但对发酵萝卜整体风味的形成具有较强的协同作用[27]。
3 结论
本研究从12份恩施泡菜与发酵母水中筛选产酸能力、抗氧化活性及耐受性强的优良乳酸菌,对其进行形态学观察及分子生物学鉴定。 应用筛选菌株发酵泡菜并考察其发酵性能。结果表明,在样品中筛选得到4株具有高产酸、高抗氧化活性与高耐受性的乳酸菌,分别编号为MP4、MP30、MS12和MS15。 经鉴定,菌株MP4为副干酪乳杆菌(Lactobacillus paracasei)、菌株MP30为植物乳植杆菌(Lactiplantibacillus plantarum)、菌株MS12与MS15为乳酸片球菌(Pediococcus acidilactici)。 采用4株筛选菌株制备泡菜,发现经菌株MS15发酵的泡菜感官评分最高,为89.92分,总酸含量、咀嚼性、弹性、硬度与香味均优于自然发酵的泡菜,具有单菌发酵泡菜的潜质。在4组实验组与对照组样品中共检测到37种挥发性风味成分,包括9种醇类、6种醛类、12种酯类、2种烯类、3种酮类、4种酸类与1种胺类。实验组泡菜挥发性成分含量在2 447.34~2 833.81 mg/L之间,远高于自然发酵的萝卜泡菜(1 843.99 mg/L)。本研究结果为提升泡菜品质与工业化生产提供基础数据支撑。
[1]杨洋,杨宇航,王洪伟,等.不同发酵剂对泡萝卜挥发性风味成分及感官品质的影响[J].食品与发酵工业,2023,49(4):175-184.
[2]王艳,胡跃,方红美,等.白萝卜泡菜加工工艺的研究[J].食品工业科技,2021,42(11):185-191.
[3]周佳,龙思伊,仝静雯,等.乳酸菌接种发酵泡菜工艺研究[J].中国果菜,2018,38(12):1-6.
[4]LI H C,HUANG J T,WANG Y Q,et al.Study on the nutritional characteristics and antioxidant activity of dealcoholized sequentially fermented apple juice with Saccharomyces cerevisiae and Lactobacillus plantarum fermentation[J].Food Chem,2021,363(30):130351.
[5]史婷,高甜甜,刘伟,等.不同发酵剂对剁辣椒品质的影响[J].食品与发酵工业,2022,48(15):144-153.
[6]李苹苹,张冬梅,全永亮,等.泡菜优良发酵剂的筛选研究[J].安徽农业科学,2012,40(16):8969-8971.
[7]阿丽亚·阿达力,梅时勇,张冀芳,等.优势乳酸发酵菌株筛选、鉴定及对发酵萝卜风味品质的影响[J].食品与机械,2024,40(6):53-61.
[8]国立东,毛吾丽旦·米吉提,王丽群,等.新疆传统酸马奶源乳酸菌的分离、鉴定及其益生特性研究[J].中国酿造,2025,44(6):100-108.
[9]HU X Y,PANG X,WANG P G,et al.Isolation and characterization of an antioxidant exopolysaccharide produced by Bacillus sp.S-1 from Sichuan pickles[J].Carbohydr Polym,2019,204:9-16.
[10]KANG C H,KIM J S,PARK H M,et al.Antioxidant activity and shortchain fatty acid production of lactic acid bacteria isolated from Korean individuals and fermented foods[J].3 Biotech,2021,11(5):217.
[11]檀茜倩,程笑笑,崔方超,等.泡菜中产β-葡萄糖苷酶植物乳杆菌的益生和酶学特性[J].中国食品学报,2024,24(9):69-79.
[12]赵山山,杨园园,周玉岩,等.贵州泡菜中乳酸菌的分离鉴定及其在泡菜发酵中的应用[J].中国酿造,2020,39(12):113-119.
[13]陈偲,张明,付竹贤,等.乳酸菌与酵母菌的复配筛选及在传统泡菜中应用[J].食品工业科技,2023,44(16):155-163.
[14]刘振恒,阴耕云,肖冬,等.泡菜中乳酸菌的筛选鉴定及发酵工艺优化[J].食品与生物技术学报,2024,43(9):125-132,172.
[15]倪慧,王强,魏冰倩,等.恩施市泡萝卜中乳酸菌的分离鉴定及其对品质的影响[J].食品工业科技,2019,40(17):64-68,78.
[16]孟繁博,黄道梅,郑秀艳.不同品种芥菜发酵酸菜的品质分析[J].中国调味品,2021,46(12):155-158.
[17]黄玉立,葛黎红,马思尧,等.乳酸菌与酵母菌互作对萝卜泡菜发酵进程及风味品质的影响[J].中国酿造,2024,43(4):197-202.
[18]李庆羊,吴祖芳,翁佩芳,等.植物乳杆菌和棒状乳杆菌对发酵萝卜干风味品质的影响[J].中国食品学报,2021,21(9):150-159.
[19]CHEN A J, LUO W, PENG Y T, et al.Quality and microbial flora changes of radish Paocai during multiple fermentation rounds[J].Food Control,2019,106:106733.
[20]PERICHETTI E,DEMICHELE A,CODINI M,et al.Antioxidative capacity of Lactobacillus fermentum LF31 evaluated in vitro by oxygen radical absorbance capacity assay[J].Nutrition,2014,30(7-8):936-938.
[21]RAGUL K, SYIEM I, SUNDAR K, et al.Characterization of probiotic potential of Bacillus species isolated from a traditional brine pickle[J].J Food Sci Technol,2017,54(13):4473-4483.
[22]侯小艺,王建辉,邓娜,等.乳酸菌对发酵蔬菜风味影响研究进展[J].食品与机械,2023,39(4):232-240.
[23]欧雪.接种乳酸菌发酵低盐泡酸菜工艺优化及辐照杀菌对其品质的影响[D].雅安:四川农业大学,2022.
[24]LIU D B, ZHANG C B, ZHANG J B, et al.Metagenomics reveals the formation mechanism of flavor metabolites during the spontaneous fermentation of potherb mustard(Brassica juncea var.multiceps)[J].Food Res Int,2021,148:110622.
[25]吕欣然,王德晟,刘水琳,等.产γ-氨基丁酸植物乳杆菌对发酵萝卜风味和品质的影响[J].中国食品学报,2024,24(12):224-232.
[26]王健霞,刘袆帆,徐玉娟,等.基于顶空-气相色谱-四极杆/飞行时间质谱及相对气味活度值分析潮汕橄榄菜风味物质组成[J].食品研究与开发,2024,45(7):158-164.
[27]薛冰洁,胡荣,吴良如,等.酸笋中微生物区系演替和风味物质形成机制的研究进展[J].食品与发酵工业,2024,50(4):315-321.
[28]李婧,张敏,杨金美,等.模拟老泡菜水的蔬菜汁发酵液制备工艺优化及其风味分析[J].中国酿造,2025,44(6):252-257.
[29]胡此海,杨絮,郭全友,等.萝卜泡菜母水中乳酸菌分离鉴定与发酵特性比较[J].食品与发酵工业,2023,49(23):111-119.