白酒是一种以粮谷为原料,以酒曲为糖化发酵剂,经蒸煮、糖化、发酵、蒸馏、陈酿、勾调而成的蒸馏酒[1]。其中,浓香型白酒以浓郁醇厚的香气和绵柔甘冽的口感深受消费者喜爱。其中,大曲是白酒酿造工艺中的灵魂,制曲温度不同,大曲特性有所区别。 中高温大曲是以小麦为主要原料,在55~60 ℃条件下经拌曲、定型、堆积、发酵和成熟等工艺制成[2],其生产过程中富集了酿造环境中丰富的微生物,产生各种酶类和风味前体,在酿造过程中发挥着极为关键的作用[3]。中高温大曲具有复杂的微生物多样性,主要包括细菌、酵母菌、霉菌和少量放线菌等,其主要来源于原料、母曲和生产环境[4]。随着大曲发酵温度的升高,大部分不耐高温的酵母菌和霉菌逐渐被消亡, 大量细菌开始繁殖,且形成了以嗜热菌为主的特殊细菌类群结构[5]。杨勇等[6]研究表明,中高温大曲在不同发酵阶段的优势细菌属菌群具有明显差异,且发酵完成后主要以克罗彭斯特德菌属(Kroppenstedtia)、高温放线菌属(Thermoactinomyces)、葡萄球菌属(Staphylococcus)和部分乳酸菌为主。
Illumina MiSeq高通量测序技术灵敏度高、耗时短、成本低,广泛应用于复杂微生物类群解析[7]。 马梦月等[8]采用MiSeq高通量测序技术对山东省临沂市和河南省周口市中高温大曲的细菌多样性进行比较分析发现,不同地区中高温大曲中存在独特的细菌菌群及真菌类群差异明显。因此,对不同地区大曲的细菌多样性解析对白酒品质提升具有重要意义。
该研究采用高通量测序解析了内蒙古巴彦淖尔河套地区中高温大曲细菌菌群结构,与江西鹰潭地区中高温大曲的细菌菌群进行比较分析,通过线性判别分析效应大小(linear discriminant analysis effect size,LEfSe)分析差异菌群,并对细菌基因功能进行预测。以期为不同酿酒产区微生物资源的挖掘提供理论基础,为白酒风味形成机制的研究提供数据支撑。
1 材料与方法
1.1 材料与试剂
1.1.1 原料
15个中高温大曲样品(HT1~HT15):采集自内蒙古自治区河套地区某酒厂制曲车间,采集时间为2022年4月份,所有样品均以小麦为原料,采集的样品打磨成粉末后置于-4 ℃冰箱备用。
1.1.2 试剂
QIAGEN DNeasy mericon Food Kit 脱氧核糖核酸(deoxyribonucleic acid,DNA)基因组提取试剂盒:德国QIAGEN公司;聚合酶链式反应(polymerase chain reaction,PCR)试剂:北京全式金生物技术有限公司;正反向引物338F/806R:上海桑尼生物科技有限公司;MiSeq高通量测序配套试剂:美国Illumina公司。
1.2 仪器与设备
DFT-300小型高速粉碎机:温州顶力医疗器械有限公司;AR2202CN电子天平:奥豪斯仪器上海有限公司;Veriti FAST PCR仪:美国ABI公司;DYY-12电泳仪:北京六一仪器厂;UVPCDS8000凝胶成像分析系统:美国ProteinSimple公司;PE300 MiSeq高通量测序平台:美国Illumina公司;R930机架式服务器:美国DELL公司。
1.3 方法
1.3.1 中高温大曲宏基因组DNA提取、PCR扩增和高通量测序
精确称取样品2.50 g,参照DNA提取试剂盒的说明进行操作,借助试剂盒的裂解、吸附及洗脱技术分离纯化DNA,待提取完成后,使用1.0%琼脂糖凝胶电泳初步检测DNA的完整性,并使用Nano Drop分光光度计检测其浓度[9]。将合格的总DNA质量浓度调整至10~15 ng/μL后,以其为模板,使用正引物338F (5'-ACTCCTACGGGAGGCAGCA-3'),反向引物806R(5'-GGACTACHVGGGTWTCTAAT-3'),对细菌的16S rRNA V3~V4区域进行聚合酶链式反应(PCR)[10],为评估扩增效果,运用2.0%琼脂糖凝胶电泳对PCR产物进行进行质量检测。将检测合格的PCR产物被寄送至上海美吉生物医药有限公司,借助Illumina MiSeq高通量测序平台开展后续深度分析。测序工作完成后,所获高通量测序数据上传至美国国家生物技术信息中心(nationalcenter ofbiotechnology information,NCBI)的序列读取存档(sequence read archive,SRA)数据库中,项目对应编号为SRR32273184~SRR32273198。
1.3.2 鹰潭地区中高温大曲测序数据的下载
符漫等[11]对江西鹰潭地区不同类型大曲的细菌类群组成进行了研究,研究对象包括中高温大曲和高温大曲这两种样品各15份。本研究从NCBI的SRA数据库中下载了其中高温大曲样品的序列(SRR26667680~SRR26667695),并对其进行了重新编号,依次标记为YT1~YT15,用于后续归并分析。
1.3.3 生物信息学分析
参照CAI W C等[12]的方法基于QIIME(v1.9.1)平台对MiSeq测序所产生的对端序列进行高质量控制和筛选操作,使用基于重叠序列原理的FLASH软件(v1.2.11)对高质量序列进行合并处理[13],以确保数据的准确性与完整性,运用ChimeraSlayer对序列进行检验,筛选并剔除其中的嵌合体序列[14],以97%的相似性阈值为标准,使用UCLUST算法以97%的相似度对高质量序列进行划分并获取分类操作单元(operationaltaxonomic units,OTU)[15],最后,借助最新版本的核糖体数据库项目(ribosomal database project,RDP)数据库对具有代表性的OTU序列进行鉴定,以此分析细菌类群结构[16],并计算细菌类群的α多样性指数,基于加权和非加权的UniFrac距离进行了主坐标分析(principal coordinate analysis,PCoA)评估β多样性,并采用线性判别分析效应大小(linear discriminant analysis effect size,LEfSe)分析2个地区中高温大曲的差异菌群。
1.3.4 细菌类群基因功能的预测
为深入挖掘细菌类群在基因层面潜在的功能特性与作用机制,本研究基于PICRUSt软件,对所选取2个地区中高温大曲样品的细菌类群进行基因功能预测。同时,以直系同源蛋白数据库(clusters of orthologous groups of proteins,COG)为参照基准,对细菌类群所涉及的基因功能进行全面注释[17]。
1.3.5 数据处理
采用Excel 2016处理数据,运用两独立样本的秩和检验分析(Mann-Whitney)和置换多因素方差分析(permutational multivariate analysis of variance,PERMANOVA)比较2个地区中高温大曲样品细菌类群的差异,使用R(v4.1.3)软件绘图。
2 结果与分析
2.1 河套及鹰潭地区中高温大曲细菌类群多样性分析
本研究采用高通量测序技术对河套和鹰潭地区中高温大曲中细菌的多样性进行了解析,并在测序深度为25 010条序列的条件下计算超1指数、发现物种数、香农指数和辛普森指数,表征不同地区中高温大曲细菌类群的丰富度与多样性,结果见图1。
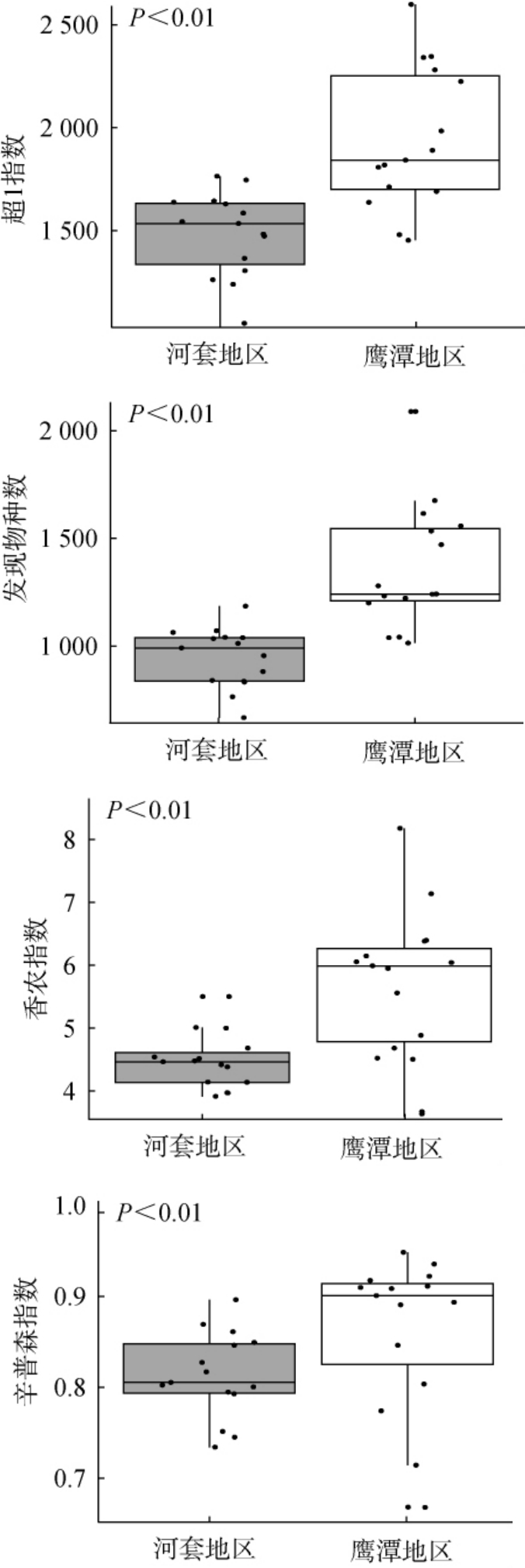
图1 两地区中高温大曲细菌菌群Alpha多样性比较分析
Fig.1 Comparative analysis of the Alpha diversity of bacterial flora in medium-high-temperature Daqu in the two regions
“P<0.01”代表差异极显著;“P<0.001”代表差异高度显著,下同。
超1指数和发现物种数主要反映微生物的物种丰富度,香农指数和辛普森指数则综合反映微生物的物种多样性,指数的值越高代表相应的物种丰富度或多样性水平越高[18]。由图1可知,河套地区中高温大曲样品的超1指数、发现物种数、香农指数和辛普森指数平均值分别为1 535、991、4.45和0.81,而鹰潭地区中高温大曲样品超1指数、发现物种数、香农指数和辛普森指数平均值分别为1 861、1 283、5.97和0.90。 经Mann-Whitney检验分析可知,河套地区中高温大曲细菌类群的超1指数、发现物种数及辛普森指数极显著低于河套地区(P<0.01),而香农指数高度显著低于河套地区(P<0.001)。由此可知,鹰潭地区大曲细菌类群丰富度和多样性均较高。
进一步利用基于加权和非加权UniFrac距离的主坐标分析(PCoA)评估β多样性,结果见图2。
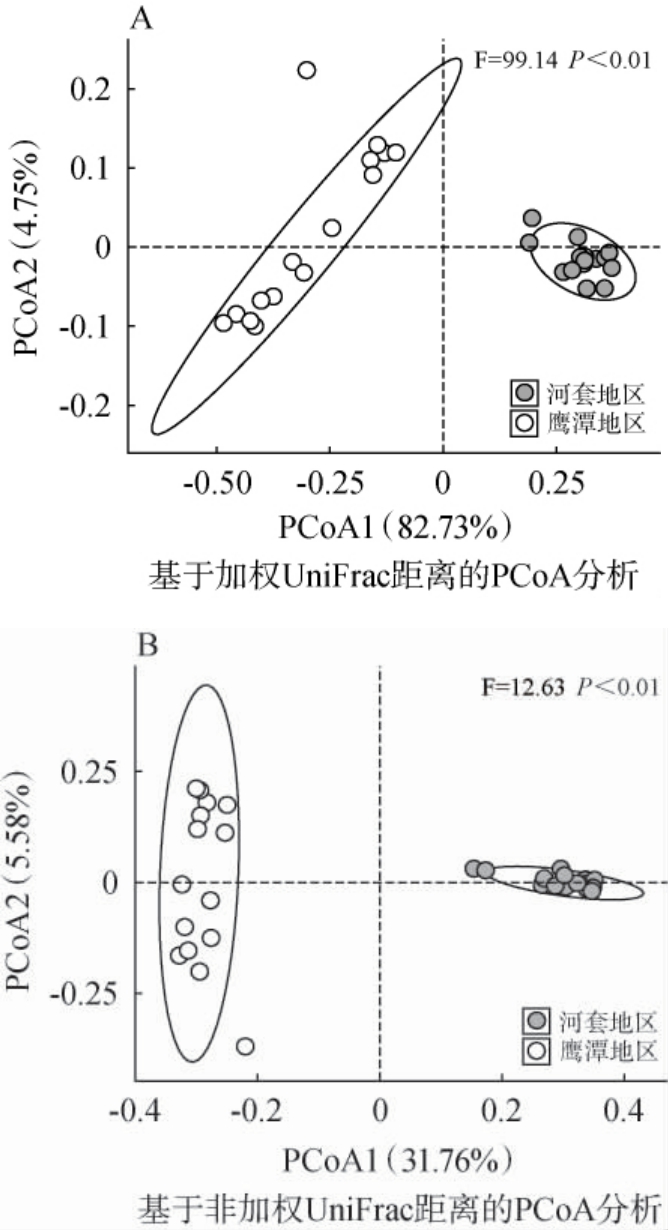
图2 两地区中高温大曲细菌菌群Beta多样性比较分析
Fig.2 Comparative analysis of the Beta diversity of bacterial flora in medium-high-temperature Daqu in the two regions
由图2A可知,在同时考虑细菌物种多样性和丰富度的条件下,PCoA1、PCoA2方差贡献率分别为82.73%、4.75%,累计方差贡献率为87.48%,由此表明这两个主成分可解释原始数据中绝大部分的变异信息。其中,河套和鹰潭地区中高温大曲样品分别主要集中于X轴正半轴和X轴负半轴,2个地区中高温大曲样品出现完全分离的趋势,经PERMANOVA检验可知,2个地区中高温大曲样品细菌菌群差异高度显著(P<0.001)。由图2B可知,在仅考虑细菌物种丰富度的条件下,PCoA1、PCoA2方差贡献率分别为31.76%、5.58%,累计方差贡献率为37.34%,由此表明这两个主成分可解释原始数据中绝大部分的变异信息。2个地区中高温大曲样品亦出现完全分离的趋势,且2个地区中高温大曲样品细菌菌群差异高度显著(P<0.001)。 由此可知,2个地区中高温大曲细菌类群存在明显差异。
2.2 河套及鹰潭地区中高温大曲细菌类群结构分析
基于上述细菌类群多样性的分析结果,进一步在门、属水平对两地区中高温大曲细菌类群结构进行分析,结果见图3。

图3 基于门(A)、属(B)水平两地区中高温大曲细菌菌群结构分析
Fig.3 Analysis of bacterial flora structure in medium-hightemperature Daqu in the two regions based on phylum(A) and genus (B) level
Other:将相对丰度<1.00%的细菌门(属)归为Other。
由图3A可知,河套、鹰潭地区中高温大曲样品中共检出厚壁菌门(Firmicutes)、放线菌门(Actinobacteria)、变形菌门(Proteobacteria)和拟杆菌门(Bacteroidetes)4个优势细菌门(相对丰度>1.0%)。其中,河套地区中高温大曲样品中检出优势细菌门为2个,为Firmicutes和Actinobacteria;而鹰潭地区中高温大曲样品中优势细菌门为4个,为Firmicutes、Actinobacteria、Proteobacteria和Bacteroidetes。经Mann-Whitney检验分析发现,河套地区中高温大曲中Actinobacteria的平均相对丰度(45.52%)极显著高于鹰潭地区(3.40%)(P<0.01),Proteobacteria和Bacteroidetes的平均相对丰度(分别为0.57%和0.86%)均极显著低于鹰潭地区(分别为41.07%和2.42%)(P<0.01)。导致两地区中高温大曲细菌菌群差异的原因可能是由于环境条件、制曲工艺及原料特性导致的,河套地区干旱低湿的气候适合Actinobacteria的生长[19],而鹰潭地区高湿环境则更利于Proteobacteria的增殖[20]。 由此可知,虽然2个地区中高温大曲细菌类群在门水平上结构组成相似,但其丰度存在较大差异。
由图3B可知,河套、鹰潭地区中高温大曲样品中共检出糖多孢菌属(Saccharopolyspora)、葡萄球菌属(Staphylococcus)、芽孢杆菌属(Bacillus)、魏斯氏菌属(Weissella)、高温放线菌属(Thermoactinomyces)、水杆状菌属(Aquabacterium)、不动杆菌属(Acinetobacter)、泥单胞菌属(Pelomonas)、劳尔氏菌属(Ralstonia)、克罗彭斯特菌属(Kroppenstedtia)和鞘脂单胞菌属(Sphingomonas)11个优势细菌属。 其中,河套地区中高温大曲样品中检出优势细菌属7个,包括Saccharopolyspora、Saccharopolyspora、Thermoactinomyces、Weissella、Bacillus、片 球 菌 属(Pediococcus)和 黏 液 乳 杆 菌 属(Limosilactobacillus);而鹰潭地区中高温大曲样品中优势细菌属10个,包括Bacillus、Aquabacterium、Acinetobacter、Weissella、Pelomonas、Ralstonia、Kroppenstedtia、Sphingomonas、副伯克霍尔德氏菌属(Paraburkholderia)和Staphylococcus。 经Mann-Whitney检验分析发现,河套地区中高温大曲中Saccharopolyspora、Staphylococcus和Thermoactinomyces的平均相对丰度(分别为44.63%、29.45%和9.63%)均极显著高于鹰潭地区(分别为0.75%、1.99%和0.72%)(P<0.01),Bacillus、Aquabacterium、Acinetobacter、Pelomonas、Ralstonia、Kroppenstedtia和Sphingomonas的平均相对丰度(分别为1.26%、0.000 4%、0.05%、0.000 2%、0.000 5%、0.04%和0.004%)均极显著低于鹰潭地区(分别为29.94%、9.57%、8.24%、6.58%、3.06%、3.00%和2.64%)(P<0.01)。除此之外,Pediococcus和Limosilactobacillus在鹰潭地区大曲中的平均相对丰度仅为0.41%和0.19%,而其作为优势细菌属在河套地区中平均相对丰度均为1.16%;Paraburkholderia虽为鹰潭地区大曲中的优势细菌属,平均相对丰度为2.00%,但其在河套地区大曲中并未检测到。由此可知,在属水平上,2个地区中高温大曲的细菌类群在结构组成和丰度方面亦均呈现出较大的差异,这也进一步验证了2.1部分中2个地区中高温大曲基于UniFrac距离细菌类群β多样性的分析结果。其原因可能与大曲制作时所处的区域性环境因素有关,有研究指出,地面和空气环境是大曲微生物在储存和发酵过程中必不可少的来源,不仅提供了谷物发酵赖以启动与持续的微生物菌群,还赋予了酿造大曲鲜明的区域特异性特征[21]。
Saccharopolyspora、Staphylococcus、Bacillus和Thermoactinomyces等菌属为中高温大曲中普遍存在的细菌菌群,其参与发酵等关键环节,在对白酒风味物质的形成和发酵效率的维持等方面均发挥着不可或缺的作用。 如Saccharopolyspora在生长代谢过程中经一系列复杂且精妙的生物化学反应后可生成酯类化合物,酯类是白酒风味物质的核心,其独特的化学结构和挥发性赋予了白酒丰富香气与醇厚口感,极大提升了白酒的风味品质[22]。毛凤娇等[23]对白酒窖泥中微生物群落与挥发性代谢物的相关性分析亦发现,Saccharopolyspora与乙酸乙酯、己酸乙酯和乳酸乙酯等酯类化合物的生成存在显著正相关关系,即该菌属在代谢活动中不仅推动这些酯类物质的合成,酯类化合物的存在也为Saccharopolyspora的生长繁殖营造适宜的微环境,二者相辅相成、相互促进。在白酒酿造所涉及的微生物代谢过程中,Staphylococcus不仅能够高效分泌淀粉酶、酯酶和纤维素酶等多种关键酶类,还具备产生吡嗪类物质及其他风味物质的能力[24],这些酶类在原料糖化和酯化反应等酿造关键环节中扮演着不可或缺的角色,而所产生的风味物质则直接参与白酒风味轮廓的构建,对白酒独特风味品质的形成起到了积极的促进作用。 Bacillus能够在较高温度下高效代谢与快速繁殖,具有丰富且多样化的酶系和生成多种风味代谢物的能力[25]。Thermoactinomyces具有典型的嗜热特性,在高温环境下代谢活跃,不仅能够分泌蛋白酶、纤维素酶、细胞溶解酶和嗜热淀粉酶等多种酶类以助力物质的转化,还可以生成挥发性风味化合物以赋予发酵产物独特的风味[26]。
2.3 河套及鹰潭地区中高温大曲样品细菌类群差异分析
为进一步明确2个地区中高温大曲中的差异性物种,采用LEfSe分析对2个地区中高温大曲样品中的生物标志物进行了高效识别[27],结果见图4。

图4 基于线性判别分析值的2个地区中高温大曲差异物种分析
Fig.4 Analysis of differential species of medium-high-temperature Daqu in two regions based on linear discriminant analysis value
由图4可知,当LDA值>4.0时,葡萄球菌科(Staphylococcaceae)、Staphylococcus、未分类的放线杆菌纲(unclassified_Actinobacteria)、放线杆菌纲(Actinobacteria)、Saccharopolyspora、假诺卡氏菌科(Pseudonocardiaceae)和假诺卡氏菌目(Pseudonocardiales)等7个差异物种在河套地区的中高温大曲中显著富集(P<0.05),Proteobacteria、芽孢杆菌科(Bacillaceae)、Bacillus、贝塔变形菌纲(Betaproteobacteria)、丛毛单胞菌科(Comamonadaceae)、伯克霍尔德氏菌目(Burkholderiales)、伽玛变形菌纲(Gammaproteobacteria)和Aquabacterium等8个差异物种在鹰潭地区中高温大曲中显著富集(P<0.05)。其中,在属水平上的差异物种有4个,分别为Staphylococcus、Saccharopolyspora、Bacillus和Aquabacterium,由于LDA值越大表明物种的富集程度越高[28],因此,Bacillus可作为河套地区中高温大曲的潜在生物标志物,而Saccharopolyspora可作为鹰潭地区中高温大曲的潜在生物标志物。有研究指出,Saccharopolyspora隶属于Actinomycetia,具有较高的耐受性,在白酒发酵酿造的复杂过程中,其可高效合成一系列酶与因子,这些物质能够有力地促进纤维素降解,并进一步深度参与到白酒原料中大分子物质的代谢分解,为白酒风味的塑造和品质的提升发挥着不可或缺的积极作用[29]。Bacillus隶属于Firmicutes,在诸如高温和高渗透压等相对极端的条件下可表现出较强的环境适应性,是白酒发酵过程中的关键功能细菌菌群之一,其分泌的淀粉酶和蛋白酶等水解酶类可将淀粉和蛋白质等大分子物质高效转化为葡萄糖和氨基酸,同时还会产生各类风味前体物质以及与之相关的化合物,对白酒风味的形成意义重大[30]。由此可见,Bacillus和Saccharopolyspora为造成河套和鹰潭地区中高温大曲中细菌类群结构差异的主要菌群,且两者均为后续酿造过程中白酒风味品质的形成发挥着重要作用。
2.4 河套及鹰潭地区中高温大曲发酵菌群功能分析
从2个地区中高温大曲样品所有细菌序列中共注释到4 189 个COGs,对其进行PICRUSt功能预测,结果见图5。由图5可知,其主要归属于23个一级功能层,可划分为代谢、信息存储和加工以及细胞过程和信号传导这三类,其中代谢包括能量生成和转换、碳水化合物运输与代谢、氨基酸转运与代谢、核苷酸转运与代谢、辅酶转运与代谢、脂质转运与代谢、无机离子运输和代谢、次生代谢物生物的合成转运和分解代谢;信息存储和加工包括翻译,核糖体结构与生物发生、核糖核酸(ribonucleic acid,RNA)的加工与修饰、转录、复制、重组与修复、染色质结构与动力学;信号传导包括细胞周期控制,细胞分裂,染色体分割、防御机制、信号转导机制、细胞壁/膜/包膜生物发生、细胞骨架、细胞运动、细胞内运输,分泌和囊泡运输、翻译后修饰,蛋白质周转,伴侣、一般功能预测。除细胞骨架、染色质结构与动力学和RNA的加工与修饰这3个基因功能表达量相对较低外,其余20个基因功能表达量均相对较高,且未知功能和一般功能预测的表达量最高。由图5亦可知,经Mann-Whitney检验分析发现,上述23个一级基因功能在河套地区中高温大曲中的表达量均极显著低于鹰潭地区大曲(P<0.01)。因此,2个地区中高温大曲中细菌基因功能亦存在较大差异,且相较于鹰潭地区中高温大曲,河套地区大曲中存在较弱的微生物代谢、信息存储和加工以及细胞过程和信号传导功能。
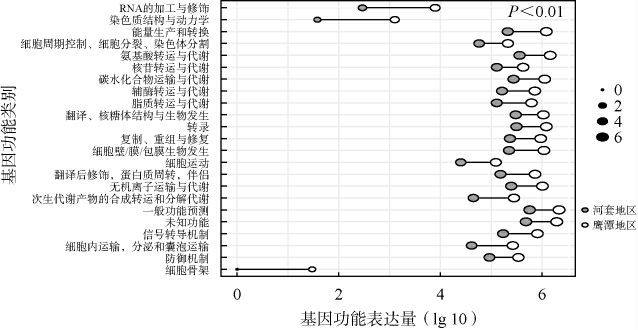
图5 两地区中高温大曲细菌菌群PICRUSt功能预测
Fig.5 PICRUSt function prediction of bacterial flora in medium-hightemperature Daqu in the two regions
3 结论
本研究通过Illumina MiSeq高通量测序技术对河套地区中高温大曲的细菌类群结构进行解析,与江西鹰潭地区中高温大曲的细菌菌群进行Alpha、Beta多样性比较分析,结果表明,河套地区大曲的细菌物种丰富度和多样性均极显著低于鹰潭地区(P<0.01),糖多孢菌属(Saccharopolyspora)、葡萄球菌属(Staphylococcus)和高温放线菌属(Thermoactinomyces)等优势细菌属(相对丰度>1.0%)相对丰度极显著高于鹰潭地区(P<0.01),而芽孢杆菌属(Bacillus)、水杆状菌属(Aquabacterium)和不动杆菌属(Acinetobacter)等极显著低于鹰潭地区(P<0.01),且Bacillus和Saccharopolyspora为造成2个地区中高温大曲中细菌类群结构差异的主要菌群,此外,河套地区中高温大曲的细菌类群在微生物代谢、信息存储和加工以及细胞过程和信号传导功能上表达相对较弱。
[1]WANG H Y, XU Y.Effect of temperature on microbial composition of starter culture for Chinese light aroma style liquor fermentation[J].Lett Appl Microbiol,2015,60(1):85-91.
[2]DU H, WANG X S, ZHANG Y H, et al.Exploring the impacts of raw materials and environments on the microbiota in Chinese Daqu starter[J].Int J Food Microbiol,2019,297(5):32-40.
[3]LIU P H, ZHANG L H, DU X W, et al.Dynamic analysis of physicochemical and biochemical indices and microbial communities of lightflavor Daqu during storage[J].J Am Soc Brew Chem,2019,77(4):287-294.
[4]ZHU M,ZHENG J,XIE J,et al.Effects of environmental factors on the microbial community changes during medium-high temperature Daqu manufacturing[J].Food Res Int,2022,153(3):110955.
[5]XIE M,LV F X,MA G X,et al.High throughput sequencing of the bacterial composition and dynamic succession in Daqu for Chinese sesame flavour liquor[J].J I Brewing,2019,126(1):98-104.
[6]杨勇,葛向阳,张龙云,等.基于高通量测序技术解析中高温制曲细菌群落的演替规律[J].酿酒科技,2022(8):34-41.
[7]LIU Y B,LI X,LI H D,et al.Taorong-type Baijiu starter:analysis of fungal community and metabolic characteristics of middle-temperature Daqu and high-temperature Daqu[J].Plos One,2022,17(10):e0274881.
[8]马梦月,郭壮,李学思,等.临沂和周口地区中高温大曲细菌群落结构与基因功能差异性研究[J].食品工业科技,2024,45(1):155-161.
[9]周书楠,席修璞,董蕴,等.琚湾酸浆面浆水细菌多样性评价[J].中国酿造,2018,37(1):49-53.
[10]CHEN L,LI Y Z,JIN L,et al.Analyzing bacterial community in pit mud of Yibin Baijiu in China using high throughput sequencing[J].Peer J,2020,8(5):e9122.
[11]符漫,姜晨阳,田龙新,等.特香型白酒中高温和高温大曲细菌类群比较分析[J].中国酿造,2023,42(5):151-156.
[12]CAI W C,WANG Y R, NI H, et al.Diversity of microbiota, microbial functions, and flavor in different types of low-temperature Daqu[J].Food Res Int,2021,150(9):110734.
[13]HU X L,WANG K L,CHEN M E,et al.Profiling the composition and metabolic activities of microbial community in fermented grain for the Chinese strong-flavor Baijiu production by using the metatranscriptome,high-throughput 16S rRNA and ITS gene sequencings[J].Food Res Int,2020,138(12):109765.
[14]POLLOCK J, GLENDINNING L, WISEDCHANWET T, et al.The madness of microbiome: attempting to find consensus "best practice"for 16S microbiome studies[J].Appl Environ Microbiol,2018,84(7):e02627-17.
[15]EDGAR R C.Search and clustering orders of magnitude faster than BLAST[J].Bioinformatics,2010,26(19):2460-2461.
[16]COLE J R,WANG Q,FISH J A,et al.Ribosomal Database Project:data and tools for high throughput rRNA analysis[J].Nucleic Acids Res,2014,42(D1):D633-D642.
[17]CHEN Y,TIAN W,SHAO Y, et al.Miscanthus cultivation shapes rhizosphere microbial community structure and function as assessed by Illumina MiSeq sequencing combined with PICRUSt and FUNGUIld analyses[J].Arch Microbiol,2020,202(5):1157-1171.
[18] LI Z X,ZHOU J,LIANG H,et al.Differences in alpha diversity of gut microbiota in neurological diseases[J].Front Neurosci, 2022, 16(6):879318.
[19]YANDIGERI M S,MEENA K K,SINGH D,et al.Drought-tolerant endophytic actinobacteria promote growth of wheat (Triticum aestivum)under water stress conditions[J].Plant Growth Regul, 2012, 68(3):411-420.
[20]ALEKHINA L K, DOBROVOL'SKAIA T G, POCHATKOVA T N, et al.Bacterial diversity in microcosms of soils with various humidity[J].Mikrobiologiia,2001,70(6):847-854.
[21]FAN G S,SUN B G,FU Z L,et al.Analysis of physicochemical indices,volatile flavor components, and microbial community of a light-flavor Daqu[J].J Am Soc Brew Chem,2018,76(3):209-218.
[22]ZHANG Y D, SHEN Y, CHENG W, et al.Understanding the shifts of microbial community and metabolite profile from wheat to mature Daqu[J].Front Microbiol,2021,12:714726.
[23]毛凤娇,黄均,周荣清,等.人工窖泥微生物群落对浓香型白酒发酵过程风味代谢物形成的影响[J].食品科学,2024,45(4):125-134.
[24]王玉荣,侯强川,田龙新,等.基于纯培养和超高深宏基因组测序技术分析茅台镇两企业高温大曲微生物多样性差异[J].食品科学,2024,45(4):108-115.
[25]JIN Y,LI D Y,AI M,et al.Correlation between volatile profiles and microbial communities: a metabonomic approach to study Jiang-flavor liquor Daqu[J].Food Res Int,2019,121:422-432.
[26]ZHU Q,CHEN L Q,PENG Z,et al.Analysis of environmental driving factors on core functional community during Daqu fermentation[J].Food Res Int,2022,157:111286.
[27]WANG Y R,HOU Q C,GUO Z,et al.Bacterial community structure in acidic gruel from different regions and its influence on quality[J].Food Res Int,2021,141:110130.
[28]张振东,王玉荣,侯强川,等.市售茨河花色腐乳和红方腐乳微生物菌群及风味物质的比较分析[J].食品与发酵工业,2022,48(13):70-77.
[29]LI H,LIAN B,DING Y H,et al.Bacterial diversity in the central black component of Maotai Daqu and its flavor analysis[J].Ann Microbiol,2014,64:1659-1669.
[30]DENG L,MAO X,LIU D,et al.Comparative analysis of physicochemical properties and microbial composition in high-temperature Daqu with different colors[J].Front Microbiol,2020,11(11):588117.