大曲作为中国传统固态发酵工艺的核心糖化发酵剂,在白酒酿造过程中具有重要地位[1]。其中,中高温大曲作为浓香型白酒生产的重要载体,其质量直接决定白酒的风格与品质;然而受原料、工艺、评价维度等因素影响,中高温大曲存在明显质量差异,其微生物群落结构、理化指标及风味也存在明显差异,这种差异不仅影响白酒生产稳定性,更制约了风味表达。因此,解析不同等级大曲的微生物组成与功能差异成为优化大曲生产工艺、提升白酒品质的关键。
通常微生物群落研究主要依赖平板分离与扩增子测序技术,但受限于培养条件与基因组覆盖度,难以全面解析微生物群落的功能潜力。 近年来宏基因组学、代谢组学与高通量测序技术(high throughput sequencing,HTS)的广泛应用,为揭示大曲微生物群落解析提供了新工具,科研人员已经能够从微观层面解读大曲微生物群落的多样性与功能,如罗建超等[2]筛选得到25株有较好的产酱香能力的芽孢杆菌(Bacillus),发现它们代谢产生的多种酶类可将甘油转化为二羟丙酮,还可分解多种糖类,生成多种酸类物质,从而推测芽孢杆菌产香的可能机制。向港兴等[3]的研究表明,不同等级中高温大曲虽然共享一套核心微生物种群,但在具体菌属的相对丰度和特定指示菌株方面存在显著差异,优级曲中克罗彭斯特菌属(Kroppenstedtia)的相对丰度显著高于一级大曲,克罗彭斯特菌属被认为在高温环境下能够保持代谢活性,可能与大曲风味物质的形成有关。 冯哲瀚等[4]研究发现,乳酸杆菌属(Lactobacillus)、葡萄球菌属(Staphylococcus)与发酵力和pH值呈正相关,而高温放线菌属(Thermoactinomyces)则与pH值呈负相关,这些复杂的关系网络说明了微生物群落结构对大曲理化特性具有重要调控作用。 此外,林涵瑞等[5]揭示了不同地域大曲的核心微生物群落结构存在明显差异;孔祥聪等[6]研究发现,中高温大曲以高温放线菌属(Thermoactinomyces)、Bacillus和不动杆菌属(Acinetobacter)为主要优势细菌属;施思等[7]研究发现,根霉属(Rhizopus)和毕赤酵母属(Pichia)是浓香型大曲中的主要优势真菌属;沈世明等[8]研究发现,高温大曲中与酸类物质呈正相关的微生物是芽孢杆菌属和毕赤酵母属;胡晓龙等[9]研究表明,河南地区中温大曲的曲皮真菌多样性较高,曲心细菌相对丰度高于曲皮;张春英等[10]研究发现,在浓香型中高温大曲的制作过程中以放线菌门(Actinobacteria)为主,且细菌群落会随发酵过程产生动态变化;王芙蓉等[11]从高温大曲中分离出了高温放线菌属的菌株,经过全基因组测序发现该菌株能够代谢产生四甲基吡嗪。 上述研究虽然展示了不同地域、不同香型大曲功能微生物与特定指标之间的直接关联,但缺乏对微生物间复杂互作机制的系统解析且研究方法标准化仍然存在缺陷,未来需在整合多组学技术的基础上加强对功能微生物的验证,同时深入挖掘工艺参数与微生物群落的关联机制,推动大曲生产从经验控制向科学设计转变。
本研究采用常规检测方法、气相色谱-质谱联用(gas chromatography-mass spectrography,GC-MS)技术及高通量测序技术分别对不同等级中高温大曲的理化指标、挥发性风味成分及微生物群落多样性进行检测分析,并结合冗余分析(redundancy analysis,RDA)与斯皮尔曼(Spearman)相关性分析,系统解析微生物群落与理化指标、挥发性风味组分的相互关系,为指导功能菌株定向选育及生产工艺优化提供了数据支撑与理论依据。
1 材料与方法
1.1 材料与试剂
1.1.1 不同等级中高温大曲样品
特级曲(31块)、优级曲(34块)、普级曲(30块)(参照文献[3,12]的方法进行等级区分):四川省古蔺郎酒厂(泸州)有限公司。随机粉碎5块大曲混合均匀并装入无菌密封袋,放入-80 ℃冰箱保存。
1.1.2 试剂
二氯甲烷(分析纯):无锡市晶科化工有限公司;无水硫酸钠(分析纯):济南箫试化工有限公司;氯化钠(分析纯):广州化学制剂厂;叔戊醇、乙酸正戊酯、2-乙基丁酸(均为色谱纯且纯度均≥99.5%):上海阿拉丁生化科技股份有限公司;Qubit3.0脱氧核糖核酸(deoxyribonucleic acid,DNA)提取试剂盒:上海凌仪生物科技有限公司;Quant-iT PicoGreen dsDNA Assay Kit荧光定量染料:美国英杰生命技术有限公司;其他试剂均为国产分析纯。
1.2 仪器与设备
7890B-5977B气相色谱-质谱联用仪、DB-WAX毛细管色谱柱(60 m×0.25 mm×0.25 μm)、三相萃取头(50/30 μm DVB/CAR/PDMS):美国安捷伦科技公司;N-Evap24位氮吹仪:上海思伯明仪器设备有限公司;DZKW-4型电子恒温水浴锅:南北科仪(北京)科技有限公司;BL2200H分析天平:岛津国际贸易(上海)有限公司;PTC-200聚合酶链式反应(polymerase chain reaction,PCR)仪:美国Bio-Rad公司;FLX800T酶标仪:美国伯腾仪器公司;DYY-6C电泳仪:北京六一生物科技有限公司;Oxford Nanopore PromethION测序仪:天津诺禾致源科技有限公司;WF型万能粉碎机:意德机器技术(安丘)股份有限公司。
1.3 方法
1.3.1 大曲理化指标的检测
根据QB/T 4257—2011《酿酒大曲通用分析方法》[13]检测大曲的水分、酸度、液化力、糖化力、酯化力、发酵力。
1.3.2 大曲微生物群落结构检测
采用Qubit3.0 DNA提取试剂盒提取大曲样品微生物的宏基因组DNA,以其为模板进行PCR扩增,细菌16S rRNA基因序列PCR扩增采用引物27F(5'-AGAGGTTTGATCMTGGCTCAG-3')和引物1492R(5'-ACCTTGTTACGACTT-3'),真菌ITS基因序列PCR扩增采用引物ITS1F(5'-CTTGGTCATTTAGAGGAAGTAA-3')和LR3(5'-CCGTGTTTCAAGACGGG-3')。PCR扩增体系:Phusion⑥High-Fidelity PCR Master Mix 15 μL、脱氧核糖核苷三磷酸(deoxyribonucleoside triphosphates,dNTPs)(2.5 mmol/L) 2 μL、上下游引物(10 μmol/L)各1 μL、DNA模板2 μL、双蒸水(ddH2O)8.75 μL、Q5 DNA聚合酶0.25 μL。PCR扩增条件:98 ℃预变性1 min;98 ℃变性10 s,50 ℃退火30 s,72 ℃延伸30 s,共30次循环;72 ℃再延伸5 min。使用2%琼脂糖凝胶电泳对PCR扩增产物进行检测,在天津诺禾致源科技有限公司的Oxford Nanopore PromethION平台上进行高通量测序。使用FLASH(Version 1.2.11)、fastp(Version 0.23.1)对序列进行质量过滤、去噪、拼接和嵌合体去除等处理,获得的有效序列,采用Uparse算法(Uparse v7.0.1001)以97%的相似度将序列聚类成为操作分类单元(operational taxonomic units,OTUs),最终与数据库进行物种注释,细菌采用SILVA 138.1数据库(http://www.arb-silva.de/),真菌采用Unite v9.0数据库(https://unite.ut.ee/)。
1.3.3 大曲挥发性风味物质的检测
前处理:称量10 g大曲,加饱和氯化钠溶液30 mL浸提1 h,然后以4 000 r/min离心5 min,保留上清液,倒入500 mL分液漏斗,加50 mL二氯甲烷振荡提取5 min。收集有机相,重复3次合并有机相;有机相中加入5 g无水硫酸钠烘干、浓缩为1 mL,加入10 μL混合内标物质(叔戊醇、乙酸正戊酯、2-乙基丁酸质量浓度均为1 g/100 mL)上机分析。
GC条件:DB-WAX毛细管色谱柱(60 m×0.25 mm×0.25 μm),载气为高纯氦气(He),进样口温度250 ℃,载气流速1 mL/min,进样量1 μL,分流比10∶1。 升温程序为初始温度35 ℃保持5 min,以3 ℃/min升至90 ℃保持1 min,随后以3 ℃/min升至150 ℃保持1 min,再以5 ℃/min升至190 ℃保持1 min,10 ℃/min升至220 ℃保持8 min。
MS条件:电子电离(electron ionization,EI)源,电离能量70 eV,离子源温度230 ℃,四极杆温度150 ℃,单离子监测(single ion monitoring,SIM)模式,质量扫描范围设定为20~300 m/z。
定性定量方法:结合美国国家标准技术研究所(National Institute of Standards and Technology,NIST)20谱库检索对大曲中各挥发性风味物质进行定性;采用内标法定量曲样中各挥发性风味物质的含量,所有曲样重复测定3次。
气味活性值(odor activityvalue,OAV)计算:参考张晓婕等[14]的方法计算各挥发性风味物质OAV,其计算公式如下:
式中:c为各挥发性风味物质的质量浓度,mg/100 mL;OT为各挥发性风味物质的阈值,μg/L。
1.3.4 数据处理
每个实验重复3次,采用SPSS20.0软件进行数据处理,采用SIMCA14.0软件进行正交偏最小二乘判别分析(orthogonalpartialleastsquares-discriminantanalysis,OPLS-DA),并计算变量重要性投影(variable importance in the projection,VIP)值,借助联川生物云平台(https://www.omicstudio.cn.)、Cnsknowall网站(https://cnsknowall.com/)绘图。
2 结果与分析
2.1 不同等级中高温大曲理化指标分析
评价大曲优劣的重要参考依据是大曲理化指标,它既是酶作用的反映,又是微生物生长状态的体现[15]。 不同等级中高温大曲的理化指标测定结果见表1。 由表1可知,不同等级中高温大曲的理化指标存在一定差异,其中,特级曲的糖化力(865.10 U)、酯化力(617.61 U)、发酵力(0.27 U)和液化力(1.78 U)最高,可能与芽孢杆菌属和霉菌的生长代谢有关[16],优级曲的水分含量较高,普级曲的酸度较高,各等级大曲理化指标的差异可能源于培菌过程中制曲温度和发酵条件等微生物生长环境的不同。
表1 不同等级中高温大曲的理化指标测定结果
Table 1 Determination results of physicochemical indicators of medium-high temperature Daqu with different grades
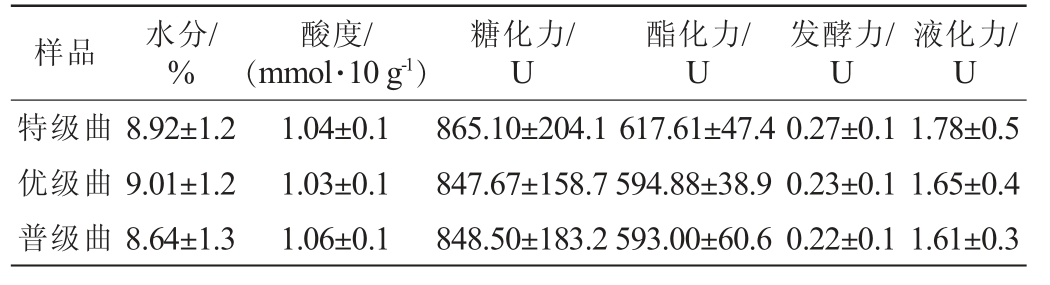
样品 水分/%酸度/(mmol·10 g-1)糖化力/U酯化力/U发酵力/U液化力/U特级曲优级曲普级曲8.92±1.2 9.01±1.2 8.64±1.3 1.04±0.1 1.03±0.1 1.06±0.1 865.10±204.1 847.67±158.7 848.50±183.2 617.61±47.4 594.88±38.9 593.00±60.6 0.27±0.1 0.23±0.1 0.22±0.1 1.78±0.5 1.65±0.4 1.61±0.3
2.2 不同等级中高温大曲微生物群落分析
2.2.1 Alpha多样性分析
Chao1指数值越高,表明群落丰富度越高;Shannon指数值越高,表明群落多样性越高;覆盖率接近1.0,表示测序结果能真实反映样品微生物群落结构[17]。不同等级中高温大曲微生物群落Alpha多样性分析结果见表2。由表2可知,所有样品微生物群落的覆盖率均为1.0,说明本研究测序结果能真实反映大曲样品中微生物的群落信息。在细菌群落方面,优级曲的Chao1指数与Shannon指数值均最高,表明其细菌群落最丰富,多样性最高;而特级曲的Shannon指数值最低,表明其菌群结构虽具一定规模但多样性较低,可能是由于发酵过程中或翻曲后曲堆不同位置存在温度、湿度差导致群落多样性水平降低[18-19];普级曲的Chao1指数值最低,表明其菌群结构最为单一,这可能与制曲条件有关[20]。在真菌群落方面,Shannon指数值表现为特级曲>普级曲>优级曲,而Chao1指数值则为普级曲>特级曲>优级曲。 这一差异反映了不同等级中高温大曲的生态特征:特级曲通过特定的发酵微环境筛选了物种间相互作用强的核心功能群落;优级曲的微环境可能对少数菌属存在定向选择,使其形成单一群落抑制了其他真菌生长,从而表现为丰富度和多样性最低;普级曲真菌群落的丰度和多样性较高,由于3种大曲所处环境的不同及发酵过程中温湿度等环境参数的调控和驯化,可能是造成其丰度和多样性差异的原因,这种微生物菌落差异为理解大曲品质差异提供了微生物学依据[21]。
表2 不同等级中高温大曲微生物群落Alpha多样性分析结果
Table 2 Alpha diversity analysis results of microbial communities in medium-high temperature Daqu with different grades
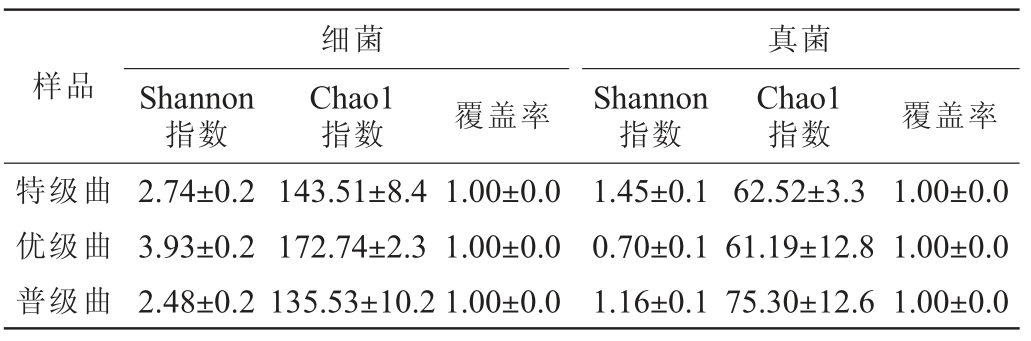
样品Shannon指数细菌Chao1指数覆盖率Shannon指数真菌Chao1指数 覆盖率特级曲优级曲普级曲2.74±0.2 3.93±0.2 2.48±0.2 143.51±8.4 172.74±2.3 135.53±10.2 1.00±0.0 1.00±0.0 1.00±0.0 1.45±0.1 0.70±0.1 1.16±0.1 62.52±3.3 61.19±12.8 75.30±12.6 1.00±0.0 1.00±0.0 1.00±0.0
2.2.2 优势微生物分析
基于属水平不同等级中高温大曲样品中的微生物群落结构见图1,将不同等级中高温大曲样品中平均相对丰度均>1%的微生物属定义为优势菌属。由图1A可知,从不同等级中高温大曲样品中共注释到6个优势细菌属,包括泛菌属(Pantoea)(39.88%)、芽孢杆菌属(Bacillus)(28.56%)、高温放线菌属(Thermoactinomyces)(2.87%)、克罗诺杆菌属(Cronobacter)(2.77%)、魏斯氏菌属(Weissella)(1.63%)、葡萄球菌属(Staphylococcus)(1.45%)。 此外,从不同等级中高温大曲样品中还注释到明串珠菌属(Leuconostoc)(0.63%)、克罗彭斯特菌属(Kroppenstedtia)(0.50%)、不动杆菌属(Acinetobacter)(0.10%)等。其中泛菌属和克罗诺杆菌属在特级曲中相对丰度最高,分别为64.97%、4.07%。 泛菌属是兼性厌氧菌,主要代谢产物为有机酸[22],向港兴等[3]研究发现,优级曲与普级曲中泛菌属的相对丰度仅为2%~3%,也有研究表明该菌属主要在发酵初期大量存在[18],其在特级曲中的高相对丰度可能反映了高温环境对非耐热菌的筛选作用[23],而在普级曲中的低相对丰度则可能与工艺波动及竞争失衡有关[24]。克罗诺杆菌属明显富集于特级曲中,可作为特级曲特有工艺条件下的关键指示菌种,在生态功能中扮演重要角色。高温放线菌属和魏斯氏菌属在优级曲中的相对丰度最高,分别为5.52%、3.73%,何猛超等[25]研究也发现这3种菌属在优级曲中相对丰度最高,与本研究结果一致。 高温放线菌属主要负责大分子物质降解,为风味形成提供前体物质,还可能参与丁酸代谢[26];魏斯氏菌属则主要贡献有机酸与酯类物质,其分泌的β-葡萄糖苷酶对纤维素降解有潜在贡献[27]。普级曲中芽孢杆菌属(73.26%)和葡萄球菌属(1.85%)的相对丰度最高,而芽孢杆菌属在特级曲、优级曲中相对丰度较低的原因可能与培菌过程的温湿度控制有关;此外,芽孢杆菌属所分泌的耐热酶系是糖化力和发酵力的核心驱动力[10],与酯类、吡嗪类等白酒中重要风味物质的生成有关[28-29],这可能是导致特级曲糖化力、发酵力处于较高水平的原因。葡萄球菌属在普级曲中的高相对丰度,说明其在普级曲的工艺条件下形成了竞争优势,该菌属与普级曲酸度偏高、菌群结构单一存在关联性。明串珠菌属、克罗彭斯特菌属、不动杆菌属虽然在大曲中作为低丰度菌群被检出,但它们共同丰富了微生态结构,是功能菌群的重要组成部分,在制曲生产中发挥的实际作用值得进一步研究。
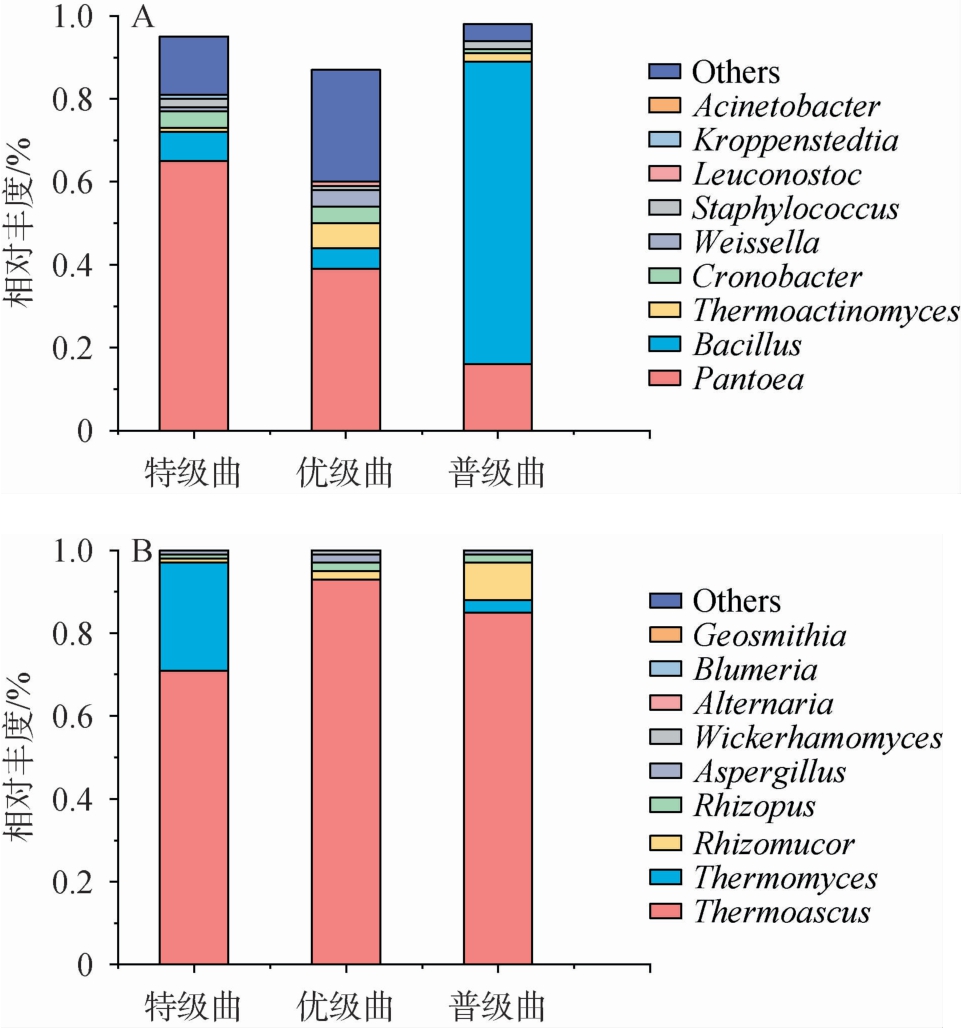
图1 基于属水平不同等级中高温大曲细菌(A)及真菌(B)群落结构
Fig.1 Structure of bacteria (A) and fungi (B) community in medium-high temperature Daqu with different grades based on the genus level
Others代表平均相对丰度排名9之后的其他菌属。
由图1B可知,从不同等级中高温大曲样品中共注释到5个优势真菌属,包括嗜热子囊菌属(Thermoascus)(83.03%)、嗜热真菌属(Thermomyces)(9.61%)、毛霉属(Rhizomucor)(4.06%)、根霉属(Rhizopus)(1.53%)、曲霉属(Aspergillus)(1.12%)。此外,从不同等级中高温大曲样品中还注释到威克汉姆酵母属(Wickerhamomyces)(0.31%)、链格孢属(Alternaria)(0.04%)、Geosmithia(0.03%)、布氏白粉菌属(Blumeria)(0.01%)等。3个等级中高温大曲中均以嗜热子囊菌属的相对丰度最高,为第一优势真菌属,在特级曲、优级曲和普级曲中的相对丰度分别为70.70%、93.45%、84.84%;嗜热真菌属为第二大优势真菌属,在特级曲、优级曲和普级曲中的相对丰度分别为26.30%、1.82%、2.50%;嗜热真菌属和嗜热子囊菌属是典型的耐高温大曲微生物,它们能代谢较高分解能力的酶类,降解原料中的大分子物质,对白酒微生物生长繁殖和香型前体物质产生正向作用,在大曲发酵过程中的四个阶段中逐渐积累成为优势真菌[30-31]。 毛霉属和根霉属在普级曲中的相对丰度最高,分别为8.85%、1.98%,这两种真菌均为好湿好氧真菌,多产生于局部水分高、通风排潮不及时的大曲,若过度繁殖不仅会抑制曲霉等核心功能菌生长,更会影响大曲风味[32-33]。曲霉属在优级曲中相对丰度最高(1.55%),明显高于特级曲(0.50%)和普级曲(1.31%),曲霉属可推动原料糖化降解进程,在表征大曲品质上起到一定作用[34-36]。综上所述,各等级中高温大曲的菌群落结构的差异性可能是由发酵过程中的温湿度差异或工艺条件波动而引起的,从而进一步影响其功能代谢与大曲品质。
2.2.3 微生物群落结构差异分析
通过线性判别分析效应大小(linear discriminant analysis effectsize,LEfSe)对不同等级中高温大曲的差异微生物进行比较,筛选标准为线性判别分析(linear discriminant analysis,LDA)值>3.5、P<0.05,结果见图2。由图2A可知,细菌菌群中共有40个差异微生物,其中特级曲有6个差异微生物,在属水平上包括克罗彭斯特菌属和泛菌属。优级曲有32个差异微生物,在属水平上包括乳球菌属(Limosilactobacillus)、魏斯氏菌属、片球菌属(Pediococcus),这与DENG Y K等[34]的研究结果一致。这些菌属在优级曲中相对丰度较高,可能是由于优级曲堆积较密或翻曲次数少一定程度造成的高温微氧环境筛选了此类菌群,此条件下它们通过高效产酸抑制杂菌,进而确立其优势地位[37]。普级曲有2个差异微生物,主要为厚壁菌门(Firmicutes)和杆菌纲(Bacilli),实际生产中普级曲的产生是由于对工艺参数的控制不如特级曲和优级曲,这造成了更适合厚壁菌门、杆菌纲微生物生存的环境。
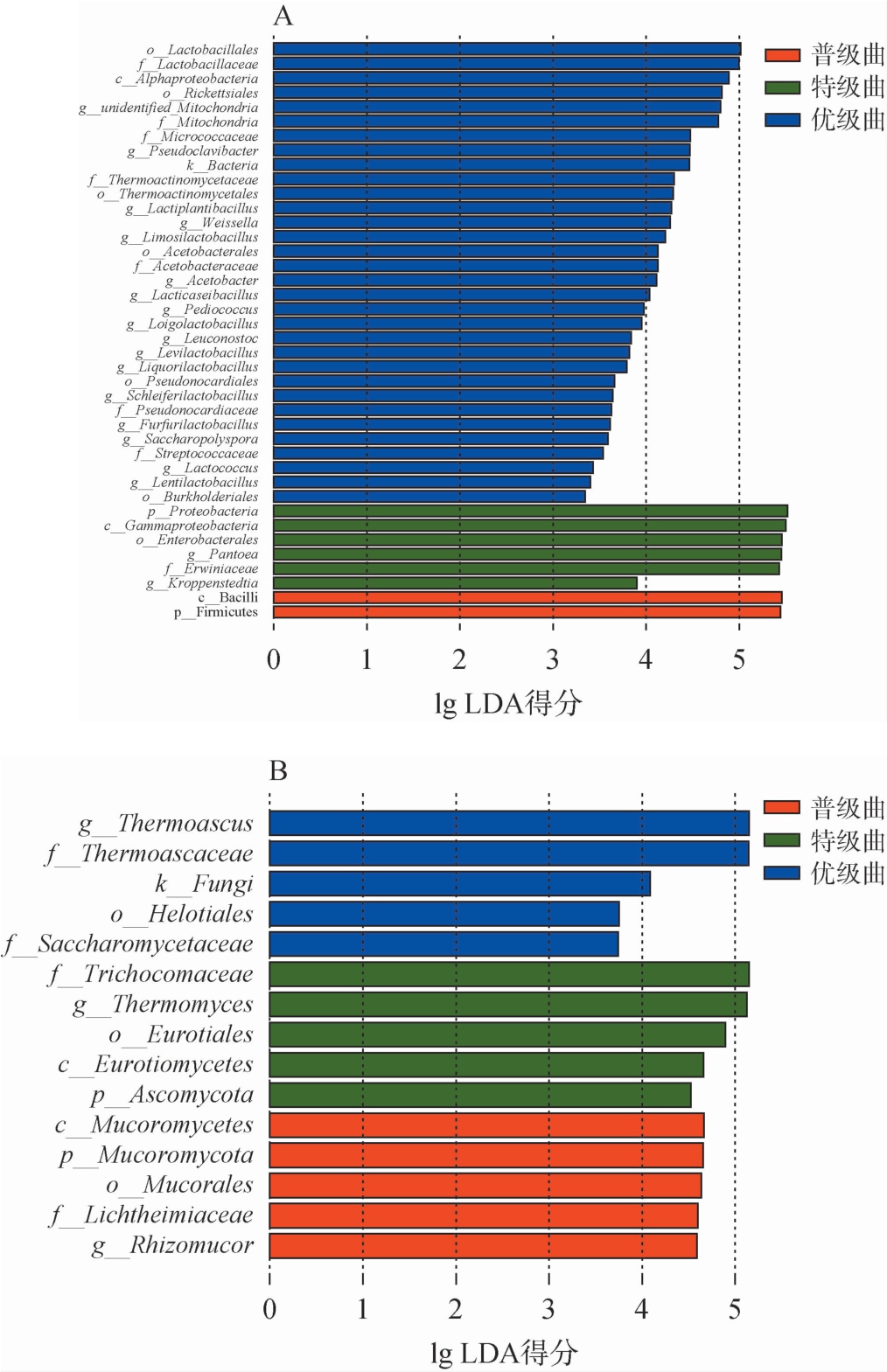
图2 不同等级中高温大曲细菌(A)及真菌(B)菌群线性判别分析效应大小分析结果
Fig.2 Linear discriminant analysis effect size analysis results of bacteria (A) and fungi (B) community in medium-high temperature Daqu with different grades
由图2B可知,真菌菌群中共有15个差异微生物,其中特级曲有5个差异微生物,在属水平上包括嗜热真菌属,嗜热真菌属是耐高温的菌种,其在特级曲中成为优势菌,表明特级曲的发酵过程达到了较高且稳定的高温阶段,为其创造了良好的生长条件。优级曲有5个差异微生物,在属水平包括嗜热子囊菌属。普级曲有5个差异微生物,在属水平上包括毛霉属,毛霉属虽然也产酶,但其热稳定性远低于耐热菌属的酶系,且毛霉过度生长可能造成与有益微生物的竞争,产生不良风味;同时毛霉菌丝生长旺盛影响大曲外观,易引发杂菌污染[33]。3种大曲之间的微生物群落结构差异明显,是由于具有环境耐受性的微生物更能适应曲房环境,在种间竞争中占据优势并大量繁殖[38],这进一步说明了温度控制条件对微生物群落的影响和产出高品质大曲的重要性[39]。
2.3 不同等级中高温大曲挥发性风味物质差异分析
2.3.1 挥发性风味物质种类及含量分析
不同等级中高温大曲挥发性风味物质GC-MS分析结果见图3。
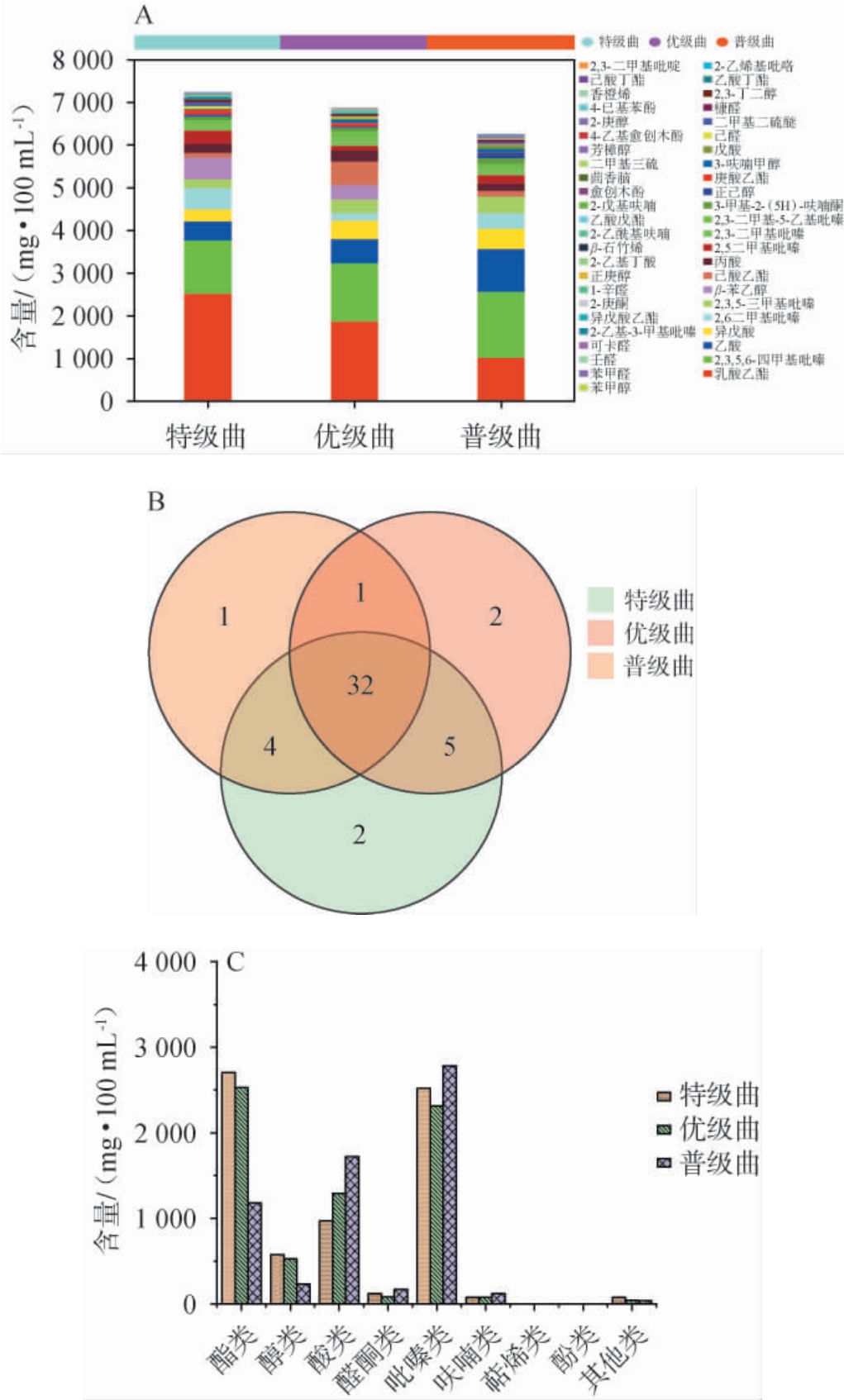
图3 不同等级中高温大曲挥发风味性物质GC-MS分析结果
Fig.3 GC-MS analysis results of volatile flavor compounds in medium-high temperature Daqu with different grades
由图3A可知,不同等级中高温大曲中共检出47种挥发性风味化合物,包括酯类7种,醇类8种,酸类5种,醛酮类7种,吡嗪类7种,呋喃类3种,萜烯类2种,酚类3种,其他类5种。 特级曲中共检出47种,挥发性风味化合物总含量为7 054.20 mg/100 mL,包括酯类7种,醇类8种,酸类5种,醛酮类7种,吡嗪类7种,呋喃类3种,萜烯类2种,酚类3种,其他类5种;优级曲中共检出40种,挥发性风味化合物总含量为6 871.30 mg/100 mL,包括酯类7种,醇类7种,酸类4种,醛酮类7种,吡嗪类7种,呋喃类3种,无萜烯类,酚类1种,其他类4种;普级曲中共检出37种,挥发性风味化合物总含量为6 253.51 mg/100 mL,包括酯类6种,醇类5种,酸类5种,醛酮类7种,吡嗪类7种,呋喃类1种,萜烯类1种,酚类3种,其他类2种。 按挥发性风味物质的总含量递减排序为特级曲、优级曲和普级曲。其中,特级曲中β-苯乙醇和乳酸乙酯含量较高,而优级曲则己酸乙酯含量较高,普级曲乙酸的含量较高。 由图3B可知,特级曲、优级曲、普级曲中共有的挥发性风味物质包括32种,特级曲、优级曲中共有的挥发性风味物质包括5种,特级曲、普级曲共有的挥发性风味物质包括4种,优级曲、普级曲共有的挥发性风味物质仅有1种;特级曲独有的挥发性风味物质为β-石竹烯、2,3-二甲基吡啶,优级曲独有的挥发性风味物质为己酸丁酯、茴香脑,普级曲独有的挥发性风味物质为香橙烯。 由图3C可知,特级曲、优级曲中酯类物质较多(分别为2 705.30 mg/100 mL、2 533.20 mg/100 mL),特级曲、优级曲、普级曲中吡嗪类物质较多(分别为2 519.71 mg/100 mL、2 314.14 mg/100 mL、2 784.40 mg/100 mL)。
2.3.2 关键挥发性风味物质筛选
OAV被广泛用于评估挥发性化合物对整体风味的贡献[40-41]。 OAV>1表明该物质对香气产生有贡献,为关键香气物质;OAV<1则表明该物质的实际呈香作用较弱[42-43]。不同等级中高温大曲中OAV>1的挥发性风味物质见图4。由图4可知,特级曲中关键挥发性风味物质数量最多(32种),优级曲次之(29种),普级曲最少(28种)。 按OAV强度分析,1<OAV<10的挥发性风味物质有5种(2-乙基丁酸、糠醛、苯甲醇、4-乙基愈创木酚、4-已基苯酚);10<OAV<500的挥发性风味物质有13种(乳酸乙酯、庚酸乙酯、芳樟醇、正己醇、β-苯乙醇、乙酸、丙酸等);500<OAV<1 000的挥发性风味物质有3种(乙酸丁酯、1-辛醛、2-乙基-3-甲基吡嗪),OAV>1 000的挥发性风味物质有11种(异戊酸、壬醛、2,5二甲基吡嗪、己酸乙酯、戊酸等)。

图4 不同等级中高温大曲中气味活性值>1的关键挥发性风味物质含量热图
Fig.4 Heat map of contents of key volatile flavor substances with odor activity values>1 in medium-high temperature Daqu with different grades
2.3.3 关键差异挥发性风味物质的筛选
基于挥发性风味物质含量对不同等级中高温大曲样品进行OPLS-DA,并结合VIP值>1和OAV>1筛选不同等级中高温大曲样品间的关键差异挥发性风味物质,结果见图5。
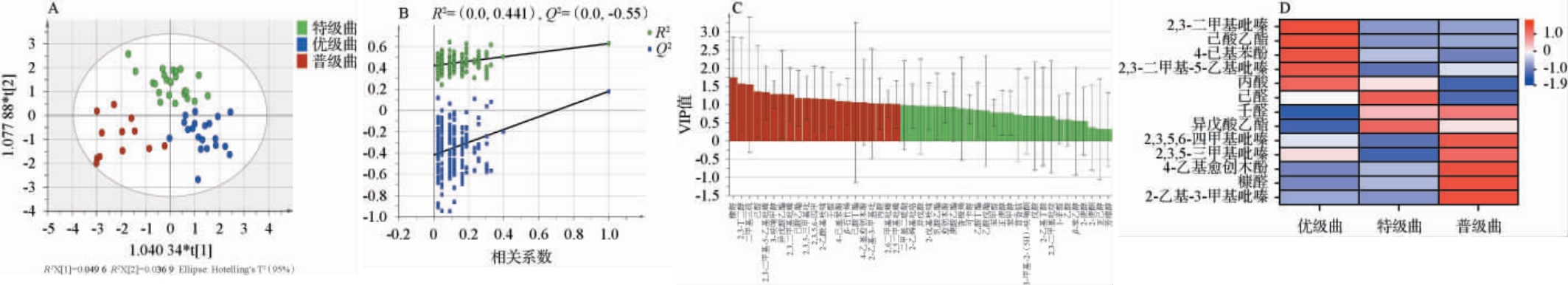
图5 不同等级中高温大曲挥发性风味物质的正交偏最小二乘-判别分析得分图(A)、200次置换检验结果(B)、变量重要性投影值(C)及含量聚类热图(D)
Fig.5 Orthogonal partial least squares-discriminant analysis score plot (A), 200 permutation test results (B), variable importance in the projection values (C) and cluster analysis heatmap (D) of volatile flavor substances contents in medium-high temperature Daqu with different grades
由图5A可知,自变量拟合指数(R2X)为0.852,因变量拟合指数(R2Y)为0.863,模型预测指数(Q2)为0.984,R2和Q2均>0.5,说明模型具有良好的可解释度和拟合度。 在此模型下,3个等级中高温大曲样品被有效区分开。由图5B可知,模型经过200次置换检验后,Q2的回归线与Y轴截距为负值,说明模型未过拟合,进一步证明模型可靠。 由图5C可知,以VIP值>1及P<0.05为依据共筛选出21种主要差异挥发性风味物质,包括3种酯类(乙酸丁酯、己酸乙酯、异戊酸乙酯)、2种醇类(3-呋喃甲醇、2,3-丁二醇)、1种酸类(丙酸)、3种醛类(糠醛、己醛、壬醛)、1种呋喃类(2-乙酰基呋喃)、2种酚类(4-已基苯酚、4-乙基愈创木酚)、1种萜烯类(β-石竹烯)、7种吡嗪类(2,3-二甲基-5-乙基吡嗪、2,3-二甲基吡嗪、2,3,5-三甲基吡嗪、2,3,5,6-四甲基吡嗪、2-乙基-3-甲基吡嗪、2,5-二甲基吡嗪、2,6-二甲基吡嗪)、1种其他化合物(二甲基三硫)。由图5D可知,VIP值>1,P<0.05且OAV>1的关键差异挥发性风味物质有13种,特级曲中2,3-二甲基吡嗪、己酸乙酯、4-已基苯酚、2,3-二甲基-5-乙基吡嗪、丙酸含量较多,优级曲中己醛、异戊酸乙酯含量较多,普级曲则含有较多的2,3,5,6-四甲基吡嗪、2,3,5-三甲基吡嗪、2-乙基-3-甲基吡嗪、4-乙基愈创木酚、糠醛、壬醛,这些物质对不同等级大曲的香气产生区别可能具有重要贡献。
2.4 优势微生物与理化指标、挥发性风味物质间的相关性分析
2.4.1 优势微生物与理化指标间的相关性分析
选择优势微生物属与理化指标进行RDA,结果见图6。由图6A可知,在细菌属水平上,芽孢杆菌属与酸度呈正相关,泛菌属与酸度、酯化力、发酵力、液化力呈正相关,魏斯氏菌属、高温放线菌属、葡萄球菌属和克罗诺杆菌属与水分、糖化力、发酵力、液化力呈正相关,有报道称大曲的糖化、酯化作用与魏斯氏菌属密切相关[44],葡萄球菌属可产生乙醇脱氢酶,与发酵力密且相关[45]。由图6B可知,在真菌属水平上,根霉属与水分、酸度呈正相关,毛霉属与酸度呈正相关;曲霉属和嗜热子囊菌属则是大曲水分保持及糖化、液化过程的关键贡献者,与这些指标呈正相关;曲霉属作为大曲常见菌群,可分泌多种水解酶[46],并通过代谢途径影响糖化力[47]。此外,嗜热真菌属与酸度、发酵力、酯化力、液化力呈正相关,其中特级曲的优势真菌为嗜热真菌属,这或许是其发酵力高和酯化力高的一个潜在原因。

图6 不同等级中高温大曲优势细菌属(A)、真菌属(B)与理化指标间的冗余分析结果
Fig.6 Redundancy analysis results of dominant bacterial genera (A), fungal genera (B) and physicochemical indicators of medium-high temperature Daqu with different grades
2.4.2 优势微生物与挥发性风味物质间的相关性分析
选择优势微生物属与13种关键差异挥发性风味物质进行相关性分析,结果见图7。 如图7A可知,细菌中的芽孢杆菌属与糠醛、壬醛、4-乙基愈创木酚呈高度显著正相关(P<0.001),与2,3,5,6-四甲基吡嗪呈显著正相关(P<0.05),而与丙酸、4-已基苯酚呈高度显著负相关(P<0.001),有研究表明芽孢杆菌属对2,3-丁二醇生成有直接促进作用[48]。葡萄球菌属与异戊酸乙酯呈高度显著正相关(P<0.001),高温放线菌属与2,3-二甲基吡嗪、2,3-二甲基-5-乙基吡嗪、己酸乙酯呈高度显著正相关(P<0.001),与4-己基苯酚呈显著正相关(P<0.05),而与异戊酸乙酯呈极显著负相关(P<0.01)。泛菌属与己醛呈高度显著正相关(P<0.001),与2,3,5,6-四甲基吡嗪、2,3,5-三甲基吡嗪、2-乙基-3-甲基吡嗪呈极显著负相关(P<0.01)。克罗诺杆菌属与丙酸、4-己基苯酚、己醛呈高度显著正相关(P<0.001);魏斯氏菌属与丙酸、4-已基苯酚呈高度显著正相关(P<0.001),而与壬醛、糠醛、4-乙基愈创木酚呈极显著负相关(P<0.01)。 由图7B可知,真菌中与异戊酸乙酯呈高度显著正相关的是嗜热真菌属(P<0.001),其生产的酶制剂具有良好的热稳定性、高效的催化速率、室温下易保存等优点,可促进白酒独特风味的形成[49];而嗜热子囊菌属与异戊酸乙酯呈高度显著负相关(P<0.001)。嗜热真菌属和嗜热子囊菌属分别与2,3-二甲基吡嗪、2,3-二甲基-5-乙基吡嗪、己酸乙酯呈高度负、正显著相关(P<0.001)。毛霉属与2,3,5,6-四甲基吡嗪、2,3,5-三甲基吡嗪、2-乙基-3-甲基吡嗪呈高度显著正相关(P<0.001),与己酸乙酯呈显著正相关(P<0.05),而与己醛呈高度显著负相关(P<0.001);曲霉属与糠醛、壬醛、4-乙基愈创木酚呈显著负相关(P<0.05),曲霉属主要产生蛋白水解酶或其他水解酶类,有助于淀粉糖化、蛋白质水解和类黄酮的形成[50]。 根霉属与2,3-二甲基吡嗪、2,3-二甲基-5-乙基吡嗪呈极显著正相关(P<0.01),而与己醛呈显著负相关(P<0.05)。综上所述,不同微生物在大曲重要挥发性风味物质合成中发挥了关键作用,揭示了微生物群落与发酵产物之间复杂的互作关系,但其具体功能角色还需进一步解析。
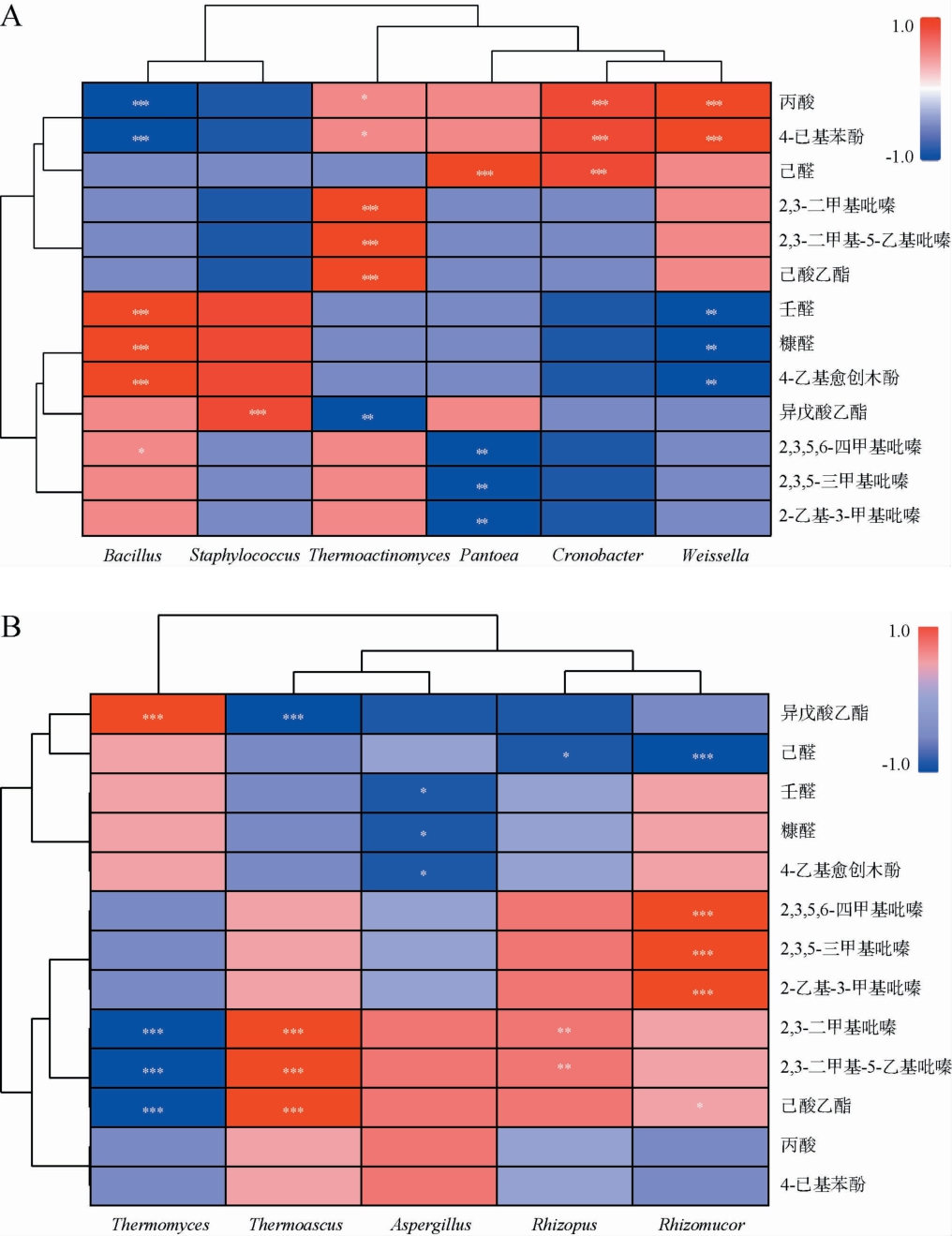
图7 优势细菌属(A)、优势真菌属(B)与关键差异挥发性风味物质的相关性热图
Fig.7 Correlation heat map of dominant bacterial genera (A),dominant fungal genera (B) and key differential volatile flavor substances
“*”代表显著相关(P<0.05),“**”代表极显著相关(P<0.01),“***”代表高度显著相关(P<0.001)。
3 结论
不同等级中高温大曲样品的品质存在一定差异,在理化指标方面,特级曲的糖化力(865.10 U)、酯化力(617.61 U)、发酵力(0.27 U)和液化力(1.78 U)最高,优级曲的水分含量(9.01%)较高,普级曲的酸度(1.06 mmol/10 g)较高。 在微生物群落方面,从大曲样品中共注释到6个优势细菌属(平均相对丰度>1%)和5个优势真菌属,基于LDA值>3.5、P<0.05共筛选得到5个差异细菌属和3个差异真菌属。 特级曲差异菌属为克罗彭斯特菌属(Kroppenstedtia)、泛菌属(Pantoea)、嗜热真菌属(Thermomyces),优级曲差异菌属为乳球菌属(Limosilactobacillus)、魏斯氏菌属(Weissella)、片球菌属(Pediococcus)、嗜热子囊菌属(Thermoas cus),普级曲差异菌属为毛霉属(Rhizomucor)。在挥发性风味物质方面,从大曲样品中共检出47种挥发性风味物质,基于VIP值>1、P<0.05及OAV>1共筛选得到13种关键差异挥发性风味物质,包括2种酯类、1种酸类、3种醛类、2种酚类、5种吡嗪类。相关性分析结果表明,优势微生物属与大曲的理化指标及挥发性风味成分存在一定的相关性。本研究明确了各等级中高温大曲在微生物群落、理化及风味组分上的差异,并分析了造成此差异的主要原因,为大曲质量提升和工艺定向调控提供了理论支持和科学依据。
[1]章克昌.酒精与蒸馏酒工艺学[M].北京:轻工业出版社,1995:434-437.
[2]罗建超,谢和.大曲中产酱香芽孢杆菌的筛选及其代谢产香探析[J].酿酒科技,2012(5):35-40.
[3]向港兴,陈莹琪,沈毅,等.不同等级浓香型大曲微生物群落结构与理化性质的比较分析[J].食品科学,2022,43(18):184-191.
[4]冯哲瀚,华德平,梅雪锋,等.乳酸乳球菌表达系统的研究进展及其应用[J].中国农业科技导报(中英文),2025,27(1):25-34.
[5]林涵瑞,刘林培,黄蜀生,等.邛崃产区中高温大曲性能及微生物动态变化研究[J].食品与发酵工业,2024,50(19):117-126.
[6]孔祥聪,邢文慧,管桂坤,等.兰陵浓香大曲理化性质和细菌群落多样性研究[J].中国酿造,2023,42(7):126-131.
[7]施思,彭智辅,乔宗伟,等.浓香型大曲贮藏过程中糖化力发酵力变化及真菌多样性分析[J].食品与发酵工业,2017,43(5):76-79.
[8]沈世明,何猛超,刘桂珍,等.酱香型大曲贮存初期微生物及风味物质变化的分析研究[J].酿酒科技,2023(2):128-135.
[9]胡晓龙,王康丽,牛广杰,等.基于高通量测序技术的中温大曲中微生物群落多样性解析[J].轻工学报,2019,34(4):21-29.
[10]张春英,张子怡,杨涛,等.浓香型中高温大曲制作过程中细菌群落变化研究[J].酿酒,2025,52(2):104-108.
[11]王芙蓉,李靖,赵益梅,等.酱香大曲中高温放线菌的筛选及其产蛋白酶条件优化[J].中国酿造,2022,41(8):132-136.
[12]李彦涛,尉军强,郭永昌,等.不同贮存期、不同质量的中高温大曲细菌群落演变分析[J].酿酒科技,2025(10):17-21,27.
[13]中华人民共和国工业和信息化部.QB/T 4257—2011 酿酒大曲通用分析方法[S].北京:中国标准出版社,2011.
[14]张晓婕,邱树毅,王晓丹,等.不同质量酱香型白酒的挥发性物质差异分析[J].中国食品学报,2022,22(10):340-351.
[15]张曼,谢军,卫春会,等.浓香型单层大曲与双层大曲的质量对比分析[J].食品与发酵工业,2018,44(12):221-228.
[16]YANG Y,WANG S T,LU Z M,et al.Metagenomics unveils microbial roles involved in metabolic network of flavor development in mediumtemperature Daqu starter[J].Food Res Int,2021,140:110037.
[17]陈磊,戴亦军.基于Illumina MiSeq高通量测序技术分析丹阳黄酒酒曲中微生物菌群多样性[J].中国酿造,2024,43(6):141-145.
[18]姚亚林,邓杰,任志强,等.不同品温大曲及其曲房空气的细菌群落变化规律和相关性[J].现代食品科技,2021,37(3):62-69.
[19]唐慧芳,黄钧,周荣清,等.空间异质性对大曲微生物群落的影响[J].食品科学,2023,44(14):206-215.
[20]向玉萍,邱树毅,曹文涛,等.酱香型白酒核心产区大曲中霉菌的分离及鉴定[J].食品与发酵科技,2021,57(2):56-65.
[21]王淑珍,孙亮霞,林一心,等.浓香大曲发酵前后微生物群落组成及溯源分析[J/OL].食品与发酵工业,1-11[2025-11-25].https://doi.org/10.13995/j.cnki.11-1802/ts.042428.
[22]陈容钦,李玲,李晓云.泛菌属内生菌YMR3提高花生植株对几种病虫害生物胁迫的抗性研究[J].中国生物防治学报,2024,40(1):71-79.
[23]姚粟,葛媛媛,李辉,等.利用非培养技术研究芝麻香型白酒高温大曲的细菌群落多样性[J].食品与发酵工业,2012,38(6):1-6.
[24]王军燕,甄攀,王晓勇.不同培曲工艺对清香型大曲细菌菌群结构的影响[J].酿酒,2023,50(4):72-74.
[25]何猛超,任义平,熊林,等.茅台地区不同高温大曲微生物群落结构解析[J].中国酿造,2022,41(6):51-57.
[26]于学健,冯慧军,翟磊,等.芝麻香型白酒高温大曲中高温放线菌及其功能基因的动态变化规律[J].食品与发酵工业,2019,45(13):71-77.
[27]陈娇,时冉冉,张军要.浓香型白酒酒醅微生物分子生物学研究[J].生物技术世界,2016(1):58.
[28]明红梅,余欢,周健,等.大曲中产香兼性厌氧细菌的筛选及挥发性成分分析[J].食品与机械,2015,31(2):7-10.
[29]HE G Q,DONG Y,HUANG J,et al.Alteration of microbial community for improving flavor character of Daqu by inoculation with Bacillus velezensis and Bacillus subtilis[J].LWT-Food Sci Technol,2019,111:1-8.
[30]DENG L,MAO X,LIU D,et al.Comparative analysis of physicochemical properties and microbial composition in high-temperature Daqu with different colors[J].Front Microbiol,2020,11:588117.
[31]吴树坤,谢军,卫春会,等.四川不同地区浓香型大曲微生物群落结构比较[J].食品科学,2019,40(14):144-152.
[32]王西,邓小鹏,万倩,等.中高温大曲表面霉菌分离鉴定与控制研究[J].中国酿造,2024,43(3):90-94.
[33]雷少楠,徐柏田,林培,等.特香型大曲表面毛霉对大曲与基酒质量的影响[J].中国酿造,2020,39(6):111-114.
[34]DENG Y K, HUANG D, HAN B L, et al.Correlation: Between autochthonous microbial diversity and volatile metabolites during the fermentation of Nongxiang Daqu[J].Front Microbiol,2021,12:688981.
[35]徐千惠,饶家权,邹永芳,等.浓香型大曲贮存期微生物群落演替及代谢产物的变化机制[J].食品科学,2023,44(22):225-234.
[36]HUANG X, LI R, XU J, et al.Integrated multi-omics uncover viruses,active fermenting microbes and their metabolic profiles in the Daqu microbiome[J].Food Res Int,2025,208:116061.
[37]陈可丹,吴晓江,陈延儒,等.顶温对特香型大曲理化指标及菌群演替的影响[J].食品与发酵工业,2020,46(5):52-58.
[38]胡令涵,李平兰,王玉.乳酸乳球菌L-H410产抗菌肽的理化性质分析及发酵工艺优化[J].乳业科学与技术,2025,48(3):1-10.
[39]WANG S,CHEN H,SUN B.Recent progress in food flavor analysis using gas chromatography-ion mobility spectrometry(GC-IMS)[J].Food Chem,2020,315:126158.
[40]TIE Y,WANG L,DING B,et al.Investigating the main contributors to esterification activity and identifying the aqueous-phase ester synthases in Daqu[J].Food Biosci,2025,66:106227.
[41]MIHINDUKULASURIYA S D F, JAYASURIYA H P W.Drying of chilli in a combined infrared and hot air rotary dryer[J].J Food Sci Technol,2015,52(8):4895-4904.
[42]曾庆军,邱树毅,刘凡,等.基于化学计量法的酱香型白酒等级分析[J].食品与生物技术学报,2024,43(8):140-150.
[43]JIA W, FAN Z, DU A, et al.Characterisation of key odorants causing honey aroma in Feng-flavour Baijiu during the 17-year ageing process by multivariate analysis combined with foodomics[J].Food Chem, 2021,374:131764.
[44]陈绍依,郎莹,邱树毅,等.茅台镇不同区域酱香大曲微生物群落结构及生产性能对比[J].食品科学,2023,44(14):134-143.
[45]刘文虎,柴丽娟,张立强,等.基于宏基因组学解析不同质量等级中温大曲微生物组的异质性[J].微生物学报,2023,63(11):4383-4398.
[46]薛宇昂,郭壮,赵慧君,等.基于MiSeq测序技术石花酒大曲中微生物多样性解析[J].中国酿造,2020,39(7):163-168.
[47]WANG X D,BAN S D,QIU S Y.Analysis of the mould microbiome and exogenous enzyme production in Moutai-flavor Daqu[J].J I Brewing,2018,124(1):91-99.
[48]张清玫,赵鑫锐,李江华,等.不同香型白酒大曲微生物群落及其与风味的相关性[J].食品与发酵工业,2022,48(10):1-10.
[49]MIN Z,JIA Z,JUN X,et al.Effects of environmental factors on the microbial community changes during medium-high temperature Daqu manufacturing[J].Food Res Int,2022,153:110955.
[50]HU Y,DUN Y,LI S,et al.Changes in microbial community during fermentation of high-temperature Daqu used in the production of Chinese'Baiyunbian'liquor[J].J I Brewing,2017,123(4):594-599.