中国白酒是世界六大蒸馏酒之一[1],在开放的环境中通过多种微生物的协同作用自然发酵制成。酒曲为白酒发酵提供了重要的微生物来源,很大程度上决定白酒的品质、产量和风格[2]。 我国酒曲主要分为大曲、小曲、麸曲这三大类,其中大曲因具有易培养、功能多、微生物菌群丰富等特点,备受众多白酒企业青睐[3]。大曲的制备包括原料制备、砖形压制、发酵和储存四个环节,采用自然接种方式,微生物来源复杂,受原料、环境等因素影响大。不同批次的原料携带的微生物种类和数量存在一定差异,导致大曲中微生物群落结构不稳定,使大曲的质量产生波动,进而影响基酒生产[4]。小曲是以米糠或米粉为原料,接种一定量的母曲培养而成的块状酒曲[5]。与大曲相比,小曲微生物菌群结构相对简单,主要为糖化发酵菌[6]。 麸曲是采用纯种菌种,以麸皮为原料经人工控制温度和湿度培养而成的,它主要起糖化作用。 张家辉等[7]采用传统培养分离法从伊力特浓香型大曲中分离筛选一株高产糖化酶和液化酶的霉菌JW-3,并通过形态学观察及分子生物学技术将其鉴定为伞枝横梗霉(Lichtheimia corymbifera)。使用该菌株制作的纯菌种麸曲糖化酶活力为409.67 U/g,液化酶活力为1 597.00 U/g,在白酒酿造过程中具有一定的应用潜力。大曲中的微生物和酶在白酒发酵过程中,将原料中的淀粉、蛋白质等分解转化,生成的酒精和其他风味物质相互协调,使得大曲白酒酒质优良、口感醇厚、香气浓郁。但是自然发酵形成的大曲中具有活性的功能微生物丰度较低,可能会影响发酵的稳定性和质量。因此,在传统大曲的基础上适当补充核心功能微生物是提高其发酵品质的潜在有效途径。乳酸菌和酵母菌是白酒酿造过程中优势菌群,与白酒中大多数醇类、酸类和酯类呈正相关[8],决定着白酒风味化合物的形成,合理运用功能菌株是实现高效生产、改善白酒风味、提高白酒品质的有效手段之一[9-10]。 HE G Q等[11]在大曲中添加产香菌株贝莱斯芽孢杆菌(Bacillus velezensis)和枯草芽孢杆菌(Bacillus subtilis),改善了大曲的风味特性,增加了不同类型白酒的乙酸乙酯含量。FAN G S等[12]向大曲中加入酿酒酵母(Saccharomyces cerevisiae)和异常威克汉姆酵母(Wickerhamomyces anomalus)不仅提高了乙酯类的含量,还增加了其他风味化合物的含量。己酸乙酯和丁酸乙酯是浓香型白酒中不可缺少的风味物质,但酒醅中批次生产不稳定性会降低白酒的品质,在浓香型白酒中添加酪丁酸梭菌(Clostridium tyrobutyricum)和酿酒酵母,增强了典型风味代谢物[13]。 HUANG X N等[14]研究发现,从清香型大曲中筛选出的植物乳植杆菌(Lactiplantibacillus plantarum)E2、植物乳植杆菌和戊糖片球菌(Pediococcus pentosaceus)E48在固态发酵过程中均能对大曲风味起到有效提升作用。 唐涛[15]研究发现,将汉逊酵母和多种酿酒酵母复配制成强化大曲后,应用于白酒生产中,其总酯含量以及2-甲基-1-丙醇、1-己醇、戊四醇等多种风味物质的含量均显著高于普通大曲。功能菌株对改善白酒风味有积极的作用,然而作为白酒酿造过程中的核心菌株乳酸菌和酵母菌的组合却鲜有研究,尤其是共培养对微生物群落结构的影响也知之甚少。
为选育优良的酵母菌和乳酸菌,本研究分别采用单菌固态发酵和模拟白酒发酵体系对来自低温大曲中的6株酵母菌和11株乳酸菌进行了发酵力、耐受性及风味代谢性能评价,选育优良酵母菌和乳酸菌,将其应用于清香型白酒酿造中,并通过优化其发酵工艺,探究功能菌株对清香型白酒酿造风味及微生物群落的影响。旨在减小批次间生产波动性、精准调控酒体中醇类与酸类物质的比例、改善风味、提高基酒的品质。
1 材料与方法
1.1 材料与试剂
1.1.1 原料和菌株
高粱、稻壳、酒糟、大曲:北京红星二锅头有限公司;玉米:市售;糖化酶(50 000 U/g)、液化酶(4 000 U/g):上海吉至生化科技有限公司;酿酒酵母(Saccharomyces cerevisiae)Y3、Y4、Y6、Y11、Y16、Y22、乳酸片球菌(Pediococcus acidilactici)Pea1、Pea2、Pea5、Pea12、Pea24、Pea27、Pea30、嗜 酸乳杆菌(Lactobacillus acidophilus)Laa1、保加利亚乳杆菌(Lactobacillus bulgaricus)Lab1、乳酸乳球菌(Lactococcus lactis)L1、酒类酒球菌(Oenococcus oeni)O1:本实验室从中低温大曲中筛选及保藏。
1.1.2 化学试剂
氢氧化钠(分析纯)、乙酸戊酯(色谱纯):上海麦克林生化科技有限公司;氯化钠(分析纯):天津市江天化工技术有限公司;盐酸(分析纯):天津市化学试剂一厂;无水乙醇(分析纯):上海麦瑞尔化学技术有限公司;2-辛醇(色谱纯):阿拉丁控股集团(上海)有限公司。
1.1.3 培养基
MRS琼脂培养基:青岛海博生物有限公司。
酵母浸出粉胨葡萄糖(yeast peptone dextrose,YPD)培养基:葡萄糖20 g/L,酵母浸粉10 g/L,蛋白胨20 g/L,琼脂20 g/L,蒸馏水1 000 mL,115 ℃灭菌20 min。
发酵培养基:称取1 500 g玉米渣,加入4 500 mL 65~70 ℃的温水,静置20 min。 加入900 μL液化酶,90 ℃液化1.5 h。降温至60 ℃,加入3 mL糖化酶,于60 ℃水浴锅中糖化16 h,纱布过滤得到上清液,即得发酵原液。 将发酵原液分别稀释至8°Brix、12 °Brix,加入0.5%的酵母浸粉,作为菌株发酵的一级和二级种子液,将发酵原液稀释至16 °Brix,作为菌株的发酵培养基,115 ℃灭菌20 min。
1.2 仪器与设备
7890A-5975C气相色谱质谱联用(gas chromatography mass spectrometry,GC-MS)仪、1200SL高效液相色谱(high performance liquid chromatography,HPLC)仪、7890A气相色谱(gas chromatography,GC)仪:美国Agilent公司;IS-RDS3恒温摇床:上海世成仪器科技有限公司;TQ8050三重四极杆气质联用仪:日本岛津公司;Synergy 4型多功能酶标仪:美国BioTek公司;PCT-200型聚合酶链式反应(polymerase chain reaction,PCR)基因扩增仪:美国BIO-RAD公司;Q1 PLUS ONE实时荧光定量聚合酶链式反应(real-time fluorescent quantitative PCR,fqRT-PCR)仪:美国Thermo Fisher公司。
1.3 方法
1.3.1 酿酒酵母的选择
将6株酿酒酵母Y3、Y4、Y6、Y11、Y16、Y22应用于清香型白酒酿造,取128 g的酒糟和8 g的稻壳分别清蒸15 min和30 min后与32 g的高粱混匀,纱布包好,闷料30 min;105 ℃高压蒸汽灭菌30 min,冷却至30 ℃左右,加二级培养的液体酵母(接种量为1.0×107 CFU/mL),拌匀,适量补水,继续摊凉至25 ℃左右装坛,于30 ℃条件下恒温发酵7 d。分别对6株酿酒酵母的发酵力、酒醅的理化指标及挥发性风味物质进行分析。
1.3.2 乳酸菌的选择
11 株 乳 酸 菌(Pea1、Pea2、Pea5、Pea12、Pea24、Pea27、Pea30、Laa1、Lab1、L1、O1)初始浓度均为109 CFU/mL,用生理盐水分别稀释至10-1、10-2、10-3、10-4、10-5五个梯度,涂布在乙醇体积分数分别为0、4%、8%、10%的MRS平板上,观察平板上菌株生长情况,探究其乳酸代谢情况,对乳酸菌菌株进行初步筛选。
将筛选的乳酸菌与酵母菌混合固态发酵,探究其风味代谢情况。具体方法为:取128 g的酒糟和8 g的稻壳分别清蒸15 min和30 min后与32 g的高粱混匀,纱布包好,闷料30 min;105 ℃灭菌30 min,冷却至30 ℃左右,将筛选乳酸菌、酵母菌以1∶1混合(接种量均为1.0×107 CFU/mL),拌匀,适量补水,继续摊凉至25 ℃左右装坛于30 ℃条件下恒温发酵7 d。发酵结束后,检测样品的酒精度和挥发性风味物质含量。
1.3.3 清香型白酒生产工艺流程及操作要点
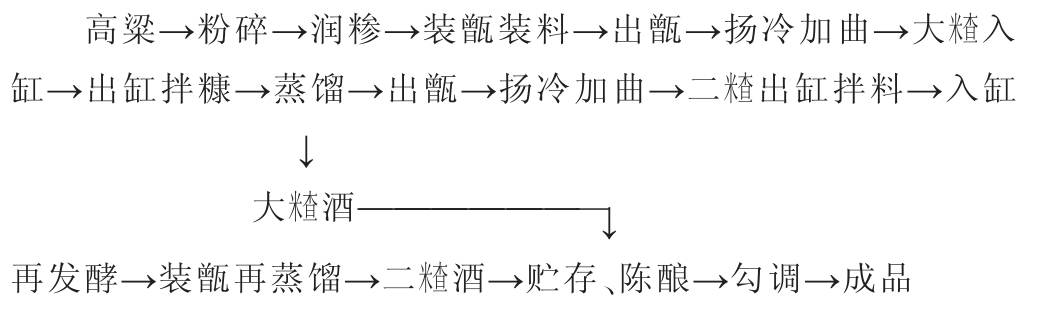
操作要点:清香型白酒酿造以高粱与大曲为核心原料[16]。高粱需颗粒饱满、皮薄壳少;大曲分清茬、红心、后火三种,按3∶3∶4配比使用[17]。原料需经粉碎,高粱破为4~8瓣,粗细粉按比例控制[18]。 配料时,将新粮、酒糟、辅料与水按比例混合,分大入缸和二入缸控制水分、用曲及辅料量,辅料清蒸30 min以上。 润糁用90 ℃热水,加水量60%~70%,要求润透无疙瘩[19],105 ℃条件下蒸料30 min,要求熟透不黏。蒸后加水量30%冷却,适时加曲(添加量10%),混合均匀后入缸。地缸发酵前用花椒水杀菌,控温入缸(22~34 ℃),保温发酵11 d,按“前缓、中挺、后缓落”原则控温[20]。发酵结束出缸蒸馏,装甑须薄匀,蒸馏时掐头去尾,收取主体酒液。新酒需贮存于阴凉通风处陈酿老熟,陶瓷容器为佳,使酒体醇厚协调。最后经勾调即得清香型白酒成品。
1.3.4 酵母菌和乳酸菌混合发酵
用接种环挑取优良乳酸菌接种至装液量为6 mL/25 mL玉米水解液中,37 ℃培养24 h获得种子液,将种子培养液摇匀后接种至装液量为54 mL/250 mL玉米水解液中,用纱布和牛皮纸将瓶口封紧,37 ℃培养24 h获得二级种子液,离心浓缩得到乳酸菌菌剂。酿酒酵母菌剂的制备方法同乳酸菌菌剂,不同的是培养温度为30 ℃。
取128 g的酒糟和8 g的稻壳分别清蒸15 min和30 min后与32 g的高粱混匀,纱布包好,闷料30 min;105 ℃灭菌30 min,冷却至30 ℃左右,将筛选得到的优良酵母菌和乳酸菌的 二 级 浓 缩 种 子 液 分 别 按1.0∶0.2、1.0∶1.0、1.0∶10.0、1.0∶50.0的比例混合(酵母接种量为1.0×107 CFU/mL,乳酸菌接种量分别为0.2×107 CFU/mL、1.0×107 CFU/mL、1×108 CFU/mL、5×108 CFU/mL),拌匀,适量补水,继续摊凉至25 ℃左右装坛,每12 h称质量一次,30 ℃静置发酵72 h。
1.3.5 清香型白酒酒醅发酵功能菌株接种比例及酒醅入池温度优化
将128 g的酒糟和8 g的稻壳分别清蒸15 min和30 min,再与32 g的高粱混匀,纱布包好,闷料30 min;高压锅105 ℃,蒸30 min,冷却至30 ℃左右,添加大曲(添加量10%)和酿酒酵母剂(接种量1×107 CFU/mL)、乳酸菌剂(接种量1.0×107CFU/mL、5×107CFU/mL、1×108CFU/mL、1.5×108CFU/mL),拌匀,适量补水,入池水分55%左右,继续摊凉至25 ℃左右装坛发酵,稍微压紧,30 ℃静置发酵11 d。 考察菌株Y6与Pea30不同接种比例(1∶1、1∶5、1∶10、1∶15)对清香型白酒主要酯类和醇类含量的影响。
将128 g的酒糟和8 g的稻壳分别清蒸15 min和30 min,再与32 g的高粱混匀,纱布包好,闷料30 min;105 ℃条件下蒸料30 min,冷却至30 ℃左右,添加大曲(添加量10%)和酿酒酵母剂(接种量1×107 CFU/mL)、乳酸菌剂(接种量5×107CFU/mL),拌匀,适量补水,入池水分55%左右,继续摊凉至25 ℃左右装坛发酵,稍微压紧,分别在入池温度22 ℃、26 ℃、30 ℃、34 ℃条件下静置发酵11 d。考察不同入池温度对清香型白酒主要酯类和醇类含量的影响。
1.3.6 功能菌株在清香型白酒酿造中的应用
CK组:只添加大曲(添加量10%)。 ZJ组:添加大曲(添加量10%)和酿酒酵母剂(接种量1×107 CFU/mL)、乳酸菌剂(接种量5×107 CFU/mL)。 入池温度26 ℃,入坛发酵水分55%,发酵时间11 d。 分别于0、3 d、7 d、11 d取样,每个样品取3个平行,共24个酒醅样品。
1.3.7 高通量测序
将上述酒醅样品采用细菌、真菌脱氧核糖核酸(deoxyribonucleic acid,DNA)提取试剂盒分离提取筛选细菌、真菌基因组DNA,使用细菌、真菌通用引物进行聚合酶链式反应(PCR),PCR结束后,将PCR扩增产物进行1%琼脂糖凝胶电泳分析,将验证合格后的送至PCR扩增产物上海派诺森生物科技有限公司进行微生物高通量测序分析。 下机数据经拼接、质控、删除嵌合体等,利用USEARCH(http://unite.ut.ee)将序列按97%相似度聚类为操作分类单元(operational taxonomic units,OTUs),再将所有序列与SILVA数据库比对得到序列的物种信息分类。
1.3.8 分析检测
(1)酒醅理化指标
总酸、还原糖、淀粉、水分含量:参考地方标准DB34/T 2264—2014《固态发酵酒醅分析方法》中的方法测定;酒精度:使用酒精计测定。
(2)风味物质
风味物质:采用GC-MS法测定。
预处理:取8 mL蒸馏酒样于20 mL顶空瓶中,加入3 g氯化钠形成饱和液,并加入10 μL 2-辛醇(质量浓度9.6 mg/L)与10 μL乙酸戊酯(质量浓度9.6 mg/L)内标,内标终质量浓度为12 μg/L。
GC-MS条件为:CP-INNOWAX色谱柱(60 m×250 μm×0.4 μm);载气为高纯氦气(He),流速1 mL/min;进样量为1 μL,不分流进样。升温程序为初始温度40 ℃,以10 ℃/min升至50 ℃,保持5.5 min,再以3 ℃/min升至80 ℃,保持8 min,最后以4 ℃/min升至200 ℃,保持13 min。 电子电离(electronic ionization,EI)源;电子能量70 eV,离子源温度230 ℃,进样口和检测器温度均为250 ℃,扫描质量范围35~500 amu。
定性与定量分析:将采集的质谱图利用内置美国国家标准技术研究所(National Institute of Standards and Technology,NIST)14.L谱库进行检索定性,筛选定性结果中可信度>80的风味物质定性。采用内标法进行定量分析。
乳酸含量:采用高效液相色谱法测定。
HPLC条件:采用Aminex HPX-87H色谱柱(300 mm×7.8 mm×9 μm),流动相为5 mmol/L硫酸,二极管阵列检测器(diode array detector,DAD),柱温60 ℃,流速为0.6 mL/min,检测波长为210 nm。
定性定量方法:依据乳酸保留时间与标准品比对定性,通过外标法定量。
乳酸乙酯、乙酸乙酯含量:采用气相色谱法测定。
GC条件:氢火焰离子检测器(flame ionization detector,FID);HP-INNOWAX色谱柱(50 m×320 μm×1.0 μm);载气为高纯氮气(N2);分流比1∶10;进样口温度200 ℃;检测器温度200 ℃;进样量1 μL。程序升温为50 ℃保持8 min,5 ℃/min升温至180 ℃,保持10 min,每个样品运行44 min。
(3)酵母菌和乳酸菌活菌数
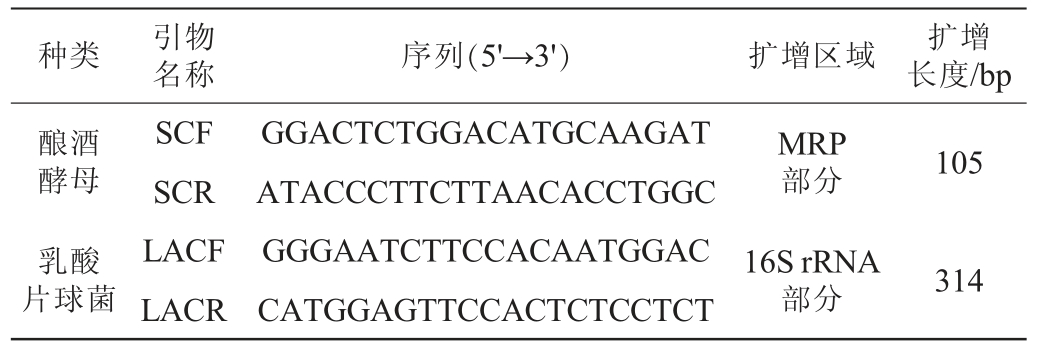
酿酒酵母Y6、乳酸片球菌Pea30活菌数:采用fqRT-PCR法进行测定。菌株Y6以MRP2为目标基因设计专一性引物:SCF和SCR;菌株Pea30以16S rRNA为目标基因设计专一性引物:LACF和LACR,见表1。 PCR扩增体系为20 μL,其中包含10 μL TB Green Premix EX Taq,上下引物各0.8 μL,0.4μLROXReferenceDye,2 μL模板和6 μL 双蒸水(ddH2O),PCR扩增程序为:95 ℃30 s,95 ℃3 s,60 ℃34 s,95 ℃15 s,共40个循环。
表1 实时荧光定量聚合酶链式反应专一性引物
Table 1 Specific primers of real-time fluorescent quantitative polymerase chain reaction
种类 引物名称 序列(5'→3') 扩增区域 扩增长度/bp酿酒酵母105乳酸片球菌SCF SCR LACF LACR GGACTCTGGACATGCAAGAT ATACCCTTCTTAACACCTGGC GGGAATCTTCCACAATGGAC CATGGAGTTCCACTCTCCTCT MRP部分16S rRNA部分314
1.3.9 数据处理与统计分析
所有统计分析均使用IBM SPSS statistics 23.0,图形由Origin 2021软件和Graphpad Prism 8.3.0绘制。
2 结果与分析
2.1 酿酒酵母的选择
酿酒酵母是白酒发酵中最核心的微生物,其具有产酒精、产酯等重要功能[21]。为了选育一株具有优良发酵特性的酿酒酵母,通过固态发酵对酵母菌株发酵力、酒醅理化指标以及风味物质含量等进行测定,结果分别见图1~图3。
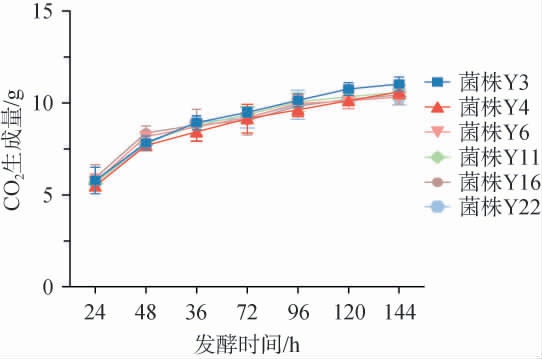
图1 酿酒酵母单菌固态发酵过程中CO2生成量变化
Fig.1 Changes of CO2 production during single-strain solid-state fermentation process of Saccharomyces cerevisiae
酿酒酵母发酵过程主要是代谢葡萄糖生成酒精、水和二氧化碳。CO2生成量多,说明发酵速度快,酵母发酵能力强。因此,可以通过发酵过程中CO2生成量的变化来评价酵母的发酵能力。由图1可知,6株酿酒酵母CO2生成量的变化基本一致,总发酵天数都为7 d,且前24 h CO2生成量最多,发酵速率最快。
由图2可知,在相同发酵条件下,6株酵母的酒精度在5.5%vol~7.1%vol之间,其中菌株Y6和Y16产酒最高。不同菌株之间的还原糖、淀粉和水分无明显差异。白酒中水和乙醇约占98%,微量成分占2%[22],其中酯类占微量成分的60%以上,并且大多数酯类阈值低,因此对风味贡献很大[23]。
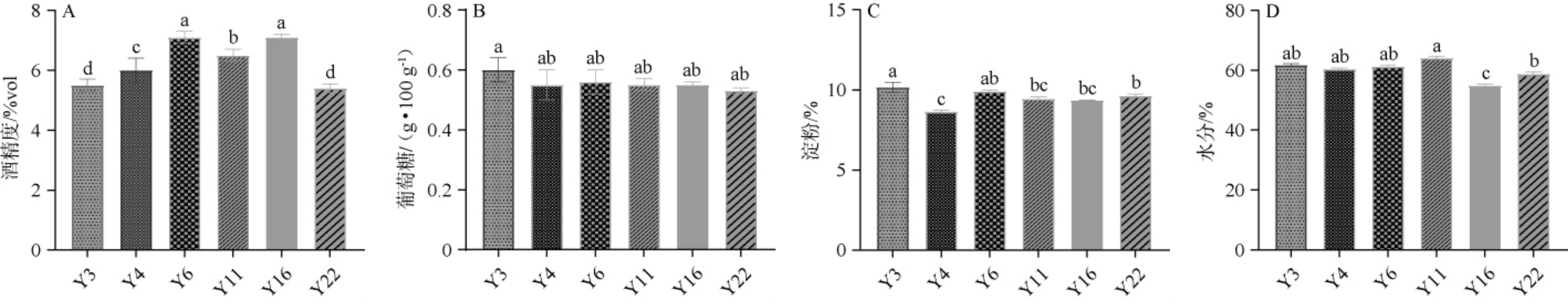
图2 酿酒酵母单菌固态发酵酒醅理化指标测定结果
Fig.2 Determination results of physicochemical indexes of fermented grains by single-strain solid-state fermentation of Saccharomyces cerevisiae
A:酒精度;B:还原糖;C:淀粉;D:水分。不同小写字母表示差异显著(P<0.05)。下同。
由图3可知,Y3、Y4、Y6、Y11、Y16、Y22 6株酿酒酵母的乙酸乙酯生成量呈梯度增加。 乳酸乙酯生成量最高的是菌株Y6,其次是菌株Y4。 6株酿酒酵母异丁醇大致呈下降趋势,其中菌株Y3的异丁醇最高。 异戊醇生成量在42~74 mg/L之间,菌株Y4和Y11苯乙醇生成量显著高于另4株酿酒酵母(P<0.05),菌株Y3正丙醇生成量最低,其他5株的正丙醇产量无显著差异。
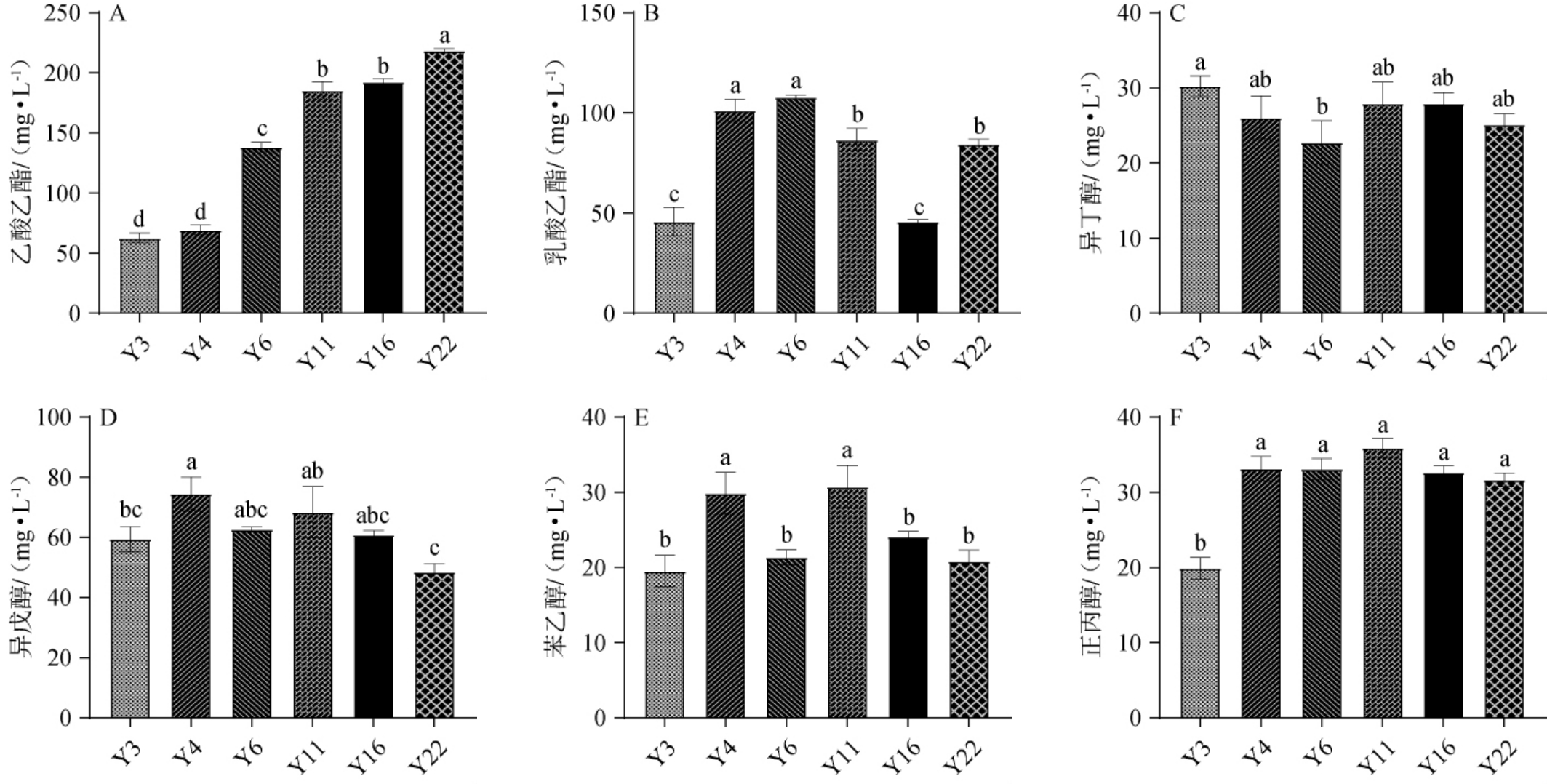
图3 酿酒酵母单菌固态发酵酒醅主要风味物质含量测定结果
Fig.3 Determination results of mainly flavor compounds contents of fermented grains by single-strain solid-state fermentation of Saccharomyces cerevisiae
A:乙酸乙酯;B:乳酸乙酯;C:异丁醇;D:异戊醇;E:苯乙醇;F:正丙醇。
综上,菌株Y6乳酸乙酯生成量最高,乙酸乙酯生成量中等(138.18 mg/L),正丙醇、异丁醇、异戊醇等高级醇生成量适中。 因此,选择酿酒酵母菌株Y6为优良菌株。
2.2 乳酸菌的选择
乳酸菌在白酒酿造过程中发挥着重要作用,可以产生有机酸和酶类等多种代谢产物,有机酸与醇类进一步生成酯类物质[24]。为了筛选到耐酒精能力优良的乳酸菌菌株,研究11株乳酸菌(7株乳酸片球菌Pea、1株嗜酸乳杆菌Laa1、1株保加利亚乳杆菌Lab、1株乳酸乳球菌L1和1株酒类酒球菌O1)耐酒精能力,结果见图4。由图4可知,乙醇体积分数在0~10%时,所有菌株在稀释度为10-1~10-4时均能在MRS培养基上生长。但在稀释度为10-5,仅有乳酸片球菌Pea24、Pea5、Pea12和Pea30、乳酸乳球菌L1、嗜酸乳杆菌Laa1和酒类酒球菌O1能在乙醇体积分数10%的MRS平板上生长,说明这7株菌株有较强的酒精耐受性。

图4 乳酸菌菌株酒精耐受性分析结果
Fig.4 Analysis results of alcohol tolerance of lactic acid bacteria strains
乳酸是清香型白酒发酵过程中合成的重要有机酸,也是合成乳酸乙酯的前体物质[25]。分析11株乳酸菌乳酸产量,并将初步筛选乳酸菌与酵母菌混合(1∶1)固态发酵,酒醅酒精度、乙酸乙酯、乳酸乙酯结果见图5。由图5A可知,通过分析检测11株乳酸菌发酵生成的乳酸含量,乳酸片球菌Pea30和嗜酸乳杆菌Laa1乳酸产量较高,分别为6.3 g/L、5.9 g/L,其次是乳酸片球菌Pea1、Pea2和Pea5,分别为5.6 g/L、5.55 g/L、5.7 g/L。结合乳酸菌菌株酒精耐受性分析,菌株Pea30、Pea5和Laa1有较强的酒精耐受性,并且产乳酸能力强。因此,初步筛选得到菌株Pea30、Pea5和Laa1 3株优良乳酸菌。
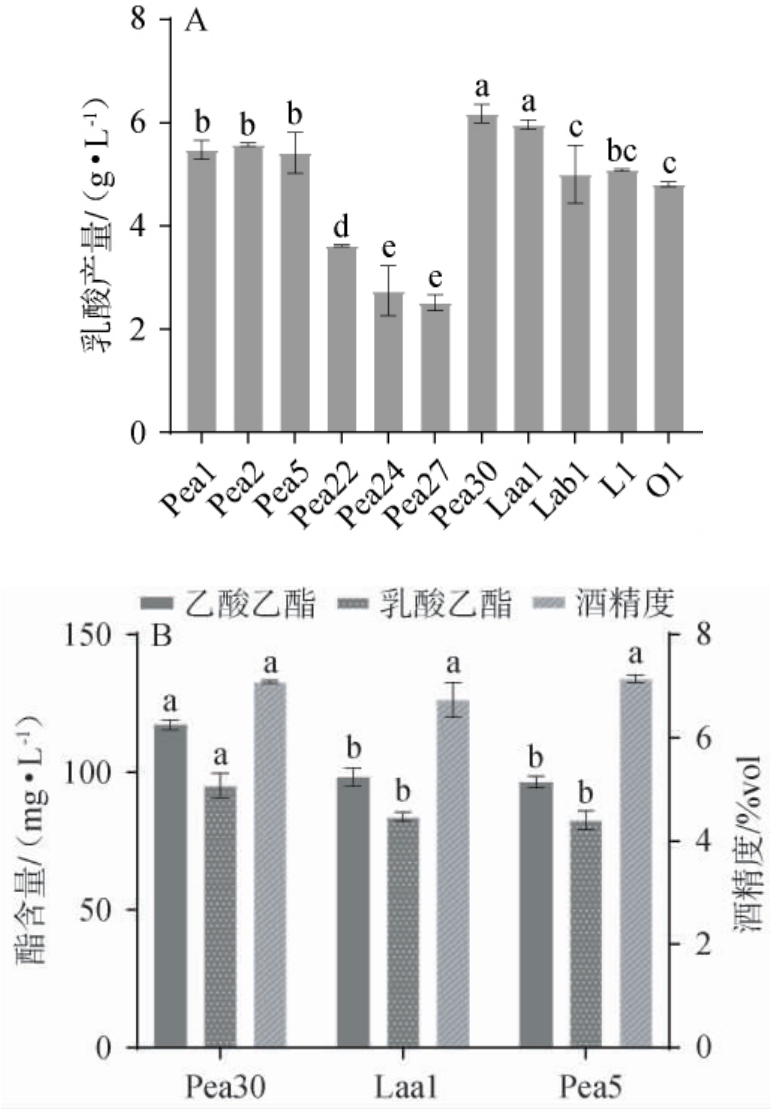
图5 不同乳酸菌发酵乳酸产量(A)、菌株Y6和优良乳酸菌混菌(1∶1)固态发酵酒醅酒精度、乙酸乙酯及乳酸乙酯含量(B)测定结果
Fig.5 Determination results of lactic acid production of different lactic acid bacteria fermentation (A), alcohol content and ethyl acetate and ethyl lactate contents in solid-state fermented grains by mixed strains of Y6 and excellent lactic acid bacteria (1∶1) (B)
由图5B可知,将乳酸菌Pea30、Pea5、Laa1分别与酿酒酵母Y6 混合(1∶1)固态发酵,其酒醅酒精度分别为7.1%vol、7.2%vol、6.9%vol,均高于酵母单菌发酵,乳酸菌的加入能促进酿酒酵母的生长,提高产酒率。菌株Pea30、Pea5、Laa1与酵母共培养体系下,乙酸乙酯含量分别为95.16 mg/L、117.24 mg/L和82.59 mg/L,乳酸乙酯含量分别为96.5 mg/L、83.82 mg/L和98.24 mg/L,菌株Pea30乙酸乙酯和乳酸乙酯含量均显著高于另两株乳酸菌(P<0.05)。因此,选择乳酸片球菌Pea30为优良乳酸菌。
2.3 菌株Y6与Pea30混菌发酵对酵母菌、乳酸菌生长的影响
通过固定酿酒酵母的接种量,改变乳酸菌的接种量,采用RT-PCR法考察固态发酵过程中酿酒酵母Y6与乳酸片球菌Pea30活菌数的变化,以探究功能菌株之间的相互作用,菌株Y6、菌株Pea30单菌以及菌株Y6与Pea30不同接种比例(1.0∶0.2、1.0∶1.0、1.0∶10.0、1.0∶50.0)混菌发酵对酵母菌、乳酸菌生长的影响,结果见图6。
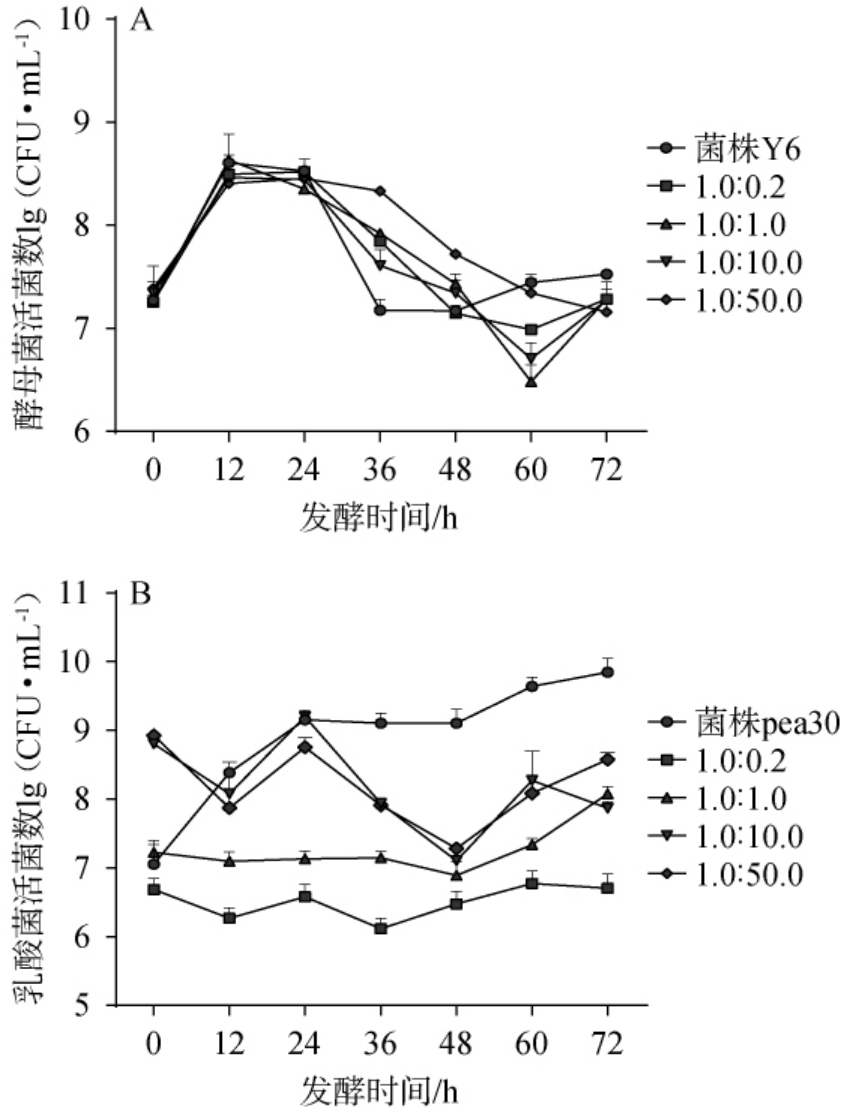
图6 菌株Y6及菌株Pea30单菌及混菌发酵对酵母菌(A)及乳酸菌(B)生长的影响
Fig.6 Effect of single-strain and mixed-strain fermentation of strains Y6 and Pea30 on the growth of yeast (A) and lactic acid bacterium (B)
由图6A可知,接入乳酸片球菌比例增加,菌株Y6活菌数呈先增加后减少再缓慢增加的趋势。发酵前12 h菌株Y6活菌数增长最快,可能酿酒酵母处于对数期生长阶段,此时菌株Pea30接种量的增多对其并没有影响。发酵12~24 h时,酵母菌群达到稳定期。发酵36~72 h时,菌株Y6活菌数快速下降并持续稳定在107 CFU/mL水平。菌株Pea30的加入减缓了酵母菌Y6在24~48 h的衰亡速度,说明菌株Pea30在发酵进程中会代谢生成乳酸及其他有机酸,可缓慢调整体系pH值,为酵母菌Y6营造出更适宜生长的弱酸条件。因此,菌株Pea30产生的代谢产物在一定程度上有助于维持酵母菌活菌数。
由图6B可知,随着接入乳酸片球菌比例增加,菌株Pea30发酵活菌数呈增长的趋势。菌株Pea30单菌发酵72 h时活菌数远高于混合发酵条件下的活菌数。 当菌株Y6和Pea30接种比例为1.0∶0.2、1.0∶1.0时,乳酸片球菌Pea30的生物量大幅度下降,可能是由于混菌体系中菌株Y6和Pea30存在营养竞争,导致乳酸片球菌Pea30营养供给不足,活菌数增长受限。 当菌株Y6和Pea30接种比例为1.0∶10.0、1.0∶50.0时,乳酸片球菌Pea30的生长仍会受到酿酒酵母的抑制,这可能是由于酵母菌产生的乙醇、有机酸等抑制物具有“低浓度即起效”的特性。
综上,与菌株Y6、菌株Pea30单菌发酵比较,混菌发酵时添加菌株Pea30可降低菌株Y6活菌数,添加菌株Y6可提升菌株Pea30活菌数。
2.4 功能菌株接种比例及入池温度对清香型白酒主要风味物质含量的影响
菌株Y6与Pea30不同接种比例(1∶1、1∶5、1∶10、1∶15)及入池温度(22 ℃、26 ℃、30 ℃、34 ℃)对清香型白酒主要酯类(乙酸乙酯、乳酸乙酯)和醇类(异丁醇、异戊醇、苯乙醇和正丙醇)含量的影响,结果见图7。 由图7A可知,菌株Y6和菌株Pea30接种比例为1∶1、1∶5、1∶10、1∶15时,清香型白酒乙酸乙酯含量依次为117.24 mg/L、126.30 mg/L、108.04 mg/L、109.61 mg/L,在菌株Y6与菌株Pea30接种比例为1∶5时,乙酸乙酯含量最高。菌株Y6与菌株Pea30不同接种比例下,乳酸乙酯含量在54.35~58.31 mg/L之间,无显著性差异(P>0.05),表明不同接种比例下产乳酸乙酯能力未受显著影响。除菌株Y6与菌株Pea30比例为1∶15外,醇类(异丁醇、异戊醇、苯乙醇和正丙醇)含量相差不大。 综合考虑,确定酿酒酵母Y6与乳酸片球菌Pea30接种比例为1∶5。
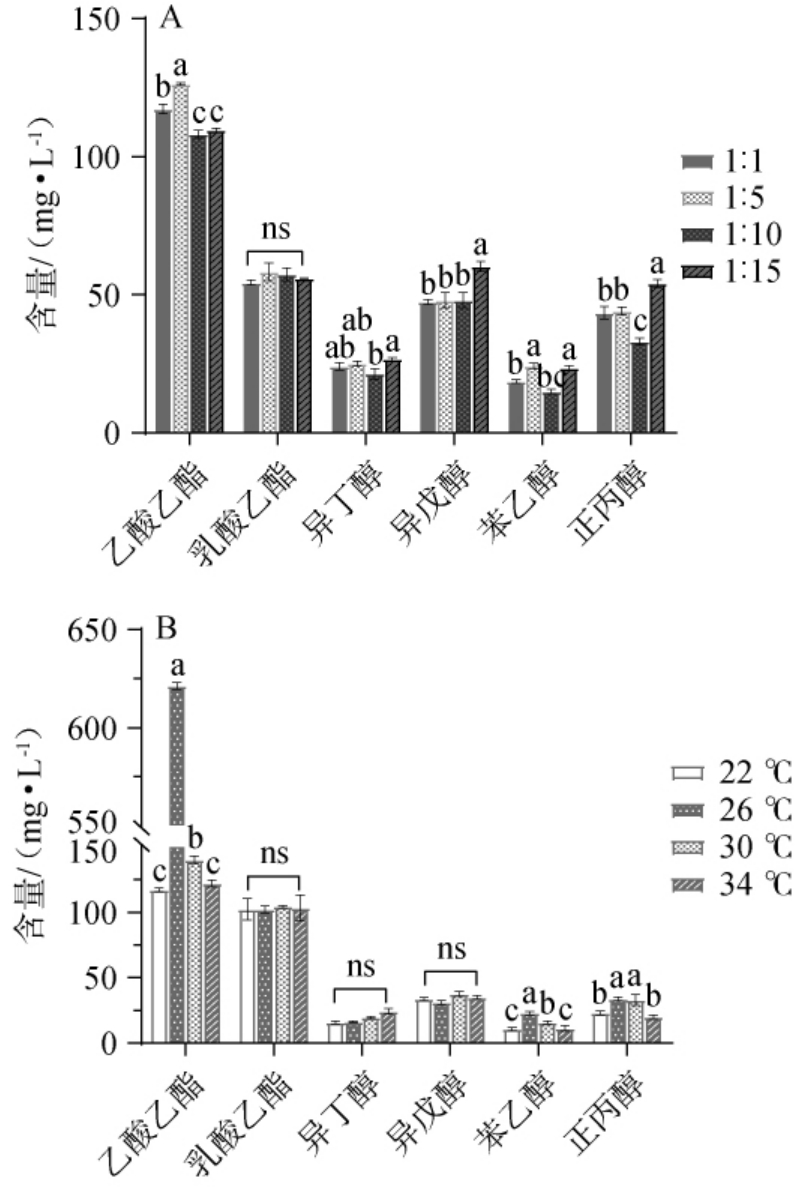
图7 菌株Y6与菌株Pea30不同接种比例(A)及入池温度(B)对清香型白酒主要酯类和醇类含量的影响
Fig.7 Effect of different inoculation proportion of strains Y6 and Pea30 (A) and loading temperature (B) on main esters and alcohols contents of light-flavor Baijiu
“ns”表示无显著差异(P>0.05)。
白酒固态发酵可通过控制入池温度来控制发酵的温度,通常采用低温入窖的方法,低温可以保证酿酒酵母的活力,加强耐酒精能力,且酶类不会受到破坏[26]。 由图7B可知,随着入池温度的升高,乙酸乙酯含量呈先升高后降低的趋势,入池温度为26 ℃时,乙酸乙酯含量达到最高(621.3 mg/L),推测26 ℃可能为菌株Y6最适生长与代谢温度,有利于乙醇和乙酸的生成,从而促进乙酸乙酯的合成。乳酸乙酯含量在不同入池温度下无显著性差异(P>0.05),为102 mg/L。因此,确定入池温度为26 ℃。
综上,酿酒酵母Y6和乳酸片球菌Pea30接种比例为1∶5,入池温度为26 ℃。在此优化条件下,乙酸乙酯含量达到621.3 mg/L,乳酸乙酯含量达到102 mg/L,异丁醇、异戊醇、苯乙醇和正丙醇含量分别为16.4 mg/L、31 mg/L、23 mg/L和34 mg/L。
2.5 功能菌株添加对清香型白酒酒醅发酵过程中理化指标的影响
以不添加功能菌株发酵的清香型白酒酒醅为对照(CK),分析酿酒酵母Y6和乳酸菌Pea30的加入对清香型白酒酒醅发酵过程中理化指标的影响,结果见图8。含水量的变化会影响微生物群落的结构和演替,从而影响白酒产品的产量和质量[27]。由图8A可知,两个发酵组含水量动态变化一致,呈上升的趋势,发酵前的酒醅水分都为55%,发酵后期都维持在58%左右。由图8B可知,CK组的还原糖含量在第1天迅速升高,ZJ组在发酵前期还原糖含量有少量增多,在发酵过程中,微生物分解原料中大分子产生还原糖,使还原糖含量增多。 之后还原糖又被微生物本身用于生长、繁殖和新陈代谢[28],还原糖含量不断下降。随着ZJ组发酵环境中微生物组成逐渐丰富,微生物还原糖消耗量逐渐增多,即菌剂的加入提高了还原糖的利用率。由图8C可知,发酵过程中淀粉水解为还原糖,进一步转化为乙醇和各种风味物质,淀粉含量均呈现整体下降的趋势,发酵至末期淀粉含量为10.44%~12.06%。由图8D可知,随着发酵的进行总酸含量逐渐升高,其中ZJ组发酵后期总酸含量达到0.98 g/kg。由图8E可知,乳酸含量在前期基本保持稳定,后期不断积累,含量迅速增多。 在发酵结束时ZJ组的乳酸含量最高(20.77 mg/L)。由图8F可知,乙酸含量先增加后下降,可能发酵后期乙酸参与乙酸酯的合成。ZJ组因为接入功能菌株,其发酵结束时酒醅中的乳酸、乙酸和总酸含量分别为20.77 mg/L、1.84 mg/L和0.98 mg/L,均高于对照。 综上,在清香型白酒酒醅发酵过程中添加了功能菌株后理化指标的含量和变化趋势都发生了改变,功能菌株的加入提高了还原糖利用率,促进了淀粉的高效转化,使发酵更彻底。同时显著增加了乳酸、乙酸及总酸含量。这些变化有助于酯类风味物质的生成,提升酒体香气和口感协调性,从而改善清香型白酒的整体品质。
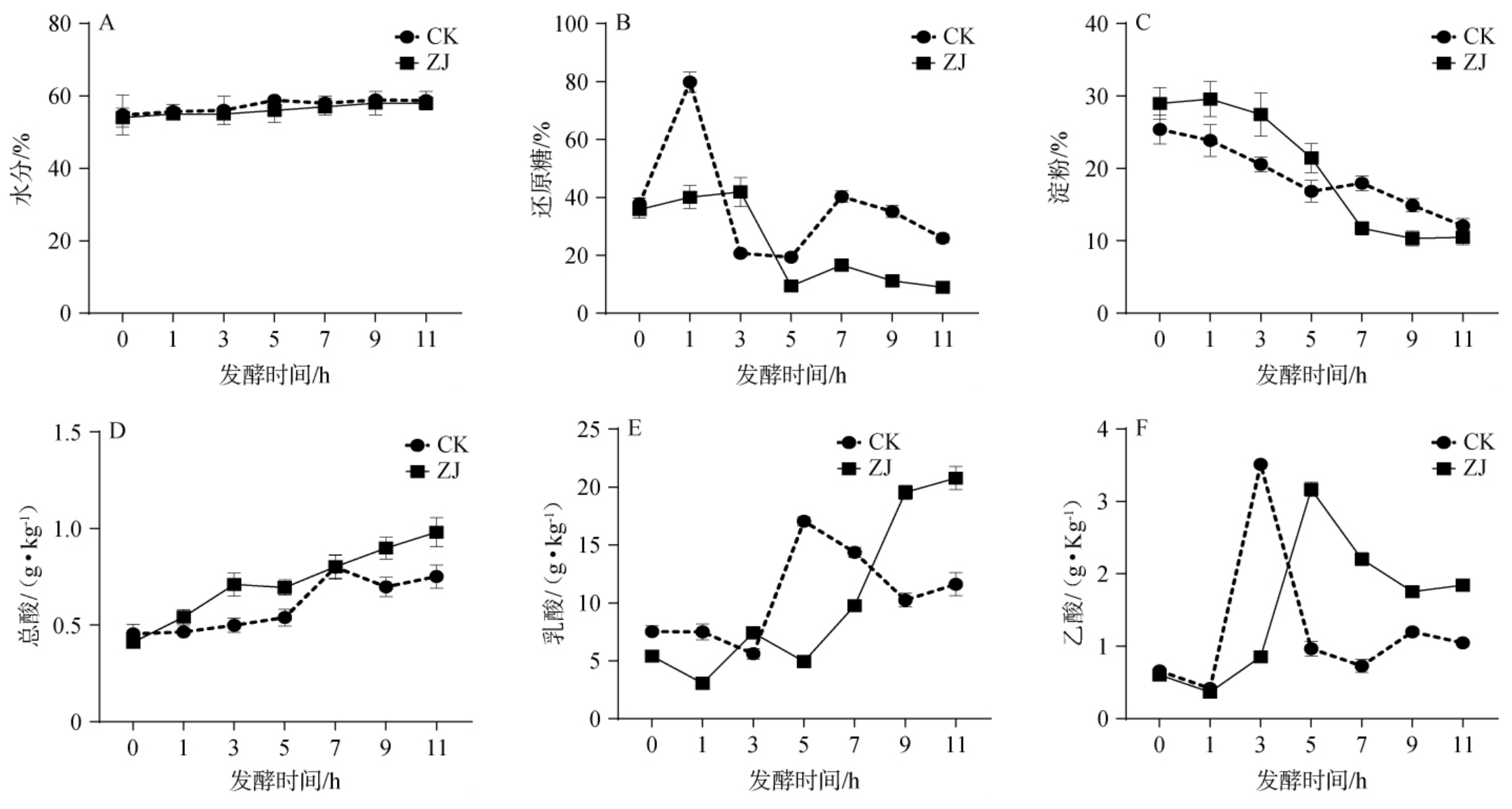
图8 清香型白酒酒醅发酵过程中理化指标变化
Fig.8 Changes of physicochemical indexes of fermented grains of light-flavor Baijiu during fermentation process
A:水分;B:还原糖;C:淀粉;D:总酸;E:乳酸;F:乙酸。
2.6 功能菌株添加对清香型白酒挥发性风味物质的影响
采用HS-SPME-GC-MS对功能菌株强化后的清香型白酒基酒中挥发性风味物质含量进行分析,对清香型白酒基酒中不同种类风味物质的数量和含量及主要酯类和醇类含量比较,结果见图9。 由图9A可知,所有样品中共检测出64种挥发性风味物质,包括35种酯类、13种醇类、5种酸类、6种醛酮类、5种酚类。CK组共检测出45种挥发性风味成分,包括25种酯类、10种醇类、3种酸类、3种醛酮类、4种酚类,ZJ组共检测出50种挥发性风味物质,包括29种酯类、8种醇类、4种酸类、5种醛酮类、4种酚类。
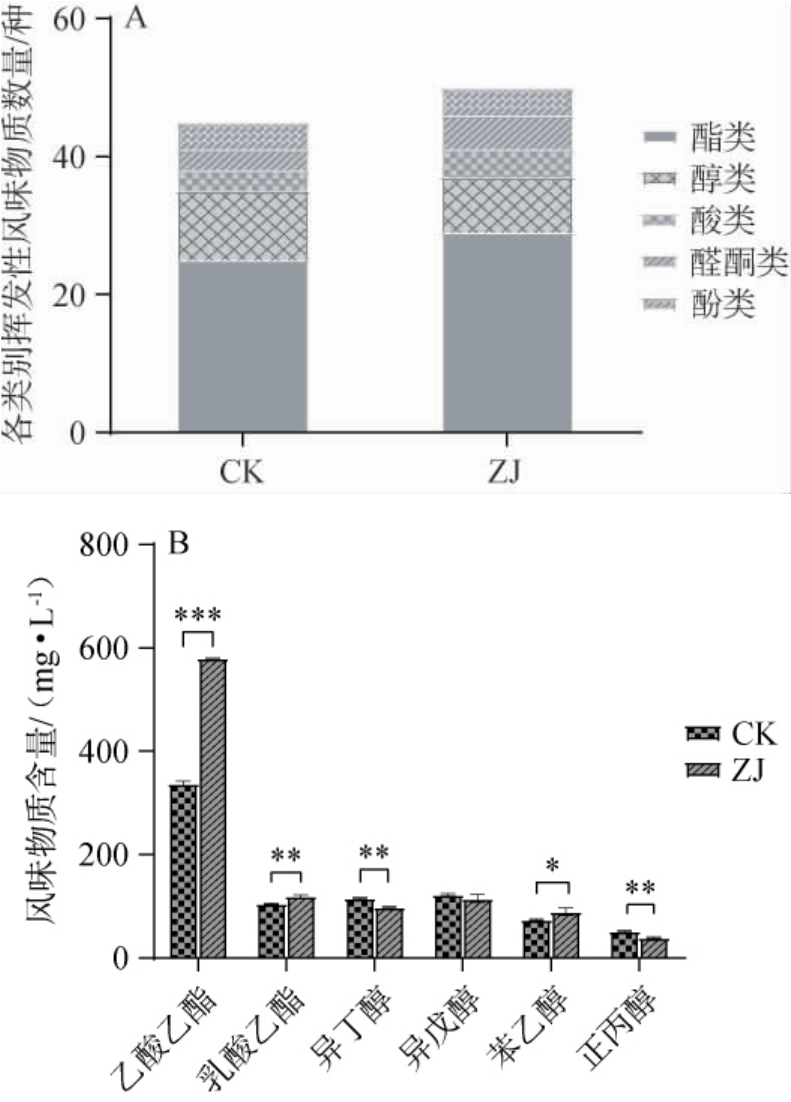
图9 清香型白酒基酒中各类别挥发性风味物质的数量(A)及主要酯类和醇类含量比较(B)
Fig.9 Quantity of various categories volatile flavor substances in base liquor of light-flavor Baijiu (A) and comparison of the contents of main esters and alcohols (B)
“*”表示差异显著(P<0.05),“**”表示差异极显著(P<0.01),“***”表示差异高度显著(P<0.001)。
由图9B可知,两个发酵组清香型白酒基酒中主要酯类和醇类挥发性风味物质含量存在显著差异。与CK组相比,ZJ组乙酸乙酯含量为596 mg/L,高度显著提高了71.9%(P<0.001);ZJ组乳酸乙酯含量为118mg/L, 极显著提高了13.5%(P<0.01);ZJ组苯乙醇含量为90 mg/L, 显著提高了21%(P<0.05);ZJ组异丁醇和正丙醇含量分别为99 mg/L、39 mg/L,极显著降低了14%、25%(P<0.01)。 同时四种高级醇总含量低于CK,降低了5.9%,高级醇含量得到有效控制。相关研究表明,乳酸菌是酸的主要生产者[29],而酿酒酵母是酯类物质的主要生产者之一,故添加这两种微生物可一定程度上促进乙酸乙酯、乳酸乙酯的生成。 高级醇是清香型白酒中不可或缺的风味成分, 作为白酒中重要的风味组分,对酒体的香气和口感具有显著贡献,但其对人体健康存在潜在影响。 与乙醇相比,高级醇具有更强的毒性和麻醉作用,在人体内的代谢速率较慢,滞留时间较长,导致对神经系统的刺激作用更为持久。 因此,过量摄入高级醇可能引发一系列不良反应, 对人体健康构成潜在风险,故适当降低白酒中的高级醇含量具有重要意义。因此,ZJ组添加酿酒酵母Y6和乳酸片球菌Pea30后的清香型白酒的风味得到了很大的改善。
2.7 功能菌株对酒醅微生物群落组成的影响
Alpha多样性可以反映样品中的物种多样性。通常使用Shannon指数来评价物种的多样性,Chao 1指数一般用来表示物种的丰富度[30]。功能菌株对酒醅微生物群落组成的影响结果见表2。由表2可知,细菌群落方面,CK组Chao1指数在发酵中前期(0~7 d)呈下降趋势,发酵后期(7~11 d)呈上升趋势;ZJ组Chao1指数在发酵中前期呈先降低后升高的趋势,发酵后期呈上升趋势。CK组Shannon指数和Chao 1指数变化趋势相同,呈先降低后升高的趋势,ZJ组Shannon指数在发酵前期(0~3 d)呈下降趋势,发酵中期(3~7 d)呈上升趋势,发酵后期(7~11 d)呈下降趋势。由表2亦可知,真菌群落方面,CK组Chao1指数总体呈下降的趋势,ZJ组Chao1指数呈先降低后升高的趋势。 CK组Shannon指数整体呈下降趋势,ZJ组Shannon指数基本稳定。综上,与CK组相比,ZJ组酒醅的微生物多样性和丰富度发生了变化,意味着添加酿酒酵母和乳酸片球菌对细菌和真菌群落组成均有显著的影响[29]。
表2 清香型白酒酒醅发酵过程中细菌和真菌Alpha多样性分析结果
Table 2 Analysis results of Alpha diversity of bacteria and fungi of fermented grains of light-flavor Baijiu during fermentation process
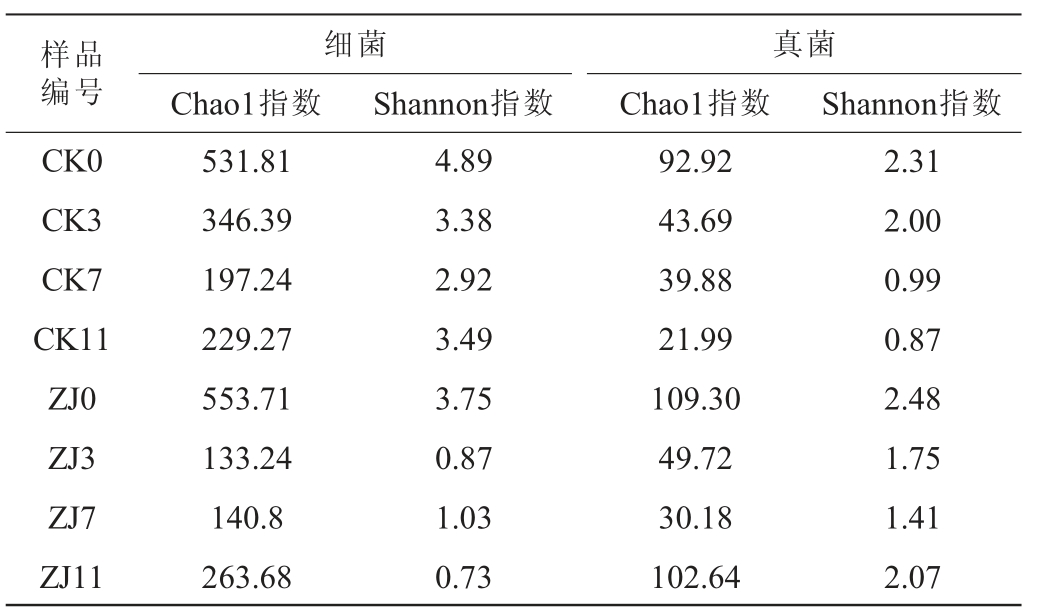
样品编号CK0 CK3 CK7 CK11 ZJ0 ZJ3 ZJ7 ZJ11细菌Chao1指数Shannon指数真菌Chao1指数 Shannon指数531.81 346.39 197.24 229.27 553.71 133.24 140.8 263.68 4.89 3.38 2.92 3.49 3.75 0.87 1.03 0.73 92.92 43.69 39.88 21.99 109.30 49.72 30.18 102.64 2.31 2.00 0.99 0.87 2.48 1.75 1.41 2.07
白酒发酵是微生物相互作用的过程,其共同决定白酒的质量[9]。基于皮尔逊相关系数(|r|>0.6)和P<0.05绘制了酒醅样品发酵过程中细菌属和真菌属间的相关性共现网络图,结果见图10。由图10可知,CK组共有109个节点和431条边,正相关占85.71%,负相关占14.29%。ZJ组共有113个节点和430条边,正相关占91.12%,负相关占8.88%。由图10A可知,CK组酿酒酵母属(Saccharomyces)与毕赤酵母属(Pichia)呈负相关,片球菌属(Pediococcus)与曲霉属(Aspergillus)、乳杆菌属(Lactobacillus)呈负相关,说明在传统发酵体系中存在一定的竞争或抑制关系。由图10B可知,ZJ组酿酒酵母属(Saccharomyces)与赤霉属(Gibberella)、嗜热子囊菌属(Thermoascus)、横梗霉属(Lichtheimia)等关键属呈正相关,片球菌属(Pediococcus)与毕赤酵母属(Pichia)、芽孢杆菌属(Bacillus)、毛霉属(Mucor)呈正相关,说明功能菌株强化了微生物间的正向互作,可能通过调节微生物群落结构,促进了微生物之间的协同代谢。与CK组相比,ZJ组芽孢杆菌属(Bacillus)、棒状杆菌属(Corynebacterium)、根霉属(Rhizopus)等占比增加,说明共现性网络模型中组成成分发生改变。 结果表明,添加功能菌株后微生物之间的正相关性增强,属间相互作用的复杂性增加,使酿酒微生态环境中微生物结构重组,改变菌株间的相互作用,核心微生物之间相互作用增强,菌群更稳定。

图10 清香型白酒酒醅中细菌属(A)及真菌属(B)间的共现性网络分析结果
Fig.10 Co-occurrence network analysis results of bacteria genus (A)and fungi genus (B) in fermented grains of light-flavor Baijiu
红点代表细菌,蓝点代表真菌,红线表示呈正相关,蓝线表示呈负相关。
3 结论
本研究通过筛选性状优良酿酒酵母和乳酸片球菌,优化其接种比例和入池温度,进一步分析对清香型白酒酿造风味及微生物群落的影响。 结果表明,酿酒酵母Y6具有优良的产酒精和产酯能力,乳酸片球菌Pea30不仅耐酒精能力强,还能显著提升乳酸和酯类物质的生成。 菌株Y6与菌株Pea30接种比为1∶5(酵母菌接种量为1.0×107CFU/mL,乳酸菌接种量5.0×107CFU/mL)、入池温度为26 ℃,发酵时间为11 d条件下,酒醅中乙酸乙酯、乳酸乙酯含量分别为621.3 mg/L、102 mg/L,分别比对照显著提高了71.9%、13.5%(P<0.05)。此外,将筛选的酵母菌及乳酸菌功能菌株应用于清香型白酒酿造,酒醅中还原糖利用率提高,淀粉转化更彻底,总酸、乳酸和乙酸含量显著上升,强化功能菌株清香型白酒基酒中共检测出50种挥发性风味成分,其中乙酸乙酯、乳酸乙酯、苯乙醇含量分别为596 mg/L、118 mg/L、90 mg/L,分别比对照提高了71.9%、13.5%、21%;异丁醇和正丙醇含量分别为99 mg/L、39 mg/L,分别比对照降低了14%、25%。微生物群落共现性网络分析结果显示,功能菌株应用后微生物群落多样性与互作关系发生显著变化,正向协同增强,核心菌群结构更稳定,有利于提升发酵效率与白酒品质。综上,酿酒酵母Y6与乳酸片球菌Pea30的协同应用,不仅能优化发酵过程,还能显著提升清香型白酒的品质与风味特征,为优质白酒生产提供了科学依据和技术支持。
[1]WANG L.Research trends in Jiang-flavor Baijiu fermentation:From fermentation microecology to environmental ecology[J].J Food Sci,2022,87(4):1362-1374.
[2]JENG K,CHEN C,FANG Y.Effect of microbial fermentation on content of statin,GABA,and polyphenols in Pu-Erh tea[J].J Agr Food Chem,2007,55(21):8787-8792.
[3]李兵,张超,王玉霞,等.白酒大曲功能微生物与酶系研究进展[J].中国酿造,2019,38(6):7-12.
[4]ZHANG L,HUANG J,ZHOU R,et al.Evaluating the feasibility of fermentation starter inoculated with Bacillus amyloliquefaciens for improving acetoin and tetramethylpyrazine in Baoning bran vinegar[J].Int J Food Microbiol,2017,255:42-50.
[5]应超,任志强,曾波,等.大曲耐热细菌富集及其在小曲白酒中的应用[J].现代食品科技,2024,40(4):64-72.
[6]田殿梅,秦辉,黄荣,等.复配浓香大曲对安琪小曲酿酒的影响研究[J].中国酿造,2022,41(8):121-126.
[7]张家辉,海超,陈国刚.伊力特浓香型大曲中优良霉菌的筛选鉴定及其麸曲制曲工艺研究[J].中国酿造,2024,43(8):93-99.
[8]DU R,WU Q,XU Y.Chinese liquor fermentation: identification of key flavor-producing Lactobacillus spp.by quantitative profiling with indigenous internal standards[J].Appl Environ Microbiol, 2020, 86(12):e00456-20.
[9]SONG Z,DU H,ZHANG Y,et al.Unraveling core functional microbiota in traditional solid-state fermentation by high-throughput amplicons and metatranscriptomics sequencing[J].Front Microbiol,2017,8:1294.
[10]CHEN G, CHEN C, LEI Z.Meta-omics insights in the microbial community profiling and functional characterization of fermented foods[J].Trends Food Sci Tech,2017,65(1):23-31.
[11]HE G Q,DONG Y,HUANG J,et al.Alteration of microbial community for improving flavor character of Daqu by inoculation with Bacillus velezensis and Bacillus subtilis[J].LWT-Food Sci Technol,2019,111:1-8.
[12]FAN G S,TENG C,XU D,et al.Enhanced production of ethyl acetate using co-culture of Wickerhamomyces anomalus and Saccharomyces cerevisiae[J].J Biosci Bioeng,2019,128(5):564-570.
[13]QIU F, LI W, CHEN X, et al.Targeted microbial collaboration to enhance key flavor metabolites by inoculating Clostridium tyrobutyricum and Saccharomyces cerevisiae in the strong-flavor Baijiu simulated fermentation system[J].Food Res Int,2024,190:114647-114647.
[14]HUANG X N, FAN Y, MENG J, et al.Laboratory-scale fermentation and multidimensional screening of lactic acid bacteria from Daqu[J].Food Biosci,2021,40(6):100853.
[15]唐涛.浓香型白酒大曲中酵母菌的分离鉴定及强化大曲的制备[D].邯郸:河北工程大学,2023.
[16]杜辉,杨芳,郭桂梅,等.清香型白酒发酵过程中理化指标变化规律及其相关性分析[J].酿酒科技,2025(6):38-40,44.
[17]谢再斌,常煦,何国庆,等.清香型白酒酿造过程中功能微生物及应用研究[J].中国酿造,2024,43(7):27-32.
[18]刘迪,吕高奇,杨磊,等.高粱与清香型白酒中氨基甲酸乙酯含量的关系[J].中国酿造,2024,43(6):108-114.
[19]王冬,王涛.清香型大曲白酒工艺研究[J].食品工程,2023(4):38-39,52.
[20]雒晓玲.清香型白酒生产工艺探讨[J].食品安全导刊,2023(1):136-138.
[21]马世源,李子健,罗惠波,等.酿酒酵母对浓香型白酒酒醅微生物群落结构及功能的影响[J].中国食品学报,2024,24(2):71-82.
[22]LIU H L, SUN B G.Effect of fermentation processing on the flavor of Baijiu[J].J Agr Food Chem,2018,66(22):5425-5432.
[23]QIAN Y L,AN Y,CHEN S,et al.Characterization of Qingke liquor aroma from Tibet[J].J Agr Food Chem,2019,67(50):13870-13881.
[24]江威,王路瑶,张宗杰,等.清香型小曲白酒酒醅中乳酸菌的筛选鉴定及其发酵特性研究[J].中国酿造,2022,41(8):57-63.
[25]赵欣怡.清香型白酒酿造过程乳酸含量和细菌菌群结构动态解析[D].无锡:江南大学,2023.
[26]高林峰,汤庆莉,吴天祥.麸曲酱香型白酒发酵过程控制条件的优化[J].酿酒科技,2011(12):40-43.
[27]LI Q,DU B,CHEN X,et al.Microbial community dynamics and spatial distribution of flavor compound metabolism during solid-state fermentation of Baijiu enhanced by Wickerhamomyces anomalus[J].Food Biosci,2024,59(6):103925-103934.
[28]ZHAO C,SU W,MU Y C,et al.Correlations between microbiota with physicochemical properties and volatile flavor components in black glutinous rice wine fermentation[J].Food Res Int,2020,138:109800.
[29]TOMISLAV P, MARIE-BERNADETTE M, AURÉLIE L, et al. Lactobacillus and Leuconostoc volatilomes in cheese conditions[J].Appl Microbiol Biot,2016,100(5):2335-2346.
[30]田德雨.梨粮共酵蒸馏酒发酵制备的研究[D].石家庄:河北科技大学,2021.