茶酒是茶叶与酿酒原料混合发酵,或茶叶提取物与白酒配制而成的具有茶风味的饮料酒,可分为蒸馏型、发酵型、露酒型、配制型等类型[1]。茶酒富含茶叶活性成分,因而具有调节体内代谢、预防心血管疾病、抗氧化和抗衰老、抑制肥胖等功效[2-4],深受人们喜爱的同时,也吸引了众多研究人员的关注。 陈顺心等[5-7]分别对信阳毛尖茶酒、普洱茶酒、红茶酒进行了工艺研究和品质特征分析。 然而,对茶酒制造过程中糖含量变化和产品糖含量的关注度较低,也缺乏茶酒中糖含量的相关指标规定。目前,酒类产品中糖含量检测方法包括酶法[8]、滴定法[9]、分光光度法[10]、液相色谱法[11]、离子色谱法[12]等,但上述方法检测的糖类范围有限,不能完全解析茶酒发酵过程及成品中糖含量的变化。因此,建立一种茶酒中糖类物质的检测方法,对于提升茶酒制备工艺和产品品质具有重要意义。
液相色谱法常用于糖类物质的检测,糖类物质无紫外吸收,多采用示差折光检测器(refractive index detector,RID)、蒸发光散射检测器(evaporativelightscatteringdetector,ELSD)等检测[11,13]。RID操作简单快捷,但基线噪音大,检出限低,能同时检测的糖类组分有限[14]。ELSD灵敏度高,但平衡时间长,且氨基酸等干扰严重。因此,为克服上述问题,大量研究者开始将糖衍生后再用紫外或荧光检测器测定[15-16]。衍生液相色谱法分为柱前衍生和柱后衍生,柱前衍生法测定糖含量常采用1-苯基-3-甲基-5-吡唑啉酮(1-phenyl-3-methyl-5-pyrazolone,PMP)作衍生剂,生成性质稳定的PMP-单糖衍生物,在波长250 nm处有较强吸收,可用紫外检测器检测[15]。PMP衍生需手动进行,衍生产物需采用氯仿萃取除杂,且无法直接检测蔗糖等非还原糖,具有一定局限性。柱后衍生液相色谱常用于氨基酸、氨基甲酸酯农药的检测[14]。 柱后衍生环节在反应器中自动完成,操作简单,重现性好,但柱后衍生测糖的研究相对较少。有采用1-萘硼酸柱后衍生液相色谱测定饮料和蜂蜜中单糖的报道[16],但需在特定的pH下进行,流动相的选择范围较窄。韩晶等[17]采用磷酸-苯肼柱后衍生测定饮料中的多种糖组分,需同时使用高浓度磷酸和中等毒性的苯肼试剂,限制了其使用。因此,基于柱后衍生液相色谱法测定糖含量的方法还有待进一步研究。
绝大部分糖分子含有大量邻二醇结构,而在糖化学研究中,高碘酸或高碘酸钠可氧化具有邻二醇结构的物质,因此,人们常用高碘酸或高碘酸钠探究糖的结构[18]。在特定条件下,高碘酸可氧化糖类物质生成甲醛、甲酸等[19]。甲醛与酚试剂(3-甲基-2-苯并噻唑啉酮腙盐酸盐水合物)在温和条件下反应形成嗪,嗪与酚试剂的氧化产物反应生成青蓝色化合物,该化合物在波长630~670 nm处有最大吸收[20-21]。 因此,本研究拟建立一种液相色谱分离、柱后高碘酸氧化与酚试剂衍生显色、紫外检测器检测的糖类物质(果糖、葡萄糖和蔗糖)含量测定方法,以期为茶酒的工艺研究、产品开发和品质提升提供新的检测技术支持。
1 材料与方法
1.1 材料与试剂
11个茶酒样品:蒸馏型茶酒样品1个—铁观音茶酒;发酵型茶酒样品1个—白茶酒;露酒型茶酒样品3个—普洱茶酒、龙井茶酒、茉莉花茶酒;配制型茶酒样品6个—玄米茶配制酒、红茶金酒配制酒、黄山毛峰茶配制酒、西湖龙井茶配制酒、云雾绿茶配制酒、茉莉花茶配制酒:市售。
乙腈(色谱纯):成都市科隆化学品有限公司;高碘酸、酚试剂、磷酸、果糖、葡萄糖、蔗糖标准品(纯度≥99.9%):上海麦克林生化科技股份有限公司。
1.2 仪器与设备
LC-16液相色谱仪、316L不锈钢反应线圈(10 m×1/16英寸,内径0.3 mm):岛津仪器(苏州)有限公司;Asahipak NH2P-50 4E色谱柱(250 mm×4.6 mm,5 μm):日本昭和电工株式会社;Vector PCX柱后衍生仪:美国Pickering Laboratories公司;101-0BS 电热恒温烘箱:绍兴市尚诚仪器制造有限责任公司;Cary 60 UV-Vis分光光度计:美国安捷伦科技有限公司。
1.3 方法
1.3.1 标准工作溶液及试剂的配制
分别准确称取90 ℃下干燥2 h的果糖0.500 0 g、葡萄糖0.500 0 g、蔗糖0.500 0 g,置于50 mL容量瓶中,加入少量超纯水溶解后,定容、摇匀,得到果糖、葡萄糖和蔗糖质量浓度均为10.0 mg/mL的标准储备液,置于4 ℃冰箱中。使用前稀释成系列糖标准工作溶液。
流动相:将乙腈和水按照75∶25(V/V)混合,添加0.5%H3PO4搅拌均匀,使用前过0.45 μm滤膜,超声脱气。
衍生剂A(2.0~5.0 g/L高碘酸):称取2.0 g、3.0 g、4.0 g、5.0 g高碘酸,分别用1.0 L超声脱气后的超纯水溶解,过0.45 μm滤膜后置于棕色试剂瓶中,待用。
衍生剂B(1.0~2.5 g/L酚试剂):称取1.0 g、1.5 g、2.0 g、2.5 g酚试剂,分别用1.0 L超声脱气后的超纯水溶解,过0.45 μm滤膜后置于棕色试剂瓶中,待用。
1.3.2 样品前处理
蒸馏型茶酒直接过0.45 μm滤膜后上机检测;其余茶酒视配料表情况处理,未添加糖的直接过0.45 μm滤膜后上机检测,添加糖的用超纯水稀释100~1 000倍,过0.45 μm滤膜后上机检测。
1.3.3 柱后衍生系统的改造
基于柱后衍生液相色谱法测定糖含量的工作过程如图1所示。
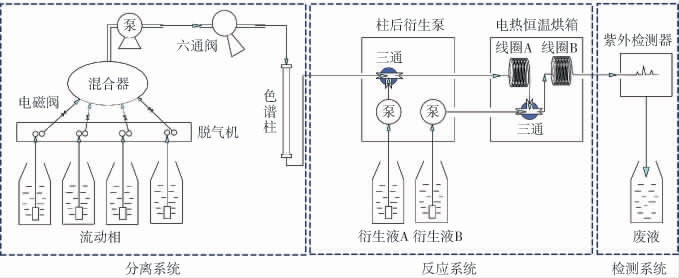
图1 柱后衍生液相色谱法检测糖类物质含量工作过程示意图
Fig.1 Schematic diagram of the working process of post-column derivatization liquid chromatography for detecting carbohydrates
该工作系统由分离系统、反应系统和检测系统组成,其中分离系统和检测系统均由岛津LC-16液相色谱仪组成,而反应系统由Vector PCX柱后衍生仪、电热恒温烘箱和两段10 m长的不锈钢反应线圈组成。 对Vector PCX柱后衍生仪进行改造,色谱柱后的管路、衍生液A的管路连接在Vector PCX柱后衍生仪的三通上,然后连接放置于烘箱中的不锈钢反应线圈A,反应线圈A末端和衍生液B的管路通过不锈钢三通与烘箱中的反应线圈B相连,经过反应后的液体进入紫外检测器检测。
1.3.4 色谱及柱后衍生反应条件
色谱分离条件参考文献[11]的方法并稍作修改:Asahipak NH2P-50 4E色谱柱(250 mm×4.6 mm,5 μm);流动相:含0.5%H3PO4乙腈-水(75∶25,V/V);流速:0.8mL/min;柱温:40 ℃;进样量:10 μL;紫外检测器波长:670 nm。在预实验的基础上,确定衍生液A为2.0 g/L高碘酸,流速0.2 mL/min;衍生液B为1.0 g/L酚试剂,流速0.2 mL/min;烘箱温度:120 ℃。
定性定量方法:根据3种糖类物质标准品在色谱图上的保留时间对待测样品进行定性,依据标准曲线回归方程得到茶酒中果糖、葡萄糖、蔗糖含量。计算公式如下:
式中:X为茶酒中待测糖含量,g/L;C为根据外标法得出的待测试液中糖的质量浓度,mg/L;V为样品稀释倍数。
1.3.5 检测条件优化
(1)色谱条件优化
检测波长的确定:分别取1.0 mL果糖、葡萄糖、蔗糖工作液于25 mL具塞试管中,以高碘酸为氧化剂,以酚试剂为显色剂,参考文献[19]的方法进行显色反应,随后分别对3种糖类物质的衍生产物于波长500~800 nm进行扫描,确定最佳检测波长。
流动相的确定:比较流动相乙腈与水不同体积比(V/V)(85∶15、80∶20、75∶25、70∶30、65∶35)对3种目标物的分离效果及峰面积的影响。
流速的确定:比较不同流速(0.8 mL/min、0.9 mL/min、1.0 mL/min、1.1 mL/min)对3种目标物的分离效果及峰面积的影响。
柱温的确定:比较不同柱温(25 ℃、30 ℃、35 ℃、40 ℃)对3种目标物的分离效果及峰面积的影响。
(2)柱后衍生条件优化
自动进样器注入10μL3种糖液混标,在固定衍生剂流速(0.2mL/min)和固定反应线圈长度(10m)的情况下,探究不同高碘酸质量浓度(2.0g/L、3.0g/L、4.0g/L、5.0g/L)、酚试剂质量浓度(1.0g/L、1.5g/L、2.0g/L、2.5g/L)和反应温度(80℃、90℃、100 ℃、110 ℃、120 ℃、130 ℃)对3种目标物峰面积的影响。
1.3.6 方法学考察
(1)标准曲线、检出限、定量限
分别吸取3种糖标准储备液适量,采用超纯水逐级稀释,得到含有果糖、葡萄糖、蔗糖质量浓度均为25.0 mg/L、50.0 mg/L、100.0 mg/L、200.0 mg/L、400.0 mg/L、500.0 mg/L、600.0 mg/L、800.0 mg/L、1 000.0 mg/L系列浓度的混合标准工作溶液,在最优的色谱条件下进行测定,以3种糖的质量浓度(X)为横坐标,峰面积(Y)为纵坐标绘制标准曲线。分别以3种糖色谱峰的3倍和10倍信噪比对应的质量浓度计算检出限、定量限。
(2)精密度与稳定性试验
取一样品经0.45 μm滤膜过滤后,按优化的色谱条件上机连续重复测定6次,计算精密度试验结果的相对标准偏差(relative standard deviation,RSD)。
取6份平行样品经0.45 μm滤膜过滤后分别置于6个进样瓶中, 按优化后的色谱条件, 在36 h内进行6次衍生测试,计算稳定性试验结果的RSD。
(3)加标回收率试验
以已知3种糖含量的茶酒为溶剂,分别按低(果糖25.0 mg/L、葡萄糖150.0 mg/L、蔗糖150.0 mg/L)、中(果糖50.0 mg/L、葡萄糖300.0 mg/L、蔗糖300.0 mg/L)、高(果糖75.0 mg/L、葡萄糖450.0 mg/L、蔗糖450.0 mg/L)3个水平进行加标试验,计算其加标回收率。
1.3.7 数据处理
所有实验均重复测定3次,结果采用“平均值±标准差”表示,采用Origin 2021绘图,采用IBM SPSS 19.0进行差异显著性检验。
2 结果与分析
2.1 检测条件优化
2.1.1 色谱条件优化结果
(1)检测波长的选择
显色反应结果见图2a。由图2a可知,果糖、葡萄糖和蔗糖均可被高碘酸氧化,氧化产物与酚试剂衍生,呈现出青绿色或灰绿色。分别对各种衍生产物进行波长扫描,结果见图2b。由图2b可知,3种糖的衍生物在波长620~670 nm处有强吸收,其中最大吸收峰在670 nm附近,因此,设置液相色谱仪紫外检测器波长为670 nm。

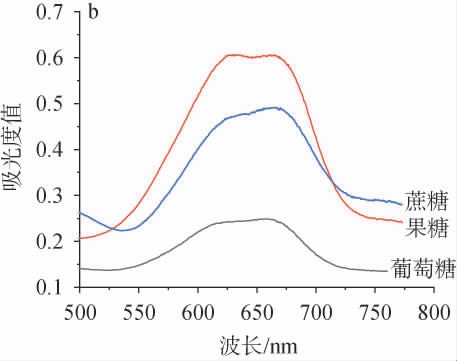
图2 果糖、葡萄糖和蔗糖衍生显色反应结果(a)及衍生产物可见光吸收光谱图(b)
Fig.2 Derivatization color reaction results of fructose, glucose and sucrose (a) and the visible light absorption spectra of their derivatives (b)
(2)流动相比例的优化
在液相分析中,常采用HILIC模式分离检测糖,多使用氨基、酰胺基色谱柱,流动相以乙腈体系为主[12,22]。随着流动相中水相比例的增加,其洗脱能力增强,但分离度降低;反之,洗脱能力减小,分离度增加,但易造成色谱峰展宽和拖尾[22]。 本研究比较了不同体积比的乙腈-水混合液对3种糖的分离效果,结果见图3。由图3可知,当流动相中水相低于30%时,三者可实现分离。当乙腈-水比例为70∶30(V/V)时,三者集中出峰时间在9~12 min之间,分离度有待提升;当乙腈-水比例为85∶15(V/V)时,三者的色谱峰宽明显增大,峰高显著降低,将影响方法的检出限,同时蔗糖出峰时间接近40 min,检测时间过长。综上,从分离效果和节约试剂等角度出发,确定流动相中乙腈与水最佳比例为75∶25(V/V)。
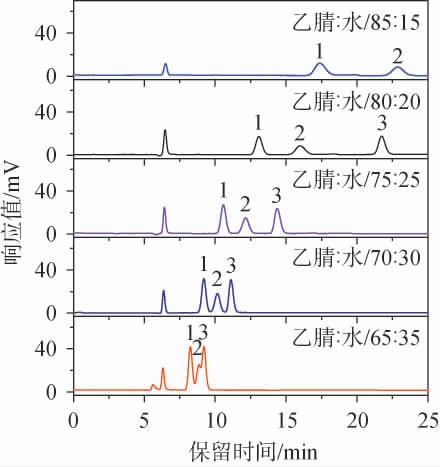
图3 不同流动相比例对果糖、葡萄糖和蔗糖分离效果的影响
Fig.3 Effect of different mobile phase ratios on separation effect of fructose, glucose and sucrose
1—果糖;2—葡萄糖;3—蔗糖,下同。
(3)流速的优化
流动相流速是影响衍生反应进程的关键因素之一,流速越慢,衍生反应越彻底,衍生产物的信号响应也更稳定,但与此同时导致目标峰的出峰时间延后,分析周期延长,反之增大流速虽加快了实验进程,但有可能造成衍生不完全,实验结果出现偏差[23]。本研究比较了不同流速对3种糖分离效果的影响,结果见图4。 由图4可知,当流速为0.8 mL/min时,各种糖衍生物的峰面积达到最大,且色谱峰型良好,可在20 min内完成分离。因此,确定最佳的流速为0.8 mL/min。
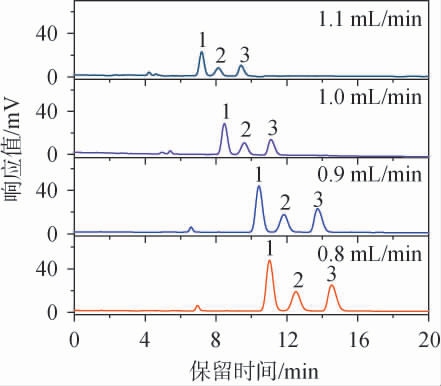
图4 不同流动相流速对果糖、葡萄糖和蔗糖分离效果的影响
Fig.4 Effect of different mobile phase flow rate on separation effect of fructose, glucose and sucrose
(4)柱温的优化
柱温箱温度对糖的分离速度有一定影响,温度过高可能会导致各组分间的分配系数差异减小,分离度下降,温度过低则延长分析时间甚至引起峰形拖尾[23]。本研究比较了不同柱温对3种糖分离效果的影响,结果见图5。由图5可知,在25~40 ℃范围内,适当提高柱温箱温度有利于提高果糖和葡萄糖的分离度,并且可提前出峰。 因此,确定最佳的柱温为40 ℃。
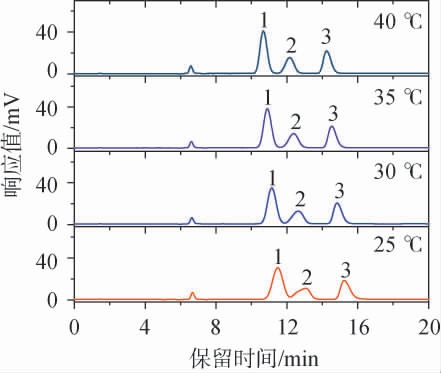
图5 不同柱温对果糖、葡萄糖和蔗糖分离效果的影响
Fig.5 Effect of different column temperature on separation effect of fructose, glucose and sucrose
2.1.2 柱后衍生条件优化结果
高碘酸氧化糖类物质生成甲醛,酚试剂与甲醛反应形成青蓝色络合物的过程,受到反应时间、反应温度以及底物浓度等因素的影响[19]。本研究比较了不同衍生剂质量浓度对3种糖峰面积的影响,结果见图6。 由图6可知,在固定酚试剂质量浓度为1.0 g/L的情况下,随着高碘酸质量浓度在2.0~5.0 g/L范围内增加,3种糖的色谱峰面积逐渐减小,这是过量的高碘酸导致酚试剂发生氧化所致;而当固定高碘酸质量浓度为2.0 g/L时,酚试剂质量浓度增加(1.0~2.5 g/L)对3种糖的峰面积均无显著影响。因此,在本实验中,高碘酸的最佳质量浓度设定为2.0 g/L、酚试剂质量浓度设定为1.0 g/L。
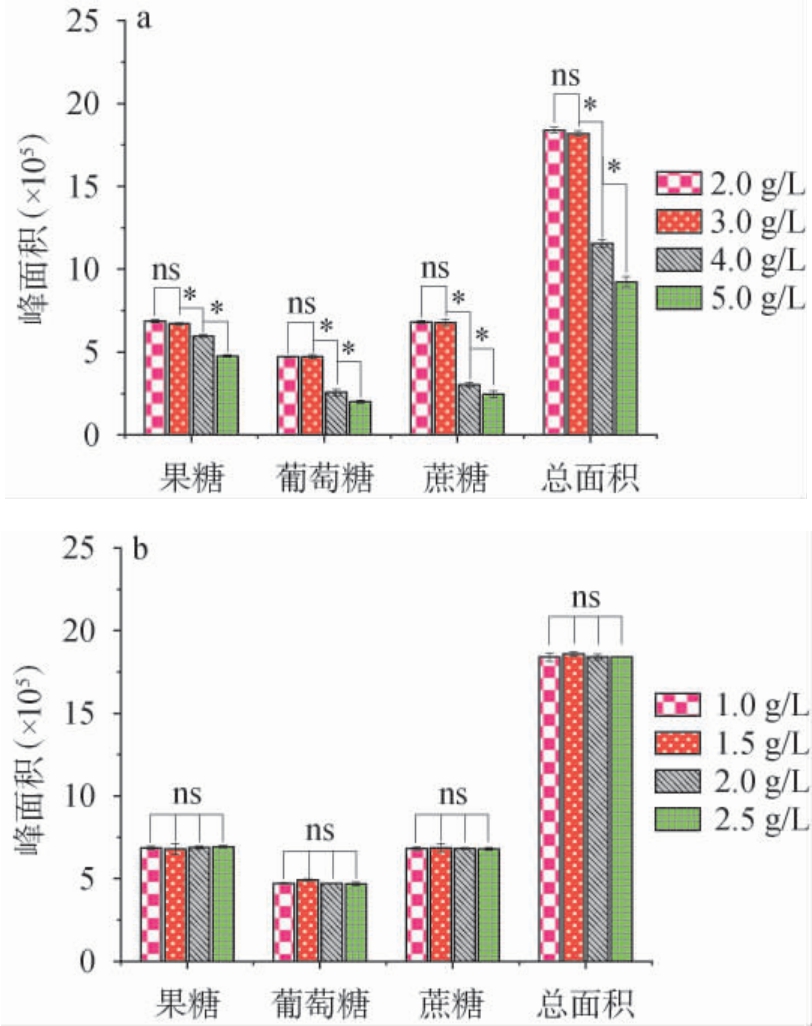
图6 不同高碘酸(a)、酚试剂(b)质量浓度对果糖、葡萄糖和蔗糖色谱峰面积的影响
Fig.6 Effect of different mass concentrations of periodic acid (a)and phenol reagent (b) on the chromatographic peak areas of fructose, glucose and sucrose
“*”表示不同峰面积差异显著(P<0.05);“ns”表示差异不显著(P>0.05)。
进一步分析了衍生反应温度对3种糖类物质峰面积的影响,结果见图7。 由图7可知,随着反应温度的升高,糖类衍生物峰面积先升高后下降,这可能是高温导致糖分子发生了分解所致[18]。 在120 ℃条件下,3种糖衍生物的总峰面积达到最大,因此设定柱后衍生最佳温度为120 ℃。
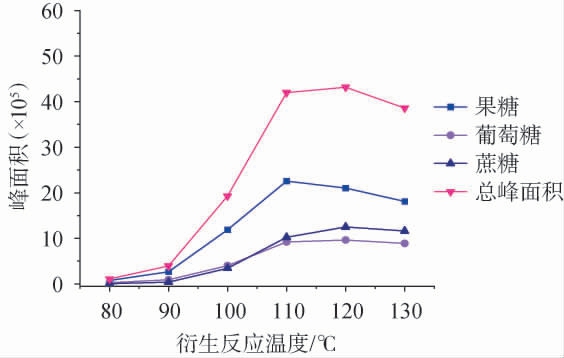
图7 不同衍生反应温度对果糖、葡萄糖和蔗糖色谱峰面积的影响
Fig.7 Effect of different derivative reaction temperature on chromatographic peak areas of fructose, glucose and sucrose
2.2 方法学考察
(1)线性回归方程、检出限及定量限
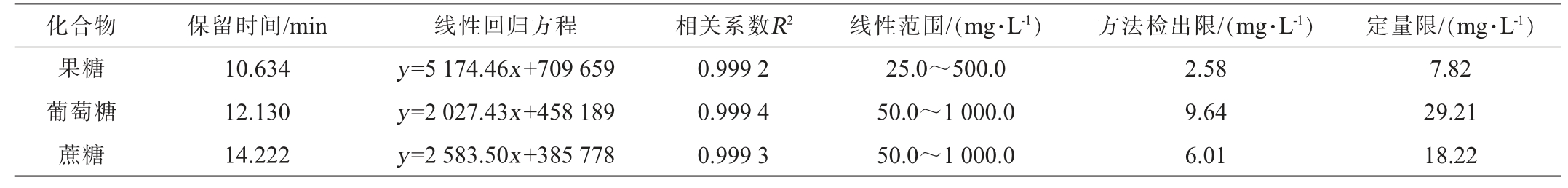
按优化后的色谱条件,对果糖、葡萄糖和蔗糖混合标准工作溶液进行检测分析,结果见表1。 由表1可知,果糖的线性范围为25.0~500.0 mg/L,葡萄糖、蔗糖的线性范围50.0~1 000.0 mg/L,3种糖的线性回归方程相关系数R2均>0.999,说明3种糖的质量浓度和峰面积之间有良好的线性关系。测得果糖、葡萄糖和蔗糖的检出限分别为2.58 mg/L、9.64 mg/L、6.01 mg/L,远低于RID方法的检出限[24-25],定量限分别为7.82 mg/L、29.21 mg/L、18.22 mg/L。
表1 果糖、葡萄糖和蔗糖的线性回归方程、检出限及定量限
Table 1 Linear regression equations, detection limits and quantification limits of fructose, glucose and sucrose
化合物 保留时间/min 线性回归方程 相关系数R2 线性范围/(mg·L-1) 方法检出限/(mg·L-1) 定量限/(mg·L-1)果糖葡萄糖蔗糖10.634 12.130 14.222 y=5 174.46x+709 659 y=2 027.43x+458 189 y=2 583.50x+385 778 0.999 2 0.999 4 0.999 3 25.0~500.0 50.0~1 000.0 50.0~1 000.0 2.58 9.64 6.01 7.82 29.21 18.22
(2)精密度试验结果
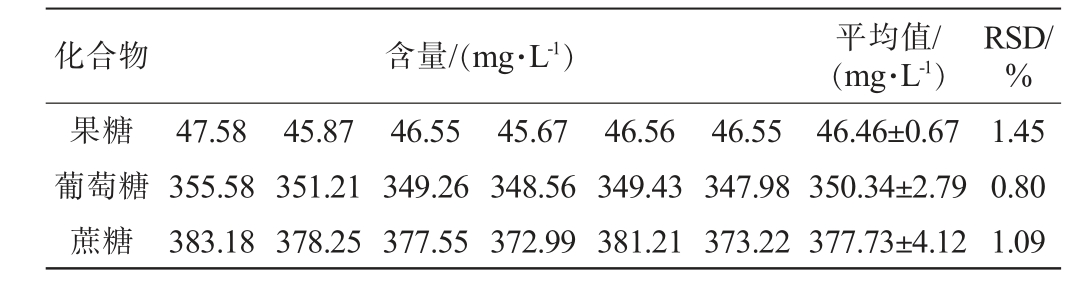
3种糖的精密度试验结果见表2。 由表2可知,果糖、葡萄糖和蔗糖精密度试验结果的RSD分别为1.45%、0.80%和1.09%,均<2.00%,表明该方法的精密度较好。
表2 果糖、葡萄糖和蔗糖精密度试验结果
Table 2 Results of precision tests of fructose, glucose and sucrose
化合物 含量/(mg·L-1) 平均值/(mg·L-1)RSD/%果糖葡萄糖蔗糖47.58 355.58 383.18 45.87 351.21 378.25 46.55 349.26 377.55 45.67 348.56 372.99 46.56 349.43 381.21 46.55 347.98 373.22 46.46±0.67 350.34±2.79 377.73±4.12 1.45 0.80 1.09
(3)稳定性试验结果
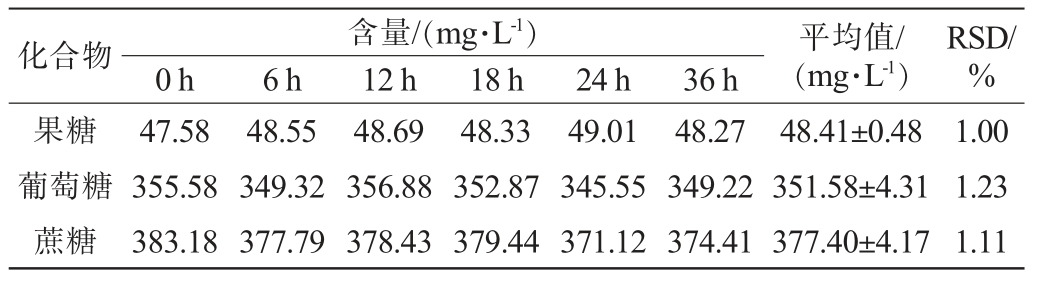
3种糖的稳定性试验结果见表3。 由表3可知,果糖、葡萄糖、蔗糖稳定性试验结果的RSD分别为1.00%、1.23%和1.11%,均<2.00%,表明该方法稳定性良好。
表3 果糖、葡萄糖和蔗糖稳定性试验结果
Table 3 Results of stability tests of fructose, glucose and sucrose
化合物 平均值/(mg·L-1)含量/(mg·L-1)0 h 6 h 12 h 18 h 24 h 36 h RSD/%果糖葡萄糖蔗糖47.58 355.58 383.18 48.55 349.32 377.79 48.69 356.88 378.43 48.33 352.87 379.44 49.01 345.55 371.12 48.27 349.22 374.41 48.41±0.48 351.58±4.31 377.40±4.17 1.00 1.23 1.11
(4)加标回收率试验结果
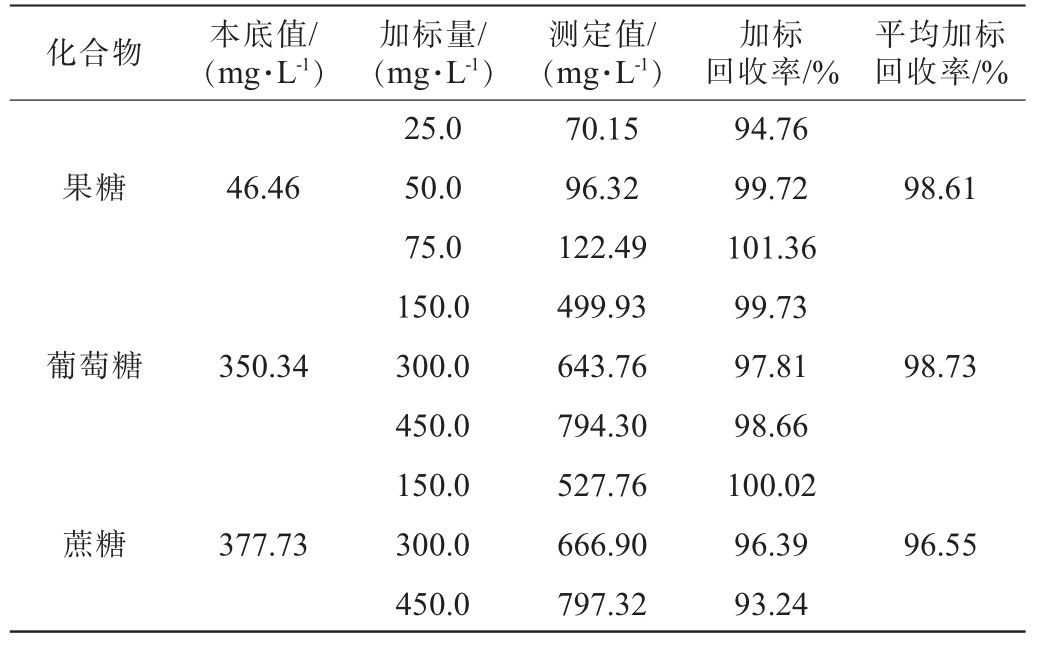
果糖、葡萄糖和蔗糖的加标回收率试验结果见表4。由表4可知,不同加标水平果糖、葡萄糖、蔗糖的平均加标回收率分别为98.61%、98.73%和96.55%,表明该方法准确度较高,可用于茶酒中3种糖的快速测定。
表4 果糖、葡萄糖和蔗糖的加标回收率试验结果
Table 4 Results of standard addition recovery rate tests of fructose,glucose and sucrose
化合物 本底值/(mg·L-1)加标量/(mg·L-1)测定值/(mg·L-1)加标回收率/%平均加标回收率/%果糖46.46 98.61葡萄糖350.34 98.73蔗糖377.73 25.0 50.0 75.0 150.0 300.0 450.0 150.0 300.0 450.0 70.15 96.32 122.49 499.93 643.76 794.30 527.76 666.90 797.32 94.76 99.72 101.36 99.73 97.81 98.66 100.02 96.39 93.24 96.55
2.3 不同类型茶酒中果糖、葡萄糖、蔗糖含量测定结果
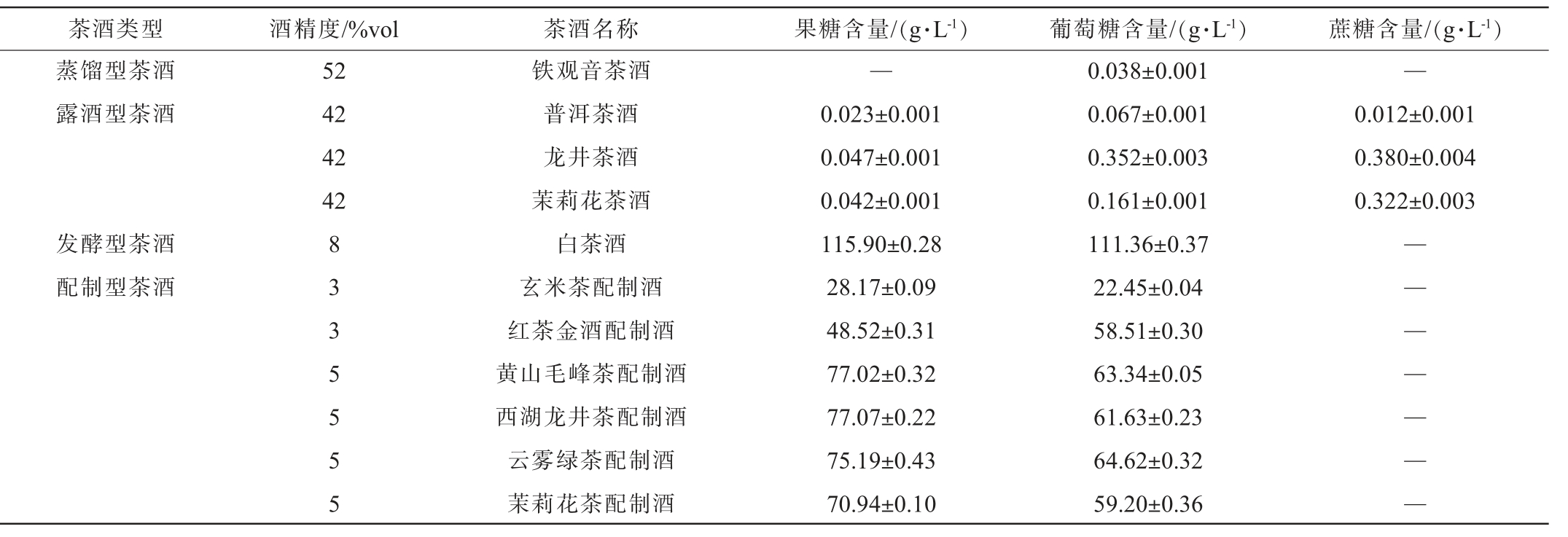
对市售的4类共11款茶酒中果糖、葡萄糖和蔗糖含量进行检测,结果见表5。 由表5可知,不同类型茶酒中3种糖类物质含量差异较大,其中4类茶酒中果糖、葡萄糖含量高低顺序依次为发酵型茶酒>配制型茶酒>露酒型茶酒>蒸馏型茶酒(仅检测到葡萄糖),此外,仅在露酒型茶酒中检测出蔗糖。
表5 11款市售茶酒中果糖、葡萄糖、蔗糖含量检测结果
Table 5 Determination results of fructose, glucose and sucrose contents in 11 kinds of commercially available tea wines
茶酒类型 酒精度/%vol 茶酒名称 果糖含量/(g·L-1) 葡萄糖含量/(g·L-1) 蔗糖含量/(g·L-1)蒸馏型茶酒露酒型茶酒52 42 42 42——0.012±0.001 0.380±0.004 0.322±0.003发酵型茶酒配制型茶酒8 3 3 5 5 5 5铁观音茶酒普洱茶酒龙井茶酒茉莉花茶酒白茶酒玄米茶配制酒红茶金酒配制酒黄山毛峰茶配制酒西湖龙井茶配制酒云雾绿茶配制酒茉莉花茶配制酒0.023±0.001 0.047±0.001 0.042±0.001 115.90±0.28 28.17±0.09 48.52±0.31 77.02±0.32 77.07±0.22 75.19±0.43 70.94±0.10 0.038±0.001 0.067±0.001 0.352±0.003 0.161±0.001 111.36±0.37 22.45±0.04 58.51±0.30 63.34±0.05 61.63±0.23 64.62±0.32 59.20±0.36——
蒸馏型茶酒是以茶叶和蔗糖(或其他酿酒原料)为原料,经微生物发酵、蒸馏而成[26],酒体清澈透明,茶香明显,滋味醇甜。 本研究在蒸馏型茶酒中仅检出了葡萄糖,含量为0.038 g/L。
露酒型茶酒是以白酒为原料,浸泡茶叶而成,其酒体颜色与茶色一致,同时具有茶叶的香气和滋味[27]。三款露酒型茶酒的果糖(0.023~0.047 g/L)、葡萄糖(0.067~0.352 g/L)和蔗糖(0.012~0.380 g/L)含量均较低,且研究表明茶酒糖含量与其茶叶中的糖含量有一定相关性[28],这表明露酒型茶酒中的糖可能主要源于茶叶原料。
发酵型茶酒是将粮食、酵母或糖类物质(如蔗糖、蜂蜜等)、茶叶进行发酵的饮料酒[29],其酒精度较低,酒体通透,茶香浓郁。 在检测的白茶酒中,其果糖和葡萄糖含量分别达到了115.90 g/L、111.36 g/L,高于其他三种茶酒,因发酵过程中的糖类物质未完全降解,故其滋味甜醇。
配制型茶酒是以茶叶(提取物)、白酒、甜味剂、酸味剂等为配料调制而成的饮料酒,是目前市场上的主流茶酒[1]。6款配制型茶酒中均未检测出蔗糖,但其果糖含量(28.17~77.07 g/L)和葡萄糖含量(22.45~64.62 g/L)较高,主要源于果葡糖浆等配料。
3 结论
本研究建立了柱后衍生液相色谱法测定茶酒中果糖、葡萄糖和蔗糖含量的方法,采用Asahipak NH2P-50 4E色谱柱(250 mm×4.6 mm,5 μm),以含0.5%H3PO4的乙腈-水(75∶25,V/V)为流动相进行等度洗脱,流速0.8 mL/min,柱温40 ℃,柱后120 ℃下采用高碘酸(质量浓度为2.0 g/L)氧化、酚试剂(质量浓度为1.0 g/L)进行衍生显色,检测波长为670 nm。在此条件下,3种糖类物质能够在20 min内完成检测。所得果糖、葡萄糖和蔗糖线性方程均在各自质量浓度范围内具有良好的线性范围,检出限为2.58~9.64 mg/L,定量限为7.82~29.21 mg/L,平均加标回收率为96.55%~98.73%,精密度、稳定性试验结果的RSD均<2.00%。 利用本方法对4类11款市售茶酒的果糖、葡萄糖和蔗糖含量进行了检测,在所有茶酒中均检测出葡萄糖,含量为0.038~111.36 g/L,其中发酵型和配制型茶酒中的葡萄糖含量较高;共有10款茶酒中检测出果糖,含量在0.023~115.90 g/L之间,同样是发酵型和配制型茶酒中含量较高;蔗糖仅在3款露酒型茶酒检出,含量为0.012~0.380 g/L。该方法具有快速简便、试剂成本低、回收率高、精密度和稳定性好等优点,可为茶酒的工艺研究、产品开发、标准制定等提供新的检测技术支持。
[1]刘洋,李国辉,曹晓念,等.茶酒的研究进展[J].食品研究与开发,2022,43(23):210-216.
[2]陈艳,高嵩,刘秋妍,等.金桔红茶酒的研制及其体外抗氧化研究[J].中国酿造,2025,44(1):226-231.
[3]周书来,吴丽,王琪,等.柑橘茶酒酿造工艺优化及抗氧化活性分析[J].中国酿造,2024,43(8):249-254.
[4]史梦娜,李怡琪,宋娓娜,等.发酵型茶酒活性成分的研究进展[J].现代食品,2022,28(13):23-25.
[5]陈顺心,陈晖,郑雪珂,等.不同采摘时期信阳毛尖对茶酒品质影响分析[J].粮食加工,2024,49(4):29-35,41.
[6]王桂圆,周晓秋,李芳香.发酵型普洱茶酒的制备工艺优化研究[J].酿酒,2024,51(5):102-107.
[7]CHEN J,LIN B,ZHENG F J,et al.Characterization of the pure black tea wine fermentation process by electronic nose and tongue-based techniques with nutritional characteristics[J].ACS Omega,2023,8(13):12538-12547.
[8]王振涛,许蓓蓓,程晓宏.一种新型双酶体系快速检测葡萄糖的方法[J].食品工业,2023,44(4):305-308.
[9]陈英,黄永剑,张帆,等.酒产品中低含量总糖和还原糖的快速检测方法[J].广州化工,2015,43(24):147-148,225.
[10]CHAWAFAMBIRA A.The effect of incorporating herbal(Lippia javanica)infusion on the phenolic,physicochemical,and sensorial properties of fruit wine[J].Food Sci Nutr,2021,9(8):4539-4549.
[11]杨成聪,凌霞,胡伟伟,等.高效液相-示差折光法测定米酒中3种糖的含量[J].食品研究与开发,2017,38(21):135-141.
[12]徐诺,姚哲渊,车金水,等.离子色谱-积分脉冲安培法检测黄酒中的阿拉伯糖、半乳糖、甘露糖、葡萄糖、核糖、乳糖[J].食品工业科技,2022,43(3):254-259.
[13]杨亚琴,余明霞,冯慧慧,等.高效液相色谱-蒸发光散射法测定油莎豆块茎发育过程中的水溶性糖[J].粮食与油脂,2024,37(6):153-157,162.
[14]王晓亮,毛卫中,汪新华,等.QuEchERs-高效液相色谱柱后衍生法测定茶叶中10种氨基甲酸酯类农药残留[J].食品工业科技,2018,39(14):190-193.
[15]卜雅琴,郝经文,陈乃富,等.基于PMP柱前衍生HPLC法测定汽爆加工对蕨菜糖类成分影响研究[J].天然产物研究与开发,2024,36(6):1004-1012.
[16]赵鑫.1-萘硼酸柱后衍生高效液相色谱荧光法测定单糖的研究[D].石家庄:河北师范大学,2013.
[17]韩晶,李永路.磷酸-苯肼柱后衍生法测定茶及茶饮料中的糖类[C]//中国化学会第八届全国仪器分析及样品预处理学术研讨会论文集.泰州:中国化学会,2015:80-82.
[18]屠鹏飞.天然糖化学[M].北京:化学工业出版社,2020:17-28.
[19]PANDEIRADA C O,ACHTERWEUST M,JANSSEN H G,et al.Periodate oxidation of plant polysaccharides provides polysaccharide-specific oligosaccharides[J].Carbohydr Polym,2022,291:119540.
[20]开学俊,万亚军.水产品中甲醛的酚试剂分光光度检测法[J].环境与健康杂志,2015,32(11):1005-1007.
[21]蒋喆.MBTH法和HPLC法测定汽车内饰挥发甲醛含量对比[J].浙江化工,2024,55(7):42-49.
[22]陈琦,李立,吴雪原,等.高效液相色谱-蒸发光检测器法检测茶叶中掺杂糖类物质[J].茶业通报,2015(1):26-30.
[23]吴国权,陈洁,郑洪国,等.高效离子色谱柱后衍生法测定环境水体中过渡金属离子含量[J].中国环境监测,2023,39(S1):105-109.
[24]张璐,张土金.HPLC-RID法测定生脉饮(党参方)中果糖、葡萄糖、蔗糖、麦芽糖[J].药品评价,2022,19(19):1161-1165.
[25]LUO X,LIU Y,XING J,et al.Comparison of ELSD and RID combined with HPLC for simultaneous determination of six rare sugars in food components[J].Microchem J,2024,201:10666.
[26]陈琳琳,胡宝东,邱树毅,等.茶叶发酵蒸馏酒生产工艺优化及挥发性成分分析[J].中国酿造,2016,35(6):40-45.
[27]吕杨俊,王霈菲,蒋玉兰,等.市售茶酒中5种高级醇含量的检测与分析[J].食品安全质量检测学报,2024,15(9):223-231.
[28]王川丕,诸力,刘新,等.超高效液相色谱-质谱联用技术测定茶叶中8种单、寡糖的含量[J].食品科学,2014,35(20):164-169.
[29]朱静,李正钰,周思远,等.发酵型茶酒的研究进展[J].蚕桑茶叶通讯,2024,49(3):20-23.