香菇(Lentinula edodes),又名花蕈、椎茸、冬菰,是我国广泛栽培种植的食用真菌。香菇中富含多酚[1]、多糖[2]、蛋白质[3]等多种活性物质,在抗炎、抑菌、代谢调节(如脂质代谢平衡)及增强免疫力等方面表现出显著功效[4-6]。 在食品工业中,香菇经常被用来制作调味酱料、菌汤速食等食品的开发。值得注意的是,多糖作为香菇的核心功能成分,因其兼具抗氧化、抗衰老、免疫调节等生物活性而使香菇成为食用菌产业的开发热点[7]。
在香菇活性物质提取制备的研究中,超声辅助技术已成为重要手段。秦令祥等[8]采用单因素试验结合正交试验法,得出香菇多糖的最优提取工艺,在料液比1∶15(g∶mL)、超声温度70 ℃及超声时间12 min条件下,香菇多糖提取得率为8.97%。 奚灏锵等[9]利用高压辅助超声处理提取香菇多糖,结果表明,在压力350 MPa,固液比为1∶35(g∶mL),温度为55 ℃,保压时间4.0 min条件下,香菇多糖得率为8.96%,与常规超声法提取效率相当。张潇等[10]利用二段辅助提取香菇多糖,相较于传统的热水浸提法,通过二段式超声辅助提取能够显著提高香菇多糖得率。作为获得多糖的重要步骤,提取过程所选取的方法往往会影响多糖的产量。 课题组前期对香菇多酚进行了优化提取,并对香菇多酚的抗氧化和稳定性进行了研究[11]。香菇多酚提取剩余物里面尚有多糖等活性成分,对香菇多酚提取剩余物进行香菇多糖的提取,可进一步促进香菇的综合利用,提升香菇的精深加工水平。
秀丽隐杆线虫(Caenorhabditis elegans),简称线虫,因其生长周期短,易培养,且与高等生物存在部分相似的药物代谢通路,对食品中活性物质的功能研究具有重要意义[12]。肖嵋方等[13]研究发现,竹荪水提物对线虫氧化应激和热应激具有调节作用,该物质不仅能有效延长线虫的平均寿命,还能显著降低线虫体内的脂质累积,提高脂质代谢功能。刘慧敏[14]利用线虫模型评估了香菇多糖对氟吡菌酰胺致线虫毒性的拮抗效应,结果表明,香菇多糖能够显著提高经氟吡菌酰胺处理过后的线虫寿命,缓解线虫体内的氧化损伤。由于线虫的这些特性能直观反映活性物质对生物体抗氧化系统的影响,故而成为研究香菇多糖抗氧化活性的理想动物模型。
本研究以经过提取多酚后的香菇剩余物为原料,采用超声辅助水提法提取多糖,以多糖提取得率为评价指标,运用单因素试验结合响应面法优化香菇多糖提取工艺,并探究香菇多糖自由基清除能力,以秀丽隐杆线虫为体内抗氧化性实验模型,考察不同浓度的香菇多糖对秀丽隐杆线虫体内超氧歧化酶(superoxide dismutase,SOD)、过氧化氢酶(catalase,CAT)活性和脂质氧化产物中的丙二醛(malondialdehyde,MDA)含量等氧化应激相关指标影响,以期为香菇的精深加工及开发利用提供理论依据。
1 材料与方法
1.1 材料与试剂
1.1.1 原料和菌株
香菇:井冈山井祥菌草生态科技股份有限公司;野生N2型秀丽隐杆线虫(Caenorhabditis elegans):福建上源生物科学技术有限公司;尿嘧啶缺陷型大肠杆菌(Escherichia coli)OP50:由本课题组传代获得。
1.1.2 试剂
硫酸、苯酚、体积分数为95%乙醇、3,5-二硝基水杨酸、维生素C(vitamin C,VC)、氯化钙(CaCl2)、胆固醇、硫酸镁(MgSO4)、磷酸氢二钾(K2HPO4)、磷酸二氢钾(KH2PO4)、氢氧化钠(NaOH)、次氯酸钠(NaClO)、蛋白胨、氯化钠(NaCl)、琼脂、磷酸氢二钠(Na2HPO4):国药集团化学试剂有限公司;1,1-二苯基-2-三硝基苯肼(1,1-diphenyl-2-picrylhydrazyl,DPPH)、2,2'-联氮-双-3-乙基苯并噻唑啉-6-磺酸(2,2'-azino-bis(3-ethylbenzothiazoline-6-sulfonic acid),ABTS):上海阿拉丁生化科技股分有限公司;超氧化物歧化酶(SOD)、过氧化氢酶(CAT)、丙二醛(MDA)检测试剂盒:南京建成生物工程研究所;二喹啉甲酸(bicinchoninic acid,BCA)蛋白浓度测定试剂盒:北京兰博利德生物技术有限公司;试验所用试剂均为分析纯。
1.1.3 培养基
M9缓 冲 液:0.6 g Na2HPO4,0.3 g KH2PO4,0.5 g NaCl溶解于100 mL去离子水中,121 ℃灭菌20 min后加入1 mol/L MgSO4溶液1 mL。
LB液体培养基:5 g蛋白胨,5 g NaCl,5 g酵母浸膏溶解于500 mL去离子水中。121 ℃灭菌20 min。
线虫生长培养基(nematode growth medium,NGM):2.5 g蛋白胨、3 g NaCl、28 g琼脂,加入去离子水至800 mL,加入CaCl2、乙醇溶解的胆固醇、MgSO4各1 mL,K3PO4缓冲液25 mL,再去离子水定容至1 L。121 ℃灭菌20 min。
尿嘧啶缺陷型大肠杆菌(Escherichia coli)OP50培养液:吸取5~10 μL大肠杆菌OP50原菌液于500 μL LB液体培养基中,37 ℃、150 r/min振荡培养过夜。
1.2 仪器与设备
SpectraMax i3x多功能酶标仪:美谷分子仪器(上海)有限公司;CF15RN日立多用途冷冻离心机:长沙科美分析仪器有限公司;KQ-400DE超声清洗机:昆山市超声仪器有限公司;DK-10D恒温水浴锅:上海百典仪器设备有限公司。
1.3 方法
1.3.1 香菇多酚提取剩余物的制备
干燥香菇打粉过60目筛,按照料液比1∶40(g∶mL)加入体积分数50%乙醇,超声功率240 W、超声温度50 ℃条件下提取40 min,以5 000 r/min离心10 min,分离得到上清液为多酚提取液,将沉淀物于60 ℃烘干24 h得到香菇多酚提取剩余物用于后续多糖提取。
1.3.2 多糖含量测定
多糖含量按照中华人民共和国农业行业标准NY/T 1676—2023《食用菌中粗多糖的测定分光光度法》中的方法测定。葡萄糖标准曲线绘制:分别移取质量浓度为0.1 mg/mL的标准葡萄糖溶液0、0.2 mL、0.4 mL、0.6 mL、0.8 mL、1.0 mL于试管中,用去离子水定容至1.0 mL,依次加入1.0 mL的5%苯酚溶液和5.0 mL的硫酸溶液,混合体系经10 min避光处理后,30 ℃水浴锅中恒温加热20 min。 使用酶标仪于波长490 nm处分别检测各个浓度体系200 μL显色液的吸光度值。以葡萄糖标准溶液质量浓度(x)为横坐标,吸光度值(y)为纵坐标绘制葡萄糖标准曲线,得到标准曲线回归方程为:y=6.248 1x+0.053 3,相关系数R2=0.996 8。 按照标准曲线回归方程计算多糖含量,计算多糖得率,其计算公式如下:
式中:c为多糖含量,g/mL;V为溶液体积,mL;n为稀释倍数;m为样品质量,g。
1.3.3 提取工艺优化
(1)单因素试验
超声时间的选择:在料液比1∶30(g∶mL),超声温度70 ℃,超声功率320 W条件下,探讨不同超声时间(20 min、30 min、40 min、50 min、60 min)对香菇多糖得率的影响。
超声温度的选择:在料液比1∶30(g∶mL),超声时间30min,超声功率320 W条件下,探究不同超声温度(55 ℃、60 ℃、65 ℃、70 ℃、75 ℃)对香菇多糖得率的影响。
料液比的选择:在超声时间50 min,超声温度75 ℃,超声功率320 W条件下,探究不同料液比(1∶10、1∶20、1∶30、1∶40、1∶50(g∶mL)对香菇多糖得率的影响。
超声功率的选择:在超声温度75 ℃,超声时间30 min,料液比1∶30(g∶mL)条件下,探讨不同超声功率(200 W、240 W、280 W、320 W、360 W)对香菇多糖得率的影响。
(2)响应面试验
在单因素试验结果的基础上,基于Box-Behnken试验设计[11],固定超声温度为75 ℃,以超声功率(A)、超声时间(B)、料液比(C)作为自变量,香菇多糖得率(Y)为响应值,进行3因素3水平的响应面试验,Box-Behnken试验因素与水平见表1。
表1 提取工艺优化Box-Behnken试验设计因素与水平
Table 1 Factors and levels of Box-Behnken experiments design for extraction process optimization
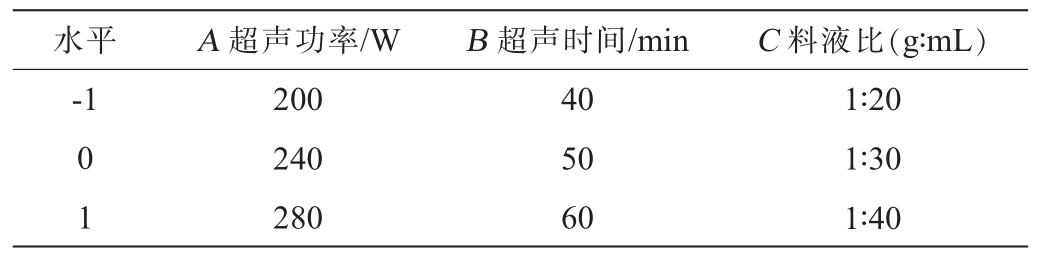
水平 A 超声功率/W B 超声时间/min C 料液比(g∶mL)-1 0 1 200 240 280 40 50 60 1∶20 1∶30 1∶40
1.3.4 香菇多糖体外抗氧化活性测定
(1)DPPH自由基清除率测定
按照王力等[15]的方法,并进行调整。取香菇多糖于试管中,加入蒸馏水,配制多糖溶液质量浓度分别为1.0 mg/mL、1.5 mg/mL、2.0 mg/mL、2.5 mg/mL、3.0 mg/mL,分别取500 μL与0.2 mmol/L DPPH溶液500 μL混匀,经遮光处理30 min后,置于波长517nm处测定吸光度值。以无水乙醇为样对照,维生素C为阳性对照,每组试验进行3次平行测定。DPPH自由基清除率计算公式如下:
式中:A0为空白组吸光度值;A1为待测样品组吸光度值;A2为对照组吸光度值。
(2)ABTS自由基清除率测定
配制香菇多糖溶液质量浓度分别为0.062 5 mg/mL、0.125 0 mg/mL、0.250 0 mg/mL、0.500 0 mg/mL、1.000 0 mg/mL、2.000 0 mg/mL,分别取50 μL样品溶液与150 μL ABTS工作液,30 ℃隔水恒温反应6 min后,于波长734 nm处测定吸光度值。 以磷酸盐缓冲液(phosphate buffer solution,PBS)为样品对照,维生素C为阳性对照,每组试验进行3次平行测定。ABTS自由基清除率计算公式如下:
式中:A0为空白组吸光度值;A1为待测样品组吸光度值;A2为对照组吸光度值。
(3)羟自由基清除率测定
配制1.5 mmol/L 硫酸亚铁溶液、6.7 mmol/L 过氧化氢溶液、20 mmol/L水杨酸溶液以及香菇多糖溶液质量浓度分别为0.062 5mg/mL、0.125 0 mg/mL、0.250 0 mg/mL、0.500 0 mg/mL、1.000 0 mg/mL、2.000 0 mg/mL[15],分别取500 μL样品溶液、250 μL FeSO4溶液和175 μL H2O2溶液混合,37 ℃水浴加热10 min后加入3,5-二硝基水杨酸溶液75 μL,再水浴30 min,离心,于波长562 nm处测定吸光度值。 去离子水为样品对照,维生素C为阳性对照,每组试验进行3次平行测定。羟自由基清除率计算公式如下:
式中:A0为空白组吸光度值;A1为待测样品组吸光度值;A2为对照组吸光度值。
1.3.5 香菇多糖体内抗氧化活性
秀丽隐杆线虫(Caenorhabditis elegans)体型微小,可以在培养基中大量培养,相较于其他动物模型具有低成本、高效率的优点。其平均寿命短,极大地缩短了研究周期。线虫具备与高等动物相似的复杂生理过程,保证了研究结果的生物学意义和参考价值,因此选用秀丽隐杆线虫作为体内抗氧化实验模型[12]。
尿嘧啶缺陷型大肠杆菌(Escherichia coli)OP50培养与接种:吸取尿嘧啶缺陷型大肠杆菌OP50原菌液5~10 μL于500 μL LB液体培养基中,于37 ℃、150 r/min条件下振荡培养过夜,取0.1 mL菌液涂布于NGM固体培养基上,37 ℃条件下培养5~6 h。
野生N2型秀丽隐杆线虫的培养与同步化:将野生N2型秀丽隐杆线虫接入含有大肠杆菌OP50的NGM固体培养基上,于20 ℃培养2 d。用M9缓冲液冲洗NGM固体培养基,将处于产卵期线虫收集2 mL置于离心管中,2 000 r/min离心3 min后弃上清液,沉淀用M9缓冲液重复洗涤和离心3次后,用移液器向虫体沉淀中加入5 mL次氯酸钠裂解液后反复吹打5~10 min,使其虫体充分溶解。2 000 r/min离心3 min后弃上清液,用M9缓冲液重复洗涤和离心3次后,用0.2 mL无菌M9缓冲液悬浮虫卵,将虫卵转移至含有大肠杆菌OP50的NGM固体培养基上,在20 ℃恒温箱培养48 h,线虫成长为四龄幼虫。
将香菇多糖溶解于大肠杆菌OP50培养液中配制成质量浓度分别为0、0.25 mg/mL、0.50 mg/mL和1.0 mg/mL,即得空白组、低剂量组、中剂量组和高剂量组的大肠杆菌OP50培养液。随机挑取完成同步化的线虫分为4组(n=250),按照以上质量浓度,每日给予对应组别200 μL培养液,置于恒温培养,72 h后收集成虫虫体。
1.3.6 SOD、CAT和MDA的测定
参考文献[13]的方法进行测定。取收集的成虫样本(n=250),加入1mLM9缓冲液进行涡旋振荡充分混匀,4000r/min离心分离10 min,保留沉淀再加入1 mL M9缓冲液重复以上步骤3次,收集沉淀。将最终沉淀物加入1 mL预冷的细胞裂解液混合,冰浴条件下裂解1 h后机械匀浆处理。 离心后取上清液分别用SOD、CAT、MDA检测试剂盒进行SOD、CAT的酶活力和MDA含量测定。
1.3.7 数据处理
Design-Expert 8.0.6、Origin 2019b和IBM SPSS Statistics 26.0软件分别用于响应面试验设计、制图、数据处理及显著性分析,每组实验重复3次,结果以“平均值±标准差”表示。
2 结果与分析
2.1 香菇多糖提取工艺优化
2.1.1 单因素试验
以香菇多糖得率为评价指标,探究不同超声时间、超声温度、料液比以及超声功率条件下对多糖得率的影响,单因素试验结果见图1。
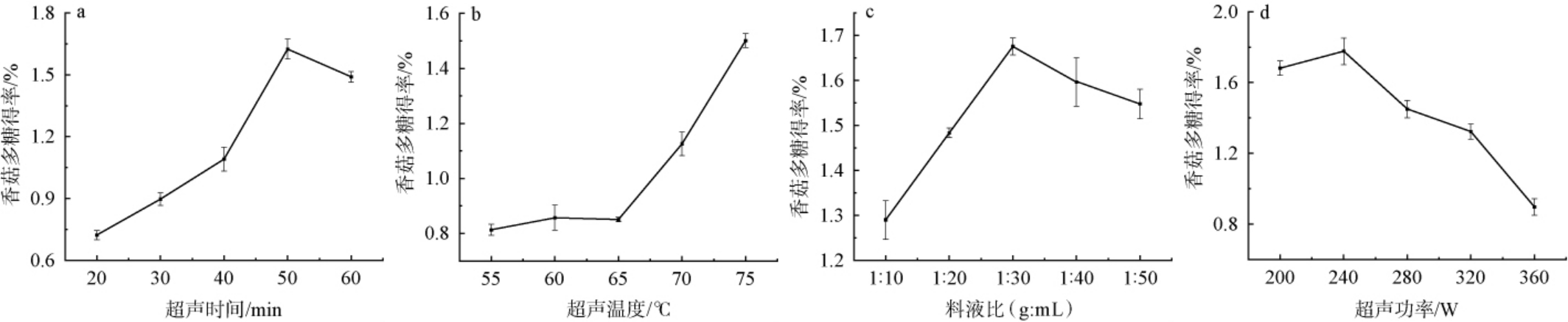
图1 超声时间(a)、超声温度(b)、料液比(c)及超声功率(d)对香菇多糖得率的影响
Fig.1 Effect of ultrasonic time (a), temperature (b), solid-liquid ratio (c) and ultrasonic power (d) on the yield of lentinan
由图1a可知,香菇多糖得率随着超声时间在20~60 min范围内的增加呈先增加后减少的趋势。当超声时间在20~50 min时,多糖得率随之增加;当超声时间在50 min时,多糖得率最高,为1.625%;当超声时间>50 min之后,多糖得率有所下降。其原因是提取时间<50 min时,细胞破壁不充分导致香菇中的多糖并未全部溶出;当超声时间>50 min后,溶出的多糖长时间处于高温和超声破碎环境中,机械应力可能引起糖苷键断裂,结构变化,导致多糖提取得率降低[18]。 因此,选取最适超声时间为50 min。 由图1b可知,超声温度对香菇多糖的提取影响较大,当超声温度在55~65 ℃时,多糖提取得率变化不大,其可能的原因为温度太低,溶剂黏度较大不利于多糖的分子运动,影响溶出率;当超声温度>65 ℃之后,多糖提取得率显著增加,随着温度升高,分子运动加强,多糖提取得率增加。本试验采用的超声提取设备在温度为80 ℃时会因设备热保护设定而停止工作。因此,选取最适超声温度为75 ℃。由图1c可知,当料液比为1∶10~1∶30(g∶mL)时,多糖得率随之增加;当料液比为1∶30(g∶mL)时,多糖的得率最高,为1.675%;当料液比为1∶30~1∶50(g∶mL)时,多糖得率有所下降。具体原因为溶剂体积较少导致溶液中黏稠度升高,不利于多糖分子运动和溶出,当料液比>1∶30(g∶mL)之后,过量溶剂可能会引起其他活性物质与多糖分子竞争,影响香菇中多糖的提取[19-20]。 因此,选择最适料液比为1∶30(g∶mL)。 超声功率对空化效应的影响呈现先促进后抑制的双向调节特性。 由图1d可知,当超声功率为200~240 W时,多糖得率随之增加;当超声功率为240 W时,多糖得率最高,为1.776%;当超声功率>240 W之后,多糖得率有所下降。一定超声功率形成的稳定空化泡可高效破碎细胞结构,而超限功率产生的剧烈剪切力将改变多糖分子构象,导致香菇多糖得率降低[21-22]。因此,最适超声功率为240 W。
2.1.2 响应面试验
根据单因素试验结果,固定超声温度为75 ℃,以超声功率(A)、超声时间(B)、料液比(C)为自变量,香菇多糖得率(Y)为响应值,进行3因素3水平Box-Behnken试验,Box-Behnken试验结果与分析见表2,回归模型方差分析结果见表3。
表2 提取工艺优化Box-Behnken试验设计与结果
Table 2 Design and results of Box-Behnken experiments for extraction process optimization
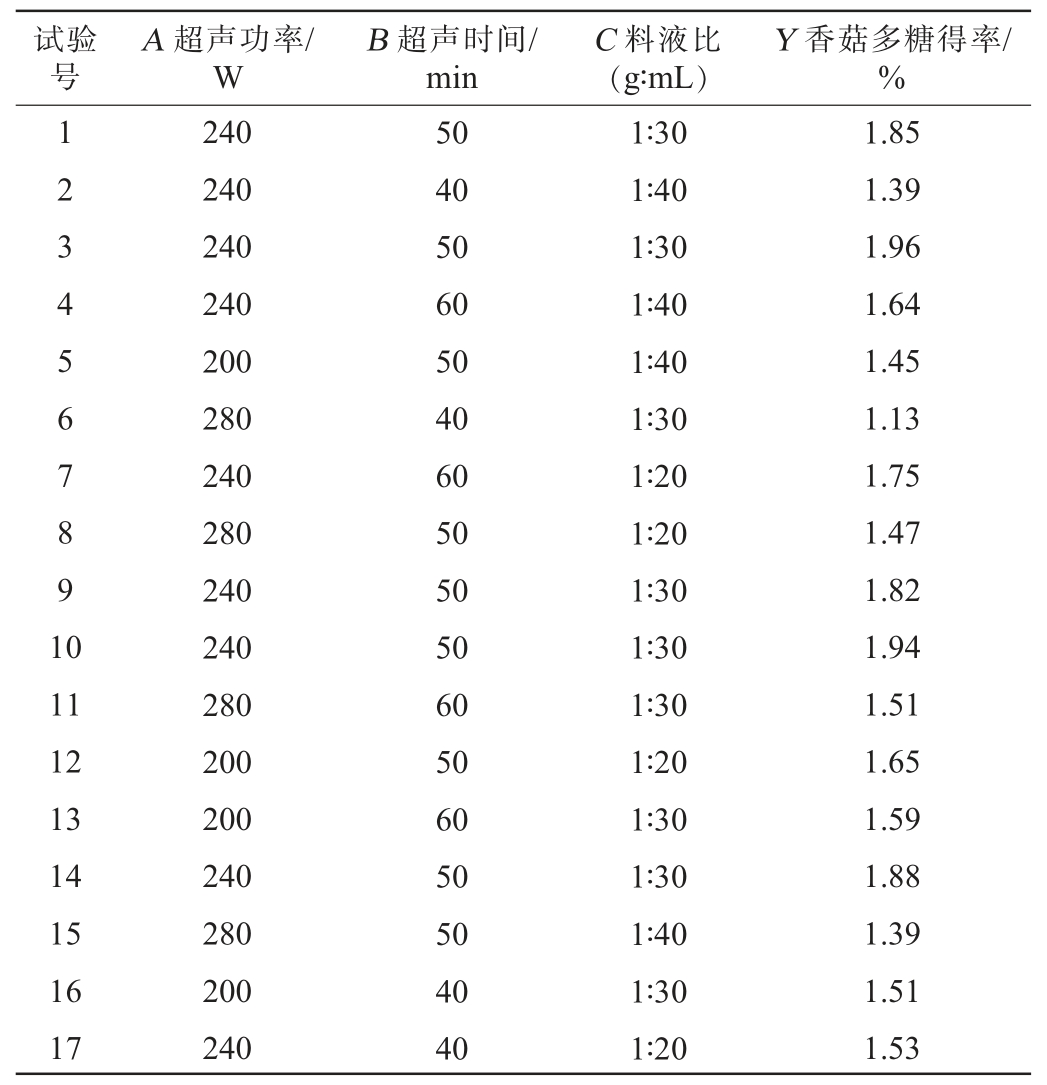
试验号A 超声功率/W B 超声时间/min C 料液比(g∶mL)Y 香菇多糖得率/%1234567891 0 11 12 13 14 15 16 17 240 240 240 240 200 280 240 280 240 240 280 200 200 240 280 200 240 50 40 50 60 50 40 60 50 50 50 60 50 60 50 50 40 40 1∶30 1∶40 1∶30 1∶40 1∶40 1∶30 1∶20 1∶20 1∶30 1∶30 1∶30 1∶20 1∶30 1∶30 1∶40 1∶30 1∶20 1.85 1.39 1.96 1.64 1.45 1.13 1.75 1.47 1.82 1.94 1.51 1.65 1.59 1.88 1.39 1.51 1.53
表3 回归模型方差分析
Table 3 Variance analysis of regression model
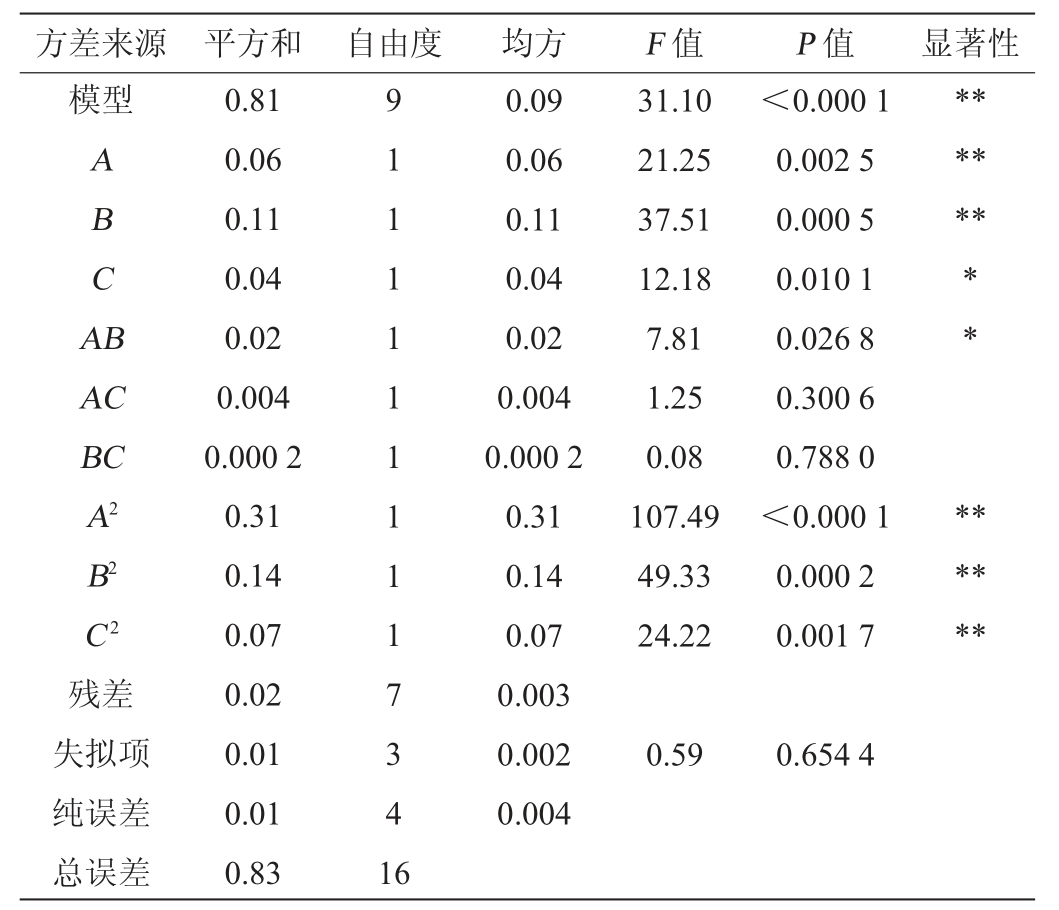
注:“*”表示对结果影响显著(P<0.05),“**”表示对结果影响极显著(P<0.01)。
方差来源 平方和 自由度 均方 F 值 P 值 显著性模型ABCA B******AC BC A2 B2 C2残差失拟项纯误差总误差0.81 0.06 0.11 0.04 0.02 0.004 0.000 2 0.31 0.14 0.07 0.02 0.01 0.01 0.83 9 1 1 1 1 1 1 1 1 1 7 3 4 1 6 0.09 0.06 0.11 0.04 0.02 0.004 0.000 2 0.31 0.14 0.07 0.003 0.002 0.004 31.10 21.25 37.51 12.18 7.81 1.25 0.08 107.49 49.33 24.22<0.000 1 0.002 5 0.000 5 0.010 1 0.026 8 0.300 6 0.788 0<0.000 1 0.000 2 0.001 7** ******0.59 0.654 4
采用Design-Expert 8.0.6软件对表2结果进行二次回归拟合分析,得出超声功率(A)、超声时间(B)、料液比(C)与多糖得率(Y)二次项回归模型方程为:Y=1.89-0.088A+0.12B-0.066C+0.075AB+0.030AC+0.007BC-0.27A2-0.18B2-0.13C2。
由表3可知,模型P值<0.000 1,极显著;失拟项P值为0.654 4,不显著,表明模型高度拟合,可信度较高。决定系数R2和调整决定系数R2Adj分别为0.975 6和0.944 2,表明模型可靠。由P值可知,一次项A、B,二次项A2、B2、C2对结果影响极显著(P<0.01);一次项C及交互项AB对结果影响显著(P<0.05),其他项不显著(P>0.05)。由F值可知,各因素对香菇多糖得率影响大小依次为超声时间(B)>超声功率(A)>料液比(C)。
2.1.3 各因素间交互作用分析
响应面越陡峭,等高线越趋于椭圆形,表明各因素间交互作用对结果影响越强;反之,响应面越平缓,等高线越趋于圆形,表明各因素间交互作用对结果影响越弱。由图2可知,超声功率与超声时间交互作用的响应面陡峭,等高线为椭圆形,表明二者交互作用对香菇多糖得率影响较大,超声功率与料液比、超声时间与料液比交互作用响应面陡峭平缓,等高线趋于圆形,表明对香菇多糖得率影响较小,这与方差分析的结果一致。
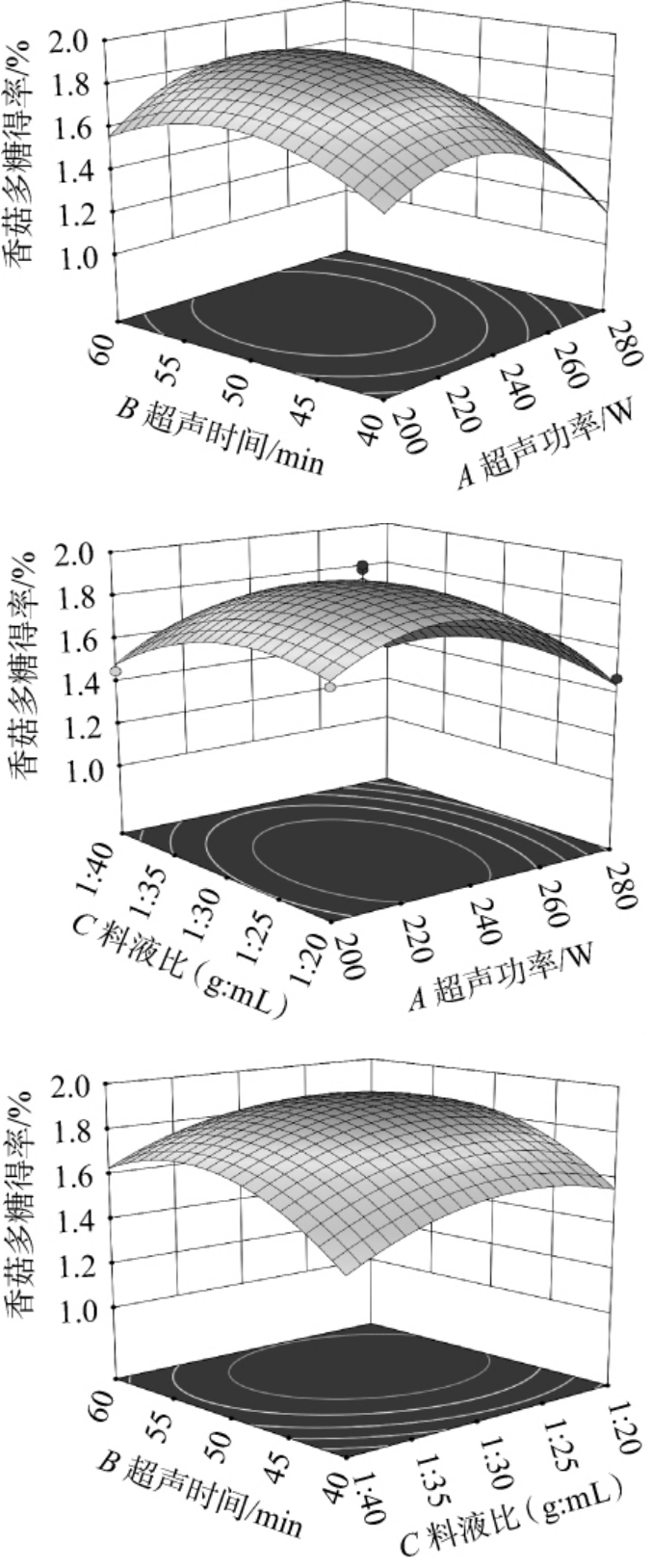
图2 各因素间交互作用对香菇多糖得率影响的响应面及等高线
Fig.2 Response surface plots and contour lines of effect of interaction between various factors on the yield of lentinan
2.1.4 验证试验
通过Design-Expert 8.0.6软件对多元二次回归方程进行最优求解,得到香菇多糖最优提取工艺条件为:超声功率234.50 W、超声时间52.83 min,料液比1∶27.36(g∶mL)。在此条件下,香菇多糖得率预测值为1.92%。考虑实际操作可行性,将菇多糖最优提取工艺条件修正为超声功率240 W,超声时间50 min,料液比1∶30(g∶mL)。在此优化条件下进行3次平行验证试验,香菇多糖得率实际值为1.89%,与预测值相对误差<1.5%,差异不显著,证明该模型结果可靠。
2.2 香菇多糖的体外抗氧化活性
不同质量浓度的香菇多糖对于DPPH、ABTS及羟基自由基的清除能力测定结果见图3。
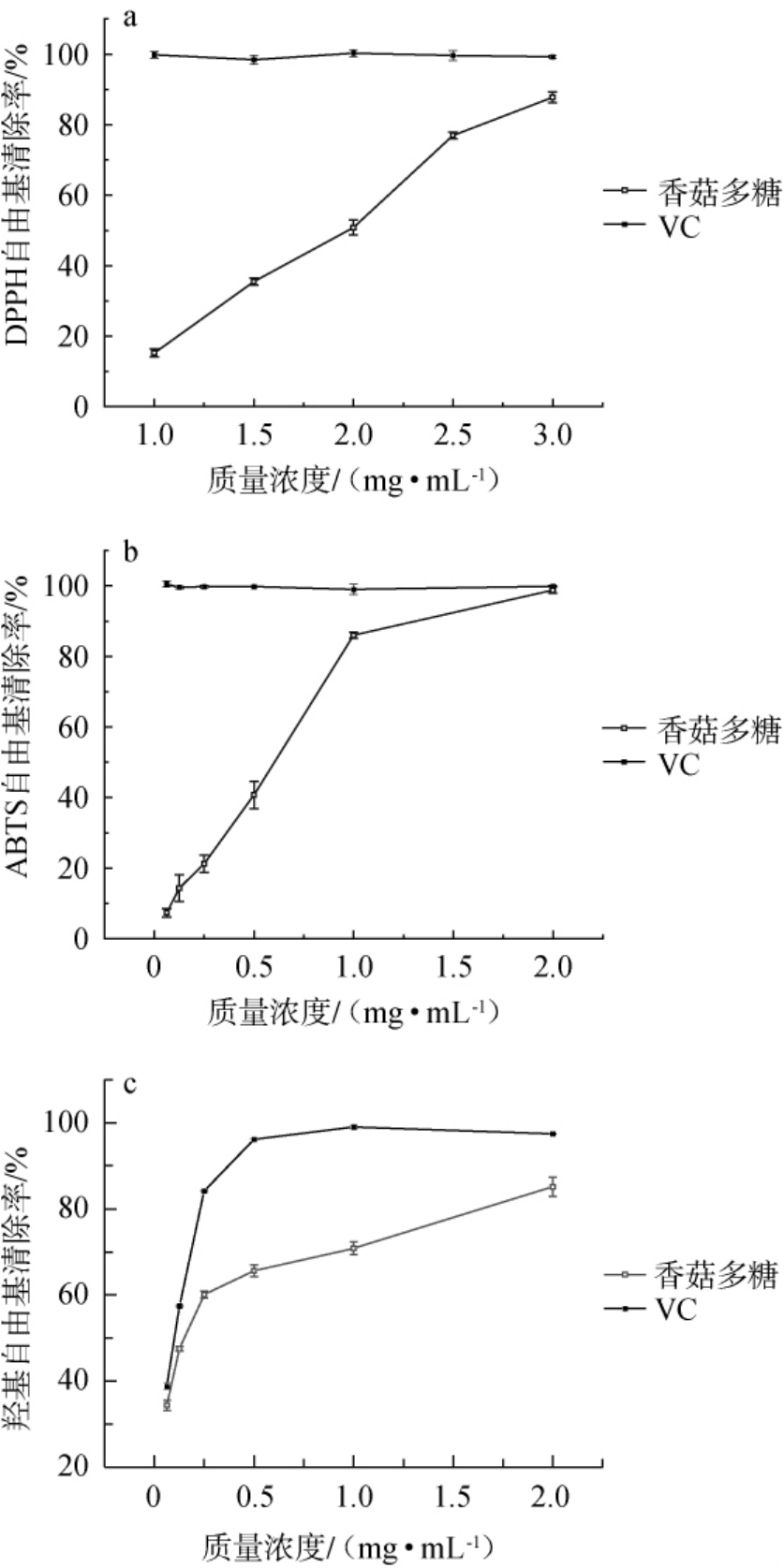
图3 不同质量浓度的香菇多糖对DPPH(a),ABTS(b)及羟基(c)自由基的清除率
Fig.3 Scavenging rates of lentinan with different mass concentration on DPPH (a), ABTS (b) and hydroxyl (c) radicals
由图3a可知,DPPH自由基清除率在香菇多糖质量浓度为1~3 mg/mL的范围内有良好的剂量效应关系,当香菇多糖质量浓度为3 mg/mL时,DPPH自由基清除率最高,为87.72%,半抑制浓度(50%inhibiting concentration,IC50)值为1.91 mg/mL,表明香菇多糖清除DPPH自由基能力较强。
由图3b可知,香菇多糖质量浓度在0.0625~2.0000mg/mL的范围内与ABTS自由基清除率呈现良好的量效关系,其自由基清除能力随浓度递增而明显增强。当香菇多糖质量浓度为2 mg/mL时,ABTS自由基清除率最高,为98.79%,IC50值为0.58 mg/mL,表明其对ABTS自由基具有极强的清除能力。
由图3c可知,香菇多糖在抑制羟基自由基活性时呈现明显的剂量依赖性,即羟基自由基清除率随香菇多糖浓度递增而显著增加。当香菇多糖质量浓度为3 mg/mL时,羟基自由基清除率最高,为87.72%,IC50值为0.16 mg/mL,表明香菇多糖具有较好的羟基自由基清除能力。该结果与侯银臣等[24]在对长根菇多糖对羟基自由基清除率的结果接近。
2.3 香菇多糖的体内抗氧化活性
以未加入香菇多糖的大肠杆菌OP50培养液为空白组,将质量浓度分别为0.25 mg/mL、0.50 mg/mL和1.0 mg/mL香菇多糖溶解于大肠杆菌OP50培养液中,即得低剂量组、中剂量组和高剂量组。 考察各试验组对野生N2型秀丽隐杆线虫体内超氧化物歧化酶(SOD)、过氧化氢酶(CAT)及丙二醛(MDA)含量的影响,结果见图4。
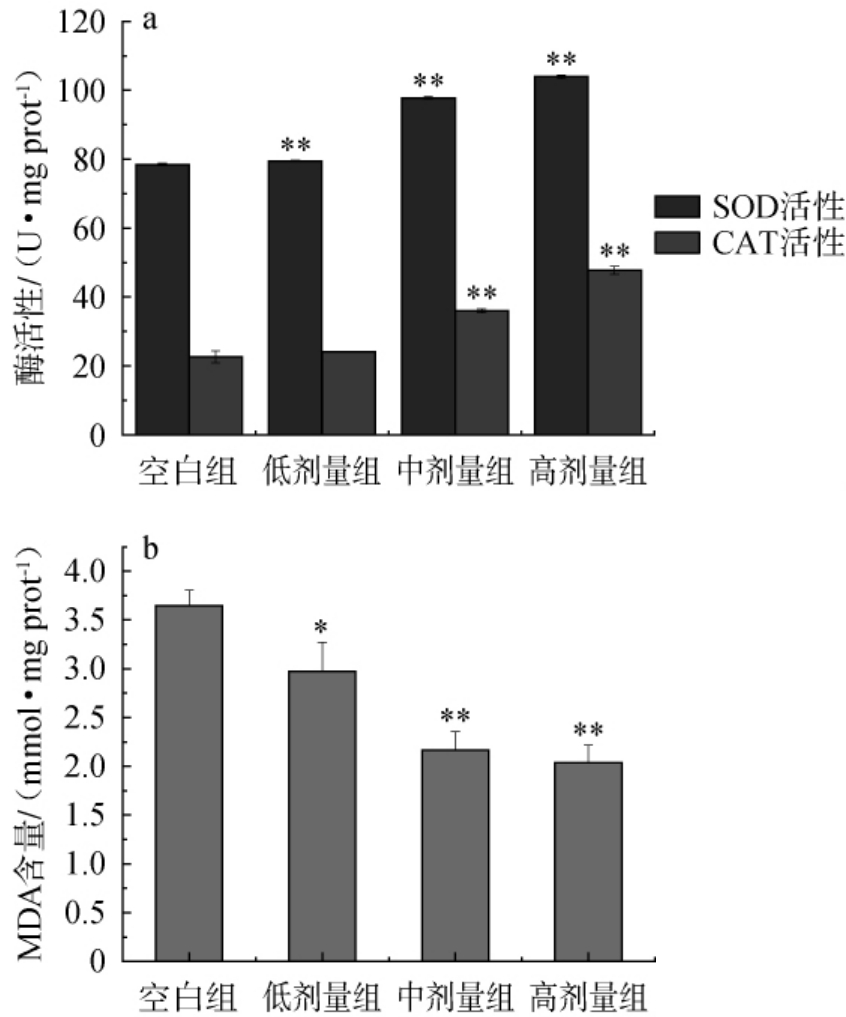
图4 不同香菇多糖对秀丽隐杆线虫体内超氧化物歧化酶、过氧化氢酶活性(a)及丙二醛含量(b)的影响
Fig.4 Effect of different lentinan on the activities of superoxide dismutase, catalase (a) and the content of malondialdehyde(b) in the body of Caenorhabditis elegans
有氧代谢是需氧生物必不可少的生命活动,其过程中会产生大量的活性氧(reactive oxygen species,ROS)。一般情况下,活性氧水平是处于动态平衡的,SOD能够清除超氧阴离子以避免氧化代谢产生过量活性氧危害身体健康[25]。由图4a可知,经过不同质量浓度香菇多糖干预后线虫体内的SOD水平相较空白对照组分别增加了13.58%、41.47%和48.45%。 表明香菇多糖能够有效提升线虫体内的SOD酶活力。SOD能催化O2-生成H2O2和O2,而CAT能进一步催化H2O2的分解生成H2O和O2,达到防止H2O2损害细胞的目的[26]。由图4a可知,线虫体内的CAT水平经香菇多糖干预72 h后较空白组分别提高了6.63%、59.19%和111.24%。 表明香菇多糖能够增强线虫体内的CAT酶活力。
MDA作为脂质氧化的代谢产物之一,其在生物体内的水平也可以直接作为衡量抗氧化能力的指标之一。由图4b可知,以不同香菇多糖质量浓度进行干预的线虫体内MDA含量较空白组降低了18.50%、40.51%和44.08%。 表明香菇多糖能显著降低线虫体内的MDA含量。
通过线虫体内实验证实,香菇多糖展现出良好的抗氧化活性,能有效提升SOD与CAT这两种抗氧化酶的酶活性,从而减轻自由基引发的脂质过氧化损伤,降低氧化产物中MDA的含量。该结果表明,香菇多糖是一种能够激活机体内在抗氧化潜能中的活性成分,在抵抗氧化应激和延缓衰老相关领域具有重要的开发潜力。
3 结论
香菇富含多种活性成分,对其多糖的提取及活性研究具有重要意义。本研究对香菇多糖的提取进行单因素及响应面试验优化,得出最优提取工艺为:超声温度75 ℃、超声时间50 min、超声功率240 W、料液比1∶30(g∶mL)。在此优化条件下,香菇多糖得率为1.89%。最优提取工艺条件下评价了香菇多糖体外抗氧化活性,香菇多糖对DPPH、ABTS、羟基自由基清除率IC50值依次为1.91 mg/mL、0.58 mg/mL、0.16 mg/mL。以线虫作为体内抗氧化实验模型,通过检测其经过不同浓度香菇多糖喂养的线虫体内的抗氧化酶活性和丙二醛的含量。 结果表明,不同香菇多糖质量浓度干预后的成虫较空白组SOD、CAT的活性都有显著提升,氧化产物MDA含量明显受到抑制。结果表明,香菇多糖具有显著的抗氧化活性。
本研究不仅为香菇活性物质高效利用提供了理论依据,更为香菇精深加工产业的多元化发展奠定了理论基础。通过多糖提取的最优工艺及深入研究其抗氧化功能,有望开发出更多高附加值的香菇产品,推动香菇产业从传统的初级加工向精深加工转型升级,实现香菇产业的可持续发展。
[1]KAŁA K, KRAKOWSKA A, SZEWCZYK A, et al.Determining the amount of potentially bioavailable phenolic compounds and bioelements in edible mushroom mycelia of Agaricus bisporus,Cantharellus cibarius,and Lentinula edodes[J].Food Chem,2021,352:129456.
[2]WANG J M, ZHOU Z, DAN D, et al.Physicochemical properties and bioactivities of Lentinula edodes polysaccharides at different development stages[J].Int J Biol Macromol,2020,150:573-577.
[3]卢士军,李泰,孙君茂,等.香菇、杏鲍菇和金针菇的氨基酸组成与蛋白质含量评价[J].中国食用菌,2022,41(1):45-51.
[4]REN Z,LIU W,SONG X,et al.Antioxidant and anti-inflammation of enzymatic-hydrolysis residue polysaccharides by Lentinula edodes[J].Int J Biol Macromol,2018,120:811-822.
[5]CHEN S, LIU C, HUANG X, et al.Comparison of immunomodulatory effects of three polysaccharide fractions from Lentinula edodes water extracts[J].J Funct Food,2020,66:103791.
[6]李泉岑,肖嵋方,刘斌,等.食药用菌多糖经由肠道菌群调节脂质代谢的研究进展[J].食品工业科技,2022,43(16):476-485.
[7]SHENG K J,WANG C,CHEN B,et al.Recent advances in polysaccharides from Lentinus edodes(Berk.):Isolation,structures and bioactivities[J].Food Chem,2021,358:129883.
[8]秦令祥,周婧琦,崔胜文,等.超声波协同复合酶法提取香菇多糖的工艺优化[J].食品研究与开发,2018,39(19):63-67.
[9]奚灏锵,袁根良,杜冰,等.超高压提取香菇多糖的研究[J].现代食品科技,2010,26(9):991-993.
[10]张潇,李波,聂远洋,等.二段式超声辅助沸水提取香菇多糖工艺研究[J].中国果菜,2024,44(7):29-33.
[11]李泉岑,蔡雯雯,李娜,等.响应面法优化香菇多酚提取工艺及稳定性研究[J].食品科技,2022,47(5):230-237.
[12]SIGMOND T,BARNA J,TÓTH M L,et al.Autophagy in Caenorhabditis elegans[J].Method Enzymol,2008,451:521-540.
[13]肖嵋方,陈欣彤,蔡雯雯,等.竹荪水提物抗氧化及改善秀丽隐杆线虫脂质代谢作用[J].食品科学,2022,43(19):191-199.
[14]刘慧敏.香菇多糖对氟吡菌酰胺致秀丽隐杆线虫毒性的保护作用研究[D].泰安:山东农业大学,2023.
[15]王力,肖嵋方,陈弘培,等.牡蛎多肽组分OE-I抗氧化活性及其对秀丽隐杆线虫抗衰老作用[J].食品科学,2022,43(3):152-160.
[16]林志银.鸡蛋卵白蛋白刺激对秀丽隐杆线虫固有免疫的影响及机制初探[D].南昌:南昌大学,2022.
[17]许欢怡,赖美英,刘斌,等.猴头菇多糖提取及抗氧化和降脂活性研究[J].食品科技,2023,48(12):205-213.
[18]滕春丽,颜蜜,向瑞琪,等.红托竹荪多糖的提取优化及膜分级分离的研究[J].食品安全质量检测学报,2021,12(12):4984-4990.
[19]孙晗,谢春阳,傅俊曦,等.响应面试验优化超声辅助法提取黄秋葵多糖工艺及对多糖脱色工艺的研究[J].陕西农业科学,2022,68(3):62-69.
[20]SUN H Y,LI C,NI Y,et al.Ultrasonic/microwave-assisted extraction of polysaccharides from Camptotheca acuminata fruits and its antitumor activity[J].Carbohydr Polym,2019,206:557-564.
[21]王君,陈新,高文彬,等.响应面法优化超声辅助提取金丝皇菊多糖工艺及生理活性研究[J].中国食品添加剂,2022,33(2):100-109.
[22]龚频,王佩佩,同美霖,等.红枣多糖的提取工艺及药理活性研究[J].食品工业科技,2022,43(13):198-207.
[23]刘馥源,黄占旺,沈勇根,等.香菇多酚超声波提取工艺及抗氧化性分析[J].中国调味品,2022,47(3):14-20.
[24]侯银臣,叶树才,梁金明,等.长根菇多糖提取工艺及其抗氧化活性研究[J].食品科技,2022,47(4):203-208.
[25]袁牧,王昌留,王一斐,等.超氧化物歧化酶的研究进展[J].中国组织化学与细胞化学杂志,2016,25(6):550-558.
[26]于德玲,王昌留.过氧化氢酶的研究进展[J].中国组织化学与细胞化学杂志,2016,25(2):189-194.