麦芽作为啤酒酿造的关键原料之一,其风味特征直接决定了啤酒的麦芽香气强度[1-2],在制麦过程中,美拉德反应生成的挥发性化合物是麦芽风味的重要组成部分。麦芽的制备主要分为浸麦、发芽、凋萎、焙焦四个阶段,在发芽阶段,淀粉和蛋白质被分解为美拉德反应所需的底物还原糖和氨基酸[3-4],这些底物在烘焙过程中通过美拉德反应转化为麦芽香风味物质。发芽过程中底物的生成与酶活性密切相关[5]。 已有研究表明[6-10],浸麦度、pH值、赤霉素以及金属离子(如Mg2+、Zn2+)能够显著影响绿麦芽中淀粉酶活性和还原糖的生成。焙焦过程是大多数麦芽产生挥发性风味物质的关键步骤,也是影响啤酒风味的重要过程。为了保证麦芽中酶的活性,温度按特定程序升高,通常从50 ℃开始,随后将温度升高到85 ℃以上以产生麦芽的特征香气和颜色[11]。 HUANG S X等[12]利用Box-Behnken响应面法分析研究了麦芽干燥及焙焦条件对淡麦芽风味形成的影响,发现较高的焙焦强度会增加甜味相关的化合物如呋喃酮的浓度。目前的研究主要集中于不同制麦工艺对美拉德反应底物或麦芽风味物质生成的影响[13],但不同制麦工艺对制麦过程淀粉酶(底物影响关键因素)、还原糖(底物)、麦芽香物质的变化规律和三者间的内在联系鲜有研究。 探究三者的内在联系,一方面有益于从影响麦芽酶活的角度,优化制麦工艺以提升麦芽的风味品质;另一方面,也为通过控制制麦过程中麦芽香物质前体物(还原糖)及其影响因素(淀粉酶活性)来确保麦芽风味的一致性和稳定性提供科学依据。
因此,本研究通过调控影响淀粉酶活性的制麦工艺,包括浸麦度(42%、45%)、浸麦水pH(6.5、8.5)、发芽过程添加酶激活剂(赤霉素、Mg2+)、焙焦温度(83 ℃、88 ℃),对制麦不同阶段麦粒的淀粉酶活性、还原糖、关键麦芽香特征物质含量进行测定,系统研究制麦过程中麦粒淀粉酶活性、还原糖和麦芽香物质含量变化规律和三者的内在联系,优化制麦工艺,为麦芽风味品质的控制和提升提供理论支撑。
1 材料与方法
1.1 材料与试剂
Copelemd大麦:欧麦(保定)麦芽有限公司;乙醚、柠檬酸、氢氧化钠、氯化钠、无水硫酸钠、氯化镁(均为分析纯):国药集团化学试剂有限公司;2-辛醇、2,5-二甲基-4-羟基-3(2H)-呋喃酮(2,5-dimethyl-4-hydroxy-3(2H)-furanone,DMHF)、麦芽酚、2-乙酰吡咯、苯乙醛、3-甲硫基丙醛(纯度>99%):美国Sigma Aldrich贸易公司;2-乙基-3,5(6)-二甲基吡嗪(纯度>98%):上海阿拉丁生化科技股份有限公司;赤霉素(纯度>90%):生工生物工程(上海)股份有限公司;3,5-二硝基水杨酸(3,5-dinitrosalicylic acid,DNS)(纯度>98%)、D(+)-无水葡萄糖(>98%)、可溶性淀粉(分析纯):北京索莱宝科技有限公司。
1.2 仪器与设备
7890-5977气相色谱-质谱联用(gas chromatographymass spectrometry,GC-MS)仪、DB-WAX毛细管色谱柱(30 m×0.25 mm,0.25 μm)、1260高效液相色谱(high performance liquid chromatography,HPLC)仪:美国Agilent公司;KrmasiL 100-NH2(4.6 mm×250 mm,5 μm):瑞典KrmasiL公司;Milli-Q超纯水系统:美国Millipore公司;UVmini-1280紫外分光光度计:日本岛津公司;MIR-253g型生化培养箱:日本三洋电机贸易株式会社。
1.3 方法
1.3.1 麦芽制备
加麦Copelemd大麦采用“4浸4断”浸麦工艺,将大麦浸泡在自来水(pH值为7.8)中,用柠檬酸、氢氧化钠调节浸麦水的pH值为GB 5749—2022《生活饮用水卫生标准》的上限8.5和下限6.5[14]。 通过调整浸湿时间来调节浸麦度(42%、45%),在最后一次浸麦时以喷淋方式添加Mg2+和赤霉素,质量浓度分别为80 mg/kg、0.4 mg/kg[15]。 随后将大麦置于15 ℃恒温恒湿生化培养箱中发芽110 h,取出麦芽低温焙焦(88 ℃或83 ℃)5 h。 待烘干结束麦芽冷却后,迅速将干麦芽的根去除,除根后的凋萎及焙焦麦芽保存于4 ℃冰箱备用。分别取浸麦后、发芽后麦芽冻干,于-20 ℃冰箱备用。 在检测前将浸麦后及发芽后冻干麦粒、凋萎和焙焦后麦芽进行粉碎,即得不同阶段麦芽样品。考察不同制麦工艺对麦芽淀粉酶活性和还原糖含量的影响,具体分组情况见表1。
表1 制麦工艺条件及分组
Table 1 Malting technology conditions and grouping
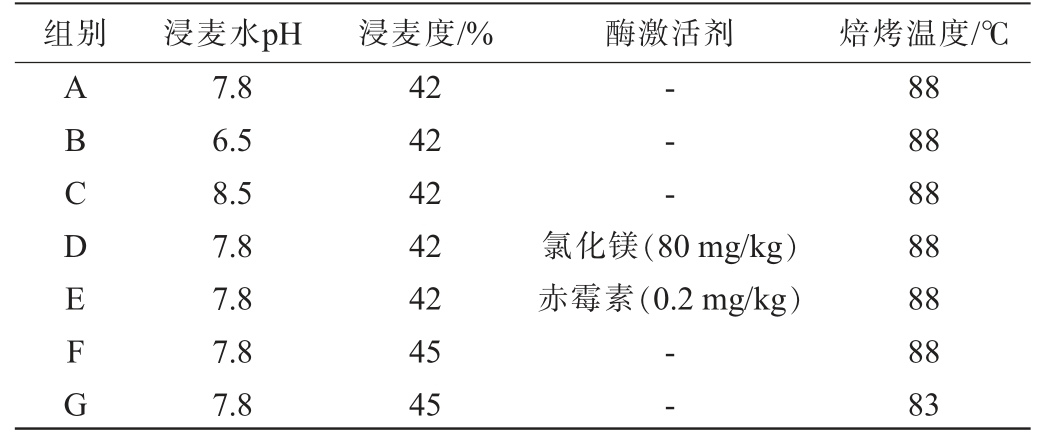
组别 浸麦水pH 浸麦度/% 酶激活剂 焙烤温度/℃ABCDEFG 7.8 6.5 8.5 7.8 7.8 7.8 7.8 42 42 42 42 42 45 45-- -氯化镁(80 mg/kg)赤霉素(0.2 mg/kg)--88 88 88 88 88 88 83
1.3.2 关键麦芽香特征物质含量测定
样品前处理:向1 g麦芽粉中加入10 mL去离子水和5 mL乙醚,室温下搅拌1 h,于4 ℃冰箱中过夜,收集上层有机相,0.22 μm滤膜过滤加入无水硫酸钠去除水分,将提取液浓缩备用[16]。 取萃取液1 μL直接进样至GC-MS进行气质检测。
GC条件:DB-WAX毛细管色谱柱(30 m×0.25 mm,0.25 μm);升温程序为初始温度40 ℃,保持3 min,以2 ℃/min升到230 ℃,保持5 min;进样口温度240 ℃;分流进样,分流比为10∶1;载气为高纯氦气(He)(纯度≥99.99%),流速为1 mL/min。
MS条件:温度为150 ℃;电子电离(electron ionization,EI)源,电子能量70eV;离子源温度为230℃;接口温度260℃;全扫描模式,扫描范围为33~280 m/z。
定性定量方法:参考文献[11,17],得到6种关键麦芽香特征物质(DMHF、2-乙基-3,5(6)-二甲基吡嗪、麦芽酚、2-乙酰吡咯、苯乙醛、3-甲硫基丙醛)。 采用6种物质标品的保留时间与质谱图离子比对定性。 采用选择离子监测(selectedionmonitor,SIM)模式扫描定量。DMHF、2-乙基-3,5(6)-二甲基吡嗪、麦芽酚、2-乙酰吡咯、苯乙醛、3-甲硫基丙醛的定量离子分别为128 m/z、135 m/z、126 m/z、109 m/z、91 m/z、104 m/z。
1.3.3 麦芽淀粉酶酶活检测
麦芽淀粉酶提取[18]:向1 g原大麦、浸麦后、发芽后、凋萎后和焙焦后麦芽粉中分别加入10 mL的醋酸-醋酸钠缓冲液(pH 5.5),冰浴条件下(0 ℃)浸提1 h,8 000 r/min离心15 min,移取上清液于离心管中作为粗酶液(A液),4 ℃冷藏。
总淀粉酶活性测定[19]:将A液稀释500倍得B液。 1 mL B液与1 mL 1%的可溶性淀粉溶液在40 ℃水浴中准确保温反应5 min,随后利用DNS法测定反应生成的还原糖含量。一个单位的酶活被定义为1 g(干质量)的麦芽在规定的测定条件下每分钟催化产生1 mg还原糖的酶量。计算公式如下:
式中:W为还原糖含量,g/mL;V为酶液总体积,mL;N为稀释倍数;V1为反应酶液体积,mL;T为反应时间,min;M为大麦或麦芽质量,g。
α-淀粉酶和β-淀粉酶活性测定:将A液置于70 ℃水浴锅中保持15 min钝化β-淀粉酶活性得C液。将C液稀释200倍后,再用DNS法测定反应生成的还原糖,得α-淀粉酶活性。总淀粉酶活性减去α-淀粉酶活性得β-淀粉酶活性。
1.3.4 麦芽中还原糖含量检测
根据GB 5009.8—2016《食品安全国家标准 食品中果糖、葡萄糖、蔗糖、麦芽糖、乳糖的测定》对麦芽中糖含量进行测定。
1.3.5 数据处理
采用SPSS 24软件进行数据处理及统计分析,采用Prism软件制图。所有试验均重复3次,结果取平均值。
2 结果与分析
2.1 不同制麦工艺对麦粒淀粉酶活性的影响
为确定不同制麦工艺对淀粉酶活性的影响,对不同制麦工艺下不同阶段麦粒的淀粉酶活性进行测定,结果见图1和图2。
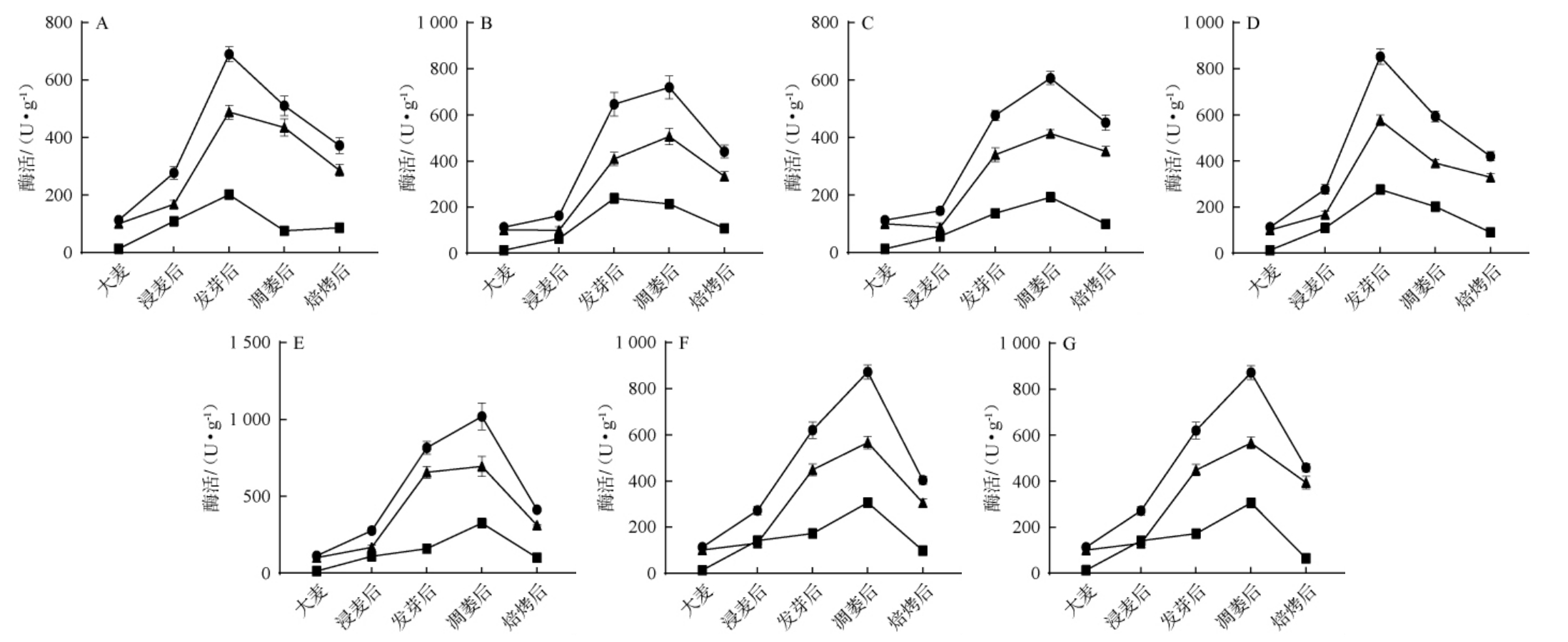
图1 不同制麦工艺条件制麦过程中麦芽淀粉酶酶活变化
Fig.1 Changes in malt amylase activities during malting process under different malting technology conditions
、 、 分别代表总淀粉酶活性、α-淀粉酶活性和β-淀粉酶活性。A~G分别代表表1中不同组别的工艺条件。
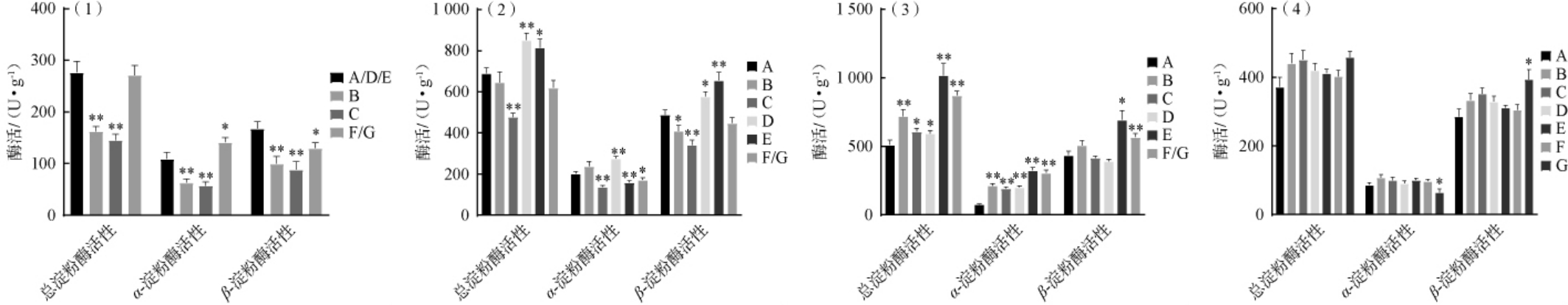
图2 不同制麦工艺条件对制麦过程中麦芽淀粉酶活性的影响
Fig.2 Effect of different malting technology conditions on the malt amylase activities during malting process
(1)~(4)分别代表浸麦后、发芽后、凋萎后和焙焦后的麦粒淀粉酶活性。 “*”表示与实验组A相比差异显著(P<0.05),“**”表示与实验组A相比差异极显著(P<0.01)。图4同。
由图1可知,整个制麦过程麦粒的淀粉酶活性呈先上升后下降的趋势,且β-淀粉酶活性始终高于α-淀粉酶,浸麦和发芽过程为麦粒淀粉酶激活阶段,焙焦为麦粒淀粉酶活性降低阶段。浸麦阶段淀粉酶活性增长缓慢,发芽阶段淀粉酶活性大幅升高,与浸麦阶段相比,发芽后A~G组麦芽总淀粉酶活力分别增长1.49倍、2.97倍、2.28倍、2.08倍、1.94倍、1.29倍、1.29倍。麦芽凋萎阶段温度为50~60 ℃,此时水分降低,麦粒生长趋于停止。但制麦工艺不同,凋萎过程淀粉酶活性的变化规律存在差异,与发芽后麦粒相比,凋萎后B、C、E、F、G组麦粒淀粉酶活性显著增高,A、D组麦粒淀粉酶活性显著降低。与α-淀粉酶相比β-淀粉酶的热稳定性较好[3,20],除C和G组,α-淀粉酶活性下降快于β-淀粉酶。 焙焦阶段温度为64~88 ℃,在该温度下各组麦粒淀粉酶活性均显著降低。与凋萎后麦芽相比,焙焦后A~G组麦芽总淀粉酶活力分别降低27.09%、38.72%、25.53%、29.14%、59.58%、53.83%、47.41%。综上,浸麦和发芽过程为麦粒淀粉酶激活阶段,焙焦为麦粒淀粉酶活性降低阶段,凋萎过程酶活的变化受制麦工艺影响。
进一步对不同制麦工艺下麦粒的淀粉酶活进行差异分析,结果见图2。 由图2可知,pH值是调控麦芽发芽关键酶活性以及代谢途径的重要环境因子。 与A组相比,升高(C组)和降低(B组)浸麦水pH均可极显著降低浸麦后麦粒总淀粉酶、α-淀粉酶和β-淀粉酶活性(P<0.01),显著或极显著增加凋萎后麦芽总淀粉酶、α-淀粉酶活性(P<0.05,P<0.01)。适当碱液浸麦可轻微腐蚀谷壳,使水分更均匀快速的渗透到麦胚中,麦粒溶解效率高,从而使得淀粉酶的活性升高。 所以浸麦水pH的影响可能是通过提高麦粒的水敏感性间接影响淀粉酶的活性。对比实验组A、B、C,当浸麦水pH为6.5时,可使凋萎后麦芽总淀粉酶活性达到最高,为(719.45±49.58)U/g。
浸麦度是麦芽制备的关键参数,对比实验组A和F,提高浸麦度可极显著增加凋萎后麦芽总淀粉酶活、α-淀粉酶活、β-淀粉酶活(P<0.01)。浸麦度为45%时,凋萎后麦芽总淀粉酶活最高,为(872.28±30.58)U/g。
赤霉素是大麦发芽过程中产生的植物激素,可诱导α-淀粉酶、蛋白酶、脱支酶等多种酶类的形成,是目前啤酒工业上常用的添加剂[15]。金属离子可与酶分子上的氨基酸侧链基团、酶或底物的中间物结合,或作为辅酶或辅基的一个组成部分激活酶[21]。与A组相比,添加赤霉素极显著增加发芽后β-淀粉酶、凋萎后麦芽总淀粉酶和α-淀粉酶活性(P<0.01),显著增加发芽后麦芽总淀粉酶和凋萎后β-淀粉酶活性(P<0.05);添加Mg2+可极显著增加发芽后麦芽总淀粉酶和α-淀粉酶、凋萎后α-淀粉酶活性(P<0.01),显著增加发芽后β-淀粉酶活性和凋萎后麦芽总淀粉酶活性(P<0.05)。发芽过程酶激活剂的添加对发芽和凋萎后麦粒淀粉酶活性起到明显的促进作用。对比实验组A、D和E,添加赤霉素使凋萎后麦芽的总淀粉酶活最高,为(1 019.26±87.02)U/g。
由图2(4)可知,对比实验组F和G,降低焙焦温度可显著提高麦芽的β-淀粉酶活性,降低α-淀粉酶活性(P<0.05),83 ℃焙焦条件下麦芽β-淀粉酶活性为(394.10±27.80)U/g。
综上,提高或降低浸麦水pH,添加酶激活剂(赤霉素和Mg2+)、提高浸麦度及降低焙焦温度对凋萎后麦芽的淀粉酶,特别是α-淀粉酶活性的促进作用显著。
2.2 不同制麦工艺对还原糖含量的影响
不同制麦工艺下不同阶段麦粒的还原糖含量测定结果见图3。

图3 不同制麦工艺条件制麦过程中麦芽还原糖含量变化
Fig.3 Changes in reducing sugar contents during malting process under different malting technology conditions
 、
、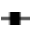 、
、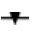 分别代表果糖、葡萄糖和麦芽糖的含量。
分别代表果糖、葡萄糖和麦芽糖的含量。
由图3可知,还原糖作为淀粉酶催化淀粉水解的主要产物,其变化趋势与淀粉酶活一致,浸麦及发芽阶段为还原糖生成阶段,焙焦阶段为还原糖消耗阶段。不同制麦工艺对还原糖含量的影响存在差异,结果见表2。由表2可知,与A组相比,升高(C)和降低(B)浸麦水pH均可抑制麦芽浸麦过程果糖、葡萄糖的生成,促进麦芽糖的生成;促进发芽过程果糖、葡萄糖、麦芽糖生成;促进焙焦过程果糖、葡萄糖的消耗。与A组相比,B组焙焦过程三种还原糖的消耗分别增加142.86%、74.16%、20.00%,C组分别增加50.00%、31.46%、392.50%。
表2 不同制麦工艺条件对制麦过程中还原糖含量的影响
Table 2 Effect of different malting technology conditions on reducing sugar contents during malting process g/100 g
注:正数为生成量,负数为消耗量。
阶段 还原糖种类A B C D E F G浸麦发芽凋萎焙焦果糖葡萄糖麦芽糖果糖葡萄糖麦芽糖果糖葡萄糖麦芽糖果糖葡萄糖麦芽糖0.20±0.08 0.81±0.11 0.46±0.09 0.31±0.09 2.09±0.54 1.00±0.03-0.03±0.12 0.73±0.62 1.22±0.43-0.14±0.08-0.89±0.15-0.51±0.12 0.09±0.06 0.64±0.12 0.64±0.07 0.48±0.05 2.69±0.65 1.58±0.17 0.01±0.02 0.68±0.20 0.37±0.19-0.34±0.05-1.55±0.42-0.18±0.34 0.03±0.05 0.58±0.10 0.73±0.12 0.48±0.38 2.60±0.42 1.27±0.39-0.05±0.09 0.34±0.24 0.31±0.33-0.21±0.08-1.17±0.58-0.08±0.36 0.20±0.08 0.81±0.11 0.46±0.09 0.37±0.12 2.54±0.44 1.43±0.23-0.08±0.09 0.30±0.29 0.72±0.40-0.27±0.03-1.07±0.18-0.08±0.55 0.20±0.08 0.81±0.11 0.46±0.09 0.50±0.11 3.21±0.66 2.11±0.67-0.19±0.09 0.19±0.30 0.01±0.19-0.31±0.06-1.79±0.22 0.19±0.21 0.03±0.01 0.36±0.13 0.63±0.09 0.71±0.12 3.14±0.39 1.20±0.23-0.35±0.09-0.35±0.28 0.28±0.16-0.09±0.11-0.65±0.30-0.35±0.12 0.03±0.01 0.36±0.13 0.63±0.09 0.71±0.12 3.14±0.39 1.20±0.23-0.35±0.09-0.35±0.28 0.28±0.16-0.12±006-0.42±0.24 0.73±036
对比实验组A、D、E和F,发芽过程添加酶激活剂(D和E组)和提高浸麦度(F组)可促进麦芽发芽过程果糖、葡萄糖、麦芽糖生成。添加酶激活剂(D和E组)可促进焙焦过程果糖、葡萄糖的消耗,与A组相比,D组焙焦过程三种还原糖的消耗分别增加92.86%、20.22%、25.00%,E组分别增加121.42%、101.12%、17.50%。说明发芽过程添加酶激活剂和增加浸麦度可增加焙焦阶段还原糖的利用率。
对比实验组F和G,降低焙焦温度促进果糖消耗,抑制葡萄糖、麦芽糖消耗。
综上,提高或降低浸麦水pH,添加酶激活剂(赤霉素和Mg2+)、提高浸麦度及升高焙焦温度会提高麦粒发芽过程中还原糖含量,促进焙焦阶段对麦芽还原糖的利用率。
2.3 不同制麦工艺对关键麦芽香特征物质的影响
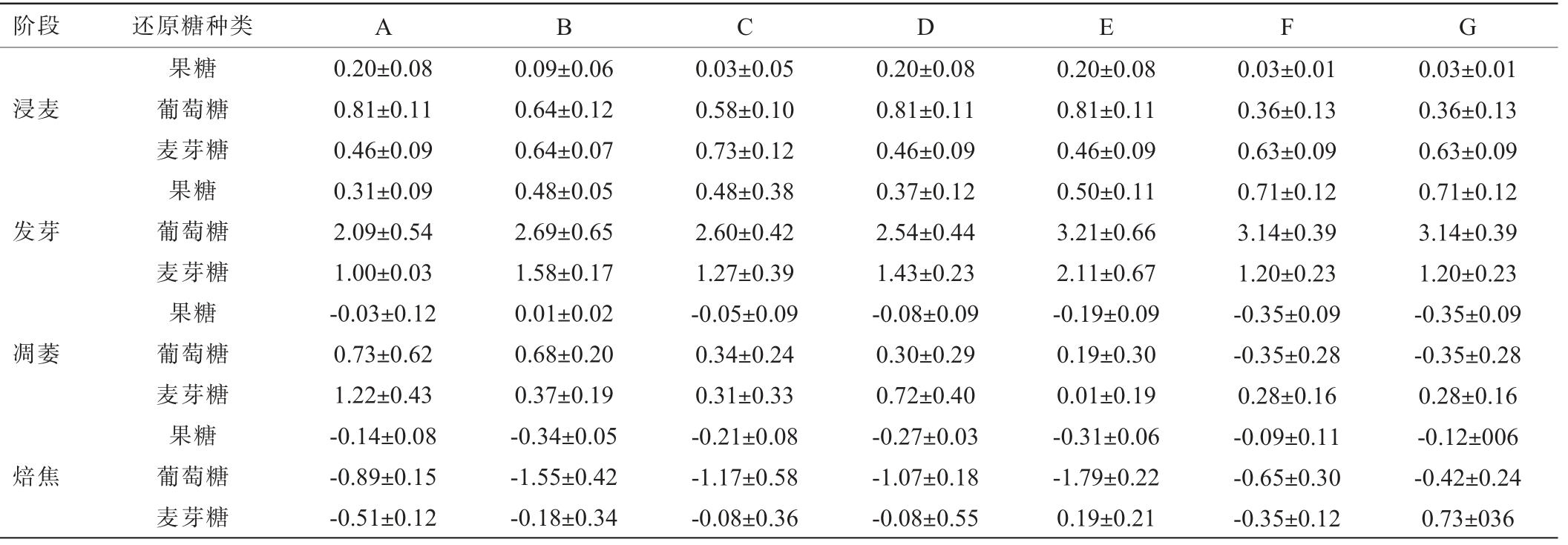
焙焦过程是整个制麦过程中香气物质形成的关键步骤,为进一步确定不同制麦工艺对风味物质生成的影响,对焙焦过程生成的关键麦芽香特征物质[11,17]包括含氧杂环(DMHF、麦芽酚)、含氮杂环(2-乙酰吡咯、2-乙基-3,5(6)-二甲基吡嗪)、醛类(3-甲硫基丙醛、苯乙醛)的含量进行测定,结果见图4。
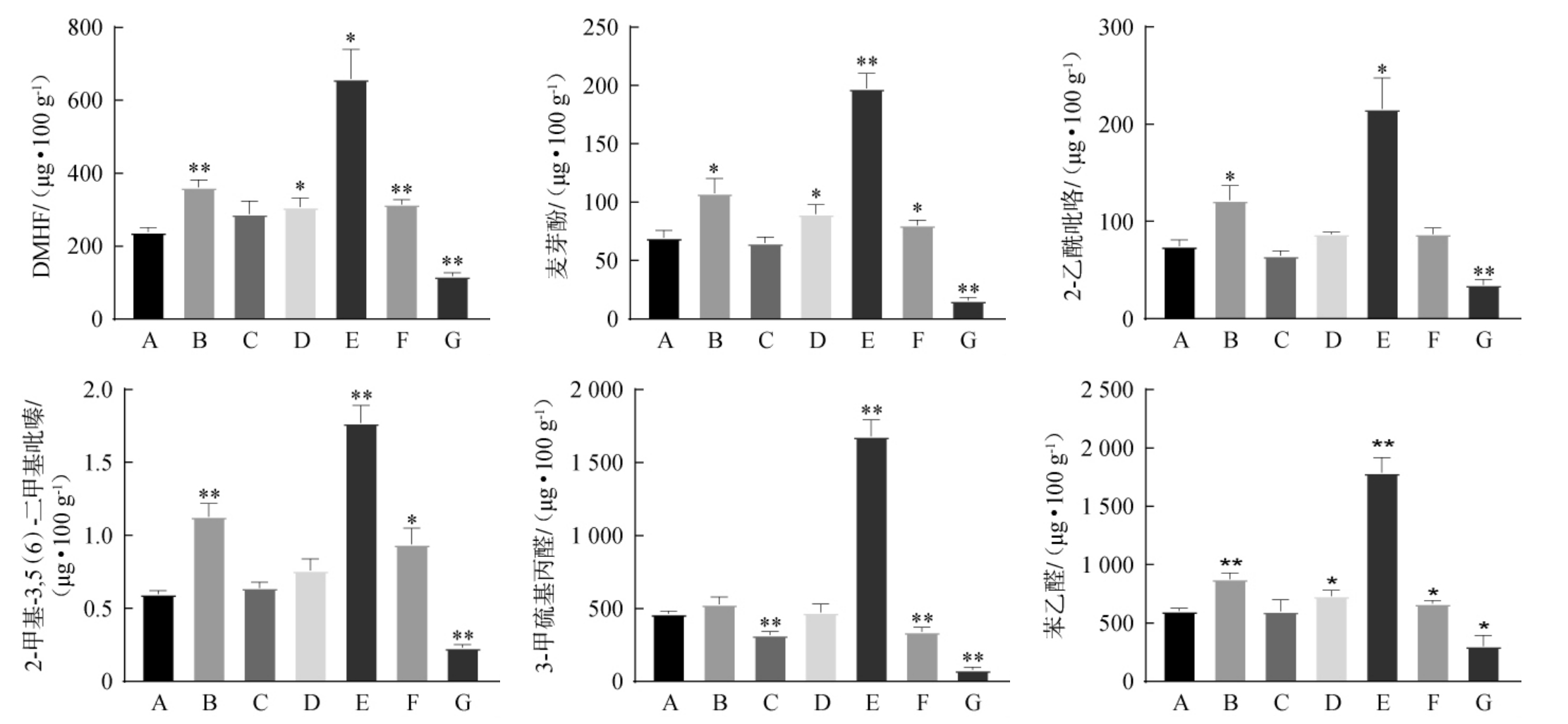
图4 不同制麦工艺条件对关键麦芽香特征物质含量的影响
Fig.4 Effect of different malting technology conditions on key malt aroma compounds contents at different stages
由图4可知,在焙焦强度一致的情况下,对比实验组A、B、C,降低浸麦水pH可增加6种麦芽香特征物质的含量,实验组B麦芽中6种麦芽香特征物质的总量为(1 999.52±152.47)μg/100 g,为A组的1.38倍;升高浸麦水pH对其影响不大。 对比实验组A和F,除3-甲硫基丙醛含量降低外,提高浸麦度可增加其他5种麦芽香特征物质的含量,实验组F麦芽中6种麦芽香特征物质的总量为(1492.82±77.75)μg/100g。对比实验组A和E,添加赤霉素可显著或极显著增加6种麦芽香特征物质的含量(P<0.05或P<0.01),此时麦芽中6种特征物质生成量为(4 542.57±201.33)μg/100 g,为A组的3.13倍。 对比A组和D组,添加氯化镁可显著增加DMHF、麦芽酚、苯乙醛的含量(P<0.05);对比F组和G组,降低焙焦温度减少了麦芽香特征物质的释放,实验组F麦芽中6种关键麦芽香特征物质生成量为G组的2.70倍。综上,不同制麦工艺中,降低浸麦水pH、添加酶激活剂(赤霉素、Mg2+)、升高焙焦温度对提升制麦过程麦芽香特征物质的生成优于其他组别,推测促进麦芽酶活性及增加美拉德反应强度的制麦工艺可增加麦芽中风味物质的含量。
2.4 淀粉酶活、还原糖、关键麦芽香特征物质相关性分析
在凋萎及焙焦过程麦芽中的还原糖、醛、酮与游离氨基酸、肽、蛋白质之间发生美拉德反应生成一系列芳香化合物,是麦芽风味物质形成的关键步骤[13,24]。美拉德反应底物(还原糖)消耗量与关键麦芽香特征物质生成量的相关性分析见表3。 由表3可知,葡萄糖的消耗量与关键麦芽香特征物质的生成量呈极显著正相关(P<0.01)。有研究表明,美拉德的反应速率与底物糖的种类和结构有关,还原糖含量与褐变速度呈正相关,单糖的反应速率大于双糖[22]。此外,与麦芽糖相比,单糖产生的风味更好[23]。综上,葡萄糖的消耗与关键麦芽香特征物质的生成具有密切关系,推测在制麦过程中葡萄糖为关键麦芽香特征物质的主要前体物质。
表3 还原糖与关键麦芽香特征物质相关性分析
Table 3 Correlation analysis between reducing sugar and key malt aroma compounds

注:“*”表示相关性显著(P<0.05);“**”表示相关性极显著(P<0.01)。
项目 果糖消耗量葡萄糖消耗量麦芽糖消耗量DMHF生成量麦芽酚生成量2-乙酰吡咯生成量2-乙基-3,5(6)-二甲基吡嗪生成量3-甲硫基丙醛生成量苯乙醛生成量果糖消耗量葡萄糖消耗量麦芽糖消耗量DMHF生成量麦芽酚生成量2-乙酰吡咯生成量2-乙基-3,5(6)-二甲基吡嗪生成量3-甲硫基丙醛生成量苯乙醛生成量1 0.290-0.653 0.362 0.307 0.387 0.378 0.353 0.387 1 0.034 0.909**0.904**0.913**0.920**0.832*0.894**1 0.103 0.158 0.061 0.171-0.016 0.019 1 0.990**0.982**0.979**0.957**0.988**1 0.989**0.980**0.960**0.987**1 0.980**0.968**0.992**1 0.911**0.961**1 0.987** 1
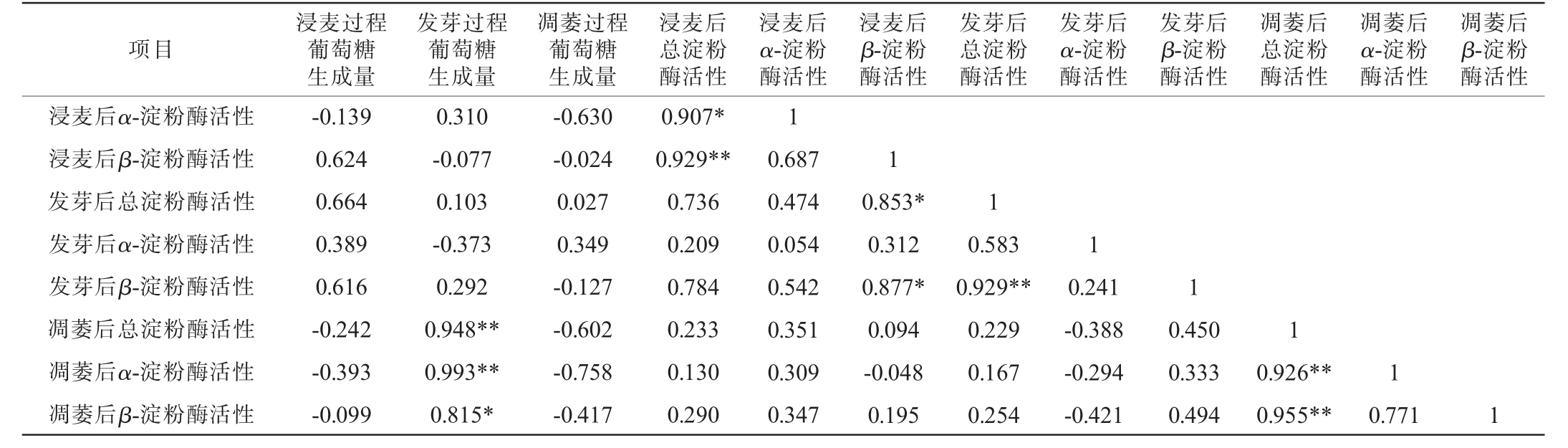
大麦在发芽过程中具有一定量的淀粉酶与蛋白质分解酶,在适宜的温度与pH下其内部的酶分解淀粉与蛋白质,生成还原糖与氨基酸,为后续焙焦时关键麦芽香特征物质的形成提供物质基础。一般认为大麦发芽强度是影响麦芽中美拉德反应的底物(游离氨基酸和还原糖)组成的重要因素,发芽强度的提高会增加美拉德底物的含量,促进美拉德反应从而形成更多的风味物质[25]。结合表3,对制麦过程中淀粉酶活性和关键麦芽香特征物质的主要前体物质(葡萄糖)进行相关性分析,结果见表4。由表4可知,发芽过程中葡萄糖的生成量与凋萎末期总淀粉酶、α-淀粉酶活性呈极显著正相关(P<0.01),与β-淀粉酶活性呈显著正相关(P<0.05)。说明凋萎后的麦芽淀粉酶活性决定麦芽的美拉德反应底物(还原糖)的含量。 对凋萎后淀粉酶活性与关键麦芽香特征物质进行相关性分析,结果见表5。
表4 淀粉酶活性与葡萄糖生成量相关性分析
Table 4 Correlation analysis between amylase activity and glucose production
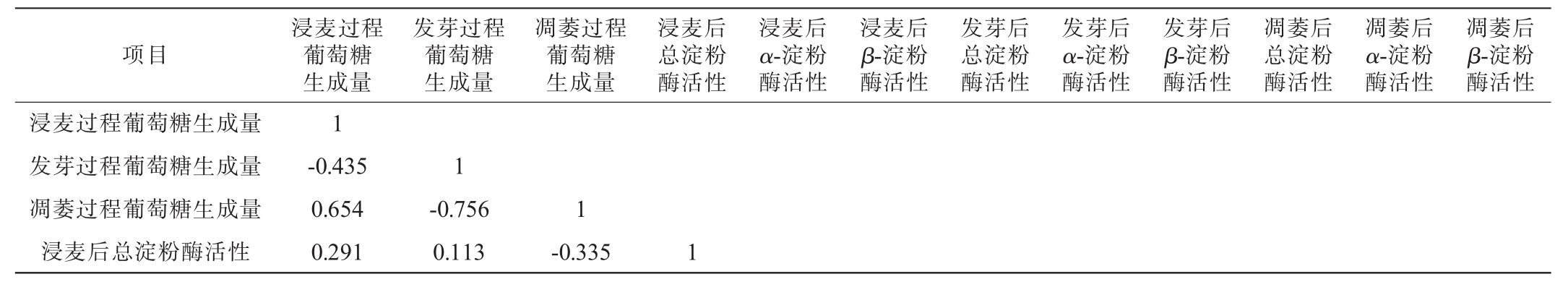
项目浸麦过程葡萄糖生成量发芽过程葡萄糖生成量凋萎过程葡萄糖生成量浸麦后总淀粉酶活性浸麦后α-淀粉酶活性浸麦后β-淀粉酶活性发芽后总淀粉酶活性发芽后α-淀粉酶活性发芽后β-淀粉酶活性凋萎后总淀粉酶活性凋萎后α-淀粉酶活性凋萎后β-淀粉酶活性浸麦过程葡萄糖生成量发芽过程葡萄糖生成量凋萎过程葡萄糖生成量浸麦后总淀粉酶活性1-0.435 0.654 0.291 1-0.756 0.113 1-0.335 1
续表
项目浸麦过程葡萄糖生成量发芽过程葡萄糖生成量凋萎过程葡萄糖生成量浸麦后总淀粉酶活性浸麦后α-淀粉酶活性浸麦后β-淀粉酶活性发芽后总淀粉酶活性发芽后α-淀粉酶活性发芽后β-淀粉酶活性凋萎后总淀粉酶活性凋萎后α-淀粉酶活性凋萎后β-淀粉酶活性浸麦后α-淀粉酶活性浸麦后β-淀粉酶活性发芽后总淀粉酶活性发芽后α-淀粉酶活性发芽后β-淀粉酶活性凋萎后总淀粉酶活性凋萎后α-淀粉酶活性凋萎后β-淀粉酶活性-0.139 0.624 0.664 0.389 0.616-0.242-0.393-0.099 0.310-0.077 0.103-0.373 0.292 0.948**0.993**0.815*-0.630-0.024 0.027 0.349-0.127-0.602-0.758-0.417 0.907*0.929**0.736 0.209 0.784 0.233 0.130 0.290 1 0.687 0.474 0.054 0.542 0.351 0.309 0.347 1 0.853*0.312 0.877*0.094-0.048 0.195 1 0.583 0.929**0.229 0.167 0.254 1 0.241-0.388-0.294-0.421 1 0.450 0.333 0.494 1 0.926**0.955**1 0.771 1
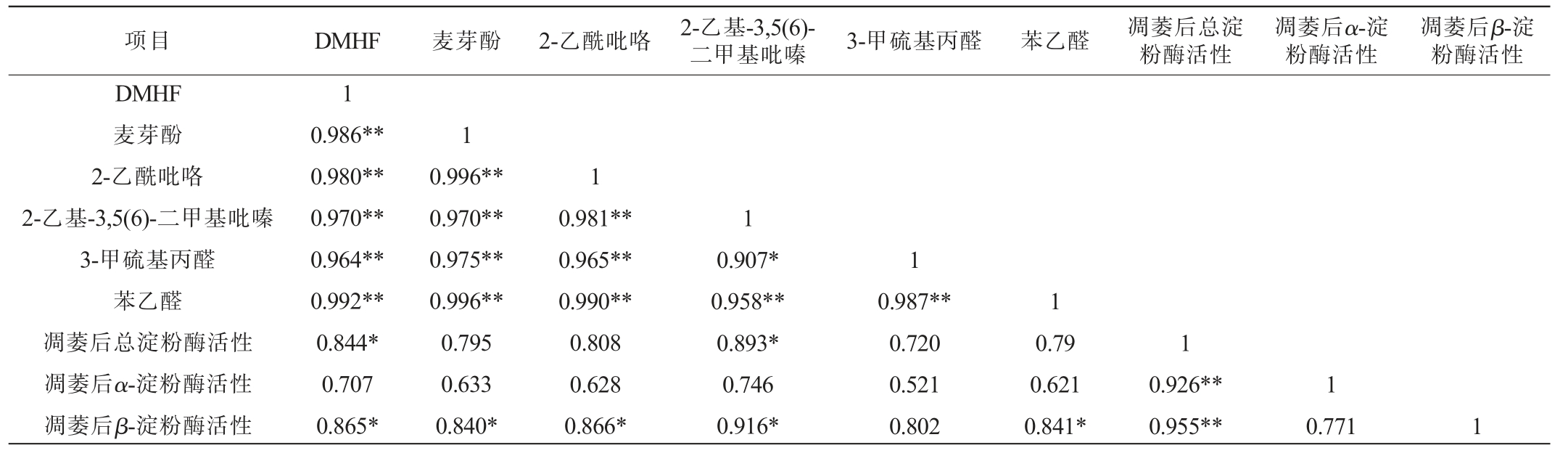
表5 淀粉酶活性与关键麦芽香特征物质生成量相关性分析
Table 5 Correlation analysis between amylase activity and key malt aroma compounds production
项目 DMHF 麦芽酚 2-乙酰吡咯 2-乙基-3,5(6)-二甲基吡嗪 3-甲硫基丙醛 苯乙醛 凋萎后总淀粉酶活性凋萎后α-淀粉酶活性凋萎后β-淀粉酶活性DMHF麦芽酚2-乙酰吡咯2-乙基-3,5(6)-二甲基吡嗪3-甲硫基丙醛苯乙醛凋萎后总淀粉酶活性凋萎后α-淀粉酶活性凋萎后β-淀粉酶活性1 0.986**0.980**0.970**0.964**0.992**0.844*0.707 0.865*1 0.996**0.970**0.975**0.996**0.795 0.633 0.840*1 0.981**0.965**0.990**0.808 0.628 0.866*1 0.907*0.958**0.893*0.746 0.916*1 0.987**0.720 0.521 0.802 1 0.79 0.621 0.841*1 0.926**0.955**1 0.771 1
由表5可知,除3-甲硫基丙醛外,其余关键麦芽香特征物质生成量与凋萎后麦芽的β-淀粉酶活性呈显著正相关,DMHF和2-乙基-3,5(6)-二甲基吡嗪与凋萎后麦芽的总淀粉酶活呈显著正相关(P<0.05)。
综上,淀粉酶活性、葡萄糖含量与关键麦芽香特征物质的相关性分析结果见图5。
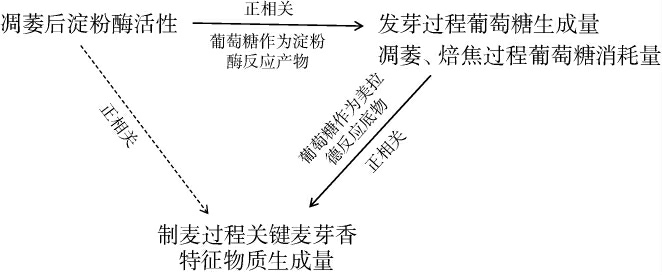
图5 淀粉酶活性、葡萄糖和关键麦芽香特征物质间的关系
Fig.5 Relationship between amylase activity, glucose and key malt aroma compounds
由图5可知,凋萎后的淀粉酶活性可表征浸麦和发芽过程中葡萄糖和焙焦过程中关键麦芽香特征物质的生成量。
3 结论
本研究通过调节制麦过程中浸麦度(42%、45%)、浸麦水pH(6.5、8.5)、添加酶激活剂(赤霉素、Mg2+)、焙焦温度(83 ℃、88 ℃),对不同制麦工艺下不同阶段麦粒的淀粉酶活性、还原糖含量进行测定。 采用GC-MS测定焙焦阶段关键麦芽香特征物质含量,并系统分析制麦过程中麦粒淀粉酶活性、还原糖和关键麦芽香特征物质含量变化的相关性。结果表明,降低浸麦水pH、发芽过程添加酶激活剂(赤霉素和Mg2+)、提高浸麦度及降低焙焦温度均可显著增加凋萎过程麦粒总淀粉酶活性、α-淀粉酶活性;促进发芽过程果糖、葡萄糖、麦芽糖生成及焙焦过程果糖、葡萄糖的消耗;提高关键麦芽香特征物质的生成。其中添加赤霉素的效果最优,凋萎后麦粒总淀粉酶活为(1 019.26±87.02)U/g,发芽阶段葡萄糖生成量为(3.21±0.66)g/100 g,焙焦阶段葡萄糖消耗量(1.79±0.30)g/100 g,6种关键麦芽香特征物质生成量为(4 542.57±201.33) μg/100 g。相关性分析表明,葡萄糖的消耗量与关键麦芽香特征物质的生成量呈正相关,凋萎后麦芽淀粉酶活性与葡萄糖生成量、关键麦芽香特征物质的生成量呈正相关。本研究通过作为美拉德反应底物和淀粉酶反应产物的葡萄糖为核心,搭建了制麦过程淀粉酶活性与关键麦芽香特征物质间的联系,为麦芽风味品质的控制和提升提供理论支撑。
[1]郭琪,王玉海,陈明,等.基于多维色谱技术的Lager啤酒特征香气成分解析[J].食品与发酵工业,2024:1-13.
[2]陈华磊,徐楠,杨朝霞.啤酒中麦芽风味的研究进展[J].中外酒业,2021(17):9-16.
[3]RANI H,BHARDWAJ R D,GREWAL S K,et al.Exploring the variation in α-amylase activity and thermostability in green malt of diverse barley(Hordeum vulgare L.)germplasm[J].J Plant Biochem Biot,2024,33(3):400-412.
[4]张翠,胡淑敏,黄树丽,等.啤酒大麦淀粉及内源淀粉酶研究进展[J].中外酒业·啤酒科技,2019(11):39-44.
[5]CAI K, WU X, YUE W, et al.Enzyme activities shape malting quality standards[J].Food Sci Nutr,2024,13(1):e4702.
[6]邵晔.小米发芽过程中淀粉酶系变化及酶活力的研究[D].沈阳:沈阳农业大学,2020.
[7]ZANAMWE P.The potential of ethylene as an alternative to GA3 treatment during malting of barley (Hordeum valgare)[J].Cereal Res Commun,2019,47(4):689-700.
[8]CHARLOTTE F D S, CHRISTOPHE M C.Reassessing the importance of barley starch and amylolytic enzyme properties in malting and brewing[J].Compr Rev Food Sci F,2024,23(6):70069.
[9]王特,薛永常.国内外不同品种啤酒大麦萌发过程中酶的变化[J].中国酿造,2011,30(3):51-54.
[10]VINKO K,IGOR H,KRESIMIR M,et al.Development of enzyme potential in different purpose barley varieties during malting[J].Glasnik Zaštite Bilja,2020,43(6):22-31.
[11]尹瑞旸,刘霞,郭立芸,等.美拉德反应对啤酒风味的影响研究进展[J].中国酿造,2023,42(12):1-8.
[12]HUANG S X,YU J,YIN H,et al.Optimization of kilning progress for equilibrating multiple parameters that strictly affect malt flavour and sensory evaluation[J].J I Brewing,2016,122(4):706-713.
[13]WANG X,LU J,CAI G,et al.Advances in Maillard reaction products on color,flavor and biological activity of specialty malt[J].Syst Microbiol Biom,2024,4(2):500-510.
[14]国家市场监督管理总局,国家标准化管理委员会.GB 5749—2022 生活饮用水卫生标准[S].北京:中国标准出版社,2023.
[15]赵旭乐,管斌,孔青,等.不同添加物对大麦发芽过程中热稳定蛋白含量的影响[J].中国酿造,2016,35(10):144-148.
[16]MICHAEL F,REGLITZ K,MALL V,et al.Molecular insights into the contribution of specialty barley malts to the aroma of bottom-fermented lager beers[J].J Agr Food Chem,2021,69(29):8190-8199.
[17]MA M T, CHEN Z Q, HUANG B, et al.Characterizing the key aroma compounds of barley malt from different origins using GC-E-Nose,HSSPME-GC-MS,and HS-GC-IMS[J].Food Biosci,2024,58:103707.
[18]何艳克,胡飞.大麦芽中淀粉酶系活力的测定及其作用特性[J].食品科学,2010,31(15):236-239.
[19]赵信池,周海龙,栾静,等.褐藻胶寡糖对大麦发芽水解酶活力和麦芽质量的影响[J].大连工业大学学报,2020,39(4):250-254.
[20]GEIINGER C,GASTL M,BECKER T.Enzymes from cereal and fusarium metabolism involved in the malting process-A review[J].J Am Soc Brew Chem,2022,80(1):1-16.
[21]董亮,赵长新,李峰,等.大麦发芽过程中添加金属离子对纤维素酶和蛋白酶活力影响研究[J].食品科技,2006(2):18-21.
[22]翟昕宇,邢晓睿,王睿粲,等.明胶-糖类互作对含糖凝胶理化特性及体外消化性的影响[J].食品工业科技,2025,46(5):99-107.
[23]YANG Y, WANG Y, QI D, et al.Color characteristics and pyrolysis volatile properties of main colored fractions from the Maillard reaction models of glucose with three amino acids[J].LWT-Food Sci Technol,2024,192(c):115739.
[24]陈文波,佟恩杰,苏红旭,等.特种麦芽品质形成机理分析及分类系统构建[J].中国酿造,2023,42(11):22-27.
[25]PRADO R, GASTL M, BECKER T.Influence of kilned specialty malt odorant markers on the aroma composition and sensory profile of beer[J].LWT-Food Sci Technol,2023,173:114195.