核桃是一种具有高营养价值的植物[1],也被称为“木本植物中的油料之王”[2],其油脂含有大量有益于身体健康的不饱和脂肪酸[3]。核桃粕是核桃油加工的副产品,其蛋白质含量丰富,并含有18种氨基酸[4],其中精氨酸、谷氨酸含量较高[5],长期食用对人体具有良好的保健效果[6]。然而,由于核桃粕质地较硬,成分复杂并带有残油的气味,难以直接作为食品供消费者使用,因此常被用作动物饲料或直接丢弃,造成资源浪费[7]。近年来,随着对核桃蛋白研究的深入,越来越多的学者开始关注核桃蛋白及其酶解产物的生物活性。 酶解技术作为一种有效的蛋白质改性方法,已被广泛应用于食品加工和营养保健品开发中[8]。通过酶解处理,可以将核桃粕中的大分子蛋白质降解为小分子多肽,这些小分子多肽不仅易于人体吸收,还具有特定的生物活性,如抗氧化、抗癌及促进细胞增殖等[9-10]。其中,促成骨细胞增殖活性对于骨骼健康及骨质疏松的预防和治疗具有重要意义[11]。
邓艳梅等[12]探究了热处理温度及均质方式对核桃蛋白稳定Pickering乳液性质的影响,发现50 ℃热处理后核桃蛋白制备的Pickering乳液经高速分散后综合性能最佳,储藏稳定性好。GUPTA A J等[13]研究结果表明,121 ℃/0~120 min下加热的膳食中产生水解产物。加热降低了膳食和水解物中的游离氨基酸及单糖含量。其中氨基酸含量分别从0.72%、14.7%降至0.27%、7.1%;单糖含量分别从3.3%、16.9%降至2.6%、7.9%。ZHAO X Y等[14]研究蒸烤处理对95 ℃不同时间(15 min、20 min和30 min)核桃仁理化和功能特性的影响。结果显示,热处理作为一种有效的方法可以改善核桃仁的物理化学、结构和功能特性,并有可能应用于食品加工。PAPOUTSI Z等[15]研究发现,核桃中没食子酸、咖啡酸和香豆酸等多酚类化合物对成骨细胞系中结节的形成具有积极作用。 李宇等[16]研究后得出,在大豆分离蛋白中有并且能分离出可以促进成骨细胞增殖的多肽。 热处理是食品加工中关键工艺环节,但热处理条件对核桃粕酶解产物的生物活性,特别是促成骨细胞增殖活性的影响有待进一步研究[17-18]。
该研究以核桃粕为原料制备核桃蛋白与酶解产物,进行不同条件的热处理,随后与成骨细胞共培养,观察其增殖效果。旨在探究不同热处理条件下对核桃蛋白与酶解产物的促成骨细胞增殖作用,从而推进核桃粕的高值化利用,为核桃粕在功能性食品研发上提供理论基础及保健品领域的应用提供新思路。
1 材料与方法
1.1 材料与试剂
核桃粕(食品级):石家庄复源科技有限公司;碱性蛋白酶(20万U/g):沧州众合众利生物制品有限公司;MC3T3-E1成骨细胞系:上海名劲有限公司;胰蛋白酶-乙二胺四乙酸(ethylene diamine tetraacetic acid,EDTA)、α-最低基础培养液(minimal essential medium,MEM):美国Hycone公司;青链霉素混合液:无锡菩禾生物医药技术有限公司;胎牛血素、磷酸盐缓冲液(phosphate-buffered saline,PBS)、噻唑蓝(thiazolylblue tetrazolium bromide,MTT)、伊红、巴比妥钠、硝酸钴、硫化铵(均为分析纯):天津市光复精细化工研究所。
1.2 仪器与设备
KNICK型pH计:深圳市上优泰科技有限公司;ROTINA-420型台式离心机:莱比信(中国)科技发展有限公司;DWPC-220A型多功能粉碎机:四川德维微纳有限公司;SZX-AR1型倒置式生物显微镜:北京创诚致佳科技有限公司;Absorbance96型酶标仪:德国Byonoy公司;XS-30W型冷冻干燥机:浙江翔盛净化有限公司;HD-MCP-170型细胞培养箱:山东霍尔德电子科技有限公司。
1.3 实验方法
1.3.1 核桃粕溶液的制备
参考代晹鑫等[19]的方法并做适量调整。将脱脂核桃饼粕用多功能粉碎机粉碎,再过0.180 mm筛,制成脱脂核桃粕粉。 取100 g脱脂核桃粕粉放入烧杯,以料液比1∶18(g∶mL)加入1 800 mL蒸馏水制备核桃粕样品溶液,用玻璃棒均匀搅拌备用。
1.3.2 核桃蛋白的制备
加入1 mol/L NaOH溶液将核桃粕溶液pH调节至9.0,置于45 ℃水浴锅中用70 W超声波辅助提取0.5 h。取出静置20 min,在4 500 r/min条件下离心0.5 h。得到上清液后,加入1 mol/L盐酸调pH至4.5,再以3 500 r/min离心0.5 h。离心后将上清液与沉淀物质分离,得沉淀物。 沉淀物用蒸馏水旋洗数次,直到样品溶液pH呈中性,再次以4 000 r/min的速度离心15 min。最后用真空冷冻干燥机将沉淀物冷冻干燥制得核桃蛋白,贮藏在-20 ℃冰箱中冷冻备用[20-21]。
1.3.3 酶解产物的制备
参照洪佳伟等[22]的方法稍作修改后制备核桃蛋白酶解产物。将核桃蛋白按照质量分数5%溶于去离子水中,并添加碱性蛋白酶,将核桃蛋白溶液放入60 ℃水浴锅中酶解,滴加1 mol/L NaOH到溶液中,将溶液pH调节至酶解最适范围。经过2.4 h的酶解处理后,将其放入100 ℃的沸水浴中加热25 min,对酶灭活。 之后,取出溶液冷却至室温,向溶液中加入1 mol/L的盐酸,并调整其pH值至4.5。 以3 500 r/min离心0.5 h,将上清液pH调至中性,冷冻干燥得到酶解产物,并保存-20 ℃冰箱中。
1.3.4 样品热处理分组
实验设置五组核桃蛋白与酶解产物样品溶液,每组核桃蛋白与酶解产物溶液200 mL,结合实际生产加工中的热处理参数,在水浴锅中对样品进行不同热处理,分别为:不进行热处理、65 ℃加热处理30 min、72 ℃加热处理10 s、85 ℃加热处理10 min和95 ℃加热处理10 min。
1.3.5 成骨细胞培养
将MC3T3-E1成骨细胞系在含有体积分数1%抗生素和体积分数10%胎牛血清的α-MEM培养液混合后,在37 ℃、体积分数5%CO2中培养成骨细胞。 在传代成骨细胞时,用0.25%胰蛋白酶-EDTA消化液消化MC3T3-E1细胞[23]。每日利用倒置显微镜对细胞的状态和生长状况进行定期观察,并拍照记录。
1.3.6 苏木精-伊红染色
采用苏木精-伊红(hematoxylin-eosin,HE)染色法,对成骨细胞进行染色处理。该方法能够清晰地显示细胞的形态结构和成分特点。在6孔板中放入无菌盖玻片,添加细胞悬液,取出细胞爬片后的盖玻片,PBS洗涤4次,每次2 min。将细胞用体积分数10%的中性福尔马林溶液固定15 min,用PBS进行2次洗涤,每次1 min。 使用苏木精对细胞进行5~10 min的染色处理,并用超纯水洗涤1 min。将盖玻片置于1%的稀盐酸酒精溶液中分色,再次用超纯水洗涤1 min。用伊红将细胞染色10 min,超纯水将盖玻片上的浮色洗净。在盖玻片上逐级脱水(用2次体积分数95%酒精、3次无水酒精,每次1 min)。 盖玻片3次浸泡进二甲苯溶液,每次30 s。滴加中性树胶,封固后通过显微镜观察并拍照记录[24-25]。
1.3.7 碱性磷酸酶染色
在6孔板中放入无菌盖玻片,再将细胞接种进板内,直至细胞长到半融合的状态时再将盖玻片取出。先用PBS冲洗取出后的盖玻片,再用10%的中性福尔马林将细胞固定15 min,蒸馏水洗涤2~3 min。 加入碱性磷酸酶(alkaline phosphatase,ALP)孵育液,37 ℃孵育5 h,取出盖玻片,用蒸馏水洗涤。 再用2%硝酸钴将盖玻片染色3~5 min,用蒸馏水洗涤30 s。将盖玻片浸入到新配的1%硫化铵中,3~5 min后使用蒸馏水洗涤,在室温中自然干燥,滴加中性树胶,封固后通过显微镜观察并拍照记录[26-27]。
1.3.8 MTT法测定成骨细胞增殖率
在MTT法中,活细胞线粒体内的酶可将外源性MTT还原,形成不溶于水的蓝紫色甲瓒结晶,沉积于细胞内,而死细胞无此功能。二甲基亚砜(dimethyl sulfoxide,DMSO)溶解甲瓒后,使用酶标仪在波长490 nm处测定光密度(optical density,OD)值,来反映活细胞数量。OD值越大,细胞增殖越多或活性越强。
参照PANDA B等[28]的方法,去掉消化液,将成骨细胞用0.25%胰蛋白酶-EDTA消化液分解,加入α-MEM培养液,得到1×105个/mL的单细胞悬液。 将细胞接种于96孔板,每孔加入100 μL细胞悬液,并在细胞周围边填充100 μL无菌的PBS。恒温箱温度设定为37 ℃,二氧化碳体积分数5%,将细胞置于其中进行培养。 加入核桃蛋白溶液和酶解产物溶液的样品组。 待细胞完全贴壁后,将96孔板里的培养液替换为每个孔含5 μL的试验组溶液和95 μL的培养液,继续培养24 h、48 h、72 h;测定前4 h,每孔中避光加入10 μL质量浓度0.5 mg/mL MTT(pH 7.2,0.01 mol/L无菌PBS配制),置于37 ℃细胞培养箱中培养4 h;弃培养液,向每个孔中加入150 μL二甲基亚砜(DMSO)溶液,并持续振荡10 min直至结晶完全溶解。采用酶标仪测定样品在波长490 nm处的吸光度值,只加培养基的空白组吸光度值记为A0;含有未经处理成骨细胞的对照组吸光度值记为A2;加入不同质量浓度核桃蛋白溶液和酶解产物溶液的样品组,记为A1。细胞增殖率计算公式如下:
式中:D为细胞增殖率,%;A0为空白组吸光度值;A1为样品组吸光度值;A2为对照组吸光度值。
1.3.9 数据处理与统计分析
实验数据用Origin 2021软件进行处理并绘图。 用SPSS 26.0软件进行显著性检验。 上述所有实验均进行至少3次平行,显著性差异为P<0.05。
2 结果与分析
2.1 成骨细胞的鉴定
显微镜下观察可见,成骨细胞密集分布,多数细胞有突起,细胞形态多呈饱满,大小适中,以不规则形和多角形为主。细胞边缘清晰,细胞质丰富,细胞核大而圆位于细胞中央或稍偏一侧。成骨细胞经过HE染色如图1(a)所示,可以观察到细胞染色均匀。 细胞质被染成粉红色,细胞中心的细胞核颜色为深紫色,形态大而圆。 细胞核内染色质分布均匀,核仁清晰可见,细胞间连接紧密,表明成骨细胞具有较高的代谢活性。成骨细胞的ALP染色后情况如图1(b)所示,成骨细胞中ALP活性部位被染成黑色,在ALP染色下,细胞形态更加鲜明,且成骨细胞的ALP染色强度较高,表明这些细胞具有较高的ALP活性,处于活跃的分化状态。在培养条件下,成骨细胞常呈单层贴壁生长。在ALP染色结果中,可以观察到成骨细胞均匀分布,排列整齐,ALP活性在细胞内均匀分布。
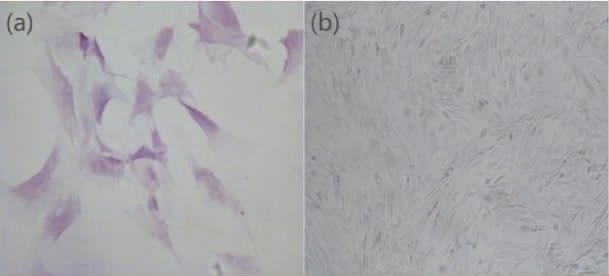
图1 成骨细胞的苏木精-伊红染色(a)和碱性磷酸酶染色(b)结果
Fig.1 Results of hematoxylin-eosin staining (a) and alkaline phosphatase staining (b) of osteoblasts
通过HE与ALP染色证实,该成骨细胞培养物状态良好,具有极高的细胞活性。 具体表现为:在形态上,细胞结构完整、连接紧密、代谢旺盛;在功能上,ALP高强度染色明确指示细胞正处于活跃的成骨分化阶段,展现出优异的功能活性。
2.2 热处理对核桃蛋白的增殖作用
2.2.1 不同热处理后培养24 h对核桃蛋白促成骨细胞增殖作用
不同热处理后培养24 h对核桃蛋白促成骨细胞增殖作用结果见图2。由图2可知,未处理、65 ℃/30 min、72 ℃/10 s、85 ℃/10 min、95 ℃/10 min五组核桃蛋白的成骨细胞增殖率分别为65.99%、67.51%、59.39%、59.39%、41.62%。可以发现随着热处理温度的升高,增殖率总体在逐渐减小,其中未处理、65 ℃/30 min、72 ℃/10 s、85 ℃/10 min四组的增殖率没有显著性差异(P>0.05),但都与95 ℃/10 min组有显著性差异(P<0.05)。 65 ℃/30 min和72 ℃/10 s两组的温度在巴氏杀菌的温度范围内,不会对蛋白质活性造成很大影响,所以与对照组相差不大,其中,65 ℃/30 min处理组与72 ℃/10 s处理组的细胞增殖率相较于对照组,呈现出先升高后降低的趋势,其原因在于当温度在65 ℃时,最接近蛋白质存活的最适温度,随着温度的升高多肽链的分子运动加快,促进分子间肽链空间结构的形成,促进细胞的增殖。72 ℃为蛋白质的热变性温度,继续加热到85 ℃和95 ℃时,蛋白质的表面电荷会导致蛋白质分子之间发生静电排斥,进而导致蛋白质发生解折叠,破坏蛋白质分子的空间结构,造成蛋白质活性的丧失,从而使细胞的增殖率降低。
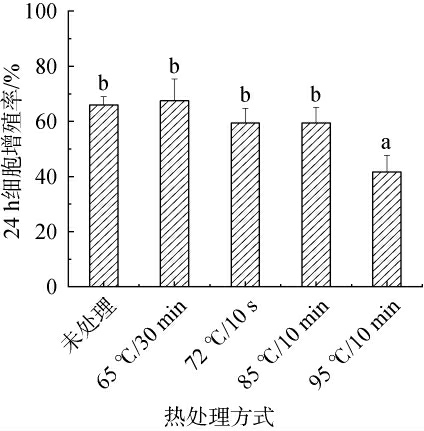
图2 不同热处理后培养24 h对核桃蛋白促成骨细胞增殖作用
Fig.2 Effect of different heat treatment on the proliferation of osteoblasts promoted by walnut protein after culture for 24 h
不同小写字母表示同一样品不同热处理方式下增殖率差异显著(P<0.05)。下同。
2.2.2 不同热处理后培养48 h对核桃蛋白促成骨细胞增殖作用
不同热处理后培养48 h对核桃蛋白促成骨细胞增殖作用结果见图3。由图3可知,未处理、65 ℃/30 min、72 ℃/10 s、85 ℃/10 min、95 ℃/10 min五组核桃蛋白的成骨细胞增殖率分别为45.06%、41.36%、27.78%、25.10%、24.07%。其中未处理、65 ℃/30 min两组之间没有显著性差异(P>0.05),72 ℃/10 s、85 ℃/10 min、95 ℃/10 min三组之间没有显著性差异(P>0.05),随着热处理温度的不断上升,增殖率总体呈现下降趋势。导致65 ℃/30 min与其他三组试验组增殖率差距较大的原因可能是,蛋白质的分子折叠在低温条件下可能不会发生明显变化,但超过某一个特定的温度时,蛋白质的分子折叠可能就会产生明显的改变。 有研究表明,乳铁蛋白在经过不同程度的热处理之后,就会发生不同情况的热聚集状态,随着加热过程中的温度不断上升,蛋白质的分子之间会发生结合作用,从而使乳铁蛋白自身的热聚集程度逐渐加强。 热聚集程度越明显,乳铁蛋白对成骨细胞活性的影响就越大,促进细胞增殖的作用也就越小。通过比较,核桃蛋白在受到高温处理时其自身的热聚集程度加强导致65 ℃后面处理的三组促进成骨细胞增殖的作用有所下降。热处理48 h与24 h相比较,五组的成骨细胞增殖率均有一定程度的下降,可能是由于成骨细胞基数变大,导致核桃蛋白作用变得不明显。
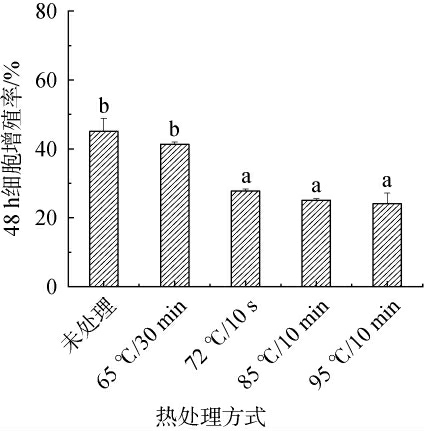
图3 不同热处理后培养48 h对核桃蛋白促成骨细胞增殖作用
Fig.3 Effect of different heat treatment on the proliferation of osteoblasts promoted by walnut protein after culture for 48 h
2.2.3 不同热处理后培养72 h对核桃蛋白促成骨细胞增殖作用
不同热处理后培养72 h对核桃蛋白促成骨细胞增殖作用结果见图4。由图4可知,未处理、65 ℃/30 min、72 ℃/10 s、85 ℃/10 min、95 ℃/10 min五组核桃蛋白的成骨细胞增殖率分别为27.53%、24.84%、22.94%、20.36%、19.73%。随着热处理温度的上升,增殖率总体呈下降趋势且五组均无显著性差异(P>0.05)。有研究表明,经过热处理的乳铁蛋白不能缓解摘除了卵巢的大鼠的骨质流失[29],证明乳铁蛋白与成骨细胞之间的协同作用被热处理打破。随着热处理温度的升高,核桃分离蛋白与成骨细胞之间的协同作用被打破了,导致了增殖率的下降。 且72 h的五组成骨细胞的增殖率均小于24 h与48 h中五组成骨细胞的增殖率,造成这一现象的原因可能是,由于培养时间过长,细胞的活力逐渐下降,更甚至有部分细胞已经失活,虽然还有增殖作用,但是效果明显降低。
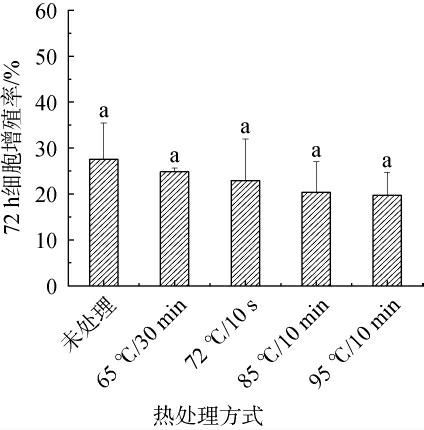
图4 不同热处理后培养72 h对核桃蛋白促成骨细胞增殖作用
Fig.4 Effect of different heat treatments on the proliferation of osteoblasts promoted by walnut protein after culture for 72 h
2.3 热处理对酶解产物的增殖作用
2.3.1 不同热处理后培养24 h对酶解产物促成骨细胞增殖作用
不同热处理后培养24 h对酶解产物促成骨细胞增殖作用结果见图5。由图5可知,未处理、65 ℃/30 min、72 ℃/10 s、85 ℃/10 min和95 ℃/10 min五组酶解产物的成骨细胞增殖率分别为43.81%、39.39%、40.63%、25.00%、28.23%。增殖率随热处理温度升高而逐渐降低。其中对照组与65 ℃/30 min和72 ℃/10 s两组热处理组没有显著差异(P>0.05),但65 ℃/30 min和72 ℃/10 s两组的增殖率都略低于对照组,85 ℃/10 min和95 ℃/10 min两组热处理组的成骨细胞增殖率显著低于未处理的成骨细胞增殖率(P<0.05),继续加热到85 ℃和95 ℃时蛋白质活性的丧失,细胞的增殖率降低,其中85 ℃/10 min组的增殖率最低。
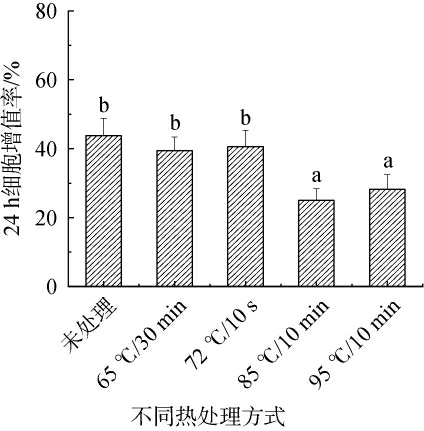
图5 不同热处理后培养24 h对酶解产物促成骨细胞增殖作用
Fig.5 Effect of different heat treatments on the proliferation of osteoblasts promoted by enzymatic hydrolysates after culture for 24 h
2.3.2 不同热处理后培养48 h对酶解产物促成骨细胞增殖作用
不同热处理后培养48 h对酶解产物促成骨细胞增殖作用结果见图6。由图6可知,未处理、65 ℃/30 min、72 ℃/10 s、85 ℃/10 min和95 ℃/10 min五组酶解产物的成骨细胞增殖率分别为28.24%、24.56%、24.31%、17.96%、17.76%。 其中对照组样品的48 h增殖率最高,且与其他四组有显著差异(P<0.05)。 65 ℃/30 min与72 ℃/10 s两组成骨细胞增殖率无显著差异(P>0.05),但显著高于85 ℃/10 min和95 ℃/10 min组(P<0.05)。高温处理时酶解产物中的蛋白质热聚集程度加强,导致其85 ℃/10 min和95 ℃/10 min两组对成骨细胞活性的促进作用没有65 ℃/30 min和72 ℃/10 s两组明显。热处理48 h与24 h相比,65 ℃/30 min和72 ℃/10 s两组与对照组相比有差异,可能随时间延长,经过热处理的蛋白被消化的速度增加,酶解产物有效浓度降低,这导致了增殖率的下降,并与未经处理的组别表现出显著的不同。
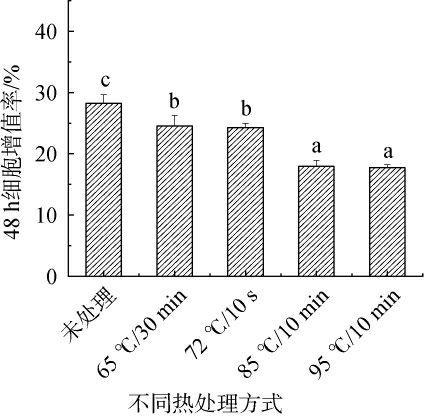
图6 不同热处理后培养48 h对酶解产物促成骨细胞增殖作用
Fig.6 Effect of different heat treatment on the proliferation of osteoblasts promoted by enzymatic hydrolysates after culture for 48 h
2.3.3 不同热处理后培养72 h对酶解产物促成骨细胞增殖作用
不同热处理后培养72 h对酶解产物促成骨细胞增殖作用结果见图7。由图7可知,未处理、65 ℃/30 min、72 ℃/10 s、85 ℃/10 min和95 ℃/10 min五组酶解产物的成骨细胞增殖率分别为19.48%、15.78%、14.84%、8.76%、7.51%。与未经处理的组相比,四组热处理组的成骨细胞增殖率显著降低(P<0.05)。65 ℃/30 min和72 ℃/10 s两组间无显著差异(P>0.05),85 ℃/10 min和95 ℃/10 min两组结果之间无显著差异(P>0.05),且显著低于65 ℃/30 min和72 ℃/10 s组(P<0.05)。 DU M等[30]研究中说明了在热处理过程中,乳铁蛋白中含有成骨作用的成分,其成骨活性被热处理破坏,或原有的协同作用被破坏。 因此随着温度的升高,成骨细胞增殖率的降低可能是因为酶解产物中的具有成骨作用的组分活性被热处理给破坏。 与24 h和48 h相比,72 h的成骨细胞增殖率显著降低,这可能是由于样品中的活性成分随作用时间延长而逐渐降解,导致其促进作用减弱。
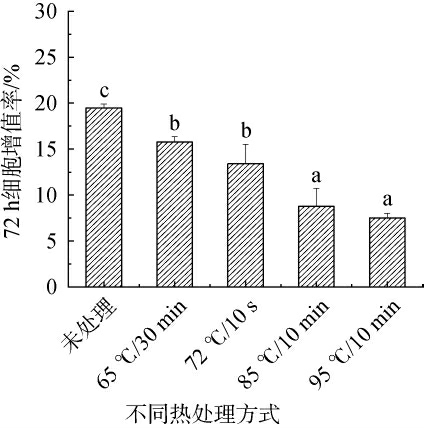
图7 不同热处理后培养72 h对酶解产物促成骨细胞增殖作用
Fig.7 Effects of different heat treatments on the proliferation of osteoblasts promoted by enzymatic hydrolysates after culture for 72 h
3 讨论
对于核桃蛋白,65 ℃/30 min处理组的细胞增殖率与对照组相比,其24 h的增殖率略有提升,表明适当的热处理可能有助于增强核桃蛋白的促成骨细胞增殖作用。然而,当热处理强度提升至72 ℃/10 s和85 ℃/10 min后培养24 h的增殖率即出现明显下降。这可能是由于蛋白质在超过其变性温度后发生了解折叠和构象破坏,导致其促进细胞增殖的关键活性结构域失活。培养48 h和72 h,各热处理组的增殖率与24 h相似呈降低趋势。热处理条件为95 ℃/10 min后培养24 h的细胞增殖率降低,显著低于其他各组(P<0.05),证明高温长时间处理对核桃蛋白的活性造成了严重损害。核桃蛋白热处理后培养48 h和72 h的促增殖活性普遍衰减,且热处理的不利影响更为显著。未处理组与65 ℃/30 min组在培养48 h仍维持相对较高的增殖活性,而72 ℃及以上的热处理组则显著降低,且组间无显著差异(P>0.05)。对于酶解产物,相较于对照组,当温度升至85 ℃和95 ℃后培养48 h和72 h的增殖率显著降低(P<0.05)。 说明高温长时间处理则导致增殖率大幅下降。 从24 h到72 h,无论是核桃蛋白还是酶解产物,其促成骨细胞增殖的作用均呈现下降趋势。这可能与细胞增殖过程中的自然衰减以及热处理对蛋白结构和功能的长期影响有关。
4 结论
该研究分别利用碱性酸沉法和超声波辅助提取核桃粕中的蛋白质,以核桃蛋白为原料,利用碱性蛋白酶制得酶解产物,对核桃蛋白和酶解产物采用不同热处理方式,经HE染色和ALP染色,通过MTT法对其成骨细胞的增殖率进行测定,来研究热处理对核桃蛋白与酶解产物促成骨细胞增殖作用。
研究发现,核桃蛋白对成骨细胞的生长有明显的促进作用且在不同时间点对成骨细胞增殖的影响不同。随着热处理强度提高,核桃蛋白在不同培养时间下的促成骨细胞增殖活性均呈下降趋势,其中85℃/10 min和95 ℃/10 min处理后的活性显著降低。 不同热处理的核桃粕酶解产物在培养24 h、48 h、72 h后,对MC3T3-E1成骨细胞均表现出有促进增殖的活性,且活性有差异,但大体趋势相似,活性均逐渐降低。 对于酶解产物,不同条件热处理后的酶解产物的成骨细胞增殖率相较于未处理有所下降,随着热处理温度的升高,酶解产物的成骨细胞增殖率总体呈现的趋势是下降的,65℃/30min和72 ℃/10 s热处理条件下酶解产物的成骨活性受影响相对较小,但85 ℃/10 min和95 ℃/10 min的热处理条件使其活性显著降低。综上,65 ℃/30 min处理组能较好地保留核桃蛋白与酶解产物的促成骨活性,而超过72 ℃的热处理则显著削弱该作用。
[1]SU G W,CHEN J Q,HUANG L,et al.Effects of walnut seed coat polyphenols on walnut protein hydrolysates:Structural alterations,hydrolysis efficiency, and acetylcholinesterase inhibitory capacity[J].Food Chem,2023,437(P1):137905.
[2]SONG X B,ZHOU N F,CHANG Y Y,et al.Spatial and temporal alterations of multiple hormones during the graft union formation process in walnut(Juglans regia)[J].Trees,2024,38(4):839-848.
[3]QIAN J Q,LI Q,MO L Y,et al.Comparison of improvement in learning and memory ability of walnut oil extracted by aqueous enzymatic extraction and cold pressing extraction[J].Eur J Lipid Sci Technol,2024,126(5):2300233.
[4]EBRU K,HILAL S A,ALI M G,et al.Phenolic and fatty acid profile,and protein content of different walnut cultivars and genotypes(L.) grown in the USA[J].Int J Fruit Sci,2020,20(S3):S1711-S1720.
[5]CHEN X M, JIA X Z, ZHANG Y, et al.The combined use of gammaaminobutyric acid and walnut peptide enhances sleep in mice[J].Ann Palliat Med,2021,10(10):11074-11082.
[6]李遇豪,李道明,田智辉,等.核桃饼(粕)的组成与加工应用研究进展[J].河南工业大学学报(自然科学版),2024,45(5):131-140.
[7]TANG H K, WANG C, CAO S N, et al.Novel angiotensin I-converting enzyme(ACE)inhibitory peptides from walnut protein isolate:Separation,identification and molecular docking study[J].J Food Biochem, 2022,46(12):e14411.
[8]KRISTINE K,EGIDIJUS D,IGNAT T,et al.Physicochemical and functional properties of rainbow trout(Oncorhynchus mykiss)hydrolysate[J].Heliyon,2023,9(7):e17979.
[9]陈佳欣.核桃粕酪氨酸酶抑制肽制备、结构鉴定及其活性研究[D].北京:北京林业大学,2019.
[10]LI W J,Li H M,LI J,et al.Structure-activity relationship of walnut peptide in gastrointestinal digestion,absorption and antioxidant activity[J].LWT-Food Sci Technol,2023,189:115521.
[11]罗湘杭,郭乔月,熊津铭.骨在能量代谢中的作用[J].中国科学:生命科学,2024,54(11):2100-2111.
[12]邓艳梅,毕会敏,范方宇.热处理及均质方式对核桃蛋白稳定Pickering乳液性质的影响[J].食品科技,2024,49(6):261-269.
[13]GUPTA A J,BOOTS J W,GRUPPEN H,et al.Influence of heat treatments on the functionality of soy protein hydrolysates in animal cell cultures[J].Food Chem,2023,429:136914.
[14]ZHAO X Y,REN X R,LIU H K,et al.Impact of steaming and roasting heat-treatment on physico-chemical and functional properties of walnut kernel[J].J Am Oil Chem Soc,2023,101(3):345-360.
[15]PAPOUTSI Z,KASSI E,CHINOU I,et al.Walnut extract(Juglans regia L.)and its component ellagic acid exhibit anti-inflammatory activity in human aorta endothelial cells and osteoblastic activity in the cell lineKS483[J].Brit J Nutr,2008,99(4):715-722.
[16]李宇,汪芳,翁泽斌,等.酶法制备大豆蛋白成骨活性肽[J].中国农业科学,2021,54(13):2885-2894.
[17]PANG X,ZHONG Z,JIANG F,et al.Juglans regia L.extract promotes osteogenesis of human bone marrow mesenchymal stem cells through BMP2/Smad/Runx2 and Wnt/β-catenin pathways[J].J Orthop Surg Res,2022,17(1):1-11.
[18]贾尚羲,张怡雪,石盼盼,等.不同时长超声波处理对鹰嘴豆分离蛋白乳化液稳定性的影响[J].轻工学报,2024,39(5):40-49.
[19]代晹鑫,徐莹,毕爽,等.核桃粕蛋白提取纯化工艺优化及其功能性质分析[J].食品工业科技,2023,44(2):241-252.
[20]HE X,ZHANG L,CAO M,et al.Characterization and functional properties of walnut protein fibrils for enhanced bioaccessibility of CoQ10 and ALA[J].Int J Biol Macromol,2024,285:138171.
[21]XIE J, CHEN S, HUAN P, et al.A novel angiotensin I-converting enzyme inhibitory peptide from walnut(Juglans sigillata)protein hydrolysates and its evaluation in Ang II-induced HUVECs and hypertensive rats[J].Int J Biol Macromol,2024,266(P2):131152.
[22]洪佳伟,肖柳柳,王爱琳,等.核桃抗氧化肽的酶法制备、鉴定及其对脂氧合酶的抑制机理[J].食品与生物技术学报,2024,43(6):112-118.
[23]于涛,王海.基于Caspase-1研究NLRP3/Caspase-1通路对成骨细胞焦亡作用机制[J].外科研究与新技术,2023,12(3):163-167.
[24]王建坤.PDZK1-CFTR调控NLRP3-焦亡途径对MC3T3-E1成骨细胞增殖和分化的影响[J].福建医药杂志,2024,46(5):52-56.
[25]王刘玉,万全会,陈军.黄芪多糖对MC-3T3-E1成骨细胞增殖的影响及作用机制研究[J].中医正骨,2023,35(8):1-7.
[26]ZHANG Z, ZHOU C, YU L.LEP O-GlcNAcylation inactivates NF-κB pathway by suppressing LEP protein level and thus mediates cellular senescence and osteogenic differentiation in mouse mesenchymal stem cells[J].BMC Mol Cell Biol,2024,25(1):26.
[27]TABUCHI Y, KURODA K, FURUSAWA Y, et al.Genes involved in osteogenic differentiation induced by low-intensity pulsed ultrasound in goldfish scales[J].Biomed report,2025,22(2):18.
[28]PANDA B,PATRI G,JENA D,et al.Comparative evaluation of the osteogenic capacity of second-generation platelet concentrates on dental pulp stem cells-An ex vivo study[J].J Conserv Dent Endodont,2024,27(8):853-859.
[29]包晓宇,陈美霞,王加启,等.牛乳中活性蛋白生物学功能研究进展[J].食品科学,2017,38(19):315-324.
[30]DU M, KONG Y, WANG C, et al.Short communication: proteins in heat-processed skim milk powder have no positive effects on bone loss of ovariectomized rats[J].J Dairy Sci,2011,94(6):2771-2774.