白酒糟是白酒酿造过程中的主要副产物,据国家统计局估算,我国白酒糟产量超2 000万t/年[1],酒糟中含有的蛋白质、淀粉、氨基酸、纤维素等物质,具有较高营养价值和资源化利用潜力。然而酒糟因微生物和水分含量高,贮存时易腐败[2-4],且低效粗放的传统处理方式(直接饲喂、焚烧、直接掩埋等)还会造成环境污染和资源的浪费[5-6],开发白酒糟高值化利用技术对可持续发展具有重要意义。微生物发酵处理具有环境友好、条件温和、降解能力高效等优点,微生物产生的多种酶系可降低酒糟中纤维素等大分子物质,提升蛋白质及氨基酸含量,提高酒糟营养价值和资源利用率[7-8]。
微生物发酵包括单菌发酵和多菌种混合发酵两种方式,多菌种混合发酵可有效克服单菌发酵酶系单一、原料利用率不高等问题[9-10]。 酒糟常用的发酵菌种包括黑曲霉(Aspergillus niger)、白地霉(Geotrichum candidum)、米曲霉(Aspergillus oryzae)、热带假丝酵母(Candida tropicalis)、产朊假丝酵母(Candida utilis)、乳酸菌(Lactobacillus)、枯草芽孢杆菌、尿肠球菌(Enterococcus faecalis)等,不同菌种代谢特性各有不同,合理组合可发挥菌种间的协同作用,有效提升发酵效果[11-12]。 时伟等[13]选取3株菌(枯草芽孢杆菌、植物乳杆菌2-41、酿酒酵母SY)混合固态发酵酒糟制备蛋白饲料,发酵后的饲料中粗蛋白(crude protein,CP)含量由14.63%提高至27.54%。张玉诚等[14]利用混菌(白地霉、米曲霉、绿色木霉、枯草芽孢杆菌)发酵白酒糟,发酵后蛋白质和氨基酸含量显著提升,粗纤维(crude fiber,CF)、酸性洗涤纤维(acid detergent fiber,ADF)、中性洗涤纤维(neutral detergent fiber,NDF)和粗脂肪(crude fat,CF)含量显著下降,但未检测黄曲霉毒素等霉菌毒素,故产品安全性无法准确评估。目前,针对白酒糟特有的理化特性,尚缺乏多菌种协同代谢机制及发酵安全性的系统研究。
本研究以复合菌剂固态发酵白酒酒糟,对优化枯草孢杆菌(Bacillus subtilis)X-1、布氏乳杆菌(Lactobacillus buchneri)、米曲霉(Aspergillus oryzae)这3株菌复配组合及比例进行优化后将其应用于酒糟发酵,通过单因素试验结合正交试验优化酒糟固态发酵条件,并对发酵后酒糟的品质指标进行分析,以期提升酒糟的营养价值,为其在混菌发酵功能性食品添加剂及高蛋白饲料领域的应用提供理论基础与技术支撑。
1 材料与方法
1.1 材料与试剂
1.1.1 材料与菌株
酒糟:由某酒厂提供;花生粕:市售;枯草芽孢杆菌(Bacillus subtilis)X-1、布氏乳杆菌(Lactobacillus buchneri)、米曲霉(Aspergillus oryzae):均为本实验室保藏。
1.1.2 试剂
碳酸钙(分析纯):河南鑫洋钙业有限公司;盐酸、硫酸、氢氧化钠、五水硫酸铜、硫酸钾、三氯乙酸(trichloroacetic acid,TCA)、硼酸、十六烷基三甲基溴化铵、无水亚硫酸钠(均为分析纯):成都市科隆化学品有限公司;黄曲霉毒素B1、呕吐毒素、玉米赤霉烯酮毒素定量快速检测试剂盒:深圳芬德生物技术有限公司。
1.1.3 培养基
MRS液体培养基[15]:蛋白胨10 g,牛肉膏10.0 g,葡萄糖20.0 g,酵母浸粉5.0 g,无水乙酸钠5.0 g,磷酸氢二钾2.0 g,柠檬酸三铵2.0 g,七水合硫酸镁0.2 g,硫酸锰0.05 g,吐温80 1.0 g,去离子水1.0 L,121 ℃灭菌15 min。
营养肉汤(nutrient broth,NB)液体培养基[16]:蛋白胨10.0 g,牛肉浸粉3.0 g,氯化钠5.0 g,去离子水1.0 L,121 ℃灭菌15 min。
马铃薯葡萄糖琼脂(potato dextrose agar,PDA)培养基:马铃薯浸粉6.0 g、葡萄糖20.0 g、琼脂20.0 g,去离子水1.0 L,121 ℃灭菌15 min。
1.2 仪器与设备
MF80BSH-2霉菌培养箱:上海新苗医疗器械制造有限公司;ZWYR-D2403智诚恒温培养振荡器:上海智城分析仪器制造有限公司;JL-UPK-I-20T金澜系列超纯水器:四川金澜科技有限公司;PHS-3C台式酸度计:上海佑科一起仪表有限公司;MB25快速水分测定仪:奥豪斯仪器(上海)有限公司;SH220F石墨消解仪:山东海能科学仪器有限公司;K1160全自动凯氏定氮仪:海能未来科技集团股份有限公司。
1.3 方法
1.3.1 菌株发酵液制备
分别挑取枯草芽孢杆菌X-1、布氏乳杆菌单菌落接种至装液量均为50 mL的MRS液体培养基。枯草芽孢杆菌X-1于37 ℃、170 r/min培养24 h;布氏乳杆菌于37 ℃培养24 h[17-20],培养结束即得菌株种子液,以2%的接种量转接至装液量分别为100 mL/250 mL的MRS和YPD液体培养基,培养条件同上述一致。挑取米曲霉单菌落接种至装液量为100mL/250mL的PDA液体培养基,于30 ℃、170 r/min培养48 h[21],培养结束即得菌株发酵液。
1.3.2 不同菌株复配比例发酵对酒糟纤维含量的影响
CF主要含有纤维素和部分木质素,ADF包括纤维素和木质素,NDF包括纤维素、半纤维素和木质素,ADF和NDF能更全面体现不同纤维成分的含量,可反映发酵对酒糟纤维成分的降解效果[22]。 基于文献[23-24]的菌种筛选依据,选择布氏乳杆菌、枯草芽孢杆菌X-1、米曲霉这3株菌进行组合,以发酵后酒糟中ADF和NDF的含量为评价指标确定混菌发酵菌株比例。将酒糟、花生粕、碳酸钙按83∶10∶7(g∶g)混匀,将不同组别菌株发酵液按10%接种量接种至酒糟中,于37 ℃发酵24 h,发酵结束后检测酒糟中ADF和NDF含量。不同组别设置如下:组别①为布氏乳杆菌∶枯草芽孢杆菌X-1∶米曲霉=1∶1∶1;组别②为布氏乳杆菌∶枯草芽孢杆菌X-1∶米曲霉=2∶1∶1;组别③为布氏乳杆菌∶枯草芽孢杆菌X-1∶米曲霉=1∶2∶1;组别④为布氏乳杆菌∶枯草芽孢杆菌X-1∶米曲霉=1∶1∶2;组别⑤为布氏乳杆菌∶枯草芽孢杆菌X-1∶米曲霉=1∶2∶2;组别⑥为布氏乳杆菌∶枯草芽孢杆菌X-1∶米曲霉=2∶1∶2;组别⑦为布氏乳杆菌∶枯草芽孢杆菌X-1∶米曲霉=2∶2∶1。
1.3.3 酒糟发酵条件优化
单因素试验:选择最佳混合菌株组合,固定接种量为10%,发酵时间为24h。分别考察发酵温度(29℃、31℃、33℃、35 ℃、37 ℃、39 ℃)、发酵时间(36 h、48 h、60 h、72 h、84 h、96 h)、接种量(6%、8%、10%、12%、14%、16%)、初始含水量(56%、57%、58%、59%、60%、61%)对酒糟中ADF和NDF含量的影响。
正交试验:基于单因素试验结果,选取发酵温度(A)、发酵时间(B)、初始含水量(C)为影响因素,以ADF和NDF含量为评价指标,进行3因素3水平L9(33)的正交试验,正交试验设计因素与水平见表1。
表1 酒糟发酵条件优化正交试验设计因素与水平
Table 1 Factors and levels of orthogonal experimental design for fermentation conditions optimization of distiller's grains

水平 A 发酵温度/℃ B 发酵时间/h C 初始含水量/%1 2 3 35 37 39 48 60 72 57 58 59
1.3.4 分析检测
ADF和NDF含量:采用滤袋法测定[25-26];ADF和NDF降![]() ;粗蛋白(CP):采用凯氏定氮法测定[27];酸溶蛋白(acid-soluble protein,ASP):采用三氯乙酸(TCA)法测定[28]。
;粗蛋白(CP):采用凯氏定氮法测定[27];酸溶蛋白(acid-soluble protein,ASP):采用三氯乙酸(TCA)法测定[28]。
pH:参照DB15/T 1458—2018《青贮饲料pH值、有机酸、氨态氮测定方法》[29]进行测定;总酸:参照GB 12456—2021《食品安全国家标准食品中总酸的测定》[30]进行测定。
黄曲霉毒素B1、呕吐毒素、玉米赤霉烯酮毒素:分别按照黄曲霉毒素B1、呕吐毒素、玉米赤霉烯酮毒素定量快速检测试剂盒要求进行测定。
1.3.5 数据处理
采用Microsoft Excel 2022整理数据并统计,SPSS 27.0进行单因素方差分析(analysis of variance,ANOVA),Duncan's法进行多重比较分析;采用Origin 2024软件绘图。结果均以“平均值±标准差”表示,P<0.05表示差异显著。
2 结果与分析
2.1 不同菌株复配比例发酵对酒糟纤维含量的影响
优化菌株复配比可增强菌株间的协同作用,提高产品稳定性和安全性。 不同菌株复配比例发酵对酒糟中酸性洗涤纤维和中性洗涤纤维含量的影响见图1。由图1可知,第②组菌株复配比例(布氏乳杆菌、枯草芽孢杆菌X-1、米曲霉=2∶1∶1)发酵酒糟中ADF和NDF含量最低,分别为20.99%和25.06%,明显低于其余处理组。其原因可能是,枯草芽孢杆菌和米曲霉分泌的纤维素酶可将纤维素降解为可溶性糖和其他营养物质,为布氏乳杆菌的生长供给营养物质,与翟昊[31]利用乳酸菌和纤维素降解菌共同作用降解柠条青贮中纤维素的研究结果类似。因此,选取第②组(布氏乳杆菌∶枯草芽孢杆菌X-1∶米曲霉=2∶1∶1)菌株复配比例进行后续实验。
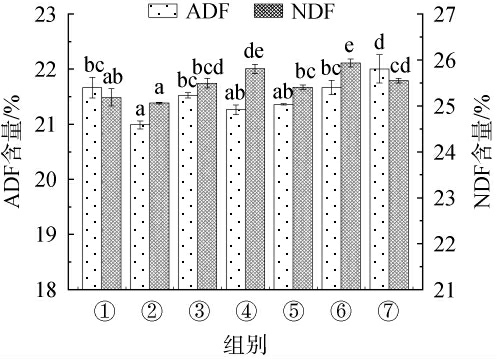
图1 不同菌株复配比例发酵对酒糟中酸性洗涤纤维和中性洗涤纤维含量的影响
Fig.1 Effect of different strain combination ratio on the contents of acidic and neutral detergent fibers in distiller's grains
不同小写字母表示差异显著(P<0.05)。下同。
2.2 酒糟发酵条件优化单因素试验结果
2.2.1 发酵温度的确定
温度对能量传递的影响至关重要,过低的发酵温度,菌株繁殖速度会减慢,其代谢活力也随之减弱,过高的发酵温度,影响菌种生长,导致产酶效果减弱[32-33]。 发酵温度对酒糟酸性洗涤纤维和中性洗涤纤维含量的影响见图2。由图2可知,随着发酵温度在29~37 ℃范围内的增加,发酵酒糟的ADF、NDF含量整体呈下降趋势;当发酵温度为37 ℃时,酒糟的ADF、NDF含量分别为20.68%和24.25%;当发酵温度>37 ℃时,酒糟的ADF含量趋于平稳,而NDF含量呈上升趋势。与陈显玲等[34]的研究结果类似,其原因可能是随着发酵温度升高,菌株产酶能力较强可有效降解酒糟中的纤维素,而过高的发酵温度影响菌株产酶效果。因此,确定最适混菌固态发酵温度为37 ℃。
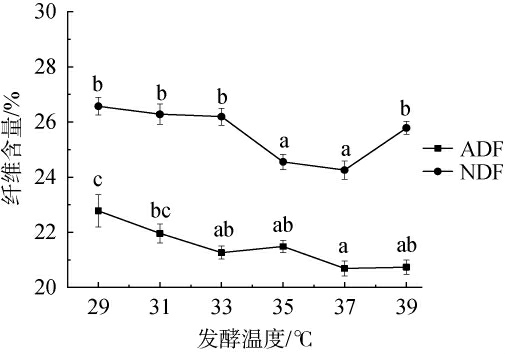
图2 发酵温度对酒糟酸性洗涤纤维和中性洗涤纤维含量的影响
Fig.2 Effect of fermentation temperature on the contents of acidic and neutral detergent fibers in distiller's grains
2.2.2 发酵时间的确定
发酵时间对酒糟酸性洗涤纤维和中性洗涤纤维含量的影响见图3。 由图3可知,随着发酵时间在36~60 h范围内的延长,发酵酒糟中ADF和NDF含量均呈下降趋势;当发酵时间为60 h时,ADF和NDF含量分别为20.58%和24.07%;当发酵时间>60 h时,ADF和NDF含量变化趋于平缓。其原因可能是随着发酵时间的增加,微生物产酶可有效降解酒糟,但随着发酵的进行,微生物可利用的营养物质不足[35]。因此,确定最适混菌固态发酵时间为60 h。
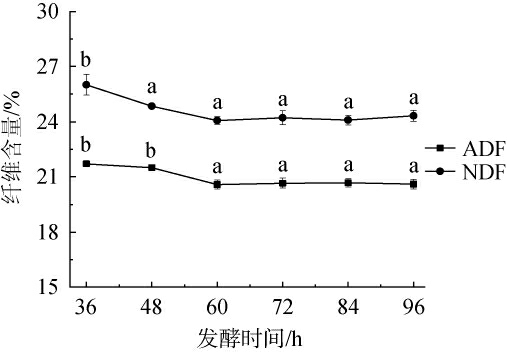
图3 发酵时间对酒糟酸性洗涤纤维和中性洗涤纤维含量的影响
Fig.3 Effect of fermentation time on the contents of acidic and neutral detergent fibers in distiller's grains
2.2.3 接种量的确定
接种量对酒糟酸性洗涤纤维和中性洗涤纤维含量的影响见图4。 由图4可知,随着接种量在6%~10%范围内的增加,发酵后酒糟中ADF和NDF含量均呈降低趋势;当接种量为10%时,发酵酒糟中的ADF和NDF含量最低,分别为20.10%和24.49%;当接种量>10%时,ADF和NDF含量变化趋于平稳。若接种量过少,菌株分泌的纤维素降解酶和蛋白酶含量较低,使纤维素等大分子物质降解不完全,不利于蛋白品质的提升;接种量过高,微生物可利用的营养物质会消耗过快[36-37]。因此,最适混菌固态发酵的接种量为10%。
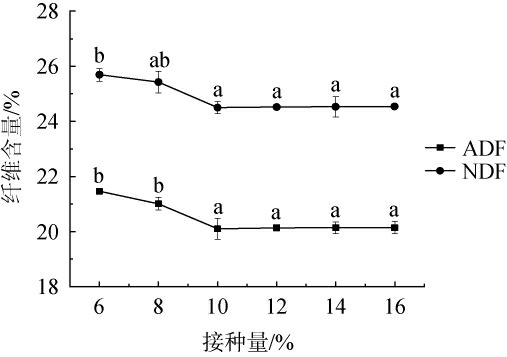
图4 接种量对酒糟酸性洗涤纤维和中性洗涤纤维含量的影响
Fig.4 Effect of inoculum on the contents of acidic and neutral detergent fibers in distiller's grains
2.2.4 初始含水量的确定
酒糟初始含水量对酒糟酸性洗涤纤维和中性洗涤纤维含量的影响见图5。由图5可知,随着初始含水量在56%~58%范围内的增加,发酵酒糟中ADF和NDF含量均呈降低趋势;当初始含水量为58%时,ADF和NDF含量分别为20.16%和23.20%;当初始含水量>58%时,ADF和NDF含量变化趋于平缓。其原因可能是当底物含水量不足时,造成营养物质溶解度下降,从而抑制其生长代谢[38],但底物含水量过高,使基质间隙率降低,阻碍氧气流通,好氧菌代谢强度被抑制,影响菌株产酶和酶活[39-40]。 因此,确定最适混菌固态发酵的初始含水量为58%。
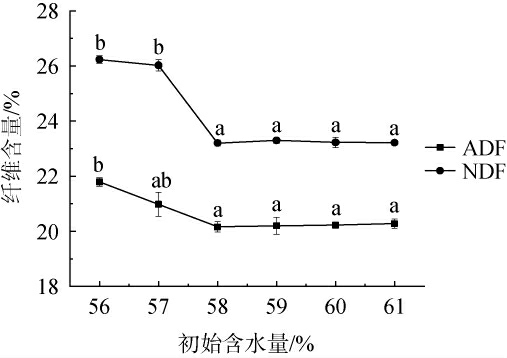
图5 初始含水量对酒糟酸性洗涤纤维和中性洗涤纤维含量的影响
Fig.5 Effect of initial moisture content on the contents of acidic and neutral detergent fibers in distiller's grains
2.3 发酵条件优化正交试验结果
基于单因素试验结果,以发酵温度(A)、发酵时间(B)、初始含水量(C)为影响因素,ADF和NDF含量为评价指标,进行3因素3水平L9(33)正交试验,白酒酒糟发酵条件优化正交试验结果与分析见表2,方差分析见表3。
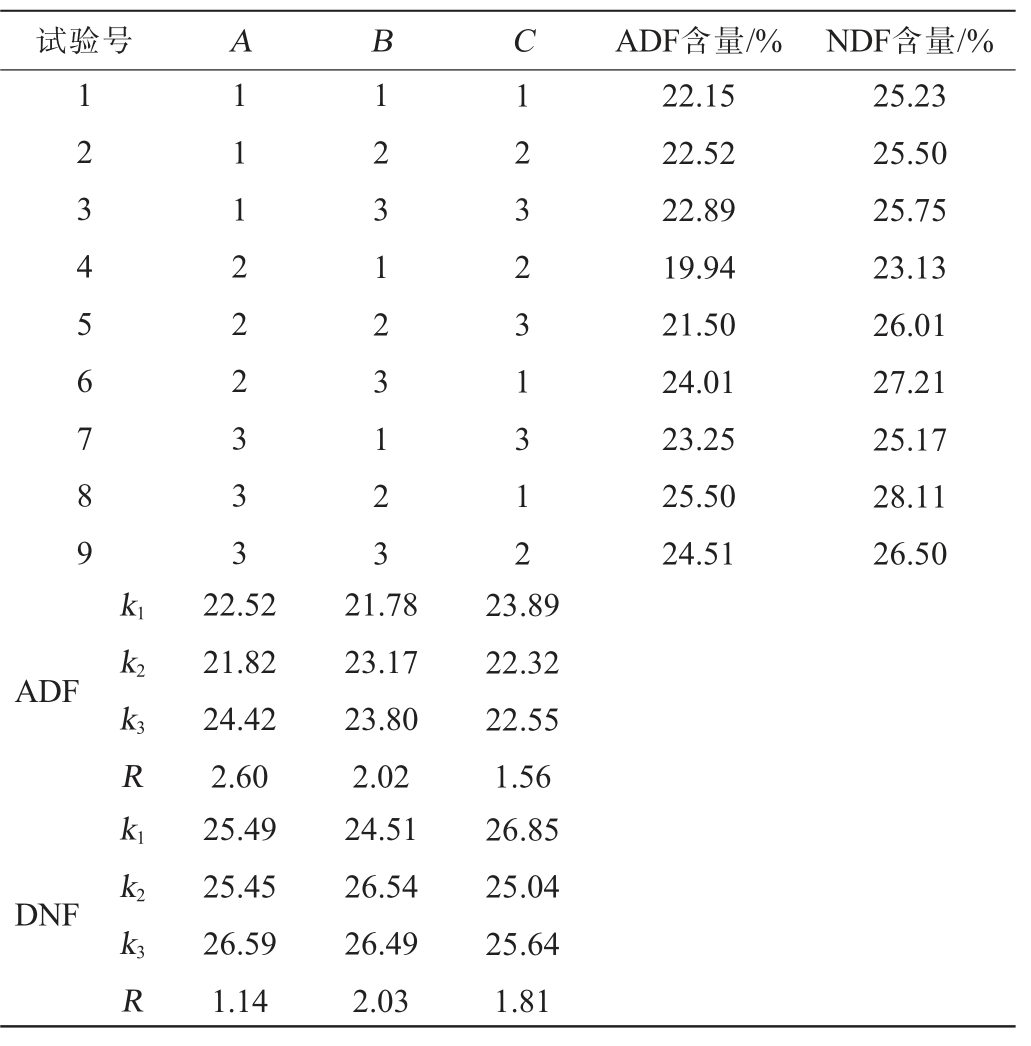
表2 发酵条件优化正交试验结果与分析
Table 2 Results and analysis of orthogonal tests for fermentation conditions optimization
试验号 A B C ADF含量/% NDF含量/%123456789 ADF DNF k1 k2 k3R k1 k2 k3R 111222333 22.52 21.82 24.42 2.60 25.49 25.45 26.59 1.14 123123123 21.78 23.17 23.80 2.02 24.51 26.54 26.49 2.03 123231312 23.89 22.32 22.55 1.56 26.85 25.04 25.64 1.81 22.15 22.52 22.89 19.94 21.50 24.01 23.25 25.50 24.51 25.23 25.50 25.75 23.13 26.01 27.21 25.17 28.11 26.50
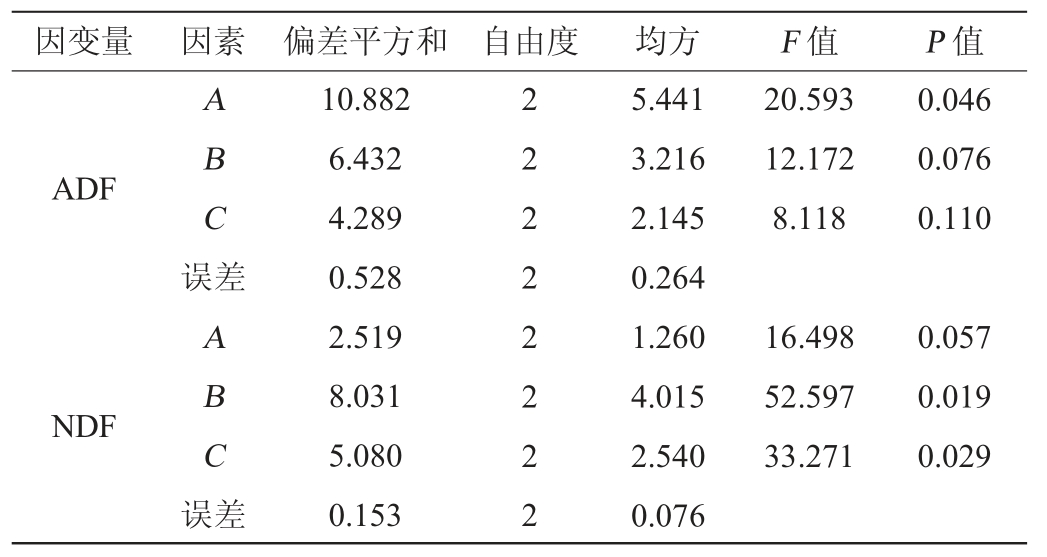
表3 正交试验结果方差分析
Table 3 Variance analysis of orthogonal experiment results
注:P<0.05表示对结果影响显著。
因变量 因素 偏差平方和 自由度 均方 F 值 P 值ADF ABC误20.593 12.172 8.118 0.046 0.076 0.110 NDF差ABC误差10.882 6.432 4.289 0.528 2.519 8.031 5.080 0.153 2 2 2 2 2 2 2 2 5.441 3.216 2.145 0.264 1.260 4.015 2.540 0.076 16.498 52.597 33.271 0.057 0.019 0.029
由表2可知,由R值可知,各因素对酒糟中ADF含量的影响顺序为发酵温度(A)发酵时间(B)>初始含水量(C);对酒糟中NDF含量的影响顺序为发酵时间(B)>初始含水量(C)>发酵温度(A)。由K值可知,对ADF和NDF降解效果最佳的发酵条件组合均为A2B1C2,出现在正交试验4,即发酵温度37 ℃、发酵时间48 h、初始含水量58%。 在此条件下,ADF和NDF含量分别为19.94%、23.13%。
由表3可知,发酵温度对酒糟中ADF含量影响显著(P<0.05),对NDF含量影响不显著(P>0.05);发酵时间和初始含水量对ADF含量影响不显著(P>0.05),但对NDF含量影响均显著(P<0.05)。
2.4 酒糟发酵前后品质指标检测结果
酒糟发酵前后品质指标检测结果见表4。
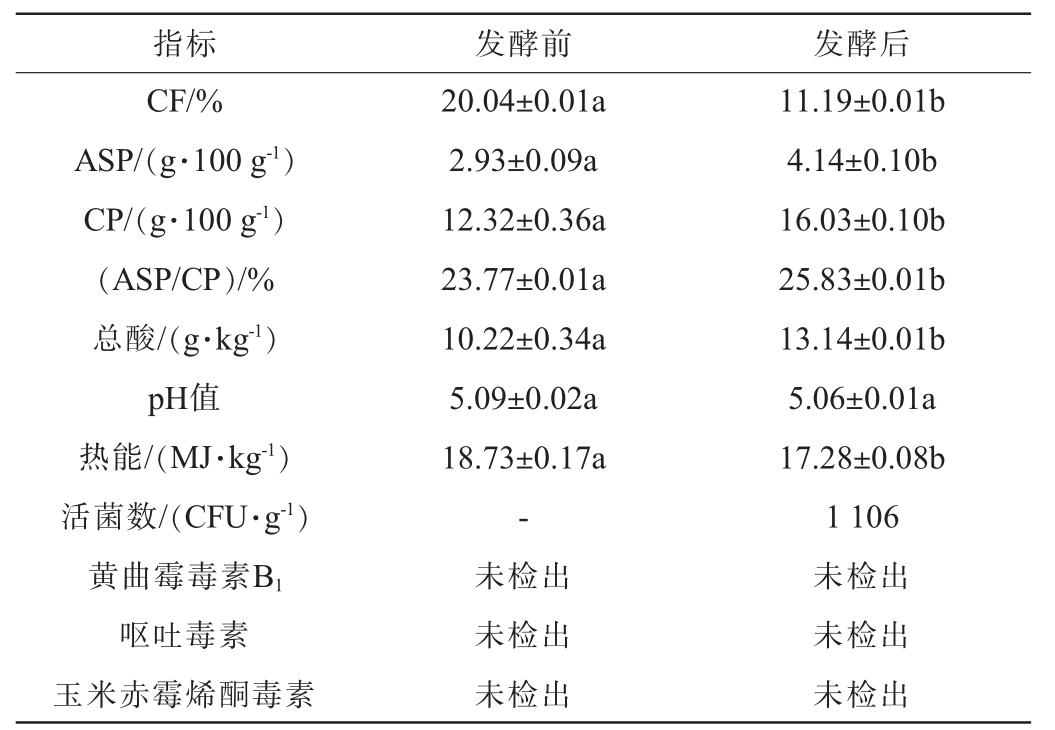
表4 酒糟发酵前后品质指标检测结果
Table 4 Detection results of quality indicators of the distiller's grains before and after fermentation
注:同一指标不同小写字母表示差异显著(P<0.05)。
指标 发酵前 发酵后CF/%ASP/(g·100 g-1)CP/(g·100 g-1)(ASP/CP)/%总酸/(g·kg-1)pH值热能/(MJ·kg-1)活菌数/(CFU·g-1)黄曲霉毒素B1呕吐毒素玉米赤霉烯酮毒素11.19±0.01b 4.14±0.10b 16.03±0.10b 25.83±0.01b 13.14±0.01b 5.06±0.01a 17.28±0.08b 1 106未检出未检出未检出20.04±0.01a 2.93±0.09a 12.32±0.36a 23.77±0.01a 10.22±0.34a 5.09±0.02a 18.73±0.17a-未检出未检出未检出
由表4可知,发酵后酒糟中CF含量为11.19%,较发酵前降低了44.15%;CP、ASP含量和ASP/CP分别为16.03 g/100 g、4.14 g/100 g和25.83%,较发酵前分别提高了30.12%、41.40%和8.67%;总酸含量为13.14 g/kg,较发酵前提升了28.57%,发酵后酒糟的pH值为5.06。 此外,发酵后酒糟中活菌数为1 106 CFU/g,其益生菌菌群可显著改善酒糟品质。由于微生物在生长繁殖过程中的能量消耗,热能较发酵前减少了7.76%。 发酵前后的底物中黄曲霉毒素B1、呕吐毒素及玉米赤霉烯酮毒素均未检出,其安全性符合GB 13078—2017《饲料卫生标准》[41],表明该发酵工艺在保障原料安全性方面表现良好。
3 结论
本研究以白酒酒糟为发酵基质,以枯草孢杆菌(Bacillus subtilis)X-1、布氏乳杆菌(Lactobacillus buchneri)、米曲霉(Aspergillus oryzae)为发酵菌株,对不同菌株复配比例进行优化,得出用于酒糟发酵的复合菌剂组合为布氏乳杆菌∶枯草芽孢杆菌X-1∶米曲霉(2∶1∶1)。通过单因素试验结合正交试验设计确定最优发酵条件为:发酵温度37 ℃、接种量10%、初始含水量58%和发酵时间48 h。在此优化条件下,发酵后酒糟的ADF、NDF含量分别为19.94%、23.13%,ADF、NDF降低率分别为31.18%、45.04%,CP、ASP含量和ASP/CP分别为16.03 g/100 g、4.14 g/100 g和25.83%,较发酵前分别提升了30.12%、41.40%和8.67%。同时,发酵产物总酸含量提升至13.14 g/kg,发酵后的热能为17.28 MJ/kg,pH值为5.06;黄曲霉毒素B1、呕吐毒素、玉米赤霉烯酮毒素在发酵前后均未检出,安全性符合GB 13078—2017《饲料卫生标准》。由于微生物对木质纤维素结构的降解效率有限,后续研究需结合外源酶处理(如纤维素酶、木聚糖酶),开展协同发酵,以进一步提升酒糟资源的生物利用效率。
[1]喻春燕,郑淋,何静,等.白酒源生物活性肽的鉴定及功能特性研究进展[J].食品与发酵工业,2025,51(21):409-419.
[2]ZHANG C, LI J L, ZENG X D, et al.Comprehensive use of distillers'grains derived from Chinese Baijiu:A review[J].J Agr Food Res,2024,18:101439.
[3]LIU Y Z,LIU S P,HUANG C H,et al.Chinese Baijiu distiller's grains resourcing:Current progress and future prospects[J].Resour Conserv Recy,2022,176:105900.
[4]唐哲仁,高勇,师雄,等.白酒酒糟资源化利用技术研究进展[J].中国酿造,2024,43(8):13-19.
[5]郝倩倩,吴书东,张昌容,等.家蝇与黑水虻对酒糟利用的比较研究[J].西南农业学报,2025,38(2):422-428.
[6]杜陶,李霞,王毓嘉,等.干化技术对酒糟生物质资源化利用的影响[J].皮革科学与工程,2024,34(6):47-54.
[7]司靖宇.茶渣膳食纤维发酵改性菌株的筛选及其对膳食纤维改性和结合多酚释放的研究[D].南昌:南昌大学,2023.
[8]张婷,罗杰,蒋政云,等.酒糟的营养价值及其在肉用反刍动物生产上的应用[J].中国饲料,2024(5):13-17.
[9]蒋四强.米曲霉和红曲霉分别制曲后混合发酵对黄豆酱品质的影响[D].成都:成都大学,2023.
[10]舒林,郑佳,李丽,等.复合益生菌固态发酵酒糟条件的研究[J].中国酿造,2024,43(1):154-158.
[11]薄学军.酒糟类饲料处理方法及应用前景研究[J].今日畜牧兽医,2025,41(1):68-70.
[12]范方勇,谢玉松,甘宁,等.酒糟饲料发酵微生物菌剂组合方案筛选[J].食品与发酵科技,2022,58(2):102-106,110.
[13]时伟,商素,郑红梅,等.混菌固态发酵酱香型白酒糟制蛋白饲料研究[J].中国饲料,2024(13):141-147.
[14]张玉诚,薛白,达勒措,等.混菌固态发酵白酒糟开发为蛋白质饲料的条件优化及营养价值评定[J].动物营养学报,2016,28(11):3711-3720.
[15]陈由运,程浩浩,李梦婷,等.鼠李糖乳酪杆菌ccpA基因缺陷型的生长能力变化[J].现代食品科技,2025,41(8):72-82.
[16]廖锴,李欣,石延霞,等.塑料拱棚不同通风方式对黄瓜细菌性角斑病传播的影响[J].中国农业科学,2025,58(10):1934-1946.
[17]王金驰,薛涵予,朱国兴,等.马克斯克鲁维酵母与酿酒酵母协同发酵米酒的特性[J].食品研究与开发,2024,45(14):43-51.
[18]沈心兰,杨梅,罗慧玲,等.不同枯草芽孢杆菌菌株对番茄灰霉菌的生防效果分析[J/OL].四川农业大学学报,1-15[2025-11-28].
[19]牛冬玉,孔令慧,刘向勇,等.草酸脱羧酶的进化和异源表达对罗伊氏乳杆菌草酸盐降解能力的影响[J].济南大学学报(自然科学版),2025,39(2):306-312.
[20]梁景龙,徐怡琳,袁海珊,等.米香型白酒酿造用产酯酵母的紫外诱变育种[J].食品与发酵工业,2025,51(10):128-135.
[21]陈晓爽,秦卓怡,许丹娜,等.米曲霉HAU491降解玉米赤霉烯酮特性研究[J].饲料工业,2025,46(2):142-147.
[22]张文辉,马晓阳,李狄科,等.基于发酵酱酒糟和谷物酒糟糖浆组合的饲粮中性洗涤纤维水平对育肥猪生长性能、胴体性状和血清指标的影响[J].动物营养学报,2025,37(9):5850-5862.
[23]时伟,张熙琳,郑红梅,等.混菌固态发酵清香型白酒糟制备蛋白饲料的研究[J].饲料研究,2024,47(4):79-84.
[24]梅世慧,朱鸣鸣,王微,等.复合益生菌固态发酵白酒糟条件的研究[J].动物营养学报,2023,35(1):632-642.
[25]中华人民共和国农业农村部.NY/T 1459—2022 饲料中酸性洗涤纤维的测定[S].北京:中国农业出版社,2022.
[26]国家市场监督管理总局,国家标准化管理委员会.GB/T 20806—2022饲料中中性洗涤纤维(NDF)的测定[S].北京:中国标准出版社,2022.
[27]国家市场监督管理总局,中国国家标准化管理委员会.GB/T 6432—2018 饲料中粗蛋白的测定 凯氏定氮法[S].北京:中国标准出版社,2018.
[28]中华人民共和国农业农村部.NY/T 3801—2020 饲料原料中酸溶蛋白的测定[S].北京:中国农业出版社,2020.
[29]中华人民共和国国家卫生和计划生育委员会.GB 5009.237—2016食品安全国家标准食品pH值的测定[S].北京:中国标准出版社,2016.
[30]中华人民共和国国家卫生健康委员会, 国家市场监督管理总局.GB 12456—2021 食品安全国家标准 食品中总酸的测定[S].北京:中国标准出版社,2021.
[31]翟昊.青贮中乳酸菌的筛选及其对柠条青贮的影响[D].呼和浩特:内蒙古农业大学,2024.
[32]张翠翠.寡糖型海带发酵饲料制备及在鲍鱼养殖中的应用研究[D].济南:齐鲁工业大学,2020.
[33]XU X Q,LIN M M,ZANG Q,et al.Solid state bioconversion of lignocellulosic residues by Inonotus obliquus for production of cellulolytic enzymes and saccharification[J].Bioresource Technol,2018,247: 88-95.
[34]陈显玲,苏龙.β-葡萄糖苷酶产生菌的筛选及产酶条件优化[J].中国饲料,2024(9):60-64.
[35]ZUO S S,NIU D Z,NING T T,et al.Protein enrichment of sweet potato beverage residues mixed with peanut shells by Aspergillus oryzae and Bacillus subtilis using central composite design[J].Waste Biomass Valoriz,2018,9:835-844.
[36]LEE B K,PIAO H Y,CHUNG W J.Production of red pigments by Monascus purpureus in solid-state culture[J].Biotechnol Bioprocess Eng,2002,7:21-25.
[37]YAO K Y,ZHANG T Z,WANG H F,et al.Upgrading of by-product from beverage industry through solid-state fermentation with Candida utilis and Bacillus subtilis[J].Lett Appl Microbiol,2018,67(6):557-563.
[38]李玉婷,董锡文,杜春梅,等.发酵豆粕作为饲料应用的研究进展[J].中国饲料,2023(7):97-102.
[39]SADH P K, DUHAN S, DUHAN J S.Agro-industrial wastes and their utilization using solid state fermentation:a review[J].Bioresour Bioprocess,2018,5:1-15.
[40]龙祝.饲料发酵菌剂的筛选及液固发酵工艺研究[D].武汉:中南民族大学,2020.
[41]国家标准化管理委员会,国家质量监督检验检疫总局.GB 13078—2017饲料卫生标准[S].北京:中国标准出版社,2017.