酸木瓜(Chaenomeles sinensis)为蔷薇科木瓜属植物,是云贵川等地的重要野生资源[1]。成熟的酸木瓜色泽金黄、气味芳香,有较高的营养价值和药用价值[2-3]。研究发现,酸木瓜果实中存在大量有价值的次生代谢物,如莽草酸、奎宁酸衍生物、类黄酮、原花青素等,较其他水果酚类化合物含量更高、抗氧化能力更强,具有抗炎、抗癌、抗过敏和免疫调节作用[4-5]。 酸木瓜鲜果具有高酸低糖、果肉坚硬且酸涩味浓重等特点,不宜鲜食,若直接用于发酵可能会具有酸高抑制发酵、发酵酒酒精度低等问题[6-7],因此,选择适宜发酵酸木瓜果酒的酵母菌种至关重要。目前,果酒酿造中酿酒酵母的使用最为广泛,但通常会导致发酵产品的特征香气不明显或香气同质化,有研究发现在果酒发酵时添加非酿酒酵母(non-Saccharomyces cerevisiae)可对果酒品质产生一定的积极作用[8],增加果酒香气的复杂性[9],改善果酒口感特性[10],提高颜色稳定性等[11]。 研究表明[12],不同属的非酿酒酵母或是同属不同地区的非酿酒酵母在发酵过程中代谢产生的香气物质各不相同,能赋予果酒独特的风味。如有孢汉逊酵母(Hanseniaspora)有助于提高具有清新水果香气的乙酸酯含量[13];耐热拉钱斯氏酵母(Lachancea thermotolerans)高产具有乳香和水果风味的乙酯[14];美极梅奇酵母(Metschnikowia pulcherrima)高产具有苹果香气的己酸乙酯和辛酸乙酯[15]。 此外,非酿酒酵母与酿酒酵母混合发酵也逐渐成为果酒酿造领域的热点,如克鲁维毕赤酵母(Pichia kluyveri)和德尔布有孢圆酵母(Torulaspora delbrueckii)混合发酵葡萄酒中己酸乙酯的含量提升了2倍[16];季也蒙迈耶氏酵母(Meyerozyma guilliermondii)与酿酒酵母混菌发酵显著提高了橘子酒中多酚和挥发性香气成分的含量[17]。
酵母在果酒发酵过程中,常会遇到强酸、高糖等环境,其中高浓度的酸、糖以及乙醇含量可能会改变酵母菌细胞膜的渗透压从而抑制其生长,此外果酒发酵过程中还会添加一定二氧化硫用于抗氧化、抑制杂菌生长,这对于酵母的环境耐受性提出了很高的要求。黄倩等[18]从羊奶果种筛选出葡萄汁有孢汉逊酵母(Hanseniaspora uvarum)H1、异常威克汉姆酵母(Wickerhamomyces anomalus)H10两株菌株,均可耐受pH 3.2、葡萄糖250 g/L、SO2 300 mg/L、乙醇含量3%、温度15 ℃,且不产H2S。高娉娉[19]筛选出6株可耐受葡萄糖350 g/L、pH 2.5、SO2 250 mg/L、乙醇含量9%的本土非酿酒酵母。
在果酒酵母的筛选与应用领域中对于菌株的环境耐受性的覆盖范围、专用性酵母菌种资源的开发以及风味研究等还存在局限和不足。因此,该研究以酸木瓜及高酸水果山楂、柠檬为原料分离非酿酒酵母,通过对分离菌株的耐受性能和发酵特性进行研究,通过形态学观察及分子生物学技术进行菌种鉴定后利用电子鼻技术探究非酿酒酵母发酵酸木瓜果酒的挥发性风味特征,并基于电子鼻响应值对其进行主成分分析(principal component analysis,PCA),以期筛选出适用于酸木瓜果酒酿造的优良非酿酒酵母菌株,为酸木瓜果酒酿造提供一定技术支持。
1 材料与方法
1.1 材料与试剂
1.1.1 材料
云南酸木瓜:云南大理市售;柠檬:云南昆明市售;山楂:山东潍坊市售。
1.1.2 试剂
酵母浸出粉、蛋白胨(均为生化试剂):北京奥博星生物技术有限公司;琼脂:青岛海博生物技术有限公司;偏重亚硫酸钾、柠檬酸(均为分析纯)、L-乳酸钾(分析纯):上海阿拉丁生化科技股份有限公司;无水葡萄糖、丙三醇、磷酸二氢钾、乳酸、溴甲酚紫、七水合硫酸镁(均为分析纯):国药集团化学试剂有限公司;甘油三丁酸酯(分析纯):上海麦克林生化科技股份有限公司;氨苄青霉素:南京都莱生物技术有限公司;2,3,5-三苯基氯化四氮唑(triphenyltetrazolium chloride,TTC)(分析纯):福州飞净生物科技有限公司。
1.1.3 培养基
WL营养琼脂培养基[20]、酵母浸出粉胨葡萄糖(yeast extract peptone dextrose,YPD) 固体培养基、YPD液体培养基[21]、亚硫酸铋葡萄糖甘氨酸酵母(bismuth sulfite glucose glycine yeast,BIGGY)琼脂培养基:青岛海博生物技术有限公司。
TTC上层培养基[22]:2,3,5-三苯基氯化四氮唑0.5 g/L、葡萄糖5 g/L、琼脂20 g/L;
TTC下层培养基:葡萄糖10 g/L、蛋白胨20 g/L、酵母浸出粉1.5 g/L、MgSO4 0.4 g/L、KH2PO4 1.0 g/L、柠檬酸1.35 g/L,氨苄青霉素1.0 g/L,琼脂20 g/L;
产酯固体培养基[23]:酵母浸出粉10 g/L、葡萄糖20 g/L、蛋白胨20 g/L、溴甲酚紫0.04 g/L、三丁酸甘油酯15 mL/L、琼脂20 g/L。
以上培养基均121 ℃高压蒸汽灭菌20 min。
1.2 仪器与设备
DH6000BII型电热恒温培养箱:天津市泰斯特仪器有限公司;SW-CJ-2FD型洁净工作台:苏净集团苏州安泰空气技术有限公司;YXD-LS-50A型立式压力蒸汽灭菌锅:上海博讯实业有限公司医疗设备厂;UV-2600型紫外可见分光光度计:日本岛津仪器有限公司;BSA224S型电子天平:赛多利斯科学仪器(北京)有限公司;PEN3型便携式电子鼻系统:德国AIRSENSE公司。
1.3 实验方法
1.3.1 样品处理
自然发酵液的制备:挑选成熟、无病虫害的酸木瓜、山楂、柠檬,清洗干净后在无菌条件下去皮,各称取果肉300 g,分别在无菌袋中压碎,打浆后放入容量为500 mL的无菌三角瓶中,密封后放入28 ℃的培养箱中培养8 d,得到果汁自然发酵酵母培养液。
表皮培养液的制备:挑选出来的酸木瓜、山楂、柠檬不进行清洗,分别在无菌条件下切取约2 g表皮放入装液量为100 mL/250 mLYPD液体培养基中,180 r/min、28 ℃摇床培养,直至观察到培养基呈现浑浊状态,得到表皮酵母富集培养液。
1.3.2 酵母菌株分离与纯化
取1.3.1中富集好的培养液,在无菌条件下吸取1 mL,加入含有9 mL无菌水的试管中并摇匀,按此条件进行梯度稀释。 按此步骤,将上述样液稀释到10-8,选取稀释梯度为10-6~10-8的菌液涂布于YPD固体培养基上,28 ℃培养2~3 d,选取具有酵母显著形态的单菌落分离纯化2~3次,编号后接入富集培养基试管斜面上,同样条件下培养并保存于4 ℃冰箱中备用。
1.3.3 酵母菌株起酵能力的研究
酵母菌发酵过程中会产生CO2气体,气体充满杜氏小管的时间可直接反应菌株的起酵能力[24]。以2%的接种量将已活化的菌株接入含有杜氏小管的YPD液体培养基试管中,28 ℃持续培养48 h,每隔12 h记录杜氏小管内的产气量和产气时间。 基于发酵能力对比,筛选出发酵性能高效的菌株进行下一步实验。
1.3.4 酵母菌株耐受性的研究
将1.3.3中筛选的菌株进行葡萄糖、柠檬酸、SO2、乙醇的耐受性试验,
(1)葡萄糖耐受性:分别添加不同质量葡萄糖调配YPD液体培养基,使培养基中葡萄糖的质量浓度为200 g/L、300 g/L、400 g/L、500 g/L,向含有倒置杜氏小管的试管中分别加入4 mL不同质量浓度葡萄糖的YPD液体培养基。
(2)酸耐受性:对YPD液体培养基使用柠檬酸调节pH值至2.0、2.5、3.0、3.5,向含有倒置杜氏小管的试管中分别加入4 mL不同pH的YPD培养基。
(3)乙醇耐受性:在含有倒置杜氏小管的试管中分别加入4 mL的YPD液体培养基,并分别添加无水乙醇至乙醇体积分数为5%、7%、9%、11%。
(4)SO2耐受性:在含有倒置杜氏小管的试管中分别加入4 mL的YPD液体培养基,并分别添加偏重亚硫酸钾溶液至SO2含量为100 mg/L、150 mg/L、200 mg/L、250 mg/L。
以上试验均将待测菌株接种在试管中,置于28 ℃的恒温培养箱中静置培养3 d,观察小管内的产气情况。
1.3.5 酵母菌株发酵特性的研究
(1)产酯能力测定:采用点板法将筛选出的菌株接种于产酯培养基上,并于28 ℃恒温培养2~3 d。观察培养皿中各菌株所形成的菌落颜色,颜色越深的菌株产酯能力越强[25]。
(2)产H2S能力测定:采用点板法将筛选出的菌株接种于BIGGY琼脂培养基上,并在28 ℃避光环境中培养2~3 d。以铋为指示剂根据选择性培养基BIGGY上菌落颜色而判断菌株产H2S能力,白色、浅棕色、深棕色、黑色分别代表产H2S能力为不产、低产、中产、高产[26]。
(3)产乙醇能力测定:采用点板法接种筛选出的菌株于TTC下层培养基中,并在28 ℃避光培养2~3 d。出现菌落后,在其表面覆盖一层TTC上层培养基,维持原先的温度和光照条件继续培养3 h后,观察显色情况,产乙醇能力强的酵母会呈深红色,次之显粉红色[22]。
1.3.6 菌株的鉴定
(1)形态学鉴定
将筛选出的菌株接种于WL培养基上,于28 ℃培养5 d,参照《酵母菌的特征与鉴定手册》及《微生物学实验技术》,用接种环挑取少量菌体置于显微镜下进行形态观察。
(2)分子生物学鉴定
根据真菌基因组脱氧核糖核苷酸(deoxyribonucleic acid,DNA)提取试剂盒说明书提取DNA,以提取真菌的总DNA为模板,采用ITS通用引物(ITS1:5'-TCCGTAGGTGAACCTGCGG-3';ITS4:5'-TCCTCCGCTTATTGATATGC-3')通过聚合酶链式反应(polymerase chain reaction,PCR)扩增序列,将扩增产物送至擎科生物科技有限公司进行测序,并将测序结果通过基本局部比对搜索工具(basic local alignment search tool,BLAST)与美国国家生物技术信息中心(national center of biotechnology information,NCBI)GenBank数据库进行比对分析,利用软件Mega 11.0软件中邻接(neighbor-joining,NJ)法构建系统发育树。
1.3.7 酸木瓜汁及发酵汁的制备
将酸木瓜洗净切块榨汁,过滤得到酸木瓜汁;酸木瓜汁添加100 g/L无水葡萄糖,分别量取150 mL至三角瓶中于80 ℃条件下灭菌15 min。将筛选出的菌株分别接种至YPD液体培养基中进行活化培养,并以5%的接种量分别接种至酸木瓜汁中,28 ℃发酵10 d后得到相应的酸木瓜发酵汁,相应编号为F-菌株号。
1.3.8 电子鼻分析
准确量取上述酸木瓜汁及不同菌株发酵的酸木瓜汁各5 mL于30 mL样品瓶中,加盖密封,室温富集30 min后将进样针插入样品瓶,采用顶空吸气法进行电子鼻分析试验。
电子鼻参数设置:传感器清洗时间300 s,传感器归零时间5 s,样品准备时间5 s,进样流量150 mL/min,检测时间120 s,选择116~118 s的数据进行分析。完成每次检测系统进行清零和标准化后再测试下一个样品,每种样品重复3次测定,电子鼻传感器名称及其响应物质具体见表1。
表1 电子鼻传感器名称及其响应物质
Table 1 Name and responsive substance of electronic nose sensor
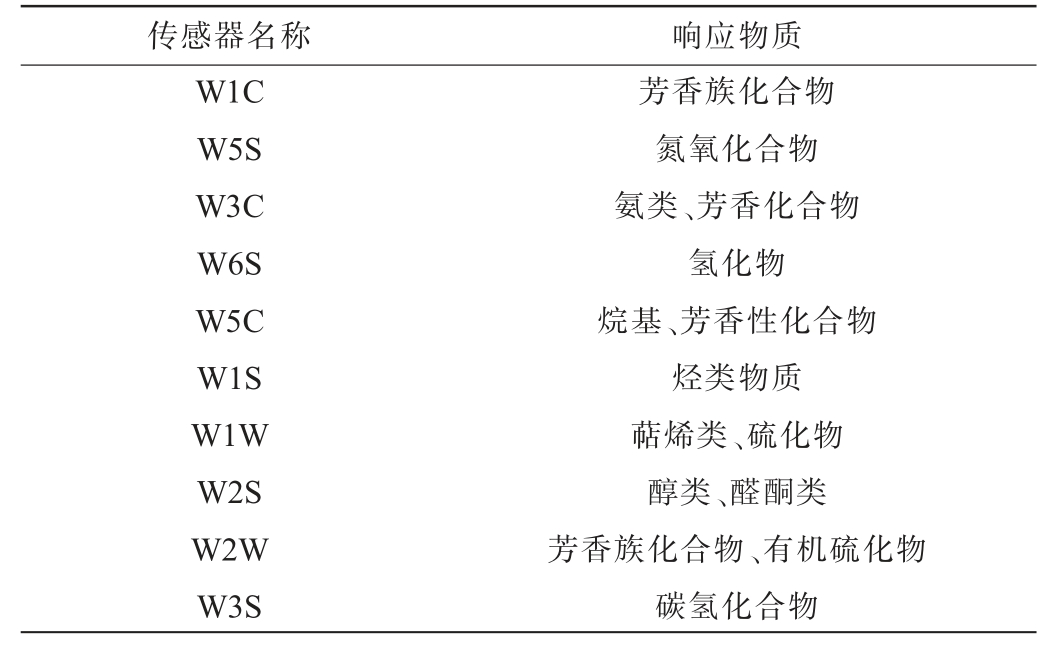
传感器名称 响应物质W1C W5S W3C W6S W5C W1S W1W W2S W2W W3S芳香族化合物氮氧化合物氨类、芳香化合物氢化物烷基、芳香性化合物烃类物质萜烯类、硫化物醇类、醛酮类芳香族化合物、有机硫化物碳氢化合物
1.3.9 数据处理
采用Microsoft Excel 2019、Origin 2021、Win Muster和Mega 11对数据进行整理和作图。 采用电子鼻PEN3的Win Muster对所测数据进行主成分分析、负荷加载分析(loading analysis,LA)以及气味雷达图分析[27]。
2 结果与分析
2.1 酵母菌的分离
共分离得到144株菌,其中从酸木瓜的自然发酵液分出22株菌株,编号为M1~M22,表皮中33株菌株,编号为G1~G33;从山楂的自然发酵液分出25株菌株,编号为S1~S25,表皮中分出22株菌株,编号为Z1~Z22;从柠檬的自然发酵液分出20株菌株,编号为N1~N20,表皮中分出22株菌株,编号为L1~L22。
2.2 酵母菌起酵特性筛选
对144株酵母菌进行杜氏小管发酵实验,分别将菌株接入到含有杜氏小管的YPD液体培养基中,28 ℃培养48 h,48 h内小管充满气体为发酵能力优秀的菌株,各菌株在48 h的产气情况见表2。 由表2可知,共有89株菌株产气性能优良,在48 h内产气量充满杜氏小管全部体积,因此选择这89株进行下一步耐受性能的筛选。
表2 筛选菌株杜氏小管产气情况
Table 2 Gas production situation of screened strains in the Durham tube

注:“-”表示杜氏小管内无气体;“+”表示产气量为杜氏小管体积的1/4;“++”表示产气量为杜氏小管的1/2;“+++”表示产气量约为杜氏小管体积的3/4;“++++”表示产气量约为杜氏小管全部体积。下同。
产气情况 数量/株 菌株编号++++M1、M3~M8、M10~M11、M15~M20、M22,G1、G3~G4、G25~G26、G28~G29、G32~G33,N1~N17、N19,L2、L4、L7、L8、L10、L12、L14、L18~L20,S1~S25,Z1~Z10 M2、M9、M12~M14、M21,G2、G5~G24、G27、G30~G31,N18、N20,L1、L3、L5、L6、L9、L11、L15~L17、L21~L 22,Z11~Z22 89-55
2.3 筛选菌株耐受性能分析
2.3.1 酸耐受性能分析
89株筛选菌株的酸耐受测定结果见表3。由表3可知,72 h内M1、M3、M4等31株菌株可在pH为2时产气量充满杜氏小管全部体积,其余58株均受到一定限制。 因此选择耐受至pH为2的31株菌株进行下一步筛选。
表3 筛选酵母菌株酸耐受测定结果
Table 3 Determination results of acid resistance of screened yeast strains

pH值 气体充满杜氏小管的菌株数量/株 菌株编号3.5 77 M1~8、M10~M11、M15~M20、M22,G1、G3~4、G25~26、G28~G29、G32~G33,N1~N17、N19,L2、L4、L7、L8、L10、L12、L14、L18~20,S13~S25,Z1~Z10 3.0 2.5 2.0 51 45 31 M1~6、M15~M16、M19,G26、G28~G29、G32~G33,N1~N2、N4~N9、N12、N16,L2、L7、L8、L10、L12、L14、L18~L20,S13~S25,Z1~Z4、Z7、Z10 M1、M3~M6、M15~M16、M19,G26、G28~G29、G32~G33,N1~N2、N4~N6、N9、N12、N16,L2、L7、L10、L12、L18~L20,S13~S25,Z1~Z4 M1、M3 ~M5、M15 ~M16、M19,G26、G28 ~G29、G32 ~G 33,N1 ~N 2、N4、N6、N9、N12、N16、L10、L19,S13、S15~S17、S21、S22,Z1~Z4
2.3.2 葡萄糖耐受性能分析
31株筛选菌株的葡萄糖耐受结果见表4。 由表4可知,72 h内G26、G28、G29等9株菌株可在葡萄糖质量浓度为500 g/L时产气量充满杜氏小管全部体积,其余22株受到一定限制。 因此选择耐受至葡萄糖质量浓度为500 g/L的9株菌株进行下一步筛选。
表4 筛选酵母菌株葡萄糖耐受测定结果
Table 4 Determination results of glucose resistance of screened yeast strains

葡萄糖质量浓度/(g·L-1)气体充满杜氏小管的菌株数量/株 菌株编号200 31 M1、M3 ~M5、M15 ~M16、M19,G26、G28 ~G29、G32 ~G 33,N1 ~N 2、N4、N6、N9、N12、N16,L10、L19,S13、S15~S17、S21、S22、Z1~S4 300 400 500 25 19 9 M1、M3、M5、M16,G26、G28~G29、G32,N1~N2、N4、N6、N9、N12、N16,L10,S13、S15~S17、S21、S22,Z1、Z3、Z4 M1、M3、M5、M16,G26、G28~G29,N1~N2、N4、N6、N12、N16,L10、L19,S13、S21、S22,Z3 G26、G28、G29,N1、N2、N4、N6,S21、S22
2.3.3 SO2耐受性能分析
9株筛选菌株的SO2耐受结果见表5。由表5可知,9株酵母菌株均能在250 mg/L的SO2胁迫环境中存活生长,且未受到明显抑制。 由于GB 2760—2014《食品安全国家标准食品添加剂使用标准》中规定果酒中二氧化硫限量指标为250 mg/L,故将9株菌全部保留进行下一步的筛选。
表5 筛选酵母菌株SO2耐受测定结果
Table 5 Determination results of SO2 resistance of screened yeast strains
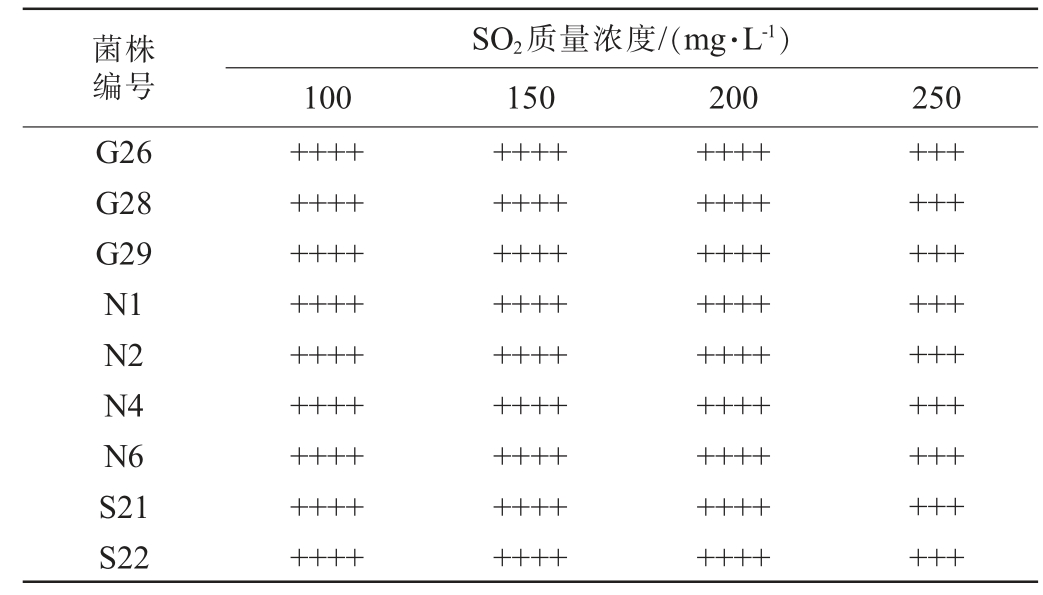
菌株编号G26 G28 G29 N1 N2 N4 N6 S21 S22 SO2质量浓度/(mg·L-1)100 150 200 250+++++++++++++++++++++++++++++++++++++++++++++++++++++++++++++++++++++++++++++++++++++++++++++++++++++++++++++++++++++++++++++++++++++++
2.3.4 乙醇耐受性能分析
9株筛选菌株的乙醇耐受性结果见表6。由表6可知,菌株G26、G28可耐受乙醇体积分数11%,菌株G29、N1、N4可耐受至乙醇体积分数9%,菌株N2、N6可耐受乙醇体积分数7%,菌株S21、S22可耐受乙醇体积分数5%。 因此选择可耐受乙醇体积分数9%的5株菌株(G26、G28、G29、N1、N4)进行下一步筛选。
表6 筛选酵母菌株乙醇耐受测定结果
Table 6 Determination results of alcohol resistance of screened yeast strains
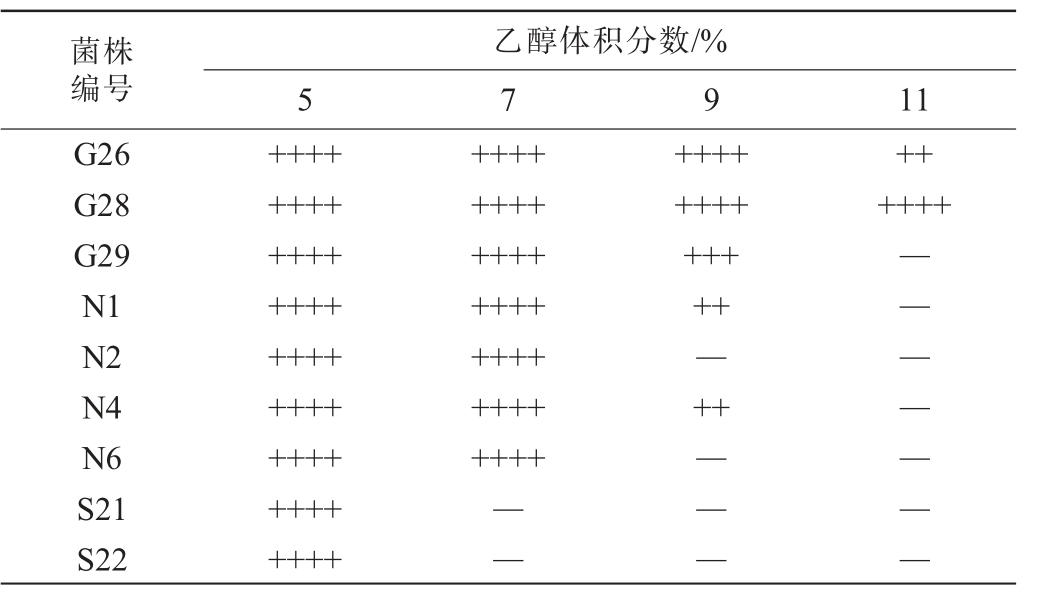
菌株编号G26 G28 G29 N1 N2 N4 N6 S21 S22乙醇体积分数/%5 7 9 11+++++++++++++++++++++++++++++++++++++++++++++++++++++++++++++++++++++++++++++—++++++++——————
2.4 酵母菌株产酯、产H2S以及产乙醇能力测定
2.4.1 产酯能力测定
选择产气及各耐受性能优良的5株菌株(G26、G28、G29、N1、N4)进行产酯能力的测定,结果见表7。由表7可知,5株菌株在产酯培养基上显色都呈黄色,菌株G26、G28、G29、N1在产酯培养基上的显色相对较深,产酯能力相对更强;而菌株N4为浅黄色,说明其产酯能力相对较低。
表7 筛选酵母菌株在产酯培养基上的显色结果
Table 7 Chromogenic results of screened yeast strains on ester producing medium
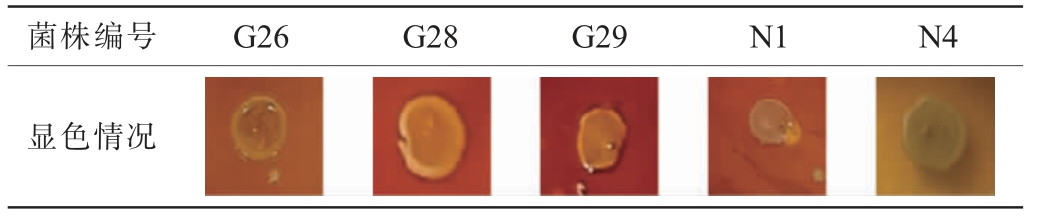
菌株编号 G26 G28 G29 N1 N4显色情况images/BZ_220_351_3070_1141_3189.png
2.4.2 产H2S能力测定
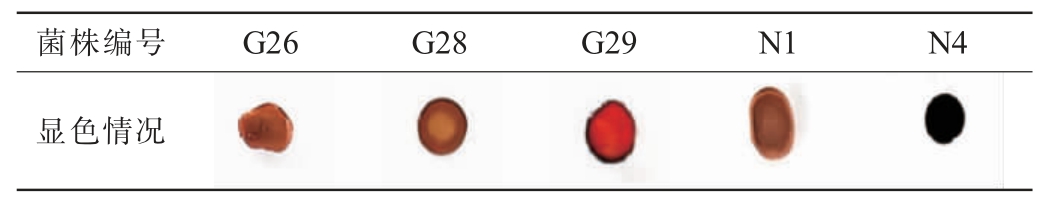
选择产气及各耐受性能优良的5株菌株进行产H2S能力的测定,结果见表8。由表8可知,菌株G26、G28、N1呈浅棕色,属于低产硫化氢类菌株;G29呈深棕色,属于中产硫化氢类菌株;N4显色呈黑色,属于高产硫化氢类菌株。
表8 筛选酵母菌株在BIGGY培养基上的显色结果
Table 8 Chromogenic results of screened yeast strains on BIGGY medium
菌株编号 G26 G28 G29 N1 N4显色情况images/BZ_220_1461_945_2251_1063.png
2.4.3 产乙醇能力测定
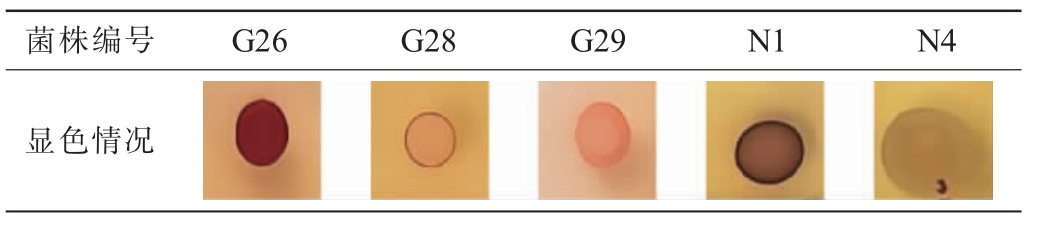
选择产气及各耐受性能优良的5株菌株通过TTC平板显色法进行产乙醇能力的测定,结果见表9。由表9可知,菌株G26、N1呈深红色,菌株G28、G29呈淡粉色,N4呈白色,说明菌株G26和N1产乙醇能力最强,菌株G28、G29产乙醇能力其次。
表9 筛选酵母菌株在TTC培养基上的显色结果
Table 9 Chromogenic results of screened yeast strains on TTC medium
菌株编号 G26 G28 G29 N1 N4显色情况images/BZ_220_1461_1776_2251_1895.png
综上,本试验筛选的4株非酿酒酵母G26、G28、G29、N1可在葡萄糖质量浓度为500 g/L、pH2、乙醇体积分数9%的条件下依旧可以生长,说明这些菌株的综合耐受性更强,更不易受到酿造环境的胁迫,同时具有良好产酯能力和产乙醇能力,在提高果酒风味丰富度上有巨大潜力。
2.5 筛选酵母菌株的鉴定
2.5.1 形态学观察
将菌株G26、G28、G29、N1划线于WL培养基上,28 ℃恒温培养5 d,其菌落形态见图1。由图1可知,在WL培养基上,G26菌落为暗粉色、圆形、饱满凸起,G28菌落为白色、圆形、形状较小,G29菌落为蓝色、圆形、表面光滑有光泽、边缘透明,N1菌落为乳白色、圆形、表面光滑有光泽;在显微镜中观察4个菌株的细胞形态均为椭圆形。
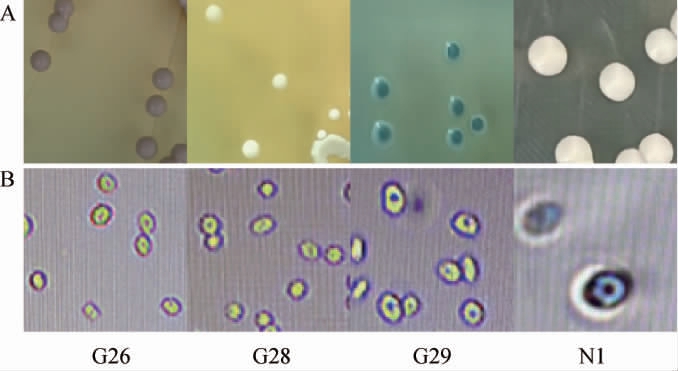
图1 筛选菌株的菌落形态及显微形态
Fig.1 Colony morphology and microscopic morphology of screened strains
2.5.2 分子生物学鉴定
基于26S rDNA D1/D2区基因序列构建4株酵母菌株的系统发育树,结果见图2。由图2可知,菌株N1与季也蒙迈耶氏酵母(Meyerozyma guilliermondii)CBS 2030聚于一支,菌株G26与美极梅奇酵母(Metschnikowia pulcherrima)NRRL Y-6546聚于一支,菌株G28与(Wickerhamomyces anomalus)CNRMA10.1139聚于一支,菌株G29与(Lachancea waltii)NRRL Y-8285聚于一支,亲缘关系最近。结合形态学观察,将菌株N1鉴定为季也蒙迈耶氏酵母(Meyerozyma guilliermondii),菌株G26鉴定为美极梅奇酵母(Metschnikowia pulcherrima),菌株G28鉴定为异常威克汉姆酵母(Wickerhamomyces anomalus),菌株G29鉴定为耐热拉钱斯氏酵母(Lachancea waltii)。

图2 基于26SrDNA D1/D2区基因序列4株酵母菌株的系统发育树
Fig.2 Phylogenetic tree of 4 yeast strains based on 26S rDNA D1/D2 region gene sequences
2.6 酸木瓜果汁及发酵汁的电子鼻分析
2.6.1 气味雷达图
采用电子鼻评价不同非酿酒酵母菌株发酵酸木瓜汁(F-N1、F-G26、F-G28、F-G29)与酸木瓜果汁(SMG)的香气特性,其气味分析传感器相应雷达图见图3。 由图3可知,5组样品中传感器W1C、W3C、W6S、W5C、W1S、W1W、W2W、W3S测定的响应值基本相同,无明显差别。F-N1、F-G26中传感器W2S和W5S测定的响应值均高于SMG,这表明2组酸木瓜发酵汁中醇类和醛酮类化合物、氮氧化合物含量均高于SMG;而F-G28、G29对比SMG有一定差异,但结果不明显。
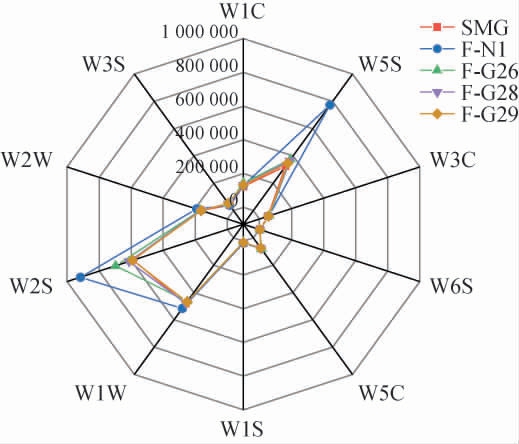
图3 不同非酿酒酵母菌株发酵酸木瓜汁电子鼻响应值雷达图
Fig.3 Radar chart of electronic nose response values of Chaenomeles sinensis juice fermented by different non-Saccharomyces strains
2.6.2 负荷加载分析
应用电子鼻对酸木瓜汁和不同酸木瓜发酵汁进行负荷加载分析(loading analysis,LA),结果见图4。由图4可知,第一主成分的方差贡献率为93.94%、第二主成分的方差贡献率为4.80%,总方差贡献率为98.74%。结合表1可知,对第一主成分较为灵敏的为芳香化合物、无机硫化物,对第二主成分灵敏度最高的为氮氧化合物。 综合来看,W5S、W1W对不同菌株酸木瓜发酵汁的风味起到了主要作用。
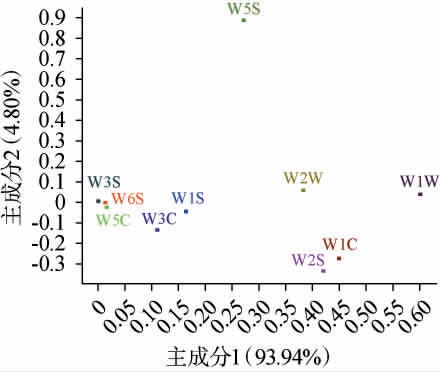
图4 负荷加载分析传感器区分贡献率
Fig.4 Discrimination contribution rate of loading analysis sensors
2.6.3 主成分分析
基于电子鼻响应值,酸木瓜汁及不同非酿酒酵母发酵酸木瓜汁的主成分分析(principal component analysis,PCA)结果见图5。由图5可知,第一主成分的方差贡献率为93.94%,第二主成分的方差贡献率为4.80%,总方差贡献率为98.74%,说明两个主成分包含了样品的大部分信息,可以反映整体挥发性物质的规律。图中第一主成分的方差贡献率远大于第二主成分,表明PC1轴上的距离越大,样品的差异性越大。 F-G26、F-G28、F-G29三个酸木瓜发酵汁的间距较小,与酸木瓜汁SMG对比距离较大,差异明显;F-N1与SMG、F-G26、F-G28、F-G29之间各主成分距离较远,均具有一定差异性,但与F-G26、F-G28、F-G29的第一主成分接近,主要差异体现在第二主成分上。 主成分分析中,四种酸木瓜发酵汁与酸木瓜汁均具有一定间距,且边界无重叠,说明发酵产生了其各自的挥发性风味成分,其中F-N1与其他样品的差异性最显著,F-G26、F-G28、F-G29三种酸木瓜发酵汁产生的风味差异性最小。
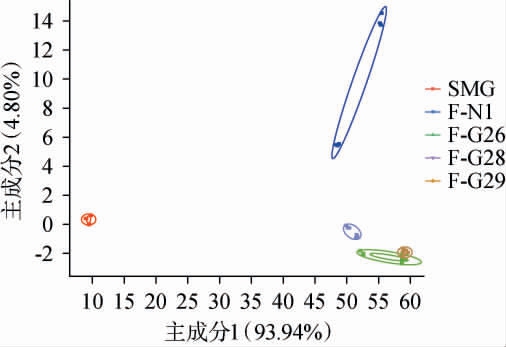
图5 基于电子鼻响应值不同非酿酒酵母菌株发酵酸木瓜汁的主成分分析
Fig.5 Principal component analysis of Chaenomeles sinensis juice fermented by different non-Saccharomyces strains based on electronic nose response values
3 结论
本试验以三种高酸水果(云南酸木瓜、山楂、柠檬)的自然发酵液及其表皮作为酵母的分离来源,分离得到的144株菌株中有4株可耐受葡萄糖质量浓度500 g/L、pH 2、SO2质量浓度250 mg/L、乙醇含量9%,同时具备优良的产酯能力和产酒精能力和低产硫化氢能力。 分别将这4株菌株进行形态学鉴定及分子生物学鉴定,确定菌株G26为美极梅奇酵母(Metshnikowia pulcherrima),菌株N1为季也蒙迈耶氏酵母(Meyerozyma guilliermonclii),菌株G28为异常威克汉姆酵母(Wickerhamomyces anomalus),菌株G29为耐热拉钱斯氏酵母(Lachancea waltii)。通过电子鼻分析4种酸木瓜发酵汁中挥发性成分的变化,结果显示,菌株N1和G26发酵酒中醇类、醛酮类化合物和氮氧化合物含量变化最显著;LA分析中显示酸木瓜发酵汁对第一主成分较为灵敏的主要为芳香化合物、无机硫化物,对第二主成分灵敏度最高的为氮氧化合物;PCA图中除F-G26和F-G29酒样有一定重叠,其他各发酵样无重叠,因此PCA分析可将不同酵母发酵的酸木瓜发酵汁进行有效区分,其中F-N1与其他样品的差异性最明显。
本研究通过菌株基本发酵特性的研究以及发酵产物主成分分析,筛选出4株潜力非酿酒酵母菌株,可为酸木瓜酒的发酵酿造奠定一定的菌种基础,通过进一步对筛选菌株进行驯化并对酸木瓜发酵汁发酵工艺进行优化,有望成为优质酸木瓜果酒酿造菌种资源,还可为酸木瓜资源的开发利用提供新的方向与理论依据。
[1]张健,赵庆桃,李静思,等.云南产区酸木瓜酒品质改良研究[J].中国果菜,2022,42(10):22-29.
[2]KOSTECKA-GUGAŁA A.Quinces(Cydonia oblonga,Chaenomeles sp.,and Pseudocydonia sinensis) as medicinal fruits of the rosaceae family:Current state of knowledge on properties and use[J].Antioxidants,2024,13(1):71.
[3]ANDRADE P B,CARVALHO A R F,SEABRA R M,et al.A previous study of phenolic profiles of quince,pear,and apple purees by HPLC diode array detection for the evaluation of quince puree genuineness[J].J Agr Food Chem,1998,46:968-972.
[4]SUT S,DALL'ACQUA S,POLONIATO,et al.Preliminary evaluation of quince (Cydonia oblonga Mill.) fruit as extraction source of antioxidant phytoconstituents for nutraceutical and functional food applications[J].J Sci Food Agr,2019,99:1046-1054.
[5]NOWICKA P,WOJDYŁO A,TELESZKO M,et al.Sensory attributes and changes of physicochemical properties during storage of smoothies prepared from selected fruit[J].LWT-Food Sci Technol,2016,71:102-109.
[6]罗文静,李燮昕,张羽晨,等.酸木瓜资源利用及加工技术的研究进展[J].新农业,2018(17):35-39.
[7]MIHARA S,TATEBA H,NISHIMURA O,et al.Volatile components of Chinese quince (Pseudocydonia sinensis Schneid)[J].J Agr Food Chem,1987,35(4):532-537.
[8]CIANI M,COMITINI F,MANNAZZU I,et al.Controlled mixed culture fermentation:A new perspective on the use of non-Saccharomyces yeasts in winemaking[J].FEMS Yeast Res,2010,10(2):123-133.
[9]ŠUKLJE K,ANTALICK G,BUICA A,et al.Inactive dry yeast application on grapes modify Sauvignon Blanc wine aroma[J].Food Chem,2016,197:1073-1084.
[10]CONTRERAS A,HIDALGO C,HENSCHKE P A,et al.Evaluation of non-Saccharomyces yeasts for the reduction of alcohol content in wine[J].Appl Environ Microbiol,2014,80(5):1670-1678.
[11]王飞,王晓宇,赵擎豪,等.果酒增香酿造技术研究进展[J].食品科学,2023,44(13):244-252.
[12]王春晓,俞俊竹,周文亚,等.非酿酒酵母属酵母的葡萄酒发酵应用研究进展[J].中国农业科学,2023,56(3):529-548.
[13]MOREIRA N,PINA C, MENDES F, et al.Volatile compounds contribution of Hanseniaspora guilliermondii and Hanseniaspora uvarum during red wine vinifications[J].Food Control,2011,22(5):662-667.
[14] HALL H, ZHOU Q, QIAN M C, et al.Impact of yeasts present during prefermentation cold maceration of pinot noir grapes on wine volatile aromas[J].Am J Enol Viticult,2017,68(1):81-90.
[15]DUTRAIVE O, BENITO S, FRITSCH S, et al.Effect of sequential inoculation with non-Saccharomyces and Saccharomyces yeasts on Riesling wine chemical composition[J].Fermentation,2019,5(3):79.
[16]罗来庆,林海明,焦宇知,等.非酿酒酵母与酿酒酵母混合发酵对葡萄酒香气的影响[J].中国酿造,2022,41(10):89-94.
[17]XU A, XIAO Y, HE Z, et al.Use of non-Saccharomyces yeast co-fermentation with Saccharomyces cerevisiae to improve the polyphenol and volatile aroma compound contents in nanfeng tangerine wines[J].J Fungi (Basel),2022,8(2):128.
[18]黄倩,蔡建,高秀,等.羊奶果果酒专用本土非酿酒酵母的筛选、鉴定及特性研究[J].中国酿造,2024,43(6):156-161.
[19]高娉娉.高产β-葡萄糖苷酶本土优良非酿酒酵母菌株筛选及应用效果评价[D].兰州:甘肃农业大学,2022.
[20]方月月,解文利,潘肇仪,等.生姜猕猴桃自然酒精发酵醪微生物多样性研究[J].中国酿造,2020,39(12):125-129.
[21]白玉峰,张文霞,田亚楠,等.宁夏贺兰山东麓降L-苹果酸葡萄酒酵母的筛选[J].中国酿造,2021,40(1):49-54.
[22]李凯,王金晶,李永仙,等.红芯火龙果酒酿酒酵母的筛选及鉴定[J].食品与发酵工业,2019,45(5):115-120.
[23]胡江南,高熳熳,马立娟,等.葡萄酒发酵优良酵母的筛选、鉴定及应用[J].中国酿造,2023,42(7):43-50.
[24]乔喜玲.干红葡萄酒酿酒酵母的优选及其酿酒特性研究[D].呼和浩特:内蒙古农业大学,2020.
[25]忻胜兵.优质特性酿酒酵母的选育及直投式发酵菌剂研发[D].呼和浩特:内蒙古农业大学,2018.
[26]PORTER T J, DIVOL B, SETATI M E.Investigating the biochemical and fermentation attributes of Lachancea species and strains:Deciphering the potential contribution to wine chemical composition[J].Int J Food Microbiol,2019,290:273-287.
[27]赵宁,魏新元,樊明涛,等.SPME-GC-MS结合电子鼻技术分析不同品种猕猴桃酒香气物质[J].食品科学,2019,40(22):249-255.