尾穗苋属于苋科(Amaranthaceae),是一种一年生草本植物[1-2]。由于南方气候温暖湿润,适合种植品质优、营养高的苋菜品种[3-4]。由于苋菜抗性强、易栽培、抗旱、耐潮、耐高温、病虫害发生率低等特点,因此逐渐被国内外人们所采用,并发展为集“粮、菜、饲料”于一体的草本植物[5-8]。
当前,苋菜在全球范围内的主要应用集中在叶子部分,而对于其籽粒(如尾穗苋籽粒)的加工利用相对有限,且有关其食品安全性的研究资料也比较匮乏。尾穗苋籽粒作为一种极具开发潜力的健康功能食品原料,是蔬菜或饲料营养丰富,同时含有丰富的酚类、黄酮、有机酸、甾醇和萜类等营养物质[9-13],而作为药物则具有抗氧化、抗肿瘤、抗溃疡、增强免疫力等作用[14-15]。其营养组成全面而独特[16-17],籽粒中淀粉含量为48%~69%,其中支链淀粉比例高达76%,蛋白质含量约17%[18-21],脂肪含量达6.2%,显著高于普通谷物,且不饱和脂肪酸与必需脂肪酸比例优异[22-23];在矿物质方面,尾穗苋籽粒的钙含量为小麦的7倍,铁含量高达大米的80倍,并富含锌、硒等必需微量元素[24-25];更突出的是,其油脂中含2%~8%的角鲨烯,这一含量远超大多数植物。 研究表明,角鲨烯能有效抑制胆固醇合成[26-27]。 BERGER A等[28]通过动物实验证实,饲喂含尾穗苋饲料可使仓鼠总胆固醇降低10%,表明其对血脂调节具有特异性作用。这些特性共同奠定了尾穗苋籽粒在功能食品开发中的重要价值。尾穗苋中草酸盐与硝酸盐积累:许多藜科植物(包括苋属)在生长过程中会富集土壤中的硝酸盐,并在叶片或种子中形成草酸结晶。高浓度的草酸可刺激消化道黏膜,影响矿物质吸收(如钙、铁),长期过量摄入可能导致肾结石等问题。虽然成熟植株通常通过代谢降低此类成分,但未充分加工的籽粒仍可能残留较高水平。 刘贤贤等[19]研究发现,木犀草素对人肝癌细胞HepG2和SMMC-7721有显著的细胞毒活性,其他化合物对以上两种细胞没有细胞毒活性。然而,目前关于尾穗苋籽粒的科学研究尚处于初级阶段,尤其是关于其毒性、安全性评估等方面的研究还不充分。鉴于我国在尾穗苋籽粒毒理学数据方面的空缺,该研究参照GB 15193.1—2014《食品安全性毒理学评价程序》,对尾穗苋籽粒进行了系统的食品安全风险评估,包括急性经口毒性试验,28 d经口毒性试验及小鼠红细胞微核试验。目的在于评估尾穗苋籽粒食用安全性,从而为尾穗苋籽粒作为新的食品原料提供坚实的科学依据,推动其在食品行业的进一步开发和广泛应用。
1 材料与方法
1.1 材料与试剂
1.1.1 材料
尾穗苋籽粒:贵州省威宁县;环磷酰胺(分析纯):上海源叶生物科技有限公司;丝裂霉素(分析纯):萨恩化学技术(上海)有限公司;中国仓鼠肺细胞株:中国科学院上海生命科学研究院细胞库;纯化水:实验室纯水机自制。
1.1.2 实验动物
无特定病原体(specific pathogen free,SPF)级SD大鼠:上海必凯科翼生物科技有限公司;生产许可证号SCXK(沪)2018-0006,合格证编号:20180006052158。 雌性大鼠初始体质量71~81 g;雄性大鼠初始体质量76~90 g。
健康成年SPF级美国癌症研究所(institute of cancer research,ICR)小鼠:南京医科大学提供,生产许可证号SCXK(苏)2021-0001,合格证编号:202278210。雌性小鼠体质量18.4~21.2 g,雄性小鼠体质量19.4~21.5 g。
1.2 仪器与设备
T1000型电子天平:广州金博仕生物技术有限公司;OLYMPUS型显微镜:北京创诚致佳科技有限公司;BBSSDC型超净工作台、STACompact型全自动血凝仪:上海寰熙医疗科技有限公司;D180型CO2培养箱:深圳市瑞沃德生命科技股份有限公司;SX-700型高压灭菌器:青岛佳鼎分析仪器有限公司;LB9110-1100ⅡA2型生物安全柜:青岛路博建业环保科技有限公司;LRH-250-S型电热恒温培养箱:东莞市广开仪器设备有限公司;THZ-312型恒温摇床:上海测博生物科技发展中心;HR40-IIA2型密理博纯水仪:南充实维仪器有限公司;DL-TG16G型高速离心机:青岛精诚仪器仪表有限公司;HTSH-3000型全自动生化分析仪:济南爱来宝仪器设备有限公司;SIEMENSADVIA2120i血液分析仪: 北京长缨飞鸿科技发展有限公司;纯水机:北京生物泽平科技有限责任公司。
1.3 方法
1.3.1 急性经口毒性试验
试验采用60只健康成年SPF级ICR小鼠作为试验对象,其中雌雄各半,分为溶剂对照组和受试样品组,每5只雌性加5只雄性为一个试验组,每组重复3次,均在特定的环境条件下饲养,温度在20~26 ℃,相对湿度控制在40%~70%范围内,利于维持生理状态稳定,减少非试验因素对试验结果的影响[29-30]。
在试验前3 d,小鼠被隔离饲养以减少外部干扰,并在试验开始前禁食16 h,但仍允许其自由饮水,确保在给药时胃部基本为空,从而避免食物对药物吸收的影响。 参照GB 15193.3—2014《食品安全国家标准急性经口毒性试验要求》一次性给予的试验剂量为10 000 mg/kg体质量。 将尾穗苋籽粒样品研磨成粉末状,使用纯化水配制成质量浓度为500 mg/mL的溶液,则按照20 mL/kg体质量的比例一次性给予配制好的样品溶液。 对照组每日给予20 mL/kg体质量的纯化水,采用限量法进行试验,给样观察14 d,观察情况。第0天、第7天、第14天称体质量一次。试验结束后,对动物进行解剖检查,如果解剖有任何病理变化,则进行组织病理学检查。计算半数致死量(median lethal dose,LD50)值并根据急性毒性(LD50)剂量分级标准见对该受试物进行急性毒性分级,分级判定标准见表1。
表1 急性毒性剂量分级标准
Table 1 Dose classification standards of acute toxicity
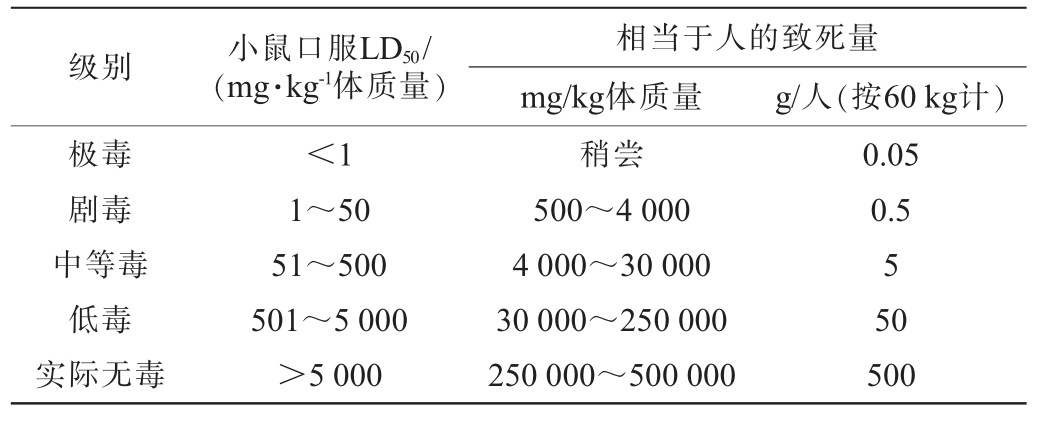
级别 小鼠口服LD50/(mg·kg-1体质量)相当于人的致死量mg/kg体质量 g/人(按60 kg计)极毒剧毒中等毒低毒实际无毒<1 1~50 51~500 501~5 000>5 000稍尝500~4 000 4 000~30 000 30 000~250 000 250 000~500 000 0.05 0.5 5 50 500
1.3.2 28 d经口毒性试验设计
28 d经口毒性试验中使用120只SPF级SD大鼠,雌雄各半。根据大鼠的体质量随机将它们分为4个试验组,每组包含30只大鼠,且保证每组内雌性和雄性大鼠各有15只,记录下每只大鼠的初始体质量。
试验设置4个不同的处理组别:空白对照组0mg/(kg·d),即不给予尾穗苋籽粒的大鼠;10 000 mg/(kg·d)剂量组,按照大鼠体质量每千克每天给予10 000 mg尾穗苋籽粒;4 000 mg/(kg·d)剂量组,按照大鼠体质量每千克每天给予4 000 mg尾穗苋籽粒;1 600 mg/(kg·d)剂量组,按照大鼠体质量每千克每天给予1 600 mg尾穗苋籽粒。
以纯化水作为溶剂,将尾穗苋籽粒粉末分别配制成500 mg/mL、200 mg/mL、80 mg/mL 3种质量浓度的溶液,以满足不同剂量组的需求。按照每只大鼠体质量每千克给予20 mL溶液的标准进行灌胃操作,每天一次,连续灌胃28 d。在这期间,大鼠可以自由进食和饮水。
1.3.3 试验指标测定
(1)体质量、食物利用率
每7 d记录一次大鼠体质量数据,结合4周体质量,再计算总体质量增加;每7 d记录一次摄食量数据,称量周初的投料量和周末的剩余料量,两者之差即为该周的摄食量,结合4周的摄食量,再计算总摄食量。
食物利用率计算公式如下:
(2)血液学指标
取大鼠血液用血液分析仪及全自动血凝仪测定各类白细胞数并计算与总白细胞的占比、血红蛋白浓度、红细胞计数、红细胞压积、血小板计数、凝血酶原时间、活化部分凝血活酶时间等。血液生化指标:取大鼠血清,用全自动生化分析仪测定血清丙氨酸氨基转移酶、门冬氨酸氨基转移酶、碱性磷酸酶、谷氨酰转肽酶、尿素、肌酐、血糖、总蛋白、白蛋白、总胆固醇、甘油三酯、氯、钾、钠等。 脏器系数:进行大体解剖检查后,小心分离心脏、胸腺、肾上腺、肝脏、肾脏、脾脏、睾丸、卵巢,用生理盐水洗净,滤纸吸水后称质量,根据脏器的质量与大鼠体质量的比值分别计算脏器系数。
1.3.4 小鼠红细胞微核试验
选取50只健康的ICR小鼠,购买后适应环境3 d。随机划分为5个小组,每组雌雄各半,受试小鼠给药后30 h在温度20.0~26.0 ℃,相对湿度40%~70%的条件下饲养。
采用30 h给受试物法,两次给受试样品间隔24 h,第二次给受试样品后6 h处死动物,取胸骨常规制片、镜检。 每鼠计数2 000个骨髓嗜多染红细胞(polychromatic erythrocyte,PCE),观察含微核的嗜多染红细胞数并计算微核发生率,以千分率计。 每鼠计数200个嗜多染红细胞(PCE)时所观察到的成熟红细胞数(normochromatic erythrocyte,NCE),并计算嗜多染红细胞与总红细胞比值(PCE/(NCE+PCE))。
本次毒性试验中,选择纯化水作为尾穗苋籽粒的溶剂,以不同剂量给大鼠灌胃,按照表2的设计进行试验。
表2 红细胞微核试验剂量设置
Table 2 Dose setting for erythrocyte micronucleus test
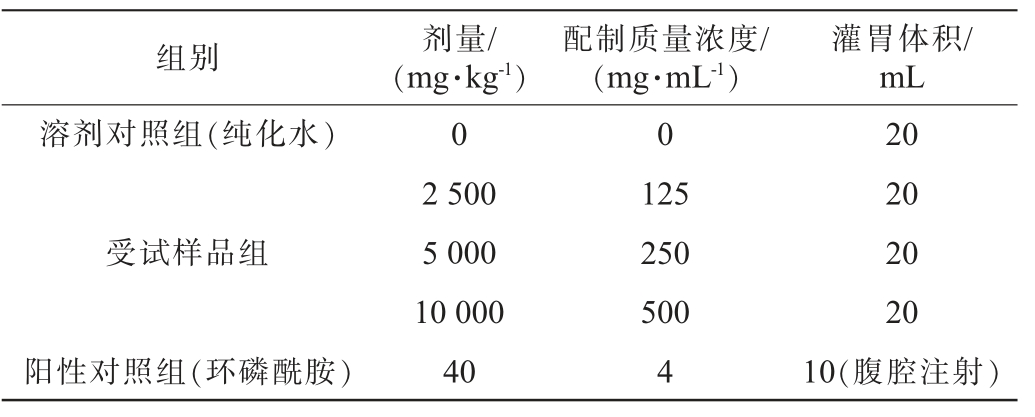
组别 剂量/(mg·kg-1)灌胃体积/mL溶剂对照组(纯化水)配制质量浓度/(mg·mL-1)0 0受试样品组阳性对照组(环磷酰胺)2 500 5 000 10 000 40 125 250 500 4 20 20 20 20 10(腹腔注射)
1.3.5 数据处理统计分析
使用IBM SPSS 25.0进行显著性分析,采用Origin 2021对所得数据进行绘图处理及统计学分析。
2 结果与分析
2.1 急性经口毒性试验
试验观察期间,灌胃剂量为10 000 mg/kg尾穗苋籽粒溶液的动物未见任何中毒表现及死亡。动物急性经口毒性试验结果见表3。由表3可知,14 d内雌雄小鼠体质量均呈上升趋势,其中雄性小鼠体质量上升幅度大于雌性小鼠。观察期结束动物大体解剖肉眼观察未见明显异常。试验表明尾穗苋籽粒雌、雄性小鼠急性经口毒性试验LD50>10 000 mg/kg,依据表1的急性毒性剂量分级标准,尾穗苋籽粒属于实际无毒级。
表3 动物急性经口毒性试验结果
Table 3 Results of acute oral toxicity test on animals
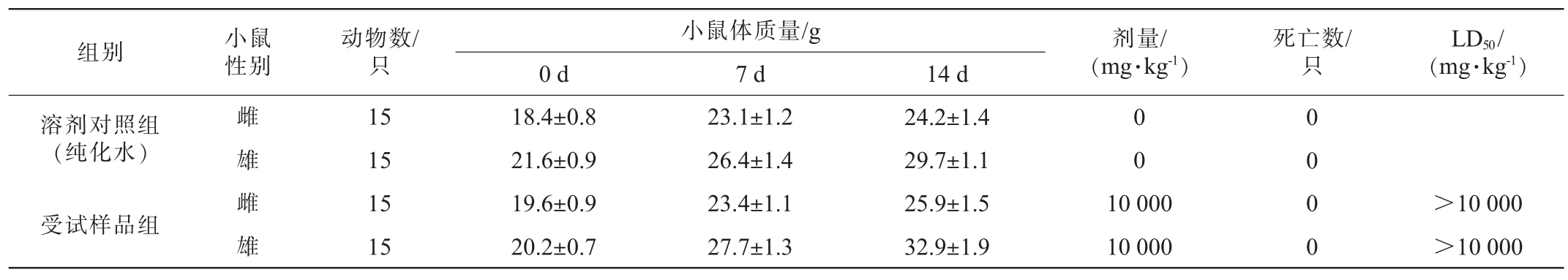
组别 小鼠性别小鼠体质量/g 7 d 14 d溶剂对照组(纯化水)动物数/只LD50/(mg·kg-1)0 d剂量/(mg·kg-1)死亡数/只雌雄雌雄15 15 15 15 18.4±0.8 21.6±0.9 19.6±0.9 20.2±0.7 23.1±1.2 26.4±1.4 23.4±1.1 27.7±1.3 24.2±1.4 29.7±1.1 25.9±1.5 32.9±1.9 0 0受试样品组10 000 10 000 0 00 0>10 000>10 000
2.2 28 d经口毒性试验
2.2.1 样品对大鼠体质量、食物利用率的影响
试验过程中,大鼠接受口服不同剂量的尾穗苋籽粒处理,并进行了持续28 d的观察。 口服籽粒苋溶液对大鼠体质量的影响见表4。 由表4可知,第0天雌、雄性各剂量组大鼠体质量差异无统计学意义(P>0.05),即试验前大鼠的体质量在各组间较为均衡。 且雌、雄性大鼠各剂量组各时间点的体质量与空白对照组比较,差异均无统计学意义(P>0.05)。说明受试物没有引起全身性毒性反应,不同剂量的尾穗苋籽粒未对雌性和雄性大鼠的正常生长发育产生任何不良影响。
表4 尾穗苋籽粒对大鼠体质量的影响
Table 4 Effect of Amaranthus caudatus seeds on body mass of rats
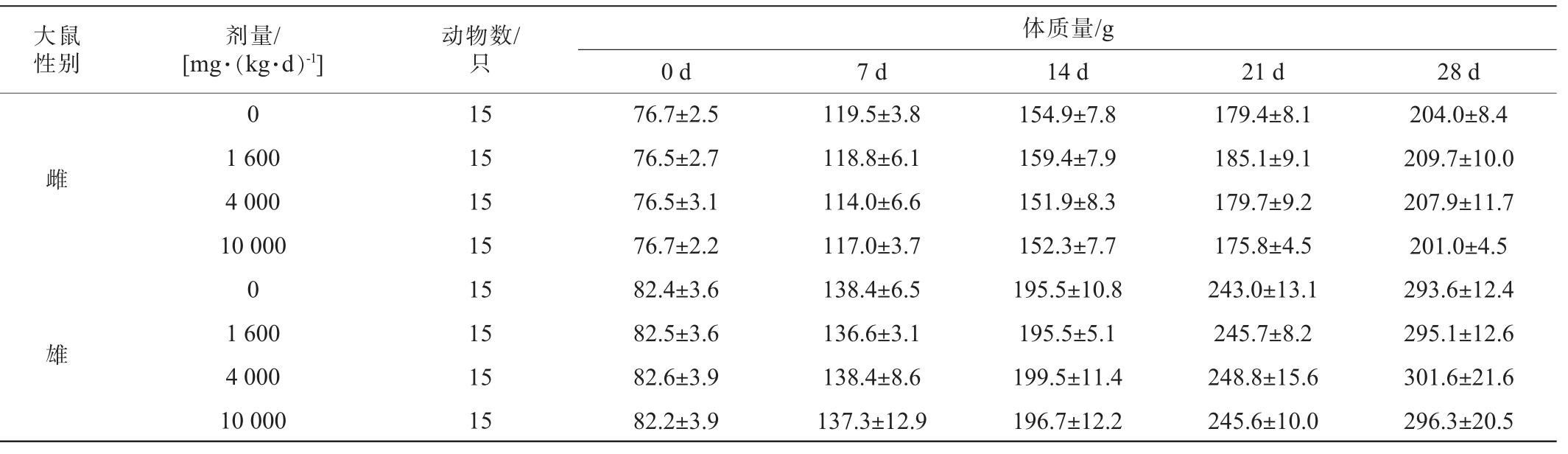
大鼠性别剂量/[mg·(kg·d)-1]动物数/只体质量/g 0 d 7 d 14 d 21 d 28 d雌雄0 1 600 4 000 10 000 0 1 600 4 000 10 000 15 15 15 15 15 15 15 15 76.7±2.5 76.5±2.7 76.5±3.1 76.7±2.2 82.4±3.6 82.5±3.6 82.6±3.9 82.2±3.9 119.5±3.8 118.8±6.1 114.0±6.6 117.0±3.7 138.4±6.5 136.6±3.1 138.4±8.6 137.3±12.9 154.9±7.8 159.4±7.9 151.9±8.3 152.3±7.7 195.5±10.8 195.5±5.1 199.5±11.4 196.7±12.2 179.4±8.1 185.1±9.1 179.7±9.2 175.8±4.5 243.0±13.1 245.7±8.2 248.8±15.6 245.6±10.0 204.0±8.4 209.7±10.0 207.9±11.7 201.0±4.5 293.6±12.4 295.1±12.6 301.6±21.6 296.3±20.5
经口给予大鼠不同剂量的尾穗苋籽粒28 d,根据各组大鼠摄食量计算各组大鼠食物利用率,结果见表5。用单因素方差分析方法中多个试验组与一个对照组间均数的两两比较方法进行统计处理。 结果可见,雌雄各剂量组的各指标与空白对照组比较,差异均无统计学意义(P>0.05)。这说明即使给予高剂量投喂,大鼠的体质量增长和食物转化效率没有受影响,未出现毒性或代谢负担。
表5 尾穗苋籽粒对大鼠食物利用率的影响
Table 5 Effect of Amaranthus caudatus seeds on food utilization rates of rats
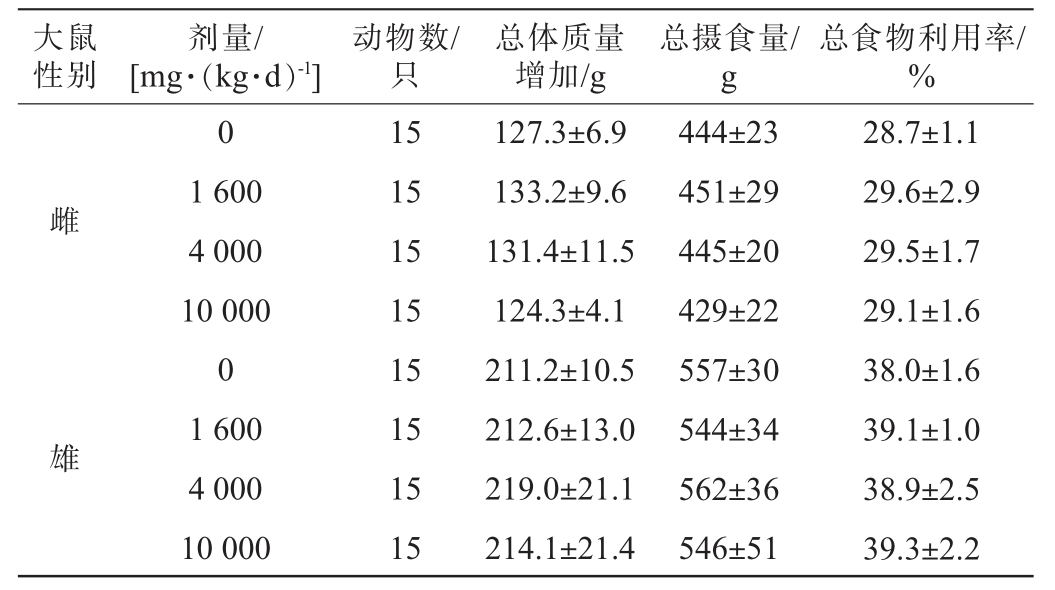
大鼠性别剂量/[mg·(kg·d)-1]动物数/只总体质量增加/g总摄食量/g总食物利用率/%0雌雄1 600 4 000 10 000 0 1 600 4 000 10 000 15 15 15 15 15 15 15 15 127.3±6.9 133.2±9.6 131.4±11.5 124.3±4.1 211.2±10.5 212.6±13.0 219.0±21.1 214.1±21.4 444±23 451±29 445±20 429±22 557±30 544±34 562±36 546±51 28.7±1.1 29.6±2.9 29.5±1.7 29.1±1.6 38.0±1.6 39.1±1.0 38.9±2.5 39.3±2.2
综合表4、表5结果可知,在试验设定的剂量范围内,大鼠进食量和食物利用率都维持在正常、稳定的水平,尾穗苋籽粒的摄入并未对大鼠体质量和总食物利用率产生显著性影响(P>0.05)。
2.2.2 样品对大鼠血常规的影响
将尾穗苋籽粒口服给予大鼠不同剂量共28 d,检测各剂量组大鼠的多项血液指标,测定各剂量组大鼠血液红细胞计数、血红蛋白水平、白细胞计数及其分类等指标、红细胞压积、血小板计数、凝血酶原时间、活化部分凝血活酶时间等指标,结果分别见表6、图1和图2。
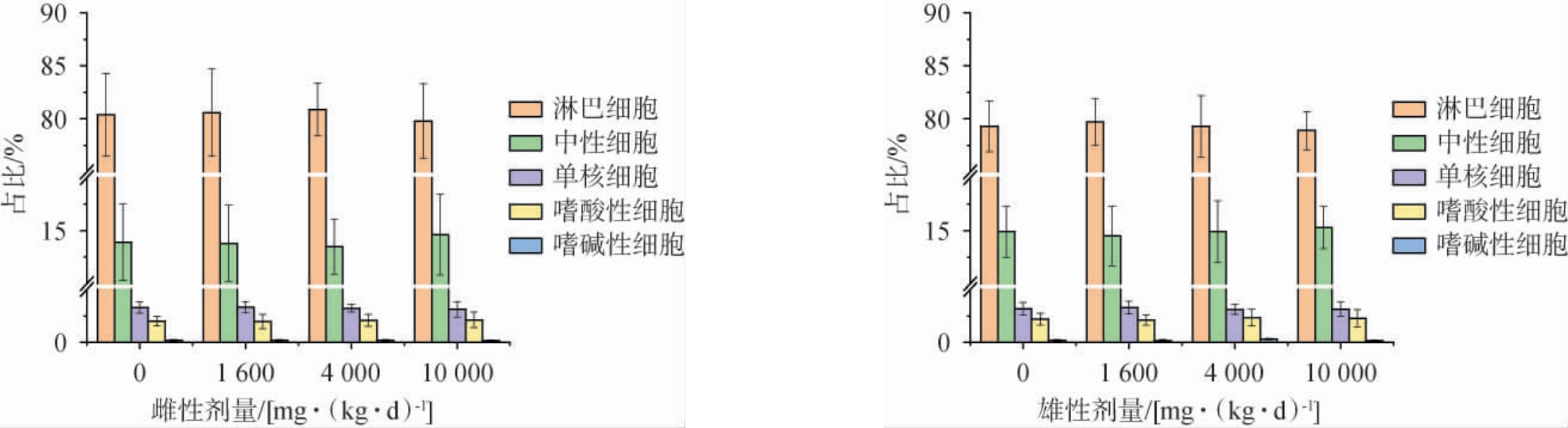
图1 尾穗苋籽粒对大鼠血液中各类白细胞的影响
Fig.1 Effect of Amaranthus caudatus seeds on different types of leukocyte in rat blood
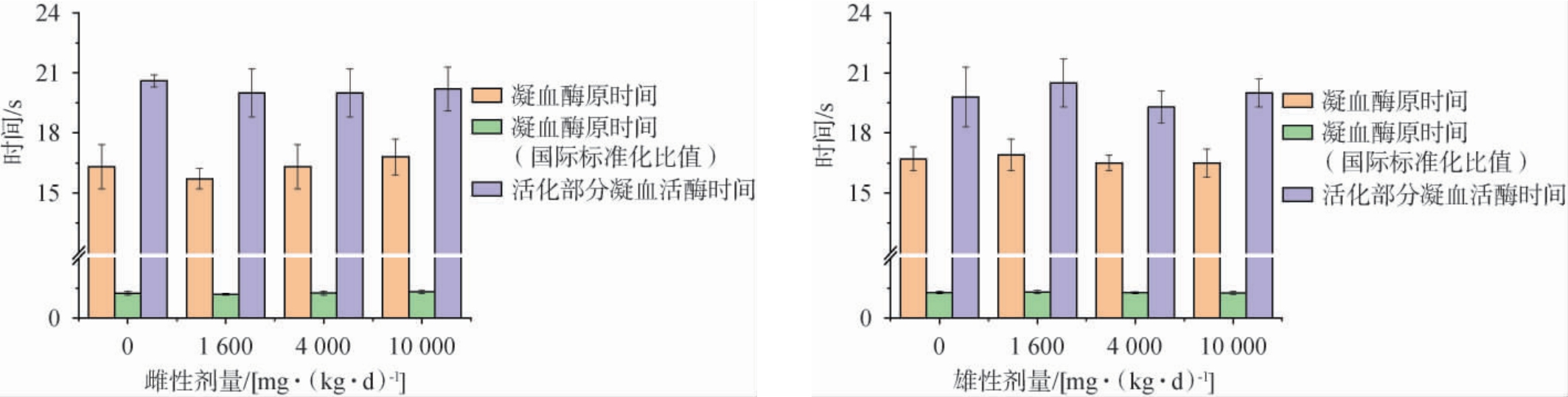
图2 尾穗苋籽粒对大鼠血液凝血时间的影响
Fig.2 Effect of Amaranth caudatus seeds on blood clotting time of rats
表6 尾穗苋籽粒对大鼠血液学指标的影响
Table 6 Effect of Amaranth caudatus seeds on hematological indicators of rats
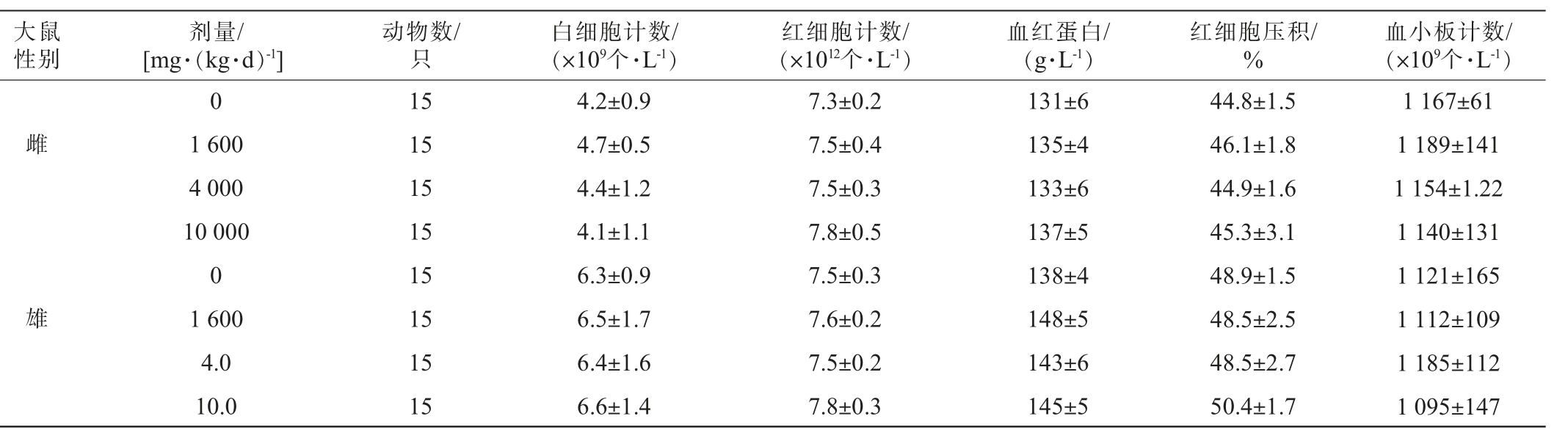
大鼠性别剂量/[mg·(kg·d)-1]动物数/只白细胞计数/(×109个·L-1)红细胞计数/(×1012个·L-1)血红蛋白/(g·L-1)红细胞压积/%0雌雄1 600 4 000 10 000 0 1 600 4.0 10.0 15 15 15 15 15 15 15 15 4.2±0.9 4.7±0.5 4.4±1.2 4.1±1.1 6.3±0.9 6.5±1.7 6.4±1.6 6.6±1.4 7.3±0.2 7.5±0.4 7.5±0.3 7.8±0.5 7.5±0.3 7.6±0.2 7.5±0.2 7.8±0.3 131±6 135±4 133±6 137±5 138±4 148±5 143±6 145±5 44.8±1.5 46.1±1.8 44.9±1.6 45.3±3.1 48.9±1.5 48.5±2.5 48.5±2.7 50.4±1.7血小板计数/(×109个·L-1)1 167±61 1 189±141 1 154±1.22 1 140±131 1 121±165 1 112±109 1 185±112 1 095±147
由表6可知,用单因素方差分析方法中多个试验组与一个空白对照组间均数的两两比较方法进行统计处理。各剂量组的各指标与对照组[0 mg/(kg·d)]比较,均无显著性差异(P>0.05),表明样品对试验大鼠的血液学指标无不利影响。由图1可知,与对照组相比,随着剂量的增加,尾穗苋籽粒未对雌性和雄性大鼠的淋巴、中性、单核、嗜酸性和嗜碱性等细胞产生任何具有生物学意义的毒性影响,与空白对照组相比无显著差异(P>0.05)。 由图2可知,随着剂量的增加,雌性和雄性大鼠各剂量组的凝血酶原时间、国际标准化比值及活化部分凝血活酶时间与空白对照组比较,均无显著性差异(P>0.05),表明受试物在本试验条件下未对大鼠凝血功能产生不良影响。
2.2.3 样品对大鼠血液生化指标的影响
对大鼠连续28 d经口给予不同剂量的尾穗苋籽粒,然后对各剂量组大鼠的血液生化指标进行了测定,结果见表7。 由表7可知,与对照组相比,各个剂量组的大鼠血液生化指标并没有显著变化(P>0.05),数值基本平衡,且所有组别间的差异均不显著(P>0.05)。各剂量组之间的指标也没有显著差异(P>0.05)。这说明在试验所设定的剂量范围内,尾穗苋籽粒对大鼠血液生化指标无不利影响。
表7 尾穗苋籽粒对大鼠血液生化指标的影响
Table 7 Effect of Amaranth caudatus seeds on blood biochemical indexes of rats
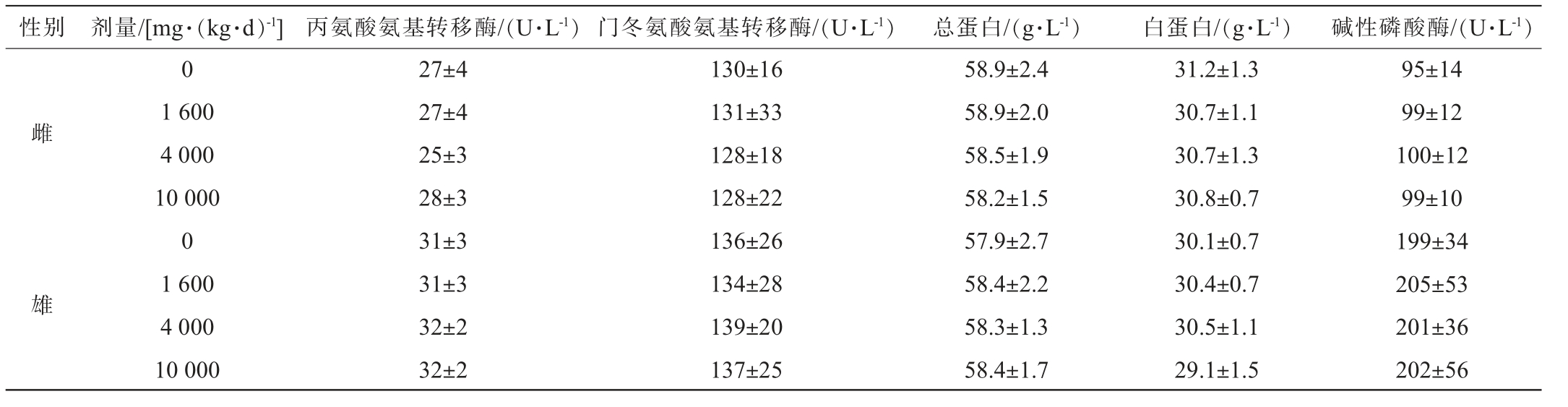
性别 剂量/[mg·(kg·d)-1] 丙氨酸氨基转移酶/(U·L-1) 门冬氨酸氨基转移酶/(U·L-1) 总蛋白/(g·L-1) 白蛋白/(g·L-1) 碱性磷酸酶/(U·L-1)0雌雄1 600 4 000 10 000 0 1 600 4 000 10 000 27±4 27±4 25±3 28±3 31±3 31±3 32±2 32±2 130±16 131±33 128±18 128±22 136±26 134±28 139±20 137±25 58.9±2.4 58.9±2.0 58.5±1.9 58.2±1.5 57.9±2.7 58.4±2.2 58.3±1.3 58.4±1.7 31.2±1.3 30.7±1.1 30.7±1.3 30.8±0.7 30.1±0.7 30.4±0.7 30.5±1.1 29.1±1.5 95±14 99±12 100±12 99±10 199±34 205±53 201±36 202±56
续表
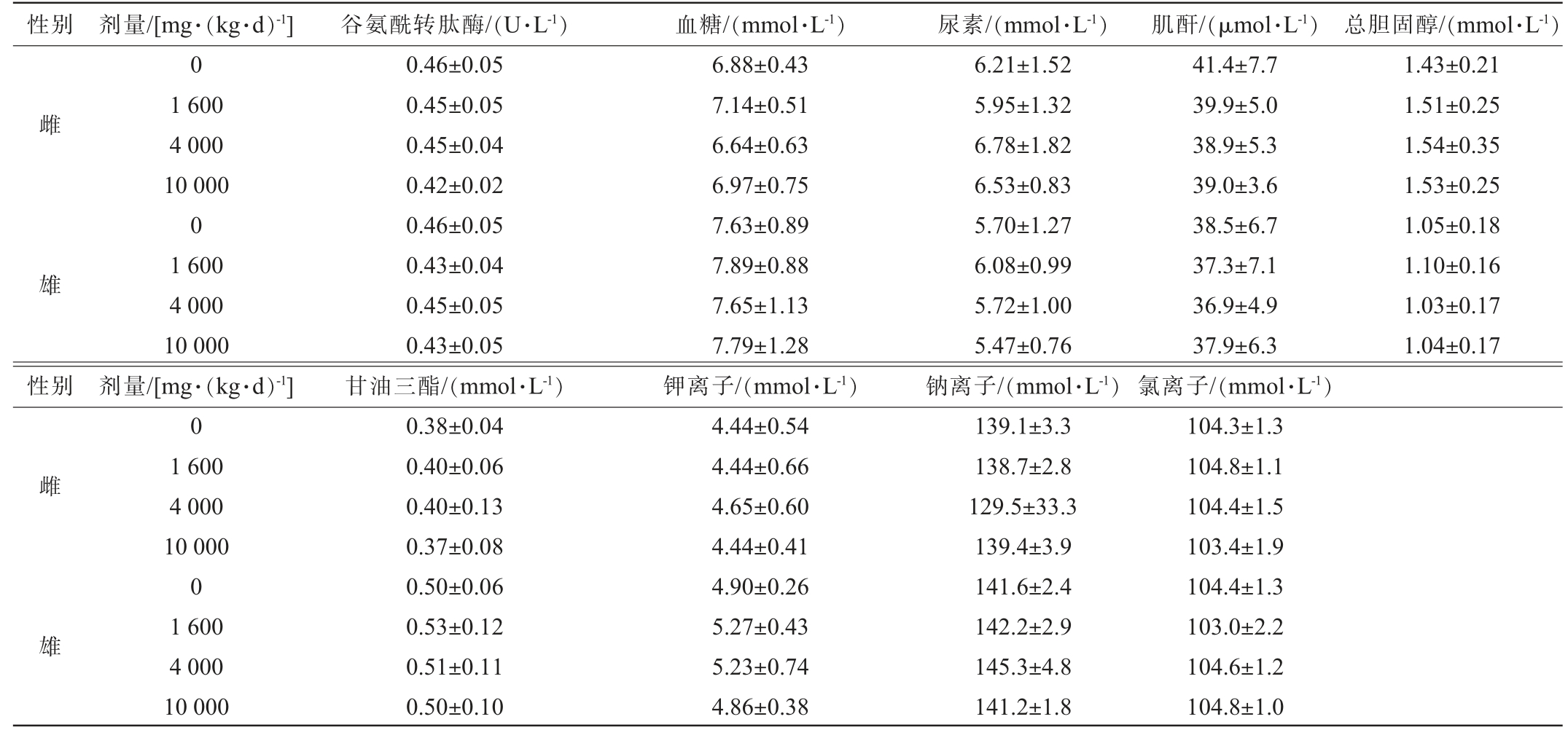
性别雌雄总胆固醇/(mmol·L-1)1.43±0.21 1.51±0.25 1.54±0.35 1.53±0.25 1.05±0.18 1.10±0.16 1.03±0.17 1.04±0.17性别雌雄剂量/[mg·(kg·d)-1]0 1 600 4 000 10 000 0 1 600 4 000 10 000剂量/[mg·(kg·d)-1]0 1 600 4 000 10 000 0 1 600 4 000 10 000谷氨酰转肽酶/(U·L-1)0.46±0.05 0.45±0.05 0.45±0.04 0.42±0.02 0.46±0.05 0.43±0.04 0.45±0.05 0.43±0.05甘油三酯/(mmol·L-1)0.38±0.04 0.40±0.06 0.40±0.13 0.37±0.08 0.50±0.06 0.53±0.12 0.51±0.11 0.50±0.10血糖/(mmol·L-1)6.88±0.43 7.14±0.51 6.64±0.63 6.97±0.75 7.63±0.89 7.89±0.88 7.65±1.13 7.79±1.28钾离子/(mmol·L-1)4.44±0.54 4.44±0.66 4.65±0.60 4.44±0.41 4.90±0.26 5.27±0.43 5.23±0.74 4.86±0.38尿素/(mmol·L-1)6.21±1.52 5.95±1.32 6.78±1.82 6.53±0.83 5.70±1.27 6.08±0.99 5.72±1.00 5.47±0.76钠离子/(mmol·L-1)139.1±3.3 138.7±2.8 129.5±33.3 139.4±3.9 141.6±2.4 142.2±2.9 145.3±4.8 141.2±1.8肌酐/(μmol·L-1)41.4±7.7 39.9±5.0 38.9±5.3 39.0±3.6 38.5±6.7 37.3±7.1 36.9±4.9 37.9±6.3氯离子/(mmol·L-1)104.3±1.3 104.8±1.1 104.4±1.5 103.4±1.9 104.4±1.3 103.0±2.2 104.6±1.2 104.8±1.0
2.2.4 样品对大鼠脏器系数的影响
28 d经口毒性试验探究不同剂量尾穗苋籽粒对大鼠心、胸腺、肝、肾、肾上腺、脾、睾丸、卵巢的绝对质量及脏器系数(脏器质量占体质量百分比)的影响,结果见表8。
表8 尾穗苋籽粒对大鼠脏器质量与脏器系数的影响
Table 8 Effects of Amaranth caudatus seeds on organ weight and organ coefficient of rats

性别 剂量/[mg·(kg·d)-1] 停食后体质量/g 心脏质量/g 心脏系数/% 胸腺质量/g 胸腺系数/% 肝脏质量/g 肝脏系数/%雌雄性别雌雄性别雌雄0 1 600 4 000 10 000 0 1 600 4 000 10 000剂量/[mg·(kg·d)-1]0 1 600 4 000 10 000 0 1 600 4 000 10 000剂量/[mg·(kg·d)-1]0 1 600 4 000 10 000 0 1 600 4 000 10 000 270.2±9.2 268.9±9.9 264.4±10.9 272.8±4.5 404.7±12.9 408.4±12.0 410.0±20.3 413.4±20.7停食后体质量/g 270.2±9.2 268.9±9.9 264.4±10.9 272.8±4.5 404.7±12.9 408.4±12.0 410.0±20.3 413.4±20.7停食后体质量/g 270.2±9.2 268.9±9.9 264.4±10.9 272.8±4.5 404.7±12.9 408.4±12.0 410.0±20.3 413.4±20.7 1.44±0.10 1.50±0.17 1.42±0.06 1.38±0.10 1.87±0.13 1.89±0.15 1.79±0.14 1.86±0.13肾脏质量/g 2.41±0.10 2.64±0.09 2.47±0.20 2.38±0.05 3.28±0.11 3.34±0.08 3.30±0.21 3.09±0.21睾丸质量/g// / /3.45±0.21 3.70±0.15 3.68±0.11 3.86±0.14 0.53±0.06 0.55±0.08 0.53±0.04 0.51±0.05 0.46±0.04 0.46±0.07 0.44±0.08 0.45±0.04肾脏系数/%0.89±0.05 0.98±0.05 0.93±0.08 0.86±0.03 0.81±0.04 0.82±0.04 0.80±0.12 0.75±0.03睾丸系数/%// / /0.852±0.101 0.904±0.056 0.910±0.072 0.934±0.115 0.91±0.09 0.95±0.10 0.89±0.07 0.99±0.06 0.88±0.07 0.98±0.08 0.84±0.13 0.91±0.10肾上腺质量/g 0.108±0.008 0.102±0.004 0.105±0.011 0.101±0.004 0.084±0.004 0.087±0.008 0.084±0.009 0.091±0.009卵巢质量/g 0.19±0.03 0.22±0.03 0.21±0.02 0.19±0.03// / /0.34±0.04 0.35±0.05 0.34±0.03 0.36±0.05 0.22±0.03 0.24±0.03 0.20±0.05 0.22±0.03肾上腺系数/%0.040±0.004 0.037±0.004 0.040±0.007 0.037±0.003 0.021±0.003 0.021±0.004 0.012±0.003 0.022±0.004卵巢系数/%0.070±0.022 0.081±0.015 0.079±0.015 0.069±0.013// / /9.75±0.49 9.55±0.52 9.48±0.64 9.19±0.41 13.54±0.45 13.79±0.70 14.05±1.05 14.21±1.09脾脏质量/g 0.60±0.08 0.71±0.06 0.74±0.06 0.71±0.04 1.09±0.08 1.14±0.09 1.11±0.10 1.02±0.13 3.61±0.25 3.55±0.28 3.56±0.29 3.37±0.23 3.35±0.16 3.38±0.24 3.43±0.54 3.34±0.22脾脏系数/%0.22±0.06 0.26±0.03 0.28±0.03 0.26±0.03 0.27±0.03 0.28±0.05 0.27±0.05 0.25±0.04
由表8可知,大鼠体质量未出现异常变化;肝脏、肾脏、脾脏和睾丸的质量亦无异常,且所有脏器系数均与对照组相比无显著差异(P>0.05)。进一步对心、胸腺、肝、肾、肾上腺、脾以及雄性大鼠睾丸、雌性大鼠卵巢的质量及脏器系数指标分析发现,各籽粒苋剂量组与空白对照组之间,均未呈现具有规律性的、显著的剂量相关性差异,组间差异在统计学上无显著性(P>0.05)。 综上,在本试验条件下,所设置剂量的籽粒苋对大鼠心、胸腺、肝、肾、肾上腺、脾、睾丸、卵巢的质量和脏器系数无显著影响(P>0.05)。
2.3 小鼠红细胞微核试验
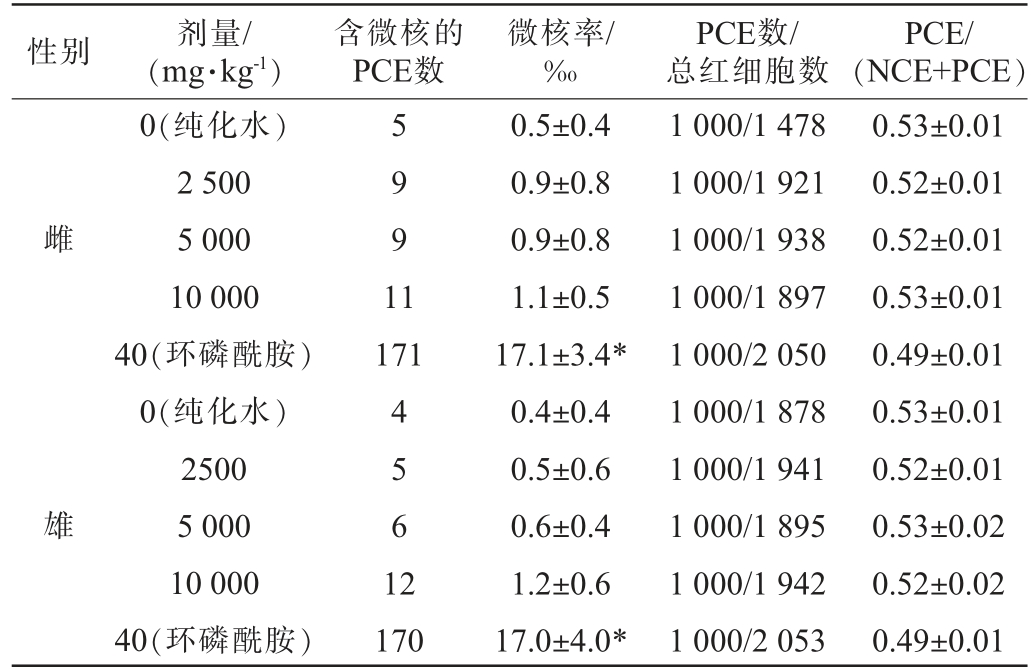
微核率的大小与作用因子的剂量或辐射累积效应呈正相关,这一点与染色体畸变的情况一样。 微核率越高,表明受试样品对小鼠骨髓细胞增殖的抑制作用越明显。PCE/NCE比值越高,也表明受试样品对小鼠骨髓细胞增殖的抑制作用越明显。尾穗苋籽粒对小鼠骨髓细胞微核发生率和嗜多染红细胞与总红细胞比值的影响见表9。
表9 尾穗苋籽粒对小鼠骨髓细胞微核发生率和嗜多染红细胞与总红细胞比值的影响
Table 9 Effects of Amaranth caudatus seeds on the incidence of micronucleus in mouse bone marrow cells and the ratio of polychromatic erythrocytes to total erythrocytes
注:“*”表示与阴性对照组比较,差异显著(P<0.05)。
性别 剂量/(mg·kg-1)含微核的PCE数微核率/‰PCE数/总红细胞数PCE/(NCE+PCE)雌0.53±0.01 0.52±0.01 0.52±0.01 0.53±0.01 0.49±0.01 0.53±0.01 0.52±0.01 0.53±0.02 0.52±0.02 0.49±0.01 0(纯化水)2 500 5 000 10 000 40(环磷酰胺)0(纯化水)2500 5 000 10 000 40(环磷酰胺)5 991 1 171雄4561 2 170 0.5±0.4 0.9±0.8 0.9±0.8 1.1±0.5 17.1±3.4*0.4±0.4 0.5±0.6 0.6±0.4 1.2±0.6 17.0±4.0*1 000/1 478 1 000/1 921 1 000/1 938 1 000/1 897 1 000/2 050 1 000/1 878 1 000/1 941 1 000/1 895 1 000/1 942 1 000/2 053
由表9可知,在各剂量水平下,受试样本引发的小鼠骨髓嗜多染红细胞微核频率与阴性对照组无明显差异(P>0.05),受试物质并未引起显著的微核生成增多。反之,阳性对照组的微核比率远超阴性对照组(P<0.05),有力证实了试验程序的可靠性和有效性。 受试样品各剂量组的嗜多染红细胞(PCE)与总红细胞(PCE+NCE)的比值(PCE/PCE+NCE)与对照组的差异均不超过对照组的20%,表明受试样品对小鼠骨髓细胞增殖没有明显抑制作用。
综合微核率和PCE/(PCE+NCE)的结果,未观察到尾穗苋籽粒对小鼠骨髓嗜多染红细胞微核形成有任何促进作用,同时对嗜多染红细胞与总红细胞比值也未产生显著影响(P>0.05)。 基于这些数据,可以得出结论:尾穗苋籽粒在小鼠红细胞微核试验中表现为阴性结果,即在本次试验条件下,尾穗苋籽粒对小鼠骨髓遗传物质稳定性及红细胞增殖未显示出潜在的遗传毒性或细胞毒性。
3 结论
本研究经过急性经口毒性试验、28 d经口毒性试验及小鼠红细胞微核试验得知,急性经口毒性试验LD50>10 000 mg/kg,按急性毒性剂量分级标准尾穗苋属实际无毒无害。以不同剂量给予大鼠灌胃28 d,受试动物体质量,血常规、脏器系数等各项指标与对照组无显著差异(P>0.05),这说明在试验所设定的剂量范围内,尾穗苋籽粒对大鼠无不利影响。 小鼠红细胞微核试验得知,尾穗苋籽粒试验结果为阴性。综上所述,尾穗苋属实际无毒物,为尾穗苋籽粒作为食品原料的发展提供科学依据,推动其在食品行业的进一步开发和广泛应用。
[1]王秋实.中国苋属植物的经典分类学研究及其入侵风险评估[D].上海:华东师范大学,2015.
[2]于淑玲.药食保健野菜——苋菜的开发利用[J].资源开发与市场,2010,26(2):141-142.
[3]曾庆鸿,冯霞,杨巍,等.苋菜高效栽培技术要点[J].农技服务,2022,39(10):11-14.
[4]王保瑞,楚晓真,刘格,等.河南地区苋菜高产栽培技术要点[J].长江蔬菜,2022(5):34-35.
[5]薛丽芝.尾穗苋籽粒在食品工业中的研究进展及前景[J].食品工业,2016,37(5):257-260.
[6]阿如汗,禄炳云,许云,等.籽粒苋的营养价值及其在酒行业中的研究进展[J].酿酒,2024,51(1):5-11.
[7]聂婷婷,李芳,祝振洲,等.尾穗苋籽粒的应用研究进展[J].安徽农业科学,2016,44(4):8-10,31.
[8]廖石榴.苋菜水提取物的抑菌活性及抑菌蛋白的研究[D].长沙:湖南农业大学,2018.
[9]NOGOY K M C,YU J,SONG Y G,et al.Evaluation of the nutrient composition,in vitro fermentation characteristics,and in situ degradability of Amaranthus caudatus,Amaranthus cruentus,and Amaranthus hypochondriacus in cattle[J].Animals,2021,11(18):1-13.
[10]蔡红燕,聂婷婷,党长英,等.籽粒苋淀粉理化性质研究[J].粮食与油脂,2019,32(10):64-66.
[11]JENNY M,JONATHAN S P,BJÖRN B,et al.Nutritional composition of six amaranth (Amaranthus caudatus) Andean varieties[J].Crops, 2023,3(1):78-87.
[12]KARAMAC′ M, GAI F, LONGATO E, et al.Antioxidant activity and phenolic composition of Amaranth(Amaranthus caudatus)during plant growth[J].Antioxidants,2019,8(6):173.
[13]YAO H L,LI H H.Extraction and purification process optimization and antioxidant activity in vitro of flavonoids in Amaranthus caudatus L.[J].Med Plant,2020,11(4):48-53.
[14]BANG H J, JO H I, SEBASTIN R, et al.Comparative analysis of polyphenolic compounds in different Amaranthus species: Influence of genotypes and harvesting year[J].Antioxidants (Basel, Switzerland),2024,13(4):501.
[15]RORIZ C L,XAVIER V,HELENO S A,et al.Chemical and bioactive features of Amaranthus caudatus L.flowers and optimized ultrasound assisted extraction of betalains[J].Foods,2021,10(4):779.
[16]KUMAR A S B,LAKSHMAN K,KUMAR A A P,et al.Protective effect of methanol extract of amaranth spike on liver injury induced by paracetamol in rats[J].J Integr Med,2011,9(2):194-200.
[17]JUNHYOUNG B, JUN K L, TEA W J, et al.Antioxidant activity and phytochemical content of nine Amaranthus species[J].Agronomy,2021,11(6):1032.
[18]刘贤贤,覃丽清,经孝腾,等.尾穗苋化学成分及其抗氧化活性[J].中成药,2023,45(6):1870-1876.
[19]刘贤贤,覃丽清,张业,等.尾穗苋体外细胞毒活性成分的研究[J].食品与药品,2023,25(2):103-109.
[20]NOGOY K M C, YU J, SONG Y G, et al.Evaluation of the nutrient composition, in vitro fermentation characteristics, and in situ degradability of Amaranthus caudatus,Amaranthus cruentus,and Amaranthus hypochondriacus in cattle[J].Animals,2021,11(18):1-13.
[21]肖荣飞,陈旭峰,郭娅,等.尾穗苋粒发酵小曲清香型白酒的研究[J].中国酿造,2018,37(7):127-131.
[22]陈曦.苋粒酱香型白酒发酵工艺研究[D].贵阳:贵州大学,2023.
[23]聂婷婷,李芳,祝振洲,等.籽粒苋的应用研究进展[J].安徽农业科学,2016,44(4):8-10,31.
[24]廖芙蓉.籽粒苋淀粉和色素的提取及其性质研究[D].重庆:西南大学,2012.
[25]杨东湘.论微量元素对人体健康的重要作用[J].科协论坛(下半月),2010(6):103-104.
[26]程金芝.粮、饲、菜兼用作物-籽粒苋在吉林省的发展与展望[J].白城师范学院学报,2008(3):32-35.
[27]陈飞平,周家华,曾凡坤.苋籽ACE抑制肽的大孔树脂分离纯化[J].食品工业科技,2013,34(11):271-276.
[28]BERGER A,MONNARD I,DIONISI F,et al.Cholesterol-lowering properties of amaranth flakes, crude and refined oils in hamsters[J].Food Chem,2003,81(1):119-124.
[29]李淑琴,边林秀,李学敏,等.辣木果急性毒性及亚慢性毒性研究[J].毒理学杂志,2024,38(6):455-460.
[30]王明秋,赵云财,孟琳,等.草苁蓉急性经口毒性和遗传毒性研究[J].酿酒,2024,51(5):131-134,140.