浓香型白酒是四大基本香型之一,具有芳香浓郁、绵柔甘洌、香味协调、入口甜、落口绵等特点[1]。在浓香型白酒中乙醇和水占总质量的98%,微量成分占2%,而这些微量成分的种类和含量比例是决定浓香型白酒风格和质量的重要影响因素,酯类物质是浓香型白酒的主要微量成分,其中己酸乙酯含量占总酯的40%左右,是浓香白酒中主要酯类成分,其次为乙酸乙酯、乳酸乙酯、和丁酸乙酯[2-3]。
大曲作为白酒酿造过程中重要的糖化发酵剂,其中微生物种类和数量决定着白酒酒质、酒率和风味成分,是评价传统大曲品质的重要指标[4]。大曲中的微生物主要来源于自然环境的富集,功能菌的利用对于改善传统大曲的品质具有深远影响。酵母菌是一类重要的白酒酿造微生物,具有产酯、产醇和生香的作用,在大曲中主要包含的酵母种类有酵母属(Saccharomyces)、汉逊酵母属(Hansenula)、假丝 酵 母 属(Candida)、毕 赤 酵 母 属(Pichia)、红 酵 母 属(Rhodotorula)、接合酵母属(Zygosaccharomyces)等[5-7]。 酿酒酵母(Saccharomyces cerevisiae)有较强的产乙醇能力,在一程度上决定着白酒的产量[4]。边名鸿等[8]以产酒能力为主要指标,筛选出一株具有优良产酒酵母,经鉴定为酿酒酵母。 而产香酵母是大曲中香味成分物质的主要来源,在酯酶的作用下合成酯类物质, 影响着白酒中香气成分[9]。李秋晓等[10]从清香型白酒大曲中筛选出一株高产乙酸乙酯的异常威克汉姆酵母(Wickerhamomyces anomalus),并发现其具有良好的乙醇、乙酸、温度和糖耐受能力,能较好的适应白酒酿造环境,为实际生产过程中提供了优质的菌种资源和理论保障。 余伟民等[11]在酒醅中添加产酯酵母,发现酒体中总酯、四大乙酯类物质等呈味成分含量均有较大幅度的增加,说明在发酵体系中加入产酯酵母可在保持酿制白酒酒体风格的同时,增加酒体的醇厚感,提高原酒酒质。因此,筛选出发酵性能及产香性能优良的酵母是大曲发酵的关键。
本研究以浓香型大曲为研究对象,利用传统培养分离方法对大曲中的酵母菌进行分离纯化,通过发酵性能测试、耐受性实验及风味代谢能力分析筛选高耐受性的产香优良酵母菌株,并利用分子生物学技术对其进行菌种鉴定,为提升白酒风味品质、保障发酵稳定性、推动酿造工艺现代化提供核心菌种与科学依据。
1 材料与方法
1.1 材料与试剂
1.1.1 样品与试剂
浓香型大曲:劲牌南溪酒业(宜宾)有限公司;糖化酶(酶活≥100 000 U/g)、淀粉酶(酶活≥3 700 U/g)、无水乙醇(分析纯)、葡萄糖(分析纯)、蛋白胨、琼脂粉(均为生化试剂):国药集团化学试剂有限公司;酵母浸粉(生化试剂):维百奥(北京)生物科技有限公司;真菌基因组脱氧核糖核酸(deoxyribonucleic acid,DNA)提取试剂盒:天根生化科技(北京)有限公司;TS-GelRed核酸琼脂染料Ver.2、1.1×T3 Super聚合酶链式反应(polymerase chain reaction,PCR)Mix:北京擎科生物科技股份有限公司;其他试剂均为国产分析纯或色谱纯。
1.1.2 培养基
酵母浸出粉胨葡萄糖(yeast extract peptone dextrose,YPD)固体培养基[12]:1%酵母膏,2%蛋白胨,2%葡萄糖,2%琼脂粉。121 ℃条件下高压蒸汽灭菌20 min。灭菌后加入0.2%乙酸、0.03%氯霉素(200 mg/L)。
YPD液体培养基:YPD固体培养基中不添加琼脂。
高粱水解液培养基[3]:取250 g高粱并粉碎,以质量比1∶4加入1 L蒸馏水,加热煮沸使其糊化。待温度冷却至40 ℃左右,加入0.3%(按高粱质量计)的淀粉酶液化1 h,液化后补加250 mL温水(60 ℃)。 搅拌均匀后加入5%(按高粱质量计)的糖化酶,在60 ℃条件下糖化,用稀碘液试之不显蓝色为止。采用细纱布过滤后,调整糖度为7°Brix后分装。121 ℃条件下高压蒸汽灭菌20 min。
1.2 仪器与设备
UV-8000分光光度计:上海元析仪器有限公司;TGL-16B离心机:上海安亭科学仪器厂;WSI-50可叠加振荡培养箱:维根技术(北京)有限公司;WSI-50 PCR仪:莫纳(武汉)生物科技有限公司;EPS300凝胶电泳仪、2500B全自动凝胶成像分析仪:上海天能科技有限公司;BXP-280S微生物培养箱:上海博讯医疗生物仪器股份有限公司;AS2-6S1 Esco生物安全柜:新加坡艺思高科技有限公司;8890气相色谱(gas chromatography,GC)仪、1260高效液相色谱(high performance liquid chromatography,HPLC)仪:安捷伦科技(中国)有限公司。
1.3 方法
1.3.1 浓香型大曲中酵母菌的分离纯化
称取10 g粉碎过筛后的大曲,加入90 mL的0.9%生理盐水中,于30 ℃、120 r/min条件下振荡30 min,并按10倍梯度逐级稀释至10-4。 分别吸取稀释度为10-2、10-3、10-4的稀释液100 μL涂布于YPD固体培养基上,于30 ℃条件下培养48 h。挑取生长较好、菌落形态不一的单菌落进行多次划线分离,得到纯菌落。
1.3.2 产气能力分析
将分离纯化后的酵母菌株接种至YPD液体培养基中,30 ℃、180 r/min条件下培养48 h,调整各菌株发酵液中的活菌数为107 CFU/mL作为种子液。 将种子液以5%(V/V)的接种量接种至带有杜氏小管的10 mL试管中,加入1 mL YPD液体培养基,30 ℃条件下静置培养24 h。每隔2 h观察杜氏小管内气体的含量,并记录。淘汰产气少或不产气的菌株,筛选发酵快、产气多的菌株进行复筛。
1.3.3 耐受性试验
分别将酵母菌种子液以2%(V/V)的接种量接种至含不同乙醇体积分数(3%、5%、7%、9%、11%、13%、15%)、pH值(1.0、2.0、3.0、4.0、5.0、6.0、7.0)的YPD液体培养基中,于30℃、180 r/min条件下培养48 h后,于波长600 nm处测定培养液的吸光度值(OD600 nm值),考察菌株对乙醇和pH的耐受性;分别将酵母菌种子液以2%(V/V)的接种量接种至YPD液体培养基中,于不同温度(35 ℃、40 ℃、45 ℃、50 ℃、55 ℃、60 ℃)及180 r/min条件下培养48 h后,于波长600 nm处测定培养液的吸光度值(OD600nm值),考察菌株对温度的耐受性。
1.3.4 风味物质的检测
以未接种的高粱水解液培养基为空白对照(Control),将酵母菌种子液按10%(V/V) 的接种量分别接种于高粱水解液培养基,在30 ℃、180 r/min条件下培养72 h。 发酵结束后,发酵液经10 000 r/min、4 ℃离心后,取上清液,备用。
有机酸含量的测定:采用HPLC测定有机酸含量[13]。HPLC条件:Diamonsil ODS色谱柱(4.6 mm×250 mm,5 μm),流动相为pH为2.3的0.02 mol/L磷酸二氢钾-乙腈(98∶2,V/V),等度洗脱,流速为0.5 mL/min,紫外检测波长为210 nm,柱温30 ℃,进样量10.0 μL。 定性定量方法:根据保留时间进行定性,采用外标法进行定量。
挥发性风味物质的测定:采用GC仪对异丁醇、异戊醇、已酸乙酯和乙酸乙酯4种重要挥发性风味物质进行检测[14]。
GC条件:DB-WAX毛细管色谱柱(30 m×0.25 mm×0.25 μm),进样口温度250 ℃,分流比为37∶1,采用程序升温(初始温度50 ℃,保留2 min,以10 ℃/min的速率升至180 ℃,保留2 min,再以6 ℃/min的速率升至230 ℃,保留2 min);检测器温度为250℃,载气为高纯氦气(He),流速为1mL/min。
MS条件:电子电离(electron ionization,EI)源,电子能量为70 eV,扫描范围为50~350 amu,离子源温度和接口温度均为250 ℃。
定性定量方法:根据标准物质的保留时间进行定性,采用外标法进行定量。
1.3.5 分子生物学鉴定
使用真菌基因组DNA提取试剂盒提取酵母菌基因组DNA,以其为模板,采用26S rDNA通用引物NL1(5'-GCATATCAATAAGCGGAGGAAAAG-3')和NL4(5'-GGTCCGTGTTTCAAGACGG-3')PCR 扩 增 酵 母 菌 的26S rDNA D1/D2区基因序列。PCR扩增体系:1 μL DNA样品,1 μL引物NL1(20 μmol/L),1 μL引物NL4(20 μmol/L),4 μL脱氧核糖核苷三磷酸(deoxynucleotide triphosphates,dNTPs),4.5 μL 10×Taq反应缓冲液、0.5 μL Taq聚合酶(5 U/μL)和37.5 μL双蒸水(ddH2O)。PCR扩增程序:95 ℃预变性3 min;95 ℃变性45 s,55 ℃退火45 s,72 ℃延伸45 s,共进行30个循环;72 ℃再延伸10 min。PCR扩增产物经1%琼脂糖凝胶电泳检测合格后,委托北京擎科生物科技股份有限公司进行测序。将测序结果提交至美国国家生物信息中心(national center for biotechnology information,NCBI)的GenBank数据库中,采用基本局部比对搜索工具(basic local alignment search tool,BLAST)进行同源性比对,选取同源性较高的模式菌株的26S rDNA D1/D2区基因序列,使用MEGA X软件中的邻接(neighbor-joining,NJ)法构建系统发育树,以确定菌种分类属性。
1.3.6 数据处理
每个实验重复3次,采用SPSS22.0软件处理和分析数据,结果以“平均值±标准差”表示;采用Graphpad Prism作图。
2 结果与分析
2.1 浓香型大曲中酵母菌株的分离纯化
采用传统培养分离法从浓香型大曲中共分离纯化得到10株不同形态的酵母菌株,编号为JM-1~JM-10,其菌落形态特征见图1,形态特征描述见表1。
表1 分离酵母菌株的菌落形态特征描述
Table 1 Description of colony morphological characteristics of isolated yeast strains
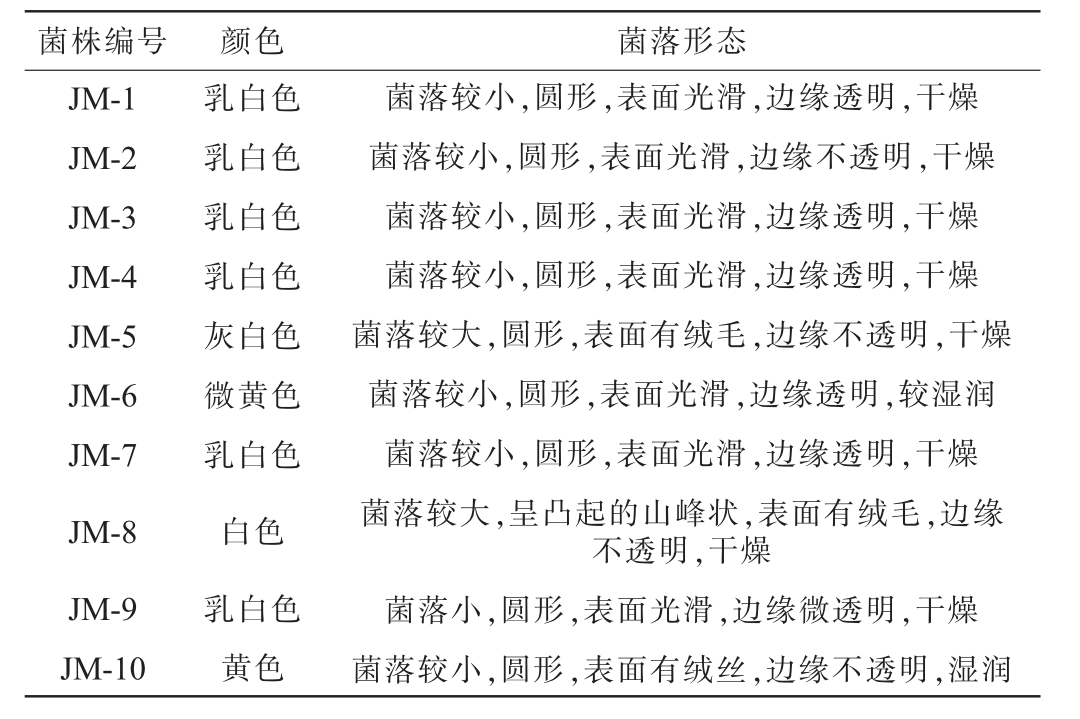
菌株编号 颜色 菌落形态JM-1 JM-2 JM-3 JM-4 JM-5 JM-6 JM-7 JM-8 JM-9 JM-10乳白色乳白色乳白色乳白色灰白色微黄色乳白色白色乳白色黄色菌落较小,圆形,表面光滑,边缘透明,干燥菌落较小,圆形,表面光滑,边缘不透明,干燥菌落较小,圆形,表面光滑,边缘透明,干燥菌落较小,圆形,表面光滑,边缘透明,干燥菌落较大,圆形,表面有绒毛,边缘不透明,干燥菌落较小,圆形,表面光滑,边缘透明,较湿润菌落较小,圆形,表面光滑,边缘透明,干燥菌落较大,呈凸起的山峰状,表面有绒毛,边缘不透明,干燥菌落小,圆形,表面光滑,边缘微透明,干燥菌落较小,圆形,表面有绒丝,边缘不透明,湿润

图1 分离酵母菌株的菌落形态特征
Fig.1 Colony morphological characteristics of isolated yeast strains
由图1及表1可知,菌株JM-6的菌落呈微黄色,菌株JM-10的菌落呈黄色,菌株JM-8的菌落呈白色,其他菌株的菌落呈乳白色;所有菌株的菌落均呈圆形;除菌株JM-2、JM-5、JM-8和JM-10的菌落边缘不透明外,其他菌株的菌落边缘透明;除菌株JM-6和菌株JM-10菌落表面湿润外,其他菌株的菌落表面均干燥;菌株JM-5、JM-8和JM-10的菌落具有绒毛、呈放射状,其他酵母菌的菌落表面光滑,部分中间凸起。
2.2 分离酵母菌的产气能力分析
为了筛选发酵性能较好的酵母菌株,对10株分离酵母菌株进行产气实验,结果见表2。由表2可知,菌株JM-6在培养24 h后未产气;菌株JM-5、JM-8、JM-10产气时间较晚,能力较弱;菌株JM-1、JM-2、JM-3、JM-4、JM-7、JM-9培养24 h后能产满管气,产气性能较好,因此,初步筛选这6株酵母菌株为发酵性能较好的菌株。
表2 分离酵母菌的产气试验结果
Table 2 Results of gas production of isolated yeast strains
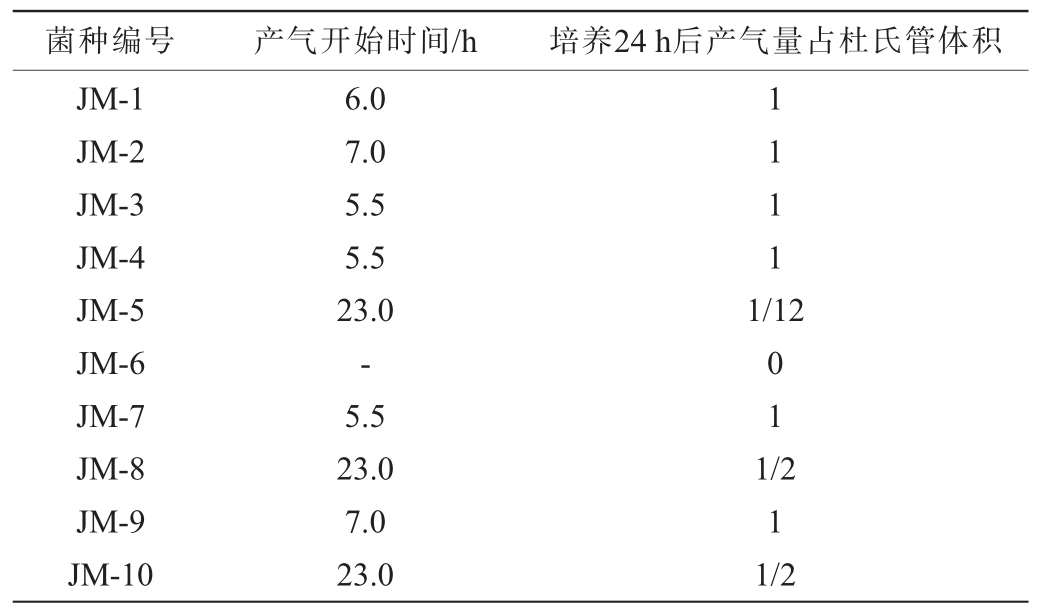
注:“-”表示未产气。
菌种编号 产气开始时间/h 培养24 h后产气量占杜氏管体积JM-1 JM-2 JM-3 JM-4 JM-5 JM-6 JM-7 JM-8 JM-9 JM-10 6.0 7.0 5.5 5.5 23.0-5.5 23.0 7.0 23.0 1111 1/12 01 1/2 1 1/2
2.3 初筛酵母菌株的耐受性分析
2.3.1 乙醇耐受性分析
在白酒酿造过程中,酒精度是影响酵母生长的重要因素,高体积分数的乙醇会干扰酵母细胞膜转运蛋白的结构和功能,导致细胞膜稳定性下降和通透性增加,从而抑制酵母的生长[9]。因此,考察6株初筛酵母菌株对乙醇的耐受性,结果见图2。由图2可知,在乙醇体积分数≥11%时,6株菌株生长均受到强烈抑制,但是仍能够微弱生长。其中,菌株JM-9的乙醇耐受力较弱,在乙醇体积分数为5%时,生长受到严重抑制;其余大部分酵母菌株在乙醇体积分数为3%~7%的范围内均能良好的生长,表现出较好的乙醇耐受能力。其中,菌株JM-4和JM-7的耐乙醇能力尤为突出,能够在乙醇体积分数高达9%的环境中良好的生长,说明这两株菌均对乙醇耐受能力最好。
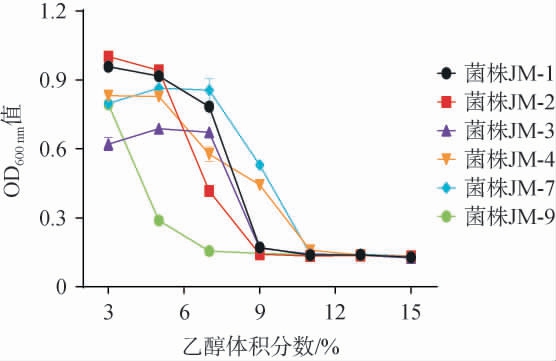
图2 6株酵母菌株的乙醇耐受性试验结果
Fig.2 Results of ethanol tolerance in 6 yeast strains
2.3.2 酸耐受性分析
在白酒传统固态发酵过程中,窖池内因乳酸菌、醋酸菌等产酸菌的代谢活动,常形成动态变化的酸性环境[15-16],此时酵母菌需通过质子泵维持胞内pH稳态,以抵抗酸胁迫引发的多重生理损伤——包括质子跨膜梯度紊乱导致的营养物质吸收抑制、胞内酶(如糖酵解关键酶)活性降低,以及细胞膜脂质过氧化引发的膜流动性改变[17]。耐酸菌株通过增强膜完整性、优化离子转运系统及激活应激蛋白等机制,可有效维持乙醇脱氢酶、酯合成酶等风味物质生成相关酶系的活性[18-20]。在白酒酿造中,高耐酸菌株不仅能保障发酵期产香代谢的持续性,更可通过竞争性抑制杂菌的过度增殖,维持发酵体系微生物群落的功能平衡,这对提升酒醅发酵稳定性以及形成特征性风味物质具有双重调控价值。因此,深入解析酵母耐酸机制并筛选优良菌种,是构建可控发酵体系、实现白酒风味定向调控的重要技术支撑。 6株初筛酵母菌株对酸的耐受性见图3。 由图3可知,当pH在3~7范围内,6株酵母菌株均能正常生长,但当pH<3时,6株酵母菌株的生长均受到不同程度的抑制。当pH为2时,仅有菌株JM-1、JM-2、JM-3、JM-4能生长,pH<2,所有菌株都不能生长,说明菌株JM-1、JM-2、JM-3、JM-4展现出较好的酸胁迫适应性。值得注意的是,在浓香型白酒酿造过程中,糟醅入窖时的酸度通常可达到2.0左右[21],菌株JM-1、JM-2、JM-3、JM-4的耐酸性有助于保证稳定发酵过程,在浓香型白酒酿造中具有较好的适用性。
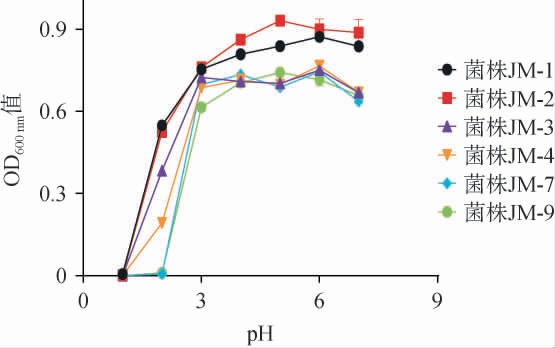
图3 6株酵母菌株的酸耐受性试验结果
Fig.3 Results of acid tolerance in 6 yeast strains
2.3.3 温度耐受性分析
在白酒传统固态发酵过程中,窖池内温度常呈现动态变化,酵母菌的温度耐受性直接决定其生存能力和发酵效能[22]。耐高温菌株不仅能维持淀粉酶、酯化酶等关键酶系的活性[23],还可通过增强抗氧化系统有效清除活性氧簇(reactive oxygen species,ROS),从而保障发酵体系中有益代谢产物(如乙醇、酯类、芳香化合物)的稳定生成[24-25]。 因此,选育具有高温适应性的优良酵母菌种,不仅能提升白酒出酒率,更能通过维持微生物群落稳态来保证酒体风味物质的结构平衡。温度对酵母细胞代谢活动具有双重调控作用:一方面通过影响酶促反应速率直接影响发酵进程,另一方面高温胁迫会引发ROS过量累积,导致蛋白质变性、DNA损伤及脂质过氧化等细胞毒性效应[18]。6株酵母菌株的温度耐受性试验结果见图4。
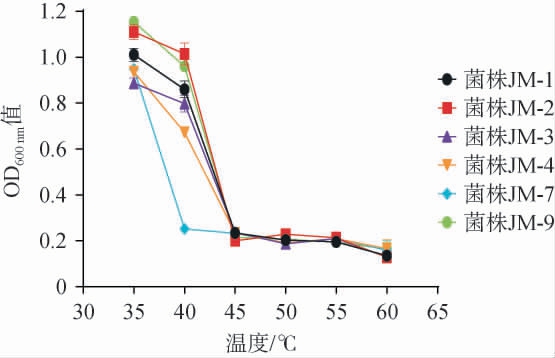
图4 6株酵母菌株的温度耐受性试验结果
Fig.4 Results of temperature tolerance in 6 yeast strains
由图4可知,当发酵温度为40 ℃时,6株酵母菌株均能生长,但菌株JM-7的生长受到严重抑制,只能微弱生长;当发酵温度为45 ℃时,所有菌株的生长速率趋近于零,但仍有微弱的生长。说明6株酵母菌株均可耐受40 ℃的高温,且菌株JM-1、JM-2、JM-3、JM-4、JM-9的耐受性更好。在浓香白酒发酵过程中,窖池温度通常为30~35 ℃,本研究筛选出可耐40 ℃温度的酵母菌,有助于保障白酒酿造生产稳定[26]。
综上,菌株JM-4和JM-7的乙醇耐受性较好,菌株JM-1、JM-2、JM-3、JM-4的酸耐受性最好,菌株JM-1、JM-2、JM-3、JM-4、JM-9的温度耐受性更好。
2.4 初筛酵母菌株产风味特性分析
2.4.1 有机酸含量分析
在浓香型白酒的酿造过程中,有机酸作为酯类化合物的关键前体物质,通过酯化反应直接影响酒体中果香、花香等典型风味的形成[27]。 然而,过高的有机酸含量会导致醋味和腐败异味的产生,显著降低酒体品质[28],因此,有机酸含量的控制也是调控白酒质量的重要因素之一。以未接种菌株的高粱水解液培养基为空白对照(Control),通过高粱汁发酵体系对酵母菌株的有机酸代谢特性进行考察,结果见图5。
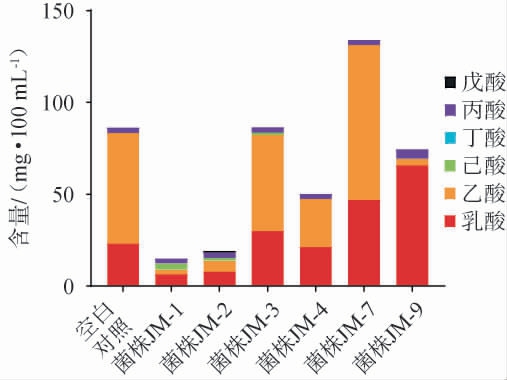
图5 6株酵母菌株产有机酸含量测定结果
Fig 5 Determination results of organic acid contents produced by 6 yeast strains
由图5可知,与空白对照相比,各处理组有机酸组成及含量呈现显著差异。菌株JM-1、JM-2和JM-4发酵液的乳酸含量均降低,分别为(6.53±0.65)mg/100mL、(7.94±0.73)mg/100mL和(21.47±1.23)mg/100mL,降幅达71.8%、65.7%和7.3%;而菌株JM-3发酵液中的乳酸含量略微升高[(30.18±1.50)mg/100mL],菌株JM-7和JM-9发酵液中的乳酸含量则明显升高,分别为(47.01±2.13)mg/100 mL和(65.84±3.69) mg/100 mL。 菌株JM-7发酵液中的乙酸含量升高至(84.32±4.22)mg/100 mL(增幅达39.7%),而菌株JM-1、JM-2、JM-3、JM-4、JM-9发酵液中的乙酸含量明显下降,分别为(2.41±0.66)mg/100 mL、(5.93±0.52)mg/100 mL、(52.19±1.89)mg/100 mL、(26.16±2.30)mg/100 mL、(3.58±0.87)mg/100 mL,降幅分别为96.0%、90.2%、13.5%、56.7%、94.1%。除菌株JM-9发酵液中的丙酸含量[(5.15±0.52) mg/100 mL]升高外,其余组无明显变化。 此外,空白对照组未检出己酸,但在菌株JM-1[(3.50±0.13) mg/100 mL]、JM-2[(1.56±0.74) mg/100 mL]和JM-3[(1.31±0.99)mg/100 mL]发酵液中微量积累。仅在菌株JM-2发酵液中检出戊酸[(0.69±0.21)mg/100 mL],而在所有组发酵液中丁酸的含量均维持在极低水平。
白酒中的酸类物质主要分为挥发性酸和不挥发性酸两大类。常见的挥发性酸包括乙酸、丙酸、丁酸、己酸和乳酸等[29]。 值得注意的是,菌株JM-1、JM-2、JM-4、JM-7和JM-9对关键有机酸表现出差异化的代谢特性。这种特异性很可能源于它们胞内酯化酶系活性或有机酸跨膜转运机制的不同[29]。而这种代谢上的差异,为构建功能明确的酵母菌株组合提供了重要的理论依据。
2.4.2 主要挥发性物质含量分析
异丁醇和异戊醇是高级醇类物质,对酒体的香气和口感有显著影响;已酸乙酯是浓香型白酒中主体香味成分,乙酸乙酯则是生香酵母利用葡萄糖代谢中间产物(乙醇和乙酸)在胞内酯酶催化下直接合成的典型酯类[30]。为了重点分析酵母在白酒发酵过程中产生的关键挥发性风味物质,对6株酵母菌发酵液中的异丁醇、异戊醇、已酸乙酯和乙酸乙酯4种重要挥发性风味物质进行检测,结果见图6。
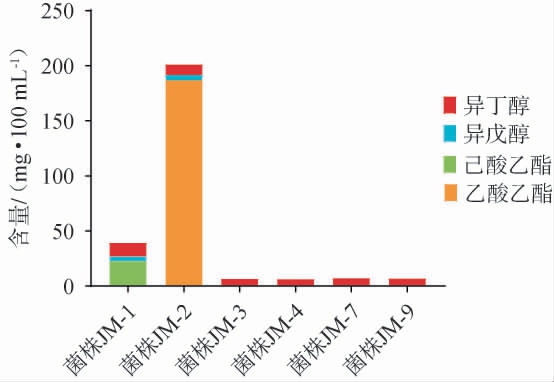
图6 6株酵母菌株产主要挥发性风味成分含量测定结果
Fig.6 Determination results of main volatile flavor compounds contents produced by 6 yeast strains
由图6可知,菌株JM-1发酵液中异丁醇、异戊醇及己酸乙酯含量分别为(12.26±1.85)mg/100 mL、(4.20±0.46)mg/100 mL、(22.71±0.74)mg/100 mL,乙酸乙酯未检出;菌株JM-2发酵液中异丁醇、异戊醇及乙酸乙酯含量分别为(9.54±0.37)mg/100 mL、(4.83±0.47)mg/100 mL、(186.97±18.64)mg/100 mL,己酸乙酯未检出;菌株JM-3、JM-4、JM-7、JM-9发酵液中异丁醇含量分别为(6.77±0.79)mg/100 mL、(6.50±0.45) mg/100 mL、(7.35±1.02) mg/100 mL、(7.13±0.91)mg/100 mL,而异戊醇、乙酸乙酯及己酸乙酯在这4株酵母菌中均未检出。结果说明不同酵母菌株在代谢产生的挥发性风味物质上表现出明显差异。 其中,菌株JM-1具有较高的产己酸乙酯能力,而菌株JM-2则表现出较强的产乙酸乙酯能力。这种差异可能与菌株的代谢途径和酶活性有关,菌株JM-2可能具有更高的醇乙酰转移酶活性,从而更高效地将乙醇和乙酸转化为乙酸乙酯。
结合菌株的耐受性及风味代谢特性分析结果,最终选择菌株JM-1和JM-2为高耐受性的产香优良酵母菌株。
2.5 优良酵母菌株的分子生物学鉴定
基于26S rDNA D1/D2区基因序列构建菌株JM-1和JM-2的系统发育树,结果见图7。由图7可知,菌株JM-1和JM-2分别与Nakaseomyces glabratus和Clavispora lusitaniae聚于一支,亲缘关系最近,结合形态学特征,最终将菌株JM-1和JM-2分别鉴定为光滑念珠菌(Nakaseomyces glabratus)和葡萄牙棒孢酵母(Clavispora lusitaniae)。
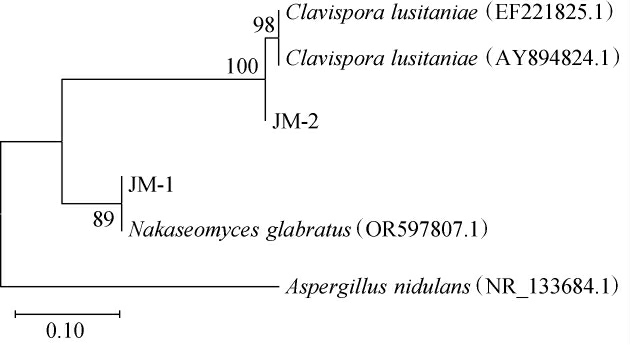
图7 基于26S rDNA D1/D2基因序列菌株JM-1及JM-2的系统发育树
Fig.7 Phylogenetic tree of strains JM-1 and JM-2 based on 26S rDNA D1/D2 gene sequence analysis
3 结论
本研究通过传统培养分离技术从浓香型大曲中共分离纯化得到10株酵母菌株(JM-1~JM-10),通过产气性能初筛获得6株发酵特性优良的酵母菌株(JM-1、JM-2、JM-3、JM-4、JM-7、JM-9)。综合耐受性与风味代谢特性分析筛选得到2株高耐受性产香优良酵母菌株(编号分别为JM-1、JM-2)。菌株JM-1与JM-2均可耐受pH 2、乙醇体积分数7%、温度40 ℃,二者具有突出的风味定向调控能力,其中菌株JM-1具有71.8%的乳酸降幅能力,并特异性合成己酸乙酯(22.71 mg/100 mL),而菌株JM-2高产乙酸乙酯(186.97 mg/100 mL)且同步降低乳酸与乙酸(降幅分别为65.7%与90.2%)。通过分子生物学技术鉴定菌株JM-1、JM-2分别为光滑念珠菌(Nakaseomyces glabratus)和葡萄牙棒孢酵母(Clavispora lusitaniae)。结果表明,菌株JM-1和JM-2兼具环境适应性、有机酸平衡调控能力及特征酯类合成优势,具备浓香型白酒酿造所需的高效功能特性。
[1]焦凯瑞,邓波,宋萍,等.浓香型白酒生产中的功能微生物及其协同作用研究进展[J].南京师大学报(自然科学版),2024,47(4):68-76.
[2]孙金涛,田小雨,李学思.浓香型白酒在贮存过程中主要风味物质变化规律的研究[J].酿酒,2024,51(3):84-86.
[3]张慧,韩美月,张亚,等.浓香型大曲产香酵母的筛选、鉴定及应用[J].中国食品学报,2024,24(11):176-185.
[4]何小容,张庆,唐家环,等.浓香型白酒大曲发酵过程中主要微生物群系及其作用研究进展[J].中国酿造,2024,43(8):1-6.
[5]毛晶晶.浓香型大曲微生物多样性的研究[D].洛阳:河南科技大学,2022.
[6]LIU W H,CHAI L J,WANG H M,et al.Bacteria and filamentous fungi running a relay race in Daqu fermentation enable macromolecular degradation and flavor substance formation[J].Int J Food Microbiol, 2023,390:110118.
[7]LIU Y,LI X,LI H,et al.Taorong-type Baijiu starter: Analysis of fungal community and metabolic characteristics of middle-temperature Daqu and high-temperature Daqu[J].PloS one,2022,17(10):e0274881.
[8]边名鸿,万世旅,代梅,等.产酒酵母的筛选鉴定及其在小曲中的应用[J].中国酿造,2016,35(3):57-60.
[9]张新红,张源.浓香型大曲质量影响因素研究进展[J].生物化工,2020,6(4):118-122.
[10]李秋晓,庞泽敏,张茹,等.高产乙酸乙酯酵母的筛选鉴定及发酵条件优化[J].中国酿造,2024,43(6):80-87.
[11]余伟民,徐小明,林培,等.生香酵母对特香型白酒风味风格的影响研究[J].酿酒科技,2012(1):24-27.
[12]宜宾南溪酒业有限公司.一种浓香型大曲酵母菌的检测方法:CN202311069717.7[P].2023-12-19.
[13]陈静,黄义芬,左勇,等.耐受性酵母的筛选及其在猕猴桃果酒中的应用研究[J].中国调味品,2025,50(7):90-95.
[14]张旭姣,闫裕峰,郎繁繁,等.耐高温产香酵母的分离筛选及麸曲制作工艺优化[J].中国酿造,2025,44(2):108-114.
[15]李超.酱香型白酒耐酸粟酒裂殖酵母高酸胁迫响应的分子机制研究[D].天津:天津科技大学,2022.
[16]罗惠波,李光辉.耐酸酵母菌的筛选研究[J].四川理工学院学报(自然科学版),2004(Z1):151-154.
[17]刘兴艳,贾博,赵芳,等.酿酒酵母对弱有机酸胁迫的应激机制研究进展[J].食品与发酵工业,2013,39(6):125-129.
[18]LIN N X,XU Y,YU X W.Overview of yeast environmental stress response pathways and the development of tolerant yeasts[J].Syst Microbiol Biomanufactur,2022,2(2):232-245.
[19]AKITA H, MATSUSHIKA A.Transcription analysis of the acid tolerance mechanism of Pichia kudriavzevii NBRC1279 and NBRC1664[J].Fermentation,2023,9(6):559.
[20]DENG N, DU H, XU Y.Cooperative response of Pichia kudriavzevii and Saccharomyces cerevisiae to lactic acid stress in Baijiu fermentation[J].J Agr Food Chem,2020,68(17):4903-4911.
[21]刘明.浓香型白酒酿造过程中酸类物质的调控[J].酿酒科技,2014(8):62-64.
[22]陶洪驰,李星,赵荣寿,等.浓香型白酒发酵过程中窖池内不同时空物质变化规律的研究[J].酿酒科技,2023(8):24-27.
[23]VIEILLE C, ZEIKUS G J.Hyperthermophilic enzymes: Sources, uses,and molecular mechanisms for thermostability[J].Microbiol Mol Biol R,2001,65(1):1-43.
[24]MORANO K A,GRANT C M,MOYE-ROWLEY W S.The response to heat shock and oxidative stress in Saccharomyces cerevisiae[J].Genetics,2012,190(4):1157-1195.
[25]EDGARDO A,CAROLINA P,MANUEL R,et al.Selection of thermotolerant yeast strains Saccharomyces cerevisiae for bioethanol production[J].Enzyme Microb Tech,2008,43(2):120-123.
[26]常强,吴再节,崔战友,等.不同入窖温度对浓香型白酒度夏压排产酒影响的研究[J].酿酒科技,2025(10):77-80.
[27]CAO Y,WU Z,WENG P.Comparison of bayberry fermented wine aroma from different cultivars by GC-MS combined with electronic nose analysis[J].Food Sci Nutr,2020,8(2):830-840.
[28]HAN Y Y,SU Z C,DU J H.Effects of apple storage period on the organic acids and volatiles in apple wine[J].LWT-Food Sci Technol,2023,173:114389.
[29]张河云,王学娇,张曼,等.酸类物质对浓香型白酒风味的影响研究[J].中国酿造,2023,42(11):82-89.
[30]汪晗,高瑞杰,杨团元,等.白酒酿造中低产高级醇酿酒酵母的筛选及应用研究[J].中国酿造,2023,42(8):78-83.