猕猴桃(Actinidia chinensis Planch)是猕猴桃科、猕猴桃属藤本落叶果树,其果实富含维生素C[1]。目前,猕猴桃种植已在农业发展中具有重要的经济地位,且我国猕猴桃种植面积和产量已居全球首位[2]。 溃疡病是猕猴桃栽培中常见的病害,其主要由丁香假单胞菌猕猴桃致病变种(Pseudomonas syringae pv.actinisia)引起,具有发生范围广、传播速度快、致病性强等特点,对猕猴桃的生产和品质具有巨大危害,严重制约猕猴桃产业的发展[3-5]。
目前,猕猴桃溃疡病的防治主要有选择抗性品种、化学防治和生物防治[6-9]。 其中,使用最广泛的是化学防治,但长期使用大剂量的化学药剂会致使病原菌对化学药剂的抗药性增加[10]。生物防治是利用有益微生物及其代谢产物来防治植物病害的技术。生物防治因低毒、无农药残留、不易产生抗药性和环境友好等特点,在植物病害防治和保护生态环境安全方面具有广阔的发展和应用前景[11-14]。
根际微生物作为土壤的重要组成部分,在植物的生长发育中发挥着不可或缺的协同作用[15-16]。大量研究证明,根际微生物的固氮、溶磷、溶钾和抗菌等功能在根际区植物根系与土壤进行养分和能量的交换中起着关键作用[17-20]。潘彦硕[21]考察了干旱胁迫下根际微生物群落对冬小麦生长和产量的影响,结果表明,根际微生物群落的多样性提高了冬小麦在干旱胁迫下的抗逆能力以及生长所需的促生因子。 YANG S等[22]研究发现,施用添加了硫磺粉的基肥可以显著提高根际微生物群落的多样性和丰度,降低猕猴桃细菌性溃疡病的发病率和严重程度。尹志诚[23]研究发现,由红树林幼球菌(Kineococcus mangrovi)、蒙氏肠球菌(Enterococcus mundtii)和嗜根寡养单胞菌(Stenotrophomonas rhizophila)构建的菌群对猕猴桃溃疡病的防治效果显著高于单一菌种,表明微生物间的协同作用增强了对猕猴桃溃疡病的防治效果。解析猕猴桃根际土壤的微生物群落结构和优势菌门,有助于构建具有协同作用的菌群用于猕猴桃溃疡病等常见病害的防控。
因此,本研究拟以采集自南阳市西峡县奎文村、屈原岗村、王营村的健康猕猴桃根际土壤为研究对象,采用常规检测方法对其理化指标进行检测,采用Illumina MiSeq高通量测序技术对其微生物群落多样性进行分析,并对土壤理化性质和微生物群落间的相关性进行分析,以期对后续筛选有益微生物防治猕猴桃溃疡病的发生及揭示微生物与猕猴桃根际的协同互作作用奠定研究基础。
1 材料与方法
1.1 材料与试剂
1.1.1 样品
猕猴桃根际土壤:在南阳市西峡县奎文村(111.26°E,33.35°N)、屈原岗村(111.58°E,33.25°N)、王营村(116.70°E,33.14N),采用随机取样法在各个取样点分别选取3个3 m×3 m样方,每个样方中随机选定5棵多年生健康猕猴桃植株,清除0~5 cm表层土壤,深挖至根部,采集根部下方及周围5 cm内土壤,相同取样点采集的土壤样品混合均匀后作为1个样品,储存于无菌自封袋内,每个取样地采集样品3个,贮存于-20 ℃冰箱备用。 取自奎文村、屈原岗村、王营村的样品分别编号为KW、QYG、WY。
1.1.2 试剂
E.Z.N.A.R Soil脱氧核糖核酸(deoxyribonucleic acid,DNA)提取试剂盒:美国Omega Bio-Tek公司;FastPfu聚合酶(5U/μL):生工生物工程(上海)股份有限公司;AxyPrep DNA Gel Extraction Kit:康宁生命科学(吴江)公司;NEXTFLEXR Rapid DNA-Seq Kit:美国PerkinElmer公司;MiSeq Reagent Kit v3:美国Illumina公司;琼脂糖(电泳级):西班牙Biowest公司。
1.2 仪器与设备
Eppendorf 5424R高速台式冷冻离心机:德国Eppendorf公司;NanoDrop2000超微量分光光度计、Varioskan Flash酶标仪:美国Thermo Scientific公司;QuantiFluorTM-ST微型荧光计:美国Promega公司;聚合酶链式反应(polymerase chain reaction,PCR)仪:德国Biometra公司;Illumina Miseq高通量测序仪:美国Illumina公司。
1.3 方法
1.3.1 土壤理化性质的测定
参考《土壤农化分析》(第三版)[24]测定土壤样品的pH、有机质(organic matter,OM)含量、有效磷(available phosphorus,AP)含量、速效钾(available potassium,AK)含量、碱解氮(alkali-hydrolyzable nitrogen,AN)含量。
1.3.2 高通量测序与分析
使用E.Z.N.A.R Soil DNA提取试剂盒提取土壤样品的基因组DNA,检测合格后,以此为模板,分别使用引物338F(5'-ACTCCTACGGGAGGCAGCAG-3') 和806R(5'-GGACTACHVGGGTWTCTAAT-3')PCR扩增细菌菌群16S rRNA序列的V3~V4可变区,使用引物ITS1F(5'-CTTGGTCATTTAGAGGAAGTAA-3')和ITS2R(5'-GCTGCGTTCTTCATCGATGC-3')PCR扩增真菌菌群的ITS1区基因序列[25]。PCR扩增产物纯化后构建文库,得到高质量的测序样品,委托上海美吉生物医药科技有限公司进行高通量测序。
测序得到的原始序列经Trimmomatic软件质控,使用FLASH软件进行拼接。 根据PE Reads之间的Overlap关系,将过滤质控后的成对Reads拼接为一条序列。通过调整方向,得到有效序列,借助Uchime软件剔除嵌合体,按照97%的相似度将有效序列聚成不同的操作分类单元(operational taxonomic unit,OTU)。 高通量测序结果的多样性分析、物种丰度分析、冗余分析(redundancy analysis,RDA)通过上海美吉生物医药科技有限公司在线分析平台完成。
1.3.3 数据处理与统计分析
采用Excel 2021处理数据,使用SPSS 27.0软件进行统计分析。
2 结果与分析
2.1 猕猴桃根际土壤理化性质分析
不同采样点猕猴桃根际土壤理化性质的测定结果见表1。由表1可知,3个猕猴桃根际土壤样品的有机质含量无显著差异(P>0.05),而pH、有效磷含量、速效钾含量和碱解氮含量均存在显著差异(P<0.05),其中QYG样品的pH最高,其次为KW样品;WY样品的有效磷含量和碱解氮含量最高,其次为QYG样品。 结果表明,不同采样点猕猴桃根际土壤样品的理化性质存在明显的差异。
表1 猕猴桃根际土壤样品的理化性质
Table 1 Physicochemical properties of rhizosphere soil samples of kiwifruit
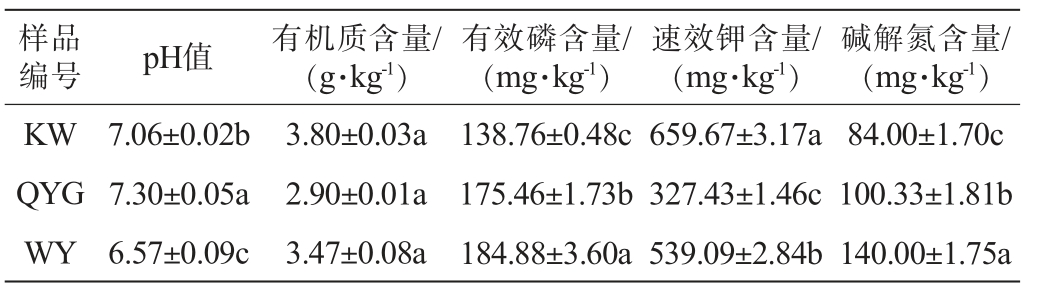
注:同列不同字母代表差异显著(P<0.05)。下同。
样品编号 pH值 有机质含量/(g·kg-1)有效磷含量/(mg·kg-1)速效钾含量/(mg·kg-1)碱解氮含量/(mg·kg-1)KW QYG WY 84.00±1.70c 100.33±1.81b 140.00±1.75a 7.06±0.02b 7.30±0.05a 6.57±0.09c 3.80±0.03a 2.90±0.01a 3.47±0.08a 138.76±0.48c 175.46±1.73b 184.88±3.60a 659.67±3.17a 327.43±1.46c 539.09±2.84b
2.2 猕猴桃根际土壤微生物群落多样性分析
2.2.1 Alpha多样性分析
通过对猕猴桃根际土壤样品中的细菌及真菌群落进行高通量测序,分别共得到序列500 131条、502 772条,经拼接、过滤后,分别共得到393 309条、422 037条有效序列,在97%相似度水平下分别共划分得到7 528个、2 397个OTUs。选取OTUs绘制韦恩图,结果见图1。由图1a可知,KW、QYG和WY样品中共有细菌OTUs为2 319个,特有细菌OTUs分别为1 148个、929个、1 048个;由图1b可知,共有真菌OTUs为256个,特有真菌OTUs分别为555个、447个、622个。 结果表明,不同采样点猕猴桃根际土壤样品中微生物群落存在异同。
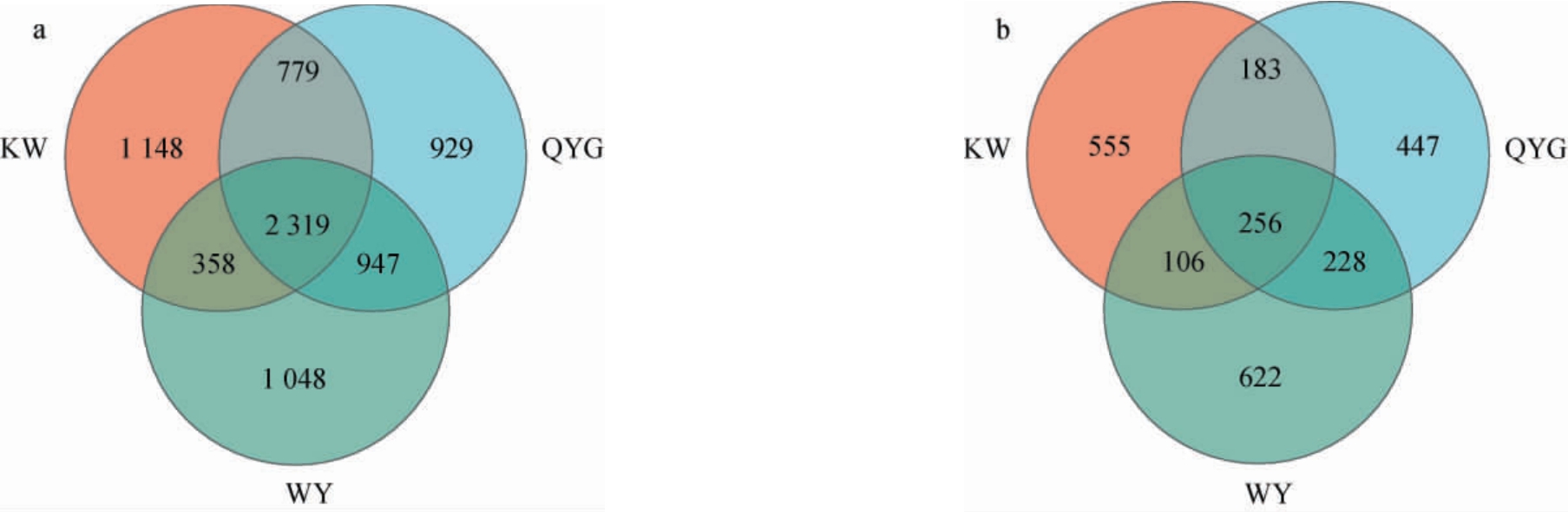
图1 猕猴桃根际土壤样品中细菌(a)及真菌(b)群落操作分类单元韦恩图
Fig.1 Venn diagram of the operational taxonomic units of bacterial (a) and fungal (b) communities in the rhizosphere soil samples of kiwifruit
α多样性指数通常用来反映微生物群落的多样性和丰度,包括Shannon指数、Simpson指数、Ace指数、Chao1指数和覆盖率[26]。 微生物群落的多样性常使用Shannon指数和Simpson来表征,Shannon指数数值越大,Simpson指数数值越小,表示微生物群落的多样性越高;Ace指数和Chao1指数反映微生物群落的丰度,其数值越大表示微生物群落丰度越高;覆盖率数值越高,表明样品中序列被测出的概率越高。 不同采样点猕猴桃根际土壤样品中微生物群落的α多样性分析结果见表2。由表2可知,猕猴桃根际土壤样品KW、QYG和WY中微生物群落的覆盖率均>98%,说明样品中新物种没有被测出的概率很低。猕猴桃根际土壤样品KW、QYG和WY中细菌菌群的α多样性指数差异不显著(P>0.05)。结果表明,3处采样点的猕猴桃根际土壤样品细菌群落多样性和物种丰度没有明显区别。样品QYG真菌菌群的Shannon指数显著低于样品KW(P<0.05),Simpson指数显著高于KW样品(P<0.05),但样品WY的多样性指数与其他两个样品无显著差异(P>0.05);3个样品间的Ace指数和Chao1指数无显著差异(P>0.05)。 结果表明,样品QYG中真菌群落的多样性最高,样品KW中真菌群落的多样性最低,但3处采样点猕猴桃根际土壤中真菌群落的物种丰度一致。
表2 猕猴桃根际土壤样品微生物群落α多样性分析结果
Table 2 Analysis results of α-diversity of microbial communities in rhizosphere soil samples of kiwifruit
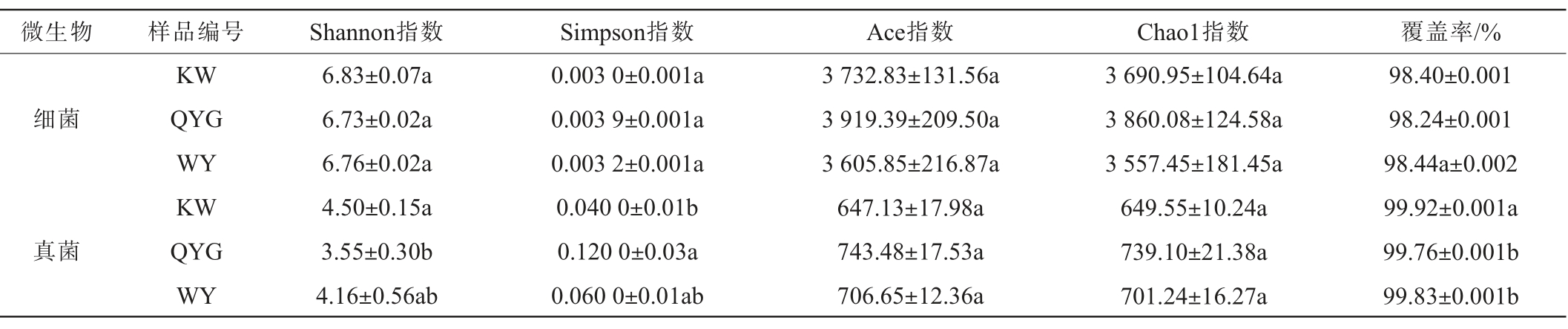
微生物 样品编号 Shannon指数 Simpson指数 Ace指数 Chao1指数 覆盖率/%细菌真菌KW QYG WY KW QYG WY 6.83±0.07a 6.73±0.02a 6.76±0.02a 4.50±0.15a 3.55±0.30b 4.16±0.56ab 0.003 0±0.001a 0.003 9±0.001a 0.003 2±0.001a 0.040 0±0.01b 0.120 0±0.03a 0.060 0±0.01ab 3 732.83±131.56a 3 919.39±209.50a 3 605.85±216.87a 647.13±17.98a 743.48±17.53a 706.65±12.36a 3 690.95±104.64a 3 860.08±124.58a 3 557.45±181.45a 649.55±10.24a 739.10±21.38a 701.24±16.27a 98.40±0.001 98.24±0.001 98.44a±0.002 99.92±0.001a 99.76±0.001b 99.83±0.001b
2.2.2 群落结构分析
从不同采样点猕猴桃根际土壤样品中共注释到51个细菌门和16个真菌门,基于门水平对不同采样点猕猴桃根际土壤样品中的微生物群落结构进行分析,结果见图2。由图2a可知,从样品KW、QYG和WY中分别注释到12个、13个、10个优势细菌门(相对丰度>1%),其中相对丰度排名前6的优势细菌门均为假单胞菌门(Pseudomonadota)、酸杆菌门(Acidobacteriota)、芽孢杆菌门(Bacillota)、绿弯菌门(Chloroflexota)、放 线 菌 门(Actinomycetota)、拟 杆 菌 门(Bacteroidota)。KW样品中特有的优势细菌门为浮霉菌门(Planctomycetota)、迟杆菌门(Latescibacterota)、Methylomirabilota,QYG样品中特有的优势细菌门为衣原体门(Chlamydiota)和蛭弧菌门(Bdellovibrionota)。

图2 基于门水平猕猴桃根际土壤样品中细菌(a)及真菌(b)群落结构
Fig.2 Community structure of bacteria (a) and fungi (b) in the rhizosphere soil samples of kiwifruit based on phylum level
由图2b可知,从样品KW、QYG和WY中分别注释到5个、5个、4个优势真菌门(相对丰度>1%)。3个土壤样品中共有的优势真菌门为子囊菌门(Ascomycota)、被孢霉门(Mortierellomycota)、担子菌门(Basidiomycota),其中子囊菌门(Ascomycota)相对丰度最高,分别为60.02%、67.33%、44.37%。KW样品中特有的优势真菌门为壶菌门(Chytridiomycota),QYG样品中特有的优势真菌门为罗兹菌门(Rozellomycota)。
目前,用于猕猴桃溃疡病生物防治的微生物主要为细菌,且多为单一菌株。 盛存波等[27]从猕猴桃根际土壤筛选获得一株芽孢杆菌(Bacillus)B56-3,对猕猴桃溃疡病具有很好的抑菌活性,其发酵液稀释100倍后经喷雾和刮除涂抹对田间猕猴桃溃疡病的防治效果达86.5%以上;杜贞娜等[28]从健康的猕猴桃组织和土壤中分离到3株芽孢杆菌,对猕猴桃溃疡病有很好的拮抗效果;关鹏等[29-30]分别报道了放线菌对猕猴桃溃疡病防治的显著效果。已报道的防治猕猴桃溃疡病的菌株多数属于放线菌门、芽孢杆菌门,且尚无有关真菌防治猕猴桃溃疡病的报道。本研究的高通量测序结果显示,放线菌门、芽孢杆菌门在3种猕猴桃根际土壤样品中均为优势细菌门,这有助于筛选得到防治猕猴桃溃疡病的有益微生物,且更有利于构建具备协同作用的微生物菌群,制备菌剂用于猕猴桃溃疡病的防治。
2.3 猕猴桃根际土壤微生物群落与土壤理化性质的相关性分析
选取平均相对丰度排名前10的优势细菌门和所有优势真菌门,采用RDA研究猕猴桃根际土壤微生物群落与土壤理化性质的相关性,结果见图3。

图3 猕猴桃根际土壤样品中优势细菌门(a)及优势真菌门(b)与理化性质的冗余分析结果
Fig.3 Redundant analysis results of dominant bacterial phylum (a)and dominant fungal phylum (b) and physicochemical properties in the rhizosphere soil samples of kiwifruit
由图3a可知,前2个排序轴共解释了细菌群落变化的77.65%,说明土壤理化性质对细菌群落分布具有显著影响。 土壤理化性质对猕猴桃根际土壤细菌群落的影响程度表现为速效钾含量(r2=0.85)>有效磷含量(r2=0.81)>pH(r2=0.69)>碱解氮含量(r2=0.63)>有机质含量(r2=0.43)。选取与已报道的猕猴桃溃疡病生防菌相关的优势菌门(Bacillota、Actinomycetota)进行分析,发现芽孢杆菌门与pH、有效磷含量、碱解氮含量呈正相关,与有机质含量、速效钾含量呈负相关;放线菌门与有机质含量、速效钾含量碱解氮含量呈正相关,与pH、有效磷含量呈负相关。
由图3b可知,前2个排序轴共解释了真菌群落78.70%的总方差,说明土壤理化性质对真菌群落分布具有显著影响。土壤理化性质对猕猴桃根际土壤真菌群落的影响程度表现为pH(r2=0.83)>碱解氮含量(r2=0.71)>有效磷含量(r2=0.28)>有机质含量(r2=0.084)>速效钾含量(r2=0.083)。优势真菌门中子囊菌门、被孢霉门和罗兹菌门均与pH呈正相关,与有机质含量、有效磷含量、速效钾含量及碱解氮含量呈负相关;担子菌门与速效钾含量、碱解氮含量和有效磷含量呈正相关,与有机质含量和pH呈负相关;未分类真菌门、壶菌门均与有机质含量、有效磷含量、碱解氮含量、速效钾含量呈正相关,与pH呈负相关。
为探究土壤理化性质对猕猴桃根际土壤微生物群落结构的影响,为后续筛选猕猴桃溃疡病生防菌奠定基础,进一步对猕猴桃根际土壤微生物群落结构和土壤理化性质的相关性进行分析,结果见图4。
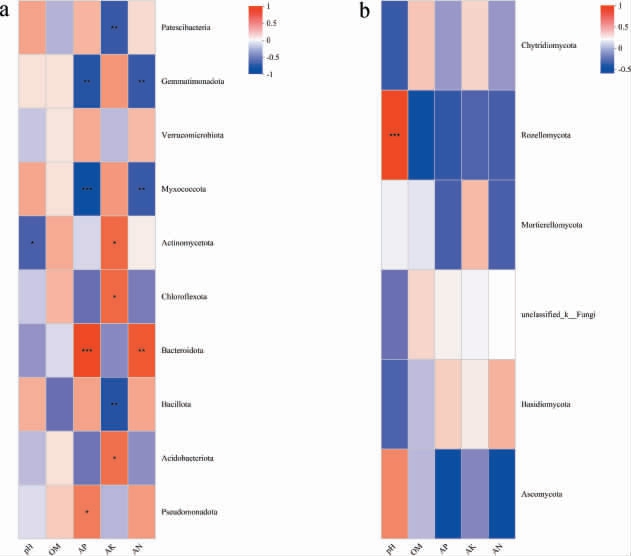
图4 猕猴桃根际土壤样品优势细菌门(a)和优势真菌门(b)与理化性质的相关性分析结果
Fig.4 Correlation analysis results of dominant bacterial phylum (a)and dominant fungal phylum (b) and physicochemical properties in the rhizosphere soil samples of kiwifruit
“*”表示显著相关(P<0.05),“**”表示极显著相关(P<0.01),“***”表示高度显著相关(P<0.001)。
由图4a可知,芽孢杆菌门与速效钾含量存在极显著负相关关系(P<0.01),与其他土壤理化性质无显著相关关系(P>0.05),表明速效钾含量高不利于芽孢杆菌门在猕猴桃根际土壤微生物群落中富集;放线菌门与pH存在显著负相关关系(P<0.05),与速效钾含量呈显著正相关(P<0.05),表明高pH不利于放线菌门在微生物群落结构中富集,速效钾含量高则有利于放线菌门在微生物群落结构中保持优势地位。 由图4b可知,罗兹菌门与pH之间存在高度显著正相关关系(P<0.001),表明pH促进了罗兹菌门在真菌群落结构中的富集。 其他优势真菌门与土壤理化性质之间不存在明显的相关性(P>0.05)。
根际土壤微生物在植物与土壤的物质循环和转化中发挥着重要作用[31]。根际微生物将土壤中的有机物分解为小分子有机物,不仅为自身生长繁殖和植物生长提供营养物质,同时产生的多种多谢物质,如有机酸、多糖等可以调节土壤的理化性质,改善土壤结构和肥力[32]。白茹[33]的研究表明,不同药用植物根际土壤的理化性质具有异质性,且与根际土壤微生物的群落结构差异有相关关系,这与本研究结果一致。 本研究中冗余分析及相关性分析结果显示,芽孢杆菌门与速效钾含量呈极显著负相关,放线菌门与速效钾含量呈显著正相关,与pH呈显著负相关;pH与罗兹菌门存在极显著正相关关系。这反映了真菌优势菌门在猕猴桃根际土壤中群落结构稳定,受土壤理化性质影响较小。由于已报道的猕猴桃溃疡病生防菌多属于芽孢菌门和放线菌门,且无相关报道真菌可以防治猕猴桃溃疡病[34-35]。因此,后续筛选猕猴桃溃疡病生防菌时,应重点关注芽孢杆菌门和放线菌门,关注根际土壤的速效钾含量及pH。
3 结论
本研究采用常规检测方法检测南阳市西峡县奎文村(KW)、屈原岗村(QYG)、王营村(WY)猕猴根际土壤样品的基本理化指标,结果发现,除了有机质含量无显著差异外(P>0.05),3个样品的pH、有效磷含量、速效钾含量、碱解氮含量差异显著(P<0.05)。 通过Illumina MiSeq高通量测序技术分析3个猕猴根际土壤样品微生物群落多样性,结果发现,3个样品细菌群落多样性及物种丰度无显著差异(P>0.05),QYG样品真菌群落多样性最高,KW样品最低,但3个样品真菌群落的物种丰度无显著差异(P>0.05)。 从3个样品中共注释到51个细菌门和16个真菌门,包括16个优势细菌门(相对丰度>1%)和6个优势真菌门,其中芽孢杆菌门(Bacillota)和放线菌门(Actinomycetota)作为潜在的猕猴桃溃疡病生防细菌,在3个样品中均为优势菌门。通过对土壤理化指标及优势微生物间的相关性分析,结果发现,土壤理化性质对猕猴桃根际土壤微生物群落分布具有显著影响,其中,芽孢杆菌门与速效钾含量呈极显著负相关(P<0.01),放线菌门与速效钾含量碱解氮含量呈显著正相关(P<0.05),与pH呈显著负相关(P<0.05);pH与罗兹菌门呈高度显著正相关(P<0.001)。本研究结果有助于筛选得到防治猕猴桃溃疡病的有益微生物,且更有利于构建具备协同作用的微生物菌群,制备菌剂用于猕猴桃溃疡病的防治。
[1]陈海生,江景勇,潘仙鹏,等.猕猴桃根腐病发生对其植株根际土壤真菌群落结构影响[J].四川农业大学学报,2023,41(4):631-639.
[2]任春光,苏文文,潘丽珊,等.基于高通量测序研究猕猴桃苗不同生育期根际真菌群落结构及多样性[J].土壤,2021,53(3):545-554.
[3]PEREIRA C,COSTA P,PINHEIRO L, et al.Kiwifruit bacterial canker:An integrative view focused on biocontrol strategies[J].Planta,2021,253(2):49.
[4]张敏,孙雷明,付蓉,等.猕猴桃抗细菌性溃疡病研究进展[J].果树学报,2025,42(1):196-206.
[5]WANG H, WANG N, TAN Y, et al. Paenibacillus polymyxa YLC1: A promising antagonistic strain for biocontrol of Pseudomonas syringae pv.actinidiae,causing kiwifruit bacterial canker[J].Pest Manag Sci, 2023,79(11):4357-4366.
[6]尹志诚,顾佳颖,李南羿,等.猕猴桃溃疡病生防菌群的构建及其生防效应[J].林业科学,2024,60(12):101-110.
[7]田野,李丽丽,杜春梅,等.猕猴桃溃疡病的研究进展[J].江苏农业科学,2023,51(15):8-15.
[8]贺占雪,朱太富,李欣,等.不同砧穗组合对猕猴桃溃疡病的抗性差异及机制分析[J].河南农业科学,2023,52(1):95-107.
[9]刘露.猕猴桃细菌性溃疡病复配拮抗菌的筛选及发酵工艺优化[D].杨凌:西北农林科技大学,2023.
[10]朱海云,马瑜,柯杨,等.猕猴桃溃疡病菌拮抗菌的筛选、鉴定及其对植物病原真菌的抗性[J].生物技术通报,2021,37(6):66-72.
[11]HU R,XU X,JIA Y,et al.Phage cocktail alleviates bacterial canker of kiwifruit by modulating bacterial community structure in field Trial[J].Microorganisms,2025,13(1):104.
[12]杜贞娜,晏子英,候忠余,等.猕猴桃溃疡病病原菌的鉴定及生防菌的筛选[J].西南农业学报,2021,34(4):755-761.
[13]钟彩虹,李黎,潘慧,等.猕猴桃细菌性溃疡病的发生规律及综合防治技术[J].中国果树,2020(1):9-13,18.
[14]甘林,兰成忠,占仕发,等.福建地区猕猴桃细菌性溃疡病菌的生物学特征及其杀菌剂筛选[J].福建农业学报,2024,39(11):1280-1288.
[15]李峰卿,刘素贞,罗桂生,等.不同生境沙氏鹿茸草根际土壤细菌群落结构和多样性分析[J].林业科学,2025,61(1):47-56.
[16]李世金,林硕,马称心,等.生物质灰加生物菌剂对烟草根际土壤微生物群落的影响以及对青枯病的防治效果[J].江苏农业学报,2024,40(12):2237-2243.
[17]TRIVEDI P,LEACH J E,TRINGE S G,et al.Plant-microbiome interactions:From community assembly to plant health[J].Nat Rev Microbiol,2020,18(11):607-621.
[18]BABALOLA O O,EMMANUEL O C,ADELEKE B S,et al.Rhizosphere microbiome cooperations:Strategies for sustainable crop production[J].Curr Microbiol,2021,78(4):1069-1085.
[19]杨睿.猕猴桃溃疡病菌的鉴定及其胁迫下根际土壤细菌群落结构的解析[D].吉首:吉首大学,2022.
[20]徐国益.有益微生物菌肥对猕猴桃根围土壤—生物系统的调节及对果实品质的影响[D].杨凌:西北农林科技大学,2018.
[21]潘彦硕.干旱胁迫下冬小麦-根际微生物互作研究[D].杨凌:西北农林科技大学,2023.
[22]YANG S,SHU R,YIN X,et al.Response of soil microbial community structure mediated by sulfur-induced resistance against kiwifruit bacterial canker[J].Front Microbiol,2022,13:883463.
[23]尹志诚.猕猴桃细菌性溃疡病生防菌群的构建及其生防效应[D].杭州:浙江农林大学,2024.
[24]鲍士旦.土壤农化分析(第三版).北京:中国农业出版社,2000:25-106.
[25]朱怡,吴永波,安玉亭.基于高通量测序的禁牧对土壤微生物群落结构的影响[J].生态学报,2022,42(17):7173-7146.
[26]张守梅,郭玉秋,张娜娜,等.基于高通量测序分析玉米浸泡副产物中细菌群落结构和多样性[J].山东农业科学,2021,53(12):143-148.
[27]盛存波,安德荣,鲁燕汶,等.生防菌住B56-3防治猕猴桃溃疡病的初步研究[J].上海农业学报,2006(3):75-78.
[28]杜贞娜,晏子英,候忠余,等.猕猴桃溃疡病病原菌的鉴定及生防菌的筛选[J].西南农业学报,2021,34(4):755-761.
[29]关鹏,贺志有,代小娟,等.猕猴桃细菌性溃疡病生防放线菌的筛选与鉴定[J].生物资源,2024,46(3):276-282.
[30]刘巍,王华,杨若兰,等.淡紫灰链霉菌gCLA4对猕猴桃溃疡病预防效果及抑菌活性成分分离鉴定[J].西北农业学报,2023,32(8):1289-1296.
[31]邵秋雨,董醇波,韩燕峰,等.植物根际微生物组的研究进展[J].植物营养与肥料学报,2021,27(1):144-152.
[32]ZHANG T, WANG Z, LV X, et al.Variation of rhizosphere bacterial community diversity in the desert ephemeral plant Ferula sinkiangensis across environmental gradients[J].Sci Rep,2020,10(1):18442.
[33]白茹.土壤根际微生物对新疆五种药用植物的响应及新疆紫草根际解磷菌的分离[D].伊犁:伊犁师范大学,2024.
[34]ZHANG S, LIU X, ZHOU L, et al.Alleviating soil acidification could increase disease suppression of bacterial wilt by recruiting potentially beneficial rhizobacteria[J].Microbiol Spectrum,2022,10(2):e02333-21.
[35]翟杨.猕猴桃溃疡病生防菌筛选、鉴定及其生防机理研究[D].北京:中国农业科学院,2022.