新阿波罗栖热袍菌(Thermotoga neapolitana)是一种超嗜热菌,属于革兰氏阴性菌,经培养后可产多种嗜热酶(如α-葡萄糖苷酶、纤维素酶、直链淀粉酶、木聚糖酶等),这些酶由于具有较强的耐热性而具有广泛的应用前景。耐热酶来源的原始菌株多为嗜热菌和超嗜热菌,这些嗜热菌的培养条件极为苛刻,因此,通过基因克隆和基因重组的手段使得高温酶的基因片段在常温菌中表达,可实现大规模培养并可大量获得所需高温酶。
普鲁兰酶属于α-淀粉酶家族[1],它可以特异性水解支链淀粉、糊精、普鲁兰糖的α-1,6糖苷键[2],广泛应用于淀粉糖化、酿造、生物燃料转化、纺织工业和医药工业等领域[3-4],起到缩短糖化时间、提高产率和转化率的作用。 REN P F等[5]通过表达系统优化和生物膜固定化发酵策略提高葡聚糖酶的产量。 KANG J H等[6]从新阿波罗栖热袍菌(Thermotoga neapolitana)中克隆PulA基因,并在大肠杆菌BL21(DE3)中克隆与表达,获得了分子质量约为93 kDa的重组酶,该酶的最适作用温度为80 ℃,最适pH值5.0~7.0。王明道等[7]选择来源于极端嗜热菌Thermosipho melanesiensis的普鲁兰酶基因,以基因组为模板,扩增普鲁兰酶基因TM-pulA,构建了重组质粒pET21a-TM-pulA,转入大肠杆菌DE3中诱导表达获得重组酶TM-pulA,其为I型普鲁兰酶,最适pH为5.8,最适温度为80 ℃。目前国际上普鲁兰酶的工业化生产被丹麦垄断,我国仅局限于实验室研究,且酶活较低。 因此,开发普鲁兰酶对食品加工领域具有重要的工业价值。
普鲁兰酶与异淀粉酶不同,它可以将最小单位的支链分解,最大限度地利用淀粉原料。 异淀粉酶虽然也能水解分支点的α-1,6糖苷键,但不能水解由2~3个葡萄糖残基组成的短支链。 因此,普鲁兰酶在淀粉加工和改性方面具有独特的优势。 多孔淀粉是通过化学、物理或酶法改性制备的淀粉产品[8],具有高孔隙率、高比表面积及负载量大等优点,在食品工业、医药与健康、化妆品、环保、农业和包装材料等领域应用广泛[9]。莲子是我国重要的特产经济作物和食药两用植物,具有抗肿瘤、抗肥胖、抗炎和维持血糖含量稳定等功能[10]。多孔莲子淀粉的吸附和消化特性得到显著改变,成为一种优良的负载材料(包埋材料)。LIN Y J等[11-12]研究了协同酶处理方法和湿热复合酶处理方法制备多孔淀粉,采用高温普鲁兰酶Pul-K25单酶加上超声辅助,方法简便,易于操控。 王琦等[13-14]制备的多孔莲子淀粉的吸水率、吸油率、溶解力和溶胀力都显著提高,显著改变了多孔莲子淀粉的特性。 淀粉颗粒溶解力和溶胀力的显著提高,有利于提高淀粉的持水性、糊化能力、透明度和消化性和营养吸收[15],提高了淀粉的品质。传统多孔淀粉制备多依赖中温α-淀粉酶或糖化酶,需在温和温度下长时间反应,效率低且易滋生杂菌[16]。此外,单一酶解难以精准控制淀粉孔结构,导致吸附性能不均衡[17]。高温普鲁兰酶能够特异性水解淀粉分子中的α-1,6-葡萄糖苷键,作用于淀粉颗粒的无定型区,不改变淀粉的晶体结构,制备成多孔淀粉。
本研究采用分子生物技术从新阿波罗栖热袍菌(Thermotoga neapolitana)KCCM 41025中克隆普鲁兰酶,在大肠杆菌(Escherichia coli)BL21感受态中冷休克诱导表达,对重组普鲁兰酶进行酶学性质分析。将其应用于多孔莲子淀粉的制备,通过扫描电子显微镜、傅里叶红外光谱及X射线衍射表征其结构,并对多孔莲子淀粉的特性进行研究,以期为制备多孔莲子淀粉提供一种新的方法。
1 材料与方法
1.1 材料与试剂
1.1.1 菌株和载体
新阿波罗栖热袍菌(Thermotoga neapolitana)KCCM 41025、大肠杆菌(Escherichia coli)DH5α、E. coli BL21、质粒表达载体pET28a(+):本实验室保存。
1.1.2 试剂
质粒小量抽提试剂盒、Protein Marker、脱氧核糖核酸(deoxyribonucleic acid,DNA)Marker:天根生化科技(北京)有限公司;Taq聚合酶链式反应(polymerase chain reaction,PCR)Master Mix、引物合成:生工生物工程(上海)股份有限公司;卡那霉素:上海阿拉丁生化科技有限公司;限制性内切酶XbaI和XhoI:美国NEB(New England Biolabs)公司;麦芽糖、葡萄糖、3,5-二硝基水杨酸(3,5-dinitrosalicylic acid,DNS)(均为分析纯):阿拉丁试剂(上海)有限公司。
1.1.3 培养基
LB(Luria-Bertani)液体培养基:1%蛋白胨,1%氯化钠,0.5%酵母粉。
LB固体培养基:LB液体培养基中添加1.5%琼脂。
含卡那霉素的LB液体培养基:1%蛋白胨,1%氯化钠,0.5%酵母粉,50 μg/mL卡那霉素。
含卡那霉素的LB平板:含卡那霉素的LB液体培养基中添加1.5%琼脂。
上述培养基灭菌条件均为121 ℃灭菌20 min。
1.2 仪器与设备
YXQ立式压力蒸汽灭菌锅:上海博迅实业有限公司;YXQ-LB-75SI全温振荡培养箱:上海欣蕊自动化设备有限公司;SW-CJ-1CU超净工作台:苏净集团苏州安泰空气技术有限公司;Centrifuge 5910Ri高速离心机:艾本德(中国)有限公司;T100TM PCR扩增仪、ChemiDocTM凝胶成像分析仪:美国Bio-Rad公司;SCIENTZ-IID超声波细胞破碎机:宁波新芝生物科技股份有限公司;Regulus8230扫描电子显微镜:日本日立公司;NicoletTMiS50傅里叶红外光谱仪、Multiskan SkyHigh全波长酶标仪:美国Thermo Fisher公司;X'PERT POWDER X-射线衍射仪(X-raydiffraction,XRD):荷兰PANalytical公司。
1.3 方法
1.3.1 基因组DNA提取
从Gen Bank 中检索Thermotoga neapolitana KCCM 41025的基因的序列,注册号为GenBank:FJ716701.1。采用SnapGene 8.1.0软件进行分子克隆设计,在目标序列5'和3'末端分别添加XbaI与XhoI限制性内切酶识别位点。经开放阅读框(open reading frame,ORF)完整性验证及蛋白编码正确性分析后,委托上海生工生物有限公司进行合成。
1.3.2 PCR扩增目的基因
对Pul-K25序列进行PCR扩增。将冻干的普鲁兰酶基因质粒(Pul-K25)以5 000×g离心2 min,加入20 μL无菌水充分溶解,静置2 min。取5 μL溶解质粒与50 μL冰上预冷的E.coli DH5α感受态细胞轻柔混匀,冰浴30 min。42 ℃水浴热激90 s后立即冰浴2~3 min,加入600 μL LB培养基,37 ℃、180 r/min振荡复苏培养1 h。 取50 μL菌液均匀涂布于含卡那霉素的LB平板,37 ℃倒置培养12 h至单菌落形成。 挑取单菌落接种至5 mL含卡那霉素LB液体培养基,37 ℃、180 r/min培养12 h后,取菌液进行PCR扩增。 PCR扩增体系:引物F(10 μmol/L)2 μL,引物R(10 μmol/L)2 μL,Pul-K25 DNA 1 μL,Taq PCR Master Mix 25 μL,无菌去离子水20 μL;PCR扩增条件:98℃、5min,98℃、10s,55℃、5s,72℃、1min,72℃、10 min,共34个循环。 PCR产物经1%琼脂糖凝胶电泳验证后,送上海生工生物有限公司进行测序分析。
1.3.3 重组质粒载体构建
采用限制性内切酶XbaI 和XhoI 对Pul-K25基因片段及pCold I表达载体进行双酶切(酶切体系:XbaI 1 μL,XhoI 1 μL,CutsmartBuffer 5 μL,DNA 5μL,无菌去离子水13 μL),37 ℃反应4 h以线性化载体并释放黏性末端。使用DNA纯化试剂盒回收酶切产物,通过T4 DNA连接酶(16 ℃连接12 h)将目的基因与载体定向连接。
取5 μL连接产物与100 μL E.coli DH5α感受态细胞冰浴混合30 min,42 ℃热激30 s后冰浴3 min。加入900 μL LB培养基,37 ℃、180 r/min复苏振荡培养1 h。 12 000×g离心2 min后弃900 μL上清,剩余菌体重悬并涂布于含卡那霉素的LB平板,37 ℃培养至单菌落形成。挑取单菌落扩增培养后,提取重组质粒并通过双酶切及测序验证插入序列正确性[15]。
1.3.4 重组普鲁兰酶基因的克隆与表达
设计引物并在上下游引物序列的5'端分别添加XbaI和XhoI两个酶切位点。T.neapolitana KCCM 41025的普鲁兰酶Pul-K25的基因序列(GenBank:FJ716701.1):F-GGATAACAATTCCCCTCTAGAATGAAGACCAGATTCTGGATCCTG,R-GTGGTGGTGGTGGTGCTCGAGTCATTCCCTGTACCAGAACGTAGGC。 将含有普鲁兰酶基因的质粒pCold I转化E.coli DH5α感受态细胞中,冰浴30 min,再42 ℃水浴热激90 s,然后快速转移到冰浴中放置2~3 min,向离心管中加入600 μL的LB液体培养基,37 ℃、180 r/min条件下振荡培养1.5 h,取菌液50 μL涂布含卡那霉素的LB平板上,37 ℃倒置培养12~16 h。 对菌株进行PCR扩增,PCR产物由上海生工生物有限公司测序验证。
挑取生长良好的单菌落至LB液体培养基中活化8 h得到种子液。以4%的接种量,接种种子液至终浓度100 mmol/L卡那霉素的抗性LB液体培养基中37 ℃、180 r/min条件下振荡培养,当培养液的OD600nm值达到0.6~0.8时,添加异丙基-β-D-硫代半乳吡喃糖苷(isopropyl-beta-D-thiogalactopyranoside,IPTG)至终浓度0.1~1.0 mmol/L,16 ℃、180 r/min条件下振荡培养48 h进行诱导表达。
将发酵液在4 ℃、1 000×g条件下离心15 min后弃去上清液加入适量磷酸盐缓冲液(phosphate buffer solution,PBS)混匀,继续离心10min,弃上清。重复上述步骤后,再次加入适量PBS并与沉淀混匀后,将混合物进行超声波破碎30min。在4 ℃、1 000×g条件下离心10 min后得到上清液即为粗酶液。
1.3.5 重组普鲁兰酶Pul-K25的测定
采用3,5-二硝基水杨酸(DNS)法测定普鲁兰酶活力[10]。
麦芽糖标准曲线的绘制:分别吸取0.2%标准麦芽糖液0、10μL、20 μL、40 μL、60 μL、80 μL、100 μL、120 μL、140 μL、160 μL、180 μL、200 μL,依次加入到试管中,补加蒸馏水至200 μL,配制成相应含量的麦芽糖标准溶液。加入等体积的DNS试剂,于沸水浴中煮沸5 min,取出后立即加入蒸馏水3 mL,混匀冷却后,取样在波长540 nm条件下测定吸光度值(OD540nm值)。以标准麦芽糖量(x)为横坐标,以对应的OD540nm值(y)为纵坐标,绘制标准曲线,得到麦芽糖标准曲线回归方程为y=1.024 13x+0.089 79,相关系数R2为0.996 2。
在试管中分别加入2%的高温普鲁兰糖和100 mmol/L的乙酸-乙酸钠缓冲液75 μL,在待测温度下预热5 min,然后加入50 μL酶液反应20 min,随后加入200 μL的DNS终止反应,将试管置于沸水中煮沸5 min,加入3 mL超纯水并混匀。以超纯水为对照,吸取200μL反应液在波长540nm下测定吸光度值。按照麦芽糖标准曲线回归方程计算普鲁兰酶酶活力。
普鲁兰酶活定义:每分钟催化普鲁兰酶生成1 μmol/L麦芽糖所需的酶量为一个酶活单位(U/mL)。
1.3.6 重组普鲁兰酶Pul-K25的酶学性质
最适作用温度:将酶液分别在40 ℃、50 ℃、60 ℃、70 ℃、80 ℃、90 ℃和100 ℃条件下水浴反应20 min后,加入200 μL DNS终止反应,于波长600 nm处测定吸光度值(OD600nm值)。以纯水为空白对照组,以最高酶活为100%,计算其他温度条件的相对酶活。
温度稳定性:将酶液分别在70 ℃、80 ℃和90 ℃条件下进行保温处理放置5 h,每1 h取样测定酶的残余酶活,以最高酶活为100%,计算其他温度条件的相对酶活。
最适作用pH:将酶液分别在pH 4.0~9.0条件下测定酶活性。选择3种缓冲液(覆盖pH 4.0~9.0的范围,大多数淀粉酶的最适pH通常在5.5~7.0,而某些耐酸酶可能在pH 4.5~5.5仍有活性,确保不遗漏酶的潜在最适pH区间),分别为50 mmol/L乙酸-乙酸钠缓冲液(pH 4.0~6.0)、50 mmol/L磷酸盐缓冲液(pH 5.0~7.0)和50 mmol/L盐酸-Tris缓冲液(pH 7.0~9.0)。以最高酶活为100%,计算其他pH条件的相对酶活。
pH稳定性:将酶液分别用缓冲液50 mmol/L乙酸-乙酸钠缓冲液、50 mmol/L磷酸盐缓冲液和50 mmol/L盐酸-Tris缓冲液配制,在该酶的最适温度下保温4 h,测定酶的残余酶活。以最高酶活为100%,计算其他pH条件的相对酶活。
通过三种缓冲液组合,覆盖pH 4.0~9.0的范围,大多数淀粉酶的最适pH通常在5.5~7.0,而某些耐酸酶可能在pH 4.5~5.5仍有活性,确保不遗漏酶的潜在最适pH区间覆盖目标pH范围,可确保实验设计的全面性,平衡缓冲能力与酶活性,避免成分干扰。
金属离子对酶活的影响[18]:将酶液中的金属离子Cu2+、K+、Mg2+、Na+、Ca2+、Fe2+、Zn2+的终浓度分别为1 mmol/L和5mmol/L。以最高酶活为100%,计算其他pH条件的相对酶活。
有机溶剂对酶活的影响[19]:将酶液中的吐温80、甲醇、曲拉通X-100、二甲基亚砜、乙醇、乙二胺四乙酸(ethylene diamine tetraacetic acid,EDTA)的终浓度分别为1 mmol/L。以最高酶活为100%,计算其他pH条件的相对酶活。
1.3.7 普鲁兰酶粗酶液的制备和多孔莲子淀粉的制备
鲁兰酶粗酶液的制备:发酵液在4 ℃、12 000×g离心15 min,弃去上清液,加入适量磷酸盐缓冲液(PBS)吹打混匀,12 000×g离心10 min,弃上清,重复上述操作3次。加入PBS与沉淀混匀后在冰浴中超声波破碎30 min。 在4 ℃、12 000×g离心15 min,上清液即为粗酶液,-20 ℃保存备用。
酶解法协同超声制备多孔莲子淀粉[20]:取1 g莲子淀粉,溶于10 mL pH 6.5,100 mmol/L的磷酸氢二钠-柠檬酸缓冲溶液中,加入10 mL酶液并在60 ℃下水浴中超声处理30 min。在60 ℃、180 r/min下分别振荡孵育0 h、6 h、12 h、18 h,迅速将样品置于冰水中终止反应。 加入50 mL去离子水,振荡混匀,然后在5 000×g离心20 min收集沉淀,重复上述步骤3次后,冷冻干燥多孔莲子淀粉,研磨后分装,4 ℃保存备用。
1.3.8 多孔莲子淀粉的结构表征
扫描电子显微镜(scanning electron microscope,SEM)检测:以天然莲子淀粉为对照,取多孔莲子淀粉样品和对照分别涂于导电带表面,覆盖金粉,用扫描电子显微镜观察样品形态,加速电压为50 kV。
傅里叶红外光谱(Fouriertransforminfrared,FTIR)检测:以天然莲子淀粉为对照,将多孔莲子淀粉样品和对照分别加入300%的溴化钾,充分研磨后压制成片,于傅里叶红外光谱仪中测定波数4 000~400 cm-1范围的透过率,扫描完成后扣除大气背景,观察峰的变化情况。
X射线衍射检测:以天然莲子淀粉为对照,使用X射线衍射仪检测多孔莲子淀粉粉末,设置为电压40 kV、电流40 mA、扫描测量范围2θ=0°~35°、扫描速度1°/min,获得X衍射图。计算结晶度[21],其计算公式如下:
式中:Ig为总衍射强度,J/cm2·s;In为非结晶相衍射强度,J/cm2·s。
1.3.9 多孔莲子淀粉的特性
吸水(油)率检测:称取0.05 g多孔莲子淀粉样品于10 mL离心管中,加入5 mL水(油)后涡旋混匀1 min,静置30 min后10 000×g离心8 min。弃上清后,将离心管倒置10 min后称质量。吸水(油)率计算公式[22]如下:
式中:W1表示多孔莲子淀粉的质量,g;W2表示离心管的质量,g;W3表示离心后多孔莲子淀粉和离心管的总质量,g。
溶解力与溶胀力测定[23]:将0.1 g天然莲子淀粉和多孔莲子淀粉分别置于10 mL去离子水中,充分混合,加入预称离心管质量。将装有样品的离心管在60 ℃、180 r/min条件下振荡培养30 min。12 000×g离心10 min,取上清加入新的预称质量离心管中。12 000×g离心10 min后,沉淀在110 ℃干燥过夜并称质量。溶解力和溶胀力计算公式如下:

1.3.10 数据处理
试验均设置3组平行,实验结果统计分析采用IBM SPSS Statistics 23.0,使用Origin 2018制图。
2 结果与分析
2.1 重组普鲁兰酶基因的克隆与表达
将重组高温普鲁兰酶Pul-K25基因的质粒转到E.coli DH5α感受态细胞中,挑取单菌落,进行菌液PCR,扩增完成后进行凝胶电泳检测,并送往上海生工生物有限公司进行测序,测序结果为基因长度为2 532 bp,蛋白质分子质量为96 kDa,与目的基因完全相同。将转入E.coli DH5α后提取的质粒重新转化到E.coli BL21感受态细胞中,并用PCR检测结果,结果见图1。由图1a可知,PCR扩增产物大小符合预期。由图1b和1c可知,酶切后条带单一说明酶切成功。将目的基因与质粒载体连接构建重组质粒。

图1 重组普鲁兰酶Pul-K25基因的克隆及表达
Fig.1 Cloning and expression of recombinant pullulanase Pul-K25 gene
(a)M为marker,泳道1为目的基因PCR扩增产物;(b)M为marker,泳道1为目的基因双酶切产物;(c)M为marker,泳道1为大肠杆菌BL21重组质粒双酶切产物。
2.2 重组普鲁兰酶Pul-K25的酶学性质
2.2.1 重组普鲁兰酶Pul-K25的最适作用温度及其温度稳定性
重组普鲁兰酶Pul-K25的最适作用温度及其温度稳定性结果图2。由图2a可知,作用温度为40~70 ℃时,重组普鲁兰酶Pul-K25的相对酶活随之升高;作用温度为70 ℃,重组普鲁兰酶Pul-K25的相对酶活最高;作用温度>70 ℃之后,普鲁兰酶Pul-K25的相对酶活随之下降。因此,重组普鲁兰酶Pul-K25的最适温度为70 ℃。 由图2b可知,在70 ℃和80 ℃条件下保温5 h,仍保留90%以上的酶活,90 ℃时2 h仍保留约50%活力。高温普鲁兰酶Pul-K25的热稳定性高,在80 ℃条件下5 h可保持90%酶活。
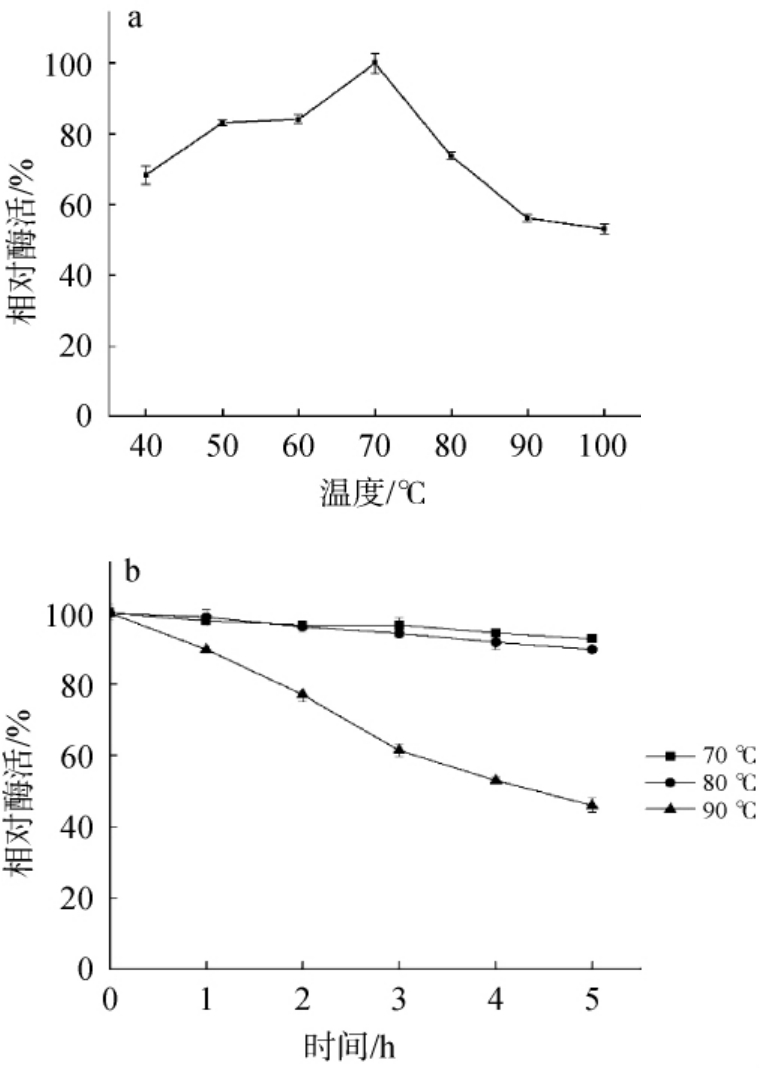
图2 重组普鲁兰酶Pul-K25最适作用温度(a)及温度稳定性(b)
Fig.2 Optimal reaction temperature (a) and temperature stability (b)of recombinant pullulanase Pul-K25
2.2.2 重组普鲁兰酶Pul-K25最适作用pH及pH稳定性
重组普鲁兰酶Pul-K25最适作用pH及pH稳定性结果见图3。由图3a可知,作用pH为4.0~6.0时,重组普鲁兰酶Pul-K25的相对酶活随之升高;作用pH为6.0时,重组普鲁兰酶Pul-K25的相对酶活最高;作用pH>6.0之后,重组普鲁兰酶Pul-K25的相对酶活随之下降。因此,该酶的最适作用pH为6.0。由图3b可知,在pH 4.0~9.0时,重组普鲁兰酶活均保留40%以上。在pH 7.0时稳定性最好,当pH值在4.0~9.0时,酶活均可保留60%以上。重组普鲁兰酶Pul-K25的pH稳定性也很高,在pH为4.0~9.0时,相对酶活均保持在60%以上。重组普鲁兰酶Pul-K25耐热耐酸碱的特性可以满足工业生产中的一些特殊要求,具有广阔的应用前景。
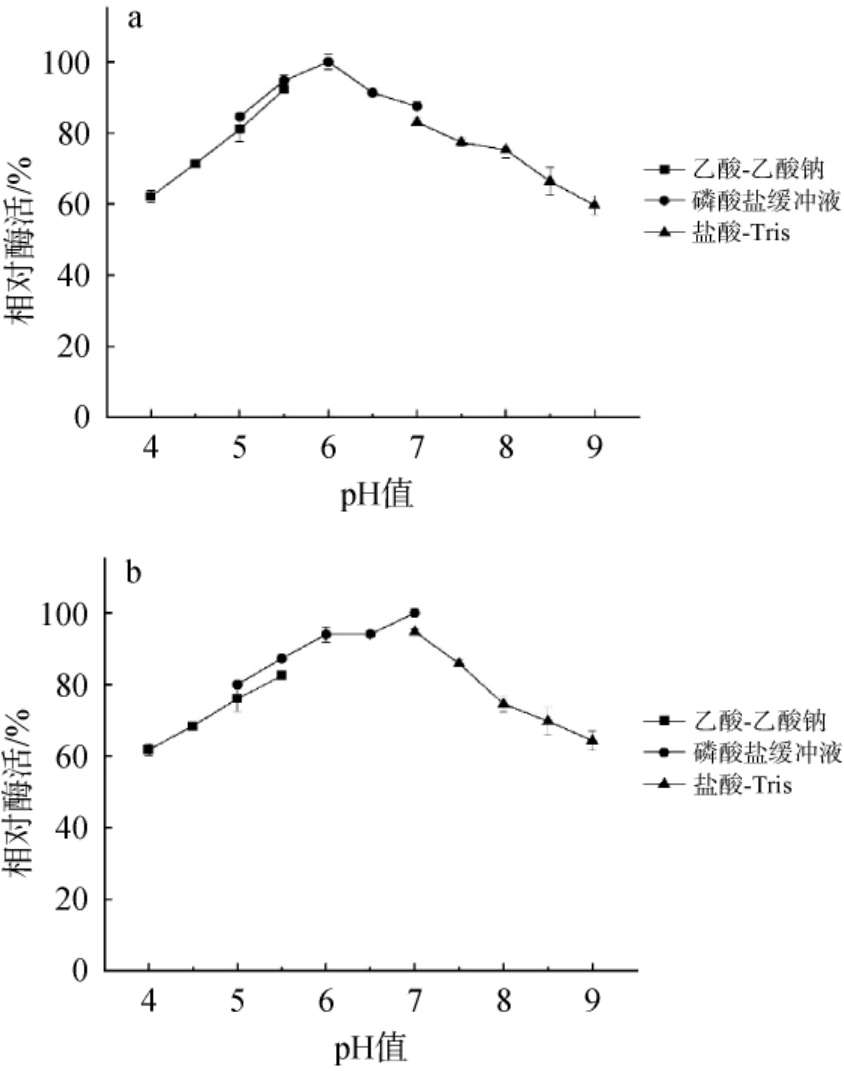
图3 重组普鲁兰酶Pul-K25的最适作用pH(a)及pH稳定性(b)
Fig.3 Optimal reaction pH (a) and pH stability (b) of recombinant pullulanase Pul-K25
2.2.3 金属离子及有机溶剂对重组普鲁兰酶Pul-K25活性的影响
金属离子及有机溶剂对重组普鲁兰酶Pul-K25活性的影响结果见图4。 由图4a可知,5 mmol/L的Fe2+、Zn2+对该酶具有显著的激活作用;而1 mmol/L Cu2+、K+、Mg2+、Na+、Ca2+对酶活有一定的抑制作用。由图4b可知,吐温80可以显著地提高该酶的活性;甲醇、曲拉通X-100、二甲基亚砜、乙醇、EDTA等对酶活的影响较小。
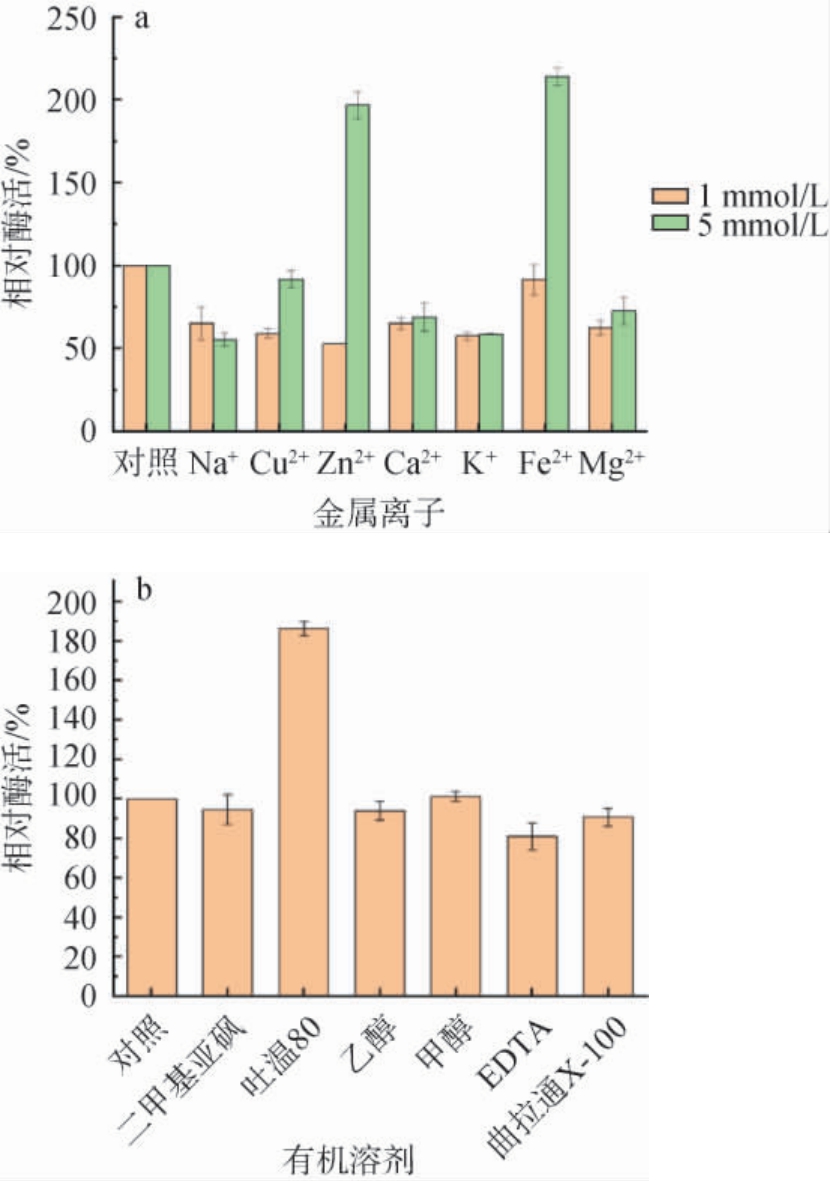
图4 金属离子(a)及有机溶剂(b)对重组普鲁兰酶Pul-K25酶活的影响
Fig.4 Effect of metal ions (a) and organic solvent (b) on the activities of recombinant pullulanase Pul-K25
2.3 多孔莲子淀粉的结构表征
2.3.1 扫描电镜检测
以天然莲子淀粉为对照,多孔莲子淀粉的扫描电镜检测结果见图5。由图5可知,天然莲子淀粉的表面光滑且无孔隙,酶解6 h、12 h、18 h的多孔莲子淀粉颗粒表面均出现孔隙,其中,重组普鲁兰酶Pul-K25酶解12 h的多孔莲子淀粉微观形态最佳,推测是淀粉中无定形非结晶区域的支链淀粉被酶水解[26]。该结构较为松散,首先会被酶水解,当无定形区域被完全水解后,可导致淀粉中该区域的坍塌,形成多孔形态。

图5 不同重组普鲁兰酶Pul-K25处理时间多孔莲子淀粉颗粒结构扫描电镜图
Fig.5 Scanning electron microscope of porous lotus seed starch granules with different treatment time of recombinant pullulanase Pul-K25
2.3.2 傅里叶红外光谱检测
以天然莲子淀粉为对照,多孔莲子淀粉的傅里叶红外光谱检测见图6。
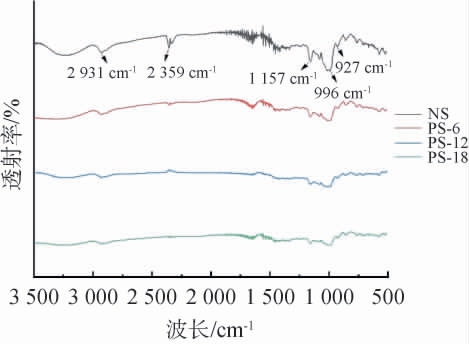
图6 不同重组普鲁兰酶Pul-K25处理多孔莲子淀粉的傅里叶红外光谱图
Fig.6 Fourier transform infrared spectroscopy of porous lotus seed starch with different treatment time of recombinant pullulanase Pul-K25
NS:天然莲子淀粉;PS-6、PS-12、PS-18:酶解6 h、12 h、18 h的多孔莲子淀粉。下同。
由图6可知,天然莲子粉红外波谱图在波数3 300~3 000 cm-1处出现较宽吸收峰,与分子内和分子间OH的拉伸振动有关[27]。波数2 359 cm-1处的尖峰与C-H的拉伸有关,通常在多糖的亚甲基中可以观察到。在天然莲子粉红外波谱图中波数500~1 200 cm-1范围中出现的特征峰通常归因于C-C和C-O间的拉伸振动[28]。淀粉的红外光谱衍射峰在波数1 100~900 cm-1的范围内十分敏感,通常淀粉的特征峰在这个范围内。 酶解前后的红外光谱在波数600~1 200 cm-1的范围显示出相似条带,表明普鲁兰酶Pul-K25处理的多孔莲子淀粉没有发生官能团的改变[29]。
2.3.3 X射线衍射及结晶度
以天然莲子淀粉为对照,多孔莲子淀粉在XRD衍射图见图7。由图7可知,在15°、17°、18°和23°均出现了衍射峰,表明天然莲子淀粉和多孔莲子淀粉结晶型均为A型,与大多数谷物类淀粉相同[30-31]。结果表明,天然莲子淀粉经过重组普鲁兰酶Pul-K25酶解后,晶体类型没有改变,酶解过程没有水解淀粉的结晶区域。
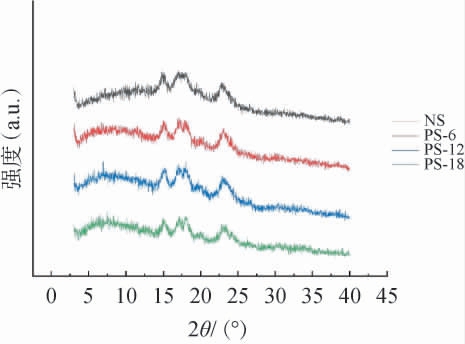
图7 不同重组普鲁兰酶Pul-K25酶解处理时间多孔莲子淀粉的X射线衍射图
Fig.7 X-ray diffraction pattern of porous lotus seed starch with different treatment time of recombinant pullulanase Pul-K25
根据XRD图谱计算非结晶区面积,结果见表1。由表1可知,与天然莲子淀粉比较,多孔莲子淀粉的结晶度显著提高(P<0.05),酶解12 h后结晶度提高了15%,表明酶解作用多发生在淀粉的无定形区[21]。多孔莲子淀粉的结晶度有所提高,孔洞的形成增加了酶与底物的接触面积,可能促进了更有效的脱支和水解;而结晶区的增强则提高了形成后的多孔骨架的稳定性。
表1 不同重组普鲁兰酶Pul-K25酶解处理时间多孔莲子淀粉的结晶度计算结果
Table 1 Calculation results of crystallinity of porous lotus seed starch with different treatment time of recombinant pullulanase Pul-K25
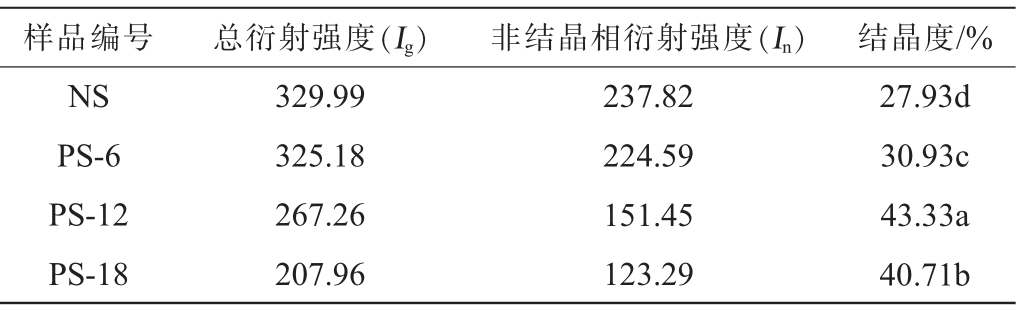
注:同一列内不同字母表示差异显著(P<0.05)。下同。
样品编号 总衍射强度(Ig) 非结晶相衍射强度(In) 结晶度/%NS PS-6 PS-12 PS-18 27.93d 30.93c 43.33a 40.71b 329.99 325.18 267.26 207.96 237.82 224.59 151.45 123.29
2.4 多孔莲子淀粉的特性
2.4.1 吸水率和吸油率测定
以天然莲子淀粉为对照,多孔莲子淀粉的吸水率和吸油率测定结果见表2。 由表2可知,多孔莲子淀粉酶解处理12 h后,其吸水率提升至123.03%,是天然莲子淀粉的1.91倍,吸油率提升至85.33%。 表明多孔莲子淀粉颗粒的比表面积显著增大,多孔结构使莲子淀粉的吸水和吸油率大幅提升。 其中,吸水率显著提高,表明多孔结构的表面为亲水基团[32-33]。
表2 多孔莲子淀粉的吸水率和吸油率测定结果
Table 2 Determination results of water and oil absorption rates of porous lotus seed starch
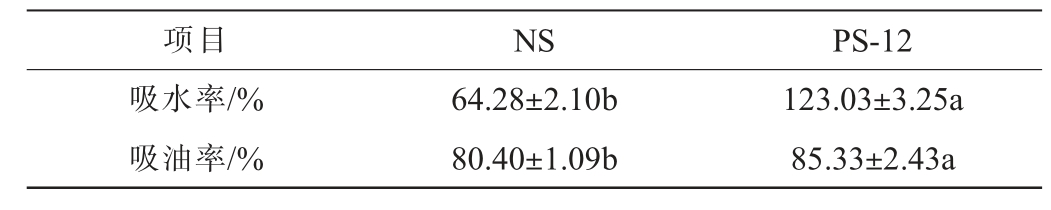
项目 NS PS-12吸水率/%吸油率/%64.28±2.10b 80.40±1.09b 123.03±3.25a 85.33±2.43a
2.4.2 溶解力和溶胀力测定
以天然莲子淀粉为对照,多孔莲子淀粉的溶解力和溶胀力测定结果见表3。 由表3可知,多孔莲子淀粉酶解处理12 h后,其溶解力和溶胀力相比于天然莲子淀粉均显著提高,其中,溶解力从1.93%提高到4.01%,溶胀力从2.08%提升至3.68%。 淀粉颗粒的完整性和淀粉链之间的相互作用是影响淀粉溶解力和溶胀力的重要因素。
表3 多孔莲子淀粉的溶解力和溶胀力测定结果
Table 3 Determination results of solubility and swelling power of porous lotus seed starch
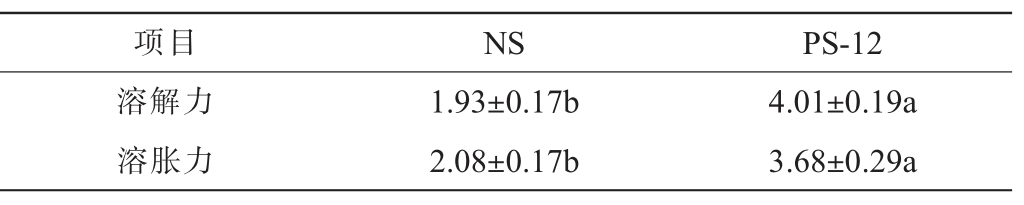
项目 NS PS-12溶解力溶胀力1.93±0.17b 2.08±0.17b 4.01±0.19a 3.68±0.29a
3 结论
本研究将古菌新阿波罗栖热袍菌(Thermotoga neapolitana)的普鲁兰酶Pul-K25基因克隆至宿主E.coli BL21中通过冷休克启动子的质粒pCold Ⅰ诱导成功表达,对重组普鲁兰酶进行酶学性质分析,并将其应用于多孔莲子淀粉的制备中,研究多孔莲子淀粉的特性。结果表明,得到重组普鲁兰酶Pul-K25基因长度为2 532 bp,编码834个氨基酸,分子质量为96 kDa;重组普鲁兰酶Pul-K25的最适作用温度为70 ℃,最适作用pH为6.0;5 mmol/L的Fe2+、Zn2+、吐温80对该酶具有显著的激活作用。在超声辅助下,重组普鲁兰酶Pul-K25酶解12 h的多孔莲子淀粉效果最佳,普鲁兰酶Pul-K25处理的多孔莲子淀粉没有发生官能团的变化,晶体类型没有改变,酶解12 h后结晶度提高了15%。 酶解法协同超声制备多孔莲子淀粉,使其吸水率由64.28%提高至123.03%,吸油率由80.40%提升至85.33%,溶解力由1.93%增至4.01%,溶胀力由2.08%提升至3.68%。 本研究结果为该酶制备的多孔莲子淀粉提供了实验依据。
[1]HENRISSAT B,BAIROCH A.New families in the classification of glycosyl hydrolases based on amino acid sequence similarities[J].Biochem J,1993,293(3):781.
[2]SINGH R S, KAUR N, RANA V, et al.Pullulan: A novel molecule for biomedical applications[J].Carbohydr Polym,2017,171:102-121.
[3]XIA W,ZHANG K,SU L,et al.Microbial starch debranching enzymes:Developments and applications[J].Biotechnol Adv,2021,50:107786.
[4]WANG X, NIE Y, XU Y.Industrially produced pullulanases with thermostability: Discovery,engineering,and heterologous expression[J].Biores Technol,2019,278:360-371.
[5]REN P F,DONG Q W,ZHOU C W,et al.Enhanced pullulanase production through expression system optimization and biofilm-immobilized fermentation strategies[J].Int J Biol Macromol,2025,297:139933.
[6]KANG J H, PARK K M, CHOI K H, et al.Molecular cloning and biochemical characterization of a heat-stable type I pullulanase from Thermotoga neapolitana[J].Enzyme Microb Tech,2011,48(3):260-266.
[7]王明道,邢岩,邱爽,等.极端嗜热菌Thermosipho melanesiensis普鲁兰酶基因的异源表达与酶学性质分析[J].信阳师范学院学报(自然科学版),2018,31(2):197-202.
[8]YI M X,TANG X C,LIANG S X, et al.Effect of microwave alone and microwave-assisted modification on the physicochemical properties of starch and its application in food[J].Food Chem,2024,446:138841.
[9]陶利,渠广民,李兆明,等.多孔淀粉在食品药品中的应用进展[J].食品与药品,2018,20(6):480-483.
[10]YU X J, WANG Y T, YAN X L, et al.Metabolomics combined with correlation analysis revealed the differences in antioxidant activities of lotus seeds with varied cultivars[J].Foods,2024,13(7):1084.
[11]LIN Y J,LIU L,LI L,et al.Properties and digestibility of a novel porous starch from lotus seed prepared via synergistic enzymatic treatment[J].Int J Biol Macromol,2022,194(1):144-152.
[12]XIE Y,LI M N,CHEN H Q,et al.Effects of the combination of repeated heat-moisture treatment and compound enzymes hydrolysis on the structural and physicochemical properties of porous wheat starch[J].Food Chem,2019,274:351-359.
[13]王琦.莲子抗性淀粉降血糖功效及其机理研究[D].福州:福建农林大学,2018.
[14]孙锦,关欣,寇宗亮,等.淀粉纳米颗粒的高效制备及吸附性能[J].食品与发酵工业,2019,45(9):108-116.
[15]CARCEA D M, ACQUISTUCCI D R.Isolation and physicochemical characterization of fonio (Digitaria exilis Stapf) starch[J].Starch-Stärke,1997,49(4):131-135.
[16]HII S L,TAN J S,LING T C,et al.Pullulanase:Role in starch hydrolysis and potential industrial applications[J].Enzyme Res,2012,2012(3):921362.
[17]ZHANG Y,et al.Heterologous expression and characterization of a novel pullulanase from Bacillus subtilis with high thermostability[J].J Agr Food Chem,2020,68(10):3126-3134.
[18]聂慧慧.嗜热普鲁兰酶基因的克隆表达及其酶学性质研究[D].郑州:河南农业大学,2017.
[19]GOLDFEDER M,FISHMA A.Modulating enzyme activity using ionic liquids or surfactants[J].Appl Microbiol Biot,2014,98(2):545-554.
[20]HAO Y,LIU M, NI H, et al.Preparation of sweet potato porous starch by marine dextranase and its adsorption characteristics[J].Foods,2024,13(4):549.
[21]陈福泉,张本山,卢海凤,等.X射线衍射在淀粉颗粒结晶度研究中的应用[J].食品科学,2010,31(3):284-287.
[22]JUNG Y S,LEE B H,YOO S H.Physical structure and absorption properties of tailor-made porous starch granules produced by selected amylolytic enzymes[J].Plos One,2017,12(7):1-14.
[23]ZHANG Q Q,XU C,CAO J Y,et al.Preparation and properties of rice porous starch by wet heat treatment-assisted enzymatic method[J].Chinese Journal of Cereals and Oils,2022,37(1):66-71.
[24]LIU S,REIMER M,AI Y.In vitro digestibility of different types of resistant starches under high-temperature cooking conditions[J].Food Hydrocol,2020,107:105927.
[25]白芸.不同种类及脱支处理对淀粉与脂质相互作用的影响研究[D].西安:陕西科技大学,2019.
[26]江佳妮,向贵元,邓佳宜,等.脂肪酸链长对高直链玉米淀粉—脂质复合物结构及理化性质的影响[J].食品与机械,2022,38(3):25-31.
[27]LIU D,TANG W, XIN Y, et al.Comparison on structure and physicochemical properties of starches from adzuki bean and dolichos bean[J].Food Hydrocol,2020,105:105784.
[28]GENG D H,ZHANG X J,ZHU C Y,et al.Structural,physicochemical and digestive properties of rice starch modified by preheating and pullulanase treatments[J].Carbohydr Polym,2023,313:120866.
[29]REDDY C K, HARIPRIY S, MOHAMED A N, et al.Preparation and characterization of resistant starch Ⅲfrom elephant foot yam (Amorphophallus paeonifolius)starch[J].Food Chem,2014,155:38-44.
[30]ASHWAR B A,GANI A,WANI I A,et al.Production of resistant starch from rice by dual autoclaving-retrogradation treatment: In vitro digestibility,thermal and structural characterization[J].Food Hydrocol,2016,56:108-117.
[31]HAAROS M,PEEREZ O E,ROSELL C M.Effect of steeping com with lactic acid on starch properties[J].Cereal Chem,2004,81(1):10-14.
[32]KIM D L, LEE H A, CHE J J, et al.Formation, characterization, and glucose response in mice to rice starch with low digestibility produced by citric acid treatment[J].J Cereal Sci,2007,45(1):24-33.