在清香型白酒的酿造过程中,酵母菌的主要作用包括酒精发酵和风味物质的生成。 通过糖酵解途径,酵母菌将可发酵性糖(如葡萄糖)转化为乙醇和二氧化碳,为白酒提供酒精基础。产酯酵母是一类能够高效合成酯类化合物的酵母菌,主要包括酿酒酵母和非酿酒酵母,广泛应用于白酒、啤酒和葡萄酒的酿造中,通过其代谢活动生成的酯类化合物是清香型白酒风味物质的核心组成部分[1]。这些酵母菌通过代谢活动生成乙酸乙酯、乳酸乙酯、己酸乙酯等关键风味物质,赋予酒类独特的果香、花香和奶香等香气特征。 例如使用产酯酵母酿造的猕猴桃酒,兼具原果香味及酒香,酸甜可口,醇厚纯净[2];而将其运用在青稞酒的酿造中,则使得原酒更加协调,清香纯正、突出[3]。由此可得,产酯酵母对于塑造酒体风格起着至关重要的作用。然而多数产酯酵母在乙醇体积分数超过6%~9%时生长显著受抑[4],而葡萄酒发酵后期乙醇体积分数集中在11%~13.5%。然而,目前针对高乙醇胁迫下菌株存活率的研究仍不充分,限制了其在实际酿造过程中的应用潜力[5]。
本研究立足于葡萄酒产业的发展趋势和市场需求,针对全球气候变化引起的酿酒葡萄果实成熟速度加快,糖分含量提高,酸味下降,风味物质较为寡淡等关键问题[6]。通过从清香型白酒大曲中分离并筛选耐乙醇、耐高温的高产酯酵母,采用单因素试验结合Box-Behnken响应面法对其培养基组成进行优化,将其接种于葡萄汁中进行发酵制备葡萄酒,从而优化葡萄酒的风味。基于响应面法的培养条件优化建立培养基碳氮比、微量元素配比的动态优化模型,突破传统菌株在极端发酵环境中的活性瓶颈,为产酯酵母在葡萄酒酿造中的应用提供理论参考。
1 材料与方法
1.1 材料与试剂
1.1.1 材料
大曲:山西汾阳市某清香型白酒公司;鲁氏结合酵母(Zygosaccharomyces rouxii)A7:安琪酵母股份有限公司;异常毕赤酵母(Pichia anomalus)J7(为已知高产酯酵母):实验室保藏;高粱:山西冠丰高粱有限公司。
1.1.2 试剂
无水葡萄糖、蔗糖、乳糖、甘露糖、麦芽糖、半乳糖(均为分析纯)、琼脂粉、蛋白胨、酵母浸粉、牛肉浸粉(均为生化试剂):天津市福晨化学试剂厂;胰蛋白胨、酵母提取物(生化试剂):美国Thermo Fisher Scientific公司;无水乙醇、盐酸羟胺、氢氧化钠、浓盐酸、硫酸铵、硫酸锌、硫酸镁(均为分析纯):天津市北方天医化学试剂厂;氯化钠、三氯化铁、硝酸锰、磷酸二氢钾、乙酸乙酯、碳酸钙、硫酸锰、硫酸二氢铵(均为分析纯):天津市康科德科技有限公司。
1.1.3 培养基
酵母浸出粉胨葡萄糖(yeast peptone dextrose,YPD)培养基:葡萄糖2%,蛋白胨2%,酵母浸粉1%,琼脂2.5%。115 ℃高压灭菌20 min。
马铃薯葡萄糖琼脂(potato dextrose agar,PDA)培养基:马铃薯浸粉0.6%,葡萄糖2%,琼脂2.5%。121 ℃高压灭菌20 min。
三丁酸甘油酯透明圈培养基:马铃薯浸粉0.6%,葡萄糖2%,琼脂2.5%,加入20 mL乳化液(乳化液为9 mL 3 g/100 mL聚乙烯醇和1 mL三丁酸甘油酯混合,振荡混匀)。121 ℃高压灭菌20 min。
高粱汁培养基(发酵培养基):将高粱原料用粉碎机粉碎后准确称取10 g于250 mL三角瓶中,加入适量冷水(约20 mL)润湿即可,置于电炉上,立即倒入180 mL沸水,不断搅拌使其糊化。121 ℃高压灭菌20 min。
马铃薯葡萄糖肉汤(potato dextrose broth,PDB)培养基:马铃薯浸粉0.6%,葡萄糖2%。121 ℃高压灭菌20 min。
酵母氮源基础(yeast nitrogen base,YNB)培养基:北京奥博星生物技术有限责任公司。
1.2 仪器与设备
ZHJH-C1112B型超净工作台:上海智诚分析仪器制造公司:GB204型电子分析天平:上海精密仪器仪表有限公司;DZKW-C型电子恒温水浴锅:河北黄骅市航空仪器厂;UV-1500全波长酶标仪:美国Thermo Fisher Scientific公司;YXQ-LS-50SII型高压蒸汽灭菌锅:上海博讯实业有限公司;TGL-16B型高速台式离心机:上海安亭科学仪器;ETS-D5型磁力搅拌加热装置:德国IKA公司;S20K型pH计:上海梅特勒-托利多仪器有限公司;UVmini-1240紫外分光光度计:苏州岛津仪器有限公司;BIOSCREEN C PRO微生物生长曲线自动分析仪:芬兰Bioscreen公司;HYG-W1型回旋式恒温调速摇瓶柜:上海欣蕊自动化设备有限公司;H2500R型低温高速离心机;湖南湘仪实验室仪器开发有限公司。
1.3 方法
1.3.1 清香型白酒大曲中酵母的分离、筛选与鉴定
(1)菌株的分离
使用分析天平称取(2.00±0.01)g清香型白酒大曲样品。将样品转移至锥形瓶中,加入100 mL经灭菌的0.85%生理盐水。将锥形瓶置于恒温摇床中,30 ℃、150 r/min振荡培养30 min,使大曲充分分散,制备成20 mg/mL的菌悬液。使用移液枪吸取0.2 mL制备好的大曲菌悬液,分别接种于PDA和YPD平板培养基表面。 采用涂布法,将菌悬液均匀涂布于整个培养基表面[7],每个培养基设置3个平行样。
(2)菌株的筛选
产酯酵母能够分泌酯酶,将三丁酸甘油酯水解生成丁酸,丁酸与培养基中的钙离子反应生成不溶于水的丁酸钙,在菌落周围形成透明圈。 通过观察透明圈的大小,可以初步判断酵母菌株的产酯能力[8-9]。将待测酵母菌株接种至含三丁酸甘油酯的平板培养基上,每个平板可接种3~5个菌株。30 ℃恒温培养24 h。观察菌落周围是否出现透明圈,出现透明圈即为产酯酵母。 根据透明圈直径(D)与菌落直径(d)的比值(D/d)筛选高产的菌株。
(3)菌株的鉴定
生理生化试验:将接种后的平板倒置于30 ℃恒温培养箱中培养48~72 h,观察菌落生长情况并记录[10]。挑取疑似酵母菌落进行革兰氏染色镜检。 酵母菌为革兰氏阳性,细胞呈圆形或椭圆形,可见出芽生殖现象[11]。
分子生物学鉴定:对目标菌株的ITS-26S rDNA区域(ITS1+5.8S+ITS2+26S D1/D2)进行扩增及高通量测序后,将获得的序列数据提交至美国国家生物技术信息中心(national center for biotechnology information,NCBI)的GenBank数据库进行注册。利用NCBI的基本局部序列比对算法的搜索工具(basic local alignmentsearch tool,BLAST)算法对核苷酸序列进行同源性比对分析,筛选出具有显著相似性的模式菌株。
1.3.2 酵母菌性能评价
(1)产酯性能评价
乙酸乙酯在碱性条件下与羟胺反应生成羟肟酸[12],羟肟酸与三价铁离子反应生成红棕色络合物,该络合物在520 nm波长处有最大吸收峰,通过测定吸光度值(optical density,OD)可定量分析乙酸乙酯含量。 将不同酵母菌株接种于YPD斜面培养基,30 ℃培养48 h活化。将活化后的菌株接种于YPD液体培养基中,30 ℃、200 r/min振荡培养24 h。以5%的接种量将菌液接入50 mL高粱汁培养基中,30 ℃静置培养7 d。发酵结束后,取5 mL发酵液,8 000 r/min离心10 min,收集上清液。以乙酸乙酯标准溶液质量浓度(x)为横坐标,吸光度值(y)为纵坐标绘制乙酸乙酯标准曲线[13],并根据乙酸乙酯标准曲线回归方程y=0.001 93+0.222 79x,相关系数R2=0.993 31,计算样品中乙酸乙酯含量[14]。
(2)耐受性评价
乙醇耐受性:将不同酵母菌株接种于YPD斜面培养基,30 ℃培养48 h活化。将活化后的菌株接种于YPD液体培养基中,30 ℃、200 r/min振荡培养24 h。 配制乙醇体积分数分别为0、3%、6%、9%、12%、15%的YPD液体培养基[15]。 每个乙醇体积分数设置3个平行样。以5%(V/V)的接种量将活化后的菌液接入不同乙醇体积分数的YPD液体培养基中。30 ℃、200 r/min振荡培养48 h。 以无菌YPD培养基为空白对照,测定600 nm波长处的吸光度值,比较不同菌株的乙醇耐受性[16]。
温度耐受性:挑取单菌落接种于YPD液体培养基,30℃、120 r/min振荡培养24 h至对数生长期。以5%(V/V)接种量将菌悬液接入YPD液体培养基中,设置培养温度分别为25℃、30 ℃、35 ℃、40 ℃,每个温度设置3个重复。将接种后的培养基于相应温度、200 r/min条件下恒温振荡培养24 h。以无菌YPD培养基为空白对照,测定600 nm波长处的吸光度值,比较不同菌株的温度耐受性。
1.3.3 高产乙酸乙酯酵母发酵培养基优化
单因素试验:制备无碳源的YNB培养基、无氮源的基础培养基和不含无机盐离子的基础培养基。分别考察添加量均为2%碳源种类(麦芽糖、蔗糖、乳糖、葡萄糖、甘露糖、半乳糖)、最佳碳源添加量(2%、3%、4%、5%、6%、7%、8%)、添加量均为2%氮源种类(酵母浸粉、氯化铵、硫酸铵、硫酸二氢铵、牛肉浸粉)、最佳氮源添加量(1%、2%、3%、4%、5%、6%、7%)、添加量均为0.2%无机盐种类(硫酸锌、硫酸镁、硝酸锰、磷酸二氢钾、碳酸钙)、最佳无机盐添加量(0.1%、0.2%、0.3%、0.4%、0.5%、0.6%、0.7%)对酵母发酵的影响。将产酯酵母接种至YPD培养基中,30 ℃、200 r/min振荡培养24 h,使菌体达到对数生长期。将稀释后的菌液分别接种至相应的培养基中,接种量为1%(V/V)。将接种后的培养基置于恒温摇床中,30 ℃、200 r/min振荡培养24 h,测定培养液的OD600 nm值,以无菌培养基为空白对照。
响应面试验:选择对酵母生长影响显著的因素(碳源添加量、氮源添加量、无机盐离子添加量)作为试验考察因素。基于前期单因素试验的结果,使用响应面法中的Box-Behnken设计为每个因素设定3个水平(低、中、高)。 使用统计软件对试验数据进行分析[17-18],拟合二次回归模型,评估各因素及其交互作用对产酯酵母生长的影响。
1.3.4 酵母菌剂的应用分析
菌剂RW的制备:将活化后的菌株A7以2%接种量接入YPD培养基,30 ℃、200 r/min振荡培养24 h,得新鲜菌液;随后将菌液置于4 ℃、6 000 r/min离心5 min,弃上清收集菌泥;向菌泥中加入等体积冻干保护剂(海藻糖10%、脱脂乳粉10%、甘油2%),充分混匀制成菌悬液;再将菌悬液分装于无菌冻干瓶,在-40 ℃、10 Pa真空度下冻干24 h,即得存活率≥84.6%、活菌数≥9.4×108 CFU/g的RW菌剂。
以无添加鲜榨赤霞珠葡萄汁(总糖22.5°Brix,pH为3.8)为发酵基质[19]。 实验组接种2%筛选酵母的菌悬液(菌体密度2×108CFU/mL),对照组等量添加菌株A7所制备菌剂(RW),考察不同组别的发酵效果。 采用葡萄酒三段式发酵程序:1~3 d,以温度(16±0.5) ℃启动;4~7 d缓升至(20±0.5) ℃主发酵;8~14 d降至(14±0.5)℃保香并促进酯合成。同时设置50 r/min间歇搅拌程序(每2 h运行10 min)以维持溶氧均匀性。通过数字折光仪动态监测发酵液糖度,当残糖≤4°Brix时立即降温至8 ℃终止发酵[20]。
1.3.5 挥发性风味物质检测
挥发性风味物质分析采用顶空固相微萃取-气相色谱质谱联用技术[21]。
样品前处理:取5mL发酵液样品,加入1g氯化钠与10μL 4-甲基-2-戊醇内标溶液(50 mg/L),于40 ℃恒温水浴平衡30 min后,采用50/30 μm DVB/CAR/PDMS复合萃取头(美国Supelco)在50 ℃条件下吸附40 min完成挥发性物质富集。
气相色谱条件:分离使用Agilent DB-WAX极性色谱柱(60 m×0.25 mm×0.25 μm),载气为高纯氦气(He)[22],流速1.0 mL/min,程序升温设置为:初始温度40 ℃保持3 min,以4 ℃/min速率升至230 ℃并维持10 min。
质谱条件:采用电子电离(electron ionization,EI)源,电子能量70 eV;离子源温度230 ℃,传输线温度250 ℃;四极杆温度250 ℃;溶剂延迟4.5 min;质量扫描范围35~450 m/z,采集速率3.2 scan/s。
定性定量:定性分析依据美国国家标准与技术研究院(National Institute of Standards and Technology,NIST)17质谱库进行匹配(相似度>85%),采用内标法进行定量分析[23]。
1.3.6 数据处理
采用Geneious、Design-Expert 13.0软件对数据进行分析处理,使用Origin进行数据分析和图表绘制。 实验数据结果用“平均值±标准差”来表示,显著性差异的准则是P<0.05。
2 结果与分析
2.1 酵母的筛选结果
2.1.1 产酯酵母的分离与初筛
所分离的96株酵母菌株中有24株均表现出不同程度的酯酶活性[24],其D/d值汇总结果见表1。由表1可知,24株菌的D/d值分布范围为1.75至4.47,菌株031354表现出最高的酯酶活性,其D/d值达到(4.47±0.12);其次为菌株021233和120752,D/d值分别为(4.41±0.15)和(4.23±0.18)。 从整体分布来看,其中14株菌株D/d值超过3.0,表明这些菌株具有较高的产酯潜力。
表1 产酯酵母的D/d值汇总
Table 1 Summary of D/d values for ester-producing yeasts
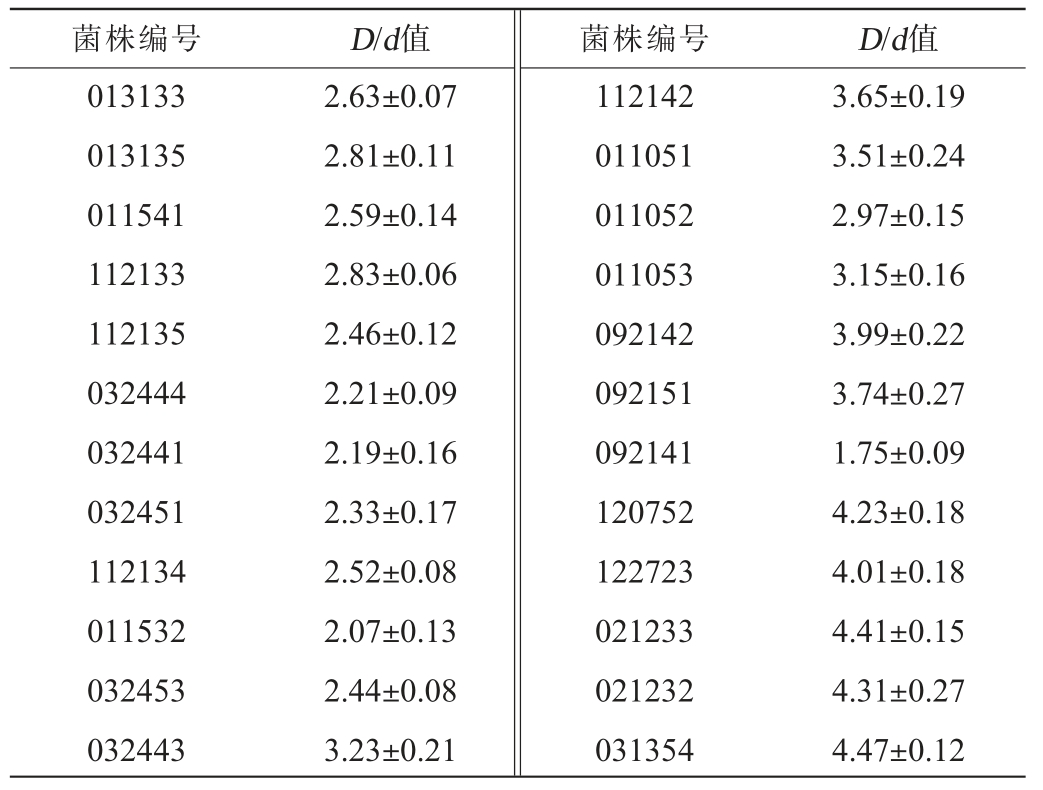
菌株编码规则为:月份+日期+组别+个数。 例如:013133为1月
31日筛出的第3组的第3个;112133为11月21日筛选出的第3组的第3个。
菌株编号 D/d值 菌株编号 D/d值013133 013135 011541 112133 112135 032444 032441 032451 112134 011532 032453 032443 3.65±0.19 3.51±0.24 2.97±0.15 3.15±0.16 3.99±0.22 3.74±0.27 1.75±0.09 4.23±0.18 4.01±0.18 4.41±0.15 4.31±0.27 4.47±0.12 2.63±0.07 2.81±0.11 2.59±0.14 2.83±0.06 2.46±0.12 2.21±0.09 2.19±0.16 2.33±0.17 2.52±0.08 2.07±0.13 2.44±0.08 3.23±0.21 112142 011051 011052 011053 092142 092151 092141 120752 122723 021233 021232 031354
2.1.2 产酯酵母的复筛
对筛选出的14株产酯酵母的乙酸乙酯产量进一步测定,结果见表2。由表2可知,各菌株的乙酸乙酯产量呈现明显差异,其产量范围为0.77~1.80 g/L。 筛选出的5株高产乙酸乙酯酵母分别为:菌株031354(1.80 g/L)、菌株120752(1.69 g/L)、菌株021232(1.59 g/L)、菌株021233(1.39 g/L)和菌株122723(1.37 g/L)。 这些菌株的乙酸乙酯产量显著高于已知高产乙酸乙酯菌株J7(1.30 g/L)(P<0.05)。
表2 筛选酵母菌株的乙酸乙酯产量
Table 2 Production of ethyl acetate by screened yeast strains g/L
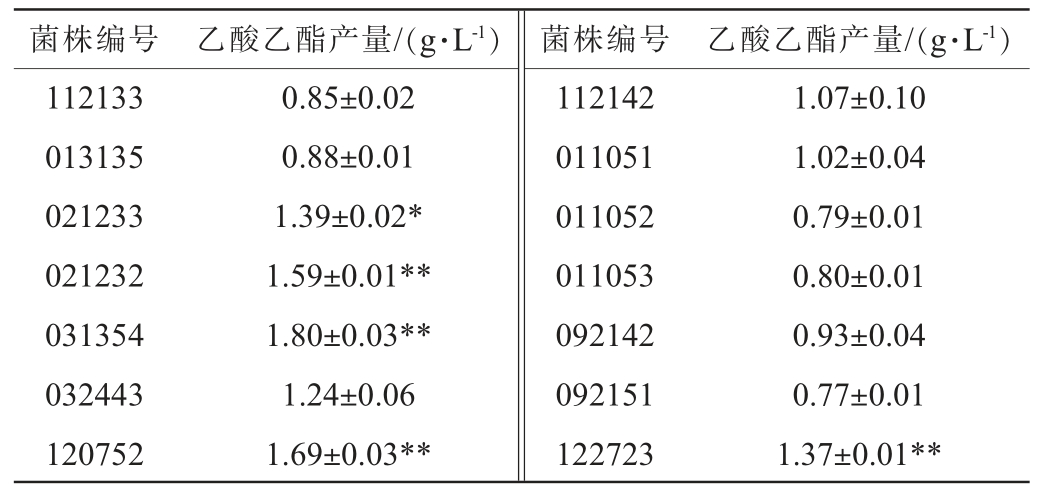
注:“*”代表与对照菌株J7相比差异显著,0.01<P<0.05;“**”代表与对照菌株J7相比差异极显著,0.001<P<0.01。
菌株编号 乙酸乙酯产量/(g·L-1) 菌株编号 乙酸乙酯产量/(g·L-1)112133 013135 021233 021232 031354 032443 120752 0.85±0.02 0.88±0.01 1.39±0.02*1.59±0.01**1.80±0.03**1.24±0.06 1.69±0.03**1.07±0.10 1.02±0.04 0.79±0.01 0.80±0.01 0.93±0.04 0.77±0.01 1.37±0.01**112142 011051 011052 011053 092142 092151 122723
2.2 酵母菌耐受性评价
2.2.1 产酯酵母对乙醇的耐受性
对五株高产酯酵母进行了系统的耐酒精性能测试[25],通过测定不同乙醇体积分数(0~18%)的OD600 nm值来评估各菌株的乙醇耐受性,结果见图1。 由图1可知,基于乙醇体积分数9%条件下OD600nm值高于0.300,且在乙醇体积分数15%下仍能保持一定生长能力(OD600 nm>0.100)的菌株的筛选标准[26],筛选出两株具有优异乙醇耐受性的产酯酵母021233和120752。菌株021233表现出最强的乙醇耐受性,在乙醇体积分数12%下,其OD600nm值仍达到(0.372±0.024),显示出卓越的耐受性能。菌株120752在乙醇体积分数12%下仍能维持(0.109±0.011)的生长水平,表明其具有良好的乙醇适应性。因此菌株021233和120752的乙醇耐受性能较好。
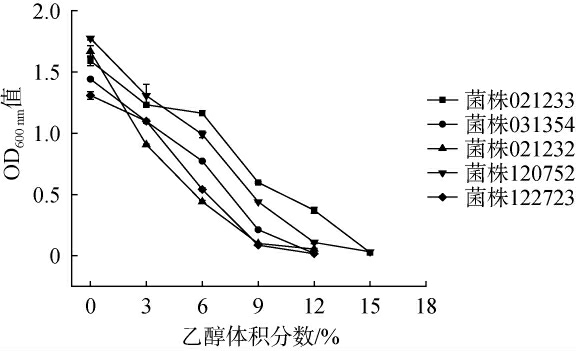
图1 不同产酯酵母对乙醇的耐受性结果
Fig.1 Results of alcohol tolerance of different ester-producing strains
2.2.2 产酯酵母对温度的耐受性
对2.2.1选出的两株产酯酵母(120752和021233)进行了耐温环境下的产酯性能测试,并以市售产酯酵母A7作为对比菌株。 通过测定不同温度(25~40 ℃)下的OD600 nm值,评估各菌株在不同温度范围内的生长性能,结果见图2。
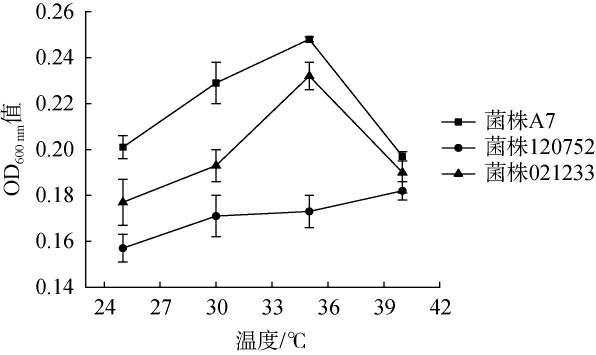
图2 不同产酯酵母对温度的耐受性结果
Fig.2 Results of temperature tolerance of different ester-producing strains
由图2可知,基于菌株在高温(35~40 ℃)环境下生长稳定性(标准偏差低)更好的筛选标准[27]。 筛选出一株在耐温环境中产酯潜力更高的菌株021233,该菌株在35 ℃条件下的OD600nm值达到0.232±0.006,明显高于菌株120752(0.173±0.007), 表明其在高温环境下具有更高的生物量积累能力[28]。此外,菌株021233在40 ℃下OD600nm值仍能达到0.19±0.009,进一步证明了其在高温环境下的适应性和产酯潜力。 因此选择菌株021233进行后续研究。
2.3 酵母菌的分子生物学鉴定结果
采用MEGA-X软件包中的最大似然法(maximum likelihood,ML)对拼接后的ITS-26S rDNA序列(ITS1-5.8S-ITS2-26SD1/D2)进行多序列比对并构建系统发育树,通过1000次bootstrap重复验证分支节点置信度。 基于ITS-26S rDNA联合序列构建的菌株021233系统发育树见图3。 由图3可知,菌株021233与扣囊复膜酵母(Saccharomycopsis fibuligera)模式菌株MW165540.1聚于同一高支持率分支(bootstrap=100%),且与该种内参考菌株Sf1序列完全一致,从而菌株021233被鉴定为扣囊复膜酵母(Saccharomycopsis fibuligera)。

图3 基于ITS-26S rDNA基因序列菌株021233的系统发育树
Fig.3 Phylogenetic tree of strain 021233 based on ITS-26S rDNA gene sequence
2.4 发酵培养基优化
2.4.1 碳源对酵母生长的影响
考察不同碳源种类对产酯酵母021233的生物量积累的影响,结果见图4。由图4可知,以葡萄糖作为碳源时,菌株021233的OD600nm值达到2.990±0.115,高于其他碳源,表明其对菌体生长的促进作用效果最佳,适合作为碳源用于菌体培养。
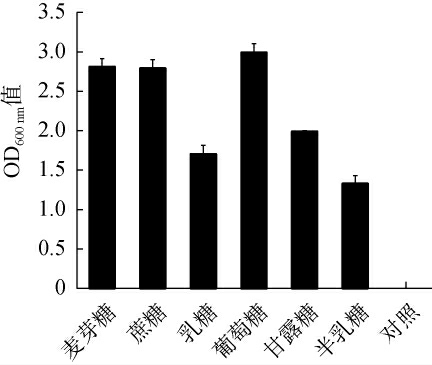
图4 不同碳源对菌株021233生长的影响
Fig.4 Effect of different carbon sources on the growth of strain 021233
考察了葡萄糖添加量(2%~8%)对产酯酵母021233生长的影响,结果见图5。由图5可知,菌体生物量(OD600nm值)随葡萄糖添加量升高而逐渐增加,从葡萄糖添加量2%时的2.697逐步提升至8%时的3.065,但增速明显减缓,通过变异系数(coefficient of variation,CV)评估实验重复性可知,葡萄糖添加量5%时表现突出:OD600 nm值达3.02,标准差仅0.006(CV=0.20%),兼具高生长量与高重复性。因此最佳葡萄糖添加量为5%。
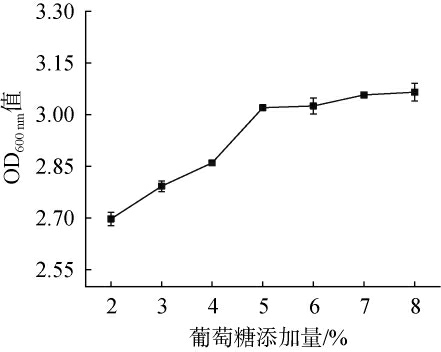
图5 葡萄糖添加量对菌株021233生长的影响
Fig.5 Effect of glucose addition on the growth of strain 021233
2.4.2 氮源对酵母生长的影响
考察不同氮源种类对产酯酵母021233的生物量积累的影响,结果见图6。由图6可知,酵母浸粉作为氮源的菌体生物量(OD600 nm值=2.611)优于其他氮源,其次为硫酸二氢铵和硫酸铵,表明其对菌体生长的促进作用效果最佳,因此选择酵母浸粉为最佳氮源。
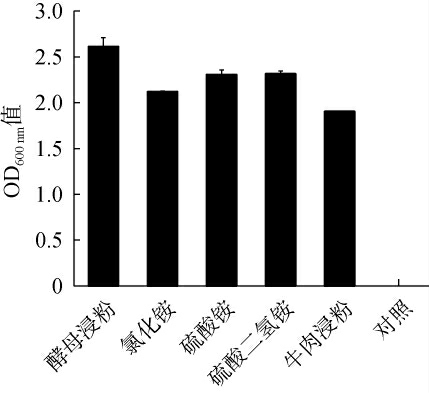
图6 不同氮源对菌株021233生长的影响
Fig.6 Effect of different nitrogen sources on the growth of strain 021233
考察了酵母浸粉添加量(1%~7%)对产酯酵母021233生长的影响,结果见图7。 由图7可知,菌体生物量(OD600 nm值)随酵母浸粉添加量增加而先升高后降低,其中添加量2%时菌体生物量最高(OD600 nm值=3.734),而添加量7%时生长抑制最明显(OD600nm值=1.188)。因此最佳酵母浸粉添加量为2%。
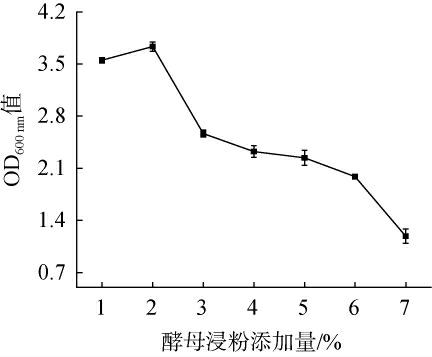
图7 酵母浸粉添加量对菌株021233生长的影响
Fig.7 Effect of yeast extract addition on the growth of strain 021233
2.4.3 无机盐对酵母生长的影响
酵母生长受无机盐种类、添加量及相互作用的协同调控,因此考察不同无机盐种类对产酯酵母021233生长的影响,结果见图8。 由图8可知,硫酸镁组菌体生物量(OD600 nm值=4.022)优于其他组,较对照组(OD600 nm值=3.311)提升21.5%。 碳酸钙(OD600 nm值=3.781)与磷酸二氢钾(OD600 nm值=3.321)次之,而硝酸锰组生长量最低(OD600nm值=3.085)。通过CV评估实验重复性:对照组稳定性最佳:CV=0.73%,表明基础培养基条件稳定;硫酸镁综合表现最优,因此选择最佳无机盐为硫酸镁。
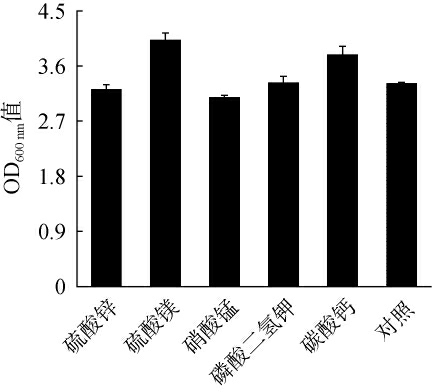
图8 不同无机盐对菌株021233生长的影响
Fig.8 Effect of different inorganic salts on the growth of strain 021233
考察不同硫酸镁添加量(0.1%~0.7%)对产酯酵母021233生长的影响,结果见图9。 由图9可知,当硫酸镁添加量在0.1%到0.5%范围内,酵母平均生物量维持在较高水平(OD600nm值=4.31~4.53),其中硫酸镁添加量为0.2%时获得最大生物量(OD600nm值=4.53±0.14)。值得注意的是,当硫酸镁添加量超过0.6%后,生物量呈现断崖式下降(OD600nm值=1.64~1.76),表明高盐环境已产生明显抑制作用。因此最佳硫酸镁添加量为0.2%。
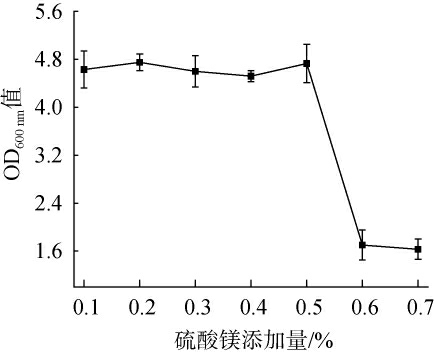
图9 硫酸镁添加量对菌株021233生长的影响
Fig.9 Effect of inorganic salt addition on the growth of strain 021233
2.5 培养基配方优化响应面试验
在单因素试验的基础上,采用响应面法优化产酯酵母021233的培养条件[29],考察葡萄糖添加量(A)、酵母浸粉添加量(B)和硫酸镁添加量(C)3个关键因素对菌体生长(OD600nm值)的影响,响应面试验结果与分析见表3,方差分析见表4。
表3 培养基配方优化响应面试验设计与结果
Table 3 Design and results of response surface methodology for culture medium formula optimization
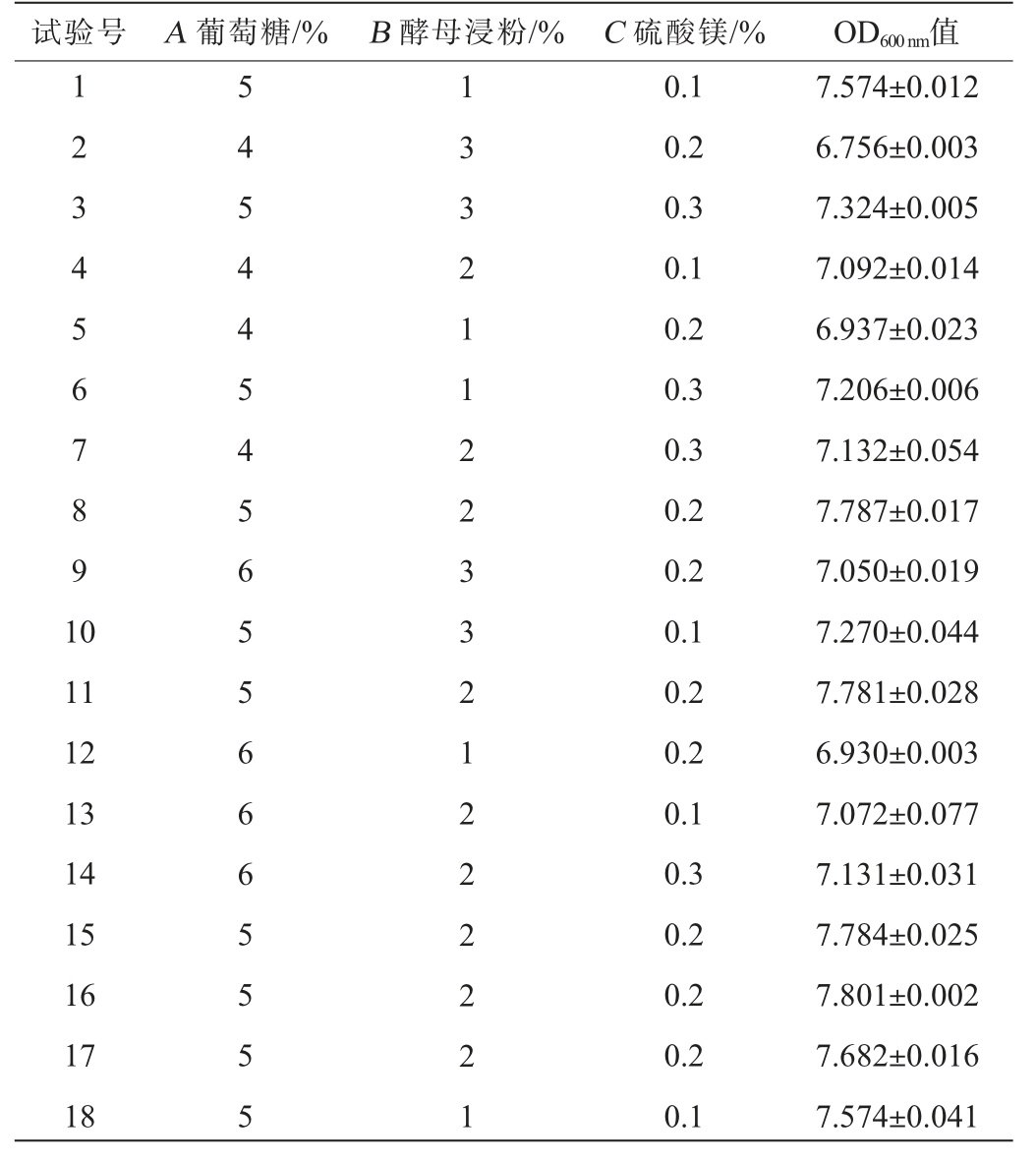
试验号 A 葡萄糖/% B 酵母浸粉/% C 硫酸镁/% OD600 nm值1 2 3 4 5 6 7 8 9 1 0 11 12 13 14 15 16 17 18 5 4 5 4 4 5 4 5 6 5 5 6 6 6 5 5 5 5 1 3 3 2 1 1 2 2 3 3 2 1 2 2 2 2 2 1 0.1 0.2 0.3 0.1 0.2 0.3 0.3 0.2 0.2 0.1 0.2 0.2 0.1 0.3 0.2 0.2 0.2 0.1 7.574±0.012 6.756±0.003 7.324±0.005 7.092±0.014 6.937±0.023 7.206±0.006 7.132±0.054 7.787±0.017 7.050±0.019 7.270±0.044 7.781±0.028 6.930±0.003 7.072±0.077 7.131±0.031 7.784±0.025 7.801±0.002 7.682±0.016 7.574±0.041
表4 回归模型方差分析
Table 4 Variance analysis of regression model
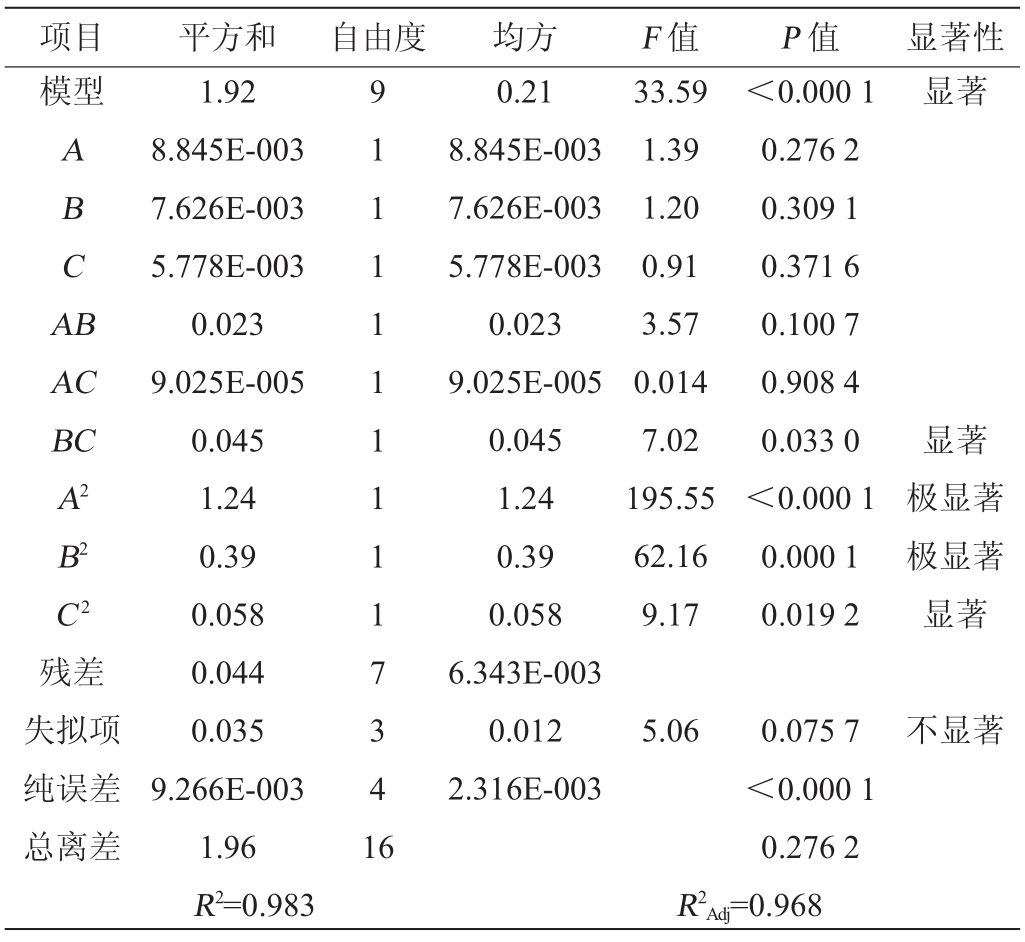
项目 平方和 自由度 均方 F 值 P 值 显著性模型显著ABCA B AC BC A2 B2 C2 33.59 1.39 1.20 0.91 3.57 0.014 7.02 195.55 62.16 9.17<0.000 1 0.276 2 0.309 1 0.371 6 0.100 7 0.908 4 0.033 0<0.000 1 0.000 1 0.019 2显著极显著极显著显著残差失拟项纯误差总离差1.92 8.845E-003 7.626E-003 5.778E-003 0.023 9.025E-005 0.045 1.24 0.39 0.058 0.044 0.035 9.266E-003 1.96 R2=0.983 9 1 1 1 1 1 11 1 17 3 4 1 6 0.21 8.845E-003 7.626E-003 5.778E-003 0.023 9.025E-005 0.045 1.24 0.39 0.058 6.343E-003 0.012 2.316E-003 5.060.075 7<0.000 1 0.276 2=0.968不显著R2Adj
应用Design-Expert13.0软件对表3数据进行多元回归拟和分析,得到菌株021233生物量对葡萄糖(A)、酵母浸粉(B)、硫酸镁(C)的二次多项回归方程为:Y=-18.206+4.347A+3.249B+6.905C-0.361A2-0.403B2-4.583C 2-0.020AB+0.075AC+0.028BC。
由表4可知,模型的F值为33.59,P值<0.000 1,表明模型具有高度显著性,能够很好地拟合试验数据;模型的决定系数R2值较高,说明模型能够解释大部分试验变异;失拟项的P值=0.075 7>0.05,表明失拟项不显著,模型拟合良好。一次项葡萄糖(A)、酵母浸粉(B)和硫酸镁(C)对OD600 nm值的影响均不显著(P>0.05),表明单独改变某一因素对菌体生长的影响较小。 二次项(A2、B2)对OD600 nm值的影响均极显著(P<0.01),表明各因素与菌体生长之间存在非线性关系,且存在最优浓度范围。二次项C2、交互项BC对OD600 nm值的影响显著(P<0.05),表明酵母浸粉和硫酸镁的协同效应对菌体生长有显著影响;其他交互作用(AB、AC)不显著(P>0.05),表明葡萄糖与酵母浸粉、葡萄糖与硫酸镁之间的协同效应较弱。各因素交互作用对菌体生长影响的响应面和等高线结果见图10。
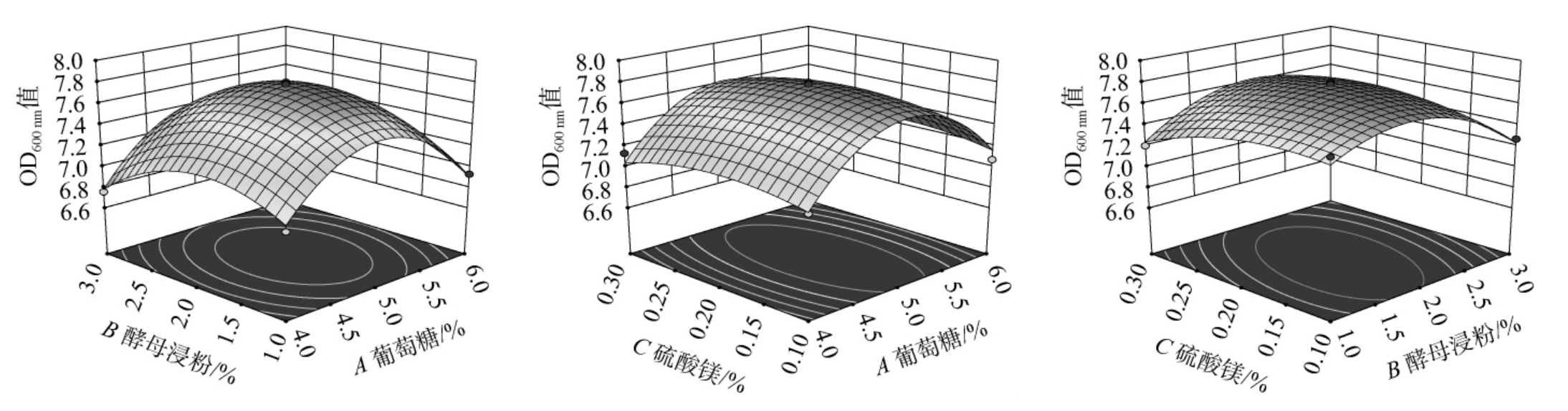
图10 各因素交互作用对菌体生长影响的响应面和等高线
Fig.10 Response surface plots and contour lines of effect of interaction between various factors on strain growth
由图10可知,葡萄糖、酵母浸粉与硫酸镁对响应值影响的响应面图均呈非线性隆峰形态,并伴随不同程度的交互作用。 其中,葡萄糖与硫酸镁(AC)组合响应面峰形尖锐,等高线密集且主轴明显斜拉,表明二者存在较弱交互作用,低葡萄糖时硫酸镁几乎无效,高葡萄糖时其促进作用增强;葡萄糖与酵母浸粉(AB)组合呈宽顶山丘,等高线呈椭圆形倾斜,交互作用中等,响应值对两者浓度变化较稳健;酵母浸粉与硫酸镁(BC)组合呈鞍型,等高线轻度扭曲,交互作用较强。这与方差分析结果一致。
通过回归方程可以得出最优培养基为:葡萄糖4.554%、酵母浸粉1.199%、硫酸镁0.09%。 在实际条件下为了操作便捷,将培养基修正为:葡萄糖4.6%、酵母浸粉1.2%、硫酸镁0.1%。在此条件下进行3次平行验证试验,得到菌体生物量达到最大值(OD600nm值=7.88)。
2.6 菌剂在葡萄酒中的应用分析结果
通过气相色谱-质谱联用技术对使用菌株021233以及菌株A7制备的菌剂RW发酵的葡萄酒样品中的挥发性物质进行了系统性分析,并以菌剂RW发酵葡萄酒的挥发性香气物质峰面积为基准,计算筛选菌株发酵葡萄酒挥发性香气物质峰面积的变化率。酯类物质与醇类是葡萄酒挥发性成分的主体,其含量与感官阈值的关系揭示了酒体香气特征的关键调控机制,因此该研究只列出酯类和醇类物质,结果见表5。
表5 不同菌剂发酵葡萄酒中酯类和醇类物质含量对比
Table 5 Comparison of esters and alcohols contents in wines fermented with different microbial starters

序号 CAS 化合物 试验菌株酒样峰面积 菌剂RW酒样峰面积 相对含量变化率/%酯类1 2 3 4 5 6 7 8 9 1 0 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 141-78-6 123-92-2 123-86-4 109-60-4 106-32-1 628-63-7 1191-16-8 142-92-7 110-19-0 5205-07-2 620-11-1 123-25-1 2305-25-1 93-92-5 25560-91-2 140-11-4 141-12-8 106-33-2 103-45-7 6846-50-0 101-97-3 124-06-1 85-91-6 706-14-9 628-97-7 122-70-3 61931-81-5 77-68-9乙酸乙酯乙酸异戊酯乙酸丁酯乙酸丙酯辛酸乙酯乙酸戊酯乙酸戊烯酯乙酸己基酯乙酸异丁酯3-甲基-3-丁烯醇乙酸酯乙酸-3-戊酯丁二酸二乙酯3-羟基己酸乙酯乙酸苏合香酯4-乙酰氧基丁酸乙酯乙酸苄酯橙花醇乙酸酯十二烷酸乙酯乙酸苯乙2,2,4-三甲基-1,3-戊二醇二异丁酸酯苯乙酸乙酯十四烷酸乙酯N-甲基邻氨基苯甲酸甲酯γ-癸内酯十六烷酸乙酯2-苯基乙基丙酸酯顺式-3-己烯醇乳酸酯2-甲基-丙酸3-羟基-2,2,4-三甲基戊基酯363 007 481.38 42 161 066.44 42 5271.81 6 687 054.62 732 429.31 58 463.07 20 462.37 1 474 523.04 5 887 679.11 132 412.57 129 131.48 233 799.33 49 452.39 2 706 148.29 466 565.45 591 091.51 157 035.34 284 519.27 54 647 139.26 214 942.02 306 544.11 87 166.61 1 636 014.47 396 030.45 182 079.22 69 096.71 218 280.12 92 646.78 89 141 261.91 5 266 139.16-560 655.84 339 358.83-- -251 703.45-- - -3 936 411.51 241 102.11 195 037.11-230 289.89 30 124 231.54 105 896.83 589 584.81 48 933.57 1 450 910.43 23 565.62 186 771.52-424 902.07 93 799.34+307.2+700.6-+1 092.7+115.8-- -+2 239.1-- - --31.3+93.5+203.1-+23.5+81.4+102.9-48.0+78.1+12.8+1 580.5-2.5--48.6-1.2
续表
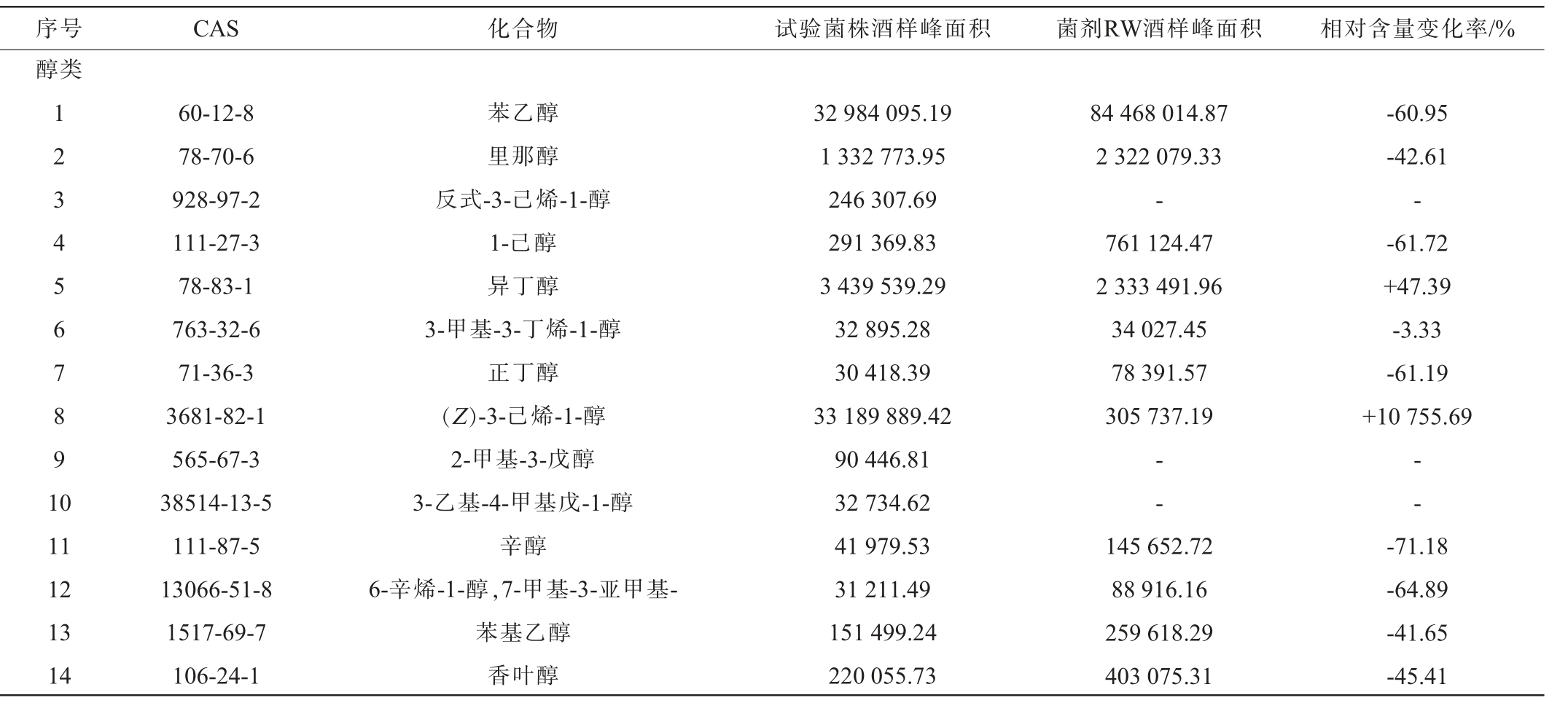
序号 CAS 化合物 试验菌株酒样峰面积 菌剂RW酒样峰面积 相对含量变化率/%醇类1 2 3 4 5 6 7 8 9 1 0 11 12 13 14 60-12-8 78-70-6 928-97-2 111-27-3 78-83-1 763-32-6 71-36-3 3681-82-1 565-67-3 38514-13-5 111-87-5 13066-51-8 1517-69-7 106-24-1苯乙醇里那醇反式-3-己烯-1-醇1-己醇异丁醇3-甲基-3-丁烯-1-醇正丁醇(Z)-3-己烯-1-醇2-甲基-3-戊醇3-乙基-4-甲基戊-1-醇辛醇6-辛烯-1-醇,7-甲基-3-亚甲基-苯基乙醇香叶醇32 984 095.19 1 332 773.95 246 307.69 291 369.83 3 439 539.29 32 895.28 30 418.39 33 189 889.42 90 446.81 32 734.62 41 979.53 31 211.49 151 499.24 220 055.73 84 468 014.87 2 322 079.33-761 124.47 2 333 491.96 34 027.45 78 391.57 305 737.19--145 652.72 88 916.16 259 618.29 403 075.31-60.95-42.61--61.72+47.39-3.33-61.19+10 755.69---71.18-64.89-41.65-45.41
由表5可知,实验菌株对酒体酯类物质的合成表现出正向的调控作用。实验菌株发酵酒中共检测出28种酯类物质,而菌剂RW发酵酒中仅仅检测出18种酯类物质。 相对于菌剂RW,实验菌株发酵酒中酯类物质的相对含量提高了262.6%。 实验菌株发酵酒中检测出的乙酸戊酯,乙酸戊烯酯,乙酸己基酯,乙酸-3-戊酯等10种酯类物质在市售菌剂发酵酒中均未检出。 其中乙酸戊酯具有类似香蕉、苹果和梨的果香,带有甜味和轻微脂肪气息。 在白酒中通常作为协调香气成分,可提升酒体的果香层次感;乙酸己基酯具有水果香气,特别是类似梨的甜酸味,它能为酒带来一种清新的果香,使酒的香气更加丰富和诱人;丁二酸二乙酯具有微弱的果香气味,同时带有微甜、涩和苦的味道。它在酒中可能起到一定的修饰作用,为酒的香气增添一些微妙的层次。除此之外,乙酸乙酯、乙酸异戊酯和乙酸丙酯的峰面积分别达到市售菌剂的307.2%、700.6%和1 092.7%,表明实验菌株通过增强乙酰辅酶A转移酶活性或优化酯化反应途径[30],显著提升了短链酯类的合成效率。乙酸异丁酯的增长率高达2 239.1%,其较高的含量可能赋予酒体独特的甜香和果香特征,推测实验菌株可能激活了支链脂肪酸代谢途径,促进异丁醇与乙酰辅酶A的结合。此外,γ-癸内酯的增长率达1 580.5%,该化合物是典型的内酯类物质,常与奶油和椰香风味相关,其显著增加可能与菌株的酮酸脱羧酶活性增强有关。
由表5可知,实验菌株对酒体中醇类物质的合成与代谢表现出显著的选择性调控特征。在实验菌株发酵酒中检测出醇类物质有14种,市售菌剂组仅有11种,但实验菌株组的相对含量降低了20.9%,虽然醇类物质有所增加,但相对含量稍微下降,而醇类物质的降低可能有助于改善酒的风味平衡。过高的醇类物质可能会带来一些不良的口感,如苦味或刺激性。实验菌株组较低相对含量的醇类物质,可能使酒的口感更加柔和、协调,提升了酒的感官品质。 其中反式-3-己烯-1-醇仅仅存在与实验菌株组,它具有新鲜绿叶香味,是一种清香型名贵香料,可用于香精配方,化妆品行及食品香料中。在酒中,它可能为酒带来一种清新自然的香味,类似于绿叶或青草的香气,有助于提升酒的香气层次和复杂度。而异丁醇的峰面积较市售菌剂增加47.39%,表明实验菌株可能通过强化支链氨基酸(如缬氨酸)的Ehrlich代谢途径,促进异丁醇的合成。该物质是果香和甜香的重要前体。
3 结论
该研究从清香型白酒大曲中分离菌株,利用三丁酸甘油酯透明圈法进行筛选,再使用比色法进行乙酸乙酯定量分析,复筛得到5株高产酯菌株。 通过菌株的耐受性实验,最终成功筛选出1株高产酯且耐受性突出的菌株(编号021233)。 通过ITS-26S rDNA序列鉴定,该菌株被鉴定为扣囊复膜酵母(Saccharomycopsis fibuligera)。 经单因素试验结合Box-Behnken响应面法,确定了最优培养基配方:葡萄糖4.6%、酵母浸粉1.2%、硫酸镁0.1%。对筛选菌株及市售菌株制备的菌剂发酵的葡萄酒样进行挥发性风味成分测定,结果显示,试验菌株组的酯类物质相对含量较市售菌剂组增长了262.6%,其中乙酸乙酯的相对含量增长率高达307.2%,新增的丁二酸二乙酯具有典型的酒曲香和水果香。与此同时,醇类物质的相对含量较市售菌剂组降低了20.9%,较低的醇类物质含量有助于改善酒的风味。综上,该研究成功筛选出了一株兼具高产酯特性和强环境耐受性的扣囊复膜酵母菌株021233。这一研究成果揭示了扣囊复膜酵母在葡萄酒酿造体系中的高产酯特性,其耐环境胁迫能力与代谢可塑性为开发新型复合发酵剂提供了理论依据,对实现葡萄酒风味的定向调控具有重要的实践价值。
[1]ZHAO H,DU B,ZHAO P,et al.Analysis of ester-producing performance in high-yield ethyl hexanoate yeast and the effect on metabolites in bioenhanced Daqu,the starter for Baijiu and other traditional fermented foods[J].J Appl Microbiol,2024,135(4):lxae081.
[2]张阳阳,曹珍,吕培楷,等.不同生香酵母对猕猴桃酒品质的影响[J].食品科技,2024,49(9):82-89.
[3]张天俊,唐东恒,喇录忠,等.生香酵母在青稞酒中的应用研究[J].酿酒科技,2024(8):56-59.
[4]李棒,邓梦菲,陈延儒,等.高酸度水果果酒酿造产酯酵母的鉴定及发酵特性研究[J].中国酿造,2020,39(4):103-108.
[5]刘薇,栾春光,王德良,等.高产酯酵母的筛选、鉴定及其发酵特性研究[J].食品与发酵工业,2021,47(23):311-318.
[6]杨婕,王玉华,米兰,等.耐热克鲁维酵母与酿酒酵母顺序接种发酵对霞多丽干白葡萄酒感官品质的影响[J].食品与发酵工业,2019,45(18):144-154.
[7]YINGB B, CAI J, GAO X, et al.Isolation, identification, and tolerance analysis of yeast during the natural fermentation process of Sidamo coffee beans[J].Arch Microbiol,2024,206(6):279.
[8]CAI W,LI B,CHEN Y,et al.Increase the content of ester compounds in blueberry wine fermentation with the ester-producing yeast: Candida glabrata,Pichia anomala,and Wickerhamomyces anomalus[J].Foods,2022,11(22):3655.
[9]QU C,PENG L,FEI Y,et al.Screening ester-producing yeasts to fortify the brewing of rice-flavor Baijiu for enhanced aromas[J].Bioengineered,2023,14(1):2255423.
[10]LOCRA MANDUJANO G P,ALVES H C,PRADO C D,et al.Identification and selection of a new Saccharomyces cerevisiae strain isolated from Brazilian ethanol fermentation process for application in beer production[J].Food Microbiol,2022,103:103958.
[11]HU X Q, LIU Q, HU J P, et al.Identification and characterization of probiotic yeast isolated from digestive tract of ducks[J].Poult Sci,2018,97(8):2902-2908.
[12]JIA Z C,LIU D,MA H D,et al.Yeast Metabolic engineering for biosynthesis of caffeic acid-derived phenethyl ester and phenethyl amide[J].ACS Synth Biol,2023,12(12):3635-3645.
[13]WANG C, FU X, WANG J, et al.Comprehensive characterization of Chinese beers based on chemical composition, antioxidant activity and volatile metabolomics[J].Sci Rep,2025,15(1):10204.
[14]MAITY D,GOVINDARAJU T.A turn-on NIR fluorescence and colourimetric cyanine probe for monitoring the thiol content in serum and the glutathione reductase assisted glutathione redox process[J].Org Biomol Chem,2013,11(13):2098-2104.
[15]YANG Y,XIA Y,LIN X,et al.Improvement of flavor profiles in Chinese rice wine by creating fermenting yeast with superior ethanol tolerance and fermentation activity[J].Food Res Int,2018,108:83-92.
[16]KONG I I, TURNER T L, KIM H, et al.Phenotypic evaluation and characterization of 21 industrial Saccharomyces cerevisiae yeast strains[J].FEMS Yeast Res,2018,18(1):1-12.
[17]ORAEI M, RAZAVI S H, KHODAIYAN F.Optimization of effective minerals on riboflavin production by Bacillus subtilis subsp. subtilis ATCC 6051 using statistical designs[J].Avicenna J Med Biotechnol,2018,10(1):49-55.
[18]INTHACHAT W, TEMVIIRIYANUKUL P, ON-NOM N, et al.Optimization of phytochemical-rich Citrus maxima Albedo extract using response surface methodology[J].Molecules,2023,28(10):4121.
[19]ZHANG P,ZHANG R,SIRISENA S,et al.Beta-glucosidase activity of wine yeasts and its impacts on wine volatiles and phenolics:A mini-review[J].Food Microbiol,2021,100:103859.
[20]DE FRANCESCO G,SANNINO C,SILEONI V,et al.Mrakia gelida in brewing process: An innovative production of low alcohol beer using a psychrophilic yeast strain[J].Food Microbiol,2018,76:354-362.
[21]HOU X, JIANG J, LUO C, et al.Advances in detecting fruit aroma compounds by combining chromatography and spectrometry[J].J Sci Food Agr,2023,103(10):4755-4766.
[22]VALLARINO J G,ERBAN A,FEHRLE I,et al.Acquisition of volatile compounds by gas chromatography-mass spectrometry (GC-MS)[J].Methods Mol Biol,2018,1778:225-239.
[23]ZHU B,GAO H,YANG F,et al.Comparative characterization of volatile compounds of Ningxiang Pig,Duroc and Their Crosses(Duroc x Ningxiang)by using SPME-GC-MS[J].Foods,2023,12(5):1059.
[24]DANK A, SMID E J, NOTEBAART R A.CRISPR-Cas genome engineering of esterase activity in Saccharomyces cerevisiae steers aroma formation[J].BMC Res Notes,2018,11(1):682.
[25]LIU S,SKORY C,QURESHI N.Ethanol tolerance assessment in recombinant E. coli of ethanol responsive genes from Lactobacillus buchneri NRRL B-30929[J].World J Microb Biot,2020,36(12):179.
[26]WOLF I R,MARQUES L F,DE ALMEIDA L F,et al.Integrative analysis of the ethanol tolerance of Saccharomyces cerevisiae[J].Int J Mol Sci,2023,24(6):5646.
[27]ZHANG T,TANG Y,LUAN Y,et al.Herbaceous peony AP2/ERF transcription factor binds the promoter of the tryptophan decarboxylase gene to enhance high-temperature stress tolerance[J].Plant Cell Environ,2022,45(9):2729-2743.
[28]PRADO C D,MANDRUJANO G P L,SOUZA J P,et al.Physiological characterization of a new thermotolerant yeast strain isolated during Brazilian ethanol production, and its application in high-temperature fermentation[J].Biotechnol Biofuels,2020,13:178.
[29]SIEW K S, YEE C F, SULAIMAN M R.Optimization of bacteriocin production by Lactobacillus plantarum using response surface methodology[J].Open Confer Proceed J,2013,4:81.
[30]XU Y,ZHAO J,LIU X,et al.Flavor mystery of Chinese traditional fermented Baijiu:The great contribution of ester compounds[J].Food Chem,2022,369:130920.