大曲通常以小麦、豌豆、大麦等为原料,在开放环境中通过固态自发发酵过程生产[1]。 根据发酵过程中的峰值温度,大曲可细分为低温大曲(40~50 ℃)、中温大曲(50~55 ℃)、中高温大曲(55~60 ℃)和高温大曲(60~70 ℃),用于清香型、浓香型和酱香型白酒的发酵[2]。据报道,作为白酒发酵的核心发酵剂,大曲贡献了61.1%~80.0%的真菌群落[3],这些真菌对于发酵底物的代谢至关重要,同时它们可以通过复杂的代谢网络形成独特的风味特征[4]。例如,王秀秀等[5]研究发现,假丝酵母菌属(Candida)与芳香类、吡嗪类物质存在显著相关性,毕赤酵母属(Pichia)与己酸己酯和亚油酸乙酯等物质存在显著相关性。 PU S等[6]研究发现,接种异常威克汉姆酵母(Wickerhamomyces anomalus)YE010强化大曲的挥发性酸类(22.17 μg/mL)、酯类(103.38 μg/mL)、醇类(41.28 μg/mL)等物质的含量最高。由此可见,通过解析真菌群落组成,能够深入阐释白酒酿造机理,为品质提升提供理论依据。然而,以往对大曲真菌群落的研究大多使用二代测序技术[7-8],该技术读段太短、通量不够高,所以只能在属水平进行分析。 近些年来,以PacBio SMRT测序技术为代表的三代测序技术因具有高精度、长读长等特点[9],被应用于各类样品微生物群落的研究。因此,后来研究者对大曲真菌群落的解析可以具体到种水平。
环境条件是影响大曲发酵的主要因素,包括温度、湿度、酸度和氧(O2)等[2]。其中,温度与湿度作为调控大曲真菌群落演替的关键驱动力[10],其核心作用在于直接影响大曲的水分含量及分布,因此水分对大曲中真菌的生长繁殖具有决定性影响。例如,崔海灏等[11]研究发现,当大曲的水分含量在35%~36%时,酵母菌的生长、繁殖和代谢活动更旺盛。吴正坤等[12]研究发现,水分含量与红曲霉属(Monascus)的含量呈现正相关,与微小根毛霉(Rhizomucor pusillus)的含量呈现负相关。由此可见,作为关键环境驱动因子,水分指标通过选择性调控特定真菌物种的增殖速率和代谢活性,直接影响大曲的真菌群落结构。此外,水分含量和分布对大曲产品质量存在显著影响,因此越来越多的研究者聚焦于大曲的水分研究。例如,SUN T等[13-14]采用近红外高光谱成像技术结合空间信息和多粒度级联森林算法,实现了对大曲的水分含量的预测。纪圩等[15]以期通过接种芽孢杆菌,利用其能够产生生物膜的特性调控大曲的保水性。综上所述,通过系统研究大曲水分指标,可实现对微生物群落的精准调控,进而推动大曲品质的持续改进。
鲁西北运河位于山东省西北部,地处海河水系卫运河流域[16],海拔约50~200 m,年均气温12.9 ℃,年均降水量547.5 mm,年均相对湿度63.4%。 不同地区独特的地理环境与气候条件等地域因素,孕育出不同的酿酒微生态体系,进一步造就了酒体风格的差异化。因此,本研究以采集自鲁西北运河产区某酒厂的5份中高温大曲和5份高温大曲样品为研究对象,采用PacBio SMRT测序技术对2种类型大曲的真菌群落结构差异进行解析,通过常规理化检测方法和低场核磁共振(lowfield-nuclearmagneticresonance,LF-NMR)技术对大曲的水分含量、水分活度(water activity,Aw)、结合水含量、不易流动水含量和结合水含量进行测定,并对优势真菌与水分指标之间的相关性进行分析,以期为鲁西北运河产区中高温和高温大曲品质的改善提供数据支撑。
1 材料与方法
1.1 材料与试剂
中高温大曲、高温大曲:鲁西北运河产区某白酒厂。TGuide S96磁珠法土壤/粪便基因组脱氧核糖核酸(deoxyribonucleic acid,DNA)提取试剂盒:天根生化科技(北京)有限公司;正反向引物ITS1F(5'-CTTGGTCATTTAGAGGAAGTAA-3')/ITS4(5'-TCCTCCGCTTATTGATATGC-3')、KOD ONE NM高保真DNA聚合酶、无核酸酶水(nuclease-free water,NFW):北京百灵克生物科技有限责任公司;MinElute聚合酶链式反应(polymerase chain reaction,PCR)产物纯化试剂盒:德国Qiagen公司。
1.2 仪器与设备
BF-10小型高速粉碎机:河北本辰科技有限公司;8411型电动振筛机:绍兴市上虞星星仪器设备有限公司;Nano Drop显微分光光度计、Qubit 4.0荧光计:赛默飞世尔科技(中国)有限公司;Veriti96-Well PCR仪:美国Applied Biosystems公司;R930机架式服务器:美国DELL公司;MS-70快速水分测定仪:上海右一仪器有限公司;AW-1水分活度仪:无锡碧波电子设备厂;NMI20-025V-I型核磁共振成像分析仪:上海纽迈电子科技有限公司。
1.3 实验方法
1.3.1 大曲样品采集
从贮藏室内随机均匀分别采集5块高温大曲(编号为GW1~GW5)和5块中高温大曲(编号为ZGW1~ZGW5),装进无菌自封袋内,低温条件下送至实验室。采用粉碎机对大曲进行粉碎,过20目筛后采用四分法将样品混匀,转移至无菌自封袋密封后于-40 ℃冰箱保存。
1.3.2 中高温和高温大曲样品总DNA提取、扩增和PacBio SMRT测序
使用试剂盒提取大曲样品DNA,产物经NanoDrop显微分光光度计和Qubit 4.0荧光计质量检测合格后,使用引物ITS1F(5'-CTTGGTCATTTAGAGGAAGTAA-3')和ITS4(5'-TCCTCCGCTTATTGATATGC-3')扩增全长ITS序列。PCR扩增体系为30 μL,包含1.5 μL基因组DNA,11.7 μL 无核酸酶水(NFW),15 μLKOD ONE NM高保真DNA聚合酶,0.9 μL 正向引物ITS1F,0.9 μL 反向引物ITS4。PCR扩增程序为:95 ℃初始变性5 min;95 ℃变性30 s→55 ℃退火30 s→72 ℃延伸45s(8个循环);95℃变性30s→60℃退火30s→72℃延伸45 s(24个循环);72 ℃下再延伸5 min。扩增产物纯化后,送至北京百迈客生物科技有限公司,采用PacBio Sequel II测序系统进行PacBio SMRT测序。
1.3.3 原始序列处理和生物信息学分析
使用SMRTlink v6.0软件对原始读长进行质量过滤后,基于QIIME 2软件包进行分析。 使用UCHIME算法去除嵌合体序列;使用Uparse软件以97%的相似性对序列进行操作分类单元(operational taxonomic units,OTU)聚类;使用UNITE数据库(https://unite.ut.ee/)注释代表OTU序列的物种信息;基于Bray-Curtis距离计算β多样性,通过主坐标分析(principal coordinates analysis,PCoA)进行可视化。
1.3.4 水分指标的测定
大曲水分含量:采用快速水分测定仪测定;大曲水分活度:采用水分活度仪测定。
大曲水分分布(结合水、不易流动水和自由水含量):采用低场核磁共振分析仪测定。仪器预热2 h,使用食用油在Q-FID序列下进行校准,随后称取3 g样品,使用CPMG脉冲序列进行测定。横向弛豫参数(T2)时间在0.1~10 ms、10~100 ms和>100 ms的峰分别定义为结合水、不易流动水、自由水[17],每个样品重复3次取均值。
1.3.5 数据处理和统计分析
使用Mann-Whitney检验对优势门、优势种、水分指标之间差异的显著性进行分析;使用R软件绘制稀释曲线(vegan包)、等级丰度曲线(ggplot2包)、PCoA散点图(ggplot2包)、优势门/种堆积柱形图(ggplot2包)、线性判别分析效应大小(linear discriminant analysis effect size,LEfSe)分析柱形图(microeco包)、普氏分析散点图(ggplot2包);使用Cytoscape软件绘制优势真菌种与水分指标的相关性网络图。
2 结果与分析
2.1 中高温和高温大曲样品真菌测序结果
十个大曲样品的测序数据经质控后,共获得130 406条真菌ITS有效序列,基于97%的相似性聚类后共获得498个OTU。 基于OTU数据,对中高温和高温大曲样品真菌测序深度进行分析,结果见图1。
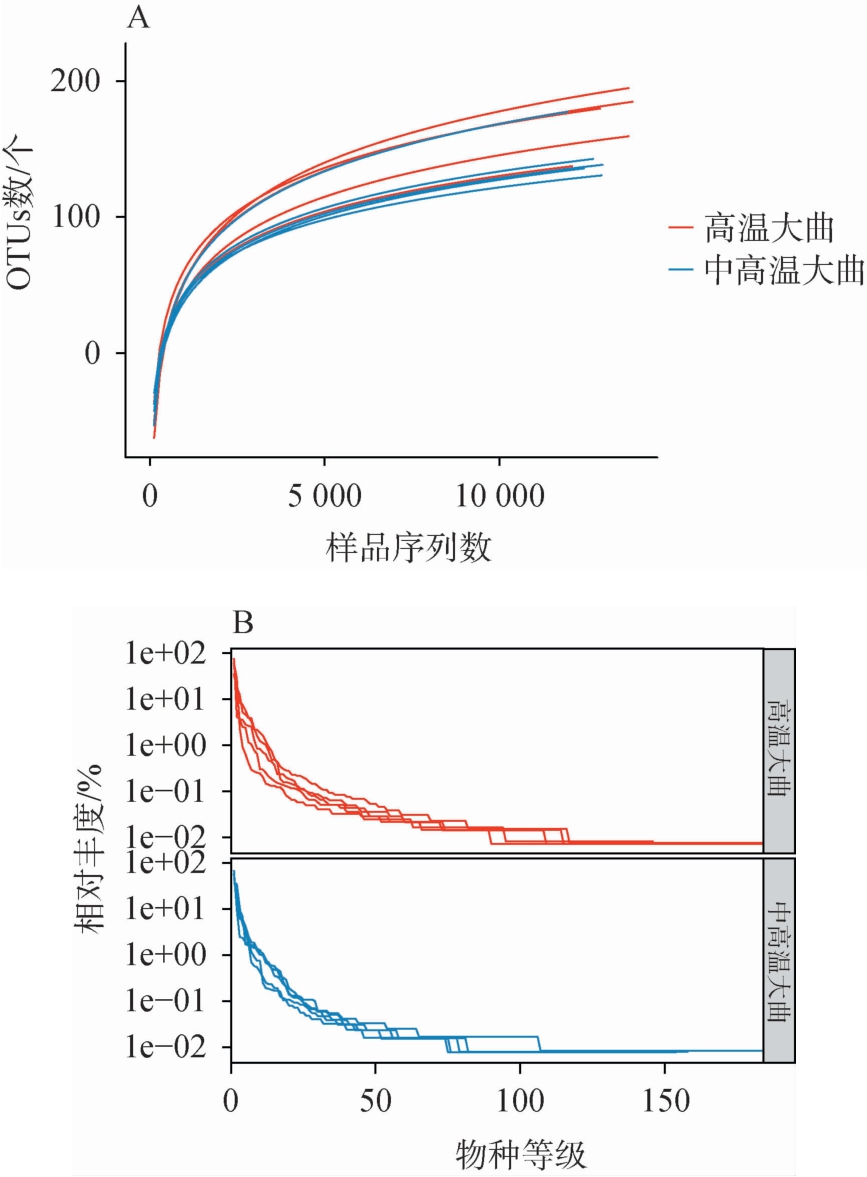
图1 中高温和高温大曲真菌稀释曲线(A)和等级丰度曲线(B)
Fig.1 Rarefaction curves (A) and rank abundance curves (B) of fungi in medium-high-temperature and high-temperature Daqu
稀释曲线和等级丰度曲线一般用来评估测序数据的合理性[18]。由图1A可知,随着测序深度的增加,高温和中高温大曲样本真菌群落稀释曲线的变化趋势相同,并且曲线逐渐降趋于平坦,表明测序深度可以反映大曲样品的真菌信息。由图1B可知,等级丰度曲线在横轴上的范围较大,在垂直方向渐进平缓,表明各样本所含物种的丰富度和均匀度都已达到一定的水平,亦证明测序深度合理,能够覆盖大曲样本中绝大部分微生物。
2.2 中高温和高温大曲样品真菌群落结构分析
2.2.1 真菌群落β多样性分析
为评估中高温和高温大曲的真菌群落结构差异,基于Bray-Curtis距离对2种类型大曲的真菌群落结构进行主坐标分析,结果见图2。
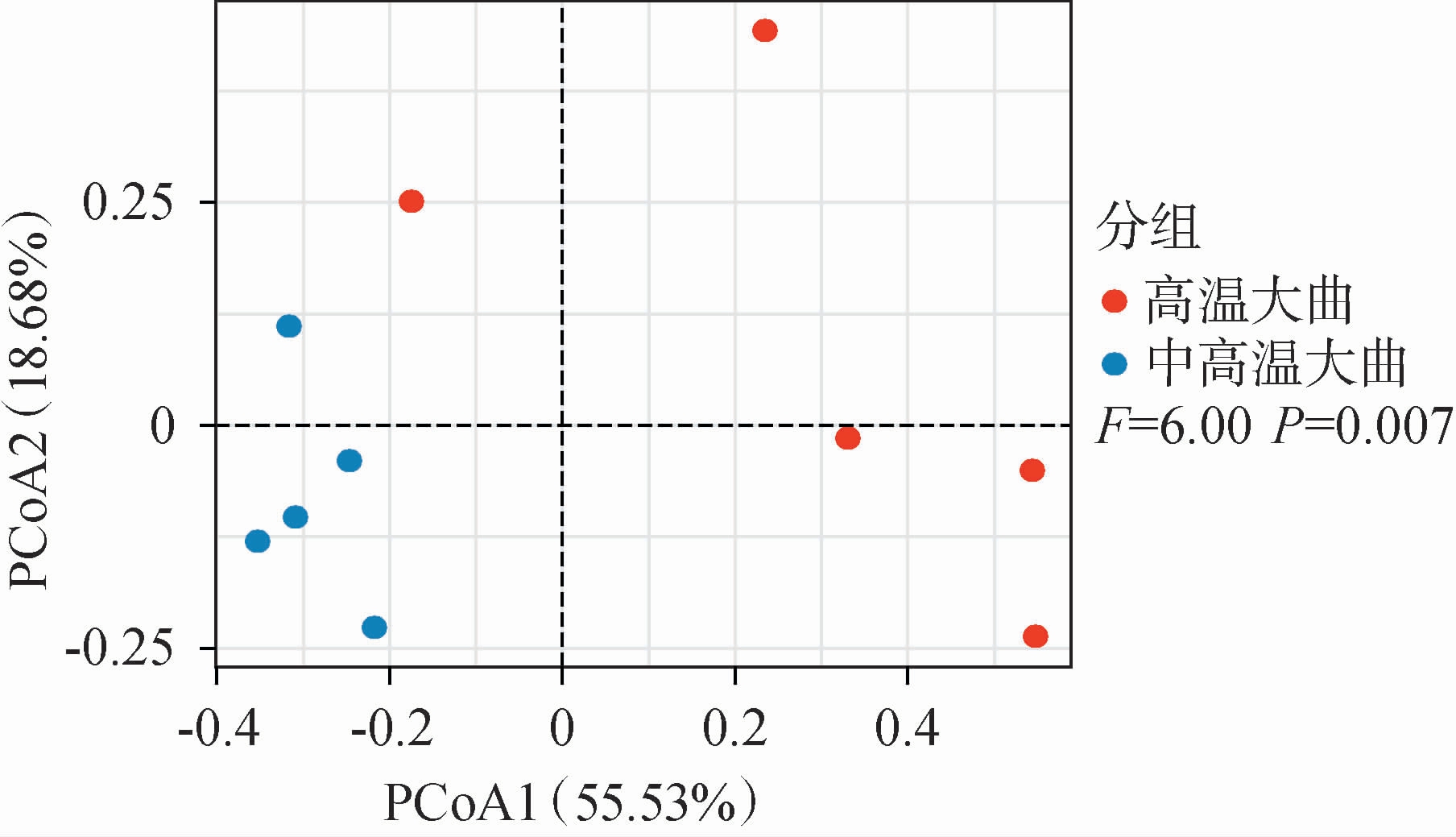
图2 基于Bray-Curtis距离的真菌群落结构主坐标分析
Fig.2 Principal coordinates analysis of fungal community structure based on Bray-Curtis distance
由图2可知,中高温和高温大曲沿X轴方向存在明显的分离趋势,其中中高温大曲主要集中于X轴负半轴,且较为集中,高温大曲主要集中于X轴正半轴。 此外,结合PERMANOVA检验发现,2种类型大曲真菌群落之间存在极显著差异(P=0.007<0.01)。
2.2.2 门水平上真菌群落结构差异分析
在门水平上对高温和中高温大曲样品的群落结构进行差异分析,结果见图3。
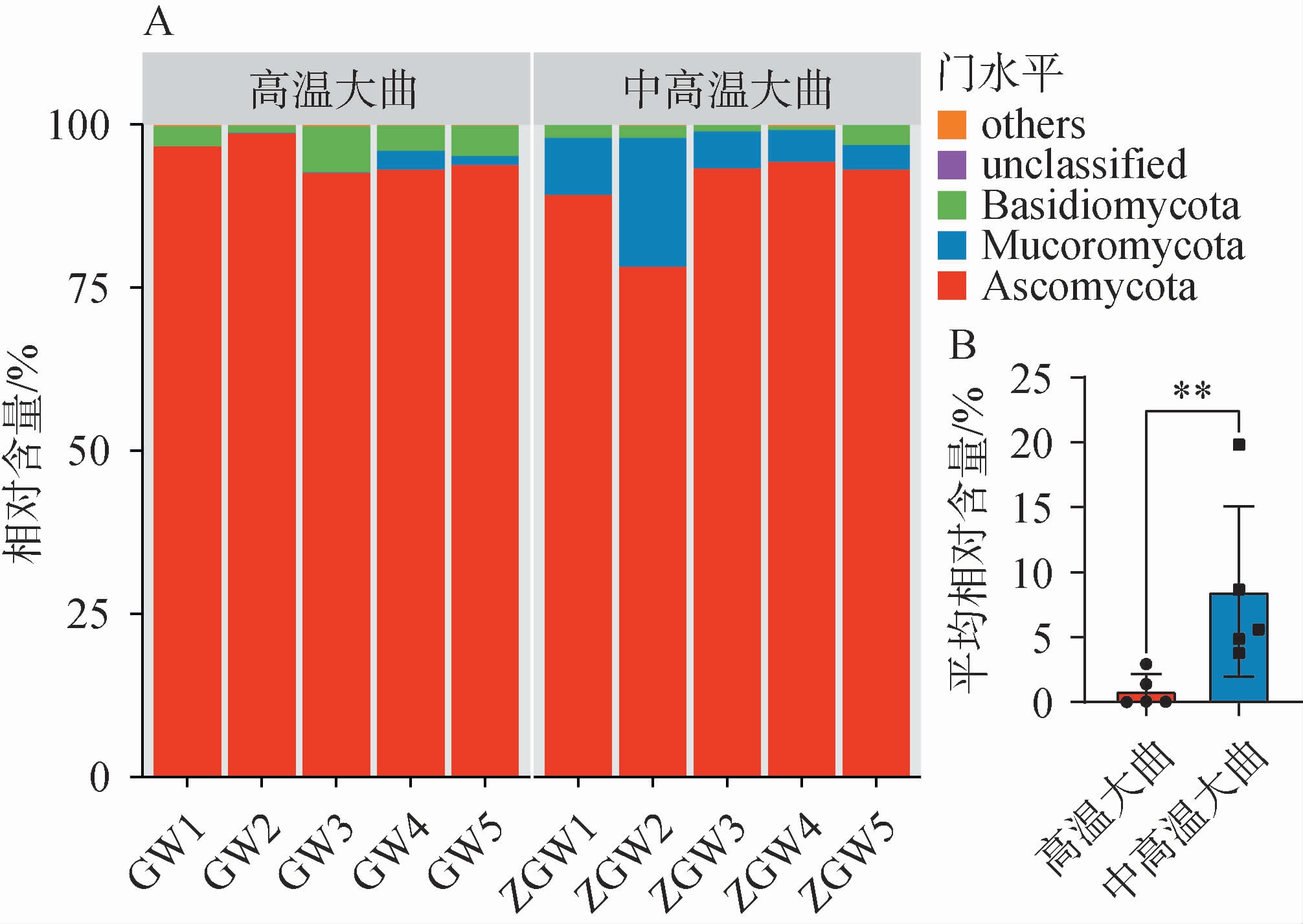
图3 基于门水平中高温和高温大曲样品真菌群落结构分析(A)及优势真菌相对丰度差异分析(B)
Fig.3 Fungal community structure analysis (A) and relative abundance difference analysis of dominant fungus (B)of medium-high-temperature and high-temperature Daqu samples at the phylum level
“**”表示差异极显著(P<0.01)。
由图3A可知,在门水平上,共检测到3个优势真菌门(平均相对含量>1%),分别为子囊菌门(Ascomycota)、毛霉门(Mucoromycota)和担子菌门(Basidiomycota),其相对丰度分别为78.20%~98.70%、0.01%~19.82%和0.61%~7.13%。 由图3B可知,3个优势真菌门基于平均相对丰度采用Mann-Whitney分析发现,子囊菌门(Ascomycota)和担子菌门(Basidiomycota)平均相对丰度在高温和中高温大曲之间均无显著差异(P>0.05),但子囊菌门(Ascomycota)在高温和中高温大曲的各个样本中均占据主导地位,也是低温和中温大曲中的主要优势真菌门[19]。作为真菌类群中的一个重要门类,Ascomycota不仅具有很强的环境适应性,而且隶属于Ascomycota的真菌大多能够分泌淀粉酶、蛋白酶及脂肪酶等[20],从而在酿造过程中促进风味化合物的生成。 此外,中高温大曲中还检测出一定含量的毛霉门(Mucoromycota),其平均相对丰度为8.54%,极显著高于高温大曲毛霉门的相对丰度(0.88%)(P<0.01),这与YANG Y等[21-22]的研究结果相似,究其原因可能与发酵温度密切相关。
2.2.3 种水平上真菌群结构差异分析
在种水平上对高温和中高温大曲样品的群落结构进行差异分析,结果见图4。
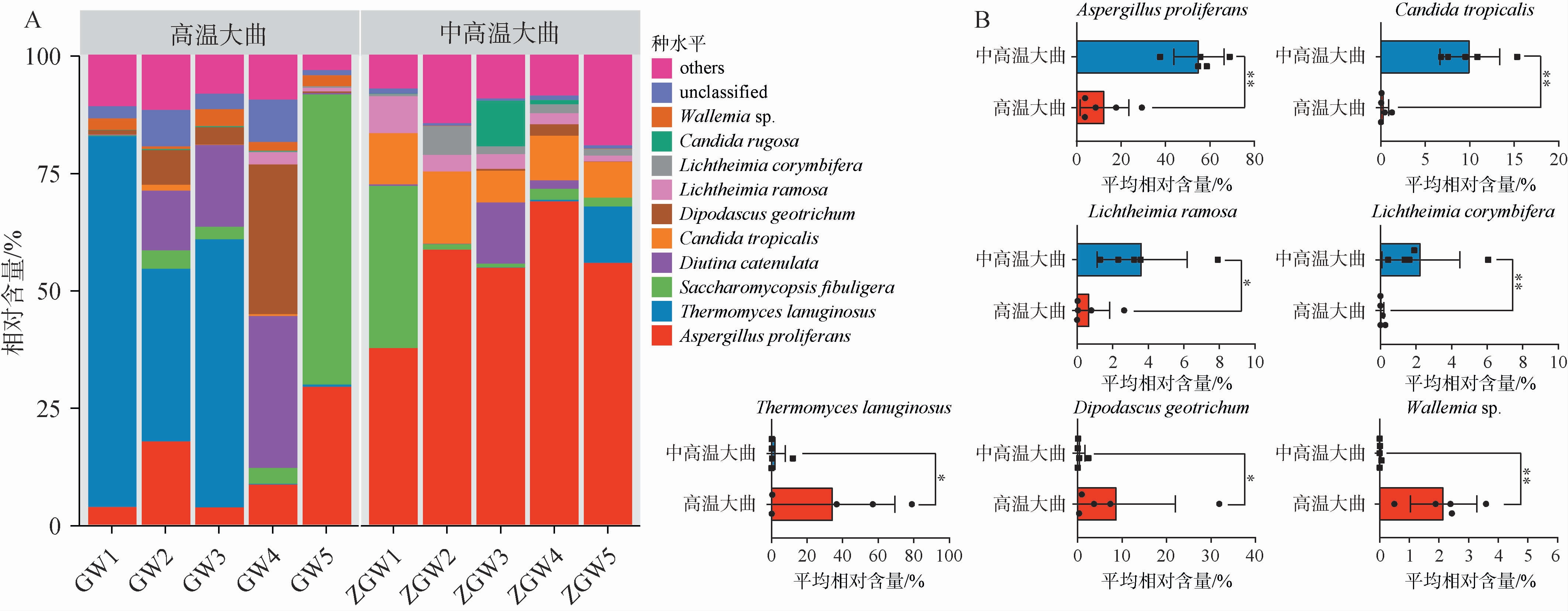
图4 基于种水平中高温和高温大曲样品真菌群落结构分析(A)及优势真菌相对丰度差异分析(B)
Fig.4 Fungal community structure analysis (A) and relative abundance difference analysis of dominant fungus (B) of medium-high-temperature and high-temperature Daqu samples at the species level
“*”表示差异显著(P<0.05);“**”表示差异极显著(P<0.01)。 下同。
由图4A可知,在种水平上,共检测到10个优势真菌种(平均相对丰度>1%),分别为多育曲霉(Aspergillus proliferans)、疏棉状嗜热丝孢菌(Thermomyces lanuginosus)、扣囊复膜孢酵母(Saccharomycopsis fibuligera)、Diutina catenulata、热带假丝酵母(Candida tropicalis)、地丝双足囊菌(Dipodascus geotrichum)、总状横梗霉(Lichtheimia ramose)、伞枝横梗霉(Lichtheimia corymbifera)、皱褶假丝酵母(Candida rugose)和Wallemia sp.。中高温大曲以Aspergillus proliferans为主,平均相对丰度为50.08%,类似的结果也在采集于湖北省宜昌市的中高温大曲中观察到[23]。在中高温大曲发酵过程中,通常添加豌豆等辅料进行发酵,Aspergillus proliferans能够高效分泌纤维素酶[24],因此该菌种的富集显著加速了中高温大曲原料的分解与转化。 此外,Aspergillus proliferans会产生有机酸[25],这些有机酸通过酯化反应与醇类物质结合生成酯类化合物,同时也可以与氨基酸发生反应生成鲜味物质,丰富了白酒的感官层次。高温大曲主要以Thermomyces lanuginosus为主,平均相对含量为34.66%。Thermomyces lanuginosus是一种分布广泛的嗜热真菌,于1899年由Tsiklinskaya首次从马铃薯中分离获得,培养条件为52~53 ℃[26]。该菌种具有极大的工业应用潜力,这与其能够分泌木聚糖酶、脂肪酶、半纤维素酶和纤维素酶、淀粉酶、蛋白酶等功能密不可分[27]。 同时,其分泌的广泛酶类物质是白酒发酵的关键组成部分,一方面能够赋予大曲更高的液化力、糖化力等功能特性,另一方面能够催化风味物质前体的转化[28]。
由图4B可知,10个优势真菌种基于平均相对丰度采用Mann-Whitney分析发现,共有7个优势真菌种相对丰度在高温大曲及中高温大曲之间存在显著差异。 中高温大曲中Aspergillus proliferans、Candida tropicalis 和Lichtheimia corymbifera的平均相对丰度极显著高于高温大曲(P<0.01),分别为55.08%、10.01%和2.28%,其在高温大曲中平均相对丰度分别为12.63%、0.36%和0.13%。 中高温大曲中Lichtheimia ramosa的平均相对丰度显著高于高温大曲(P<0.05),在二者中相对丰度分别为3.66%和0.70%。高温大曲中Wallemia sp.的平均相对丰度极显著高于中高温大曲(P<0.01),平均相对丰度分别2.16%和0.014%;高温大曲中Thermomyces lanuginosus和Dipodascus geotrichum的平均相对丰度显著高于中高温大曲(P<0.05),平均相对丰度分别为34.66%、8.83%,其在中高温大曲中平均相对丰度为2.52%和0.58%。在酿造过程中,Candida tropicalis不仅能够通过醇和乙酰辅酶A在醇乙酰转移酶的催化作用下产生酯类物质[29],还可以利用不同的碳源产生有机酸、醇类等风味物质,以及木聚糖酶、植酸酶、葡糖苷酶等酶类物质[30],加速原料的利用和风味的完善。 Lichtheimia ramosa和Lichtheimia corymbifera同隶属于横梗霉属(Lichtheimia),两者形态特征相似,均能形成球形孢子囊,且可以在>45 ℃的温度条件下生长(Lichtheimia ramosa的耐热极限达49 ℃)[31]。在功能特性方面,两者均能产生β-葡萄糖苷酶,然而Lichtheimia ramosa酶系更丰富,还能合成淀粉酶、嗜热木聚糖酶及纤维素酶等多种酶类[32]。Dipodascus geotrichum菌丝粗壮,生长迅速,能够产生酯类和醛类等物质,同时还被纳入《传统发酵食品用微生物菌种名单》[33]。Wallemia sp.隶属于节担菌属(Wallemia),研究发现Wallemia与大曲的淀粉含量[34]和糖化力[35]显著正相关(P<0.05)。 综上可见,真菌群落在大曲发酵中起着至关重要的作用,与大曲的风味、营养物质和理化指标密切相关。
2.2.4 真菌群落组间LEfSe分析
采用LEfSe分析,对高温和中高温大曲样品真菌生物标志物进行分析,结果见图5。

图5 中高温和高温大曲样品真菌群落线性判别分析效应大小分析结果
Fig.5 Linear discriminant analysis effect size analysis results of fungal communities in medium-high-temperature and high-temperature Daqu samples
由图5可知,基于线性判别分析(linear discriminant analysis,LDA)得分>3.0,LEfSe分析共鉴定出12个种水平的显著差异物质,其在2种类型大曲样品中呈现明显差异。其中,中高温大曲组有显著差异物质8种,分别为Aspergillus proliferans、Candida tropicalis、Lichtheimia ramosa、Lichtheimia corymbifera、Lichtheimia ornata、Pseudopithomyces chartarum、粉状米勒酵母(Millerozymafarinose)和皱褶假丝酵母(Diutina rugose)。Millerozyma farinose(原名为Pichia farinose)是一种广泛存在于传统发酵食品中的嗜盐酵母菌,该菌种具有较强的乙醇耐受适应性,此外还具备降胺能力和产酯能力。张霞等[36]使用从浓香型白酒酿造环境中分离的Millerozyma farinoseWLY-Y-91进行模拟发酵,结果发现发酵产物中乙酸乙酯、正丙醇及异戊醇的含量分别显著升高了143.8%、20.3%、132.1%,该结果进一步证实了Millerozyma farinose在白酒发酵中的产酯增效作用。高温大曲组有显著差异物质4种,分别为Thermomyces lanuginosus、Dipodascus geotrichum、Wallemia sp.和半乳糖霉菌(Galactomyces geotrichum)。Galactomyces geotrichum不仅能够在46 ℃高温条件下存活,还能通过降解蛋白质和脂质生成多种挥发性风味前体物质,进而显著影响白酒的风味特征[37]。
结果表明,2种类型大曲真菌群落结构之间存在明显差异,这种差异很可能是2种类型大曲在制曲过程中温度控制的不同所导致的,其中Aspergillus proliferans和Thermomyces lanuginosus可分别作为中高温和高温大曲的生物标志物。中高温大曲培曲管理中,主要采用“前缓、中挺、后缓落”的工艺(40~55 ℃),为酵母菌创造了适宜生长条件,而高温大曲则通过“高温发酵”的工艺(曲块温度>60 ℃),促进了嗜热真菌的定向富集。
2.3 中高温和高温大曲样品水分指标分析
水分是影响大曲真菌群落演替和代谢的关键因素[38],因此本研究对2种类型大曲的水分指标进行测定,结果见图6。
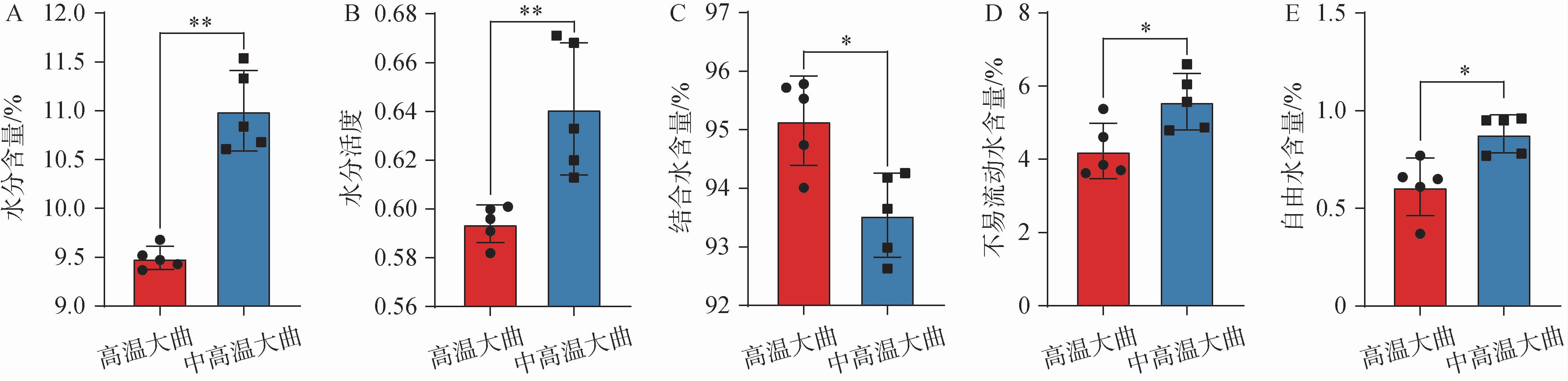
图6 中高温和高温大曲样品水分指标分析结果比较
Fig.6 Comparison of moisture indicators analysis results of medium-high-temperature and high-temperature Daqu samples
水分含量是发酵过程监测的关键参数,该指标的优化与调控可以进一步提升酒曲的品质。 由图6A可知,中高温大曲样品的平均水分含量为11.00%,极显著高于高温大曲的平均水分含量(10.09%)(P<0.01),这种差异可能归因于峰值温度。相较于中高温大曲,高温大曲曲房环境温度更高,显著加速了水分的蒸发,最终形成较低的水分含量。对于真菌群落而言,酵母菌存活率与水分含量和环境温度呈显著负相关(P<0.05)[11],这与中高温大曲中酵母菌含量较高的测序研究结论相互印证,表明水分含量的调控对微生物群落结构具有重要影响。水分活度是指系统中水分存在的状态,即水分的结合程度(游离程度)。水分活度值越高,结合程度越低;水分活度值越低,结合程度越高。 由图6B可知,中高温大曲样品的平均水分活度(Aw)为0.641,极显著高于高温大曲的平均水分活度(Aw)0.594(P<0.01)。WANG Y等[39]对湖北省某白酒公司中高温和高温大曲研究发现,高温大曲的水分活度显著低于中高温大曲(P<0.05),与本研究结果一致。尽管较高的水分含量有利于微生物的生长,然而水分活度过高不利于大曲的贮藏与品质的保证。由图6C、6D、6E可知,中高温大曲样品的平均结合水含量为94.00%,显著低于高温大曲的平均结合水含量(94.96%)(P<0.05),平均不易流动水和自由水含量分别为5.04%和0.96%,显著高于高温大曲的平均不易流动水和自由水含量(4.37%和0.67%)(P<0.05)。究其原因,一方面可能是当微生物代谢旺盛时,结合水会转化为自由水,使结合水含量降低[40],另一方面可能是高温作用下造成自由水流失[41]。综上可知,中高温和高温大曲之间水分指标存在较大差异,这种差异可能与微生物和发酵温度密切相关。
2.4 大曲样品水分指标与优势真菌种关联分析
采用普鲁克(普氏)分析(Procrustes analysis)和基于Spearman相关系数相关性分析,研究优势真菌种与水分指标之间关联性,结果见图7。
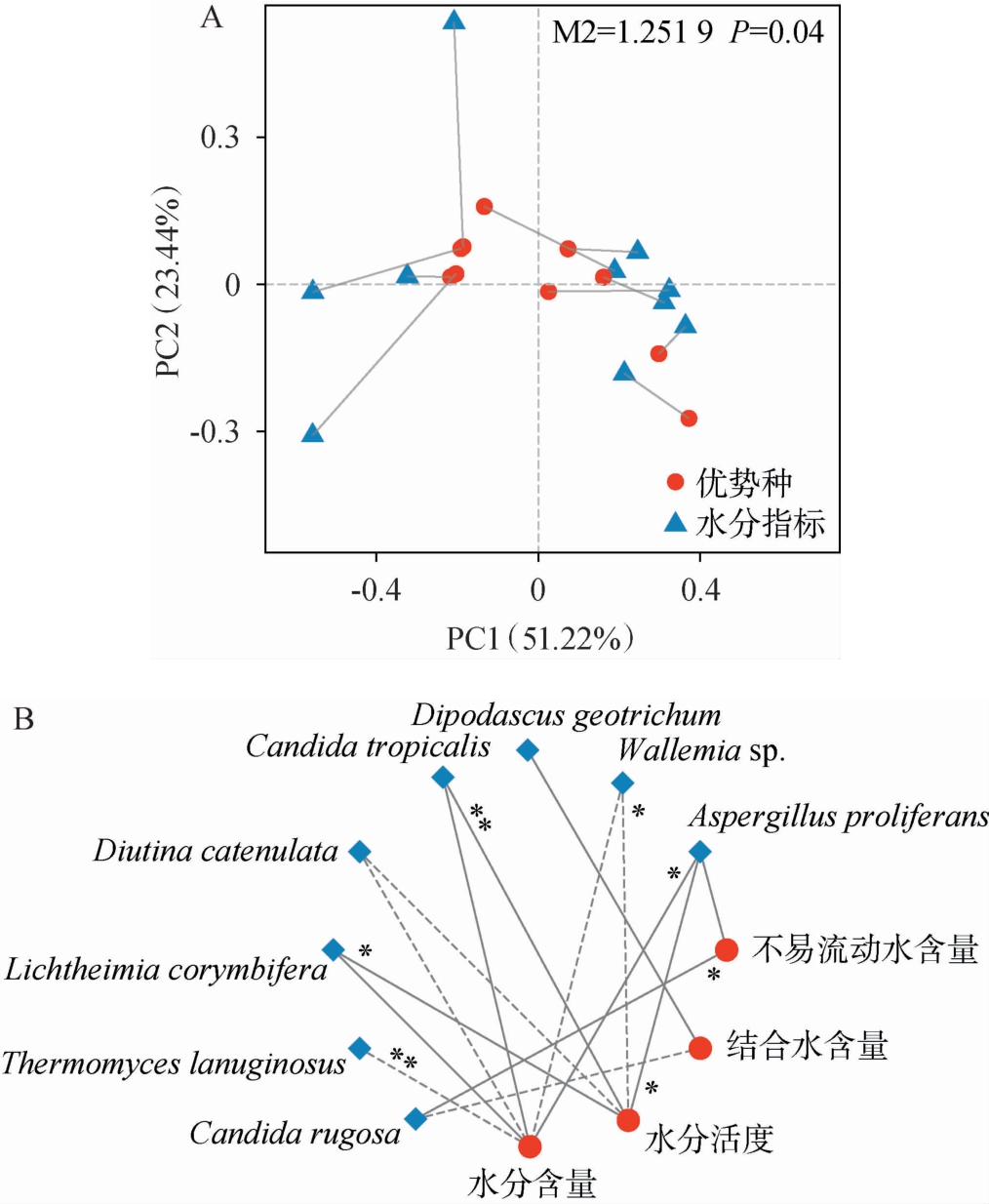
图7 水分指标与优势真菌种之间普鲁克分析(A)及基于Spearman相关系数相关性分析(B)
Fig.7 Procrustes analysis (A) and correlation analysis (B) based on Spearman correlation coefficient between moisture indicators and dominant fungal species
由图7A可知,主成分1(PC1)和主成分2(PC2)的方差贡献率分别为51.22%、23.44%,累计方差贡献率为74.66%,表明前两个主成分可以有效解释原始数据中大部分信息。同时,大曲的水分指标与优势真菌种两个数据集之间存在显著一致性(M2=1.251 9,P<0.05),表明两者之间存在关联性。 由图7B可知,水分含量与Aspergillus proliferans(P=0.019,相关系数r=0.72)呈显著正相关(P<0.05),与Thermomyces lanuginosus(P=0.009 3,相关系数r=-0.77)呈极显著负相关(P<0.01);水分活度与Aspergillus proliferans(P=0.013,相关系数r=0.75)呈显著正相关(P<0.05),与Candida tropicalis(P=0.003 1,相关系数r=0.830)呈极显著正相关(P<0.01),与Lichtheimia corymbifera(P=0.013,相关系数r=0.75)呈显著正相关(P<0.05),与Wallemia sp.(P=0.024,相关系数r=-0.70)呈显著负相关(P<0.05);不易流动水含量与Candida rugose(P=0.031,相关系数r=0.68)呈显著正相关(P<0.05)。
3 结论
本研究以采集自鲁西北运河产区某酒厂的中高温大曲和高温大曲为研究对象,采用PacBio SMRT测序技术解析2种大曲的真菌群落结构,通过常规理化检测方法和低场核磁共振技术对大曲的水分含量、水分活度、结合水含量、不易流动水含量和结合水含量进行测定,并对优势真菌与水分指标之间的相关性进行分析。 测序结果表明,中高温大曲以多育曲霉(Aspergillus proliferans)为主,高温大曲以疏棉状嗜热丝孢菌(Thermomyces lanuginosus)为主。线性判别分析效应大小(LEfSe)共鉴定出12种显著差异物质,其在2种类型大曲中存在明显差异,其中Aspergillus proliferans和Thermomyces lanuginosus可分别作为中高温和高温大曲的生物标志物。 相关性分析结果表明,优势真菌种与水分指标之间呈现显著或极显著相关性(P<0.05或P<0.01)。本研究结果可为提升鲁西北运河产区中高温和高温大曲品质提供科学依据。
[1]CAO D, LV J, CHU J, et al.Relationship between dynamic changes of microorganisms in Qupi and the quality formation of Fengxiangxing Huairang Daqu[J].Front Microbiol,2024,15(7):1435765.
[2]DENG J,ZHENG J,HUANG D,et al.Characterization of physicochemical properties,volatile compounds and microbial community structure in four types of Daqu[J].LWT-Food Sci Technol,2023,184(7):115064.
[3]ZHU M,DENG Z,TIE Y,et al.Unveiling the synthesis of aromatic compounds in sauce-flavor Daqu from the functional microorganisms to enzymes[J].Food Res Int,2024,190(8):114628.
[4]LUO Y, WU L, WU M, et al.Intelligent manufacturing challenges and directions of the Baijiu starter culture-Daqu industry: Microbiome and engineering perspectives[J].Trends Food Sci Tech,2024,153(11):104724.
[5]王秀秀,吕志远,刘玉涛,等.大曲微生物群落结构及其风味组分相关性研究[J].酿酒科技,2025(2):31-38.
[6]PU S,ZHANG Y,LU N,et al.Yeasts from Chinese strong flavour Daqu samples:Isolation and evaluation of their potential for fortified Daqu production[J].Amb Express,2021,11(1):176.
[7]LI W, HAN M, ZHANG H, et al.Exploring the differences in sauceflavour Daqu from different regions and its contribution to Baijiu brewing based on microbial communities and flavours[J].Int J Food Sci Tech,2024,59(10):7357-7371.
[8]孙羊羊,尹亚格,吴雨甍,等.基于高通量测序技术分析天津高温大曲微生物菌群多样性[J].中国酿造,2023,42(5):28-34.
[9]ZENG X,LI T,CAO W,et al.Proposal of a novel standard for determining the aging period of high-temperature Daqu based on the species-level bacterial composition through PacBio sequencing[J].Indian J Microbiol,2024,12(12):1-11.
[10]LIU S,ZHOU Y,MA D,et al.Environment microorganism and mature Daqu powder shaped microbial community formation in mechanically strong-flavor Daqu[J].Food Biosci,2023,52(4):102467.
[11]崔海灏,孟姣姣.大曲质量与原料粉碎度、水分的关系研究[J].酿酒,2016,43(2):86-88.
[12]吴正坤,刘蒲临,杨团元,等.不同贮存期高温大曲微生物群落演替与理化指标相关性分析[J].中国酿造,2023,42(7):160-166.
[13]SUN T,HU X,TIAN J,et al.Combination of spectral and spatial information of hyperspectral imaging for the prediction of the moisture content and visualizing distribution in Daqu[J].J Am Soc Brew Chem,2023,81(1):181-189.
[14]HUANG H,HU X,TIAN J,et al.Multigranularity cascade forest algorithm based on hyperspectral imaging to detect moisture content in Daqu[J].J Food Process Eng,2021,44(3):e13633.
[15]纪圩,廖辉,吴梦尧,等.中高温大曲发酵过程中芽孢杆菌生物膜对保水性的调控机制研究[J].食品与发酵工业,2025,51(22):32-40.
[16]薛汇贤,陈晓月,张元勋,等.影响德州市武城县农户济麦22种植行为的因素剖析[J].中国种业,2025(4):18-26.
[17]李玉梅,司徒慧媛,高加龙,等.温度波动对大黄鱼冷链流通期间鲜度品质及水分迁移的影响[J].食品与发酵工业,2024,50(1):211-218.
[18]陈骏飞,申挥,张珂铭,等.嗜根考克氏菌与植物乳植杆菌复合发酵对香肠品质及细菌群落的影响[J].肉类研究,2025,39(2):1-10.
[19]ZHOU Q,MA K,SONG Y, et al.Exploring the diversity of the fungal community in Chinese traditional Baijiu Daqu starters made at low-,medium-and high-temperatures[J].LWT-Food Sci Technol,2022,162:113408.
[20]ZONG E,BO T,DANG L,et al.Different functions can be provided by low temperature Daqu with different appearance features due to variations in the microbial community structure during fermentation[J].LWT-Food Sci Technol,2024,193(1):115763.
[21]YANG Y,NIU M S,YU H,et al.Exploring the contribution of temperature-adapted microbiota to enzyme profile of saccharification in Daqu using metagenomics and metaproteomics[J].LWT-Food Sci Technol,2024,197(4):115916.
[22]LIU Y,LI X,LI H,et al.Taorong-type Baijiu starter:Analysis of fungal community and metabolic characteristics of middle-temperature Daqu and high-temperature Daqu[J].Plos One,2022,17(10):e0274881.
[23]崔梦君,王玉荣,侯强川,等.基于三代测序技术高温和中高温大曲真菌多样性解析及酵母菌的分离鉴定[J].食品工业科技,2025,46(2):175-183.
[24]王勇,张育铭,朱洪磊,等.高效纤维素降解菌的筛选及产酶活力测定[J].江苏农业科学,2020,48(23):255-260.
[25]SURKOVA D,LAVRENOVA V,KLYAGIN S,et al.Screening of proteases produced by Aspergillus micromycetes active against proteins of the hemostasis system[J].Curr Med Mycol,2023,9(1):8-13.
[26]SHAMA Z,MUNIBA J,SHOMAILA S,et al.Thermomyces lanuginosus:A prospective thermophilic fungus for green synthesis and stabilization of BioAgNPs through glucoamylase[J].Mater Chem Phys,2023,297,127442.
[27]SINGH S, MADLALA A M, PRIOR B A. Thermomyces lanuginosus:Properties of strains and their hemicellulases[J].FEMS Microbiol Rev,2003,27(1):3-16.
[28]韩冰玙,陈辉太,李宗军.酱、浓、清香型白酒酿造过程中真菌及其功能特性研究进展[J].中国酿造,2024,43(3):27-32.
[29]LIU Q,LI X,SUN C,et al.Effects of mixed cultures of Candida tropicalis and aromatizing yeast in alcoholic fermentation on the quality of apple vinegar[J].3 Biotech,2019,9(4):1-10.
[30]QUEIROZ S S,JOFRE F M,BIANCHINI I A,et al.Current advances in Candida tropicalis:Yeast overview and biotechnological applications[J].Biotechnol Appl Biochem,2023,70(6):2069-2087.
[31]DA CRUZ M O, LEE H B, CORDEIRO T R L, et al.Description of a novel coprophilous Lichtheimia (Mucoromycotina, Mucorales) species with notes on Lichtheimia species and an identification key for the genus[J].Mycol Prog,2024,23(1):12-26.
[32]SILVA C A A, LACERDA M P F, LEITE R S R, et al.Production of enzymes from Lichtheimia ramosa using Brazilian savannah fruit wastes as substrate on solid state bioprocessess[J].Electron J Biotechn,2013,16(5):2225.
[33]姚粟,王鹏辉,白飞荣,等.中国传统发酵食品用微生物菌种名单研究(第二版)[J].食品与发酵工业,2022,48(1):272-307.
[34]侯小歌,惠明,王文琪,等.不同品种小麦中温大曲真菌群落多样性及其品质分析[J].中国酿造,2024,43(7):162-170.
[35]冯智伟,郭松波,孙朋朋,等.酱香型白酒高温大曲贮曲过程理化性质与微生物演替规律分析[J].中国酿造,2024,43(9):44-49.
[36]张霞,雷学俊,王晓妹,等.一株粉状米勒氏酵母的耐受性及所产挥发性风味物质研究[J].中国酿造,2024,43(4):39-44.
[37]GRYGIER A,MYSZKA K,RUDZIN′ SKA M.Galactomyces geotrichummoulds from dairy products with high biotechnological potential[J].Acta Sci Polon Techn,2017,16(1):5-16.
[38]ZENG H,JIANG X,WANG Z,et al.Environmental and physicochemical characterization and fungal community of two batches of Chinese Luzhou-flavored Daqu[J].J Am Soc Brew Chem,2023,81(1):190-197.
[39]WANG Y, GAI J, HOU Q, et al.Ultra-high-depth macrogenomic sequencing revealed differences in microbial composition and function between high temperature and medium-high temperature Daqu[J].World J Microb Biot,2023,39(12):337.
[40]曹杨,徐梦雪,徐平,等.包装方式对鲜湿豆丝贮藏品质的影响[J].中国调味品,2025,50(3):60-67.
[41]吴晓龙,涂宗财,胡月明,等.不同高温处理方式对草鱼肉理化性质及滋味品质的影响[J].食品工业科技,2024,45(19):84-93.