“曲乃酒之骨”,在白酒酿造中,酒曲是集“产酒、生香”等功能于一体的复合微生态制品,为粮食谷物等原料提供了丰富的菌群以及酶系,是白酒酿造的动力源泉[1]。根据不同的制曲工艺可将酒曲分为:大曲、小曲、麸曲等,其中以大曲为糖化发酵剂酿造的白酒风味更为丰富、醇厚,是中国白酒品质的象征,如茅台、五粮液、汾酒等均是采用大曲酿造。
大曲是以小麦、大麦、豌豆等为原料,其制曲方式具有生料制坯、自然接种、菌酶共存的特点,通常根据制曲顶火温度可分为低温大曲(以清香型为代表)、中温大曲(以浓香型为代表)、高温大曲(以酱香型为代表)等[2]。目前,关于浓香型大曲微生物群落结构的研究较多,基本确定浓香型大曲真菌以嗜热子囊菌属(Thermoascus)、嗜热真菌属(Thermomyces)、扣囊复膜酵母属(Saccharomycopsis)、红曲霉属(Monascus)、丝衣霉菌属(Byssochlamys)和曲霉属(Aspergillus)等为主[3-5],细菌以魏斯氏菌属(Weissella)、乳杆菌属(Lactobacillus)、葡萄球菌属(Staphylococcus)、片球菌属(Pediococcus)和明串珠菌属(Leuconostoc)等为优势菌群[6-7]。但不同地区浓香型大曲中的优势菌占比具有明显差异,如四川宜宾、泸州地区大曲中Weissella、高温放线菌 属(Thermoactinomyces)、Thermomyces、Thermoascus 比例高于遂宁地区大曲[8]。由于大曲固态发酵的空间异质性,在发酵过程中不同部位的发酵状态和外观特征存在显著差异[9],因此本研究以浓香型成品大曲为样本,将曲块由外到内分为曲皮、曲中、曲心三个部分,探究不同部位浓香型大曲理化指标及微生物群落结构差异,深入解析浓香型大曲微生物群落组成及其质量差异,旨在为大曲功能研究提供理论基础,同时为高品质大曲的生产提供指导。
1 材料与方法
1.1 材料与试剂
1.1.1 材料
大曲样品:取自四川绵阳某酒企,贮存期150 d,随机从三个曲房分别取样。
1.1.2 化学试剂
氢氧化钠、邻苯二甲酸氢钾、葡萄糖、硫酸铜、酒石酸钾钠、L-酪氨酸、酪蛋白、乙二胺四乙酸二钠(ethylene diamine tetraacetic acid,EDTA)-2Na、三羟甲基氨基甲烷(Tris base)、磷酸氢二钠、磷酸二氢钠、氯化钠(均为分析纯):成都科龙化工试剂厂;三氯乙酸(分析纯):上海阿拉丁生化科技股份有限公司;十六烷基三甲基溴化铵(cetyltrimethyl ammonium bromide,CTAB)、十二烷基硫酸钠(sodium lauryl sulfate,SDS)(均为分析纯):美国Sigma-aldrich公司;饱和酚(分析纯):北京索莱宝科技有限公司;福林试剂:上海源叶生物科技有限公司;溶菌酶(2×104 U/mg)、蜗牛酶(生化试剂):上海翊圣生物科技有限公司;己酸乙酯(色谱纯):国药集团化学试剂有限公司;AxyPrep 脱氧核糖核酸(deoxyribonucleic acid,DNA)凝胶回收试剂盒:北京华越洋生物科技有限公司。
1.2 仪器与设备
BS-2F数控恒温摇床培养箱:常州精成国华仪器有限公司;MJ-250培养箱:上海齐欣科学仪器有限公司;HWS-12型恒温水浴锅:上海一恒科学仪器有限公司;UV-2000型紫外可见分光光度计:上海美谱达仪器有限公司;PHS-3C型酸度计:上海博取仪器有限公司;MyCycler型聚合酶链式反应(polymerase chain reaction,PCR)仪、JY-SP-C型水平电泳槽、ChemiDoc XRS+型凝胶成像系统:美国Bio-Rad公司;Lynx6000高速落地离心机:美国Thermo公司;7890A/5975B气相色谱-质谱联用仪(gas chromatography-mass spectrometry,GC-MS):美国Agilent公司。
1.3 试验方法
1.3.1 样品处理
根据大曲横截面的特点,以火圈以外为曲皮,火圈以内以大约1∶1 的尺寸比例切取,分别作为曲中和曲心,粉碎后,过40目筛,保存至4 ℃。
1.3.2 大曲理化指标的测定
水分含量、酸度、发酵力、酸性蛋白酶活力、糖化酶活力的测定:参考《酿酒分析与检测》[10]。大曲酯化力的测定:参考《酿酒分析与检测》的方法制备酯化液,并通过GC-MS采用外标法对己酸乙酯进行测定。
大曲固态发酵质量损失的测定:称取高粱300 g,加入450 mL H2O,置于1 000 mL的丝口瓶中,放入灭菌锅中,于121 ℃中灭菌20 min后取出,冷却至约28 ℃时,加入90 mL无菌水、60 g大曲粉(以绝干计,精确至0.01 g),并拌匀。 密封后,称质量,置于28 ℃恒温箱内发酵15 d。 发酵完毕后,再次称质量,并计算发酵前后的质量差(g)。
1.3.3 大曲基因组的提取
参考文献[8]的方法采用CTAB法提取大曲DNA。
1.3.4 引物设计及扩增测序
针对细菌16S V3-V4区和真菌内转录间隔区(internal transcribed spacer,ITS)1区序列,设计带接头的特异引物。细菌引物为338F(5'-ACTCCTACGGGAGGCAGCAG-3')、806R(5'-GGACTACHVGGGTWTCTAAT-3'),真菌引物为ITS1F(5'-CTTGGTCATTTAGAGGAAGTAA-3')、ITS2R(5'-GCTGCGTTCTTCATCGATGC-3')[11]。PCR扩增条件:95 ℃预变性3 min;95 ℃变性30 s,55 ℃退火30 s,72 ℃延伸45 s,28个循环;72 ℃延伸10 min,10 ℃保持至停止。用2%琼脂糖凝胶电泳检测,并使用AxyPrep DNA凝胶回收试剂盒切胶回收PCR产物,随后送样测序。测序工作由上海美吉生物医药科技有限公司完成。
1.3.5 数据处理
大曲理化数据结果用“平均值±标准差”表示,使用SPSS 27.0软件中的单因素Duncan法对数据进行方差分析,并用Excel 2019软件绘图。
高通量测序完成后,去除有效序列中的非特异性扩增片段、模糊碱基、单碱基高重复区、长度过短的序列(序列长度<200 bp)以及PCR过程中产生的一些嵌合体,得到精准分析的优化序列。根据序列的相似性,将序列相似性大于97%分归为同一操作分类单元(operational taxonomic unit,OTU)[12],将所有序列与Silva库比对,得到序列的分类学信息。
2 结果与分析
2.1 不同部位浓香型大曲的理化指标
大曲理化指标测定可在一定程度上反映大曲的酿造性能。 不同部位浓香型大曲理化指标测定结果见表1。 由表1可知,不同部位浓香型大曲水分含量无显著差异(P>0.05),且均<11%,符合优质大曲的水分控制标准。较低的水分有利于制曲发酵所积累的微生物和酶能更好的保存,避免杂菌污染,从而使大曲的酿造性能保持稳定。曲中的酸度最高,显著高于曲皮和曲心(P<0.05)。这是由于曲中包含了大曲火圈部分,与杨勇等[13]研究发现,中高温成品大曲火圈部位酸度远高于曲皮和曲心的结果一致。酸性蛋白酶是大曲有机物分解的重要指标[14],在酸性条件下可以分解原料的蛋白质,生成多种氨基酸及多肽,提供氮源。曲皮的酸性蛋白酶活力最高,曲中和曲心的酸性蛋白酶活力显著低于曲皮(P<0.05),尤其是曲心的酸性蛋白酶活力几乎丧失。在酿造过程中,大曲糖化酶是将淀粉质原料分解为可发酵性糖最重要的酶。大曲糖化力呈现出曲皮>曲中>曲心的规律,且三者间存在显著差异(P<0.05),曲皮的糖化力比曲中、曲心分别高92%、132%。 张倩[15]研究发现,在制曲过程中,大曲糖化力在发酵初期最高,整个过程曲皮的糖化力始终高于曲心。造成这种现象的原因可能是糖化酶的主要贡献者—霉菌为好氧菌,大曲内部的缺氧环境限制了霉菌的生长代谢。 酯化力是衡量大曲生香能力的重要指标,其对白酒生成酯类风味物质具有至关重要的作用。曲皮的酯化力显著高于曲中和曲心(P<0.05)。曲皮的发酵力最高且显著高于曲心(P<0.05),与曲中的发酵力无显著差异(P>0.05),大曲发酵力的高低主要反映酿造中发酵速度的快慢。 为了更加贴近实际发酵模式,本试验首次采用了固态模拟发酵,通过发酵前后的质量差(即质量损失)评估大曲的发酵能力。结果发现,固态发酵质量损失与发酵力结果较为一致,均为曲皮>曲中>曲心,且差异显著(P<0.05),说明曲皮的发酵能力最好。 总体来看,曲皮在酸性蛋白酶活力、糖化力、酯化力、发酵力、质量损失等多个指标均优于曲中和曲心。任道群等[16]利用浓香型大曲外层和曲心分别进行投粮酿造,发现曲外层的出酒率、四大酯、总酯指标均低于曲心,而总酸反之,但该研究为下曲量一致,为根据曲样的指标特点进行取量调整,这可能由于曲皮糖化力、发酵力过高,导致窖内升温加速,无法缓慢发酵,从而升温、升酸快,影响出酒率和酒质。
表1 不同部位浓香型大曲理化指标
Table 1 Physicochemical indicators in different parts of strong-flavor Daqu

注:同列不同字母表示差异显著(P<0.05)。
部位 水分/%酸度/(mmol·100 g-1)酸性蛋白酶/(U·g-1)糖化力/(U·g-1)酯化力/(mg·g-1)发酵力/[gCO2·(g·72 h)-1]质量损失/g曲皮曲中曲心66.76±5.96a 51.57±3.51b 45.77±2.81c 9.53±0.83a 8.87±1.19a 8.47±0.59a 11.79±0.69b 14.22±0.68a 11.47±0.95b 15.23±6.44a 1.14±0.40b 0.01±0.00b 549.66±9.37a 285.96±15.95b 237.12±18.40c 10.08±0.45a 5.97±0.48b 5.75±1.51b 1.59±0.02a 1.43±0.17a 1.00±0.16b
2.2 不同部位浓香型大曲微生物Alpha多样性分析
Alpha多样性主要是用来评估样本菌群多样性的方法[17],Sobs表示所观测到的OTU数量。由表2可知,不同部位浓香型大曲Coverage指数均>0.99,说明测序结果能基本反映样品微生物真实情况。细菌OTU数量和丰富度指数ACE、Chao1均为曲心>曲中>曲皮,说明曲块由外到内微生物种类依次增加。分析多样性指数发现,Shannon指数为曲皮>曲中>曲心,而Simpson指数反之,表明细菌多样性为曲皮>曲中>曲心,这是由于Shannon、Simpson指数在反映物种多样性时,不仅考虑了物种数量,还考虑了物种相对丰富度的影响,即物种分布均匀度的影响,因此物种丰富度高不代表物种多样性高。真菌方面,大曲的OTU数量、丰富度指数、多样性指数表明曲皮的物种丰富度及多样性最高,并向内到曲心依次降低,这可能是由于大曲内部属于缺氧环境,不利于真菌的生长繁殖。
表2 不同部位浓香型大曲微生物Alpha多样性指数
Table 2 Alpha diversity indexes of microorganisms in different parts of strong-flavor Daqu
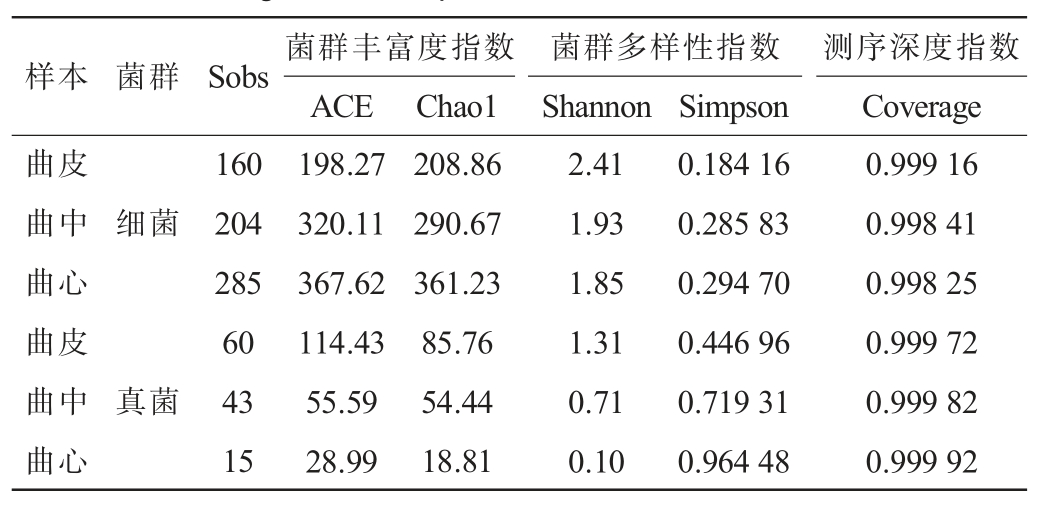
样本 菌群 Sobs 菌群丰富度指数ACE菌群多样性指数Shannon测序深度指数Coverage曲皮曲中曲心曲皮曲中曲心细菌真菌160 204 285 60 43 15 198.27 320.11 367.62 114.43 55.59 28.99 Chao1 Simpson 208.86 290.67 361.23 85.76 54.44 18.81 2.41 1.93 1.85 1.31 0.71 0.10 0.184 16 0.285 83 0.294 70 0.446 96 0.719 31 0.964 48 0.999 16 0.998 41 0.998 25 0.999 72 0.999 82 0.999 92
2.3 不同部位浓香型大曲细菌群落结构分析
2.3.1 基于门水平分类的细菌群落结构
基于门分类学水平,将相对丰度<1%的门归为一类,即others,将没有明确的分类信息的归为unclassified。由图1可知,不同部位浓香型大曲样品中的优势细菌门包括厚壁 菌 门(Firmicutes)、变 形 菌 门(Proteobacteria)、蓝 藻 门(Cyanobacteria)、拟杆菌门(Bacteroidetes),其中厚壁菌门是绝对的优势物种,相对丰度高达60.2%~87.8%,且在曲块不同部位中占比呈曲皮>曲中>曲心的趋势。另一类优势菌变形菌门在曲样中的相对丰度为8.5%~36.4%。此外,蓝藻门主要在曲皮中累积,相对丰度达3.32%,但在曲中和曲心内相对丰度较低,尤其在曲心的相对丰度仅0.13%;而拟杆菌门与蓝藻门相反,其在曲心中相对丰度为1.9%,且由内向外丰度依次降低,在曲皮的丰度仅0.12%。厚壁菌门和变形菌门成为大曲主要优势菌,原因是大曲水分含量较低,无法满足多数微生物的生长,而厚壁菌门类的微生物大多可产生芽孢,对恶劣环境具有较强的耐受性[18],变形菌门类微生物的遗传多样性极为丰富,涵盖了极为广泛的生理代谢类型,因此面对不同的环境能及时做出有利于自身生长的调节。
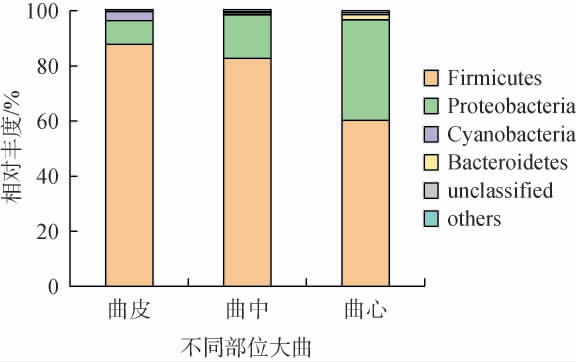
图1 基于门水平不同部位浓香型大曲中细菌群落结构
Fig.1 Bacterial community structure in different parts of strong-flavor Daqu at the phylum level
2.3.2 基于属水平分类的细菌群落结构
基于属分类学水平,将相对丰度占比<1%的属归为一类,即others,将没有明确的分类信息的统一归为unclas sified。由图2可知,在不同部位浓香型大曲样品中一共获得10个优势细菌属(相对丰度>1%),曲皮以Bacillus、Thermoactinomyces、Pseudomonas、Weissella、Lactobacillus、Cyanobacteria、Leuconostoc、Pantoea为优势菌,曲中以Bacillus、Thermoactinomyces、Pseudomonas、Weissella、Lactobacillus为优势菌,曲心以Bacillus、Thermoactinomyces、Pseudomonas、Lactococcus、Apibacter为优势菌。
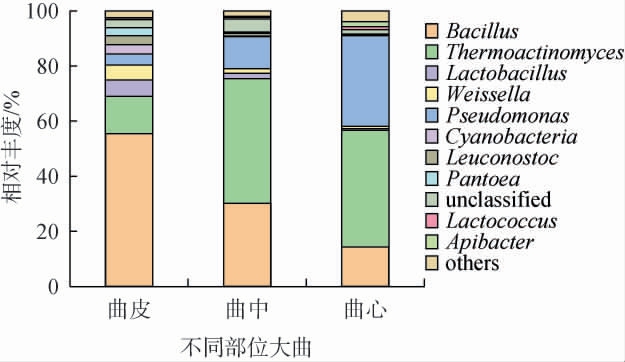
图2 基于属水平不同部位浓香型大曲中细菌群落结构
Fig.2 Bacterial community structure in different parts of strong-flavor Daqu at the genus level
综 合 分 析 发 现,Bacillus、Thermoactinomyces和Pseudomonas不同部位浓香型大曲样品中均占主导地位,三者比例之和分别占曲皮、曲中和曲心的73.1%、87%、89.6%。Bacillus、Weissella、Lactobacillus、Cyanobacteria、Leuconostoc、Pantoea均呈曲皮>曲中>曲心的规律,但Pseudomonas、Lactococcus、Apibacter呈相反趋势,其中Pseudomonas在曲心相对丰度高达32.9%。Thermoactinomyces在曲中和曲心的相对丰度达42%以上,但在曲皮相对丰度仅有13.6%,这是由于Thermoactinomyces是对温度具有极高的该耐受力,能产生气生菌丝和孢子,通常能在45~60 ℃的温度下繁殖[19-20]。通过分析细菌属的分布,发现虽然曲心和曲中的物种数量高于曲皮,但集中为Bacillus、Thermoactinomyces和Pseudomonas三类物种,其他较多的种群丰度较低,归入了others,而曲皮中各类优势菌的分布更加均匀,这与表1 中细菌Alpha多样性的分析结果一致。
2.4 不同部位浓香型大曲真菌群落结构分析
2.4.1 基于门分类水平的真菌群落结构
由图3可知,在不同部位浓香型大曲样品中获得的优势门类为子囊菌门(Ascomycota)、接合菌门(Zygomycota)。其中子囊菌门微生物占绝对优势,这与夏玙等[21-22]研究结果相同,Zygomycota在曲皮中少量存在,在曲中部位相对丰度高达24.2%,但在曲心中又几乎不存在。
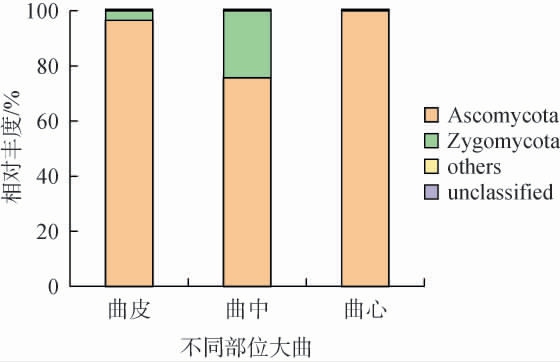
图3 基于门水平不同部位浓香型大曲中真菌群落结构
Fig.3 Fungal community structure in different parts of strong-flavor Daqu at the phylum level
2.4.2 基于属分类水平的真菌群落结构
由图4可知,在不同部位浓香型大曲样品中一共获得8个优势真菌属(相对丰度>1%),曲皮以Thermoascus、Aspergillus、Candida、Wickerhamomyces、Rhizomucor、Byssochlamys为优势菌,曲中以Thermoascus、Rhizomucor、Aspergillus、Rhizopus、Thermomyces为优势菌,曲心仅有Thermoascus一个优势菌属。有研究表明[23-26],在河南、湖北、四川等多个地区浓香型大曲占主导的优势真菌均为Thermoascus。
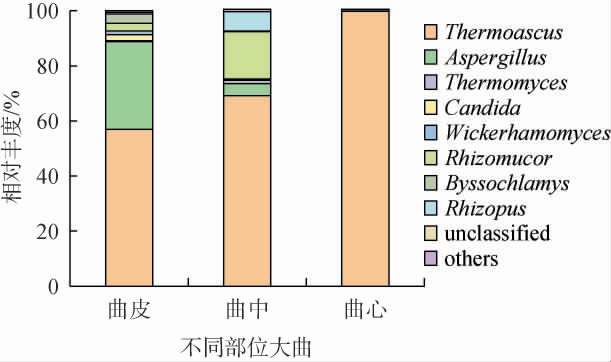
图4 基于属水平不同部位浓香型大曲中真菌群落结构
Fig.4 Fungal community structure in different parts of strong-flavor Daqu at the genus level
通过分析真菌属的分布,发现优势菌属种类数量曲皮>曲中>曲心,曲皮部位以Thermoascus、Aspergillus为主(二者占比88.7%),Candida、Rhizomucor、Byssochlamys、Wickerhamomyces呈均匀 分布,其中Candida、Byssochlamys、Wickerhamomyces仅在曲皮中为优势菌。 曲中部位优势菌属以Thermoascus、Rhizomucor为主(二者占比86.3%),且还包含Rhizopus、Aspergillus、Thermomyces三类优势菌,其中Rhizopus、Thermomyces仅为曲中的优势菌。而曲心的物种比较单一,Thermoascus占99.8%。 造成此现象的原因可能为在制曲过程中,曲块表层更易密集到环境微生物,同时真菌一般需要氧气才能生长繁殖,而曲块表层接触空气多,越到内部氧气越少,限制了真菌的生长,因此真菌多样性曲皮>曲中>曲心。
2.5 不同部位浓香型大曲微生物群落与理化指标关联性分析
在属分类水平上筛选分类学信息明确且相对丰度>1%的优势菌群,这些优势细菌属相对丰度占比94.2%,优势真菌属相对丰度占比99.7%。将其与理化指标相结合进行冗余分析(redundancy analysis,RDA),结果见图5。
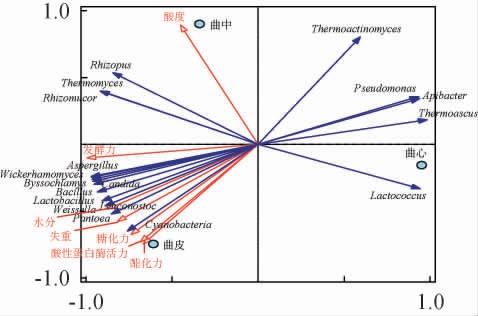
图5 不同部位浓香型大曲微生物群落与理化指标的冗余分析结果
Fig.5 Redundancy analysis results of microbial community and physicochemical indicators of different parts of strongflavor Daqu
由图5可知,物种信息与理化指标关系能被100%解释,其中第一轴能解释84.17%的变异信息,第二轴能解释15.83%的变异信息。Thermoactinomyces、Pseudomonas、Apibacter、Lactococcus、Thermoascus之间呈正相关且主要指向曲心;酶活(酸性蛋白酶、糖化力、酯化力)和发酵能力指标(发酵力、质量损失)与Aspergillus、Byssochlamys、Candida、Wickerhamomyces、Bacillus、Weissella、Lactobacillus、Cyanobacteria、Leuconostoc、Acetobacter之间呈高度正相关且主要指向曲皮;而Rhizomucor、Rhizopus、Thermomyces、Thermoactinomyces、Aspergillus、Byssochlamys与酸度之间呈正相关且主要指向曲中部位。 总体来看,影响曲皮的微生物种类更多,其次是曲中,而曲心微生物种类相较单一,微生物的差异会直接影响不同部位大曲的酿造特性。
3 结论
通过研究分析不同部位浓香型大曲的理化特性和微生物多样性,结果表明:酸性蛋白酶活力、糖化力、酯化力指标和发酵力、失重指标均为曲皮>曲中>曲心,一定程度反映了不同部位大曲的酿造性能。微生物多样性方面,在属分类水平上,曲皮含有Bacillus、Thermoactinomyces、Pseudomonas、Weissella、Lactobacillus、Cyanobacteria、Leuconostoc、Pantoea这8类优势细菌和Thermoascus、Aspergillus、Candida、Wickerhamomyces、Rhizomucor、Byssochlamys 这6类优势真菌,曲中含有Bacillus、Thermoactinomyces、Pseudomonas、Weissella、Lactobacillus这5类优势细菌和Thermoascus、Rhizomucor、Aspergillus、Rhizopus、Thermomyces这5类优势真菌,曲心含有Bacillus、Thermoactinomyces、Pseudomonas、Lactococcus、Apibacter这5类优势细菌和Thermoascus这1类优势真菌。 总的优势菌群种类为曲皮>曲中>曲心。 通过RDA发现,酶活指标和发酵能力指标与Aspergillus、Byssochlamys、Candida、Wickerhamomyces、Bacillus、Weissella、Lactobacillus、Cyanobacteria、Leuconostoc、Acetobacter之间具有较强相关性,而Rhizomucor、Rhizopus、Thermomyces和酸度之间相关性较强。
综上,大曲的酶活及发酵性能指标和优势菌群数量总体呈曲皮>曲中>曲心的规律,但该结果与传统制曲工艺要求的“皮薄”常识相冲突。由于此类试验粮、曲消耗巨大,导致目前相关研究较少。因此结合大曲不同部位的指标特点,以适宜的投曲比例开展酿造效果对比是未来的研究方向之一,也是优化制曲工艺的重要途径之一。
[1]泸州老窖集团有限责任公司.泸型酒技艺大全[M].北京:中国轻工业出版社,2011:156-158.
[2]韩培杰.中国白酒大曲微生物多样性研究[D].福州:福建农林大学,2023.
[3]DENG J,ZHENG J,HUANG D,et al.Characterization of physicochemical properties,volatile compounds and microbial community structure in four types of Daqu[J].LWT-Food Sci Technol,2023,184:115064.
[4]周虞.浓香大曲复产前后微生物差异及环境来源解析[D].无锡:江南大学,2023.
[5]YANG Y, WANG S T, LU Z M, et al.Metagenomics unveils microbial roles involved in metabolic network of flavor development in mediumtemperature Daqu starter[J].Food Res Int,2021,140:110037.
[6]圣群航,王俊麟,彭东,等.襄阳地区中温大曲细菌多样性及其滋味品质解析[J/OL].食品与发酵工业,1-12[2025-08-23].https://doi.org/10.13995/j.cnki.11-1802/ts.042884.
[7]HE M,JIN Y,ZHOU R,et al.Dynamic succession of microbial community in Nongxiangxing Daqu and microbial roles involved in flavor formation[J].Food Res Int,2022,159:111559.
[8]吴树坤,谢军,卫春会,等.四川不同地区浓香型大曲微生物群落结构比较[J].食品科学,2019,40(14):144-152.
[9]WEN Z,HAN P J,HAN D Y,et al.Microbial community assembly patterns at the species level in different parts of the medium temperature Daqu during fermentation[J].Curr Res Food Sci,2024,9:100883.
[10]王福荣.酿酒分析与检测.第2版[M].北京:化学工业出版社,2012:10-17.
[11]ZHOU Y,LI Y,DONG Y,et al.Microbial community of Nongxiangxing Daqu during storage: microbial succession, assembly mechanisms and metabolic functions[J].J Sci Food Agr,2025,105(7):3665-3678.
[12]SCHMIDT T S B, MATIAS RODRIGUES J F, MERING C V, et al.Limits to robustness and reproducibility in the demarcation of operational taxonomic units[J].Environ Microbiol,2015,17(5):1689-1706.
[13]杨勇,李燕荣,姜雷,等.中高温大曲曲块部位间生化指标的差异及变化规律[J].食品与发酵工业,2019,45(19):73-78.
[14]LI P, LIN W, LIU X, et al.Environmental factors affecting microbiota dynamics during traditional solid-state fermentation of Chinese Daqu starter[J].Front Microbiol,2016,253(7):1237.
[15]张倩.中高温大曲发酵过程中曲皮和曲心微生物群落结构和功能差异及形成机制[D].宜宾:四川轻化工大学,2021.
[16]任道群,唐玉明,姚万春,等.浓香型大曲曲外层和曲心的差异研究[J].酿酒科技,1997(6):13-14.
[17]YAN C,HUANG Z,TU R,et al.Revealing the differences in microbial community and quality of high-temperature Daqu in the Southern Sichuan-Northern Guizhou region[J].Foods,2025,14(4):570.
[18]WOLF M,MÜLLER T,DANDEKAR T,et al.Phylogeny of Firmicutes with special reference to Mycoplasma(Mollicutes)as inferred from phosphoglycerate kinase amino acid sequence data[J].Int J Syst Evol Micr,2004,54(3):871-875.
[19]冯慧军,翟磊,程坤,等.高温放线菌属研究进展[J].食品与发酵工业,2017,43(11):257-261.
[20]翟威涛,吴双全,柴丽娟,等.酱酒酒醅中普通高温放线菌的筛选及其挥发性物质代谢分析[J].食品科学,2025,46(12):118-126.
[21]夏玙,罗惠波,周平,等.不同处理方式的大曲真菌群落差异分析[J].食品科学,2018,39(22):166-172.
[22]王生艳,孙亮霞,赵新民,等.中高温大曲发酵过程中曲皮、曲心微生物群落的差异性和变化规律[J].中国酿造,2024,43(11):92-98.
[23]王清龙,李海登,刘延波,等.河南不同地区浓香型白酒大曲理化性质和微生物多样性分析[J].中国酿造,2022,41(11):31-38.
[24]杨少勇,黎婷玉,蔡文超,等.襄阳地区高温大曲和中高温大曲真菌多样性解析[J].中国酿造,2021,40(5):76-80.
[25]刘孟华,陈仪,樊科权,等.不同制曲季节浓香型大曲真菌群落结构多样性的研究[J].食品与发酵科技,2024,60(3):82-85
[26]邓杰,张曼,周杰,等.2种浓香型白酒大曲中微生物群落结构及功能研究[J].食品科学技术学报,2024,42(4):75-85.