白酒产业作为我国的传统产业,2023年我国的白酒产量达44.9亿升,据估算生产1 t酒精度为65%vol的白酒约耗水60 t,产生废水48 t,同时产生约废水量3%的酿酒污泥[1]。酒厂污泥中有机质、氮、磷、钾等养分及水分含量很高,在收集、转运及处置的过程中,不仅容易产生二次污染还会导致资源的大量浪费,因此,酒厂污泥的处置和资源化是酒厂污水处理的最后一个难点。
好氧堆肥是酒厂污泥资源化利用的重要手段,不仅能实现污泥的减量化、无害化,还能作为园林绿化的栽培用土和有机肥料,实现资源化利用。由于酒厂污泥与城市污泥来源不同,营养成分存在显著差异[1-2],导致其好氧堆肥过程中物料转化存在差异,刘阳等[3]使用酿酒酒槽与酒厂污泥共堆肥,为酿酒酒槽与酒厂污泥的处理提供了新思路;LIANG F等[4]研究发现,添加低共熔溶剂可以减少酒厂污泥堆肥时的氨气减排;潘昌滨等[5]研究发现,加入蚯蚓促进了酒厂污泥堆肥的肥效,减少了堆肥的营养损失。此外,堆肥规模是影响堆肥效果的重要因素,而目前对于酒厂污泥堆肥的中试研究报道较少,由规模放大引起的堆肥条件改变和堆肥过程中微生物的作用尚需要进一步研究;同时,超高温堆肥可以加速污泥水分蒸发、加快堆肥腐熟和提高无害化程度。 因此,探究中试规模酒厂污泥超高温好氧堆肥的腐熟过程及其微生物群落演替规律,对后续酒厂污泥好氧堆肥的工业化应用具有重要意义。
基于此,本研究以酒厂污泥为主料,鸡粪和锯木屑为辅料,利用超高温专用菌剂进行为期35 d的超高温好氧堆肥中试实验,探究中试规模下酒厂污泥好氧堆肥的理化性质的变化规律,并通过高通量测序研究细菌群落结构演替规律,为酒厂污泥好氧堆肥的规模化应用提供数据支撑。
1 材料与方法
1.1 材料与试剂
1.1.1 材料与菌剂
酒厂污泥(脱水)、鸡粪和锯木屑:产地四川。堆肥原料的基本理化性质见表1。
表1 堆肥原料的基本理化性质
Table 1 Basic physicochemical properties of compost raw materials
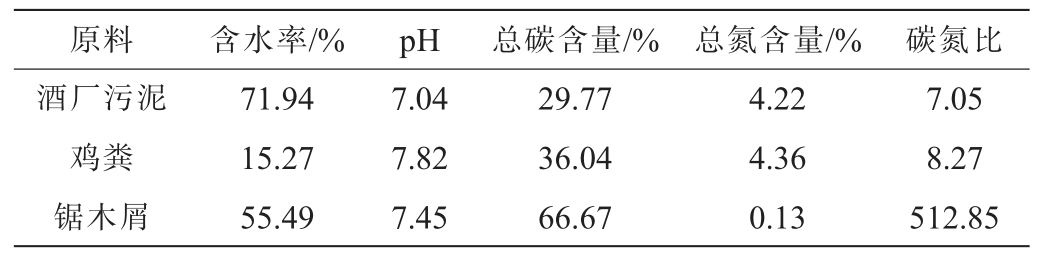
原料 含水率/% pH 总碳含量/% 总氮含量/% 碳氮比酒厂污泥鸡粪锯木屑71.94 15.27 55.49 7.04 7.82 7.45 29.77 36.04 66.67 4.22 4.36 0.13 7.05 8.27 512.85
超高温专用菌剂:本实验室自主研发,包括6株细菌,分别为枯草芽孢杆菌(Bacillus subtilis)B1和B6、嗜热脂肪地芽孢杆菌(Geobacillus stearothermophilus)B7、努比卤地无氧芽胞杆菌(Anoxybacillus rupiensis)B9、B11和Q-3,3株分解木质素和纤维素的真菌1799、3316和Y-1,2株高温放线菌(Thermobifida fusca)Y-2和Q-0。
1.1.2 试剂
基因组脱氧核糖核酸(deoxyribonucleic acid,DNA)提取试剂盒:北京诺博莱德科技有限公司;氯化钾、硫酸、盐酸、苯酚(均为分析纯):四川西陇科学有限公司;磷酸(分析纯):成都市科隆化学品有限公司;硫酸钾、硫酸铜、氨基磺酸(均为分析纯):天津博迪化工股份有限公司;二氯异氰尿酸钠、磺胺(均为分析纯):上海阿拉丁生化科技股份有限公司;N-(1-萘基)乙二胺盐酸盐(分析纯):天津市科密欧化学试剂有限公司。
1.2 仪器与设备
LCD-281 S型手持式数显温度计:天津市胜杰仪器仪表有限公司;P4PC型紫外可见分光光度计:上海美谱达仪器有限公司;S230-USP/EP型电导率仪、FE28-Bio型pH计:梅特勒-托利多仪器(上海)有限公司;Kjeltec 2200型凯氏定氮仪:瑞典FOSS公司;Vario Macro CHNS-O-CL型元素分析仪:德国elementar公司;LRH-70型生化培养箱:上海一恒科学仪器有限公司;202-OAB型电热恒温干燥箱:天津市泰斯特仪器有限公司;SHA-B型双功能水浴恒温振荡器:常州市金坛区指前镇旭日实验仪器厂;KSW-12-12型电炉温度控制器、SX2-8-10型箱式电阻炉:北京科伟永兴仪器有限公司;R2000-30型电子计重计数秤:奥豪斯仪器(常州)有限公司;Bio-Rad T100梯度聚合酶链式反应(polymerase chain reaction,PCR)仪:美国BIO-RAD公司;Illumina Nova Seq 6000 PE250高通量测序平台:美国Illumina公司。
1.3 方法
1.3.1 酒厂污泥超高温好氧堆肥
以酒厂污泥为主料,鸡粪和锯木屑为辅料,按照酒厂污泥、鸡粪和锯木屑的质量比7∶2∶1充分混合,调节含水率为55%~60%,添加辅料湿质量的1‰的超高温专用菌剂进行堆肥。堆体长4.5 m、宽3.5 m和高1.5 m。堆肥期间利用涡轮增压风机进行强制通风,每7天进行一次人工翻堆。在堆肥的第0天、第7天、第14天、第21天、第28天和第35天从堆体中部分别取3个样品,编号为D.0、D.7、D.14、D.21、D.28、D.35,每个样品分为3份,其中,一份1 kg置于4 ℃冰箱中保存,一份100 g风干磨碎后过80目筛于室温下保存,一份50 g于-80 ℃超低温冰箱中保存。
1.3.2 理化指标的测定
温度测定:堆肥过程中,每日上午和下午采用手持式数显温度计测量堆肥(上层、下层各布设3个测温点)和环境温度,分别取平均值作为当日温度;含水率的测定:参照GB/T 8576—2010《复混肥料中游离水含量的测定 真空烘箱法》;有机质含量的测定:参照HJ 761—2015《固体废物有机质的测定灼烧减量法》;电导率(electrical conductivity,EC)的测定:参照HJ 802—2016《土壤 电导率的测定 电极法》;pH值和种子发芽指数的测定:分别参照NY/T 525—2021《有机肥料》中的附录E、F。 全氮含量的测定:参照HJ 717—2014《土壤质量 全氮的测定 凯氏法》;铵态氮、亚硝态氮含量的测定:参照HJ 634—2012《土壤 氨氮、亚硝酸盐氮、硝酸盐氮的测定 氯化钾溶液提取-分光光度法》;硝态氮含量的测定:参照GB/T 32737—2016《土壤硝态氮的测定 紫外分光光度法》;计算总氮(全氮+硝态氮+亚硝态氮)含量。 总碳含量的测定:采用Vario Macro CHNS-O-CL型元素分析仪;富里酸、胡敏酸和胡敏素含量的测定:参照NY/T 1867—2010《土壤腐殖质组成的测定 焦磷酸钠-氢氧化钠提取重铬酸钾氧化容量法》。样品鲜质量的测定:采用R2000-30型电子秤测定,并计算鲜质量减量率、干物质减量率和水分减量率,其计算公式如下:
干物质减量率=1-(堆肥后鲜质量-堆肥后鲜质量×堆肥后含水率)/(堆肥前鲜质量-堆肥前鲜质量×含水率)×100%
1.3.3 高通量测序
对-80 ℃保存的样品使用土壤和粪便基因组DNA提取试剂盒提取基因组DNA,以其为模板,采用通用引物515F(5'-GTGCCAGCMGCCGCGGTAA-3')和806R(5'-GGACTACHVGGGTWTCTAAT-3')PCR扩增16S rRNA V4区基因序列。PCR扩增体系:PhusionR High-Fidelity PCR Master Mix 15 μL、引物515F和806R(1 μmol/μL)各0.2 μL、基因组DNA 10 ng。PCR扩增条件:98 ℃变性10 min;98 ℃变性10 s、50 ℃退火30 s和72 ℃延伸30 s,共30次循环;72 ℃再延伸5 min。将PCR扩增产物纯化后送至北京诺禾致源科技股份有限公司基于Illumina NovaSeq PE250平台对细菌16S rRNA V4区基因序列进行高通量测序。
1.3.4 数据处理
理化性质数据使用Excel 2019软件整理,并采用Origin软件进行绘图。高通量测序结果根据Barcode序列进行拆分获得样品的原始数据,去除Barcode和引物后通过FLASH软件对序列数据进行拼接,使用fastp软件(Version 0.23.1)对拼接的Tags进行质控,通过物种注释数据库(Silva database https://www.arb-silva.de/for 16S/18S,Unite database https://unite.ut.ee/for ITS)进行比对检测嵌合体序列,并去除其中的嵌合体序列,之后使用QIIME2(Version QIIME2-202202)软件中的DADA2模块对序列进行降噪得到特征序列,采用Silva 138.1数据库进行物种注释,使用QIIME2软件进行Alpha多样性分析。使用Canoco5.0软件进行冗余分析(redundancy analysis,RDA),采用生科云分析平台(https://www.bioincloud.tech)进行相关性分析。
2 结果与分析
2.1 超高温好氧堆肥过程中理化指标的变化
2.1.1 温度
超高温好氧堆肥过程中环境及堆肥温度的变化见图1。由图1可知,堆肥过程中环境温度在15~25 ℃范围内波动变化,堆肥温度则呈先快速上升后上下波动的趋势。堆肥初期,由于强制曝气促进有机物质的降解产生大量的热,导致堆肥温度迅速升高,于第5天到达峰值69.3 ℃,之后温度呈现出上下波动的趋势,这主要与调整曝气量和翻堆有关,堆肥温度于第16天达到最高(73.2 ℃)。在35 d超高温好氧堆肥过程中,温度>55 ℃的高温阶段共11 d,说明堆肥有效杀灭了污泥中的病原菌满足堆肥无害化要求[6]。 随着易分解有机物的降解和微生物代谢活动减弱,堆肥温度逐渐下降,堆肥结束时,堆肥温度降低至30.0 ℃左右,接近环境温度。
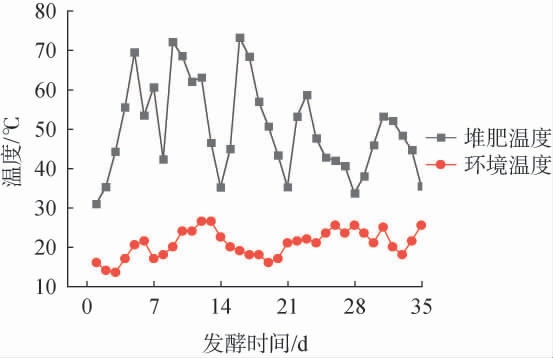
图1 超高温好氧堆肥过程中环境及堆肥温度的变化
Fig.1 Changes in environment and compost temperature during ultra-high temperature aerobic composting process
2.1.2 pH值与电导率
超高温好氧堆肥过程中堆肥pH值及电导率的变化见图2。由图2可知,堆肥过程中,堆肥的pH值呈先上升后下降在7.7附近小幅波动。分析原因可能是,堆肥前期,可利用的有机质含量高,氨化微生物繁殖和分解速度快,蛋白质等有机质被快速降解,铵根离子含量快速升高,导致堆肥pH值快速升高;堆肥后期,有机质降解速率减慢,氨化速率低于硝化速率,导致堆肥pH值下降并趋于稳定。堆肥过程中,EC值的变化趋势与pH值变化趋势一致,由开始时的2.84 ms/cm上升至4.08 ms/cm后下降至3.6 ms/cm并趋于稳定,与常远等[7]的研究结果类似。分析原因可能是,堆肥初期,有机质的降解导致堆肥中可溶性盐含量升高,从而使EC值上升;在堆肥后期,由于矿物盐的沉淀和微生物的消耗使得EC值出现下降并趋于稳定。
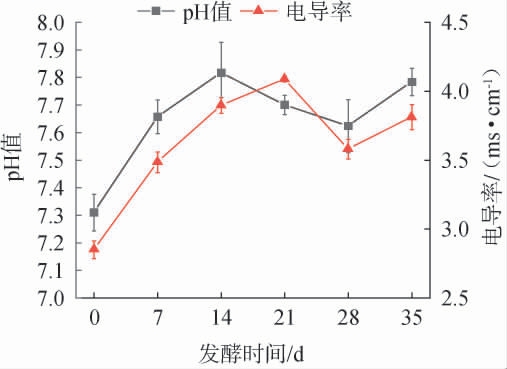
图2 超高温好氧堆肥过程中pH值和电导率的变化
Fig.2 Changes in pH value and electric conductivity during ultra-high temperature aerobic composting process
2.1.3 减量率与含水率
超高温好氧堆肥过程中堆肥减量率和含水率的变化见图3。由图3可知,堆肥过程中,堆肥的鲜质量和水分减量率均呈持续上升趋势,干物质减量率呈先上升后维持稳定的趋势;堆肥含水率则呈下降趋势。 干物质减量率的变化与李龙涛等[8]的研究结果类似,由于微生物的代谢消耗和高温导致的氨气损失等,在堆肥0~14 d干物质减量率快速上升,而后稳定在23%左右。样品的鲜质量由干物质和水分组成,在堆肥0~14 d鲜质量减量率快速上升,是因为此时干物质和水分均在快速减量,之后由于干物质减量缓慢,鲜质量减量基本都来自于水分的减量,堆肥结束时鲜质量减量率为50.70%。 含水率呈持续下降趋势可能是因为堆肥产生的高温使含水率快速下降,由初始的55.7%下降至28.2%,与余杰等[9]的结果类似。
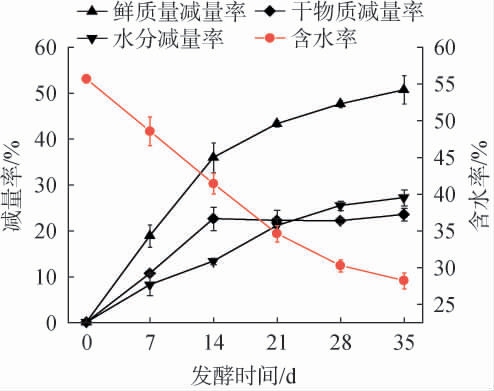
图3 超高温好氧堆肥过程中含水率和减量率的变化
Fig.3 Changes in moisture contents and decrement rates during ultra-high temperature aerobic composting process
2.1.4 总氮含量与碳氮比
超高温好氧堆肥过程中堆肥总氮含量和碳氮比的变化见图4。
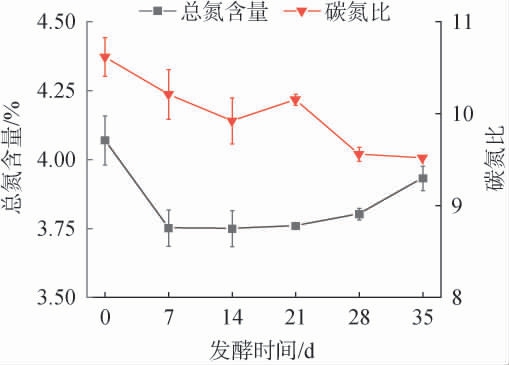
图4 超高温好氧堆肥过程中总氮含量和碳氮比的变化
Fig.4 Changes in total nitrogen contents, carbon and nitrogen ratio during ultra-high temperature aerobic composting process
由图4可知,堆肥过程中,堆肥总氮含量呈先下降后上升的趋势,由初始的4.07%降至堆肥结束时的3.93%,这与李思敏等[10]的研究结果类似。堆肥碳氮比总体呈下降趋势,由于堆肥原料初始碳氮比较低,导致碳氮比下降并不明显,堆肥结束时碳氮比由初始的10.40下降至堆肥结束时的9.63,与周有为等[11]的研究结果类似。
2.1.5 铵态氮和硝态氮含量
超高温好氧堆肥过程中堆肥铵态氮和硝态氮含量的变化见图5。由图5可知,堆肥过程中,铵态氮的含量呈先上升后下降的趋势,并在堆肥14 d以后稳定在6 g/kg左右。 分析原因可能是,堆肥初期由于含氮有机物快速分解导致铵态氮含量迅速上升,在堆肥第7天达到最高(24.58 g/kg);随着高温和翻堆,导致氨气大量挥发,加之微生物的硝化作用、固定化作用[12],导致堆肥铵态氮含量迅速下降。堆肥结束时,铵态氮含量为6.71 g/kg,较初始值下降了44.45%。硝态氮含量总体呈升高趋势,由初始的205.55 mg/kg上升到堆肥结束时的327.46 mg/kg。分析原因可能是,堆肥初期氨化微生物活性强,氨化作用占据主导地位,此时由于硝化底物铵态氮含量的增加,微生物硝化作用增强,硝态氮含量升高;随着堆肥温度的降低,堆肥硝化微生物的活性增加,有机质分解基本完全,氨化作用减弱,加速了铵态氮向硝态氮的转化,硝态氮含量逐渐升高并维持稳定[13]。
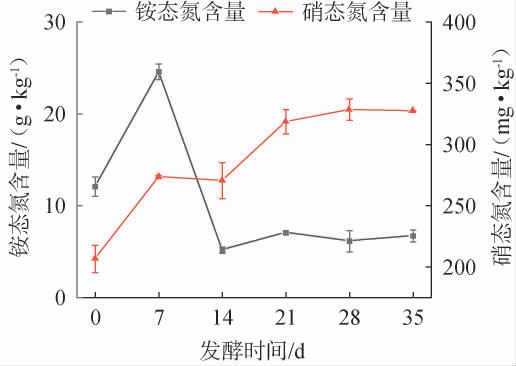
图5 超高温好氧堆肥过程中铵态氮和硝态氮含量的变化
Fig.5 Changes in ammonium nitrogen and nitrate nitrogen contents during ultra-high temperature aerobic composting process
2.1.6 腐殖酸和胡敏素含量
腐殖质含量是体现堆肥腐熟度的重要指标[14],超高温好氧堆肥过程中富里酸、胡敏酸和胡敏素含量的变化见图6。由图6可知,原料中总腐殖质(腐植酸与胡敏素之和)含量丰富,达到324.85 g/kg;堆肥过程中,胡敏酸含量持续上升,由初始的14.23 g/kg上升至堆肥结束时的59.24 g/kg,而富里酸和胡敏素含量持续下降,分别由初始的44.29 g/kg、264.48 g/kg下降至堆肥结束时的21.66 g/kg、185.88 g/kg,这与唐显梅等[15]的研究结果类似。 分析原因可能是,堆肥初期富里酸含量较高,容易被微生物消耗或转化为更复杂的胡敏酸[16];胡敏素是与矿物质紧密结合的腐殖物质,由于微生物的代谢消耗导致胡敏素含量下降[17]。
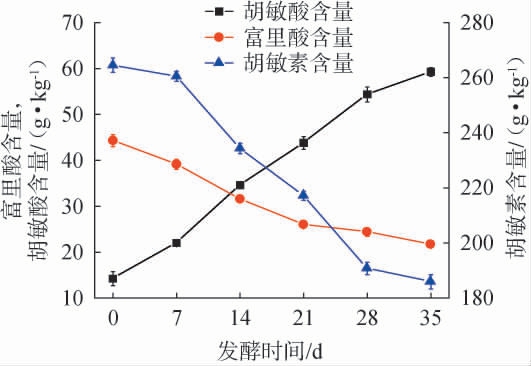
图6 超高温好氧堆肥过程中腐殖酸和胡敏素含量的变化
Fig.6 Changes in humic acid and humin contents during ultra-high temperature aerobic composting process
2.1.7 种子发芽指数和胡敏酸与富里酸比值
种子发芽指数和胡敏酸与富里酸比值可以反映堆肥的无害化程度和腐熟情况[3,14]。超高温好氧堆肥过程中种子发芽指数及胡敏酸与富里酸比值的变化见图7。由图7可知,堆肥过程中,种子发芽指数呈先下降后上升的趋势。堆肥0~7 d,由于铵态氮含量急剧上升,导致种子发芽指数下降至8.67%;之后随着堆肥的腐熟,种子发芽指数持续上升,堆肥结束时种子发芽指数升至108.90%,说明堆肥完全腐熟[18]。 堆肥过程中胡敏酸与富里酸比值持续上升,由初始值0.32持续上升至堆肥结束时的2.73,说明堆肥腐殖质的品质、稳定性和腐殖质聚合程度不断增加,满足堆肥完全腐熟的条件(胡敏酸/富里酸>1.7)[19]。
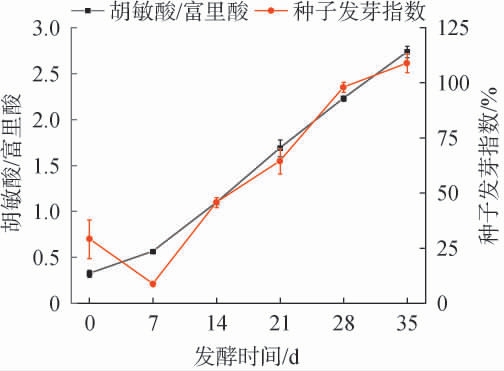
图7 超高温好氧堆肥过程中种子发芽指数和胡敏酸与富里酸比值的变化
Fig.7 Changes in germination indexes, and humic acid and fulvic acid ratio during ultra-high temperature aerobic composting process
2.2 超高温好氧堆肥过程中细菌群落的变化
2.2.1 细菌群落Alpha多样性分析
从不同堆肥时期的18个样品中共检测出1 921 145条有效的16S rRNA基因序列,在97%相似度条件下共划分为774个操作分类单元(operational taxonomic unit,OTUs),隶属于49个门、102个纲、214个目、303个科和527个属。 堆肥过程中,细菌菌群的Alpha多样性分析结果见表2。由表2可知,不同堆肥时期样品细菌菌群的Coverage值均为0.99,说明测序量合理,能代表样品中绝大多数的细菌菌群信息。堆肥0~14 d,Chao1指数呈下降趋势,Shannon指数和Simpson指数呈升高趋势,说明细菌菌群丰富度下降,多样性升高。分析原因可能是,堆肥温度的快速上升消灭部分细菌,导致群落丰富度快速下降,同时增加了细菌群落的均匀性使多样性增加,堆肥14 d后堆肥微生物适应了高温环境,群落结构趋于稳定,Chao1指数、Shannon指数和Simpson指数维持稳定。
表2 超高温好氧堆肥过程中细菌群落Alpha多样性分析结果
Table 2 Alpha diversity analysis results of bacterial communities during ultra-high temperature aerobic composting process
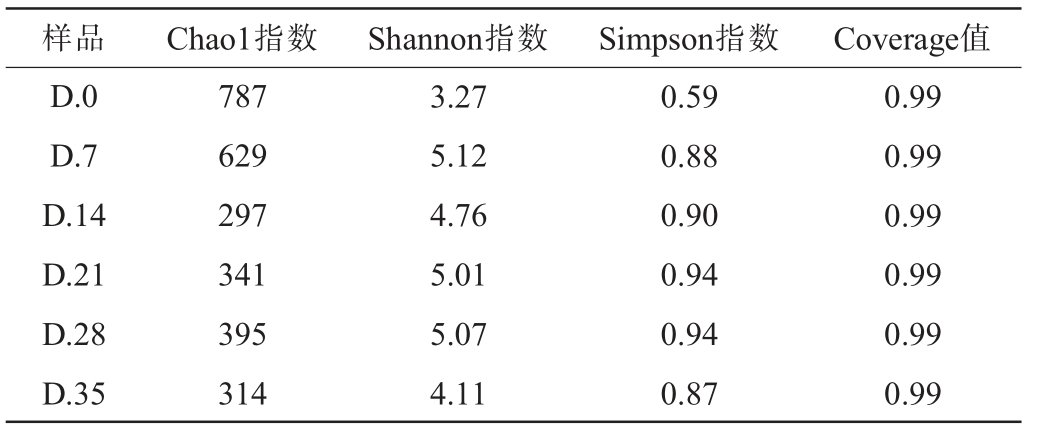
样品 Chao1指数 Shannon指数 Simpson指数 Coverage值D.0 D.7 D.14 D.21 D.28 D.35 787 629 297 341 395 314 3.27 5.12 4.76 5.01 5.07 4.11 0.59 0.88 0.90 0.94 0.94 0.87 0.99 0.99 0.99 0.99 0.99 0.99
2.2.2 细菌群落结构分析
基于门和属水平,堆肥过程中细菌菌群结构的变化见图8。由图8a可知,堆肥过程中,平均相对丰度排名前3的细菌门为变形菌门(Proteobacteria)、厚壁菌门(Firmicutes)和放线菌门(Actinobacteria),与ZHU P等[20-22]的研究结果相类似。变形菌门是原料的主要门类,其相对丰度为85.00%,随着堆肥温度的升高其相对丰度急速下降,第14天时相对丰度<1%,这可能是由于变形菌门不耐受高温,在高温期被杀死所致。厚壁菌门在原料中的相对丰度仅为10.08%,随着堆肥温度的升高,其相对丰度急剧增加,成为了整个堆肥过程中的优势菌门,并在第21天达到最高值96.02%,这与杨萍萍等[23]的研究结果类似。放线菌门的相对丰度在堆肥前中期较为稳定(1%~5%),在堆肥后期,由于可以利用难降解有机物,放线菌门的相对丰度增加,堆肥结束时达到11.81%,同时其可以通过分泌各种抗生素抑制病原微生物,有利于堆肥产品降低生物毒性[23-24],STEGER K等[25]研究发现,放线菌门可分解堆肥中的有机物,并能释放与腐殖质产生有关的无机物,这也是堆肥后期种子发芽指数升高和堆肥腐熟的重要原因。
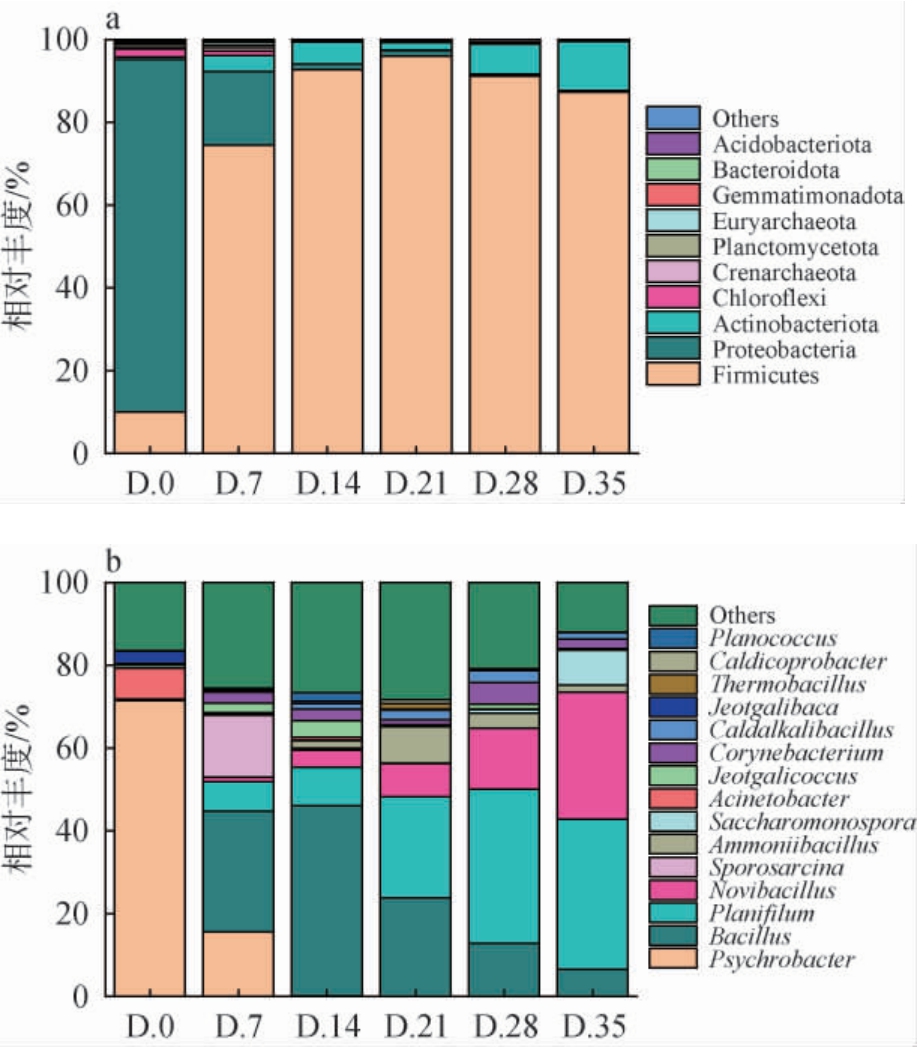
图8 基于门(a)和属(b)水平超高温好氧堆肥过程中细菌群落结构的变化
Fig.8 Changes in bacterial community structure during ultra-high temperature aerobic composting process based on phylum(a) and genus (b) levels
图a中Others代表平均相对丰度排名前5之后的细菌门,图b中Others表示平均相对丰度排名前15之后的细菌属。
由图8b可知,平均相对丰度排名前5的细菌属为嗜冷杆菌属(Psychrobacter)、芽孢杆菌属(Bacillus)、直丝菌属(Planifilum)、八叠球菌属(Sporosarcina)和嗜热新芽孢杆菌属(Novibacillus)。 嗜冷杆菌属因无法适应高温[26],其相对丰度在堆肥过程中急剧下降,由初始的71.49%下降到14 d后低于1%。 芽孢杆菌属在高温期降解有机质[27]、促进腐殖质形成[28]和抑制病原菌[29]等方面具有重要作用。因芽孢杆菌能耐受高温,其相对丰度在堆肥0~21 d由0.20%急剧增加至45.97%,而后随着易降解有机质含量降低而降低[30]。八叠球菌属在堆肥第7天的相对丰度增加,这可能与未经过翻堆,堆肥中产生了厌氧微环境有关[31]。直丝菌属是堆肥后期的优势菌属之一,其相对丰度在堆肥第14~21天明显上升,之后稳定在35%左右。这可能与直丝菌属能更好地适应木质纤维素含量较高的环境有关[20]。
2.3 细菌群落结构与理化指标的相关性分析
选取平均相对丰度排名前6的细菌门和前15的细菌属,研究堆肥过程中细菌群落变化与腐熟度相关理化指标间的相关性,结果见图9。由图9a可知,两个坐标轴累计方差贡献率为94.89%,共解释了94.89%的样本信息,说明堆肥过程中理化指标变化与细菌群落结构有关。厚壁菌门与堆肥温度、pH值、胡敏酸含量和种子发芽指数呈正相关,与富里酸含量和碳氮比呈负相关,说明厚壁菌门利于堆肥温度升高、植物毒性的降低和堆肥的腐熟;在堆肥初始阶段,变形菌门、绿弯菌门(Chloroflexi)和浮霉菌门(Planctomycetota)对样品的影响较大,主要与富里酸含量和碳氮比呈正相关,与pH值、胡敏酸含量和种子发芽指数呈负相关;在堆肥后期,放线菌门对样品的影响较大,尤其与种子发芽指数和胡敏酸含量呈正相关,这表明堆肥后期放线菌门相对丰度的增加可以有效的提高堆肥的腐熟度并降低堆肥的毒性,这也与杨萍萍等[23-25]的研究结果一致。
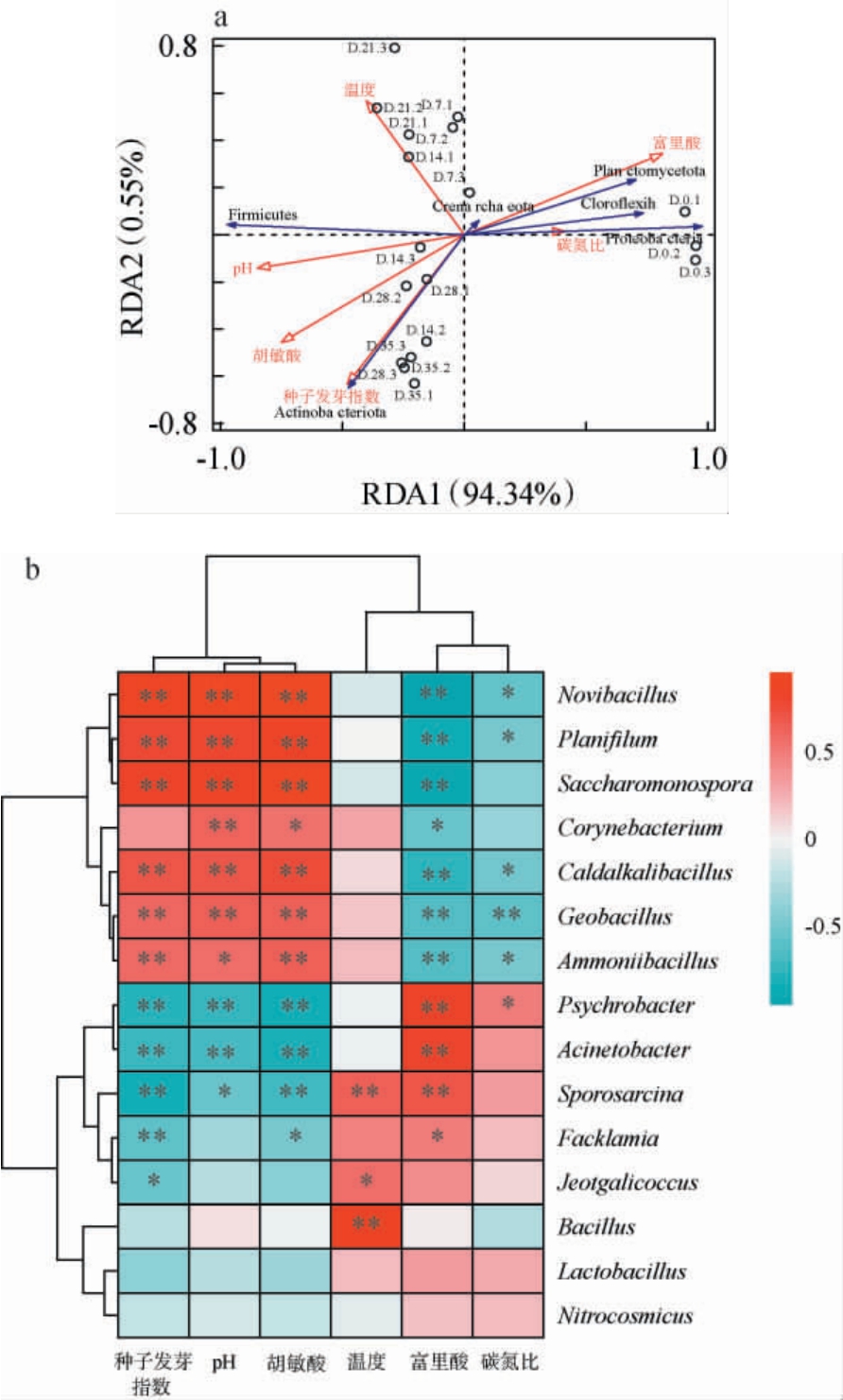
图9 细菌群落与理化指标的冗余分析(a)及相关性分析(b)
Fig.9 Redundancy analysis (a) and correlation analysis (b) of bacterial communities and physicochemical indicators
“*”表示显著相关(P<0.05),“**”表示极显著相关(P<0.01)。
由图9b可知,堆肥温度与芽孢杆菌属和八叠球菌属极显著正相关(P<0.01),表明堆肥温度升高可以促进其生长繁殖;直丝菌属、嗜热新芽孢杆菌属、糖单孢菌属(Saccharomonospora)、温泉热碱芽孢杆菌属(Caldalkalibacillus)、地芽胞杆菌属(Geobacillu)和氨芽胞杆菌属(Ammoniibacillus)与种子发芽指数和胡敏酸含量极显著正相关(P<0.01),表明这些菌属能够有效降低堆肥植物毒性,促进堆肥腐熟;同时,嗜冷杆菌属、不动杆菌属(Acinetobacter)、八叠球菌属与富里酸含量极显著正相关(P<0.01),与种子发芽指数和胡敏酸含量极显著负相关(P<0.01),费克蓝姆菌属(Facklamia) 分别与种子发芽指数和胡敏酸含量呈极显著(P<0.01)和显著(P<0.05)负相关,表明这4种菌属严重影响堆肥的腐熟。
3 结论
以酒厂污泥为主料,鸡粪和锯木屑为辅料,利用超高温专用菌剂进行为期35 d的超高温好氧堆肥中试实验,结果发现,堆肥的高温期时间、电导率均可满足堆肥无害化要求。堆肥结束时,鲜质量降低50.70%,胡敏酸含量上升至59.24 g/kg,种子发芽指数升高达到108.90%,胡富比升高达到2.73,堆肥腐殖化程度高,污泥减量化和无害化效果显著;堆肥总氮、铵态氮含量分别降低至3.93%、6.71 mg/kg,硝态氮含量提高至327.46 mg/kg,氮素营养损失较小。堆肥过程中细菌菌群丰富度降低,多样性增加,群落结构发生较大演变,在门水平上,优势菌门由变形菌门(Proteobacteria)逐渐演替为厚壁菌门(Firmicutes);在属水平上,优势菌属由嗜冷杆菌属(Psychrobacter)和不动杆菌属(Acinetobacter)逐渐演替为芽孢杆菌属(Bacillus)和直丝菌属(Planifilum)。理化指标与细菌群落相关性分析结果表明,芽孢杆菌属、八叠球菌属(Sporosarcina)与堆肥温度极显著正相关(P<0.01),直丝菌属、糖单孢菌属(Saccharomonospora)等与种子发芽指数和胡敏酸含量极显著正相关(P<0.01),有助于降低堆肥植物毒性,促进堆肥腐熟;嗜冷杆菌属、不动杆菌属等与富里酸含量极显著正相关(P<0.01),与胡敏酸含量和种子发芽指数极显著负相关(P<0.01),影响堆肥的腐熟。
[1]李文洪.白酒废水污泥特征及资源化利用研究——以五粮液酿酒废水污泥为例[D].雅安:四川农业大学,2013.
[2]王赐恩.白酒污泥污水处理生物促进剂研究[D].武汉:武汉工程大学,2017.
[3]刘阳,安明哲,张富勇,等.好氧堆肥法处置酿酒丢糟与废水污泥的原料配比[J].食品与发酵工业,2019,45(20):190-196.
[4]LIANG F, LIU X, YU X, et al.Enhancing bioavailable carbon sources and minimizing ammonia emissions in distillery sludge and distiller's grains waste co-composting through deep eutectic solvent addition[J].Bioresource Technol,2024,397:130491.
[5]潘昌滨,闫杰,吴成,等.利用蚯蚓处理酱香型白酒酒糟生产有机肥的探究[J].中国酿造,2023,42(5):201-205.
[6]张晶,孙照勇,钟小忠,等.奶牛粪条垛式模拟堆肥腐熟度及微生物群落结构变化[J].应用与环境生物学报,2016,22(3):423-429.
[7]常远,陈睿,詹亚斌,等.通风条件对餐厨废弃物辅热生物干化过程硫素转化的影响[J].农业工程学报,2022,38(S1):283-291.
[8]李龙涛,董春华,饶中秀,等.添加沼渣对餐厨垃圾堆肥腐殖化过程的影响[J].农业环境科学学报,2023,42(5):1148-1155.
[9]余杰,赵淑霞,孙长虹,等.畜禽粪污生物好氧发酵固氮研究现状及其影响因素研究[J].环境科学与管理,2017,42(8):83-88.
[10]李思敏,李思雨,唐锋兵,等.通风速率对市政污泥好氧堆肥氮素转化的影响[J].中国给水排水,2023,39(5):121-127.
[11]周有为,陈吉升,何雷,等.基于土地利用的污泥-餐厨蚯蚓堆肥中碳氮元素的转化特征[J].环境工程,2024,42(2):10-22.
[12]REN X,WANG Q,ZHANG Y,et al.Improvement of humification and mechanism of nitrogen transformation during pig manure composting with Black Tourmaline[J].Bioresource Technol,2020,307:123236.
[13]曹云,黄红英,孙金金,等.超高温预处理对猪粪堆肥过程碳氮素转化与损失的影响[J].中国环境科学,2018,38(5):1792-800.
[14]李思敏,张义竞,唐锋兵,等.生物炭添加对污泥堆肥腐殖化和氨气排放的影响[J].科学技术与工程,2022,22(31):14057-14064.
[15]唐显梅,刘方,朱健,等.白酒厂污泥与生活污泥有机组分的差异性及其淋溶迁移风险评估[J].应用化工,2024,53(3):583-587.
[16]季凯.农贸蔬菜废弃物好氧堆肥参数及菌剂添加研究[D].苏州:苏州科技大学,2022.
[17]王玉军,窦森,张晋京,等.农业废弃物堆肥过程中腐殖质组成变化[J].东北林业大学学报,2009,37(8):79-81.
[18]中华人民共和国国家质量监督检验检疫总局,中国国家标准化管理委员会.GB/T 23486—2009 城镇污水处理厂污泥处置 园林绿化用泥质[S].北京:中国标准出版社,2009.
[19]王海候,程月琴,金梅娟,等.添加生物质炭对羊粪堆肥腐殖化的影响[J].农业资源与环境学报,2022,39(4):766-774.
[20]ZHU P, QIN H, ZHANG H, et al.Variations in antibiotic resistance genes and removal mechanisms induced by C/N ratio of substrate during composting[J].Sci Total Environ,2021,798:149288.
[21]ZHOU Y, ZHAO H, LU Z, et al.Synergistic effects of biochar derived from different sources on greenhouse gas emissions and microplastics mitigation during sewage sludge composting[J].Bioresource Technol,2023,387:129556.
[22]WANG X,WANG M,ZHANG J,et al.Contributions of the biochemical factors and bacterial community to the humification process of in situ large-scale aerobic composting[J].Bioresource Technol, 2021, 323:124599.
[23]杨萍萍,尹华,彭辉,等.外接菌种对污泥堆肥效能及堆体细菌群落的影响[J].环境科学,2017,38(8):3536-3543.
[24]蔡涵冰,冯雯雯,董永华,等.畜禽粪便和桃树枝工业化堆肥过程中微生物群演替及其与环境因子的关系[J].环境科学,2020,41(2):997-1004.
[25]STEGER K,JARVIS Å,VASARA T,et al.Effects of differing temperature management on development of Actinobacteria populations during composting[J].Res Microbiol,2007,158(7):617-624.
[26]PEI F,DING H,YIN Z,et al.Evaluation of nitrogen conversion pathway during composting under amoxicillin stress: Mainly driven by core microbial community[J].Bioresource Technol,2021,325:124701.
[27]MA C,HU B,WEI M B,et al.Influence of matured compost inoculation on sewage sludge composting: Enzyme activity, bacterial and fungal community succession[J].Bioresource Technol,2019,294:122165.
[28]段曼莉,鄢入泮,周蓓蓓,等.去电子水对牛粪秸秆好氧堆肥进程及细菌群落的影响[J].环境科学学报,2022,42(2):249-257.
[29]HAO X,ZHANG W,ZHAO L,et al.Bacillus subtilis reduces antibiotic resistance genes of animal sludge in vermicomposting by improving heat stress tolerance of Eisenia foetida and bacterial community adjustment[J].Environ Res,2023,219:115088.
[30]LI L Z,LI J L,XIAO G P,et al.Enhanced growth and activities of the dominant functional microbiota of chicken manure composts in the presence of maize straw[J].Front Microbiol,2018,9:1131.
[31]孔德望,张克强,房芳,等.猪粪厌氧发酵消化液回流体系微生物群落结构特征与产气关系研究[J].农业环境科学学报,2018,37(3):559-566.